RABAT
THESE DE DOCTORAT
Présentée par
Mohamed ROUANI
Discipline : Chimie Organique
Spécialité : Phytochimie
Sous le thème
Soutenue le 03 Novembre 2015 devant le Jury :
Président :
Boujemaa DAOU : PES, faculté des Sciences de Rabat.
Examinateurs :
Rachida HASSIKOU : PES, faculté des Sciences de Rabat. Zoubida CHARROUF : PES, faculté des Sciences de Rabat. Hakima EL HAJJI : PES, faculté des Sciences de Rabat. Nadia BELHABIB : PES, faculté des Sciences de Kenitra. Mohamed TABYAOUI : PES, faculté des Sciences de Rabat. Allal DOUIRA : PES, faculté des Sciences de Kenitra. Abdelkader IL IDRISSI : PES, faculté des Sciences de Rabat.
Faculté des Sciences, 4 Avenue Ibn Battouta B.P. 1014 RP, Rabat – Maroc Tel +212 (05) 537 77 18 34/35/38, Fax: +212 (05) 537 77 42 61, http://www.fsr.ac.ma
Contribution à la valorisation du potentiel aromatique et médicinal des
plantes marocaines : Genre Artemisia.
Valorisation par combinaison des méthodes phytochimiques, de synthèse
organique et d’activité biologique
d
A mes chers parents
A ma femme
A ma fille
A mon frère
A mes sœurs
A toute ma famille
A mes amis
A tous ceux qui me sont chers
Pour leur présence de tous les instants
Pour le soutien qu’ils m’ont apporté
Avec toute mon affection et
ma reconnaissance
Faculté des Sciences, 4 Avenue Ibn Battouta B.P. 1014 RP, Rabat – Maroc Tel +212 (05) 537 77 18 34/35/38, Fax: +212 (05) 537 77 42 61, http://www.fsr.ac.ma
Faculté des Sciences, 4 Avenue Ibn Battouta B.P. 1014 RP, Rabat – Maroc Tel +212 (05) 537 77 18 34/35/38, Fax: +212 (05) 537 77 42 61, http://www.fsr.ac.ma
Faculté des Sciences, 4 Avenue Ibn Battouta B.P. 1014 RP, Rabat – Maroc Tel +212 (05) 537 77 18 34/35/38, Fax: +212 (05) 537 77 42 61, http://www.fsr.ac.ma
Le présent travail a été réalisé au laboratoire de Chimie des plantes et de Synthèse Organique et Bioorganique de l’UFR : Chimie Organique – Ecologie Chimique, de la Faculté des sciences de Rabat, sous la direction de Monsieur le
Professeur
Abdelkader Il IDRISSI.
Je tiens à le remercier pour son encadrement, pour l’attention toute particulière qu’il a toujours accordé à ma personne et à l’évolution de ce travail, ainsi que pour la confiance qu’il m’a témoignée. Il a dirigé cette thèse avec beaucoup de sollicitude, de compétence et d’enthousiasme. Son sens du devoir, sa rectitude et son dévouement resteront à jamais gravés dans ma mémoire. Qu’il me soit permis de vous exprimer mon profond respect et mon admiration pour vos qualités humaines et scientifiques.
Je tiens à remercier tout particulièrement Monsieur le professeur
Boujemaa DAOU
, pour la sympathie qu’il m’a toujours témoignée et l’aide constante et efficace qu’il m’a apporté. Ses qualités humaines et scientifiques m’ont servi de guide et d’exemple. Soyez, Monsieur le professeur, assuré de ma vive reconnaissance en me faisant l’honneur de juger ce travail et de présider ce Jury de thèse.Ce travail est le fruit d’une fructueuse collaboration avec le laboratoire de Mycologie, de Botanique et de l’Environnement sous la direction de
Madame le professeur
Rachida HASSIKO
, je lui adresse mes profondsremerciements pour l’intérêt qu’elle a apportée à ce travail en m’accueillant dans son laboratoire où ont été effectués les tests antifongiques, je lui suis très reconnaissant pour les moyens qu’elle a mis à ma disposition et le climat de confiance et d’amitié que je ne saurais oublier. En rendant hommage à ses
jury.
Mes sincères remerciements vont à Madame le professeur
Zoubida
CHARROUF
, Professeur à la faculté des sciences à Rabat et Présidente de l’Association IBN ALLBAYTAR pour la sauvegarde de l’Arganier. Son enthousiasme pour la recherche, ses compétences scientifiques et ses qualités humaines resteront pour moi un exemple. Je vous remercie vivement Madame le professeur, car malgré vos lourdes responsabilités, vous avez consenti à prendre part à ce jury.
Je tiens à adresser mes remerciements à Madame le professeur
Hakima
EL HAJJI,
Professeur à la Faculté des Sciences à Rabat, qui a porté un intérêt considérable à ce travail et qui n’a ménagé aucun effort pour siéger au jury de cette thèse.A Madame le professeur
Nadia BELAHBIB,
professeur à la Faculté des sciences de Kenitra, veuillez trouver ici l'expression de ma profonde gratitude pour avoir accepté d'examiner ce travail. Je vous prie de croire à ma respectueuse considération.Je suis très honoré par la participation à ce jury, de Monsieur le
professeur
Mohamed TABYAOUI
, de la Faculté des Sciences de Rabat et ViceDoyen chargé des affaires pédagogiques. Je tiens également à exprimer mes sincères remerciements, pour l’honneur qu’il m’a fait en acceptant de siéger dans ce jury.
la faculté des sciences de Rabat, en rendant hommage à ses qualités humaines et intellectuelles enviables ainsi que ses conseils et son encouragement. Qu’elle soit assurée de ma vive reconnaissance et de ma haute considération.
Je remercier très vivement Monsieur
Allal DOUIRA
, Professeur à la Faculté des Sciences de Kenitra, pour avoir bien voulu juger cette thèse en tant que rapporteur et membre de jury, qu’il trouve ici l’expression de ma profonde gratitude et de mon plus profond respect.Je tiens également à remercier tous les respectables Professeurs de l’UFR « Chimie Organique, Ecologie chimique et Dynamique moléculaire » pour la qualité de leurs enseignements. Qu’ils soient tous honorés par ce travail.
Bien que la thèse soit fondamentalement un travail individuel, elle n’aurait pu être menée à bien sans une équipe de collègues qui contribuent au bon fonctionnement du laboratoire, avec lesquels il est possible d’échanger conseils et suggestions. Je remercie pour cela tous mes anciens et actuels collègues de laboratoire de Chimie des plantes et de Synthèse Organique et Bioorganique, dans le désordre
:
S. Ghazi
,Z.L. Sekkat
,Dr K. Laaraj, Dr H. Bouidida, A. El
Mebtoul, B. Rahmouni, M.
EL karkour,
M. Boulhaoua.
1) M. Rouani, B. Rahmouni, M. Chammache, A. El Mebtoul, A. Il
Idrissi. Comparative study of reactivity of Carvone,
(-)-R-Linalool and (-)-(1S, 4S)-camphor derivatives: Synthesis of New
Heterocycles. European Journal of Chemistry, 2014, 5(3), pp. 383-387
2) A. El Mebtoul, M. Rouani, M. Chammache, H. Bouidida et A. Il
Idrissi. On the reactivity of (-)-(R)-Carvone and (-)-4aα, 7α, 7a
β-Nepetalactone: Synthesis of New Heterocycles. Helvetica Chimica
Acta, Vol. 94, 2011, N° 3, pp. 433-437.
3) S. Ghazi, M. Rouani, Z.L. Sekkat, A. Il Idrissi, M. arahou, R.
Hassikou. Anticandida activity of various Artemisia mesatlantica M.
extracts, Phytothérapie, Edition Lavoisier, accepté, sous presse
(2015).
4) Z.L. Sekkat, M. Rouani, S. Ghazi, A. Il Idrissi, M. arahou, R.
Hassikou. Chemical characterization of Artemisia mesatlantica
essential oils and evaluation of their anticandidosic potential,
Phytothérapie, sous presse (2015).
5) M. Rouani, M. Chammache, A. Il Idrissi. Composition chimique
en métabolites secondaires d’une asteracée endémique du Maroc :
Artemisia mesatlantica (Maire). 7
èmeRencontre Nationale sur la
Chimie Hétérocyclique. Beni Méllal (Maroc) Mars 2009.
6) M. Rouani, A. El Mebtoul, M. Chammache, A. Il Idrissi. Etude
comparative par voie chimique et phytochimique de deux asteracées :
Artemisia mesatlantica (Maire) et Artemisia arborescens (L). 4
èmeSymposium International sur les Plantes Aromatiques et Médicinales,
SIPAM4. FST Mohammadia 12-13 Mai 2011 (Maroc).
A : Artemisia
HE : Huile essentielle
E .V.E : Entraînement à la vapeur d’eau M.O : Micro-ondes
CCM : Chromatographie sur couche mince
HPLC : Chromatographie En phase liquide à haute performance CPG : Chromatographie en phase gazeuse
GC/MS : Chromatographie en phase gazeuse couplée à la spectrométrie de
masse
MS : Spectrométrie de masse TR : Temps de rétention Rdt : Rendement
IR : Infrarouge
RMN : Résonance magnétique nucléaire ppm : Partie par million
UV : Ultraviolet
: Déplacement chimique
S / d /m : Singulet / Doublet / Multiplet TMS : Tetraméthylsilane.
DMSO: Diméthyl sulfoxide.
MTT: (3-[4, 5-dimethylthiazol-2-yl]-2, 5-diphenyltetrazolium bromide). (M) : Maire.
(L) : Linné.
CMF : Activité Fongicide. CMS : Activité Fongistatique.
Introduction générale ………1
1
èrepartie : Etude phytochimique par analyse des huiles
essentielles du genre Artemisia, poussant au Maroc.
Chapitre I : Présentation du matériel végétal et les techniques utilisées : I/ Les huiles essentielles : Source des terpénoïdes……… 8I-1/ Définition………. 8
I-2/ Voie de biosynthèse des terpénoïdes……… 9
I-3/ Propriétés thérapeutiques des huiles essentielles………... 13
II/ Botanique, écologie et indications traditionnelles du genre Artemisia…….. 17
II-1/ Introduction………... 17
II-2/ Botanique, écologie et indications traditionnelles d’Artemisia mesatlantica………... 19
II-3/ Botanique, écologie et indications traditionnelles d’Artemisia Arborescens... 21
III/ Récolte du matériel végétal et obtention des huiles essentielles…………... 22
IV/ Moyens et techniques d’identification……….. 23
V/ Données chimiques et biologiques : Revue synthétique ……….. 26
Chapitre II : Etude comparative des compositions chimiques, à paramètres multiples, des huiles essentielles du genre Artemisia. I/ Introduction……….. 29
II/ Rendements obtenus en huile essentielle……… 30
III/ Techniques d’analyse et d’identification utilisées……… 35
IV/ Compositions chimiques à paramètres multiples des huiles essentielles analysées……….. 36
IV-2/ Etude comparative des compositions chimiques selon le mode
d’extraction……… 41 V/ Composition chimique d’Artemisia arborescens selon le mode
d’extraction………. 46 VI/ Comparaison des compositions chimiques des huiles essentielles
d’Artemisia mesatlantica et A. arborescens……….... 50 VII/ Purification et caractérisation des constituants majoritaires : cas de la β- Thujone et du camphre gauche………... 56
VII-1/ Introduction……… 56 VII-2/ Purification et caractérisation des constituants majoritaires : Cas de la β- Thujone………. 56 VII-3/ Purification et caractérisation des constituants majoritaires : Cas du camphre gauche………. 65
Deuxième partie : Essais de valorisation du genre Artemisia par voies de synthèse organique et des tests biologiques.
Chapitre I : Synthèse et réactivité des terpénoïdes à intérêts industriels.
I/ Introduction……… 70 II/ Réactivité et synthèse des monoterpènes……….. 70 II-1/ Réactivité des monoterpènes acycliques : Cas du β-myrcène……… 70 II-2/ Réactivité des monoterpènes monocycliques: Cas du limonène…………. 73 II-3/ Réactivité des monoterpènes bicycliques : Cas des pinènes………... 75 III/ Revue synthétique de la littérature sur le camphre………... 83
I/ Introduction……….. 93
II/ Quelques données bibliographiques………... 94
II-1/ Méthodes de synthèse des nitriloxydes……….. 94
II-2/ Réactivité des nitriloxydes……….. 95
III/ Présentation des dipolarophiles choisis………. 98
IV/ Préparation et réactivité des dipolarophiles……… 100
IV-1/ Préparation du dipolarophile I: (1S, 4S) ‐1, 7, 7‐trimethylbicyclo [2.2.1] heptan‐2‐one O‐allyloxime………... 100
IV-1-1/ Caractérisation du l-camphre………. 101
IV-1-2/ Préparation du camphoroxime………... 102
IV-1-3/ O-alkylation du camphoroxime……… 102
IV-1-4- Action du p-chlorophénylnitriloxyde sur le dipolarophile I 105 IV-1-4-1/ Préparation du p-chlorophénylnitriloxyde………….. 105
IV-1-4-2/ Condensation in-situ du dipolarophile I avec le p-chlorophényl nitriloxyde……….. 106
IV-2/ Préparation et réactivité du dipolarophile II : (-)-R-carvone…………... 108
IV-2-1/ Préparation du dipolaphile II……… 108
IV-2-2/ Condensation in-situ du dipolarophile II avec le p-chlorophényl nitriloxyde………... 110
IV-3/ Préparation et réactivité du dipolarophile III : (-)-R-linalool…………. 112
IV-3-1/ Préparation du dipolaphile III……….. 112
IV-3-2/ Condensation in-situ du dipolarophile III avec le p-chlorophényl nitriloxyde………... 115
I/ Introduction………... 121
II/ Quelques données bibliographiques……… 122
III/ Composition chimique des extraits d’Artemisia mesatlantica testés……….. 133
III-1/ Composition chimique en produits légers ………. 133
III-2/ Composition chimique en produits lourds ……… 135
III-2-1/ Méthodes d’extraction……….. 135
III-2-2/ Composition chimique en produits lourds d’Artemisia mesatlantica (M)……… 137
IV/ Méthodes de détection des métabolites recherchés……… 138
V/ Recherche et identification des lactones sesquiterpèniques………... 145
VI/ Tests de l’activité antifongique des extraits sur Candida albicans………… 148
VII/ Détermination de l’activité antifongique des produits légers d’Artemisia mesatlantica……….. 150
VII-2/ Lecture des résultats obtenus……… 153
VII-3/ Profil fongicide/ fongistatique……….. 159
VIII/ Détermination de l’activité antifongique des extraits de produits lourds (résinoides) d’artemisia mesatlantica………... 162
VIII-1/ Méthodes de travail et techniques utilisées……… 162
VIII-2/ Lecture des résultats obtenus……….. 163
VIII-3/ Résultats des tests fongicide / fongistatique ……….. 170
Discussions et conclusion……… 177
Partie expérimentale
... 182Conclusion générale………
190Bibliographie...
1971
2
Introduction générale
Les résultats de recherche que nous présentons dans ce travail entre dans le cadre de notre contribution à la valorisation de la flore aromatique et médicinale du Maroc.
Il est important de souligner que pour toucher les différents aspects de cette valorisation, nous avons adopté une démarche pluridisciplinaire associant aussi bien les travaux ethnobotanique et phytochimique que des investigations chimiques et biologique.
Il va sans dire que les plantes aromatiques et médicinales constituent actuellement un levier important pour certaines régions économiquement défavorisées au Maroc. Ces plantes constituent une richesse naturelle de première importance et pourraient même être une source de revenus non négligeables. Ceci ne serait possible que par l’étude approfondie et pluridisciplinaire des substances naturelles issue de ces régions et donc par la contribution de botanistes, d’écologistes, de généticiens, de chimistes, de biologistes et de pharmacologues.
En effet, de 1966 à 1992 le marché national des plantes aromatiques et médicinales est marqué par l’évolution de la production en termes d’exportation, allant de 3,5 millions de DH en 1966 pour atteindre 152 millions de DH en 1992, à l’exception de 453 millions de DH en 1991. A partir de 1993, la production marocaine destinée à l’exportation a été estimée à environ 1000 tonnes d’huiles essentielles et d’extraits divers par an, pour une valeur marchande de quelques 180 millions de DH.
Dans ce sens, notre laboratoire a pu contribuer dans ce domaine par plusieurs travaux, aussi bien phytochimiques que chimiques mais aussi pharmacologiques et biologiques. Plusieurs familles de plantes ont pu être étudiées, notamment les composées (astéracées), les labiées (Lamiacées), les
3
Dans la continuité logique de ces travaux de recherches, et dans le but d’apporter une contribution à la valorisation du potentiel aromatique et médicinal marocain, nous nous sommes intéressés dans le cadre du présent travail, à une étude pluridisciplinaire, aux dimensions phytochimique et chimique mais aussi biologique, de deux espèces de plante du genre Artemisia (Armoise) poussant au Maroc. Ces espèces sont largement répandues et sont utilisées en médecine traditionnelle et s’acclimatent à divers étages bioclimatiques. Il s’agit des espèces suivantes :
La première, endémique du Maroc d’où l’importance de son choix, il s’agit de l’espèce Artemisia mesatlantica (Maire) ou Armoise bleue.
La deuxième cultivée au Maroc, il s’agit de l’espèce Artemisia arborescens
(Linné).
Nous avons été guidés dans notre choix de cette plante par l’importance du genre Artemisia sur le marché, aussi bien local qu’international. En effet cette plante intéresse presque tous les secteurs : D’abord un pâturage très important pour le bétail, ensuite sur le plan industriel, l’armoise touche les secteurs de la parfumerie et de la cosmétologie.
Pour ces fins, cette plante est produite au Maroc depuis une quarantaine d’années. Sa matière aromatique est largement connue sur le marché international et ne subit pas de rude concurrence.
Le présent travail se développe en deux parties distinctes mais complémentaires :
La première partie traite de la phytochimie des deux espèces Artemisia choisies. Dans un premier chapitre nous définissons le matériel végétal utilisé et nous montrons les techniques et les méthodes employées. Dans ce sens, il sera donné un aperçu sur la biogénèse ainsi que les travaux antérieurs touchant à la phytochimie du genre Artemisia. .
Le deuxième chapitre sera consacré à une étude phytochimique comparative à paramètres multiples, en particulier l’âge de la plante et les
4
méthodes d’extraction. Il sera mis en relief l’impact de ces différents paramètres sur les rendements obtenus en matière huileuse et sa composition chimique. Nous discuterons les résultats obtenus à la lumière des analyses chromatographiques et spectroscopiques appliquées aux huiles essentielles obtenues.
Dans la deuxième partie de ce travail, nous aborderons le volet des essais de valorisation à la lumière des résultats de la première partie. Dans un premier temps, par le biais de synthèse organique, suivi dans un deuxième temps par des activités biologiques.
Ainsi, après un premier chapitre, sur des généralités traitant la synthèse et la réactivité des terpénoïdes à intérêts industriels, nous envisagerons dans un deuxième chapitre la synthèse de nouveaux hétérocycles par le biais de cycloaddition dipolaire -1,3. Cette synthèse est basée sur la transformation des constituants majoritaires des huiles essentielles étudiées.
Le troisième chapitre de cette partie porte sur l’évaluation de l’activité antimycosique des différents extraits (légers et lourds) de l’espèce Artemisia
mesatlantica (M). Les résultats de ce chapitre seront discutés à la lumière de la
composition chimique globale de cette espèce.
L’apparente disparité des différentes parties de ce travail relève en fait d’un choix volontaire. Le travail que nous avons réalisé, nous a permis de montrer l’exploitation d’une plante à trois niveaux :
D’abord une étude phytochimique permettant l’établissement des
compositions chimiques des extraits légers ou huiles essentielles et la recherche de principes actifs dans des extraits de produits lourds.
Ensuite une valorisation par voie de synthèse organique par transformation des constituants majoritaires et obtention de nouveaux hétérocycles qui pourraient constituer de nouvelles molécules susceptibles de présenter des propriétés olfactives et médicinales intéressantes.
5
Enfin une valorisation par voie biologique permettant l’évaluation des activités antimycosiques de différents extraits dont les compositions chimiques sont définies.
6
Première partie
Etude phytochimique par analyse
des huiles essentielles du genre
7
Chapitre I
Présentation du matériel végétal et les
techniques utilisées
8
I/ Les huiles essentielles : Source des terpénoïdes
Différentes plantes aromatiques sont caractérisées par la biosynthèse de molécules odorantes qui constituent ce qu’on appelle les huiles essentielles (HE). Les huiles essentielles ont, à toute époque, occupé une place importante dans la vie quotidienne de l’homme qui les utilisait pour se parfumer, aromatiser la nourriture ou même se soigner. Elles sont généralement des composés organiques volatils, aromatiques, d'un caractère huileux mais non graisseux. Les huiles essentielles sont constitués de composés organiques de structures et de fonctions chimiques très diverses. Généralement, on classe ces composés en deux groupes : les hydrocarbures terpéniques sont formés d’unités isopréniques (en C5) constituant une famille très diversifiée tant au niveau structural que fonctionnel. On rencontre principalement des mono et des sesquiterpènes (possédant respectivement 10 et 15 atomes de carbone) plus rarement des diterpènes (20 atomes de carbone) et les composés oxygénés tels que les esters, les aldéhydes, les cétones, et les alcools. Parfois la présence aussi des composés azotés et soufrés
[1 ; 2].
I-1/ Définition :
Les huiles essentielles (H.E) sont des composés aromatiques volatiles constitués par un mélange complexe de molécules odoriférantes des plantes. Ce sont des produits très volatils, généralement odorants, constitués d’un grand nombre de substances terpéniques synthétisées par les plantes et extraites à partir du matériel végétal à l’aide de procédés physiques comme la distillation à l’eau (hydrodistillation) ou à la vapeur d’eau (entraînement à la vapeur d’eau) ou par expression du péricarpe de certains citrus, suivi de décantation ou centrifugation. En chimie, une huile essentielle est un mélange hétérogène complexe pouvant contenir plusieurs dizaines de constituants dont les teneurs relatives peuvent varier de l’état de traces à plus de 90%. Les huiles essentielles sont utilisées pour
9
apporter de la saveur, ce sont les ingrédients de base pour la préparation des parfums, elles sont utilisées dans les savons, les désinfectants et dans les produits sanitaires. Elles ont des applications importantes en médecine, soit pour leurs qualités odorantes, soit pour soulager la douleur ou pour leur efficacité physiologique (aromathérapie) [3].
I-2 / Voie de biosynthèse des terpénoïdes :
Les terpénoïdes constituent une famille de produits de plus de 30 000 composés connus actuellement. Leur squelette carboné est formé à partir de l’isoprène en C5 (appelé motif biologique). On peut donc écrire une formule
générale des terpénoïdes comme étant : (C5H8) n
Isoprène C5H8
1 2
3 4
La molécule d’isoprène n’existe pas sous sa forme libre C5H8 mais elle provient,
selon un processus enzymatique, de l’acide mévalonique. Ce dernier lui-même provient de la condensation des thioesters de l’acide acétique.
H3C S - CoA O HO HO O H3C OH 1 2 3 4 5 Thioether del'acide
acétique Acide mévalonique
Toutes les réactions se font selon un processus enzymatique dicté par l’équipement génétique du tissu végétal.
1ère étape : Formation d’une molécule d’acéto-acétate par condensation de deux
10 COAS O 2 O SCOA O Condensation Aceto-acetate type "Claisen"
2ème étape : Une molécule de l’acetyl-coenzyme A est condensée à l’acéto acétate
formé sous une forme aldolique, suivi de la formation de l’acide -3R-mévalonique (Acide 3,5-dihydroxy-3-methylpentanoique)
3ème étape : Transformation de l’acide -3R-mévalonique en molécule d’isoprène, précurseur de l’élaboration des terpénoïdes.
11
4ème étape : Formation des terpènes par condensation des IPP et DMAPP.
Bilan:
12
Dans le règne végétal, les terpènes sont classés dans la catégorie des métabolites secondaires. Leur classification est basée sur le nombre de répétitions de l’unité de base isoprène (à 5 atomes de carbone). A ce jour, avec plus de 30 000 molécules identifiées, les terpènes constituent l’une des plus polymorphes et des plus grandes familles de composés naturels.
Le nom de terpènes (du nom de l'arbuste méditerranéen le térébinthe) est en principe réservé aux hydrocarbures terpénoïdes en C5, C10, C15, ..., C5n. En
pratique, l'usage est plus souple, et on parlera indifféremment de terpènes ou de terpénoïdes. n = 1 hemiterpènes (C5) n = 2 monoterpènes (C10) n = 3 sesquiterpènes (C15) n = 4 diterpènes (C20) n = 5 sesterterpènes (C25) n = 6 triterpènes (C30) n = 8 tétraterpène (C40)
13
Les monoterpénoïdes sont les constituants odorants des essences végétales, les sesquiterpénoïdes forment les fractions les plus lourdes ; les diterpénoïdes sont des constituants des résines ; les sesterpénoïdes, encore rares, sont des constituants de cires d'insectes ou de micro-organismes ; les triterpénoïdes sont des constituants universels des cellules végétales, et s'accumulent souvent dans les revêtements hydrofuges protecteurs des plantes [4 - 6].
I-3 / Propriétés thérapeutiques des HE :
Les différentes HE agissent remarquablement dans les domaines de la santé. On peut néanmoins dégager un certain nombre de grandes propriétés d’où découlent les indications. Ce sont là leurs propriétés les mieux prouvées par la recherche scientifique moderne. La grande majorité des HE ont un pouvoir antimicrobien, voir antiviral, avec des degrés d’action qui varie d’une huile à autre
[7-16].
a) Propriétés antibactériennes :
Les molécules aromatiques possédant le coefficient antibactérien le plus élevé sont les phénols : carvacrol, thymol, eugénol.
OH OH OH OCH3 Thymol Carvacrol Eugenol
Les monoterpénols : Sont des alcools à 10 carbones comme le géraniol, le
nérol, le linalool, le citronnellol, le terpinéol, le bornéol et le menthol.
14
H CH
2OH
CH2OH H
CH2OH
Géraniol Nérol Citronellol
OH Linalool OH Menthol Terpineol HO OH Bornéol
Les aldéhydes manifestent une certaine puissance antibactérienne : néral,
géranial, et citronnellal. H CHO CHO H CHO
Géranial Néral Citronellal
Les cétones présentent un intérêt dans le traitement des états infectieux : thuyone, menthone, Carvone, fenchone, camphre et pulégone.
15 O O O O O O
Menthone Carvone Pulegone
Camphre Fenchone
Thuyone
b) Propriétés antivirales :
Les virus donnent lieu à des pathologies protéiformes (très variées) dont certaines posent des problèmes de santé aujourd’hui. Les réponses classiques à ces infections étant très limitées dans l’arsenal pharmaceutique, les huiles essentielles constituent une aubaine pour traiter ces fléaux infectieux. Plus d’une dizaine d’huiles essentielles ont des propriétés antivirales.
Les virus sont très sensibles aux molécules aromatiques et certaines pathologies virales graves se trouvent très nettement améliorées grâce à elles. De plus, les cellules saines des patients utilisant des HE, acquièrent une résistance toute particulière vis-à-vis de la pénétration virale.
On a souvent recours aux HE à phénol et monoterpénol, sachant que les phénols sont nettement plus puissants, mais les monoterpénols ne présentent aucun effet secondaire.
Citons : Clous de girofle, Niaouli, Palmarosa, Ravensare, Ravintsara, Eucalyptus citronné
Les huiles essentielles parviennent au niveau cellulaire et participent à la destruction des agents pathogènes (microbes, champignons (mycoses), virus,
16
toxines infectieuses) et à l’élimination des déchets du métabolisme, tout en respectant l’intégrité de la flore bénéfique. Les défenses immunitaires sont renforcées.
L’HE agit indistinctement sur tous les virus et c’est la raison pour laquelle il faut recommander l’emploi systématique dans toutes les affections virales : grippe, herpès, poliomyélite, sida, zona… vis-à-vis desquelles la médecine chimique se trouve encore à ce jour désarmée. Les aérosols pulmonaires constituent une voie de pénétration idéale, de même que les onctions cutanées et les bains aromatiques.
c) Propriétés antifongiques :
Les infections fongiques (mycoses) sont d’une actualité criante car les antibiotiques prescrits de manière abusive favorisent leur extension. Ici, on utilisera les mêmes groupes que ceux cités plus haut mais le traitement sera plus long. On ajoutera les alcools sesquiterpéniques et les lactones sesquiterpéniques. Par ailleurs, les mycoses (candida) se plaisent bien en terrain acide. Ainsi, il faut chercher à alcaliniser le terrain en modifiant son alimentation.
Parmi les HE antifongiques : Cannelle, Clou de girofle, Eucalyptus citronné, Géranium rosat, Niaouli, Palmarosa, Ravensare, Tagète, Romarin cinéole, Calophyllum (huile végétale)
d) Propriétés antiparasitaires :
Le groupe des phénols possède une action puissante contre les parasites. Les alcools mono terpéniques et les oxydes ont une action proche des précédentes. De même les cétones et les lactones (présentent une certaine toxicité).
17 e) Propriétés antiseptiques :
Les aldéhydes et les terpènes sont réputés pour leurs propriétés désinfectantes et antiseptiques et s’opposent à la prolifération des germes pathogènes. Alors que les hôpitaux sont confrontés à des problèmes insurmontables (maladies nosocomiales, légionellose), les HE sont efficaces. La désinfection des locaux, des salles de réanimation et des chambres de malades peut faire appel à la diffusion d’HE riches en alcools et oxydes terpéniques. Citons: Cannelle, Eucalyptus citronné, Girofle, Ravensare, Romarin.
II- Botanique, écologie et indications traditionnelles du genre
Artemisia:
II-1/ Introduction :
« Il n’est point deux plantes pareilles », écrivait Carl Von Linné dans son livre Systema naturae (1735). Le célèbre botaniste, père de la classification moderne des êtres vivants et le premier à utiliser la domination à deux termes des espèces, exprimait ainsi à la fois l’émerveillement du naturaliste devant la complexité du monde végétal et le désarroi du savant qui cherche à ordonner rationnellement des milliers de groupes de plantes.
L’univers des plantes est extraordinaire de diversité. Il en existe de toutes dimensions et de toutes formes. L’étude de la flore d’un territoire, c’est d’abord faire un inventaire de l’espèce botanique qu’on y rencontre ; mais caractériser la végétation de telle ou telle zone, c’est se pencher sur les groupements de plantes, et analyser scientifiquement leurs conditions de croissance et de répartition.
La science de floristique ou botanique systématique est un outil très important dans le classement des plantes. Vu la diversité de la végétation, les plantes sont classées dans un premier temps selon leurs utilisations. On cite en particulier les plantes alimentaires et les plantes médicinales mais aussi les plantes
18
toxiques et celles qu’on prétend magiques. Mais un système de classification rigoureux semble s’imposer où les plantes sont groupées selon leur degré de parenté que l’on cite par ordre décroissant : le règne, l’embranchement, la classe, l’ordre, la famille, le genre, la section, l’espèce, la sous-espèce et la variété. En pratique on définit une plante par son binôme : le genre et l’espèce dont la norme internationale utilisée qui est le latin.
Les deux espèces que nous avons étudiées appartiennent à la même famille : les composées ou astéracées. C’est une famille homogène, naturelle et facilement identifiable. Cette famille offre de nombreuses plantes médicinales et aromatiques dont le genre Artemisia que nous avons choisi. Nous décrivons ci-dessous leurs caractères botaniques, écologiques ainsi que leurs répartitions géographiques.
19
II-2-Botanique, écologie et indications traditionnelles d’Artemisia mesatlantica :
Cette plante est une armoise de la famille des composées, atteignant 0,5 m de haut, très rameuse dans sa partie supérieure, formant des touffes assez rapprochées, constituant un ensemble homogène de nature steppique. A la base de tiges on trouve des feuilles, petites, dentelées, pétiolées, à limbe divisée en lanières (généralement trois) et bleutées. Inflorescence en panicules dense, constitue un épi compose dressé, avec des fleurs jaunes paraissent toutes fertiles. La plante couverte de poiles glanduleux sécréteurs.
20
Sur le plan écologique, c’est une espèce très répandue dans le moyen atlas, le haut Atlas, et l’anti Atlas. Indifférente à la nature de sol, elle vit aussi sur basalte (plaine de selrhet) que sur calcaire, sur silice, sur granite ou sur schiste. Elle a donc une répartition beaucoup plus large que les autres espèces endémiques.
Elle pousse dans les zones bioclimatiques semi-arides et aride
(exceptionnellement dans la subhumide) du bioclimat méditerranéen. Elle se localise entre 1400 -2500 m d’altitude et correspond à un niveau de végétation plus élevée que celui de l’armoise blanche (A. herba alba) [17-24].
La plante entière est une panacée de la médecine traditionnelle Marocaine, un dicton Marocain dit d’ailleurs :
« li mjareb shih, ma ydouze kadamo bla maydih », « celui qui a expérimenté l’armoise ne peut passer à côté sans l’emporter ».
Elle est partout prescrite comme vermifuge, emménagogue, diurétique, stomachique, antiseptique intestinal, tonique dépuratif, cholagogue, antidiabétique.
Elle est également administre dans tous les refroidissements et comme synergique de tous les antidotes.
Dans le moyen Atlas où nous avons récolté cette armoise, associée à des plantes astringentes, elle est indiquée à l´intérieur et à l´extérieur comme antirabique. Contre les troubles hépatiques (lemrâr) et les vertiges (dokha) provoquer par un foie malade.
Le miel butiné sur ses fleurs est réputé posséder, les propriétés de la plante. Cette plante sert aussi à aromatiser le café, comme l’absinthe sert à parfumer le thé !!!
C’est un pâturage aromatique très apprécié par les ovins, une expression populaire décrit ces steppes comme «le pays de l’armoise et du vent» pour dire qu’on y trouve rien d’autre que cette armoise, cette steppe est par excellence le pays de la transhumance de nomades éleveurs [25].
21
II–3–Botanique, écologie et indications traditionnelles d’Artemisia
Arborescens:
Cette espèce est une armoise de la famille des composées, se présente sous forme d’un arbuste unicaule, très ramifié pouvant atteindre 1m, à rameaux dressés étalés, très feuillés. Feuilles soyeuses, grisâtres de taille décroissante de bas en haut de la plante. Inflorescence en grappe composé, courte, dense en panicules, fleurs à corolle jaune, tridentée et tubuleuse.
Selon Jahandiez et Maire (1934), sur les falaises maritimes, dans les broussailles des collines littorales du Rif. Ailleurs au Maroc, elle est cultivée et commercialisée. Elle se cantonne à l’état spontané dans le bassin méditerranéen,
22
elle se rencontre en Algérie, Tunisie, Libye, Europe méridionale, Chypre, Syrie et Palestine [17 –24].
Absinthe arborescens : ŠÎba : abréviation de ŠÎbat al–àjûz (litt: les cheveux blancs de la vieille).
Partout au Maroc, l’absinthe en infusion (un petit rameau dans une théière), à la réputation d’être réchauffant, tonique apéritive digestive, cholagogue, diurétique, emménagogue, antispasmodique, fébrifuge, vermifuge, c’est une véritable panacée.
Ici à Rabat, on l’utilise aussi comme antidiabétique, ses propriétés abortives, à dose élevée sont connues.
En hiver, elle remplace la menthe pour parfumer le thé [3 ; 25].
III/ Récolte du matériel végétal et obtention des huiles
essentielles :
Le matériel végétal est formé par deux espèces d’armoise que nous avons choisies pour cette étude. La première est une espèce spontanée, endémique du Maroc : Artemisia mesatlantica Maire. Elle a été récoltée dans son site naturel (à 20 km d’Ifrane, Moyen Atlas) en deux dates espacées. La première en début de mois d’Août qui marque le début de floraison (formation des bourgeons floraux) et la deuxième en début de septembre, en pleine floraison (l’apogée du stade de l’épanouissement des fleurs).
La deuxième espèce est Artemisia arborescens Linné, c’est une espèce cultivée et commercialisée, elle a donc été achetée sur place (Rabat et régions). Son identification botanique a été assurée par les services de l’Institut Scientifique. Chaque espèce est mise à sécher sous forme étalée à l’abri des rayons solaires, sous ventilation, à température ambiante et la plante est régulièrement retournée. Ce traitement est généralement nécessaire, car la plupart des plantes de la famille des astéracées (composées) fournissent plus d’huile essentielle à l’état sec qu’à
23
l’état frais, sans accorder d’importance au très faible pourcentage de terpène léger qui se perd durant le séchage.
Pour extraire l’huile essentielle, nous avons adopté deux techniques d’extraction :
La première, méthode classique largement utilisée est connue sous le nom d’entrainement à la vapeur d’eau (E.V.E). Cette technique fournit une huile essentielle qui garde complètement son arome.
La seconde, méthode assez récente, très avantageuse sur le plan économique, elle est basée sur les effets du rayonnement micro-ondes vis-à-vis des glandes à huile essentielle des végétaux. Cette seconde technique, est toujours au stade expérimental, ce qui nous a poussé à entreprendre une étude comparative entre Les deux techniques sur le plan du rendement d’extraction et aussi au niveau de la composition chimique des huiles essentielles.
Les eaux d’entrainement des huiles, issues des deux méthodes, subissent une extraction à l’acétate d’éthyle.
IV/ Moyens et techniques d’identification :
La détermination rigoureuse des compositions chimiques des huiles essentielles nécessite des analyses parfaites et reproductibles.
Les diverses techniques récentes que nous avons utilisées ont constitué un instrument puissant pour parvenir à établir la constitution naturelle des huiles essentielles.
IV-1 / Moyens et techniques utilisés :
chromatographique :
L’analyse des huiles essentielles par chromatographie en phase gazeuse (C.P.G) a été réalisée sur deux types de chromatographe :
24
Le premier est de type GIRDEL série 300 équipé d’un détecteur à ionisation de flamme, alimenté par H2 /Air dont les débits respectifs sont 25 et 350 ml/min.
L’analyse est faite sur une colonne remplie 3mx2mm (ov17/4%) le gaz vecteur utilisé est l’azote ordinaire séché sur tamis moléculaire.
La température de la colonne est programmée automatiquement de 60°C à 200 ° à raison de 2°C/mn .les températures de l’injecteur et du détecteur gardent une valeur constante de 250°C.les volumes des échantillons injectés sont de l’ordre de 0,1µ à l’aide d’une micro seringue type S.G.E de contenance 1 µl.
L’enregistrement a été fait avec une vitesse de déroulement du papier de 2,5 mm/min.
Le second est le type DANI 8521 équipé d’une colonne capillaire en silice fondue de 50 m de long et de 0,32 de diamètre intérieur.
La détection est assurée par un détecteur à ionisation de flamme, alimenté par le mélange H2/Air.la pression de l’hydrogène est de 0,4 bar, celle de l’air est de 0,5
bar. Le gaz vecteur utilisé est l’azote ordinaire.
La température de la colonne est programmée automatiquement de 50°C à 230°
C avec élévation de 5°C/min
L’injecteur et le détecteur gardent une température constante égale respectivement, à 225°C à 232 °C durant toute l’opération.
Le volume des échantillons injectés et de 0,2 µl. le chromatographe est relié à un intégrateur électronique type chromatopac C-R6A.
Caractérisation par CPG/SM :
L’identification qualitative des pics a été réalisé par un chromatographe en phase gazeuse type Hewlett pachard 5890 série II, couplée à un spectromètre de masse de type 5972 A équipée d’une colonne DB5, 30m, de diamètre 0,25mm et d’épaisseur de film 0,25 mm. Les conditions d’analyse sont les suivantes :
25
La température est programmée de 50° C pendant 4 min puis elle monte de
5°C/min jusqu’à 230 °C, le temps final est de 50 min. la température de l’injecteur
est de 230 °C, la température du détecteur est 270°C.
Techniques d’identification:
La détermination des compositions chimiques des huiles essentielles par identification de leurs constituants a été réalisée par diverses méthodes. D’abord les temps de rétention qui servent à pressentir la présence de certains constituants commercialisés.
Ensuite, l’utilisation de la chromatographie gazeuse couplée à la spectrométrie de masse vient compléter l’identification. Il arrive parfois qu’un échantillon contient un composé majoritaire (>25 %), dans ce cas on procède par méthodes chimiques à son isolement à l’état pur. Son identification est assurée ensuite par méthodes spectroscopiques habituelles à la chimie organique.
26
V/ Données chimiques et biologiques : Revue synthétique de la
littérature :
V-1/ Historique :
L’odeur parfumée des plantes est due en grande partie aux huiles essentielles dans leur organisme. Ces composés organiques volatiles extraits de différentes parties des plantes aromatiques ou d’arbres, ont été utilisées depuis des milliers d’années datant aussi loin que les anciennes civilisations. Ils les utilisent pour guérir, améliorer, adoucir et exciter le corps et l’esprit, on les retrouve d’ailleurs dans les tombeaux égyptiens datant de l’an 1000.
Le nom latin commun à toutes les armoises est Artemisia ce qui les consacre à la déesse Artémis, qui signifie en grec, intégrité, qui n’aime pas les hommes en tant que males. Elle devient pour cette raison, une déesse protectrice de toutes les femmes et permet ainsi à ces dernières de franchir plus aisément les deux étapes essentielles qui marquent leur vie : la puberté et la ménopause. Entre ces deux périodes clé de la vie féminine, elle intervient en régularisant les cycles menstruels qui sont liés aux phases de la lune.
Les huiles essentielles de l’armoise ont été mentionnées dans de nombreuse recette en usage thérapeutique, comme étant tonique, stimulant, fébrifuge (qui fait tomber la fièvre), antihelminthique (qui chasse les vers), antiseptique, diurétique et emménagogue (qui fait venir les règles)
V-2/ Données chimiques et biologiques :
Le tableau 1 ci-dessous regroupe quelques données sur les compositions
chimiques des espèces étudiées. D’après les données de la littérature, les constituants identifiés ont souvent montré un potentiel antimicrobien important.
27
Tableau 1 : Données de la littérature sur Artemisia mesatlantica Maire et Artemisia arborescens Linné.
Espèce lieux de récoltes Parties traitée Principaux constituants % Réf A. arborescens Etats unis Fleurs Feuilles Brindilles β–Thujone Myrcène Camphène α–pinène Camphre Chamazulène ND 5,05 2,81 3,24 16,71 39,6 [23] A. Arborescens Italie Fleurs Feuilles Brindilles α–pinène β–Thujone Camphre β–Caryophyllène chamazulène 3,17 23,97 23,73 3,32 7,66 [18] A. Arborescens Maroc Fleurs Feuilles Brindilles β–Thujone Camphre 1–8 -cinéol Linalool Germacrène Terpinéol-4-ol Chamazulène 30,06 21,67 Tr 2,06 2,03 3,34 1,45 [18]
A.mesatlantica Maroc Fleurs Feuilles Brindilles β–Thujone α–Thujone bornéol Camphre 1–8 cinéol 61 3,8 1,4 3,85 5,8 [26] [27]
ND: Non détecté Tr: Trace
28
Chapitre II
Etude comparative des compositions
chimiques à paramètres multiples des
huiles essentielles, du genre Artemisia
29 I/ Introduction :
Les huiles essentielles constituent des extraits naturels obtenues généralement par entrainement à la vapeur d’eau de la partie aérienne d’un végétal.
Par leur utilisation dans les industries de parfum, de cosmétique, de l’agroalimentaire et de la pharmacie, les huiles essentielles représentent une matière importante.
Les huiles essentielles sont généralement des composés organiques volatiles, aromatiques d’un caractère huileux.
Elles contiennent les terpènes, des sesquiterpènes et d’autres composants. Obtenues à partir des végétaux soit par l’entraînement à la vapeur d’eau, soit par expression du péricarpe frais de certains citrus [31].
De point de vue chimique une huile essentielle est un mélange hétérogène complexe pouvant contenir plusieurs dizaines de constituants dont les teneurs relatives peuvent varier de l’état de traces à plus de 90%.Ces constituants sont des hydrocarbures, des éthers, des aldéhydes, des cétones [35‒36].
Parmi les multiples fonctions possibles des huiles essentielles on peut citer : La protection contre les prédateurs de la plante.
L’attraction des insectes pollinisateurs.
l’inhibition de la multiplication des bactéries et des champignons. La stimulation de l’humeur.
Les huiles essentielles sont recherchées aussi pour leurs propriétés organoleptiques. En effet les huiles essentielles trouvent des applications dans des branches d’industrie chimique. Elles sont utilisées dans la formulation des parfums et des produits cosmétiques, elles sont également utilisées dans l’industrie pharmaceutique [33].
30
En médecine, certaines huiles essentielles sont utilisées pour leurs propriétés anesthésiques, antiseptiques et stimulantes de l’expectoration [33].
Artemisia mesatlantica Maire, en raison de son endémisme strict sur des parties
restreintes du territoire marocain, et parce qu’elle n’est pas bien distinguée des autres armoises, surtout de l’armoise blanche (Artemisia herba halba) morphologiquement très proche. Peu de travaux ont été effectués sur cette espèce montagnarde, citons les recherches de valorisation de sa partie volatile et fixe
[28-29]. Dans ce cadre il nous a paru utile de valoriser cette armoise endémique
par l’étude de la variation de la composition chimique de son huile essentielle avant et durant la période de floraison. Cette variabilité sera discutée en fonction des méthodes d’extraction en mettant en relief la nouvelle technique des micro - ondes. Enfin nous nous intéresserons à la recherche et à l’identification partielle de sa partie fixe, que nous exposerons dans la deuxième partie de ce travail. L’espèce Artemisia arborescens Linné, est une espèce cultivée et peut s’adapter à plusieurs climats, par conséquent elle marque son endémisme sur le territoire méditerranéen [30]. Sur le plan chimique, cette espèce n’a connu que l’analyse de son huile essentielle [18] et n’a jamais été le siège de comparaison avec les espèces de sa famille.
II/ Rendements obtenus en huile essentielle
II-1/ Rendement en huile essentielle d’Artemisia mesatlantica selon l’âge de la plante :
Les deux méthodes d’extraction employées, à savoir l’entrainement à la vapeur d’eau (EVE) et les micro-ondes (μ-ondes), ont donné des résultats variables en rendements. Nous consignons dans le tableau 1 les valeurs en rendement obtenues suivant l’âge de la plante de l’espèce Artemisia mesatlantica
31
Les rendements en huile essentielle sont calculés par rapport au poids sec du matériel végétal.
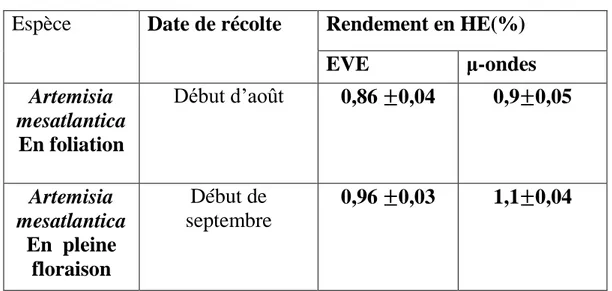
Tableau 1 : dates de récolte et rendements en huile essentielle
Espèce Date de récolte Rendement en HE(%)
EVE μ-ondes Artemisia mesatlantica En foliation Début d’août 0,86 ±0,04 0,9±0,05 Artemisia mesatlantica En pleine floraison Début de septembre 0,96 ±0,03 1,1±0,04
II-2/ Comparaison des Rendements d’Artemisia mesatlantica (M) et d’Artemisia arborescens (L) :
Les deux espèces sont soumises à des conditions identiques d'extraction, aussi bien par entraînement à la vapeur d’eau (EVE) qu'à l'aide des micro-ondes (µ-ondes). Les chiffres obtenus, consignés dans le tableau et le graphe ci-dessous, ont bien montré une certaine richesse en huile essentielle de l'espèce A.
arborescens. Cette richesse est observée quel que soit le mode d'extraction
employé.
De point de vue comparatif, nous avons soumis les deux espèces étudiées aux mêmes conditions d’extraction, selon les deux techniques, dans le but de comparer le rendement en HE des deux espèces du genre Artemisia.
32
Nous consignons dans le tableau 2, les deux techniques d’extraction et la moyenne des rendements calculés par rapport au poids sec de la plante après
différentes prises d'essai.
Tableau 2: Moyenne des rendements en HE des deux espèces étudiées
II-3/ Discussions:
Le rendement est un élément important de comparaison. La grande variabilité observée des rendements en huile essentielle selon l’âge de la plante de l’espèce
Artemisia mesatlantica, montre clairement l’influence des facteurs biologiques
et physiologiques (cycle végétatif), si on se réfère à quelques données de la littérature.
Les deux espèces du même genre, présentent un rendement différent en HE. On trouve que l’espèce cultivée en étage humide et subhumide, Artemisia Arborescens dépasse l’espèce spontanée, Artemisia mesatlantica en étage aride et semi-aride. Cela est valable pour les deux techniques d’extraction utilisées, et
Mode d’extraction
Rendement moyen
Espèce Essais E.V.E Essais µ-ondes E.V.E µ- ondes A. mesatlantica adulte 0,96 % 0,97 % 0,96 % 1,1 % 1,2 % 1 % 0,96 % 1,1 % A. arborescens 1,9 % 2,2 % 2,1 % 1,2 % 1,3 % 1,3 % 2,06 % 1,26 %
33
montre que les facteurs taxonomique et climatique ont bien une influence sur le rendement en HE.
Notons aussi que le rendement en huile essentielle, est lié à la méthode d’extraction utilisée, à savoir que l’espèce A. mesatlantica présente une légère augmentation en HE, vis-à-vis des rayonnements micro-ondes. Par contre l’espèce arborescens a chuté en rendement quand la méthode des micro-ondes est utilisée. Selon ces paramètres de comparaison on pourra conclure avec certitude, que l’extraction par micro-ondes revêt une certaine importance, car il est synonyme du gain du temps et de l’énergie.
A. MESATLANTICA A.MESATLANTICA ADULTE A.ARBORESCENS
0,86% 0,96% 2,06% 0,9% 1,1% 1,26% EVE MICRO-ONDES
Fig 1 : variation du rendement en fonction du mode d’extraction, l’âge de la plante et l’espèce étudiée.
34 II- 4/ Effet du temps de radiation :
Le calcul des rendements à la fin de chaque cycle d’irradiation nous a permis l’étude de la variation du rendement en huile essentielle en fonction de la durée d’exposition aux micro-ondes pour les deux espèces étudiées.
Tableau 3 : Étude cinétique des huiles essentielles extraites par micro-ondes Temps d’irradiation A. mesatlantica A. Arborescens
0 0 0 3 0,02 0,03 6 0,12 0,32 9 0,37 0,50 12 0,36 0,82 15 0,70 0,96 18 0,86 1,13 21 0,96 1,26
Les courbes des rendements de production de l’huile essentielle montrent que les six premiers minutes sont très peu productives (Tab : 3 - Fig : 2), la majorité de
0 0,02 0,12 0,37 0,36 0,7 0,86 0,96 0 0,03 0,32 0,5 0,82 0,96 1,13 1,26 O 3 6 9 12 15 18 21 R e n d e me n t ( % )
fig 2: Evolution du rendement des huiles essentielles en fonction de la durée d'irradiation
35
l’huile essentielle apparaît après un temps de séjour de 15 minutes. Au-delà de 18 minutes toute l’huile essentielle est presque recueillie.
En comparaison, l’étude de l’effet du temps d’extraction sur le rendement dans le cas de E.V.E s’est révélée impossible vu le temps très court que nécessite une extraction par micro-ondes, car en 15 min ou même 20 min, les condensats recueillis en E.V.E sont très faibles voire inexistants pour calculer un quelconque rendement.
III/ Techniques d’analyse et d’identification utilisées
Une fois l’extrait en huile essentielle est obtenu, l’analyse permet d’identifier et de quantifier les produits qui le composent. Les progrès des méthodes analytiques permettent d’identifier rapidement un très grand nombre de constituants. La méthode la plus adéquate à nos jours est la chromatographie en phase gazeuse (CPG).
La chromatographie en phase gazeuse (CPG) est, comme toutes les techniques de chromatographie, une technique qui permet de séparer des molécules d'un mélange éventuellement très complexe de nature très diverses. Elle s'applique principalement aux composés gazeux ou susceptibles d'être vaporisés par chauffage sans décomposition. Elle est de plus en plus utilisée dans les principaux domaines de la chimie.
Le mélange à analyser est vaporisé à l'entrée d'une colonne, qui renferme une substance active solide ou liquide appelée phase stationnaire, puis il est transporté à travers celle-ci à l'aide d'un gaz porteur (ou gaz vecteur). Les différentes molécules du mélange vont se séparer et sortir de la colonne les unes après les autres après un certain laps de temps qui est fonction de l'affinité de la phase stationnaire avec ces molécules.
36
IV/ Compositions chimiques à paramètres multiples des huiles
essentielles analysées.
IV-1/ Compositions chimiques des huiles essentielles d’Artemisia mesatlantica selon l’âge de la plante :
Les différents étapes d’étude restent les mêmes pour les échantillons étudies depuis la récolte du matériel végétal jusqu’à l’identification de sa composition chimique.
Nous reproduisons ci-après les chromatogrammes obtenus selon l’âge de la plante. Le tableau 4 regroupe les résultats d’identification.
37
Tableau 4 : Composition chimique d’A. mesatlantica selon l’âge de la
plante :
Plante jeune (EVE)
Plante adulte (EVE)
Pic TR Identification % Pic TR Identification %
1 6,36 α–pinène 0,55 1 7,78 Sabinène 1.64
2 7,75 Sabinène 2,64 2 9,36 Terpinène 0,48
3 9,35 Camphène 0,70 3 9,64 p-cymene 0,69
4 9,62 α–phellandrène 1,03 4 9,89 Eucalyptol 3,93
5 9,87 Eucalyptol 5,80 5 10,97 Sabinène hydrate 0,99
6 10,69 Sabinène hydrate 1,34 6 11,29 α – terpinéol 0,29
7 11,26 α – terpinéol 0,44 7 12,45 β–terpinéol 0,33 8 12,44 β–terpinéol 0,50 8 12,71 α– Thujone 4,68 9 12,70 α– Thujone 3.65 9 13,20 β–Thujone 62,05 10 13,17 β–Thujone 58,08 10 14,11 Camphre 4,47 11 14,11 Camphre 3,85 11 14,95 Bornéol 1.01 12 14,96 Bornéol 0,70 12 15,39 Sabinol 4,12
13 15,40 Sabinol 3,89 13 15,88 Alcool fenchylique 0,54
14 15,89 Alcool fenchylique 0,58 14 16,10 Myrténol 0,84
15 16,11 Myrténol 1,26 15 17,22 Acétate de bornyle 0,56
16 17,24 Acétate de bornyle 0,70 16 21,89 Oxyde de pipériténone 0,33 17 19,53 Acétate de sabinyle 0,29 17 25,32 ∆–carèn–4–0l 0,61
18 21,65 Eugénol 0,31 18 25,62 Germacrène 1,57 19 25,27 ∆–carèn–4–0l 0,69 19 25,95 Farnesol 0,49 20 25,65 Germacrène 1,87 20 28,46 - 1,62 21 25,98 Farnesol 0,75 21 29,22 - 0,59 22 26,31 - 0,29 22 29,37 Elemene 0,99 23 28,65 Caryophyllène oxyde 1,47 23 29,61 - 0,83 24 29,39 Elemene 1,05 24 29,97 - 2,43 25 29,64 - 1,03 25 30,28 Aromadendrène 0,92 26 30,31 Aromadendrène 1,00 26 30,80 Bisabolène 1,57 27 30,82 Bisabolène 2,02 27 31,17 Caryophyllène 0,28 28 32,71 - 0,35 28 32,67 - 0,32 29 33,14 - 0,59 29 33,11 - 0,37 - - - - 30 33,82 - 0,28
39
Lecture des résultats du tableau 4:
Avant d’entrer dans la comparaison de la composition chimique des huiles essentielles des deux échantillons analysés, on pourra remarquer d’une façon générale que l’H.E de cette armoise endémique présente une forte teneur en β–
Thujone (58,08 à 62, 05%) qui l’emporte sur l’isomère α– Thujone (3,65 à 4,68%).
Les huiles essentielles obtenues à partir des deux échantillons d’A. mesatlantica selon l’âge de la plante ont été analysées strictement sous les mêmes conditions. Les compostions chimiques obtenues ont montré des différences aussi bien qualitatives que quantitatives.
De point de vue qualitatif, les compositions chimiques renferment globalement le même nombre de constituants. Cependant ces constituants sont différents par leur nature d’un échantillon à un autre. Notons à titre d’exemple l’absence de certains terpènes légers de l’échantillon en fin de cycle végétatif comme l’ α–pinène ; le camphène et le α–phéllandrène. Ces derniers sont assez représentés dans la plante jeune. La même remarque est observée au niveau des terpènes oxygènes car on note la présence de l’oxyde de pipériténone dans la plante âgée alors que cet oxyde est remplacé par l’Eugénol et l’Acétate de sabinyle dans la plante jeune. Quant aux sesquiterpènes, ils sont tous représentés dans les deux échantillons. De point de vue quantitatif, on voit bien clairement que l’âge de la plante influe beaucoup sur les terpènes légers qui totalisent 12.07% et 7,73% respectivement dans la plante jeune et la plante adulte. Par contre les terpènes oxygènes voient leur pourcentage sensiblement augmentée en passant de 74,94% à 80,09 % respectivement dans la plante jeune et la plante adulte. Les sesquiterpènes à leur tour ont augmenté de pourcentage dans la plante car ils passent de 10,42% à
40
Tableau 5 : Variation des principaux terpènes selon le cycle végétatif d’Artemisia mesatlantica Maire.
Monoterpènes légers Monoterpènes
oxygènes Sesquiterpènes
Plante
jeune 12,06 % 74,94 % 10,42 %
Plante
adulte 7,73 % 80,09 % 12,17 %
En conclusion, nous avons montré par cette étude comparative que la composition chimique d’huile essentielle est sujette de façon permanente à des changements dans la nature des constituants et leurs taux dans la plante. Les facteurs de ces variations sont multiples, en particulier les influences climatologiques, mais dans notre cas nous n’avons envisagé que l’influence de l’âge de la plante.
Discussions des résultats :
Les conditions expérimentales utilisées d’une façon identique pour les deux échantillons provenant des deux récoltes, laissent penser de loin à des transformations dues au mode d’extraction, ou bien aux moyens technologiques employés, alors le phénomène intervenant est le facteur physiologique qui détermine en quelque sorte le programme biogénétique interne de fabrication des produits rencontrés.
L’augmentation de teneurs en monoterpènes légers, laisse penser et proposer que la plante durant la période de floraison dispose l’odeur et l’arôme comme astuce qui attire les insectes pollinisateurs. L’apparition de quelques sesquiterpènes dans l’H.E de la plante en fin de cycle végétatif dénote que la plante dispose de ces substances pour renforcer son arsenal immunitaire pour faire face contre tous les
41
parasites d’opportunité qui cherchent le nectar floral. Cela est conforme avec les recherches de la littérature qui confirment que la composition quantitative et qualitative des différents constituants varie avec l’âge de la plante et de son cycle végétatif [14].
IV-2/ Etude comparative des compositions chimiques selon le mode d’extraction
IV-2-1/ Introduction :
Dans le cadre de la recherche de nouvelle méthode d’extraction de produits naturels, il s’est révélé que l’exposition d’un matériel végétal, en contact avec un extractant, à un rayonnement micro-onde permet une extraction rapide et accrue de celui-ci.
Loin d’être exploitée dans toutes les dimensions, la technique des micro- ondes fait toujours l’objet d’investigation visant l’amélioration de ses performances. Notre objectif principal est de développer une technique d’extraction des huiles essentielles dont les performances souhaitées seraient :
Rendement amélioré.
Extraction accélérée.
Economie d’énergie.
Dans ce sens, nous avons entrepris l’étude du potentiel d’extraction d’une telle technique afin de le comparer à celui des méthodes beaucoup plus classiques telle que l’entrainement à la vapeur d’eau (E.V.E). Nous avons utilisés ces deux méthodes d’extraction pour traiter les deux espèces choisies à savoir Artemisia