SYNTHÈSE DE NOUVEAUX AGENTS THÉRAPEUTIQUES GL YCOCONJUGUÉS MONO- ET MULTIVALENTS
MÉMOIRE PRÉSENTÉ
COMME EXIGENCE PARTIELLE DE LA MAITRISE EN CHIMIE
PAR CÉLIA SEHAD
Avertissement
La diffusion de ce mémoire se fait dans le respect des droits de son auteur, qui a signé le formulaire Autorisation de reproduire et de diffuser un travail de recherche de cycles
supérieurs (SDU-522 - Rév.10-2015). Cette autorisation stipule que «conformément à
l'article 11 du Règlement no. 8 des études dè cycles ~upérieurs, [l'auteur] concède à· l'Université du Québec à Montréal une licence non exclusive d'utilisation et de publication de la totalité ou d'une partie importante de [son] travail de recherche pour des fins pédagogiques et non commerciales. Plus précisément, [l'auteur] autorise l'Université du Québec à Montréal à reproduire, diffuser, prêter, distribuer ou vendre des · copies de [son] travail de recherche à des fins non commerciales sur quelque support que ce soit, y compris l'Internet. Cette licence et cette autorisation n'entraînent pas une renonciation de [la] part [defauteur] à [ses] droits moraux ni à [ses] droits de propriété intellectuelle. Sauf entente contraire, [l'auteur] conserve la liberté de diffuser et de commercialiser ou non ce travail dont [il] possède un exemplaire.»
Tout d'abord, je tiens à remercier mon directeur de recherche, le professeur René Roy, pour m'avoir offert l'opportunité de travailler dans son équipe de recherche pour découvrir et apprendre les bases de la chimie des sucres et de la chimie médicinale. Je lui suis tout particulièrement reconnaissante pour toutes nos discussions, pour ses précieux conseils et pour sa confiance envers moi. Son écoute et sa patience m'ont permis de réaliser tous mes projets avec succès et dépasser toutes les difficultés que nous avons rencontrées.
Je tiens egalement à remercier le Pr. Azouz pour son soutien et ses encouragements tout au long de ma maitrise.
Je remercie tout pai1iculiérment mon mentor et ami Chichi Tze Chieh pour tous ses conseils et son aide dans tous les domaines. Je le remercie beaucoup pour sa disponibilité, sa gentillesse et sa patience. Je remercie infiniment notre assistant de recherche, Dr. Rabindra Rej, ainsi que le post-doctorant Rahul Baghul pour leurs collaborations. Leur disponibilité, leurs conseils et leur aide m'ont été précieux au cours de ces deux années de maîtrise. Je remercie également tous les membres du laboratoire pour leur soutien et leur bonne humeur quotidienne qui ont rendu ces deux années de travail très agréables.
Je remercie également tous les membres du dépai1ement de chimie, tout particulièrement Madame Sonia Lachance pour toute son aide et sa disponibilité lorsque j 'avais besoin d'informations administratives, ainsi que tous les professeurs que j'ai côtoyés à l'UQAM, le Pr. Steve Bourgault, Pr. Alexandre Gagnon, Pr. Mohamed Siaj et Pre. Lekha Sleno.
Bien évidemment, je souhaite remercier chaleureusement tous les membres de ma famille qui m'ont soutenue depuis le début, et qui ont été très présents malgré la distance. Ces échanges quasi journaliers avec eux m'auront été d'un grand réconfort. Je voudrais également remercier l'homme qui partage ma vie, pour son amour, son aide et son soutien quotidien. Un grand merci aussi à tous mes amis qui ont toujours été là dans les bons comme dans les mauvais moments.
REMERCIEMENTS
LISTE DES FIGURES ... vii
LISTE DES SCHÉMAS ... X LISTE DES TABLEAUX ... xii
LISTE DES ABBRÉVIATIONS ... xii
RÉSUMÉ ... XV CHAPITRE I INTRODUCTION ... 1
1.1 Introduction à la glycobiologie ... 1
1.1. l Importance des interactions multivalentes protéines-glucides ... 3
1.2 Introduction aux dendrimères ... 4
1.2.1 Généralités sur les dendrimères ... 4
1.2.2 Historique de synthèse des dendrimères ... 7
1.2.3 Introduction aux glycoclusters et glycodendrimères ... 14
1.2.4 Autres type de dendrimères et leurs applications ... 20
CHAPITRE II CIBLE THÉRAPEUTIQUE 1 - BIOFILM D'
ESCHERJCHJA
COLI ... 312.1 Introduction aux infections du tractus urinaire ... 31
2.1.1 Problème de résistance aux antibiotiques ... 32
2.1.3 Biofihn bactérien ... ... ... 3 7 2.1.4 Rôle du pilus de type 1 dans l'adhésion des UPEC aux parois urinaires 38
2.1.5 Interaction du FimH avec les résidus mannosides ... 39
2.1.6 Objectif du travail décrit dans la section 2.2 ... ... 45
2.1. 7 Description des différentes études menées ... ... .4 7 2.2 Effect of Dendrimer Generation and Aglyconic Linkers on the Binding Properties of Mannosylated Dendrimers Prepared by a Combined Convergent and Onion Peel Approach ... ... 51
2.2.1 Abstract ... ... 53
2.2.2 Introduction ... .... 54
2.2.3 Results and discussion ... 56
2.2.4 Materials and methods ... ... ... ... 68
2.2.5 Conclusion ... ... 85
2.2.6 References ... ... 87
2.2.4 Supporting Information .... ... ... ... 94
CHAPITRE III CIBLE THÉRAPEUTIQUE 2- GALECTINES ... ... ... .... 150
3 .1 Introduction aux galectines ... ... ... 150
3.1 .1 Introduction à la protéine GRIFIN ... 155
3 .1.2 Dérivés de ligands sulfatés ... ... 161
3.1.3 Synthèse de nouveaux glycomimétiques sulfatés pour l'inhibition sélectives des galectines ... ... ... 166
CHAPITRE IV CONCLUSION ... 171
ANNEXE A PARTIE EXPÉRIMENTALE COMPLÉMENTAIRE AU CHAPITRE I ... ... ... ... ... 173
ANNEXE B CHICKEN GRIFIN: STRUCTURAL CHARACTERIZATION IN CRYSTALS AND IN SOLUTION ... ... 190
ANNEXE C PARTIE EXPÉRIMENTALE COMPLÉMENTAIRE AU
CHAPITRE III ... ... ... 239 RÉFÉRENCES ... ... 276
Figure Page
1.1 Représentation schématique d'une membrane cellulaire ... 2 1.2 Récepteurs typiques qui reconnaissent et lient les saccharides à la surface
cellulaire . . . .. . ... .. . .. . .... .. . . .. .... . . .. ... ... .... . . .. .... .. . . .. ... . . .. ... 3 1.3 Représentation schématique des unités constitutives d'un dendrimère... 6 1.4 Classification des polymères .. . . ... ... .... . . .... ... . ... . .. . .. . . .. .... .. . . 7 1.5 Différentes stratégies de synthèse de dendrimères 10 1.6 Exemples de structures glycodendritiques « glycocluster et
glycodendrimère
» ... ... .... .... . . ... ... ... . . ... .... ... . . .. ... .. . . .. .... .. . .
15 1.7 Structures de quelques dendrimères commerciaux utilisés pour la synthèsede glycodendrimères ... 19 1.8 Représentation des dendrimères 2 et 7 combinés au cuivre (Il). ... 29 2.1 Vessie atteinte d'une cystite et reins de pyélonéphrite dans un tractus
urinaire infecté par Escherichia coli ... 32 2.2 Étude SMART de la Prévalence des ESBLs d' E. coli dans le cas
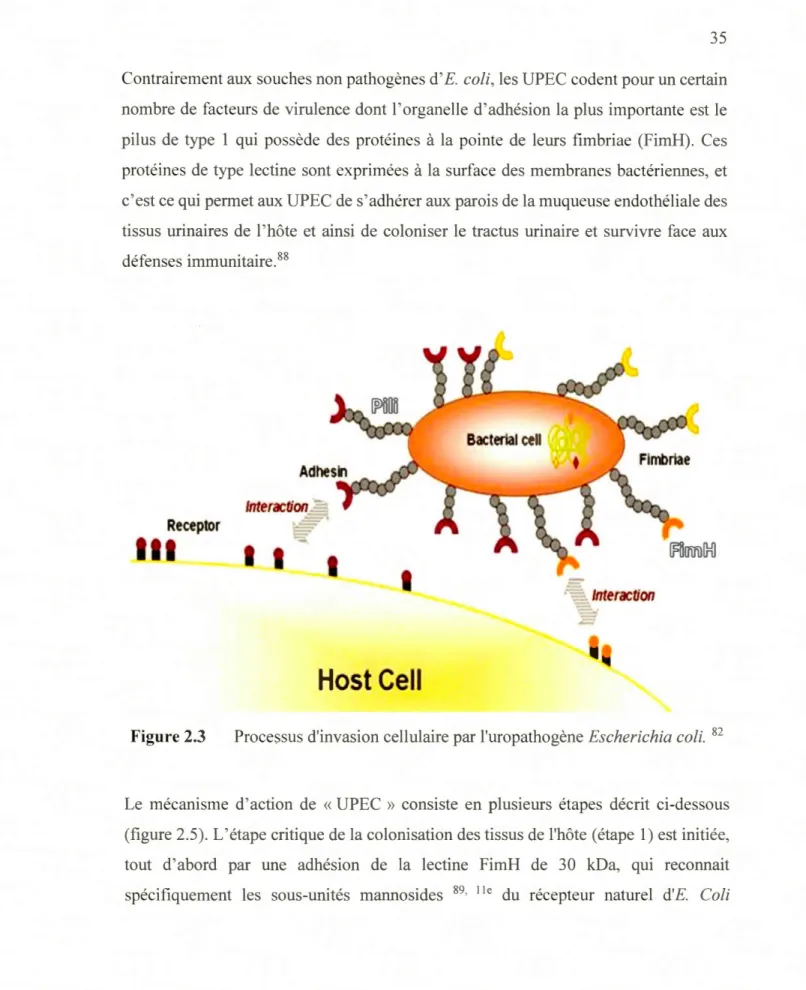
d'infections urinaires dans le monde de 2009 à 2011 ... 33 2.3 Processus d'invasion cellulaire par l'uropathogène Escherichia coli... 35 2.4 Structure cristalline et moléculaire de l'Uroplakin la ... 36
2.5 Etapes de formation du biofilm bactérien... 37 2.6 Structure du pilus porteur de l'adhésine FimH... 39
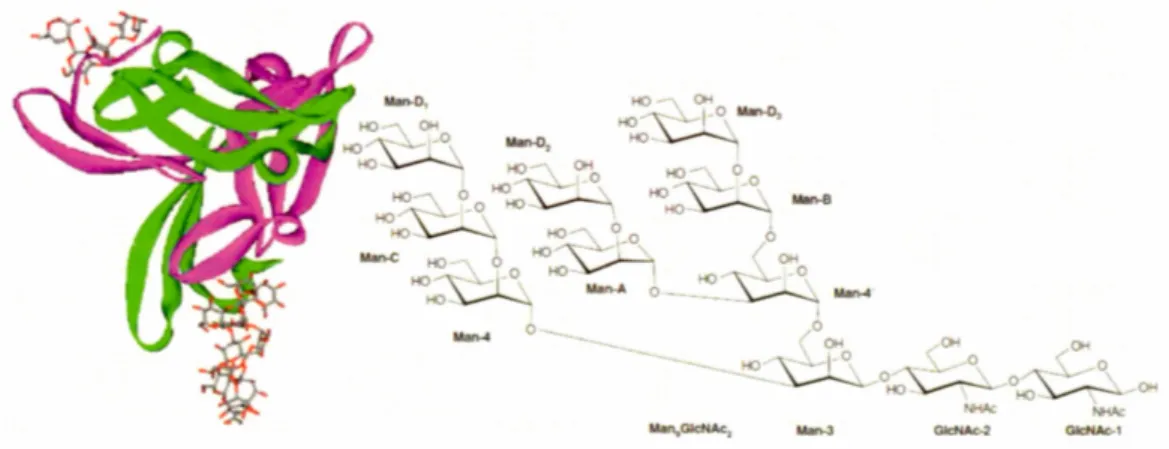
2.7 Structure par Rayons-X du n-Heptyl a-D-Mannopyranoside (HM) avec le FimH à Porte Tyr fem1ée... ... 41 2.8 a) Modélisation moléculaire de la réticulation du tétramère 11 de quatre
monomères de concanavaline A, illustrant la capacité du composé 11 à former des réseaux réticulés multiples et insolubles. b) structure cristalline de la ConA. .. . .. .... . .. . . ... ... . . .. . ... .... . . ... .... .... . .. . . ... .. . . . .. . . ... ... . . ... .... . . .. . 44 2.9 Microscopie confocal du Biofilm de P. aeruguinosa. (A) Formation de
colonies de P. aeruguinosa en l'absence du dendrimère FD2. (B) Absence de fmmation des colonies de P. aeruguinosa en présence du dendrimère FD2 ... 45 2.10 Schéma illustrant la stratégie thérapeutique anti-biofilm choisie... 46 2.11 Quelques structures dotées d'un cœur phosphorylé synthétisées... 48 2.12 Étude prévisionnelle par modélisation moléculaire par
«
docking»
dumannose pegylé (voir section 2.2) dans le CRD du FimH en portes tyrosines fermées (PDB 4 LOV). .. . ... . . ... ... . . .... . . .. . . .. .... .. . . .. ... . . . 50 3 .1 Trois types architecturaux représentants les différentes sous-familles de
galectines . . .. . . .. .. .. . . .. .. . . .. . . . .. . .. . .. . . .. . .. . . .. .. . .. . . .. .. . .. .. . . .. . . .. . .. . .. . . .. . .. . .. . . 151 3.2 Ligands naturels se liants préférentiellement au CRD des galectines ... 154 3.3 Exemples d'inhibiteurs naturels possédants une meilleure affinité pour les
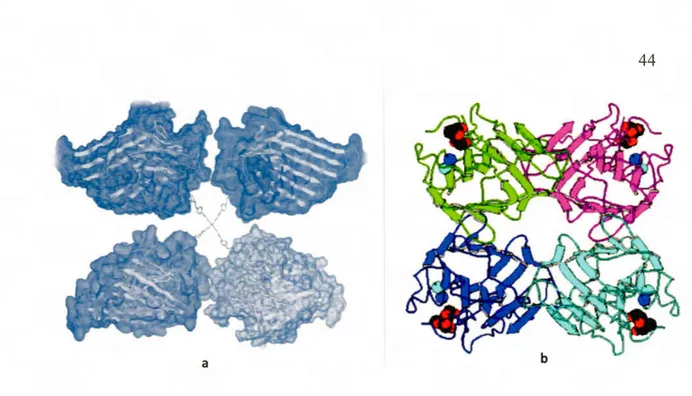
galectines . .... .... .. . . .. . ... .. . . .. . .... .... .. ... . .... ... . . . .. . . .. .... . . .. . .. . ... . ... ... . . .... . . . .. . . .. 154 3 .4 Structure monomérique de la protéine C-GRIFIN représentant le pli
typique ~-sandwich ainsi que le site de liaison au ligand (lactose) ... 157 3.5 Représentation de la densité électronique du ligand en contact avec les
stabilisant ce dernier dans le site de liaison du carbohydrate chez les C-GRIFIN (B) ... ... 158 3.6 Effet anomérique de 14 expliquant la formation stéréosélective de 15... 160 3.7 Galectine-8 humaine (surfaces de Connolly et sites de liaison) en
interaction avec le lactose sulfaté . .. .. . .. .. .. .. .. .. . .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. .. 163 3.8 La galectine-3 reste soluble en présence d'un seul ligand glycoside
multivalent, mais elle devient totalement insoluble lorsqu'elle forme un agrégat avec plusieurs glycosides tétravalents .... ... ... .... .... .... .. .. . 165 3.9 Exemples de glycodendrimères tri-, tétra- et hexavalents ciblés pouvant
Schéma
1.1 Mécanisme proposé par Sharpless et al. de la réaction de cycloadition
1,3-dipolaire pour la formation régiosélective d'un triazole. ... 12
1.2 Mécanisme proposé par Fokin/Sharpless et Medal pour la réaction CuAAC ... 14
1.3 Mécanisme de la réaction click de type thiol-ène à initiation radicalaire ... 23
1.4 Synthèse du dendrimère phosphorylé 2 . . .. ... . .. . . . .. .... ... . . ... .. . .. . . . .. ... . . .. . .. 24
1.5 Préparation du monomère 5 ... ... 25
1.6 Synthèse du glycodendrimère phosphorylé allylé 6 ... 25
1. 7 Synthèse du dendrimère phosphorylé 7 ... .. . ... .. . . .. ... ... . ... ... .. ... ... . 26
2.1 Synthèse du dendrimère 11 tétravalent par la réaction de Sonogashira : meilleur inhibiteur de la librairie avec un Kd de 0,45 nm ... 42
3.1 Synthèse du ligand analogue methyl ~-D-lactopyranoside 15 ... 159
3.2 Mécanisme détaillé de la sulfatation du résidu ~-D-lactopyranoside 15 .... 162
3.3 Approche pour la synthèse du sel (2-azidoethyl) 3-0-sulfo-~-D-lactopyranoside de sodium 21 .... .. ... ... .... 167
3.4 Synthèse du 7-(2-azidoethoxy)-2-naphthol 25 ... 168
Tableau Page
2.1 Affinités relatives des composés mannopyranosylés au FirnH des souches
Alpha
Ac Acétyl
Anhydride acétique
AcOEt Acétate d'éthyle
Arg Arginine
Asp Aspartique
Asn Asparagine
Béta
BU2SnO Oxyde de dibutylétain
oc
Degré CelsiusCCM Chromatographie sur couche mince
CDCb Chloroforme deutéré
CRD Domaine de reconnaissance du carbohydrate
CuAAC Cu-catalyzed azide-alkyne 1,3 dipolar cycloaddition
Déplacement chimique
Oxyde de deutérium
E. coli Escherichia coli
éq. Equivalents
G(n) Génération (n)
Glu Glutamate
Gln Glutamine
GRIFIN Galectin Related Inter-Fiber protein
h Heure
Hz Hertz
His Histidine
Ko Constante de dissociation
Lys Lysine MeOH Méthanol mL Millilitres µM Micromolaires MHz MégaHertz mm Minutes
ppm Partie par million
PAMAM Poly(amidoamine)
PEG Poly( éthylèneglycol)
RMN'H Résonance magnétique nucléaire du proton
RMN3Ip Résonance magnétique nucléaire du phosphore
rt Room temperature
Ser Sérine
Substitution nucléophile
En science du vivant, toute cellule est dotée de dérivés glycanes à enchevêtrement multi-antenaire en composantes structurelles de surface. Ces dérivés glycanes constituent des ligands permettant l'adhésion et la colonisation tissulaire par des pathogènes dans des cas d'infections bactériennes et virales. Différents dendrimères ayant des fonctionnalités périphériques et des espaceurs variés sont considérés comme de nouveaux agents thérapeutiques potentiels qui pourraient être utiles pour l'inhibition sélective de la formation des biofilms bactérien d' E. coli, ainsi que des galectines et des cellules cancéreuses. Dans une première section, nous décrivons brièvement la synthèse de quelques structures dendritiques comportant des métaux, qui agiraient comme agents anti-cancéreux. Ceci représente le fondement d'un premier article en cours de rédaction, dont ma contribution est co-auteur à part égale avec le Dr. Tahir. Dans un second article dont je suis l'auteure principale, nous avons synthétisé une chimiothèque de glycodendrimères mannosylés, pour lutter contre la formation et/ ou développement de biofilm bactérien grâce à la chimie click catalysée par cuivre. Les dendrons mannosylés ont été construits autour d'échafaudages variés allant de 2 à 18 par « pelure d'oignon », des aglycones à courtes et longues chaines ont été utilisé afin d'évaluer leurs effets sur la cinétique de liaison. Ces glucides ont été conçus pour lutter contre les infections urinaires en inhibant la formation de biofilms bactériens, neutralisant ainsi la pointe de leurs fimbriae contre les récepteurs d'oligomannosides naturels « uroplakine la » exprimés sur les tissus uroépithéliaux. Les études préliminaires en DLS de réticulation de la lectine ConA par les dendrimères mannosylés synthétisés ont démontré leurs potentiels à être utilisés comme nouveaux agents thérapeutiques pour lutter contre l'adhésion d' E. coli et la formation de biofilms. Dans une troisième section, des glycoconjugués ont été synthétisés dans le but de f01mer un inhibiteur sélectif des galectines. Pour ce faire, une réaction de sulfatation a été utilisée pour préparer des glycoconjugués sulfatés en 0-3'. Ce groupement sulfaté permet une meilleure affinité et une meilleure inhibition de la galectine que son ligand naturel. En parallèle, cetiaines de ces structures ont également conduit à une participation dans une troisième publication, sur l'étude structurale et fonctionnelle de ces lectines, notamment chez la lectine GRIFIN, afin de mieux comprendre son rôle.
INTRODUCTION
1.1 Introduction à la glycobiologie
En science du vivant, tout système est doté de composantes structurelles principales, allant des acides nucléiques aux protéines. Leur abondance naturelle égalerait presque le groupe des glycanes, présents dans la nature sous forme de polysaccharides et à la surface cellulaire des mammifères sous forme de glycoconjugués liés à des protéines, à des lipides ou encore à des constituants cellulaires appelés, respectivement, glycoprotéines, glycolipides et protéoglycanes à enchevêtrement multi-antenaires (Figure 1.1 ).1 Ces oligosaccharides constituent des transducteurs de signal entre les
milieux extra- et intracellulaires lors de plusieurs processus biologiques. 2 En effet, ces dérivés glycanes peuvent être ciblés par des récepteurs de toxines, d'anticorps ou encore par des protéines liants les glucides (lectines) exprimés par les agents pathogènes. Ils constituent donc des ligands permettant l'adhésion et la colonisation tissulaire par des pathogènes dans des cas d'infections bactériennes et virales (Figure 1.2). 3 Ils peuvent aussi être sollicités lors d'évènements tels que la reconnaissance
cellulaire, la défense immunitaire, la régulation de la croissance, les processus internes, l'apoptose cellulaire et la xénotransplantation. 4
Outside of cell Cell membrane lnslde of cell (cytoplasm) Figure 1.1
The Fluid Mosaic Madel
proteins Cholesterol
Représentation schématique d' une membrane cellulaire.1b
L'omniprésence de ces glycocomposants cellulaires a suscité l' intérêt des scientifiques, et a permis de compiler leurs différents éléments constitutifs. Comme il est courant pour les acides aminés dans les protéines, des substitutions sur les sucres telles que la phosphorylation ou la sulfatation peuvent jouer un rôle dans le métabolisme cellulaire5 ou servir d'entremise dans les processus d' inflammations.6 Cette modification post-synthétique souligne leur implication dans le codage génétique et l'activité cellulaire. Effectivement, la présence de plusieurs groupes hydroxyles et du lien glycosidique permet de mettre en évidence la capacité particulière des glucides à coder la bio-information. 7 Il est donc essentiel de bien définir la relation structure-activité, 8 qui survient par le biais de reconnaissance intermoléculaire par liaison hydrogène et interaction hydrophobe. Ceci fait de ces dérivés glycanes un concept de clefs qui interagissent avec des serrures de récepteurs moléculaires naturelles. 9 Ce concept a été introduit initialement par Fischer, afin de schématiser la spécificité des interactions entre les enzymes et leurs substrats.10
Figure 1.2
Enzyme
Toxm
Gtycopro em Glycol d
Récepteurs typiques qui reconnaissent et lient les saccharides à la surface cellulaire. 4e
1.1.1 Importance des interactions multivalentes protéines-glucides
Les interactions entre les glucides monovalents et les protéines sont caractérisées par des constantes d · association plutôt faibles de l'ordre du millimolaire (mM) avec une spécificité et une sélectivité limitée pour une seule unité saccharidique.11 Toutefois, un
ligand présent sur une surface extracellulaire expose naturellement plusieurs unités de saccharides de manière agencée, augmentant ainsi exponentiellement la force d "interaction avec le récepteur par cet effet synergique et coopératif multivalent connu sous le nom d'effet «cluster glycoside ou dendritique».12 Ce phénomène stabilisateur
par réticulation macroscopique a initialement été observé avec les récepteurs de asialoglycoprotéines présents sur les hépatocytes.13 De plus, cette stabilisation stérique
est décrite dans plusieurs exemples.12a-c, 14, 12e, 12g Étant présent à une certaine concentration, le ligand multivalent induit une multiple agrégation ligand- récepteur en se liant aux sites de reconnaissance des récepteurs adjacents, phénomène connu sous l'appellation "cross-linking". Par conséquent, la multivalence d'un glycoside est favorisée dans la nature lors de phénomènes biologiques car elle peut mener à une affinité et sélectivité accrue vis-à-vis d'un CRD (domaine de reconnaissance des glucides) d'un récepteur donné, par rapport aux interactions monovalentes en occupant entièrement un site actif à la fois.15 Il n'est pas à omettre, que cette reconnaissance ligand-récepteur dépend de plusieurs paramètres, dont la structure tridimensionnelle du récepteur, la valence et le nombre d'unités saccharides à la surface du ligand ainsi que la nature et taille des espaceurs qui lient ces unités monomériques. C'est pourquoi les interactions multivalentes sont considérées comme une stratégie omniprésente dans la nature pour un large éventail d'applications, et elles offrent de nombreux avantages qui ne peuvent être atteints avec les interactions monovalentes. Dès lors, les structures synthétiques telles que les dendrimères (présentés ci-dessous) peuvent être utilisées pour optimiser des interactions à faible affinité.16
1.2 Introduction aux dendrimères 1.2.1 Généralités sur les dendrimères
Les dendrimères sont des macromolécules synthétiques monodispersées, de structure tridimensionnelle bien définie, multivalentes et hyper-ramifiées. Le concept de structure polymérique hyperbranchée tridimensionnelle a tout d'abord été introduit par Paul Flory17 en 1940. Trente-huit ans plus tard, le scientifique allemand Fritz Vogtle18 synthétise en 1978 des molécules polyamines qu'il appela « molécules en cascade ». Ce n'est qu'en 1985, que Newkome 19 et Tomalia 20 ont introduit le te1me « dendrimère» qui provient de l'association de dendron (arbre ou branche en grec) et meros (partie en
grec). Ils ont ainsi rapporté la synthèse des premiers dendrimères selon un processus itératif divergent, nommés respectivement « arborols » et « PAMAM ».
Les dendrimères sont généralement de forme globulaire ou pseudo-globulaire, constitués d'unités de branchement répétitives qui se lient chimiquement les unes aux autres de façon arborescente autour d'un cœur central polyfonctionnel. Ceci fonne différentes générations de dendrimères pouvant comporter divers groupements fonctionnels en périphérie. Ces groupements interagissent principalement avec l'environnement extérieur et constituent l'une des unités les plus importantes pour déterminer les propriétés finales du dendrimère.2 1 En général, chaque couche d'unité
de branchement supplémentaire double le nombre de groupement périphérique et augmente le nombre de génération du dendrimère (Figure 1.3).22 Le choix du cœur
central et des unités de branchements aura un effet important sur la densité des groupes de surface présentés à chaque génération.23 Un dendrimère de quatrième génération à
noyau tétra-fonctionnel aura 64 groupes de surface, tandis qu'un dendrimère doté d'un noyau trifonctionnel en aura seulement 48.20-21 La flexibilité du cœur central et des branches aura donc un effet important sur la structure du dendrimère. Les unités à liaisons multiples rigides conduisent à une structure plus grande et plus ouverte, tandis que les unités plus flexibles conduisent à des dendrimères globulaires compacts dues aux branches flexibles qui se replient sur elles-mêmes fonnant des cavités internes qui peuvent être utilisées pour encapsuler de petites molécules d'intérêt. 24
Figure 1.3
Grouoements de surface
----· Branches
Point focal --- · --- • Dendron
Représentation schématique des unités constitutives d' un dendrimère. n b
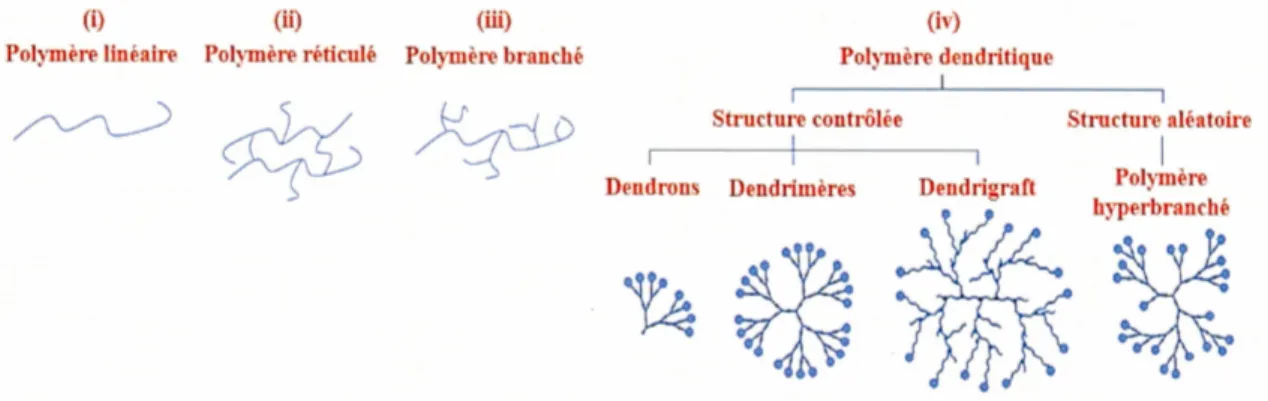
Les dendrimères représentent la quatrième classe maJeure des architectures polymériques.23 • 25 À la différence des polymères (Figure 1.4), ils peuvent êtres synthétisés selon un processus itératif très bien contrôlé, grâce à des stratégies versatiles et reproductibles qui permettent de définir parfaitement leur structure tridimensionnelle en dépit de leur grandes masses moléculaires, ainsi que leurs vastes expansions dans l'espace.26
(i) (ü) (fu)
Polymère linéaire Polymère réticulé Polymère branché
Dendrons
(iv) Polymère dendritique
Structure contrôlée Structure aléatoire
1
*~·~
Figure 1.4 Classification des polymères. 23
La chimie des dendrimères suscite un grand intérêt et fait l'objet d'un développement constant depuis plusieurs décennies compte tenu des vastes champs d'application des dendrimères, que ce soit en science des matériaux, science environnementale et catalytique mais surtout son utilisation accrue en science du vivant et en science pharmaceutique. Dans cette optique, une multitude d'approches synthétiques ont été développées afin d'améliorer le contrôle des structures dendritiques, leur caractère hydrophile/hydrophobe et leur avidité. Des méthodes de purification et de caractérisation mieux adaptées ont aussi été mises en place.27 Ces différentes stratégies sont décrites ci-dessous.
1.2.2 Historique de synthèse des dendrimères
Effectivement, les premières molécules en cascade furent synthétisées en 1970 par Vogtle et al.18 Bien qu'elles ne soient pas encore appelées dendrimères, ces
macromolécules hyper-ramifiées sont les premiers exemples de dendrimères trouvés dans la littérature. Contenant un cœur aromatique ou aliphatique et un squelette de poly (propylène-imine) (PPI), les molécules en cascade développées par le groupe Vogtle ont donné naissance à l'un des types de dendrimères les plus utilisés.
Actuellement connus sous le nom de dendrimères PPI, ils sont disponibles dans le commerce sous le nom d'Astramol TM (DSM, Sigma-Aldrich) et ont été largement
étudiés pour diverses applications.24a, 28 La synthèse des dendrimères PPI peut être obtenue de manière divergente en commençant par l'ajout d'acrylonitrile à une diamine primaire par addition de Michael. Les groupements terminaux de nitriles résultants sont ensuite réduits en amines par catalyse. Ce cycle de synthèse peut être répété pour former les générations suivantes telles que reportées dans la littérature. 29 Comme mentionné plus haut, les prochains développements majeurs dans la chimie des dendrimères ont été fait en 1985 avec le système en cascade arborescent préparés par le laboratoire de Newkome.19 Ainsi que la synthèse divergente introduite par Tomalia
et al.20
1.2.2.1 Méthodes de synthèse
Les dendrimères peuvent être préparés par deux voies de synthèse principales, de manière divergente ou de manière convergente (figure 1.5).
1.2.2.1.1 Méthode divergente
Qualifié d'approche « en cascade », elle est introduite en 1985 par Tomalia et al.,20
c'est une synthèse interne qui utilise une série d'étapes itératives d'activation et d'addition, en partant d'un cœur central (A) vers la fixation de groupements tem1inaux en périphérie, couche par couche jusqu'à l'obtention d'un dendrimère de génération G(n) voulu (voir figure 1.5). Le groupe de Tomalia a introduit les dendrimères poly( amidoamine) (P AMAM) qui sont disponibles commercialement (Dendritech, Sigma-Aldrich) mais qui peuvent aussi être synthétisés de manière divergente à paiiir d'un cœur primaire à terminaison amine, tel que l'éthylènediamine (EDA). L'acrylate de méthyle est ajouté aux amines terminales par une addition de Michael, par la suite, une amidation des groupements ester terminaux résultants en utilisant de l'EDA,
régénère les groupements aminés terminaux et augmente le nombre de générations de la structure. La synthèse peut ainsi être répétée pour obtenir les générations suivantes. C'est une méthode de croissance exponentielle. Néanmoins, les générations supérieures peuvent devenir très encombrées à la périphérie, ce qui conduit à une fonctionnalisation incomplète et donc à des défauts structurels, augmentant la polydispersité des macromolécules. Bien que l'ajout d'un large excès de réactifs puisse être envisagé pour contourner ce problème, une limite stérique à la croissance régulière, appelée « empilement dense de Gennes
»
est invariablement atteinte à une certaine génération. De plus, la purification des dendrimères est difficilement achevable du fait de la similitude des propriétés chimiques des structures macromoléculaires obtenues. Malgré tout, cette méthode de synthèse constitue une approche efficace donnant accès à une multitude de structures dendritiques commerciales aux propriétés pharmacologiques reconnus comme étant non-toxiques et non-immunogènes.301.2.2.1.2 Méthode convergente
Introduite en 1990 par Hawker et Fréchet,31 elle consiste tout d'abord, à la synthèse
individuelle de bras hyperbranchés appelés
«
dendrons », préparés de l'extérieur à l'intérieur couche par couche et possédant des groupements fonctionnels en périphérie et une fonction focale réactive. Cette dernière permet le couplage d'un ou plusieurs dendron(s) sur un second échafaud ou sur un cœur dendritique formant ainsi le dendrimère final de génération G(n) souhaité (Figure 1.5). Cependant, à des générations élevées, un encombrement stérique des grosses entités (très grands dendrons) à coupler peut rendre difficile la fixation à une molécule de cceur, en induisant une dissimulation de ses fonctions réactives.23 L'avantage principal de cette méthode réside dans la facilité de purification des dendrimères qui ont des propriétés physico-chimiques distinctes mais aussi des structures différentes et plus importantes que les sous-produits à chaque étape.32 Cette méthode sera privilégiée lors de lasynthèse de molécules mixtes présentant différentes fonctions périphériques et/ou intemes.12a. 12b. 33
1.2.2.1.3 Méthode« pelure d'oignons»
Récemment développée par notre laboratoire, cette méthode consiste à incorporer divers échafauds de molécules possédant un groupement fonctionnel à leurs périphéries en utilisant différentes réactions chimiques adaptés à chaque couche ou génération. Cette architecture d'échafauds variés, au sein d'une même molécule, permet d'introduire une multifonctionnalité et d'acquérir diverses propriétés. 34a_ 123· 12b. 34b-d
(Méthode Divergente)
y·~ ·y
ol.
..,-w
·="'
A3 coeur Couplage G0 (3) G1 (6) G2 (1 2)( Méthode Convergente ) ~ Même unité de répétition ~ ~ _
~
Y
~V
Y
oiY'?&
~ eurÔ
AB2'l
AB2y
--A3 coeur Activation/
G0 (3) G2 (4) Couplage G2 (8)
Onion peel ; Par Méthode Divergente o u Convergente
Î ~ÏA t
AB4 G2 (72) - G3 (21 6) A6 coeur G0 (6) Figure 1.5 Différentes unités de répétitions1.2.2.2 Importance de la Chimie
«
click » ou CuAAc«
Cu-catalyzed azide-alkyne 1,3-dipolar cycloaddition » en synthèse de dendrimèreUn soin particulier doit être apporté à la conception de blocs de construction dotés de multiples fonctionnalités compatibles.36 L'introduction de la chimie click en 2001 par Sharpless et al.37 a révolutionné le domaine de la synthèse des dendrimères. Le
mécanisme réactionnel proposé par ce dernier est une réaction non concertée mettant en jeu plusiems intermédiaires réactionnels et complexes activés (Schéma 1.1 ). Puisque la synthèse des dendrimères est par définition un processus en cascade, il est nécessaire d'utiliser des réactions à haut rendement qui fonctimment de manière fiable en présence de multiples fonctionnalités diverses. La chimie click est parfaitement adaptée à cette fin. Les réactions de click sont une classe de réaction dans laquelle deux unités sont couplées, avec des rendements quantitatifs et peu de produits secondaires. Trois réactions sont actuellement connues sous le nom de réactions de click: la première et la plus communément employée est la cycloaddition alcyne-azide catalysée par le cuivre (I) (CuAAC) (Schémas 1.1 et 1.2), la seconde est la cycloaddition de Diels-Alder (DA), et enfin la réaction de couplage thiol-ène (TEC) (Schéma 1.3) ou thiol-yne. La synthèse du premier dendrimère préparé à l'aide de la chimie click a été réalisée en 2004, en utilisant la réaction click CuAAC, où diverses structures à base de triazole ont été générées par une collaboration entre Hawker, Fréchet, Sharpless et Fokin.38 Les dendrimères ont été préparés de manière convergente en cliquant sur un dérivé propargyl un azoture en conservant un point focal fonctionnalisable. La séquence a été répétée jusqu'à ce que la génération souhaitée soit atteinte et les dendrons résultants ont ensuite été cliqués sur un noyau de polyacétylène. Telle que mentionnée précédemment, la chimie click est largement utilisée dans la préparation des dendrimères. D'ümombrables exemples sont recensés au sein du groupe Roy dans l'utilisation de la chimie click CuAAC pour synthétiser des dendrimères et glycodendrimères à application biologique, envirom1ementale et pharmaceutique. 34a, 12a-c, 12e-g, 33, 34b-d
.N, R2 (E) N' W
M
R1..
H ,N, R2 {D) N' W>=Z
R1 Culx R1=
H (Cul xJ R1==
Cul x {A)Schéma 1. 1 Mécanisme proposé par Sharpless et al. de la réaction de cycloadition 1,3-dipolaire pour la formation régiosélective d'un triazole.37
Ainsi, la « chimie click
»
CuAAC constitue l'un des modes de couplage les plus utilisés ces dernières années dû à son efficacité et sa régiosélectivité. Découlant de la cycloaddition de Huisgen 1 ,3 dipolaire initiale qui n'était pas régiosélective à cause du chauffage prolongé, celle-ci permet, d'obtenir exclusivement un cycle triazole disubstitué en 1,4 dans des conditions douces. Un mélange de dérivés triazole disubstituée en 1 ,4 et 1.5 n ' est donc plus obtenu.39Depuis, plusieurs groupes de recherche se sont focalisés dans l' optimisation des conditions réactionnelles.36, 40 Dans notre travail de recherche, nous avons privilégié l'utilisation du sulfate de cuivre 5 fois hydraté (CuSÜ4.SH20) avec l'ascorbate de sodium (Vitamine C) dans un mélange (3:1) THF/H20 (v/v),33 car l'ajout d'une base n'est pas requise dans ce cas précis, contrairement aux conditions d'utilisation de Cu (I) dans un milieu exclusivement organique.40a Dans ces conditions choisies, le cuivre (Il)
est réduit in situ en cuivre (0) par l'acide ascorbique, et par comproportionnation du Cu (II) initial et du Cu(O) généré, le Cu (I) est à son tour généré. Les sels de cuivres (II) permettent une réaction rapide et sélective à température ambiante, favorable pour la formation de l' isomère 1,4. Le premier mécanisme proposé par Sharpless de la CuAAC à la (Schéma 1.1) est initié par le cuivre (I) qui se complexe par addition oxydante à l'alcyne terminal pour fom1er un complexe acétylure (A). Ensuite, le côté enrichi en électrons de l'azoture se complexe avec le cuivre (B). Cette étape est responsable de la régiosélectivité de la réaction. En effet, la formation du métallocycle à 6 chaînons (C) est rendu possible grâce aux orbitales 3d du cuivre. Cependant, le métallocycle se contracte en un cycle à 5 chaînons (D) et l'élimination réductrice du cuivre dans la dernière étape permet la fom1ation du complexe triazole 1,4-disubstitué désiré (E).41
Un autre mécanisme a également été avancé par Fokin et sharpless42 dans lequel il y aurait l'intervention de deux cuivres lors de la réaction catalytique. Le passage supposé par des espèces di-cuivrées est également invoqué dans le mécanisme proposé par Meldal et al. 4
oa,
qui considère aussi que l'azoture est coordiné à un troisième atome de_)
Schéma 1. 2 Mécanisme proposé par Fokin/Sharpless et Medal pour la réaction CuAAC.42, 4üa
1.2.3 Introduction aux glycoclusters et glycodendrimères
La haute densité de fonctionnalisation des dendrimères utilisant de petites entités telles que les saccharides a donné naissance à une nouvelle classe de néoglycoconjugués monodispersés multivalents tels que les glycoclusters et les glycodendrimères,34a, 12a-c,
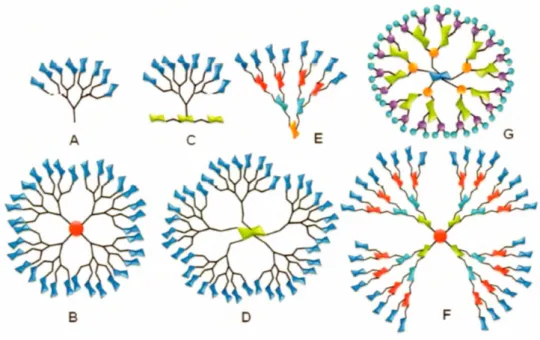
12e-g, 33, 34b-d, 43 décrite ci-dessous dans ce chapitre. Leurs structures (Figure 1.6) et
propriétés uniques ont motivé leur utilisation dans de nombreuses applications, en tant que systèmes de délivrance de médicaments,44 de thérapie génique anticancéreuse, mais aussi en tant qu'agents antibactériens, antiviraux et antitumoraux. 10, 45 De plus,
des études biologiques menées pour déterminer la biocompatibilité, la biostabilité et l' immunogénicité des dendrimères occasionnent leurs utilisations accrues.46
B
Figure 1.6 Exemples de structures glycodendritiques
«
glycocluster et glycodendrimère »351.2.3.1 Glycoclusters
Les « glycoclusters » peuvent être considérés comme des mimétiques des oligosaccharides multi-antennaires naturels. Ces structures glycoconjuguées multivalentes sont construites à partir d'échafaudages synthétiques ou commercials qui ne contiennent pas d'unités répétitives. Ces caractéristiques structurelles permettent de faire la distinction entre ces architectures à plutôt faible valence qui peuvent constituer une unité du corps d' un glycodendrimère multigénérationnel présenté dans la section suivante.
L'accessibilité synthétique à des structures assez petites, a amené l'utilisation d'une grande variété de glycoclusters basés sur des échafaudages multivalents ces dernières années. Des échafaudages aliphatiques ou aromatiques ramifiés, les calixarènes, les porphyrines et leurs dérivés, les peptides cycliques, les glucides et les cyclodextrines, ainsi que plusieurs autres structures centrales, furent utilisés comme cœur, pour concevoir de petits glycoconjugués multivalents ayant une avidité accrue par rapport aux glucides monovalents correspondants.16, 35
L'optimisation de ces systèmes et de leur valence fut investiguée, en introduisant des fonctions appropriées, avec des chaines de longueurs et flexibilité optimales.11ct, l Ie Ce qui a conduit à une amélioration spectaculaire des interactions entre protéines et néoglycoconjugués, permettant de trouver de meilleures structures pour une plus grande affinité de liaison avec les protéines correspondantes comparées aux structures monovalentes. Ceci confirme l'utilité de ces modifications pour la détermination des paramètres géométriques d'association, ainsi que les distances optimales entre les épitopes de saccharide. Il convient de noter que la majorité de ces glycoclusters ont également été utilisés pour construire des glycodendrimères multigénérationnels plus complexes, en particulier des systèmes orthogonaux ABx, tels que les dérivés de l'acide gallique. 35
Pour mieux comprendre le rôle critique des interactions oligosaccharides-récepteurs et de leurs mécanismes moléculaires à travers l'effet du cluster et accéder ainsi à des ligands synthétiques optimisés, plusieurs groupes de recherche ont fait preuve de créativité en proposant des plates-formes multivalentes originales qui pourraient permettre des valences, des dimensions et des orientations adaptées, comme par exemple, celles citées précédemment. Un large panel d'échafaudages multivalents utilisant la chimie click a été optimisé par Roy et al. , menant à la conception de candidats multivalents biologiquement actifs contre diverses pathologies.34a, 12a, 12b, 16, 12c, 12e-g, 33, 34b-d, 43
D'autre structures ont été investiguées par Santoyo-Gonzalez,47 ou encore, Burke et
al.48 qui ont étudié un ensemble de ligands basé sur un échafaudage macrocyclique bien
défini sur lequel trois résidus mannoside sont reliés à l'aide d'un linker pégylé. Un cœur hydropyran cyclooligolide a été obtenu selon une séquence synthétique itérative à multi-étapes impliquant notamment une macrolactonisation en étape clé dans des conditions de dilution élevée de Keck-Steglich.49 De plus, les études de modélisation
moléculaire ont prédit une séparation maximale entre les résidus de mannose d'environ 35 A 0 • Étant donné que les sites de liaison dans la lectine tétramèrique Concanavalin A (Con A) sont séparés de 65 à 70 A 0 , le ligand trivalent ne peut occuper simultanément deux sites de liaison au mannose dans Con A. Par conséquent, il pourrait être utilisé pour explorer les mécanismes de liaison de ligands multivalents en l'absence de l'effet chélaté. Effectivement, des tests en SPR avec Con A ont indiqué l'absence d'interactions non spécifiques, et a mis en évidence le fait que le glycocluster favorise et n'inhibe pas la liaison de la Con A. Les données suggèrent que le glycocluster est capable de se lier simultanément à deux ou trois tétramères Con A et de former des amas solubles à forte avidité pour les ligands inm10bilisés. 50
1.2.3.2 Glycodendrimères
Les glycodendrimères sont une classe intéressante de biomacromolécules synthétiques bien définies pouvant posséder une unité de répétition pour atteindre diverses générations. Ils ont initialement été conçus pour résoudre le problème de faible affinité rencontré lors des interactions carbohydrate-protéine dans de nombreux phénomènes biologiques. 25
Afin d'élargir notre compréhension sur ces structures, YC Lee, l'un des pionniers de la chimie des glycoconjugués et de la biochimie introduit « l'effet cluster-glycosides
»
133.Dans sa version largement répandue, on suppose que l'effet du cluster-glycoside provient de l'affinité accrue d'un glycoside multivalent vis-à-vis d'un CRD donné en occupant entièrement « un site actif » à la fois. Comme tous les autres dendrimères
organiques arborisant, les glycodendrimères peuvent prendre plusieurs architectures structurelles, car ils peuvent être préparés sous forme de dendrons, de dendrimères sphériques ou globulaires et même d'hybrides de dendrimères polymères appelés dendronisés.51 Faisant partie des dendrimères, les glycodendrimères peuvent également être synthétisés par des stratégies convergentes, divergentes,
«
pelures d'oignon»
(Figure 1.5), ou à double étapes utilisant un cœur hypercore. De plus, ils peuvent être synthétisés avec simplicité et à coût réduit, en optant pour une procédure à une seule étape pour la synthèse d'échafaudage interne, utilisant des méthodologies de polymères hyper-ramifiés. Ceci peut être réalisé sur la base de monomères AB2 commerciaux tels que les polyglycérols hyberbranchés, la polyéthylèneimine hyper-ramifiée (PEI) et les dendrimères Boltorn® de faibles dispersités (Figure 1.7).45
Les premières structures glycodendritiques rapportées par le groupe du Pr. Roy,52 ont été synthétisées par méthode divergente en phase solide sur résine de Wang. Ces glycodendrimères construits autour d'échafauds glycopeptidiques de L-lysines comportaient des acides sialiques en périphérie, afin de contrer l'hémagglutinine du virus de la grippe. L'introduction d'espaceurs de chloroacétylglycines, a permis d'obtenir de meilleures activités aux structures monovalentes de référence. D'une autre paii, la substitution des glucides en périphérie de ces structures, par des maimosides possédant un aglycone aromatique, a permis une meilleure interaction avec les bactéries uropathogéniques d' E. coli K12 par rapport aux ligands de références. Dans la même optique, d'autres structures de glycodendrimères multivalents ont été étudiées dans le but d'inhiber l'infection bactérienne uropathogénique causé par E. coli, en bloquant les interactions entre cellules hôtes et agents pathogènes. Ces glycodendrimères se sont avérés comme des inhibiteurs potentiels avec une grande affinité pour la lectine FimH. 53, 5
°
Ceci représente l'une des cibles thérapeutiques traitée dans mes travaux de recherche décrit, dont de plus amples détails seront donnés dans le chapitre 2.Tout un panel d'autres cibles thérapeutiques pouvant être visées par les glycodendrimères ont été étudiées et ont démontré des propriétés biologiques intéressantes, dont des aptitudes antivirales contre le VIH, une capacité inhibitrice des facteurs de virulence de la bactérie Pseudomonas aeruginosa PA-IL et PA-IlL,54 ou encore le ciblage des galectines-1, -3, -5 et -7, lectines impliquées dans le développement de certains cancer.16, 10
Aslramol·Dab G(3) dmdi'imer
PAMAM starburst™ G(3),dendrimer
Hyperbranc:hed polyglyoorol Boltorn demi.rimer H20
Figure 1. 7 Structures de quelques dendrimères commerciaux utilisés pour la synthèse de glycodendrimères.45
Grâce aux propriétés thérapeutiques des glycodendrimères, leur synthèse par obtention rapide et de manière contrôlée est primordiale. De ce fait, les différentes méthodes de synthèse énumérée précédemment permettent l'obtention de glycodendrimères à structures adaptées en fonction de la cible biologique à atteindre. L'élaboration sur mesure se fait tout d'abord par modification des saccharides périphériques en fonction de l' application thérapeutique, ainsi que les aglycones et de leurs flexibilités, sans oublier la valence de la structure et son aptitude de compaction pour une meilleure accessibilité des unités saccharides. En général, les groupements périphériques régissent la structure fonctionnelle du dendrimère. Toutefois, dans le cas des dendrimères appelés« core-functionalized », le noyau de la macromolécule détermine la majorité de ses propriétés.55 Il faut noter, que la disponibilité commerciale des structures dendritiques de type P AMAMs, Poly(propylene imine) (PPl), Boltorn® et polyglycérols (Figure 1. 7), a représenté un atout majeur dans 1 'élaboration rapide de glycodendrimères hyperbranchés dans certaines études. 16 Cependant, le contrôle de la croissance dendritique est déterminé par le nombre d'entités de branchement choisies de type AB2, ABJ ou à motifs multivalents tels que les dendrimères phosphorylés.34a, 12a, 12b, 16, 12c, 12e, 12f, 35, 12g, 33, 34b-d, 43
1.2.4 Autres type de dendrimères et leurs applications 1.2.4.1 Dendrimère phosphorylé
Bien que la majorité des dendrimères soient de nature organique, il existe de nombreux exemples de dendrimères contenant des hétéroatomes et / ou des centres métalliques. Des travaux révolutionnaires dans le domaine des dendrimères phosphorylés ont été réalisés par le groupe Majoral 3oa-c, 3oe en 1994 lors de la synthèse du premier dendrimère contenant un cœur phosphorylé.56 La synthèse a été réalisée par une séquence répétée de deux réactions, la première créant une liaison phosphore-oxygène
et laissant une structure terminée par un aldéhyde, et la seconde pour générer une liaison imine et laissant une structure à terminaison chloro. Tous les dendrimères examinés jusqu'à présent n'ont qu'un seul type de groupe de surface actif. Pour certaines applications, en particulier dans le domaine médical, il est souhaitable de pouvoir attacher plus d'un fragment à la périphérie pour un effet multivalent. Par exemple, un dendrimère qui délivre une molécule de médicament tout en fournissant simultanément une solubilité aqueuse.57
Touaibia et Roy ont utilisé des dérivés du cyclophosphazène biodégradables et biocompatibles en tant que plates-formes multivalentes permettant d'obtenir des glycocluster de a-D-mannosides hautement fonctionnalisés.58 L'utilisation d'une stratégie de synthèse en une étape efficace telle que le couplage de Sonogashira et la « chimie click » a donné une variété de glycoclusters autour du cyclotriphosphazène à différentes valences, espaceurs et arrangements spatiaux_44,34ct Des dérivés hexavalents ont été obtenus à partir de l'hexachlorocyclotriphosphazèhe (N3P3Cl6) commercial sur lesquels divers dérivés phénoliques ont été conjugués par substitution nucléophile. Un couplage croisé catalysé par Pd ou par
«
chimie de click » du ligand a -D-mannoside est effectué suivie d'une déprotection ultérieure dans des conditions de Zemplén ont donné des glyconjugués hexavalents avec d'excellents rendements (Section 2.2).34a, 34ct Des glycocodendrimères à valence plus élevée ont également été obtenus.Pour évaluér l'influence des paramètres structuraux régis par le coeur cyclophosphazène sur la valence et l'orientation spatiale, ainsi que sur la nature des espaceurs utilisés pour lier les maimosides, les auteurs ont réalisé des essais turbidimétriques cinétiques préliminaires avec Con A. Des complexes réticulés insolubles se sont formés rapidement pour les composés. En revanche, l' incorporation d'unités supplémentaires de mannosides ne conduit qu' à des améliorations statistiques de l'interaction et de l'affinité. Bien que les exemples soient assez rares, l'utilisation de ces cœurs phosphorés a généré des glycoclusters biologiquement pertinents. Par exemple, les glycodendrimères comp01iant des mam1osides ont montré des propriétés inhibitrices intéressantes contre l'adhérence d'Escherichia coli fimbrées de type 1 aux
érythrocytes de cochon d'Inde,59 ainsi que d'intéressantes propriétés de liaison à la Con
A.60 Dans notre travail, décrit dans la section 2.2, on utilisera particulièrement la chimie
click «CuAAC» afin de contrer les infections urinaires causées par E. coli.
Face à l'intérêt biologique que possèdent les dendrimères phosphorylés, un autre type de dendrimère phosphorylé ont été synthétisé afin d'y incorporer par la suite des métaux de cuivre II dans le but de cibler les cellules cancéreuse (voir annexe A). Ces dendrimères ont été synthétisés en utilisant la chimie thiol-ene et thiol-yne (TEC), qui est une réaction click émergeant dans le domaine de la synthèse des dendrimères en tant qu'alternative de CuAAC car la réaction de click de thiol-ène ne nécessite pas l'utilisation de catalyseurs de métaux de transition toxiques.61 La thiol-ène a été découverte il y a presque 100 ans et a été utilisée dans la construction de réseaux réticulés62. Cette réaction procède par l'addition de radicaux thiols à des doubles liaisons non activées, soit thermiquement, soit photochimiquement de manière anti-Markovnikov pour dom1er des thioéthers (Figure 1. 10). Bien qu'une initiation radicalaire puisse être obtenue en utilisant une lumière UV de 254 mn par homolyse de liaisons soufre-hydrogène, mais pour une génération de radicaux plus rapide, divers photo-initiateurs sont utilisés et les plus couramment utilisés sont la benzophénone et le DMP A. Cette réaction, telle que la CuAAC click, est très efficace et facile à exécuter. Elle peut même parfois être réalisée sans solvant. Roy et al. ont développé une approche orthogonale accélérée en combinant la chimie du thiol et la réaction SN2 pour construire des structures dendritiques multifonctionnels. 63 Hawker et al ont également des exemples d'utilisation de cette chimie pour la synthèse de dendrimères poly (thioéther) de 4ème génération en 8 étapes en utilisant des monomères commerciaux.64
Produit thiolène
,
•
R1- SH + Initiateur - - - ----,-- R1- S ou rayons UV/
Schéma 1.3 Mécanisme de la réaction click de type thiol-ène à initiation radicalaire.
Dans notre cas, on a d'abord synthétisé le coeur 1 dont la synthèse est détaillée dans la Section 2.2. Par la suite, le dendrimère 2 a été formé par couplage du thioglycerol sur les groupements propargylés de 1 comme illustré sur la (Schéma 1. 4) par chimie click de type thiol-yne en présence de DMPA, d' une fonction propargyl et d'un thiol sous des radiations de lumière UV (365 nm) (voir annexe A).
•
R1-SH +Initiateur - -- ---- R1-S ou rayons
UV
Schéma 1.3 Mécanisme de la réaction click de type thiol-ène à initiation radicalaire.
Dans notre cas, on a d'abord synthétisé le coeur 1 dont la synthèse est détaillée dans la Section 2.2. Par la suite, le dendrimère 2 a été formé par couplage du thioglycerol sur les groupements propargylés de 1 comme illustré sur la (Schéma 1. 4) par chimie click de type thiol-yne en présence de DMPA, d'une fonction propargyl et d'un thiol sous des radiations de lumière UV (365 nm) (voir annexe A).
HO OH
sy
( HO OH r s_)--,' 0Schéma 1.4 Synthèse du dendrimère phosphorylé 2.
Afin d'atteindre une plus grande multivalence, la construction d'un nouveau dendrimère phosphoré a été effectuée à partir d'un dendron trivalent allylé 5. La synthèse de ce bras est décrite dans la (Schéma 1. 5). Lors d'une première synthèse de Williamson, l'éther de dichloroéthyle a été couplé à 3 selon un mécanisme de type SN2 pour former le composé 4 avec un rendement de 62 %. Ensuite, le monomère 5 a été synthétisé, à paiiir de 4 en présence d'azoture de sodium avec un rendement de 83 %.
NaOH 50%, Bu4NHS04, rt, 36 h 62% NaN3,DMF, 85 ·c. 5 h 83%
Schéma 1.5 Préparation du monomère 5.
Le couplage des bras monomériques 5 a été effectué sur le cœur phosphoré 1 par chimie click pour former le dendrimère allylé 6 possédant 18 point d'ancrage en périphérie (Schéma 1.6). Finalement, le second dendrimère 7 a été obtenu par une alkylation de l'éther de dichloroéthyle et le composé 6 (Schéma 1.7), fom1é par un mécanisme radicalaire en utilisant une chimie click de type thiol-ene, dans les mêmes conditions utilisées lors de la formation du cluster 2 précédent. (Voir annexe A) Le dendrimère 7
a pu être caractérisé par RMN 31 P. La présence d'un seul pic de phosphore prouve la
substitution complète du dendrimère 7 sans formation de produits secondaires non désirés.
1 + 5
CuS04, NaAsc, THF/H2D, 50 ·c.
2 h, puis rt, 6 h 50%
Ces deux dendrimères phosphorés 2 et 7 synthétisés sont les premiers d' une grande chimiothèque que nous souhaitons construire dans notre laboratoire. L' intérêt biologique de ce type de dendrimère et leur possible application en tant qu'agents antitumoraux ou antimicrobiens suite à un couplage métallique (cuivre, argent, or) en périphérie, nous poussent à poursuivre nos investigations dans cette voie.
6 OH HS~ OH DMPA, DMF 365 nm, 2h 90% HO OH
'-Cs
OH \ HO~ S ~ O OH 0 , ~ HO~ s --- ·, 0 ---0 0 0 ~ 7Schéma 1.7 Synthèse du dendrimère phosphorylé 7.
HO OH
1.2.4.2 Dendrimères métalliques en tant que puissants agents antitumoraux et antimicrobiens
Une approche de développement de système de délivrance de médicament en utilisant des dendrimères, consiste à exploiter leur valence bien définie pour fixer des molécules
de médicaments anticancéreux à leurs périphéries. La charge de médicament peut être ajustée en faisant varier le nombre de générations du dendrimère, et la libération du médicament peut être contrôlée en incorporant des liaisons biodégradables entre le médicament et le dendrimère. Par exemple, l'encapsulation du cisplatine, un médicament anticancéreux bien connu, dans les dendrimères de type P AMAM, a permis la synthèse de dendrimères présentant une libération plus lente, une plus f011e accumulation dans les tumeurs et une toxicité inférieure à celle du cisplatine libre. 65 À
cet égard, Malik et al. 66 ont préparé des promédicaments anticancéreux, des
dendrimères PAMAM à terminaison carboxylate complexés avec du cisplatine. Les molécules de cisplatine ont pu être libérées de l'échafaudage des dendrimères par hydrolyse. De plus, les promédicarnents présentaient un comportement à libération prolongée ( <1 % après 80 h), avec une plus grande dose maximale tolérée, une biodisponibilité du cisplatine et une période de survie prolongée chez les souris p011euses de tumeurs. De même, Malik et Duncan67 ont montré que les platinates de polymères dendritiques pouvaient être administrés par voie intraveineuse, orale, parentérale, sous-cutanée à un animal présentant une tumeur maligne en une quantité qui inhibe efficacement la croissance de la tumeur. En outre, les platinates de polymères dendritiques présentent une efficacité médicamenteuse élevée, une bonne solubilité dans l'eau, une toxicité réduite ainsi qu'une activité antitumorale améliorée
in vivo. En revanche, les travaux de Balogh et al. 68 ont montré que l'encapsulation de
sels d'argent dans les dendrimères de type PAMAM présentaient des taux de libération d'argent lents et une activité antimicrobienne contre la bactérie Staphylococcus aureus, Pseudomonas aeruginosa et Escherichia coli. Outre les dendrimères P AMAM, la
première génération du dendrimère poly(propylèneimine) [DAB(PA-Pt-Cl)4] substitué par quatre fractions trans-diaminechloroplatinum a été étudiée. 69 Ce complexe à quatre bras devait former des liaisons croisées avec un ADN différent de ceux formés avec le cisplatine et, par conséquent, surpassé la résistance au cisplatine dans les cellules cancéreuses. Ce complexe présentait une faible cytotoxicité contre les lignées cellulaires de leucémie de souris L1210/0 et L1210/2 et contre sept lignées de cellules
tumorales humaines (cellules MCF7, EVSA-T, WIDR, IGROV, M19, A498 et H226). De plus, de nombreux autres structures dendritiques à base de Pt (II) ont également été préparés notamment par Jang et al. 70 En combinant le ~is-dichlorodiamineplatinum (II), un dérivé du cisplatine, sur un dendrimère de phtalocyanine, des micelles à complexe polymère-métal utiles pour la libération prolongée de médicaments et pour la thérapie photodynamique ont été formées. Plusieurs autres travaux ont également été rapportés sur la synthèse et la cytotoxicité des complexes de métaux de transition avec les ligands à base de Schiff. La synthèse de complexes de Pt (II), Pd (II), Cu (II) et Hg (II) avec le N-[2- (pyridine-2-ylméthylidène) amino) éthyl] acétamide présentent des effets modérés à faibles activités contre la leucémie humaine (MOLT-4) et le cancer du sein (MCF-7).71
Plus récemment, de nouveaux agents anticancéreux ont été développés par Majoral et
at.30d, 72 Un analogue de dendrimère phosphoré multivalent combiné à du Cu (II)
(1G3-Cll.4s) a été élaboré et a présenté une efficacité élevée contre plusieurs lignées cellulaires cancéreuses humaines (ICso;::; 0,5-0,6 µM). L' analogue non couplé au cuivre 1 G3 s'est quant à lui révélé moins actif contre les mêmes lignées cellulaires tumorales (ICso ;::; 1,2-1,5 µM). Ces résultats démontrent que l'utilisation du cuivre (II) joue un rôle important et pourrait donc constituer un nouveau candidat antitumoral pour la chimiothérapie. De plus, l'effet causé par la substitution du cuivre Cu (II) de 1 G3-Cll.4s par de l'or Au (III), nommé 1G3-[All.4s][AuCl4]4s, a été observé sur les activités antiprolifératives et antimicrobiennes.73 Cette complexation du dendrimère phosphoré avec le métal Au (III) a fortement augmenté les activités antiprolifératives à la fois contre les lignées cellulaires tumorales KB et HL-60, montrant des ICso de l'ordre du nanomolaire. Ce métallodendrimère présente également une faible activité sur la lignée cellulaire inactive EPC par rapport à son activité antiproliférative puissante contre les cellules en division active.
HO HO 2-Cu Figure 1.8 OH a· c1· eu'•
.
OHHO· fill _} "cu1• c1·
HO a · ~~ 1
i !. ..
-K> a· N N 0 r= o-N " N ~-OH ;i ~-OH s- C~ Cl ( OH s ' + cil c1· a· N'""i, --\ ,=, N N ... ,,;-,-0 0 p N p O -= --..,'.,-N _ o 0 -'..=., NPNO\\_'-- O NN 0 0 ....-N ~,,....- 0 - o-· N N 7-Cu O r--"" N N N o r o 0 0 --S ! 00 01< --~ - l -OH , c1i:,i~.0ti c:w +, ~ ,_ Cl. HO OHReprésentation des dendrimères 2 et 7 combinés au cuivre (II).
Face aux résultats prometteurs obtenus par Majoral et al. ï.J avec les analogues de
dendrimère phosphoré multivalent combinés au Cu (II) et à Au (III), nous avons décidé d'ajouter du CuCb aux dendrimères 2 et 7 pour les combiner au cuivre (II) comme représenté sur la figure 1.8 (les procédures synthétique et les résultats sont joints en annexe A). Les analyses RMN ont démontré qu'il n y avait pas de cleavage de la laison S-C durant la coordination, ce qui signifie que le souffre forme une liason dative avec le cuivre. Les analyses ITC ont révélé une complexation entre Je dendrimère 2 et le cuivre, avec une valeur de constante de dissociation à des concentrations micromolaires (9 µM), De ce fait, l'affinité est suffisamment bonne pour maintenir un complexe stable. Cependant, la constante d'association n' étant pas de l' ordre du nanomolaire, le dendrimère devrait délivrer optimalement le cuivre au sein des cellules tumorales. Comme les études faites auparavant montrent que ces complexes cuivrés sont cytotoxiques uniquement vis-à-vis des cellules tumorales,73 le dendrimère 2 combiné
au cuivre pourrait potentiellement être un agent antitumoral. En perspective de ces premiers résultats obtenus, des analyses de cytotoxicité sur des cellules cancéreuses
vont être effectuées avec ce même dendrimère cuivré 2. Des analyses ITC sur le composé 7 combiné au cuivre vont être également réalisées. A la suite de ces analyses, des tests de cytotoxicité seront également effectués afin de déterminer le pouvoir cytotoxique de ces dendrimères pour cibler uniquement des cellules cancéreuses. D'autres métaux tels que l'or et l'argent seront également complexés avec ces dendrimères afin d'obtenir de nouveaux agents anticancéreux et antimicrobiens.
Comme indiqué auparavant, d'autres travaux de synthèses de glycodendrimères ont été entrepris dans ce mémoire et sont décrits dans les chapitres 2 et 3. Ces travaux constituent le corps de ce mémoire dont la cible principale est, l'inhibition d'adhésion des biofilm bactériens. Cette dernière est tout d'abord brièvement introduite dans le chapitre 2 ci-dessous, le travail de recherche à cet effet est quant à lui présenté dans la section 2.2. Finalement, le chapitre 3 introduit à la synthèse d'analogues glycomimétiques contre les galectines. Des travaux menés sur les lectines Grifin sont également décrits dans la chapitre 3. Les procédures expérimentales reliées à ces travaux sont rapportées dans l'annexe B et C.
CIBLE THÉRAPEUTIQUE I - BIO FILM D'ESCHER/CHIA COLI
2.1 Introduction aux infections du tractus urinaire
L'infection du tractus unnaire (UTI) est l'une des maladies infectieuses les plus répondues dans le monde à cause de la résistance accrue aux antibiotiques. 75 Chaque année des milliers de cas sont emegistrées dans les hôpitaux, créant un fardeau économique considérable dû aux dépenses en frais médicaux à des fins de diagnostic et de traitement.76 En effet, cette pathologie touche autant les hommes que les femmes de tout âge, cependant les recensements ammels effectués par les organismes de santé démontrent qu'une femme adulte sur deux en est atteinte, au moins une fois au courant de sa vie. 77 La majeure partie de ces infections sont symptomatologiques,
récurrentes, 78• 77 et si elles sont mal traitées, elles entrainent de graves complications telles que la septicémie (propagation de bactéries et de leurs toxines dans le sang) 79 pouvai1t être mortelles dans certains cas. 80 Les UTis sont généralement localisées dans les voies urinaires basses et hautes, et sont induites par des germes pathogènes d'origine bactérienne à savoir les souches Uropathogéniques d' Escherichia Coli (UPEC) dans 80% des cas.81 Ces bactéries prédominantes dans le système digestif, s'accrochent et
se multiplient, tout d'abord au niveau de la muqueuse de l' urètre induisant des brûlures et une inflammation 'urétrite', puis elles poursuivent leurs chemins vers la vessie en provoquant une inflammation aiguë ou chronique appelée « cystite » (Figure 2.1 ), elles peuvent ensuite étendre leurs propagations et multiplications aux reins en provoquant
de plus amples dommages tissulaires appelés « pyélonéphrite » (Figure 2.1 ). 78 D'autres syndromes cliniques des UTis peuvent êtres induits tel que « les prostatites
»
ou encore « épididymite ».80Figure 2.1
Rein
Pyelonéphrite
Vessie
Cystite
Vessie atteinte d'une cystite et reins de pyénonéphrite dans un tractus urinaire infecté par Escherichia coli. 78· 82
2.1.1 Problème de résistance aux antibiotiques
À cet effet, plusieurs antibiotiques ont été élaborés depuis les années 90, afin de lutter contre les infections bactériennes. Malheureusement, la surutilisation des antibiotiques tels que la méthicilline, l'oxacilline, la nafcilline ou la vancomycine83 ont
involontairement produits de nouvelles souches de bactéries résistantes et ont accru notre vulnérabilité face aux infections bactériennes.84 De plus, au cours des dernières
émergé de la recherche fondamentale. À partir de cette famille de nouvelles oxazolidinones, le linézolide puissant a été approuvé en 2000. 85 Cependant, des bactéries résistantes à l'oxazolidinone sont déjà apparues.86· 4c La prévalence des
souches résistantes d' Escherichia coli (E. coli) qui est en constante augmentation
contre les agents antimicrobiens de première ligne traditionnels tels que triméthoprime / sulfaméthoxazole (Tmp / Smx), gentamicine (Genta), pipéracilline / tazobactam (Pip / tazo ), ceftriaxone (Ctx) et ciprofloxacine ( Ci pro) deviennent presque obsolètes. 84b Une étude récente sur la surveillance des tendances de la résistance aux antimicrobiens (SMART) mondiale a permis de suivre, jusqu'en 2011 , les profils de résistance in vitro
des bacilles à Gram négatif induisant des infections urinaires aux agents antimicrobiens et démontrent que la résistance aux carbapénèmes et le taux de ~-lactamases à spectre étendu (ESBLs) est toujours aussi important (illustré à la figure 2.2).76b
0.0 40.0 Q,I u ~ Cl) ~ 30.0 ::, Q)
&:
...J CQ 20.0 Il) LLI'#.
10.0 0.0 Figure 2.2 • Asia Middleast
• Latin America•
rope • Africa • Sout h Pacif ie•
orth America 2009 2010 201 1Étude SMART de la Prévalence des ESBLs d' E. coli dans le cas