La trajectoire post-opératoire à long terme des patients
gériatriques admis pour une fracture de la hanche: Une
étude de cohorte prospective
Mémoire
Philippe Beauchamp-Chalifour
Maîtrise en épidémiologie - avec mémoire
Maître ès sciences (M. Sc.)
Résumé
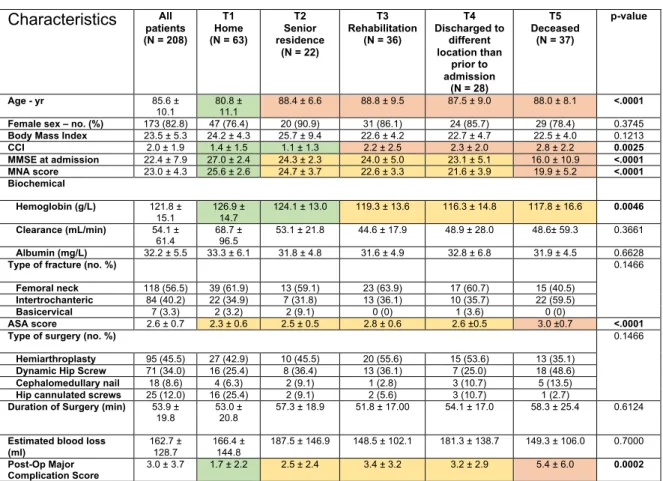
Ceci est une étude de cohorte prospective, avec un suivi d’un an, s’intéressant à la trajectoire postopératoire des patients gériatriques admis pour une fracture de la hanche. Un total de 254 patients étaient inclus dans cette cohorte. Cinq groupes de patients avec des trajectoires similaires ont été formés; 1-retour à domicile (n=63), 2-retour à la résidence (n=22), 3-réadaptation avant retour au milieu de vie original (n=36), 4-changement de milieu de vie (n=28) et 5-décès (n=37). Les patients évoluant dans la trajectoire 1 (évolution favorable) étaient plus jeunes. Les patients évoluant dans la trajectoire 5 (évolution défavorable) étaient plus âgés, étaient malnutris selon l’outil Mini Nutritional Assessement (MNA) et présentaient des troubles neurocognitifs selon leurs pointages du Mini-Mental State Examination (MMSE). Un délai chirurgical allongé était associé avec une mortalité à un an plus élevée, mais ces patients présentaient plus de comorbidités selon l’index de comorbidité de Charlson (CCI). Le délai entre le congé du patient et son départ réel de l’hôpital était associé avec le besoin d’un transfert dans un centre de réadaptation. Il y a donc un besoin de milieux intermédiaires pouvant accueillir les patients gériatriques ayant subi une chirurgie pour fracture de la hanche, afin qu’ils puissent quitter l’hôpital. Les efforts pour améliorer les soins aux patients gériatriques avec fracture de la hanche devraient être déployés pour résoudre ces enjeux.
Abstract
This is a prospective observational cohort study of patients admitted for a hip fracture between 2011 and 2017, with a one-year follow-up. A total of 254 patients were enrolled in this cohort. Most patients evolved in one of the following trajectories at one year; (1) 30% went back at home (2) 11% went back to their senior residence (3) 16% needed readaptation (4) 13% were discharged to a different location than prior to admission (5) 18% were deceased at one year. Patients evolving in trajectory 1 (favorable outcome) were younger. Patients evolving in trajectory 5 (poor outcome) were older, had lower Mini Nutritional Assessment (MNA) scores and had lower Mini-Mental State Examination scores (MMSE). Longer surgical delay was associated with higher mortality and comorbidities. The delay between discharge from the attending staff and real departure from the hospital was associated with the need for a readaptation. There is a need for intermediate residences such as readaptation centers to facilitate discharge from the hospital. Efforts to improve the postoperative care for elderly patients with a hip fracture should focus on those issues.
Table des matières
Résumé ... ii
Abstract ... iii
Table des matières ... iv
Liste des tableaux ... v
Remerciements ... vi
Avant-propos ... vii
Introduction ... 1
Chapitre 1 – La fracture de la hanche gériatrique : un fardeau sociétal ... 2
1.1 Épidémiologie ... 2
1.2 Impact socio-économique ... 3
1.3 Les facteurs de risques ... 3
1.4 Anatomie clinique ... 4
1.5 Mécanisme de fracture ... 8
1.6 Présentation clinique ... 8
1.7 Imagerie ... 9
1.8 Classifications des fractures de la hanche ... 10
1.9 Traitement conservateur ... 11
2.0 Traitement chirurgical ... 14
2.1 Thromboprophylaxie post-opératoire ... 30
2.2 Complications post-opératoires ... 32
2.3 Évolution post-opératoire ... 33
2.4 Enjeux en recherche clinique concernant les interventions chirurgicales ... 33
Chapitre 2 – The long-term postoperative trajectory of geriatric patients admitted for a hip fracture: A prospective observational cohort study ... 35
Résumé ... 36
Abstract ... 37
Article ... 38
Conclusion ... 51
Bibliographie ... 56
Annexe A – Tableaux complets de l’étude ... 80
Annexe B – Scores clinique utilisés dans l’étude ... 83
Liste des tableaux
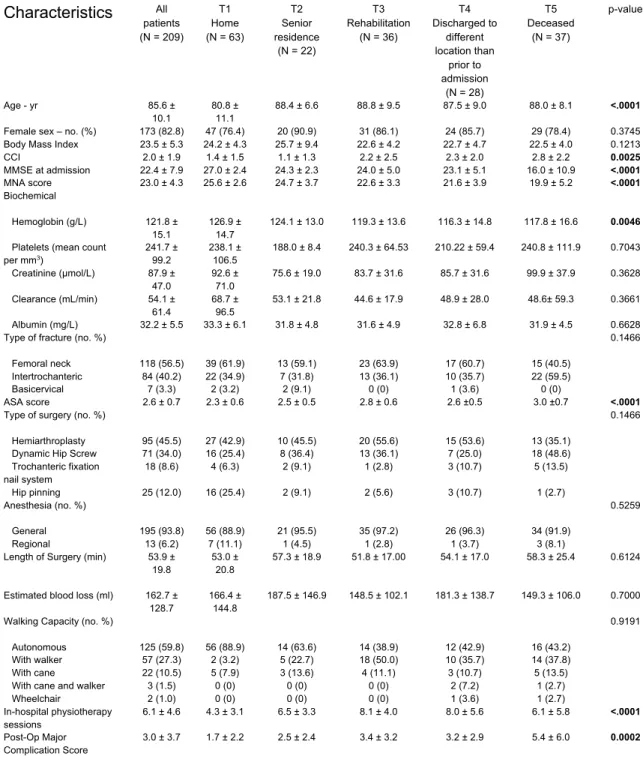
Table 1 – Characteristics of patients’ baseline, according to trajectories Table 2 – Length of stay, according to trajectories
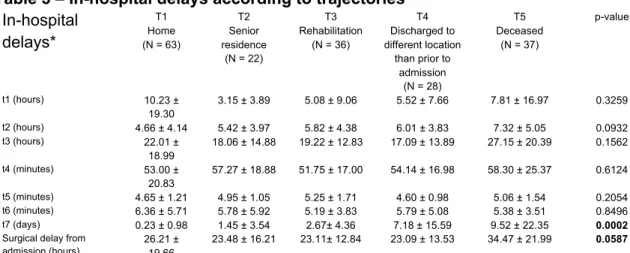
Table 3 – In-hospital delays according to trajectories
Table 4 – Correlation between patients’ characteristics and in-hospital delays Table 5 – Surgical delay according to death and anticoagulation status
Remerciements
J’aimerais remercier le docteur Stéphane Pelet pour son temps à la direction de cette maîtrise. J’aimerais également remercier mon codirecteur de maîtrise, le docteur Étienne L. Belzile. Leur dévouement comme professeur, chirurgien orthopédiste et chercheur a été une grande source d’inspiration pour moi. Ils m’ont motivé à développer mes propres compétences comme médecin résident et chercheur. Je remercie Louis-Charles Racine, Marie-Pier Nolet, Stéphane Lemire et Sonia Jean pour leur contribution au projet. Je remercie Hélène Côté et Sylvie Turmel de l’équipe de recherche du Centre Hospitalier Universitaire (CHU) de Québec – Hôpital de l’Enfant-Jésus pour leur support dans l’avancement de mes projets. Je remercie les docteurs Laetitia Michou et Jean-Christophe Murray pour leur révision de ce mémoire.
Avant-propos
Ma contribution personnelle à ce projet fut la réorganisation de la base de données, l’analyse des données et la vulgarisation du projet (présentations et rédaction de l’article). Je suis l’auteur principal de l’article. Le protocole et la collecte de données avaient déjà été entamés par l’équipe de recherche du CHU de Québec – Hôpital de l’Enfant-Jésus. J’ai synthétisé les multiples informations collectées pour présenter un portrait compréhensible de la situation actuelle, avec la grande contribution des Drs Stéphane Pelet et Étienne L. Belzile. Je remercie Louis-Charles Racine pour la collecte de données. Je remercie Marie-Pier Nolet, Stéphane Lemire et Sonia Jean pour la rédaction du protocole. Ce projet a été présenté par poster au 20e congrès de l’European Federation
of National Associations of Orthopaedics and Traumatology (EFORT) 2019 à Lisbon et à la réunion annuelle de l’Association Canadienne d’Orthopédie (ACO) 2019 à Montréal. J’ai eu l’occasion de le présenter à la Journée de la recherche du département de chirurgie de l’Université Laval 2019 (1er prix de la recherche clinique), à la
38e journée scientifique d’orthopédie de l’Université Laval (3e prix) et à la 18e journée scientifique d’orthopédie
de l’Université de Sherbrooke. J’ai écrit l’article en anglais et en français et ce dernier a été publié dans le journal Orthopaedics and Traumatology – Surgery and Research (OTSR), le 1er mai 2020. J’ai été récipiendaire d’une
bourse d’excellence et de détermination pour le recrutement à la maîtrise Wilbrod-Bhérer de l’Université Laval. J’ai été récipiendaire d’une bourse de maîtrise du Fonds de recherche en orthopédie de Québec. J’ai été récipiendaire de la bourse d’études supérieures au niveau maîtrise Frederick-Banting des Instituts de recherche en santé du Canada.
Introduction
Ce premier chapitre vise à faire l’état des connaissances actuelles en fracture de la hanche chez la personne gériatrique. Nous aborderons d’abord la fracture de la hanche comme enjeu sociétal. Par la suite, nous réviserons l’anatomie clinique de la hanche. Les différentes classifications, principes de traitement et complications postopératoires seront présentés. Nous aborderons les débats et enjeux quant au traitement chirurgical des fractures de la hanche. Le deuxième chapitre sera constitué de l’article en anglais publié le 1er
mai 2020 dans le journal Orthopaedics and Surgery: Traumatology and Research.
Bien qu’il y ait beaucoup de littérature sur les fractures de la hanche, la complexité de la prise en charge de cette fracture chez une population hétérogène pose un défi aux sociétés modernes vieillissantes. La prise en charge doit considérer l’ensemble du tableau clinique et être adaptée à chaque cas.
À ce jour, de nombreuses études ont été faites pour évaluer les complications postopératoires, la mortalité et l’évolution fonctionnelle de ces patients après leur fracture. Elles ont d’ailleurs permis de soulever diverses problématiques, notamment en ce qui concerne les besoins de relocalisation temporaire ou permanente suite à une fracture de la hanche. En effet, certains patients doivent demeurer à l’hôpital plusieurs semaines après leur chirurgie avant d’avoir accès à un milieu pour poursuivre leur réadaptation ou encore un milieu de relocalisation permanente. Dans la littérature actuelle, quelques études se sont intéressées au milieu de sortie des patients au départ de l’hôpital, mais très peu de données sont disponibles en ce qui concerne l’ensemble de leur trajectoire postopératoire, c’est-à-dire de leur départ de l’hôpital jusqu’à ce qu’ils atteignent leur trajectoire finale, c’est-à-dire le milieu de vie qui deviendra leur nouveau domicile permanent.
Le but de cette étude observationnelle de cohorte prospective était d’illustrer le portrait global des trajectoires post-opératoires de patients gériatriques avec fracture de la hanche, puisqu’elles étaient inconnues et pourraient potentiellement mener à des pistes de solution pour alléger ce fardeau sociétal.
Chapitre 1 – La fracture de la hanche gériatrique :
un fardeau sociétal
1.1 Épidémiologie
Chaque année, au moins 1.3 million de patients subissent une fracture de la hanche dans le monde et ce chiffre devrait atteindre 6.3 millions d’ici 20501,2. Il est estimé que le nombre de fractures de la hanche augmentera de
12 % d’ici 20303. Au Canada, il y a eu 23 621 hospitalisations chez les patients de plus de 60 ans pour une
fracture de la hanche en 20034. Aux États-Unis, 258 000 patients de plus de 65 ans ont été hospitalisés pour
une fracture de la hanche en 20103. Cette augmentation en nombre absolu est notamment due à l’augmentation
de l’espérance de vie et au vieillissement de la population5. Selon l’Institut National de Santé publique du
Québec, la proportion de la population âgée de 65 ans et plus passera de 17,5 % (2015) à 25 % en 20306.
En contrepartie, l’incidence des fractures de la hanche aurait diminué significativement entre 1990 et 2006 aux États-Unis pour les patients de plus de 65 ans7. Chez les hommes, l’incidence est passée de 54.6 à 48.8 par 10
000 personnes-années (test de tendance, p=0.007)7. Chez les femmes, l’incidence est passée de 108.4 à 91.7
par 10 000 personnes-années entre 1985 et 2005 (test de tendance, p=0.001)7. Ce phénomène a également
été observé en Angleterre où l’incidence par 100 000 habitants a diminué globalement de 2.8% entre 2002 et 20098. Plusieurs facteurs ont possiblement réduit cette incidence comme le dépistage de la densité osseuse et
les traitements d’ostéoporoses avec bisphosphonates9. Par contre, les faibles taux de dépistages de densité
osseuse et la sous-utilisation des bisphosphonates suggèrent qu’il y a d’autres facteurs qui expliquent cette diminution d’incidence10,11. L’amélioration des habiletés fonctionnelles et l’augmentation des indices de masses
corporelles (IMC) moyens pourraient notamment être en cause12,13.
L’ethnie semble être aussi un déterminant dans le risque de fracture de la hanche. L’incidence semble être plus élevée chez les Caucasiens vivants à haute latitude. L’incidence globale la plus élevée de fracture de la hanche a été observée dans les pays scandinaves (Danemark à 439/100 000 et Norvège à 420/100 000) et la plus basse en Équateur à 55/100 00014,15. L’exposition solaire diminuerait le risque de fracture de la hanche. Il est
estimé que pour chaque changement de 10 degrés en latitude par rapport à l’équateur, le risque de fracture de la hanche augmente de 0.6%16. Toutefois, environ 30% des fractures de la hanche dans le monde surviennent
chez la population asiatique en raison de la grande population17. Une récente étude menée à Taiwan a démontré
une incidence modérée chez cette population à 296/100 00018.
La fracture de la hanche représentait 20% de la charge de travail chirurgicale en orthopédie en 199819. Il serait
hospitalisations dues aux blessures musculo-squelettiques étaient causées par la fracture de la hanche20. Les
fractures du col fémoral représentent environ 50 % des fractures de la hanche21. Les fractures de la région
trochantérienne représentent l’autre moitié. Les patients avec une fracture intertrochantérienne ont tendance à être plus vieux et fragiles que ceux se présentant pour fracture du col fémoral22.
1.2 Impact socio-économique
La fracture de la hanche a un impact majeur dans la vie des patients gériatriques, étant associée à un taux de mortalité élevé. La mortalité périhospitalière peut s’élever jusqu’à 15%23. À un an, 26-33 % des patients seront
décédés et ce nombre atteint 50% s’il y a présence concomitante de trouble neurocognitif23,24. À 5 ans, environ
60% des patients seront décédés23. De plus, 63 à 80 % des patients ne retrouveront jamais leur statut fonctionnel
d’origine25. Un sondage réalisé chez des femmes de plus de 75 ans a d’ailleurs démontré que 80% préfèreraient
mourir plutôt que de perdre leur indépendance et leur qualité de vie suite à une fracture de la hanche26.
Le coût total au Canada en 2008 pour les fractures de la hanche a été évalué à 650 M$ CAD24. Aux États-Unis,
le coût direct à 6 mois pour une fracture de la hanche est évalué entre 34 509 à 54 054 $ US par fracture27.
Peu d’études se sont concentrées sur l’aspect purement économique des fractures de la hanche. Keating et al.28 ont comparé les coûts entre une prothèse totale de la hanche, une hémiarthroplastie et une fixation pour
fracture du col fémoral. Ils ont constaté que ce n’était pas le coût de l’implant qui déterminait la rentabilité d’une intervention, mais principalement la durée de l’hospitalisation et les coûts associés aux révisions.
1.3 Les facteurs de risques
Les facteurs de risques pour une fracture de la hanche peuvent être divisés en trois catégories. Il y a d’abord les facteurs de risque qui prédisposent à une diminution de la densité osseuse, menant à l’ostéoporose29.
Certains sont non modifiables, soit le sexe féminin (80% des fractures du col fémoral surviennent chez les femmes), l’ethnie (caucasien), l’âge, un bas niveau d’œstrogène et une histoire familiale30,31. Il est d’ailleurs
estimé qu’une femme sur trois qui vit jusqu’à l’âge de 80 ans subira une fracture de la hanche14. L’ostéoporose
est un sujet vaste qui ne sera pas abordé dans ce mémoire qui s’intéresse plutôt aux aspects cliniques de la fracture de la hanche.
D’autres sont modifiables comme l’utilisation du tabac, l’utilisation d’alcool, le poids (IMC<18.5), le niveau d’activité physique, le niveau d’exposition solaire et le statut nutritionnel30,32,33. Certaines maladies chroniques
sont aussi connues comme facteurs de risque de fracture de la hanche comme le VIH, le diabète, l’insuffisance rénale chronique et la dépression30. Les inhibiteurs de pompe à proton, les corticostéroïdes et les médicaments
antipsychotiques sont aussi connus pour prédisposer à l’ostéoporose30,31. En contrepartie, les diurétiques
thiazidiques, les bêtabloqueurs, les inhibiteurs de canaux calciques et les inhibiteurs de l’enzyme de conversion de l’angiotensine (IECA) sont connus protecteurs pour les fractures de fragilité34,35.
L’autre catégorie de facteurs de risque prédisposant à une fracture de la hanche est celle en lien avec le risque de chute chez la personne âgée. La faiblesse musculaire, les troubles de l’équilibre, les maladies neurologiques (parkinson), la diminution de l’acuité visuelle (cataractes) et la médication sédative ou augmentant l’hypotension orthostatique sont parmi les facteurs les plus importants36.
L’adhérence à une diète méditerranéenne (riche en fruits, légumes, noix, poissons) aurait en contrepartie un effet protecteur modéré du risque de fracture de la hanche (HR 0.80, 95%CI [0.66-0.97])37. Il y aurait une
diminution du risque absolu de fracture de la hanche de 0.29% et un NNT de 342 (95%CI, 249-502) selon une analyse post-hoc d’une étude de cohorte prospective de 90 014 patientes en post-ménopause aux États-Unis37.
1.4 Anatomie clinique
La hanche est une articulation comprenant le fémur proximal et l’acétabulum au bassin. Le fémur proximal est divisé en trois parties, soit la région du col fémoral, intertrochantérienne et sous-trochantérienne38. Lorsqu’on
parle de fracture de la hanche, on fait référence à une fracture du col fémoral ou une fracture intertrochantérienne.
La fracture du col fémoral est une fracture intracapsulaire. La fracture intertrochantérienne (reliant le petit et le grand trochanter) est une fracture extracapsulaire. La capsule articulaire est un ensemble de ligaments contigus dans laquelle l’articulation est contenue et où le liquide synovial circule38. La capsule est la structure d’attache
principale du fémur proximal au bassin38. Les autres structures d’importances sont les insertions
myotendineuses des muscles moyens et petits fessiers sur le grand trochanter, du muscle ilio-psoas sur le petit trochanter et des rotateurs externes en postérieur du grand trochanter38. Bien que la fracture
intertrochantérienne soit extracapsulaire, la capsule articulaire peut tout de même être lésée. La capsule articulaire a donc son importance pour la réduction d’une fracture intertrochantérienne, puisqu’une capsule intacte garde une certaine stabilité au niveau de la région trochantérienne et rendrait la réduction de la fracture plus facile38. Si la capsule est atteinte lors d’une fracture intertrochantérienne, les déplacements des fragments
du fémur dépendront des attaches myotendineuses. Ainsi, le grand trochanter sera amené en abduction et rotation externe par le moyen fessier et les rotateurs externes. La diaphyse fémorale sera déplacée proximalement et médialement par les muscles adducteurs et ischiojambiers, résultant à la déformation souvent vue en coxa vara dans les fractures intertrochantériennes à la radiographie38. Pour les fractures du col fémoral,
attaches myotendineuses. Le muscle iliopsoas, qui s’insère sur le petit trochanter, produit une flexion de la hanche. Si le col est lésé, la force résultante de ce muscle produira une rotation externe sur la diaphyse fémorale, vu le bras de levier modifié par la fracture.
De façon générale, l’angle du col fémoral est de 130 ± 7 degrés38. L’antéversion du col fémoral, c’est à dire
l’angle entre le col fémoral et l’axe transcondylien du fémur distal dans le plan transverse, est de 10 ± 7 degrés32.
La région du col fémoral a un mauvais potentiel de guérison, lorsque comparé à la région trochantérienne. Premièrement, la vascularisation principale (environ 82%) de la tête et du col fémoral se fait à rebours (distal vers proximal) par une branche de l’artère fémorale profonde, soit l’artère circonflexe médiale39. L’artère
circonflexe médiale donne des branches qui se dirigent vers la tête fémorale en postérieur dans le rétinaculum de Weitbrecht, une extension fibreuse de la capsule articulaire. Le col fémoral étant intracapsulaire, une fracture déplacée à ce niveau met donc la vascularisation de la tête fémorale à risque d’ischémie pouvant mener à l’ostéonécrose. Le reste de la vascularisation provient de l’artère circonflexe latérale et de l’artère fovéale, mais celles-ci ne peuvent assurer une vascularisation complète de la tête fémorale38. Deuxièmement, il y a peu de
périostes au niveau du col fémoral, siège principal des cellules souches servant à la guérison osseuse38,40. La
guérison du col fémoral doit donc dépendre d’une couche cellulaire plus profonde de l’os où se trouve le deuxième réservoir en importance de cellules souches osseuses, appelée l’endosteum32,40. Par contre,
l’endosteum s’atrophie avec la malnutrition, prévalente chez plus de 50% des patients avec fracture de la hanche41–45. Ceci explique pourquoi la guérison de cette fracture est hasardeuse et plus longue qu’avec un os
cortical. Finalement, le liquide synovial intracapsulaire limiterait la formation de cal osseux en guérison de fracture, puisqu’il liserait les caillots sanguins qui se forment au niveau du site fracturaire (ceux-ci déclenchent la cascade inflammatoire menant à la guérison)46. Le site usuel pour une fracture du col est situé juste sous la
surface articulaire en supéro-latéral, l’endroit le plus faible du col selon des études s’intéressant à la perte osseuse à la tomodensitomértie38.
Une fracture de la région trochantérienne (autrement appelée intertrochantérienne) est une fracture entre le grand et le petit trochanter. La fracture intertrochantérienne est distale à la vascularisation de la tête fémorale et se situe au niveau de l’os spongieux, qui est bien vascularisé47. Le risque d’ostéonécrose de la tête fémorale
ou le risque de non-union suite à une fracture intertrochantérienne est donc beaucoup moins élevé que suite à une fracture du col fémoral47. L’os spongieux est organisé en trabécules osseuses selon la loi de Wolff48,49. Cette
loi propose que les trabécules osseuses du fémur proximal s’orientent en réponse aux contraintes de mise en charges physiologiques (marche, course, monter des escaliers)48,49. Ceci rendrait ainsi l’os le plus
mécaniquement efficace possible pour un minimum de poids48,49. Bien que la loi de Wolff date de 1893, son
ces trabécules en quatre zones de compression : les zones de compression et les zones tensiles, principales et secondaires51,52. Au centre de ces zones, on retrouve le triangle de Ward qui est la localisation la moins dense
du fémur proximal53. Une récente étude biomécanique a d’ailleurs confirmé la validité de ces vieux concepts à
l’aide d’un modèle trois-dimensions de fémur proximal reconstruit par TDM avec 23.3 millions d’éléments finis et un voxel de 175 µm54. Ils ont d’abord créé un modèle anisotropique de fémur proximal, auquel ils ont modélisé
mathématiquement deux jours de mise en charge54. Utilisant une analyse qualitative s’intéressant à la
distribution minérale osseuse, ils ont confirmé que l’orientation des trabécules osseuses respectait bien la loi de Wolff54.
Entre les zones de compression et tensiles principales, on retrouve une région anatomique d’importance : le calcar femorale (autrement appelée Arche de Adam). Le calcar femorale est défini comme une lame verticale dense d’os spongieux localisée au niveau du cortex postéro-médial s’étendant jusque sous le petit trochanter50.
La stabilité de la région intertrochantérienne dépend de l’intégrité du cortex postéro-médial ou calcar femorale et a longtemps été reconnu comme l’élément le plus important38,47. Par contre, un autre élément anatomique
majeur, voire même plus important, a été mis à l’avant par Gotfried en 2004 : le mur latéral du grand trochanter55.
Il a rétrospectivement observé 24 cas d’effondrement du mur latéral suite à une chirurgie pour fracture intertrochantérienne par plaque et vis (sliding hip screw)55. Tous les cas (24/24) avaient une fracture du mur
latéral en postopératoire, suggérant que le mur latéral a un rôle prédominant comme appui de compression pour ostéosynthèse par plaque et vis dynamique55. Bien que ce soit une étude à seulement 24 patients, un chirurgien
et sans groupe contrôle, le concept a été réexploré et confirmé dans plusieurs études subséquentes56–58. Une
étude de cohorte prospective danoise s’est notamment intéressé au risque de réopération des patients ayant subi une chirurgie pour fracture intertrochantérienne en regard à l’intégrité du mur latéral59. Ils ont démontré que
10/46 (22%) des patients avec une fracture du mur latéral ont été réopérés à 6 mois par rapport à seulement 5/168 (3%) des patients avec un mur latéral intact (p<0.010)59. Ainsi, l’implant sliding hip screw a aussi besoin
d’un mur latéral pour faire guérir la fracture de façon stable.
La région sous-trochantérienne débute au petit trochanter et se termine cinq centimètres distalement à celui-ci60. Les fractures de la région sous-trochantérienne ne font pas partie des fractures de la hanche. Celles-ci
surviennent à une région anatomique particulière; à la transition entre l’os spongieux de la région intertrochantérienne et entre l’os cortical de la diaphyse fémorale38,61. À cette région, il y a une moins bonne
vascularisation du fémur38,61. La région sous-trochantérienne est également soumise à des forces compressives
importantes au niveau du cortex médial (jusqu’à 1200 livres/pouce carré chez un patient de 200 livres) et tensiles au niveau du cortex latéral (jusqu’à 900 livres/pouce carré chez un patient de 200 livres)38,62. Ceci augmente
leur risque de non union63. De plus, ces fractures sont soumises à des formes déformantes plus importantes,
il y a également présence des branches perforantes de l’artère fémorale profonde qui augmente aussi leur risque de saignement63. Pour ces raisons, les fractures sous-trochantériennes évoluent différemment et ne sont pas
traitées comme des fractures de la hanche.
Les structures nerveuses motrices d’importance au niveau de la hanche sont le nerf fémoral en antérieur et le nerf sciatique en postérieur. Ils sont rarement vus lors des différentes approches chirurgicales38. Par rapport à
l’innervation sensitive de la capsule articulaire, celle-ci a été décrite dans plusieurs études neuro-anatomiques selon la revue de 17 articles de Simons et collègues64. Le nerf obturateur, le nerf fémoral, le nerf sciatique et le
nerf glutéal supérieur sont tous contributoires64. La capsule antérieure est l’endroit le plus innervé de la
capsule64. L’innervation de la région trochantérienne est par contre moins bien décrite65. Genth et al. ont fait 7
dissections sur cadavres et n’ont trouvé qu’une seule branche nerveuse se dirigeant vers le grand trochanter66.
Elle avait pour origine le nerf fémoral et suivait le trajet de l’artère fémorale circonflexe médiale66. L’intérêt
derrière ces notions d’anatomie est de diminuer les douleurs causées par la fracture, les douleurs dues positionnement pour la chirurgie et les douleurs postopératoires subséquentes à l’aide de blocs nerveux65. Les
blocs du nerf fémoral ou du fascia iliaque sont deux options populaires65. L’avantage conféré par le bloc fascia
iliaque est sa rapidité, son efficacité et sa facilité technique65,67,68. En termes d’efficacité, les deux plus grands
essais cliniques randomisés (ECR) sur le sujet sont arrivés à des résultats similaires. Reavley et al. ont randomisé 83 patients au bloc du nerf fémoral et 79 patients au bloc du fascia iliaque pour les patients ayant une fracture du col fémoral dans leur département d’urgence69. L’échographie a été utilisée pour faire les blocs
du nerf fémoral et le bloc du fascia iliaque a été fait à l’aide de repères anatomiques. Ils ont obtenu des pointages d’échelle analogue (VAS) similaires de 35 mm vs 38 mm à 60 minutes, respectivement (différence de moyenne, 3 mm, 95%CI [-4.7 à 10.8])69. Un autre ECR a comparé les pointages VAS à 2h post-bloc suite aux deux types
de blocs et a trouvé une diminution plus marquée du pointage VAS dans le groupe du bloc du nerf fémoral par rapport au bloc du fascia iliaque (3.7 mm vs 2.8 mm, p=0.047)70. Le besoin en opioïde dans les 12h suivant le
bloc étaient également moins important dans le groupe du bloc du nerf fémoral (39% vs 54%, p=0.041)70. À
noter que les blocs du nerf fémoraux étaient faits avec un stimulateur nerveux. Bien que la deuxième étude semble démontrer un certain avantage au bloc du nerf fémoral, l’amélioration de 2.8 à 3.7 mm sur une échelle de 100 mm n’est probablement pas cliniquement significative, peu importe le bloc utilisé. L’avantage serait surtout la réduction de la consommation d’opioïde. Les deux blocs semblent démontrer une certaine utilité pour contrôler les douleurs liées aux fractures de la hanche. Les moments idéaux et les indications pour effectuer les blocs restent à déterminer, puisqu’ils pourraient potentiellement nuire à la réadaptation des patients en postopératoire71. Il pourrait être intéressant d’explorer leur utilisation en soins palliatifs.
1.5 Mécanisme de fracture
90 % des fractures du col fémoral sont associées à une chute de sa hauteur38. Le mécanisme le plus commun
pour une fracture du col et intertrochantérienne est le même, c’est-à-dire un impact direct sur le grand trochanter qui transmet la force soit à la région trochantérienne ou au col fémoral38. Un autre mécanisme possible pour
une fracture du col est une rotation externe de la jambe. La capsule articulaire devient plus rigide avec l’âge. La tête fémorale peut alors rester fixée dans l’acétabulum lorsque le col fémoral tente de faire une rotation externe. C’est à ce moment qu’une fracture surviendrait32,72.
La direction de la chute et les mécanismes de rattrapages sont également intéressants. Si la chute est sur le côté, c’est signe que le patient est âgé et fragile38. Les patients qui chutent vers l’avant auraient de meilleurs
mécanismes d’équilibre et seraient moins malades38. Si la chute est vers l’avant, les patients ont tendance à
vouloir se rattraper avec leurs membres supérieurs (causant alors des fractures du radius distal ou de l’humérus proximal). Deux à trois pourcent des fractures de la hanche sont pathologiques ou secondaires à une fracture de stress73.
1.6 Présentation clinique
Suite à leur chute, les patients sont en général incapables de mise en charge et se présentent à l’urgence dans ce contexte.
L’examen physique est souvent peu révélateur : il y a peu de différences cliniques entre les fractures du col fémoral et intertrochantérienne à l’examen physique. Il est rare de voir une déformation visible. Les fractures du col fémoral sont toutefois associées à un raccourcissement et rotation externe de la hanche de façon typique32,38.
Les fractures intertrochantériennes peuvent également être raccourcies, tel que discuté dans la section anatomie clinique. À l’examen physique, tous les mouvements de l’articulation de la hanche sont douloureux.
Deux éléments de l’examen physique peuvent avoir un impact sur la prise en charge et le positionnement du patient pour la chirurgie. Premièrement, certains patients peu mobiles ont des contractures en flexion de la hanche et du genou, ce qui peut rendre la tâche du chirurgien plus difficile38. Deuxièmement, les lésions de
pressions devraient être notées puisqu’elles peuvent avoir un impact sur le risque d’infection et la mobilisation en postopératoire38.
La plupart des fractures de la hanche sont isolées, mais il faut rester vigilant chez cette patientèle. Jusqu’à 4% des patients avec fracture de la hanche auraient une autre fracture ou luxation associée, selon une étude de cohorte prospective 1971 patients de plus de 60 ans avec fracture de la hanche74. Quatre-vingt-huit pourcent
(71/81) de ces blessures étaient des fractures au radius distal ou de l’humérus proximal74. Les patients avec
fracture de l’humérus proximal semblaient plus malades que ceux avec une fracture du radius distal.
1.7 Imagerie
Une radiographie du bassin antéro-postérieur (AP) et une radiographie latérale de la hanche sont demandées de routine. Ces radiographies permettent en général de porter le diagnostic. Par contre, une radiographie normale n’exclut pas une fracture dans un contexte clinique de fracture de la hanche (jusqu’à 10 % de faux négatifs)75.
Dans cette situation, une imagerie par résonance magnétique ou une tomodensitométrie peuvent être utilisées. Le standard étalon pour détecter ces fractures occultes est l’imagerie par résonnance magnétique (IRM). Dans une étude de cohorte de 67 patients avec douleurs à la hanche et radiographies négatives, l’IRM et la tomodensitométrie (TDM) ont été comparées pour diagnostiquer des fractures de la hanche occultes. Le TDM a présenté une sensibilité de 87% (95%CI [0.60-0.98]) lorsque comparé à l’IRM76. Certaines séries récentes ont
tout de même rapporté des sensibilités de 100% en utilisant le TDM uniquement75,77. Le TDM est plus rapide,
plus simple d’utilisation et plus disponible. Avec l’amélioration de la précision de cet examen, il est raisonnable d’utiliser cette imagerie avant l’IRM, même si théoriquement moins sensible. Les faux négatifs avec le TDM surviennent surtout lorsque l’imagerie est faite dans les 72 heures suivant le fracture ou lorsque le plan de la fracture est dans le plan de coupe du TDM38.
De nouvelles modalités d’imagerie plus dynamiques sont en développement pour tenter de prédire le risque de nécrose avasculaire de la tête fémorale suite à une fracture du col. Il y a d’abord la tomographie par émission de positron (PET/CT) qui serait capable de prédire le risque de nécrose avasculaire78. Dans une étude de
cohorte prospective de 62 patients subissant une fixation par 3 vis, le statut de la vascularisation à 6 semaines en post-opératoire était prédictif d’une nécrose avasculaire78. Par contre, 80% des patients qui avaient une
atteinte vasculaire en préopératoire avaient un regain de la vascularisation à 6 semaines en post-opératoire. Il y a aussi la magnetic renonance imaging – positive enhancement integral color mapping (MRI-PEICM) en préopératoire qui se voudrait utile pour prédire le risque de non-union des fractures du col fémoral non déplacées, selon une étude de cohorte prospective de 68 patients79. Les taux de non-union étaient de 0 % pour
les patients avec perfusion normale, 6.7% dans le groupe de perfusion réduite et de 50 % dans le groupe sans perfusion79. Pouvoir mieux prédire le risque de nécrose avasculaire ou de non-union pourrait potentiellement
1.8 Classifications des fractures de la hanche
Il existe plusieurs classifications des fractures de la hanche. Seulement les plus utiles en clinique (qui orientent le traitement) pour le col fémoral et la région intertrochantérienne sont présentées.
1.8.1 Classification de Garden (Col fémoral)
La plus utilisée est la classification de Garden ; Garden I – incomplète ou complète impactée en valgus, Garden II – complète non déplacée, Garden III – complète avec déplacement partiel, Garden IV – complètement déplacée (les trabécules osseuses ne sont plus alignées)32.
Bien qu’elle soit la plus utilisée, il n’y a qu’un accord interobservateur de 22% (k=0.22) pour les 4 grades80. En
contrepartie, une étude plus récente (N=100) a démontré un meilleur accord interobservateur de 52% (k=0.52) lorsque la classification était simplifiée pour les fractures non déplacées (I-II) et déplacées (III-IV)81. C’est
d’ailleurs le déplacement de la fracture qui oriente le traitement.
1.8.2 Classification de Pauwels (Col fémoral)
La classification de Pauwels dépend de la verticalité du trait de fracture par rapport à l’horizontale38,82. Pauwels
avait prédit que plus le trait était vertical, plus l’instabilité de la fracture augmentait et donc, le risque de non-union ou d’échec de fixation38,82. La classification est décrite selon trois types : Type I – 30 degrés ou moins,
Type II – entre 30 et 50 degrés, et Type III – plus grand que 50 degrés. Malheureusement, cette classification n’a pas été démontrée fiable pour prédire l’évolution de ces fractures et l’accord interobservateur était seulement de 31% (k=0.31)38,83,84.
Elle a par contre été démontrée utile chez une patientèle jeune (entre 20 et 60 ans) pour prédire le risque de non-union et le risque de nécrose avasculaire de la tête fémorale85. Dans une étude de cohorte rétrospective,
suite à une mesure ajustée par modèle de régression logistique, le rapport de cotes (OR) de nécrose avasculaire était de 0.15 (95%CI [0.12-0.93]) pour un type I par rapport à un type 3, alors que la classification de Garden simplifiée ne prédisait pas la nécrose avasculaire (p=0.28)85. Ces auteurs ont également utilisé une méthode
différente pour mesurer l’angle d’inclinaison de la fracture en traçant la ligne de référence perpendiculaire à l’axe de la diaphyse fémorale et non simplement l’axe horizontal85. En effet, la mesure classique de l’angle de Pauwels
ne prenait pas en considération la position du patient sur la table d’imagerie85. L’accord interobservateur s’en
surtout chez le jeune patient et en utilisant la technique modifiée par Wang et al. pour mesurer l’angle d’inclinaison.
1.8.3 Classification de l’AO et OTA (Intertrochantérienne)
La classification dépend de la stabilité de la fracture. Pour qu’une fracture soit instable, il faut une atteinte du cortex postéro-médial, une atteinte du mur latéral ou un patron « oblique renversé ». Cette classification simplifiée est divisée en trois, mais il existe des sous-classifications de l’AO qui ont peu d’utilité en clinique38.
La fracture de type A1 est stable et en deux parties. La fracture de type A2 est instable et comminutive (atteinte du cortex postéro-médial). La fracture de type A3 est instable par son atteinte du mur latéral et son orientation perpendiculaire à la région trochantérienne. La stabilité de la fracture oriente le traitement.
Un accord interobservateur modéré (k=0.60) a été démontré en utilisant les sous-divisions simplifiées de l’AO86.
1.9 Traitement conservateur
Le traitement conservateur en fracture de la hanche gériatrique reste un sujet très controversé. De 0.2 à 18% des patients avec fracture de la hanche se verront offrir un traitement conservateur87–91. Peu de données sont
disponibles pour guider les cliniciens, ce qui explique une hétérogénéité marquante en termes de pratique clinique. La majorité des études rapportent toutefois 10% de traitement conservateur87–91. La dernière revue
Cochrane sur le sujet de 2008 avait d’ailleurs mis de l’avant l’absence d’ECR de qualité sur le sujet et la difficulté éthique de conduire de telles études89. La dernière revue de la littérature de 2019 a aussi signalé le manque
d’études prospectives utilisant des pointages cliniques pour prédire les bénéfices d’un traitement conservateur90.
1.9.1 Fracture du col fémoral non déplacée
Bien que certains auteurs aient démontré un taux d’union de 69% avec un traitement conservateur pour des fractures non déplacées du col fémoral (mobilisation avec 25% de mise en charge pour 4-6 semaines), le risque de déplacement de ces fractures varie de 19 à 46%88,92–94. Il est d’ailleurs bien difficile de connaître la vraie
valeur d’une mise en charge à 25% chez cette patientèle âgée et avec des troubles cognitifs. Un ECR dont seules les données sont disponibles a comparé le traitement conservateur au traitement chirurgical par fixation pour fracture non déplacée du col fémoral. 10/16 patients traités de façon conservatrice comparés à 0/7 patients des patients traités par fixation étaient en non-union à 35 jours (RR 9.88, 95%CI [0.66-148.48])95. Neuf patients
sur ces 10 ont dû subir une hémiarthroplastie secondaire à un déplacement de la fracture, ce qui correspond à une chirurgie plus invasive que s’ils avaient eu une chirurgie par fixation au départ95. Il est donc nécessaire
d’intervenir chirurgicalement chez les patients avec fracture non déplacée ou impactée du col fémoral, puisque la plupart des fractures vont se déplacer et seront au final opérées. De plus, la chirurgie diminue la longueur d’hospitalisation et permet une mobilisation plus rapide et facile88,93,94.
1.9.2 Fracture du col fémoral déplacée
En 1994, Harper et al. avaient tenté de faire un ECR comparant un traitement conservateur (mobilisation selon tolérance) à l’hémiarthroplastie chez des patients avec une fracture déplacée du col fémoral88,89,96. L’étude avait
dû prendre fin à 9 mois après avoir recruté 21 patients, car les résultats du traitement conservateur étaient trop insatisfaisants88,89. Le traitement conservateur ne semble donc pas une avenue possible pour ces patients.
1.9.3 Fractures intertrochantériennes
Pour les fractures gériatriques de la région intertrochantérienne, il y a aussi peu de place pour le traitement conservateur38. Le traitement conservateur proposé est une traction par fiches trans-osseuses au niveau du
tibia89. Le temps moyen d’une telle traction était de 51 jours dans l’étude Hornby et al. de 1989, l’ECR la plus
descriptive comparant le traitement chirurgical à la traction de Hamilton Russell97. Il n’y avait par contre pas de
clarification sur la mobilisation post-opératoire97. Hornby et al. avaient aussi débuté une étude similaire en 1975,
mais seulement les données ont été publiées89,97. Une revue Cochrane de 2008 a combiné les données de leurs
deux études et n’a pas trouvé de différence sur le risque de pneumonie, de plaies de pression ou d’événements thromboemboliques entre les deux groupes (p>0.05), ce qui est surprenant89. Les patients étaient moins vieux
et malades à l’époque, la mobilisation post-opératoire précoce n’était pas encore de routine et les techniques d’anesthésie n’étaient pas raffinées comme elles le sont aujourd’hui, ce qui laisse douter de validité externe de ces résultats. De plus, les fractures trochantériennes n’étaient pas à plus grand risque de non-union qu’elles soient opérées ou non (3/86 versus 1/333, RR 3.04, 95%CI [0.48-19.03])89. Malgré tout, le traitement
conservateur présente plusieurs désavantages89. Ces fractures peuvent d’abord guérir malalignées (19/39
versus 4/35, p<0.001) selon l’ECR de Hornby et collègues97. La déformation classique est le varus étant donné
les forces musculaires non opposées en jeu38,97. Les patients sont souffrants pendant plusieurs semaines si non
opérées38. Ils restent plus longtemps hospitalisés en moyenne de 27 jours97. Les fiches servant de traction ont
tendance à s’infecter (16%) et surtout se relâcher (39%)97. Il est aujourd’hui clairement établi que l’immobilisation
augmente les risques de complications médicales chez les patients avec fractures de la hanche : complications cardiaques, atélectasie pulmonaire (pneumonie), sepsis urinaire, délirium, embolie pulmonaire, déconditionnement et décès98,99. Les patients alités et non opérés ont également plus de chance de décéder à
30 jours que les patients opérés (OR 2.5, 95%CI [1.1-5.5]) 91. La mortalité à 30 jours chez les patients avec
façon non chirurgicale et plus élevée que chez les patients non opérés qui pouvaient se mobiliser (OR, 3.8, 95%CI [1.1-14.0])91. Selon une grande étude de base de données de 50 235 patients, la mortalité à 30 jours
chez les patients non opérés était plus élevée que chez les patients opérés (18.8% versus 11.0%, OR 1.7, 95%CI [1.6-1.8])91. Le traitement chirurgical est donc nécessaire pour prévenir les complications liées à
l’alitement, mais aussi pour contrôler la douleur lors des mobilisations, améliorer l’équilibre en position assise et faciliter les transferts lors des soins infirmiers96,100.
1.9.4 Soins palliatifs
Peu d’outils existent pour guider le chirurgien orthopédiste face à la décision d’un traitement conservateur, qui signifie aujourd’hui le recours aux soins palliatifs90. Les patients non ambulants, avec un trouble neurocognitif
majeur sévère ou qui présentent des signes imminents de décès seraient les meilleurs candidats à se voir offrir un traitement de soins palliatifs101. Il est encore controversé à savoir si les patients non ambulants ont plus de
gains à être exposés aux risques d’une chirurgie ou à ne pas être traités de façon chirurgicale90,100. Les patients
avec un trouble neurocognitif avancé (MMSE<18, Global Deterioration Scale 6-7) qui subissent une fracture de la hanche ont un taux de mortalité de 55% à 6 mois102. L’indication la plus « simple » pour les soins palliatifs est
quand le patient présente des signes imminents de décès (< 3 jours) tels que la diminution de l’état de conscience, une respiration de Cheyne-Stokes ou une oligurie103. Certains auteurs décrivent un délai de
quelques semaines comme étant un décès imminent104. Malgré tout, cette décision qui repose souvent sur
l’orthopédiste reste extrêmement délicate vu la difficulté de prédire l’évolution de ces patients en fin de vie et la difficulté d’appréhender les différences culturelles. L’absence d’un traitement de soins palliatifs standardisé et reconnu est également en cause.
Un rapport de cas de Toronto décrivant le traitement en soins palliatifs a d’ailleurs mis en évidence le manque de données sur le traitement optimal des patients en soins palliatifs104. À une semaine post-fracture, leur patient
recevait 14 mg d’hydromorphone et 20 mg de midazolam en sous-cutané104. Son membre inférieur était
immobilisé avec des sacs de sable. La douleur de la fracture était surtout vécue lors des soins infirmiers, mais était diminuée lorsque 2 personnes s’occupaient des soins et lorsque le patient était distrait durant ses soins104.
Le patient est décédé au 11e jour post-fracture104. Les auteurs considéraient que le patient avait été bien soulagé
de façon globale.
La plupart des études se sont à ce jour penchées à savoir qui il faut opérer. Il faudrait peut-être aujourd’hui renverser la question et se demander qui bénéficierait le plus d’un traitement conservateur et comment ce dernier devrait être optimisé.
2.0 Traitement chirurgical
Peu importe le type de fracture de la hanche, une chirurgie est nécessaire chez la plupart des patients101. Les
buts du traitement chirurgical sont de soulager le patient, de redonner une fonction au membre et surtout, de permettre une mobilisation rapide suite à la blessure32. Suite à une chirurgie pour fracture de la hanche, les
patients sont encouragés à se mobiliser dès le lendemain, selon leur tolérance101.
Le délai chirurgical recommandé au Commonwealth et aux États-Unis est généralement en < 48h, lorsque médicalement stable. Selon une étude canadienne récente, il se pourrait même qu’un délai < 24h post-admission réduise la mortalité à 30 jours105,106.
Il a déjà été routine dans certains centres de mettre une traction cutanée chez ces patients. Par contre, une méta-analyse de 10 ECR de 2011 de qualité modérés (N=1546) n’a pas pu démontrer d’avantages au niveau du soulagement de la douleur ou de la facilité de réduction de la fracture au bloc opératoire subséquente, suite à l’installation d’une traction107.
Dans méta-analyse de 31 études (N=3231) comparant l’anesthésie générale et l’anesthésie régionale pour la chirurgie, aucune différence concernant la mortalité, l’infarctus du myocarde ou le délirium en post-opératoire n’a été mise en évidence108.
L’antibiothérapie prophylactique à l’induction à la chirurgie est le standard de pratique, avec une réduction du risque d’infection du site chirurgical profond (RR 0.40, 95%CI [0.24-0.67])109. De plus, cette antibiothérapie
prophylactique réduit le risque d’infection du site chirurgical superficiel, d’infection urinaire et de pneumonie selon une revue Cochrane de 2010109.
Les patients avec fracture de la hanche sont souvent hypovolémiques au moment de la chirurgie. Cette hypovolémie serait contributoire à une hypoperfusion des tissus menant à une dysfonction d’organes en post-opératoire110,111. L’instauration d’un protocole de maintien de volume circulant intravasculaire périopératoire
comparé au traitement standard avait démontré un temps plus rapide de congé médical (médiane, 10 (9-15) jours versus 15 (11-40) jours, p<0.05)111.
2.0.1 Fracture du col fémoral non déplacée
Le traitement d’une fracture du col fémoral dépend du déplacement de la fracture. Pour les fractures non déplacées ou impactées en valgus (Garden I et Garden II), ces fractures sont fixées puisqu’environ 40 % de ces
fractures vont se déplacer sans intervention et qu’une mobilisation rapide est nécessaire chez ces patients32.
Suite à une chirurgie, 1 à 6 % de ces fractures vont tout de même se déplacer101. La chirurgie la plus souvent
proposée est une fixation percutanée à l’aide de trois vis. La position idéale de ces vis reste débattue (parallèles ou divergentes)38,112.Certaines études ont aussi démontré que seules deux vis pourraient être suffisantes38,112.
La technique classique est d’utiliser trois vis parallèles positionnées en triangle inversé. L’utilisation de rondelles (washer) pour les vis serait recommandée113. L’absence de rondelles avait été associée à un risque plus élevé
d’échec de la chirurgie (OR 11.2, p=0.03) dans une étude observationnelle de 80 patients113. Ceci est
potentiellement expliqué par une meilleure compression au niveau du site fracturaire.
Une fixation avec une plaque et vis de type « sliding hip screw (SHS) » peut également être utilisée, bien qu’aucune évidence n’ait démontré sa supériorité aux 3 vis dans le contexte d’un col fémoral non déplacé. L’étude la plus connue s’étant intéressée à cette question, le FAITH trial, a randomisé 557 patients à recevoir une SHS et 551 à recevoir trois vis percutanées114. Bien qu’ils aient inclus 549 fractures déplacées dans leur
série, ils n’ont pas démontré de différence significative dans la plupart des issues cliniques étudiées (réopération à 2 ans, non-union, raccourcissement, échec de l’implant et infection)114. Il y avait cependant un plus haut taux
de nécrose avasculaire de la tête fémorale avec une SHS (9%) qu’avec l’utilisation de vis percutanées (5%) (p=0.0319)114. Cette série a aussi suivi 76 fractures basicervicales (qui se comportent comme des fractures
intertrochantériennes) et l’utilisation d’une SHS pour ces fractures était associée à un plus bas taux de réopération114. L’utilisation d’une SHS était également associée à de plus bas taux de réopération dans les
sous-groupes des fumeurs et des fractures déplacées du col fémoral. L’utilisation d’une SHS pour les fractures basicervicales et pour les patients fumeurs avec fracture du col non déplacée est recommandée à la lumière de ces résultats.
Lowell a décrit l’alignement anatomique du col et de la tête fémorale sous forme de courbes en S. Il est possible de s’y référer lors de la fluoroscopie au bloc opératoire pour s’assurer que la fracture est bien non déplacée ou impactée en valgus115. Si le col est déplacé, il faut changer la stratégie chirurgicale.
2.0.2 Fracture du col fémoral déplacée
Pour les fractures déplacées (Garden III et Garden IV), la conduite dépend du type de patient qui se présente avec une telle fracture. Pour les jeunes patients avec trauma de haute énergie, il est indiqué de tenter une réduction et fixation interne pour tenter de sauver la tête fémorale (et ainsi éviter une prothèse)32.
Pour les patients de plus de 60 ans, la conduite demeure toujours controversée. La haute mortalité associée à cette fracture complique aussi l’analyse des données de la littérature. Selon une méta-analyse comparant la fixation et l’arthroplastie (reconstruction avec prothèse), les taux de réopérations étaient significativement plus élevés chez les patients ayant subi une fixation qu’une arthroplastie116. Après 4 à 6 ans de suivi, les taux de
réopérations étaient de 62/865 (7.1%) pour l’arthroplastie versus 386/844 pour les fixations (39%) (RR, 0.12, 95%CI [0.07-019])116. Ceci est notamment expliqué par les risques non négligeables associés à une fixation
d’une fracture du col déplacée (échec mécanique, nonunion et nécrose avasculaire de la tête fémorale)116. Pour
toutes fractures déplacées ayant été fixées de façon appropriée, le taux d’ostéonécrose de la tête fémorale se situent tout de même entre 20-30 %32. Le désavantage de la prothèse est le risque plus élevé de luxation qui se
situe autour de 3%38. Il n’y aurait pas de différence au niveau de la mortalité ou du risque d’infection entre les
deux procédures116. Étant donné l’avantage important de l’arthroplastie (diminution du risque de réopération)
décrit dans la plupart des essais cliniques randomisés, elle est indiquée d’emblée pour la plupart des patients. La mortalité périopératoire globale de l’arthroplastie (incluant les patients ayant subi chirurgie élective pour arthrose) est évaluée à 0.18%117.
Prothèse totale de la hanche versus hémiarthroplastie
Deux options sont possibles en arthroplastie : la prothèse totale de la hanche (PTH) ou l’hémiarthroplastie (HA). La différence entre une PTH et l’HA est la cupule acétabulaire (bassin) dans une PTH. Dans une HA, il y a un contact direct entre l’os (acétabulum) et le métal (tête prosthétique). Un essai clinique randomisé multicentrique du groupe HEALTH investigators (N=1495) s’est d’ailleurs récemment intéressé à savoir quel implant amenait les meilleurs résultats cliniques pour les patients ambulants pré-fracture de plus de 50 ans118. Ils n’ont pas pu
démontrer une différence dans le taux de réopération entre les deux procédures après deux ans de suivi (57/718 (7.9%) pour la PTH versus 60/723 (8.3%) pour l’HA (p=0.79)118. Les patients avec une PTH ont par ailleurs eu
de meilleurs pointages de fonction de hanche au Western Ontario and McMaster Universities Arthritis Index (WOMAC) (différence de moyenne, -6,37; 99%CI [-9,18- -3.56])118. Par contre, ce résultat tombe sous le seuil
de résultat cliniquement significatif (9 à 22 points pour le WOMAC)118. Il n’y avait pas de différence quant aux
pointages de qualité de vie (EQ-5D, SF-12) et fonctionnels (Time Up and Go (TUG))118. Les patients avec PTH
semblaient être plus à risques de luxations ou d’instabilité que les patients avec HA (34/718 (4.7%) versus 17/723 (2.4%), HR, 2.00[0.97-4.09], sans que cela ne soit statistiquement significatif. Ainsi, la PTH n’a pas d’avantages en termes de réopération et de qualité de vie lorsque comparée à l’HA sur un suivi de 2 ans et aurait tendance à causer plus de luxation. L’HA (chirurgie plus rapide, moins invasive) est donc le standard étalon chez ces patients dont la mortalité en post-opératoire est élevée. Le suivi des patients dans cette étude s’arrêtant à 2 ans, il est difficile de conclure sur les potentiels bénéfices d’une PTH à plus long terme pour les patients moins malades dont la survie sera plus longue qu’anticipée. La prothèse totale de hanche pourrait demeurer une option valable pour les patients entre 60 et 80 ans chez qui l’on estime une espérance de vie plus
longue, bien que cette pratique ne soit pas à ce jour supportée par de bonnes évidences. Chez les patients de plus de 80 ans, l’HA demeure le standard étalon pour la plupart des orthopédistes119.
Hémiarthroplastie unipolaire versus hémiarthroplastie bipolaire
Deux types d’HA existent encore à ce jour: l’HA unipolaire et l’HA bipolaire120. La prothèse standard est l’HA
unipolaire qui mime un remplacement de col et tête fémorale120. Le système bipolaire utilise une doublure interne
mobile qui réduirait potentiellement le mouvement entre le cartilage acétabulaire et l’implant métallique120. Le
choix entre l’HA unipolaire ou bipolaire reste controversé121–123. Certains auteurs avancent que le système
bipolaire protège le cartilage acétabulaire de l’érosion, diminuant ainsi la douleur postopératoire et améliorant par le fait même la fonction de la hanche pour les patients119,124. D’autres auteurs rapportent que la doublure
interne du système bipolaire perd sa mobilité avec le temps, devenant ainsi une prothèse unipolaire125,126. Par
contre, cette hypothèse est basée sur des études radiologiques faites sur des patients en décubitus dorsal, sans les vraies forces physiologiques appliquées sur la prothèse. Le coût d’implant d’une prothèse bipolaire a déjà été 2 à 5 fois celui d’une prothèse unipolaire, mais ce n’est plus le cas aujourd’hui119. Il n’y a pas de différence
entre la prothèse unipolaire ou bipolaire en termes de pointages de fonction de hanche et de complications selon les trois dernières méta-analyses d’essais cliniques randomisées (ECR) conduites en 2014-2015121–123.
Par contre, Liu et al. avaient plusieurs biais dans leur méthodologie (pas de graphique en forêt, pas d’analyse de sensibilité, pas de stratégie de recherche et utilisation d’une étude en double)127. Yang et al. ont seulement
inclus 6 ECR123. Zhiwei et al. n’ont pas considéré l’approche chirurgicale utilisée pour la chirurgie, leur stratégie
de recherche n’était pas assez sensible et ils n’ont pas fourni de graphique en forêt121. Il ne semble pas avoir
de grandes différences en termes d’issues cliniques entre la prothèse bipolaire et unipolaire selon les méta-analyses disponibles, mais cette question reste mal répondue notamment en raison de la qualité des évidences disponibles.
Cimentation des tiges fémorales
Un autre débat qui est survenu dans l’évolution des connaissances orthopédiques est la nécessité de cimenter la tige fémorale de la prothèse implantée en fracture de la hanche. Dans une méta-analyse (2006) de Parker et al. comparant 549 patients avec tiges non cimentées à 857 patients avec tiges cimentées, ils ont démontré que l’utilisation d’une tige cimentée était associée à moins de douleur à un an ou plus (16/25 versus 28/52, RR 0.51, 95%CI 0.31 à 0.81)128. Par contre, vu la mauvaise qualité des ECR disponibles et le peu de patients inclus dans
cette analyse, il est difficile de tirer des conclusions claires de ces résultats128. Ils n’ont pas vu de différence
dans le risque de complications128. Plusieurs essais cliniques randomisés n’ont pas pu démontrer de différence
dans la mortalité associée à l’une ou l’autre des interventions129–131. Ces études ont démontré des évidences
conflictuelles concernant les pointages de qualité de vie à un an, ce qui laisse supposer qu’il n’existe pas une grande différence entre les deux interventions pour cet issu clinique129–131. Un essai clinique randomisé de 2013
de 220 patients de > 70 ans avec 5 ans de suivi est arrivé à des conclusions intéressantes. Ils ont comparé des implants non cimentés revêtus d’hydroxyapatite (implant plus moderne) à des prothèses bipolaires cimentées129.
Ils n’ont eu que 3 pertes au suivi dans le groupe cimenté et 2 dans le groupe non cimenté129. L’élément le plus
important qu’ils ont mis en évidence dans cet article est le risque beaucoup plus élevé de fracture périprosthétique dans le groupe non cimenté (7.4% versus 0.9%, HR 9.3, 95%CI 1.16-74.5)129. Ils ont par contre
démontré que les pointages de fonction hanche (Harris Hip Score) étaient supérieurs dans le groupe non cimenté à 5 ans (86.2 vs 76.3, différence de moyenne 9.9, 95%CI 1.9-17.9)129. En reconstruction de hanche, la
différence de pointage cliniquement significative se situe entre 15.9-19 sur l’échelle de Harris Hip Score (HHS)132. Ainsi, cette différence pourrait ne pas être cliniquement significative129. La base de données suédoise
des fractures de la hanche a évalué 23 509 procédures et mis en évidence un risque de révision global de 3.8%133. L’utilisation de prothèse non cimentée était associée à un risque de fracture périprosthétique plus
significatif (HR 20, 95%CI [9-44]) lorsque comparé à des prothèses cimentées mattes133. Le risque augmenté
inacceptable de fractures périprosthétiques avec les prothèses non cimentées, surtout chez une clientèle fragile chez qui on veut éviter une deuxième chirurgie, indique que les patients sont mieux servis avec des prothèses cimentées.
Approches chirurgicales
L’approche chirurgicale à la hanche est aussi un aspect auquel se sont penchés les chirurgiens orthopédistes. Cinq approches sont communément utilisées pour arthroplastie de la hanche, soit l’approche antérieure Smith-Petersen, l’approche antérieure mini-invasive de Hueter, l’approche antérolatérale de Watson-Jones, l’approche latérale directe de Hardinge et l’approche postérieure de Moore38. Il y a beaucoup d’information conflictuelle
dans ce domaine puisque la plupart des études ne comparent que deux approches et certains auteurs interchangent les noms d’approche (antérolatérale et directe latérale). Ceci peut expliquer en partie l’hétérogénéité de pratique quant à l’approche pour l’HA dans le monde. L’approche la plus pratiquée en fracture de la hanche est l’approche directe latérale134.
Approche latérale directe (Hardinge) versus approche postérieure (Moore)
Il a été démontré dans plusieurs études que l’approche postérieure était associée à un plus grand risque de luxation en postopératoire133,135,136. Par contre, ce risque serait moins élevé avec une bonne fermeture de la
capsule postérieure et des rotateurs externes135. Les luxations récidivantes (³2) sont associées à un déclin
significatif et permanent des pointages de qualité de vie à 1 an après la chirurgie (une seule luxation est associée à un déclin temporaire des pointages de qualité de vie)137. Une étude de cohorte prospective de 739 HA avec
un suivi médian de 2.3 (0-10) années s’est penchée sur la question en 2003135. Après une analyse multivariée,
ils ont démontré un risque plus élevé de luxation avec l’approche postérieure avec réparation de capsule postérieure qu’avec une approche latérale directe (15/161 (9%) versus 13/418 (3%), OR 3.9, 95%CI [1.6-10],
p<0.001)135. Ce risque était encore plus accentué lorsque l’approche postérieure n’avait pas de réparation de
capsule postérieure (17/112 (13%) versus 13/418 (3%), OR 6.9, 95%CI [2.6-19]), p<0.001)135. De ces 45
luxations, 13 (28%) ont nécessité une chirurgie de révision135. Une autre grande étude de cohorte rétrospective
de 807 HA est arrivée à une conclusion similaire135. Ils ont observé 23 (2.9%) luxations au total. Le risque de
luxation suivant une approche postérieure était plus élevé qu’avec une approche antérolatérale (que je présume être l’approche latérale directe dans cette étude) (7/54 (13%) versus 16/753 (2.1%), OR 8.5, 95%CI [2.8-26.3], p<0.001)136. Il faut par contre prendre en considération que ces études ont incluse une grande proportion de
prothèses monobloc de Moore et de Thompson qui ne sont pas ajustables quant à la longueur du col et le décalage latéral, ce qui peut jouer sur les tensions musculaires impliquées à la hanche et pourrait potentiellement influencer le risque de luxation. Ceci rend donc ces résultats questionnables sur la validité externe dans des centres utilisant des prothèses plus modernes. Le plus récent ECR (qui utilisait aussi des prothèses de Thompson) ayant comparé les deux approches n’avait pas la puissance pour déterminer une différence en termes de luxation (N=185)138. Par contre, ils ont remarqué que l’approche postérieure avait
tendance à être associée à plus de révision (11/83 (13.3%) versus 7/102 (6.9%), OR 0.51, 95%CI [0.18-2.07], p=0.23)138. Il n’y avait pas de différence pour la douleur, les pertes sanguines, les infections et la mortalité entre
les deux approches dans cette étude138.
Approche antérieure (Smith-Peterson) versus latérale directe (Hardinge)
L’approche antérieure de Smith-Peterson inclut le détachement du fascia lata et de 50% du moyen fessier de la table externe de l’aile iliaque, ce qui est très agressif et n’est pas utilisé dans cette population38. Il n’y a pas
d’ECR comparant l’approche antérieure et l’approche latérale directe.
Approche antérieure mini-invasive de Hueter versus latérale directe (Hardinge)
Un essai clinique randomisé Suisse (2018) a comparé l’approche antérieure mini-invasive de Hueter à l’approche latérale directe de Hardinge (N=190)134. Ils n’ont observé aucune différence statistiquement
significative dans leurs issues cliniques (fonction de la hanche, complications), mais ils ont observé des tendances intéressantes134. À 3 semaines, le TUG avait une tendance à être diminué dans le groupe avec
l’approche antérieure mini-invasive à 3 semaines en postopératoire (durée médiane, -21.5%, 95%CI [-41.2-4.7], p=0.104), ce qui laisserait sous-entendre une meilleure mobilité134. Pour une raison qu’ils ignorent, la mortalité
à 1 an (28.0% versus 20.2%, p=0.149) et l’infection d’implants (8.9% versus 5.2%, p=0.281) étaient plus élevées dans le groupe avec approche mini-invasive antérieure134. D’autres études sont nécessaires pour conclure sur
cette approche. Un essai clinique randomisé de la clinique Mayo s’est intéressé à ce sujet et devrait être complété en 2022 (Clinical Trials ID number : NCT0295930).