HAL Id: dumas-01876365
https://dumas.ccsd.cnrs.fr/dumas-01876365
Submitted on 18 Sep 2018HAL is a multi-disciplinary open access archive for the deposit and dissemination of sci-entific research documents, whether they are pub-lished or not. The documents may come from teaching and research institutions in France or abroad, or from public or private research centers.
L’archive ouverte pluridisciplinaire HAL, est destinée au dépôt et à la diffusion de documents scientifiques de niveau recherche, publiés ou non, émanant des établissements d’enseignement et de recherche français ou étrangers, des laboratoires publics ou privés.
La prise en charge des diabètes : place du pharmacien
d’officine, évolutions technologiques et télémédecine
Alexia Ferrou
To cite this version:
Alexia Ferrou. La prise en charge des diabètes : place du pharmacien d’officine, évolutions tech-nologiques et télémédecine. Sciences pharmaceutiques. 2018. �dumas-01876365�
Université de Bordeaux
U.F.R DES SCIENCES PHARMACEUTIQUES
Année 2018 Thèse n°78
Thèse pour l'obtention du
DIPLOME D'ETAT DE DOCTEUR EN PHARMACIE
Présentée et soutenue publiquement par Alexia FERROU
Née le 4 juillet 1991 à Bayonne (64)
Le lundi 3 septembre 2018 à Bordeaux
LA PRISE EN CHARGE DES DIABETES : PLACE DU
PHARMACIEN D'OFFICINE, EVOLUTIONS
TECHNOLOGIQUES ET TELEMEDECINE
Directeur de thèse Madame Geneviève LACAPE
Membres du jury
Madame Marine AULOIS-GRIOT Professeur des universités Président Madame Geneviève LACAPE Maître de conférences Directeur Madame Camille BENARD Docteur en pharmacie Juge
REMERCIEMENTS
A la présidente du jury, Madame Marine Aulois-Griot, professeur à la faculté de Bordeaux, Je vous remercie d'avoir accepté de présider mon jury, et de l’intérêt que vous avez porté à mon sujet de thèse.
A ma directrice de thèse, Madame Geneviève Lacape, maître de conférence à la faculté de Bordeaux
Merci de m'avoir fait confiance et d'avoir accepté de m'accompagner durant l'élaboration de ma thèse. Je vous remercie également pour tous vos conseils et votre disponibilité.
A Camille Bénard, Pharmacien à Mérignac,
Merci d'avoir accepté de faire partie de mon jury et d'avoir pris le temps de lire mon travail, en espérant que ce nouveau statut te plaira, et merci pour ta gentillesse au travail et au quotidien. A mes parents, à mon frère, à toute ma famille,
Merci de m'avoir soutenu et accompagné dans ces longues années d'étude.
Papa, Maman, un grand merci pour m'avoir permis de réaliser mon envie de métier de petite fille, je vous laisse réaliser les votre maintenant ...
A Paul, mon chéri,
Merci pour ton aide dans la réalisation de cette thèse et pour m'avoir supporter durant ces longues périodes de stress. A partir de maintenant, c'est à moi de te soutenir dans tes projets de carrière, et à nous de réaliser des projets tous les deux.
A mes copines de Bordeaux, des Landes et d'ailleurs,
Merci pour votre soutien durant toutes ces années, je ne retiens que nos supers moments, en espérant que nous en ayons encore beaucoup d'autres.
SOMMAIRE
INTRODUCTION...4
PARTIE I : GENERALITES ...5
A Définitions...5
1 Le diabète sucré ...5
2 Anomalie de la glucorégulation ou état prédiabétique ...6
B Épidémiologie...7
C Classification des diabètes...8
1 Diabète de type 1...8
a Définition ...8
b Critères diagnostic...8
c Physiopathologie...10
d Formes particulières du diabète de type 1 ...13
2 Diabète de type 2...14 a Définition ...14 b Critères diagnostic...14 c Physiopathologie ...15 3 Diabète gestationnel...16 a Définition ...16 b Critères diagnostic...16 c Physiopathologie...17
d Complications du diabète gestationnel...17
e Prise en charge...18
4 Autres types de diabète...19
a Diabètes secondaires...19
b Diabètes iatrogéniques...19
c Diabètes monogéniques...20
D Diagnostic et suivi biologique ...21
1 Glycémie...21
a Glycémie à jeun...21
b Glycémie post-prandiale ou à n'importe quel moment de la journée...21
c Autosurveillance glycémique...22
2 Hyperglycémie provoquée par voie orale (HGPO)...22
3 Hémoglobine glyquée HbA1c ...23
4 Autres tests...23
a Glycosurie...23
b Dosage des corps cétoniques...23
E Complications...24 1 Complications aiguës...24 a Hypoglycémie ...24 b Acidocétose...24 c États hyperosmolaires...25 2 Complications chroniques ...26 a Rétinopathie diabétique ...26 b Néphropathie diabétique...27 c Complications cardiovasculaires...27 d Neuropathie diabétique...28 e Pied diabétique ...29 F Traitements...32
1 Insulinothérapie...33 a Insulines...33 b Administration du traitement...35 c Schémas thérapeutiques...36 d Insulinothérapie fonctionnelle ...37 2 Antidiabétiques oraux ...38 a Biguanides...39 b Sulfamides hypoglycémiants...39 c Glinides...40
d Inhibiteurs des alpha-glucosidases...40
e Incrétinomimétiques ...40
f Inhibiteurs des SGLT2 ou gliflozines...41
g Pharmacothérapie dans le diabète de type 2...41
PARTIE 2 : CONSEILS PRATIQUES A L'OFFICINE...43
A Autosurveillance glycémique...43
1 Définition...43
2 Les dispositifs médicaux...45
a Autopiqueurs et lancettes ...45
b Lecteurs de glycémie et bandelettes ...45
c Collecteur de déchets...47
d Carnet de surveillance...47
3 Réalisation d'un test de glycémie capillaire...47
4 Lecteur en continu du glucose interstitiel...48
B Bon usage des insulines et du matériel d'injection...52
1 Règles de conservation de l'insuline...52
2 Les zones d'injection ...53
3 Rotation des zones d'injection...53
4 Réalisation de l'injection ...54
a Avant l'injection...54
b Manipulation du stylo pour l'injection d'insuline ...54
c Manipulation d'une seringue...57
5 Adaptation des doses d'insuline...58
C Prise en charge des déséquilibres glycémiques...59
1 Hypoglycémies...59 2 Hyperglycémies ...60 D Règles hygiéno-diététiques...62 1 Diététique ...62 a Diabète de type 1...62 b Diabète de type 2...63
c Alimentation du diabétique de type 1 ou 2...63
d Conseils nutritionnels à l'officine...68
2 Activité physique ...69
a État des lieux ...69
b L'activité physique dans la prévention et le contrôle du diabète ...70
c Sport santé sur ordonnance ...70
3 Tabagisme ...71
4 Soins des pieds...71
E Aide au suivi pathologique ...73
1 Objectifs du suivi médical ...73
3 Bilans biologiques...74
4 Examens médicaux...74
5 Cas particuliers ...75
PARTIE 3 : NOUVELLES MISSIONS DU PHARMACIEN ...76
A Éducation thérapeutique...76
1 Définition ...76
2 Mise en place de l'éducation thérapeutique ...76
3 Réalisation de l'éducation thérapeutique...77
a Généralités ...77
b Personnes concernées par l'éducation thérapeutique...78
c Intervenants concernés par l'éducation thérapeutique du patient ...78
d Cas du diabète et du patient diabétique ...78
4 Le pharmacien d'officine dans l'éducation thérapeutique du patient diabétique...79
B Télémédecine...82
1 Définition ...82
2 Les modalités réglementaires de réalisation des actes ...83
a Conditions de mise en œuvre de la télémédecine...83
b Organisation de la télémédecine...84
3 Déploiement de la télémédecine...85
a Stratégie nationale de développement ...85
b Expérimentation de la télémédecine...86
c Remboursement des actes de téléconsultation et téléexpertise...86
d Financement de la télémédecine dans le droit commun en 2018...87
4 La prise en charge du diabète par télésurveillance ...87
a Généralités...87
b Réglementation...88
c En pratique, exemples de systèmes de télémédecine ...92
5 Place du pharmacien d'officine dans la télémédecine...97
CONCLUSION...100
ANNEXE...101
TABLE DES ILLUSTRATIONS
Illustration 1: Mécanisme de l'insulinopénie ...11
Illustration 2: Physiopathologie du diabète de type 1...12
Illustration 3: Physiopathologie du diabète de type 2...16
Illustration 4: Basal-bolus insulinothérapie intensifiée...37
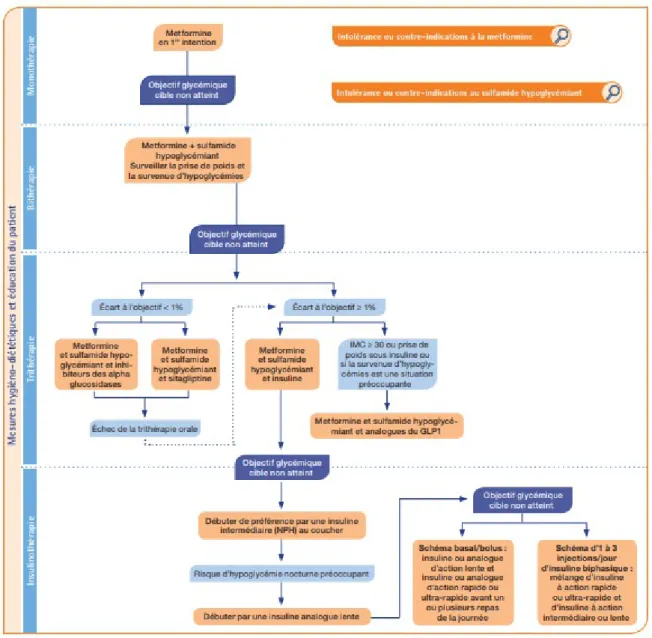
Illustration 5: Stratégie médicamenteuse patients diabétiques de type 2-HAS...43
Illustration 6: Prélèvement d'une goutte de sang capillaire...49
Illustration 7: Lecteur FreeStyle Libre®...50
Illustration 8: Rotation des zones d'injection de l'insuline...54
Illustration 9: Stylo à insuline...56
Illustration 10: Fixation de l'aiguille au stylo à insuline...57
Illustration 11: Purge du stylo à insuline...57
Illustration 12: Système Diabeloop...96
TABLEAUX
Tableau 1: Risques de diabète de type 1 en France ...13Tableau 2: Insulines ...35
Tableau 3: Objectifs thérapeutiques pour l'adaptation des traitements...45
Tableau 4: Teneur glucidique approximative des principales classes d'aliments pour 100g...65
Tableau 5: Index glycémique des principaux groupes d'aliments glucidiques ...66
Tableau 6: Classification des glucides « rapides » et « lents »...66
INTRODUCTION
Le diabète est une maladie chronique liée à un dysfonctionnement du pancréas. Il en existe deux formes principales : le diabète de type 1, dû à une production insuffisante d'insuline et le diabète de type 2, le plus courant, résultant d'une mauvaise utilisation de l'insuline par l'organisme. D'autres diabètes sont possibles, aux caractéristiques qui diffèrent légèrement des deux
principaux diabètes, notamment le diabète gestationnel, qui apparaît au moment d'une grossesse. Le diabète est, en France et dans le reste du monde, un enjeu de santé publique majeur. Cette pathologie touche des millions de personnes et le nombre de nouveaux cas ne cesse d'augmenter chaque jour. C'est une pathologie qui nécessite un traitement et un suivi régulier afin d'éviter l'apparition de complications majeures. En effet, le diabète est la première cause de cécité avant 65 ans et d'amputations non traumatiques, l'une des principales causes d'insuffisance rénale, et multiplie le risque d'accidents cardiaques ou vasculaires cérébraux par 2 ou 3 chez l’adulte. L'impact sanitaire du diabète impose donc une mobilisation de l’ensemble des professionnels de santé pour prévenir la maladie, la dépister et accompagner le patient tout au long de son parcours de soins. Le pharmacien, acteur de santé publique, joue un rôle de premier plan à toutes ces étapes. En effet, il est le professionnel de santé en contact avec le plus grand nombre de personnes, chaque jour 4 millions de français franchissent le seuil de l'officine pour venir chercher un médicament ou tout simplement demander un conseil de santé. Dans le cas des patients diabétiques, le pharmacien est là pour aider le patient à comprendre sa maladie et ses traitements ainsi que pour répondre aux questions sur la diététique, l'activité physique, les traitements proposés, leurs bénéfices attendus et leurs potentiels effets indésirables.
Outre les conseils concernant les traitements, le pharmacien doit pouvoir conseiller ses patients diabétiques sur les nouveaux outils de surveillance de la glycémie. Depuis de nombreuses années les évolutions technologiques ne cessent de se développer afin de faciliter la prise en charge par le patient lui-même de son contrôle glycémique. Les lecteurs de glycémie sont améliorés en s’incrémentant d’une facilité et d’un confort d’utilisation, ainsi ils permettent de limiter la douleur lors des piqûres, et, aujourd'hui, d’en limiter le nombre quotidien.
Récemment, un appareil novateur s’immisce dans la prise en charge du patient : un système qui permet une piqûre unique tous les 14 jours afin d'insérer un capteur de glucose interstitiel, la mesure sera alors relevée par un simple scan du capteur.
En plus des nouveautés dans le matériel de surveillance, c'est la surveillance elle-même et l'accompagnement des patients que l'on tente d'améliorer.
Le diabète est une pathologie dont le suivi est indispensable et doit être régulier. Or l'accès aux soins, en particulier aux rendez-vous médicaux, peut s'avérer difficile pour certains patients et dans certaines zones géographiques. La télémédecine a donc fait son chemin depuis quelques années afin de faciliter le suivi des patients grâce à la mise en place d'expérimentations depuis 2014. Actuellement, pour les diabétiques ce sont les résultats glycémiques et autres résultats biologiques qui sont transmis aux médecins et analysés à distance. À partir de septembre de cette année, des consultations à distance seront possibles pour certains patients, dont le suivi des personnes diabétiques.
Quelle est la place du pharmacien d'officine dans toutes ces avancées technologiques,
sociologiques et législatives ? En quoi peut-il aider le patient diabétique à suivre son traitement et à améliorer sa qualité de soins et de vie ?
PARTIE I : GENERALITES
A Définitions
1 Le diabète sucré [1, 2, 113, 114, 126]
Le diabète sucré est un trouble métabolique caractérisé par la présence d'une hyperglycémie liée à un défaut de sécrétion d'insuline par le pancréas ou à un défaut d'action de l'insuline, ou bien des deux. L'hyperglycémie chronique entraîne des complications à long terme aussi bien microvasculaires, avec atteinte des yeux, des reins et des nerfs, que macrovasculaires responsables de maladies cardiovasculaires.
Il existe plusieurs types de diabète, dont les trois principaux sont :
– le diabète de type 1 anciennement nommé le diabète insulinodépendant, qui survient le plus souvent chez l'enfant, l'adolescent et le jeune adulte, dans lequel le pancréas ne synthétise plus d'insuline de façon suffisante, empêchant l'utilisation par les cellules des différents organes du glucose circulant et provoquant une hyperglycémie ;
– le diabète de type 2, anciennement nommé diabète non insulinodépendant, qui apparaît plus tardivement que le diabète de type 1 et de façon plus fréquente. Son développement se fait sur plusieurs années avec une première phase d'insulinorésistance où les différents organes deviennent résistants à l'insuline. L'organisme, pour s'adapter, va produire de l'insuline en grande quantité mais après de nombreuses années une phase d'insulinodéficience s'installe, dans laquelle le pancréas ne peut plus sécréter d'insuline en quantité suffisante pour réguler le taux de glucose ;
– le diabète gestationnel, apparaît pendant la grossesse, il est dû à une production insuffisante d'insuline et se traduit par une intolérance au glucose entraînant une hyperglycémie et un diabète. Cet état est transitoire et disparaît après l'accouchement. D'autres types de diabètes existent, moins fréquents :
– le diabète MODY : le MODY ou Maturity Onset Diabetes of the Young, est un diabète familial de transmission autosomique dominante, monogénique, de survenue précoce, avant l'âge de 25 ans et ne nécessitant pas l'utilisation d'insuline dans les premières années après le diagnostic et répondant aux antidiabétiques oraux ;
– le diabète de type 1 lent ou LADA (Latent Autoimmune Diabetes in Adults) ; – le diabète cétosique du sujet noir ;
– les diabètes secondaires.
D'après les recommandations de l'OMS (Organisation Mondiale de la Santé), un patient présente un diabète sucré dans les cas suivants :
– une glycémie à jeun supérieure ou égale à 1,26g/l (7 mmol/l) mesurée à deux reprises ; – ou la présence de signes cliniques d'hyperglycémie et la découverte à un moment
quelconque de la journée d'une glycémie supérieure ou égale à 2g/L (11 mmol/L) et quelque soit la distance du prélèvement sanguin par rapport à un repas ;
– ou une glycémie à la deuxième heure d'une hyperglycémie provoquée par voie orale (HGPO) supérieure ou égale à 2g/L (11,1 mmol/L). Le test doit être pratiqué selon les
recommandations de l'OMS en utilisant une charge orale en glucose anhydre égale à 75g que l'on dissout dans de l'eau.
La mesure de la glycémie peut être exprimée dans plusieurs unités : – en grammes par litre (g/L) qui est l'unité usuelle en France ;
– en milligramme par décilitre (mg/dL), qui est l'unité américaine, la plus souvent utilisée sur les lecteurs de glycémie ;
– en millimole par litre (mmol/L), qui est l'unité réglementaire et qui devrait être utilisé en pratique courante.
2 Anomalie de la glucorégulation ou état prédiabétique [1]
C'est une période pendant laquelle le sujet présente un certain nombre d'anomalies cliniques ou biologiques connues comme des facteurs prédisposant au diabète de type 2 et à ses complications, il s'agit du syndrome métabolique. Ces anomalies sont : obésité, antécédents familiaux de diabète de type 2, dyslipidémie avec hypertriglycéridémie et diminution du HDL-cholestérol.
Le terme « prédiabète » renvoie, après analyse du sang veineux, à :
– une hyperglycémie modérée à jeun comprise entre 1g/L et 1,25g/L;
– ou à une intolérance au glucose pour des sujets dont la glycémie à jeun est inférieure à 1,26g/L et dont la glycémie à la deuxième heure d'une épreuve d'hyperglycémie orale (75g de glucose per os) est comprise entre 1,40g/L et 1,99g/L.
B Épidémiologie
[3, 4, 5,6]Le diabète est en expansion partout dans le monde, le nombre des personnes atteintes est passé de 108 millions en 1980 à 422 millions en 2014 et devrait atteindre les 592 millions en 2035, si bien que l'on parle actuellement d' « épidémie de diabète ».
Si le diabète de type 1 est en légère augmentation, c'est avant tout le diabète de type 2 qui est en très forte croissance. Celle ci est liée au vieillissement des populations et aux changements de mode de vie (réduction de l'activité physique, alimentation de plus en plus riche en graisses saturées avec diminution des fibres) source de prise de poids et d'obésité.Cette augmentation du nombre de diabétiques dans le monde va se poursuivre, voire même s'accentuer dans le futur. Cette « épidémie de diabète » engendre des coûts majeurs, humains et financiers, pour les individus et pour la société du fait des complications liées au diabète. Il n'est alors pas exagéré de dire aujourd'hui que le diabète représente un véritable problème de santé publique essentiellement du fait de l'expansion du diabète de type 2.
En effet, le diabète de type 1 est une maladie relativement rare, représentant moins de 10% de l'ensemble des diabètes. Alors que le diabète de type 2 lui, représente l'essentiel du problème de santé publique puisque plus de 90% des diabétiques ont un diabète de type 2.
En France, en 2015, 3,7 millions de personnes prenaient un traitement médicamenteux pour le diabète (soit 5,4% de la population). À cela, s'ajoutent les personnes diabétiques qui s'ignorent. Cette prévalence ne cesse d'augmenter et particulièrement chez les hommes, les jeunes (<20 ans) et les plus âgés (>80 ans).
Le vieillissement de la population, le dépistage précoce et l'amélioration de l'espérance de vie des personnes traitées augmentent mécaniquement les chiffres, mais ce sont surtout des facteurs sociaux et environnementaux qui expliquent cet accroissement constant. Surpoids, obésité, manque d'activité physique, sédentarité constituent les principales causes du diabète en France.
Le nombre de personnes diabétiques âgées de 75 ans et plus en France atteint 26% soit une personne sur quatre. Chez l'enfant et l'adolescent le diabète de type 1 est le plus fréquent et son incidence augmente, elle était estimée à 8 pour 100 000 enfants âgés de moins de 15 ans en 1988 et 18 pour 100 000 sur la période de 2013 à 2015. De plus, l'âge au diagnostic se décale vers des âges de plus en plus jeunes. Or les tout-petits requièrent une prise en charge hospitalière pédiatrique très spécialisée. Par ailleurs, le diabète de type 2, autrefois considéré comme une pathologie de l'adulte d'âge mûr, fait son apparition en pédiatrie suite à l'augmentation de la prévalence du surpoids et de la sédentarité. Cette émergence est inquiétante car la prise en charge du diabète de type 2 n'est pas codifiée en pédiatrie et les complications, y compris cardio-vasculaires, peuvent apparaître précocement.
C Classification des diabètes
[2]Il est classique de distinguer deux grands types de diabète : le diabète de type 1 et le diabète de type 2, auxquels s'ajoutent d'autres types de diabète qui répondent à des situations spécifiques :
– le diabète gestationnel dont la découverte est faite en cours de grossesse ;
– les diabètes relevant de causes diverses : déficits génétiques soit de la fonction des cellules bêta de Langerhans soit de la sensibilité à l'insuline, maladies du pancréas exocrine, diabètes induits par des traitements médicamenteux.
1 Diabète de type 1 [7, 8]
a Définition
Le diabète de type 1 est une maladie auto-immune spécifique d'organe, survenant sur un terrain favorable, caractérisé par des gènes de susceptibilité, et provoquée par l'intervention de facteurs liés à l'environnement.
On distingue dans la classification de l'American Diabetes Association qui fait référence, deux sous-types :
– le diabète de type 1 auto-immun, le plus fréquent (il représente plus de 90% des cas en Europe), incluant le type 1 lent ou LADA ;
– le diabète de type 1 idiopathique (caractérisé par l'absence d'anticorps) : il s'agit d'un cadre nosologique mal défini, incluant les diabètes cétosiques du sujet noir d'origine d'Afrique subsaharienne ou les diabètes de type 1 sans preuve immunologique mise en évidence.
b Critères diagnostic
Le diabète de type 1 se manifeste pas une présentation clinique initiale habituelle : – diabète juvénile ;
– diabète à révélation brutale ; – diabète cétosique ;
– insulinopénie quasi totale. • Diabète juvénile
Le diabète de type 1 survient en général chez des sujets jeunes (enfants, adolescents), avec un pic de fréquence dans la période péripubertaire. Il survient également chez des adultes jeunes et il n'est pas rare de voir un diabète de type 1 apparaître chez un sujet autour de la trentaine. Au-delà, le risque de survenue d'un diabète de type 1 devient beaucoup plus faible.
• Diabète à révélation brutale
Chez les diabétiques de type 1, la symptomatologie de départ est bruyante avec présence de signes cardinaux qui sont :
– la polyurie : augmentation de la diurèse ;
– la polydipsie : soif excessive avec augmentation de l'absorption de liquides, causée par la polyurie. C'est en général le signe d'alerte ;
– la polyphagie : faim excessive avec absence de sensation de satiété, traduisant un excès dans le comportement alimentaire ;
– l'amaigrissement : conséquence de la glycosurie car les calories représentées par les glucides éliminés dans les urines sont des calories non utilisées par l'organisme, ce qui entraîne la polyphagie.
Ces signes s'installent en général en quelques semaines ou parfois quelques jours chez des sujets jusque là en bonne santé apparente.
Cependant, la première modification qui apparaît et qui doit faire penser à un diabète de type 1 chez un sujet jeune est un amaigrissement anormal, sans modification de l'alimentation.
• Diabète cétosique
La cétose est la conséquence de l'insulinopénie. L'insuline a normalement une action antilipolytique, or en cas de carence sévère en insuline, les triglycérides du tissus adipeux sont hydrolysés. Les acides gras sont libérés de manière trop importante et une partie d'entre eux est convertie en corps cétoniques éliminés ensuite par les urines et par voie respiratoire. La recherche de corps cétoniques dans les urines à l'aide de bandelettes réactives est la meilleure méthode pour repérer les états de cétose.
• Insulinopénie [8]
L'insulinopénie est la conséquence d'une destruction des cellules bêta des îlots de Langerhans par un mécanisme dépendant des lymphocytes T. Lorsque la masse des cellules bêta de Langerhans tombe en dessous de 20% du capital normal, les signes cardinaux apparaissent.
Le diagnostic par la mesure de la glycémie veineuse doit être effectué, cependant en présence du syndrome cardinal, il n'est pas nécessaire de vérifier la glycémie à jeun pour poser le diagnostic lorsque la glycémie, à n'importe quel moment de la journée, dépasse 2g/L.
c Physiopathologie [9,10]
Le diabète de type 1 est une maladie auto-immune correspondant à la destruction progressive des cellules bêta des îlots de Langerhans, qui normalement synthétisent l'insuline, aboutissant à une carence absolue en insuline. L'hyperglycémie apparaît lorsque environ 90 % des cellules bêta ont été détruites.
La survenue d'un diabète de type 1 nécessite : – des facteurs génétiques prédisposant ; – des facteurs déclenchant ;
– le développement du processus auto-immun.
• Prédisposition génétique [12]
La prédisposition génétique est toujours présente même si dans 85% des cas il n'existe pas d'antécédents familiaux de diabète de type 1.
Les principaux gènes de prédisposition appartiennent au complexe majeur d'histocompatibilité (CMH) ; il s'agit de différents antigènes de classe II appelés HLA (human leukocyte antigen). Cette région génétique de plus forte susceptibilité est située sur le bras court du chromosome 6 et intervient pour 40% de l'ensemble du risque génétique. 90 à 95% des sujets caucasiens qui développent un diabète de type 1 dès l'enfance ou l'adolescence sont porteurs des allèles DR3 et/ou DR4. Les sujets hétérozygotes DR3/DR4 ont 50 fois plus de risques de développer un diabète que la population générale.
D'autres allèles, comme le HLA-DR15, semblent au contraire « protecteurs »vis-à-vis du diabète de type 1.
Même si l'influence du système HLA est majoritaire, la prédisposition au diabète de type 1 est polygénique, elle serait liée à l'effet conjoint de plusieurs gènes du CMH ainsi qu'à d'autres gènes appartenant à d'autres systèmes.
Risque dans la population générale Apparenté de 1er degré
Deux parents diabétiques
Apparenté de 1er degré avec identité HLA
Apparenté de 1er degré avec identité HLA et HLA-DR3 ou DR4 Jumeaux Jumeaux + HLA-DR3 ou DR4 0,4 % 5 % 30 % 12 % 16 % 50 % 70 %
Tableau 1: Risques de diabète de type 1 en France [12]
Cependant, ces facteurs génétiques ne peuvent expliquer à eux seuls le déclenchement du processus auto-immun, ceci implique que d'autres facteurs doivent se surajouter aux facteurs génétiques.
• Facteurs environnementaux initiant le processus auto-immun
Des facteurs environnementaux pourraient être impliqués dans la mise en route du processus auto-immun, nombreux sont évoqués mais aucun n'est absolument prouvé :
– infection virale : virus de la rubéole, CMV (cytomégalovirus), virus ourlien, coxsackie ; – facteurs diététiques : introduction précoce du lait de vache dans l'alimentation du
nouveau-né ; – facteurs toxiques ;
– facteurs hormonaux : puberté.
Ces facteurs ne doivent pas être confondus avec les facteurs déclenchant immédiats de l'hyperglycémie révélatrice du diabète : facteurs émotionnels (choc affectif) et pathologie intercurrente (grippe) retrouvés dans les semaines précédant la découverte de la maladie. Il s'agit alors d'un facteur de « décompensation » révélateur de la maladie, mais pas d'un facteur déclenchant le processus auto-immun, celui-ci étant probablement en cours depuis plusieurs mois voir plusieurs années.
• Le processus auto-immun
Le processus auto-immun a pour cible les cellules bêta des îlots de Langerhans du pancréas, où se développe une insulite avec infiltration lymphoplasmocytaire et une réaction inflammatoire. L'immunité cellulaire joue un rôle prépondérant, notamment par l'activation des lymphocytes T4, responsables de l'initiation de la réponse immunitaire, et par l'effet destructeur sur les cellules bêta des lymphocytes T8 cytotoxiques.
Le processus auto-immun s'accompagne de l'apparition d'auto-anticorps :
– auto-anticorps anti-GAD (anti-décarboxylase de l'acide glutamique des cellules bêta des îlots de Langerhans, enzyme qui catalyse la transformation du glutamate en acide gamma-amino-butyrique(GABA)) : présents dans 38% des cas de diabète et persistant durant toute la maladie ;
– auto-anticorps anti-cellules des îlots, les ICA (Islet Cell Antibody): très spécifiques du diabète de type 1 et détectables chez le sujet jeune, ils disparaissent par la suite chez la majorité des patients ;
particulier chez l'enfant et notamment les sujets HLA-DR4 ;
– auto-anticorps anti-IA2 : dirigés contre une tyrosine phosphatase membranaire des îlots de Langerhans et témoins de l'imminence de la maladie clinique.
La destruction des cellules bêta des îlots de Langerhans est un processus étalé sur plusieurs années avant et après l'apparition du diabète.
• Intérêt de la recherche des anticorps pancréatiques [11]
La recherche de ces auto-anticorps peut être effectuée dans deux indications :
– le dépistage des sujets en train de développer une insulite auto-immune à bas bruit, soit dans la fratrie d'un enfant diabétique, soit chez les enfants d'un parent diabétique. Plus on retrouve d'auto-anticorps différents plus le risque de développer un diabète de type 1 est important. Ce dépistage a un intérêt soit pour rassurer l'entourage si il est négatif, soit pour démarrer le plus tôt possible une insulinothérapie a minima, qui pourrait retarder la destruction des cellules bêta ;
– dans le cas d'exclusion, chez le sujet diabétique jeune qui ne présente pas toutes les caractéristiques du diabète de type 1 ou de type 2, la recherche d'auto-anticorps va mettre en évidence la présence d'un diabète auto-immun, de type MODY.
En pratique, cette recherche n'est que rarement faite.
d Formes particulières du diabète de type 1 [9, 12]
• Diabète de type 1 lent ou LADA
Le diabète LADA apparaît généralement chez les adultes entre 30 et 50 ans sans surcharge pondérale. Ce type de diabète présente une phase de pré-diabète longue avec un début tardif et et une apparition progressive.
Comme le diabète de type 1, il comporte une composante auto-immune, caractérisée par la présence d'auto-anticorps dans le sang. Ces anticorps engendrent une destruction lente et progressive des cellules bêta des îlots de Langerhans, augmentant le risque de progresser rapidement vers une dépendance à l'insuline.
Le LADA représenterait jusqu'à 10% des diabètes qui semblent à première vu être des diabètes de type 2.
• Diabète cétosique du sujet noir
Il s'agit du diabète cétosique du sujet noir d'origine africaine subsaharienne (antillais, africain, non américain). Le mécanisme de ce diabète demeure méconnu, le diagnostic repose sur l'origine ethnique du sujet et une évolution particulière de l'insulino-dépendance. En effet, le début se caractérise par une décompensation cétosique, entraînant une insulinothérapie et après normalisation de la glycémie, une possibilité d'arrêt de l'insuline dans 50% des cas. Les épisodes de cétose peuvent se répéter et sont entrecoupés de phases de rémission. L'obésité y est inconstante et les anticorps spécifiques du diabète de type 1 sont négatifs.
2 Diabète de type 2 [13, 14]
a Définition
Le diabète de type 2 est une pathologie polygénique, dont l'expression dépend de facteurs d'environnement, en particulier : la consommation excessive de graisses saturées et de sucres rapide et la sédentarité. Les personnes les plus à risque sont les personnes obèses, présentant une anomalie du métabolisme glucidique ou ayant des antécédents familiaux de diabète de type 2. Le diabète de type 2 est découvert le plus souvent à l'âge adulte.
L'insulino-déficience responsable de l'hyperglycémie du diabète de type 2 est précédée par 10 ou 20 ans d'hypersécrétion insulinique (hyperinsulinisme) secondaire à une insulino-résistance des tissus périphériques.
b Critères diagnostic [115, 116]
Les signes cliniques sont secondaires à l'hyperglycémie. Cette forme de diabète passe souvent inaperçue car l'hyperglycémie se développe graduellement mais les patients, bien qu'asymptomatiques, sont à risque de développer des complications micro et macrovasculaires. La décompensation sévère du diabète peut entraîner les symptômes suivants : polyurie, polydipsie, amaigrissement, prurit valvulaire chez la femme et balanite chez l'homme et infections récidivantes ou traînantes.
Le dépistage par la glycémie veineuse à jeun doit être réalisée :
– chez tous les sujets présentant des signes cliniques évocateurs de diabète ;
– chez tous les sujets âgés de plus de 40 ans, à répéter tous les 3 ans en l'absence de facteur de risque de diabète existant, et plus précocement en cas d'apparition d'un facteur de risque. Le risque de développer un diabète de type 2 augmente avec l'âge;
– chez les patients qui présentent un ou plusieurs facteurs de risque, à répéter tous les ans en cas de bilan normal.
Les facteurs de risque du diabète de type 2, regroupent un ensemble de caractéristiques souvent associées chez un individu et qui constituent le syndrome métabolique. Celui-ci est composé d'une obésité centrale, d'une hypertriglycéridémie, d'une baisse du HDL cholestérol, d'une hypertension artérielle et d'une intolérance au glucose.
Ces facteurs de risque doivent orienter les patients vers un dépistage, ce sont plus particulièrement :
– une obésité ou un surpoids correspondant à un Indice de Masse Corporelle (IMC) supérieur ou égal à 25kg/m² ;
– un antécédent de diabète familial au premier degré (père, mère, fratrie);
– obésité abdominale : selon les normes européennes : tour de taille supérieur à 80 cm chez les femmes et tour de taille supérieur à 94 cm chez les hommes.
– une hypertension artérielle supérieure à 140/90 mmHg traitée ou non ;
– une dyslipidémie traitée ou non : avec hypertriglycéridémie supérieure à 2g/L et/ou HDL cholestérol inférieur 0,35g/L ;
De plus, on peut retrouver comme facteurs de risque :
– chez les femmes, un antécédent de diabète gestationnel ou de naissance d'un enfant pesant plus de 4kg (macrosomie fœtale);
– un antécédent de diabète cortico-induit ;
Dans le cas de la découverte d'une hyperglycémie, les facteurs de risque listés ci-dessus deviennent les arguments en faveur d'un diabète de type 2.
Le diabète de type 2 ne doit pas être confondu avec :
– le diabète de type 1 lent LADA : caractérisé par la minceur du patient, l'absence d'antécédents familiaux et la présence d'un taux d'anticorps anti-IA2 et anti-GAD positif ; – les diabètes monogénétiques, survenant dans un contexte d'antécédents familiaux et
d'atypie : diabète MODY2 (diabète modéré du sujet jeune), diabète MODY 3 (diabète sévère du sujet jeune ou rapidement insulinoréquérant, pseudo type 1) et le diabète mitochondrial à transmission maternelle.
c Physiopathologie [13, 14, 15]
Le diabète de type 2 est caractérisé par deux anomalies du métabolisme glucidique : une insulinorésistance des tissus périphériques et une insulinodéficience, qui correspond à un défaut sécrétoire qualitatif et quantitatif de la cellule bêta des îlots de Langerhans.
L'insuline sécrétée au cours du diabète est structurellement normale, mais les tissus cibles sont beaucoup moins sensibles au message qu'elle véhicule. Cette résistance à l'action de l'insuline concerne principalement le foie, le muscle et le tissu adipeux.
L'insulinorésistance survient sur un terrain génétique de susceptibilité et se caractérise par l'incapacité de l'insuline à obtenir une réponse maximale au niveau de ses organes cibles, en particulier les muscles, responsable d'une diminution de l'utilisation du glucose ;
Au niveau clinique, elle se traduit par une obésité androïde et s'accompagne souvent d'HTA, d'hypertriglycéridémie et d'un faible taux d'HDL cholestérol.
Cette insulinorésistance entraîne pendant plusieurs années un hyperinsulinisme, c'est à dire une forte sécrétion d'insuline afin de maintenir la glycémie dans les valeurs normales (glycémie à jeun inférieure à 1,00g/L ou 5,5 mmol/L). Mais progressivement, l'insulinosécrétion baisse en même temps que la glycémie remonte et dépasse les valeurs normales, on arrive alors au stade d'insulinodéficience.
L'insulinodéficience correspond a une incapacité du pancréas a sécréter suffisamment d'insuline pour réguler le taux de glucose dans le sang. Cette insulinodéficience apparaît progressivement jusqu'à devenir totale, la glycémie veineuse à jeun dépasse 1,26g/L et le diabète s'installe.
► La prédisposition héréditaire est importante dans ce diabète : lorsque l'un des parents est diabétique, le risque pour les enfants de développer un diabète de type 2 est de 30% et augmente à 50% si les deux parents le sont.
Ceci a des conséquences en terme de santé publique et nécessite de se préoccuper de la prévention de la maladie chez les enfants et petits enfants des diabétiques en leur prodiguant des conseils diététiques visant à réduire ou prévenir la surcharge pondérale et surtout en les encourageant à avoir une activité physique. Le pharmacien, de par sa proximité auprès des patients et de leur famille, peut participer à cette prévention et apporter les conseils appropriés.
3 Diabète gestationnel [13, 16]
a Définition
Le diabète gestationnel est défini par l'OMS comme un trouble de la tolérance au glucose conduisant à une hyperglycémie de sévérité variable, débutant ou diagnostiqué pour la première fois pendant la grossesse. La prévalence du diabète gestationnel est estimée entre 2 et 6% de l'ensemble des grossesses en France.
b Critères diagnostic
Les nouvelles recommandations de la Société Francophone du Diabète et du Collège National des Gynécologues et Obstétriciens Français (CNGOF) pour le diagnostic du diabète gestationnel sont, en présence de facteurs de risque de demander :
– une glycémie à jeun au premier trimestre avec un seuil fixé à 0,92g/L, permettant d'éliminer un diabète de type 2 pré-existant (glycémie à jeun supérieure à 1,26 g/L) ; – une hyperglycémie provoquée par voie orale avec 75g de glucose entre 24 et 28 semaines
d’aménorrhée avec 3 valeurs, dont une seule pathologique permet de retenir le diagnostic de diabète gestationnel : à T0, glycémie inférieure à 0,92g/L, à T1h, glycémie inférieure à 1,80g/L et à T2h, glycémie inférieure à 1,53g/L.
Les facteurs de risque de diabète gestationnel sont : – l'âge maternel supérieur ou égal à 35 ans ;
– un surpoids maternel avant la grossesse (IMC > 25kg/m²) ; – une prise de poids excessive pendant la grossesse ;
– des antécédents de diabète au premier degré ;
– des antécédents personnels de diabète gestationnel ou de macrosomie ; – des antécédents d'hypertension artérielle.
Pour le suivi du diabète gestationnel, l'objectif est : – à jeun : une glycémie inférieure à 0,95g/L
– deux heures en post-prandial : une glycémie inférieure à 1,20g/L.
c Physiopathologie
Au cours de la grossesse, de multiples adaptations sont nécessaires afin d'assurer le flux énergétique indispensable à la croissance du fœtus. Lors du premier trimestre, l'organisme de la femme enceinte développe une sensibilité accrue à l'insuline, cette période correspond à un anabolisme facilité permettant la mise en réserve des nutriments. Dès le deuxième trimestre, la sensibilité à l'insuline va s'inverser, de façon à assurer les besoins de l'unité foetoplacentaire. Ainsi, chez la femme enceinte, l'insulinosensibilité diminue de façon physiologique et progressive au cours de la grossesse pour être à son minimum au troisième trimestre, avec une baisse d'environ 50% de l'utilisation du glucose induite par l'insuline.
Plusieurs facteurs tels que la génétique, l'âge, l'obésité, la distribution des graisses, les habitudes alimentaires et l'exercice physique influencent l'importance de cette diminution. Dans une grossesse normale, pour maintenir un état euglycémique, la sécrétion d'insuline doit être augmentée de 200 à 250%. Le diabète gestationnel se développe lorsque la réponse insulinique est insuffisante pour permettre cette compensation.
d Complications du diabète gestationnel
Le diabète gestationnel peut entraîner des complications aussi bien maternelles que fœtales et néonatales.
Les complications pour la mère sont :
– à court terme, une augmentation des risques de prééclampsie et de césarienne selon le degré de l'hyperglycémie initiale ;
– à long terme, un développement de diabète de type 2 dans 20 à 50% des cas en fonction de l'IMC maternel en pré-grossesse.
Les complications pour l'enfant sont :
– à court terme, la macrosomie qui est le risque principal, celle ci est définie par un poids de naissance supérieur à 4kg ou par un poids supérieur au 90ème percentile ;
e Prise en charge
Lorsque le diagnostic de diabète gestationnel est posé la prise en charge doit être initiée rapidement et plusieurs mesures sont mises en place : des mesures hygiéno-diététiques, une surveillance glycémique et une insulinothérapie.
• Les mesures hygiéno-diététiques
Elles constituent la base du traitement, l'apport calorique au cours du diabète gestationnel doit être déterminé selon le poids d'avant grossesse et la prise de poids durant la grossesse. L'apport recommandé est de 25 à 35 kcal/kg par jour. Dans le cas d'une obésité et en l'absence de cétonurie, une restriction calorique à 25kcal/kg par jour peut être établie.
Les apports en glucides lents, en fibres, les sources de calcium, de fer et de vitamines seront privilégiés. De plus l'apport d'aliments à faible index glycémique peut permettre de réduire la nécessité de recours à une insulinothérapie.
• La surveillance glycémique
La surveillance glycémique et plus particulièrement l'autosurveillance, fait partie d'une prise en charge globale permettant une adaptation de la diététique et une aide à l'instauration de l'insuline. Elle est recommandée entre quatre et six fois par jour, en particulier le matin à jeun et 2 heures après les repas, de façon adaptée au degré d'hyperglycémie. Les objectifs glycémiques sont les mêmes que dans le diabète prégestationnel, avec des valeurs cibles de 0,6 à 0,95g/L à jeun et de moins de 1,20g/L deux heures après les repas.
• L'insulinothérapie
Elle sera indispensable dans le cas où la glycémie reste supérieure aux objectifs malgré une semaine de prise en charge diététique. Les antidiabétiques oraux sont contre indiqués en cas de grossesse. Concernant le choix du schéma thérapeutique, celui ci dépendra des données de l'autosurveillance. Le plus souvent celui ci correspond à des injections de bolus d'insuline rapide pour contrôler les glycémies post-prandiales. La patiente réalise alors une à quatre injections par jour, avec augmentation des doses une à deux fois par semaine, afin de maintenir les valeurs de glycémie capillaire en dessous des seuils. Parmi les analogues rapides, la lispro (HUMALOG®) et l'aspart (NOVORAPID®) peuvent être utilisées.
En post-partum, l'allaitement doit être conseillé car il contribue au retour à la normale de la tolérance au glucose à distance de l'accouchement chez la mère.
Trois à six mois après l'accouchement ou après l'arrêt de l'allaitement, il est nécessaire de réaliser un test HGPO, afin d'évaluer la tolérance au glucose. Un antécédent de diabète gestationnel multiplie par 7 le risque de diabète de type 2 et par 1,7 celui de maladies cardiovasculaires.
4 Autres types de diabète[17]
Le diabète en tant que syndrome clinico-biologique, répond à un grand nombre d'étiologies. Outre les formes classiques, diabètes de type 1 et de type 2, il existe des maladies plus rares, les diabètes atypiques. Dans ces diabètes sont regroupés les diabètes secondaires, les formes iatrogènes et les diabètes monogéniques. L'ensemble pourrait représenter environ 3 à 5% des diabètes. Il est important de maintenir une vigilance et/ou une curiosité cliniques chaque fois qu'un patient présente une divergence par rapport aux critères cliniques habituels du diabète. Une telle approche permet parfois de détecter une maladie sous-jacente qui aura sa propre prise en charge et/ou dont l'enjeu pronostique dépasse celui du diabète (cancer du pancréas, hémochromatose, syndrome de Cushing …). Le diabète peut également avoir des particularités imposant une surveillance spécifique (dépistage des manifestations des cytopathies mitochondriales ou de la polyadénomatose hépatique dans le MODY 3...), enfin il peut aussi exiger des stratégies thérapeutiques particulières en terme de médicaments hypoglycémiants (sensibilité des diabètes MODY 3 aux sulfamides …) ou de traitements étiologiques.
a Diabètes secondaires
Il s'agit des diabètes qui surviennent au cours d'affections de la glande pancréatique ou de maladies endocriniennes. Le diabète s'y présente le plus souvent comme une complication, la prise en charge de la maladie causale prime, même si le diabète ne doit pas être négligé. Dans certains cas, le diabète précède les autres signes ou prend le devant sur le tableau clinique, c'est par lui que la maladie pourra être diagnostiquée.
Ces maladies du pancréas sont relativement fréquentes, on retrouve :
– le cancer du pancréas, qui domine ces étiologies par sa sévérité pronostique. Un diabète récent hors contexte familial chez un adulte peut être un mode de révélation du cancer du pancréas ;
– la pancréatite chronique alcoolique, le diabète survient aux stades tardifs de cette maladie ou après résection pancréatique ;
– l'hémochromatose, on y pensera devant une surcharge martiale et/ou des signes associés évocateurs : hépatopathie, chondrocalcinose, hypogonadisme et mélanodermie ;
– la mucoviscidose, où le diabète vient compliquer avec le temps les formes qui présentent une insuffisance pancréatique ;
– les endocrinopathies avec l'acromégalie, le syndrome de Cushing et le phéochromocytome.
b Diabètes iatrogéniques
Certains médicaments peuvent provoquer un diabète, il faut noter que d'autres éléments de prédisposition génétique (antécédents personnels ou familiaux de diabète) ou environnementaux (obésité, syndrome métabolique) sont présents chez les sujets atteints.
Les médicaments diabétogènes sont :
– les corticoïdes administrés par voie orale ou systémique. Une surveillance de la glycémie s'impose chez les sujets particulièrement à risque surtout si les doses sont élevées, si le
traitement est prolongé et/ou s'accompagne d'une prise de poids marquée ;
– les immunosuppresseurs sont responsables des cas de diabète observés après greffe d'organe, comme les inhibiteurs de la calcineurine (ciclosporine A et tacrolimus), souvent associés aux corticoïdes ;
– les neuroleptiques de deuxième génération sont capables de favoriser l'apparition d'un diabète en particulier l'olanzapine et la clozapine. La constatation d'un diabète induit par un neuroleptique doit faire discuter d'un changement de molécule si cela est possible ; – les traitements antirétroviraux de l'affection VIH peuvent favoriser le développement d'un
diabète en induisant un syndrome de lipodystrophie et d'insulino-résistance.
– Les oestroprogestatifs ou les diurétiques ne révèlent un diabète que chez des sujets à très haut risque.
c Diabètes monogéniques
Les formes classiques de diabète apparaissent comme des maladies complexes, résultat d'une interaction entre une susceptibilité oligogénique et des causes environnementales. Mais il existe des diabètes qui n'ont pour cause que la susceptibilité génétique.
• Diabète MODY [123]
Les diabètes MODY (maturity-onset diabetes of the young) regroupent des affections différentes caractérisées par les critères suivants : diabète de survenue précoce (avant l'âge de 25-30 ans), cliniquement non insulino-dépendant, au moins pendant les premières années suivant le diagnostic et de transmission autosomique dominante. Ce groupe est hétérogène et au moins six anomalies géniques ont été identifiées. Parmi ces diabètes, on trouve :
– MODY 2 : le plus fréquent, caractérisé par l'existence d'une hyperglycémie modérée portant principalement sur les glycémies à jeun et présente depuis la naissance. Ce diabète est en général bien contrôlé par le régime. Les hypoglycémiants sont rarement utiles et l'insulinothérapie est envisageable uniquement pendant la grossesse. Le pronostic est bon car les complications sont rares et peu sévères. Le diagnostic repose sur la recherche de mutations dans le gène de la glucokinase ;
– MODY 3 : il représente 25% des diabètes MODY et apparaît en général entre la vingtaine et la trentaine. L'hyperglycémie est franche et expose aux complications spécifiques du diabète. L'expression clinique peut simuler un diabète de type 1 ou de type 2. L'absence d'anticorps anti-GAD est la règle et doit être vérifiée avant tout typage génétique. Cette forme est caractérisée par une sensibilité spécifique aux sulfamides hypoglycémiants. Les autres formes de diabètes MODY sont plus rares.
• Diabète mitochondrial
Il est secondaire à une mutation au niveau de l'ADN mitochondrial (A3243G du gène mitochondrial codant l'ARN de transfert de la leucine) et appelé MIDD (maternatlly inherited diabetes and deafness). Cet ADN mitochondrial est transmit par la mère et dans 90% des cas le diabète est associé à une surdité neurosensorielle. La complexité de l'héritabilité de cette
affection, les atteintes multi-organes, la multiplicité des anomalies moléculaires, la possibilité de traitements spécifiques, font que ces malades relèvent de centres « maladie rare » spécialisés dans les mitonchondriopathies pour le diagnostic et la prise en charge (deux centres en France, un à Paris et l'autre sur les deux villes de Nice et de Marseille).
Le diagnostic de ces diabètes atypiques devra être lié à tout ce qui apparaît inhabituel dans la présentation ou l'évolution du diabète et notamment la présence de signes associés « illégitimes ».
D Diagnostic et suivi biologique
[1, 13, 18]Le diabète sucré se définit par une élévation anormale et chronique de la glycémie, cette anomalie est commune à tous les types de diabètes sucrés. Plusieurs tests permettent aussi bien le diagnostic que le suivi du diabète au niveau biologique.
Un diagnostic de diabète doit être posé si l'un des critères suivants est présent : – une glycémie veineuse à jeun > 1,26g/L (7,0 mmol/L)
– une glycémie deux heures après ingestion de 75g de glucose > 2,0g/L (11,1 mmol/L) – une glycémie aléatoire > 2,0g/L (11,1 mmol/L)
1 Glycémie
On distinguera la mesure de la glycémie à jeun et l'autosurveillance de la glycémie.
a Glycémie à jeun
La glycémie à jeun sur sang veineux est le critère de diagnostic par excellence. Le dosage de la glycémie repose sur une méthode enzymatique utilisant la glucose oxydase. Le dosage glycémique veineux se caractérise par sa fiabilité, sa reproductibilité, sa facilité de réalisation et son coût modéré. La constatation d'une élévation anormale de la glycémie à jeun impose la réalisation rapide d'un second dosage pour confirmer cette anomalie et permettre d'éliminer une éventuelle erreur de mesure.
Concernant les résultats de glycémie à jeun, plusieurs cas peuvent être rencontrés :
– la glycémie est inférieure à 1g/L, le patient n'est pas diabétique, on ne fait plus rien ; – la glycémie est supérieur ou égale à 1,26g/L, le sujet est diabétique à condition de
confirmer cette anomalie par un deuxième dosage quelques jours après. Le diagnostic est confirmé en cas de glycémie à nouveau supérieure ou égale à 1,26g/L ;
– la glycémie est comprise entre 1,10g/L et 1,25g/L, le diagnostic d'hyperglycémie modérée à jeun est posé. Il est possible de refaire quelques jours après une glycémie à jeun afin de confirmer le diagnostic.
b Glycémie post-prandiale ou à n'importe quel moment de la journée
La glycémie post-prandiale est classiquement réalisée deux heures après un repas. Elle peut permettre la mise en évidence d'une diminution de la tolérance glucidique y compris chez des sujets ne présentant pas d'hyperglycémie à jeun.
Un patient sera considéré diabétique si cette mesure de glycémie est supérieure ou égale à 2g/L et que celle ci est associée à des signes cliniques d'hyperglycémie (signes cardinaux classiques).
c Autosurveillance glycémique[19]
La mesure de la glycémie capillaire à l'aide d'un lecteur de glycémie est un outil quotidien de surveillance de l'équilibre glycémique et d'aide à l'adaptation du traitement pour les patients, mais ce n'est pas un moyen de diagnostic.
L'autosurveillance de la glycémie est un ajout utile aux autres mesures de la glycémie. Cette méthode est la seule qui permet de confirmer et de traiter adéquatement l'hypoglycémie au cours du diabète. Elle peut informer le patient des résultats obtenus à la suite des changements apportés à son mode de vie et au traitement médicamenteux, et permet d'assurer une meilleure participation du patient à son traitement. Le patient et le professionnel de santé peuvent tirer profit des informations recueillies pour apporter des modifications et des ajustements à long terme, et prendre des décisions à court terme, comme l'ajustement de l'insulinothérapie.
La fréquence des mesures de la glycémie par le patient doit être déterminée au cas par cas. Les facteurs exerçant une influence sur cette recommandation comprennent le type de diabète, le traitement prescrit, le niveau de maîtrise de la glycémie, les capacités du patient à lire, à écrire et à compter, la tendance à l'hypoglycémie, la connaissance de l'hypoglycémie, les exigences professionnelles et le caractère aigu de la maladie.
Pour les patients diabétiques de type 1 ou 2 traités par insuline, l'autosurveillance de la glycémie est un aspect essentiel de la prise en charge quotidienne du diabète. Des mesures plus fréquentes, avant les repas et deux heures après et également la nuit, sont des renseignements très utiles pour réduire le risque d'hypoglycémie, y compris une hypoglycémie nocturne méconnue.
Il peut y avoir une différence entre les résultats obtenus au moyen d'un lecteur de glycémie et ceux d'un laboratoire. En effet, la mesure capillaire est moins précise que la mesure veineuse en laboratoire. Par ailleurs la glycémie capillaire est discrètement supérieure à la glycémie veineuse en période postprandiale. Pour s'assurer de l'exactitude des résultats de l'autosurveillance de la glycémie, il faut, au moins une fois par an et chaque fois que les indicateurs de contrôle de la glycémie (HbA1c) ne correspondent pas aux résultats obtenus avec le lecteur de glycémie, comparer les mesures du lecteur de glycémie à celles de la glycémie à jeun obtenues au laboratoire.
2 Hyperglycémie provoquée par voie orale (HGPO)
Il s'agit d'une méthode standardisée qui étudie l'évolution de la glycémie après l'absorption, en moins de 5 minutes, de 75 grammes de glucose, dissous dans 200 à 300 ml d'eau. La glycémie veineuse est mesurée à jeun, puis deux heures après la charge en glucose.
Pour permettre une interprétation fiable des résultats, les conditions de réalisation de cette épreuve sont strictes : test réalisé après 12 heures de jeûne nocturne, repos strict pendant l'épreuve et absence de tabac. De plus, durant les trois jours qui précèdent le test, l'apport glucidique doit être contrôlé, un minimum de 200grammes par jour, et l'activité physique ne doit pas être modifiée.
En cas d'anomalie, un deuxième test doit être, théoriquement, pratiqué dans les jours suivants pour confirmer l'anomalie glycémique.
Ces conditions font de l'HGPO un test peu reproductible, onéreux et contraignant pour les patients. En pratique l'utilisation de ce test est donc réservée à des situations particulières comme le dépistage des troubles de glycorégulation durant la grossesse.
3 Hémoglobine glyquée HbA1c[20]
L'hémoglobine glyquée est un marqueur de l'équilibre glycémique utilisé pour le suivi des patients diabétiques. L'HbA1c est stable et reflète la moyenne des glycémies des trois mois précédant le dosage, correspondant à la durée de vie moyenne d'un globule rouge (120 jours). Le glucose plasmatique se fixe sur toutes les protéines, y compris l'hémoglobine, selon une réaction non enzymatique, la glycation. Cette réaction, dont l'intensité est proportionnelle à la glycémie, est un processus continu qui se poursuit pendant toute la vie du globule rouge. L'hémoglobine glyquée HbA1c est le produit de la fixation du glucose sur l'extrémité N-terminale des chaînes bêta de l'hémoglobine A1 qui constitue 98% de l'hémoglobine de l'adulte. Les valeurs usuelles de l'HbA1c sont chez le sujet adulte sain 4 à 6% de l'hémoglobine totale, concernant les patients diabétiques le seuil retenu est de 6,5%, l'objectif étant de se tenir le plus près possible des taux du sujet non diabétique. Lorsque le diabète est mal équilibré, les taux d'hémoglobine glyquée se situent entre 8 et 12%. Dans le cas de deux prélèvements successifs où l'HbA1c est supérieure à 8% il est recommandé de modifier le traitement
L'hémoglobine glyquée est un bon indicateur de l'efficacité du traitement et doit être mesurée tous les trois mois quand les objectifs glycémiques ne sont pas atteints et que l'on ajuste le traitement. Lorsque les objectifs glycémiques sont atteints et maintenus, on peut envisager de mesurer l'HbA1c tous les six mois.
4 Autres tests
a Glycosurie
La glycosurie correspond à la présence de glucose dans les urines, chez un sujet sain sa valeur est strictement nulle. Son apparition est liée à un taux de glucose dans le sang trop important. En effet, à partir d'une certaine valeur maximale pour la glycémie (supérieure à 1,8g/L soit 10mmo/L), les reins ne sont plus capables de réabsorber le glucose dans ce cas le surplus de glucose passe dans les urines. La détection de glucose dans les urines est réalisée à l'aide de bandelettes réactives qui sont trempées directement dans les urines. Cet examen n'est utilisé que dans de rares cas d'urgence.
b Dosage des corps cétoniques
Les corps cétoniques sont trois métabolites (l'acétylacétate, le bêta-D-hydroxybutyrate et l'acétone) produits par le foie à partir de la dégradation des lipides, et plus particulièrement des acides gras, lorsque l'organisme ne dispose plus de réserves suffisantes en glucides, notamment en glucose. Chez une personne en bonne santé, ces corps cétoniques sont recyclés, mais ce processus peut être perturbé chez le patient diabétique. Ils vont alors s'accumuler en proportion croissante (cétose), le risque est l'apparition d'une acido-cétose, urgence médicale qui impose une hospitalisation immédiate. A l'origine d'une cétose, se trouve toujours un facteur déclenchant : interruption de l'insulinothérapie, pathologie lourde (infarctus, pneumonie, grippe), prise de traitements tel que des corticoïdes … Le premier symptôme est l'augmentation de la glycémie, il faut donc contrôler les corps cétoniques, lorsque la glycémie est supérieure à 2,5g/L. La détection des corps cétoniques se fait dans les urines via des bandelettes réactives ou par prélèvement sanguin. Leur détection est intéressante lors de cas de comas inexpliqués afin d'orienter vers un diagnostic de coma diabétique.
E Complications
1 Complications aiguës [21]
a Hypoglycémie
Une hypoglycémie est définie par une valeur de glycémie inférieure à 0,60g/L et résulte d'une inadéquation de l'insulinémie par rapport à la glycémie soit en raison d'un surdosage accidentel ou volontaire en insuline, soit d'une insuffisance d'apports glucidiques (repas insuffisants ou décalés, vomissements... ) ou d'une consommation excessive par l'organisme de glucose liée à une activité physique ou enfin d'un défaut de contre-régulation hormonale (neuropathie végétative).
On parle d'hypoglycémie symptomatique lorsqu'il existe des manifestations cliniques évocatrices, et elle sera dite sévère lorsque son traitement nécessite l'intervention d'une tierce personne.
Les manifestations de l'hypoglycémie sont :
– des signes dysautonomiques ou adrénergiques : sueurs froides, palpitations, tremblements, faim. Ces manifestations sont habituellement facilement perçues par le patient, mais elles peuvent faire défaut après des années d'évolution du diabète ou en cas d'hypoglycémies répétées ;
– des signes neuroglucopéniques : troubles de la concentration ou de l'humeur, difficultés d'élocution, incoordination, diplopie, troubles du comportement. Le patient ne ressent pas toujours ces signes à un stade où il est capable d'intervenir lui même pour les corriger par prise orale de sucre. Le risque est que cette hypoglycémie conduise à des troubles de la conscience voire à un coma profond. L'association à une pâleur et des sueurs froides est très évocatrice, à ce stade la glycémie est habituellement inférieure à 0,30g/L.
Concernant le traitement, les hypoglycémies mineures sont rattrapées par la prise de 2 ou 3 morceaux de sucre ou d'un petit verre de jus de fruits. Lorsqu'il existe des trouble de la conscience, il faut recourir à l'administration de glucose intraveineux (30 à 50 mL de soluté glucosé à 50% puis perfusion de soluté glucosé à 5%). L'alternative est l'injection intramusculaire ou sous-cutanée d'une ampoule de glucagon qui peut être effectuée par une personne de l'entourage du patient informée de la pathologie et du risque d'hypoglycémie du patient.
Tout diabétique insulinotraité doit être informé des manifestations cliniques précoces et des circonstances de survenue de l'hypoglycémie et avoir à sa disposition en permanence des morceaux de sucre. Lorsqu'il existe un risque important d'hypoglycémie sévère, en particulier du fait de la non perception des hypoglycémies, il faut renforcer l'autosurveillance glycémique, optimiser les moyens d'administration de l'insuline pour limiter le risque d'hypoglycémie nocturne et revoir à la hausse les objectifs glycémiques. L'éducation thérapeutique tient une place importante dans la prévention des hypoglycémies sévères.
b Acidocétose[18]
L'acidocétose diabétique est une complication métabolique mettant en jeu le pronostic vital et survenant dans plus de 90% des cas dans le contexte d'un diabète de type 1, soit encore méconnu, soit à l'occasion d'une rupture thérapeutique ou d'une mauvaise adaptation du traitement lors d'une affection intercurrente. Cependant, son incidence est en diminution depuis l'amélioration des modalités de traitement et surtout de la surveillance du diabète de type 1.
L'acidocétose résulte d'une carence absolue ou relative en insuline conduisant à une hyperglycémie par diminution de l'utilisation périphérique du glucose et augmentation de sa production hépatique. Celle-ci conduisant à une polyurie osmotique et une perte électrolytique (déshydratation extracellulaire). La carence en insuline et l'augmentation des hormones de contre-régulation (hormones hyperglycémiantes : glucagon, cortisol, adrénaline, hormone de croissance) vont favoriser la lipolyse et la bêta-oxydation des acides gras conduisant à la production hépatique de corps cétoniques.
Cette acidocétose s'installe sur plusieurs heures voire dans certains cas sur quelques jours, au cours desquels les manifestations cliniques sont essentiellement représentées par le syndrome cardinal ainsi qu'une déshydratation globale, une respiration de Kussmaul (polypnée ample et bruyante),une odeur acétonique de l'haleine, des troubles de la conscience, des troubles digestifs, des crampes musculaires et une hypothermie.
L'acidose est compensée par le pouvoir tampon du sang et la cétose n'est attestée que par la présence de corps cétoniques dans les urines ou dans le sang capillaire. La recherche de corps cétoniques est réalisée soit dans les urines par des bandelettes réactives, soit par prélèvement de sang capillaire au moyen de bandelettes et d'un lecteur spécifiques.
La prise en charge ambulatoire est possible, lors de la phase de constitution de l'acidocétose, par l'administration de suppléments d'insuline rapide associée à un apport glucidique et une hydratation correcte. Une fois l'acidocétose installée, l'hospitalisation est nécessaire et la prise en charge comportera une correction de la déshydratation et une insulinothérapie intraveineuse. La prévention repose sur l'éducation du patient diabétique de type 1 : pas d'interruption de l'insulinothérapie, gestion des situations à risque, recherche des corps cétoniques plasmatiques ou urinaires, correction par des suppléments d'insuline rapide et contrôle de l'évolution de la cétose, avec appel au médecin en cas de persistance ou d'aggravation des troubles.
c États hyperosmolaires
Le coma hyperosmolaire, caractérisé par une hyperglycémie sévère sans cétose est une complication grave. L'état hyperosmolaire s'installe sur plusieurs jours à la faveur d'une carence insulinique. L'hyperglycémie engendrée déclenche une polyurie osmotique, la déshydratation s'installe insidieusement, se traduisant uniquement par une asthénie et une perte de poids. Progressivement, les troubles de la conscience s'aggravent pouvant conduire à un coma profond. La priorité du traitement est la correction de l'hypovolémie et la prévention de l'insuffisance rénale et du collapsus, pouvant résulter de la forte perte d'eau (jusqu'à 5L), par administration de soluté salé isotonique.
Dans de nombreux cas, le coma hyperosmolaire pourrait être évité par une information du patient et de son entourage :
– connaître les manifestations précoces : soif intense, polyurie, amaigrissement rapide, fatigue ;
– circonstances favorisantes ou déclenchantes : maladie intercurrente (infections), accident neurologique, prise de diurétiques ou corticoïdes, canicule ;
– conduite à tenir : maintien d'une hydratation correcte dans les situations à risque, surveillance glycémique et si besoin insulinothérapie transitoire en cas de pathologie intercurrente.
2 Complications chroniques [18]
La gravité du diabète est liée à l'apparition et au développement de complications chroniques, qui touchent de nombreux organes. On distingue parmi ces complications chroniques :
– la microangiopathie, atteinte des capillaires, qui s'exprime essentiellement au niveau de la rétine et des glomérules rénaux ;
– la macroangiopathie, athérosclérose des gros troncs artériels, non spécifique du diabète mais plus fréquente, plus précoce et plus diffuse chez un patient diabétique ;
– la neuropathie : qui touche à la fois les nerfs périphériques et le système nerveux végétatif ;
– le pied diabétique : conséquence de la neuropathie et de l'artériopathie, marqué par la présence de troubles trophiques chroniques.
L'ensemble de ces complications influence le pronostic fonctionnel et vital des patients. Leur caractère insidieux et peu symptomatique explique le plus souvent leur diagnostic tardif et la gravité du pronostic fonctionnel.
a Rétinopathie diabétique [22, 23, 24]
La rétinopathie diabétique est une des complications les plus fréquentes et les plus précoces de la microangiopathie diabétique. Elle représente la première cause de cécité avant l'âge de 55 ans. Son évolution est lente et progressive tout au long de la vie du patient diabétique, elle reste asymptomatique très longtemps et ne devient symptomatique qu'au stade de complications. Seul un examen régulier et systématique permet de diagnostiquer précocement la rétinopathie diabétique et de la traiter.
Elle est caractérisée par deux processus physiopathologiques associés, l'ischémie et l’œdème, secondaires à des altérations de la paroi des capillaires rétiniens (fuites vasculaires). Des mécanismes biochimiques et moléculaires conduisent à ces événements, les mécanismes moléculaires intervenant comme médiateurs de la néo-vascularisation et de l'excessive perméabilité ont été identifiés, il s'agit de la voie des polyols, la glycation des protéines, les facteurs de croissance et l'activation de la protéine kinase C.
La durée de l'hyperglycémie chronique est le principal facteur de risque d'apparition de rétinopathie diabétique. Mais d'autres facteurs favorisent une progression rapide, qui sont le déséquilibre glycémique, l'hypertension artérielle non équilibrée, l'insuffisance rénale et la protéinurie, la puberté et la grossesse.
Chez les diabétiques de type 1, la prévalence de la rétinopathie diabétique passe de 0% lors de la découverte du diabète à 90% après 15 années d'évolution. A l'inverse, chez le diabétique de type 2, la prévalence de la rétinopathie diabétique est évaluée à 23% au moment du diagnostic du diabète. Cette constatation impose donc, chez ces patients un bilan ophtalmologique très précoce, règle trop souvent non respectée, voire méconnue. L'examen clé du dépistage et de la surveillance de la rétinopathie diabétique est l'examen du fond d’œil après dilatation de la
![Illustration 1: Mécanisme de l'insulinopénie [119]](https://thumb-eu.123doks.com/thumbv2/123doknet/7335072.211900/13.892.204.703.126.536/illustration-mécanisme-de-l-insulinopénie.webp)
![Illustration 2: Physiopathologie du diabète de type 1 [120]](https://thumb-eu.123doks.com/thumbv2/123doknet/7335072.211900/14.892.169.751.87.459/illustration-physiopathologie-du-diabète-de-type.webp)
![Illustration 3: Physiopathologie du diabète de type 2 [121]](https://thumb-eu.123doks.com/thumbv2/123doknet/7335072.211900/18.892.111.783.399.930/illustration-physiopathologie-du-diabète-de-type.webp)
![Illustration 4: Basal-bolus insulinothérapie intensifiée [10]](https://thumb-eu.123doks.com/thumbv2/123doknet/7335072.211900/39.892.178.655.816.1075/illustration-basal-bolus-insulinothérapie-intensifiée.webp)
![Illustration 7: Lecteur FreeStyle Libre® [123,125]](https://thumb-eu.123doks.com/thumbv2/123doknet/7335072.211900/52.892.200.764.398.623/illustration-lecteur-freestyle-libre.webp)
![Illustration 8: Rotation des zones d'injection de l'insuline [124]](https://thumb-eu.123doks.com/thumbv2/123doknet/7335072.211900/56.892.117.827.821.1050/illustration-rotation-des-zones-d-injection-de-insuline.webp)
![Illustration 9: Stylo à insuline [53]](https://thumb-eu.123doks.com/thumbv2/123doknet/7335072.211900/58.892.169.788.111.249/illustration-stylo-à-insuline.webp)
![Illustration 10: Fixation de l'aiguille au stylo à insuline [53]](https://thumb-eu.123doks.com/thumbv2/123doknet/7335072.211900/59.892.225.701.130.446/illustration-fixation-aiguille-stylo-insuline.webp)
![Tableau 4: Teneur glucidique approximative des principales classes d'aliments pour 100g [64]](https://thumb-eu.123doks.com/thumbv2/123doknet/7335072.211900/67.892.107.811.120.401/tableau-teneur-glucidique-approximative-principales-classes-aliments-g.webp)