Copolyéthersulfones rigides-flexibles : Modulation
des propriétés par modification du segment flexible
Thèse
Adrien Faye
Doctorat de chimie
Philosophiae doctor (Ph.D.)
Québec, Canada
© Adrien Faye, 2016
Copolyéthersulfones rigides-flexibles : Modulation
des propriétés par modification du segment flexible
Thèse
Adrien Faye
Sous la direction de :
iii
Résumé
La présente thèse traite trois thèmes principaux. Le premier volet concerne le contrôle de la cristallinité et la synthèse des polyéthersulfones avec incorporation de doubles liaisons comme espaceurs dans les chaînes du polymère en utilisant deux approches différentes : la polymérisation par métathèse des diènes acycliques (ADMET) et la polycondensation. L’ADMET a permis d’obtenir des copolymères de faibles polydispersités avec des doubles liaisons régulièrement réparties le long des chaînes du polymère. La polycondensation a permis d’obtenir des copolymères de configuration cis ou trans avec incorporation régulière ou aléatoire des doubles liaisons. Pour la synthèse par ADMET, un bloc rigide, terminé par des groupements allyliques, est polymérisé dans le dichlorométhane à l’aide de l’un des catalyseurs de Grubbs : Grubbs deuxième génération (G2) ou Hoveyda-Grubbs (HG). Concernant la polycondensation, on fait réagir un bloc rigide avec un segment flexible de configuration cis ou trans pour obtenir respectivement le copolymère cis ou trans. La diffraction des rayons X et l’analyse enthalpique différentielle (DSC) ont montré que l’isomère cis inhibe complètement la cristallinité alors que la forme trans la favorise.
Le deuxième volet de ce travail repose principalement sur la polycondensation en un
seul pot « one pot en anglais» qui a permis de contrôler les températures de transition vitreuse. La spectrométrie de masse MALDI-TOF a permis de démontrer que les copolymères obtenus avec variation du ratio bloc rigide/segment flexible sont de nature aléatoire et non des copolymères blocs.
Le troisième et dernier thème de ce document concerne principalement le contrôle de l’hydrophilicité par une post-fonctionnalisation des copolymères à travers les doubles liaisons incorporées en utilisant les réactions thiol-ène clic. Le but étant de moduler les propriétés des copolymères pour les adapter à des applications bien définies. Pour une application dans la filtration membranaire par exemple, des chaînes hydrophiles ont été greffées à travers ces doubles liaisons pour augmenter l’hydrophilicité des copolymères.
iv
Abstract
This thesis deals with three main themes. The first component relates to the control of the crystallinity and the synthesis of polyethersulfones with incorporation of double bonds as a spacer in the polymer chains using two different approaches: ADMET (Acyclic Diene Metathesis Polymerization) and polycondensation reactions. ADMET leads to copolymers with low polydispersity index and double bonds regularly distributed along the polymer chains. Polycondensation allows obtaining directly cis or trans configuration copolymers with regular or random incorporation of the double bonds. For the synthesis by ADMET, a rigid block terminated by allyl groups is dissolved in dichloromethane and then polymerized using second generation Grubbs catalyst (G2) and Hoveyda-Grubbs catalyst (HG). Concerning the polycondensation reaction, a rigid block reacts with a flexible segment of cis or trans configuration to respectively give the cis or trans copolymer. X-ray diffraction and differential scanning calorimetry (DSC) showed that the cis isomer inhibits crystallization while the trans form favors it.
The second part of this work is mainly based on the one-pot polycondensation reaction which allowed control the glass transition. MALDI-TOF mass spectrometry was used to show that copolymers obtained by the variation of the rigid bloc/flexible segment ratio are random and not block copolymers.
The third subject of this document mainly concerns the control of the hydrophilicity by post-functionalization of copolymers through the double bonds incorporated using thiol-ene click reactions. The main goal is to modulate the properties of copolymers to suit well-defined applications. For example, for applications in membrane filtration, hydrophilic chains were grafted through double bonds to increase the copolymer hydrophilicity.
v
Table des matières
Résumé ... iii
Abstract ... iv
Table des matières ... v
Liste des tableaux ... ix
Liste des schémas ... x
Liste des figures ... xi
Abréviations ... xiv
Symboles ... xvii
Dédicaces ... xviii
Remerciements ... xx
Avant-propos ... xxii
Chapitre 1 : Introduction générale ... 1
1.1 Revue de la littérature sur la synthèse des PES... 2
1.2 Les réactions thiol-ène clic radicalaires ... 5
1.3 Domaine d’application des PES ... 7
1.3.1 Filtration membranaire ... 10
1.4 Problématique ... 11
I.5 Objectif du projet ... 15
1.6 Méthodologie ... 17
1.6.1 Polymérisation par métathèse des diènes acycliques (ADMET) ... 17
1.6.2 Polycondensation ... 21
1.6.3 Caractérisation des polymères ... 22
1.6.4 Post-fonctionnalisation des copolymères ... 27
1.6.5 Mesures d’angle de contact ... 27
1.7 Références ... 30
Chapitre 2: Crystallization control of etherethersulfone copolymers by regular insertion of an allyl functionality ... 34
Résumé ... 35 Abstract ... 36 2.1 Introduction ... 37 2.2 Experimental section ... 39 2.2.1 Instrumentation ... 39 2.2.2 Materials ... 40 2.2.3 Synthesis of monomers ... 41
2.2.3.1 Synthesis of 4,4’-bis(4-methoxyphenoxy) diphenyl sulfone (MPDS) (Scheme 2.1a) ... 41
2.2.3.2 Synthesis of 4,4’-Bis(4-hydroxyphenoxy) diphenyl sulfone (HPDS) (Scheme 2.1a) ... 42
2.2.3.3 Synthesis of 4,4’-bis(4-allyloxyphenoxy) diphenyl sulfone (APDS) (Scheme 2.1a) ... 43
vi
2.2.3.4 Synthesis of 4-fluoro-4’-hydroxy diphenyl sulfone (FHDS) (Scheme 2.1b) . 44 2.2.3.5 Synthesis of 4-fluoro-4’-methoxy diphenyl sulfone (FMDS) (Scheme 2.1b) 44 2.2.3.6 Synthesis of 4,4’-bis(4-(4-(4-methoxyphenylsulfonyl)
phenoxy)pentoxy)diphenylsulfone (MPSPPDS) (Scheme 2.1b)... 45
2.2.3.7 Synthesis of 4,4’-bis(4-(4-(4-hydroxyphenylsulfonyl)phenoxy)phenoxy) diphenyl sulfone (HPSPPDS) (Scheme 2.1b)... 46
2.2.4 Copolymer synthesis ... 46
2.2.4.1 ADMET polymerization of poly(allyl-co-etherethersulfone) (PA-4EES) (Scheme 2.2a) ... 46
2.2.4.2 Polycondensation of PTA-4EES, PTCA-4EES, PTA-8EES and PCA-8EES copolymers (Schemes 2.2b and 2.2c) ... 47
2.2.4.3 Polycondensation of the PAE-4EES copolymer (Scheme 2.2d) ... 47
2.2.4.4 Hydrogenation to obtain PAH-4EES and PAH-8EES ... 47
2.2.4.5 Halogenation to obtain PACl-4EES and PABr-4EES ... 48
2.2.5 Recrystallization of copolymers. ... 48
2.2.6 Results and discussion ... 49
2.2.6.1 Synthesis of polymers ... 49
2.2.6.1.1 PA-4EES copolymer obtained by ADMET polymerization ... 50
2.2.6.1.2 PTA-xEES and PCA-xEES polymers obtained by polycondensation ... 52
2.2.7 Post-polymerization reactions ... 55
2.2.8 Thermal properties of the copolymers ... 57
2.2.8.1 Thermogravimetric analysis (TGA) ... 57
2.2.8.2 Differential scanning calorimetry (DSC) ... 58
2.2.9 X-ray diffraction... 62
2.2.10 Double melting behaviour ... 68
2.3 Conclusion ... 70
2.4 Acknowledgements ... 71
2.5 References ... 72
Chapitre 3: Synthesis of High Molecular Weight Polyetherethersulfone - Allyl Copolymers of Controlled glass transition ... 74
Résumé ... 75 Abstract ... 76 3.1 Introduction ... 77 3.2 Experimental section ... 78 3.2.1 Instrumentation ... 78 3.2.2 Materials ... 80
3.2.3 Synthesis of the monomer: 4,4’-bis(4-hydroxyphenoxy) diphenyl sulfone (HPDS) ... 80
3.2.4 Polymers synthesis ... 80
3.2.4.1 PEES synthesis10 ... 80
3.2.4.2 Synthesis of poly(4EES-alt-cb) and poly(4EES-alt-tb) ... 81
3.2.4.3 Synthesis of poly(6EES-ran-4EEScb) ... 83
3.2.5 Copolymer film preparation ... 83
vii
3.3 Results and discussion ... 84
3.3.1 Optimization of the synthesis of poly(4EES-alt-cb) and poly(4EES-alt-tb) ... 84
3.3.2 One-pot synthesis of copolymers with longer rigid segments, poly(6EES-ran-4EEScb)... 86
3.3.3 MALDI-TOF investigation of the copolymers ... 88
3.3.4 Thermal properties of copolymers ... 100
3.3.4.1 Thermogravimetric analyses ... 100
3.3.4.2 DSC measurements ... 101
3.3.5 Chemical aging studies ... 104
3.4 Conclusion ... 107
3.5 Acknowledgements ... 107
3.6 References ... 108
Chapitre 4: Postfunctionalization by thiol-ene click reactions of polyetherethersulfone-allyl copolymers for applications in membrane filtration ... 109
Résumé ... 110 Abstract ... 111 4.1 Introduction ... 112 4.2 Experimental section ... 114 4.2.1 Instrumentation ... 114 4.2.2 Materials ... 115
4.2.3 Synthesis of S-2-(2-(2-hydroxyethoxy)ethoxy)ethyl thioacetate (scheme 4.1)20 ... 116
4.2.4 Synthesis of 2-(2-(2-hydroxyethoxy)ethoxy)ethanethiol (PEG2-thiol) (scheme 4.1)21 ... 116
4.2.5 Synthesis of the monomer: 4,4’-bis(4-hydroxyphenoxy) diphenyl sulfone (HPDS) ... 117
4.2.6 Polymers and copolymers used in this work ... 117
4.2.7 Post-functionalization of copolymers by thiol-ene click reactions19 ... 118
4.2.8 Solubility test of the cross-linked copolymer ... 122
4.2.9 CHNS Elementary Analysis ... 122
4.2.9.1 Cross-linking with 2,2′-(ethylenedioxy) diethanethiol (PEG2-dithiol) ... 123
4.2.9.1.1 Theoretical percentage calculation of carbon atoms contained in the copolymer after cross-linking (poly(4EES-alt-cb)-crosslink-PEG2), considering one chain grafted per double bond ... 123
4.2.9.1.2 Theoretical percentage calculation of carbon atoms contained in the copolymer after cross-linking (poly(4EES-alt-cb)-crosslink-PEG2) considering two chains grafted per double bond ... 124
4.2.9.2 Cross-linking with 1,3-propanedithiol (Pr-dithiol) ... 124
4.2.9.2.1 Theoretical percentage calculation of carbon atoms contained in the copolymer after cross-linking (poly(4EES-alt-cb)-crosslink-Pr) ... 124
4.2.10 Cross-link density measurements ... 125
4.2.11 Copolymer film preparation ... 127
4.2.12 Cross-linked copolymer film preparation ... 127
viii
4.3.1 PES and PEES ... 127
4.3.2 Alternate and random copolymer synthesis ... 128
4.3.3 Post-functionalization of copolymers by thiol-ene click reactions ... 128
4.3.4 Hydrophilicity and hydrophobicity studies ... 135
4.3.5 Film cross-linking ... 137
4.4 Conclusion ... 140
4.5 Acknowledgements ... 141
4.6 References ... 142
Chapitre 5 : Conclusion et Recommandations ... 144
5.1 Références ... 149
Annexes ... 150
ix
Liste des tableaux
Tableau 1.1 : Famille des polyéthersulfones avec leurs abréviations, structures
chimiques, noms commerciaux, producteurs et années de synthèse1 ... 2 Tableau 1.2: Réactivité des catalyseurs à base de titane, tungstène, molybdène et
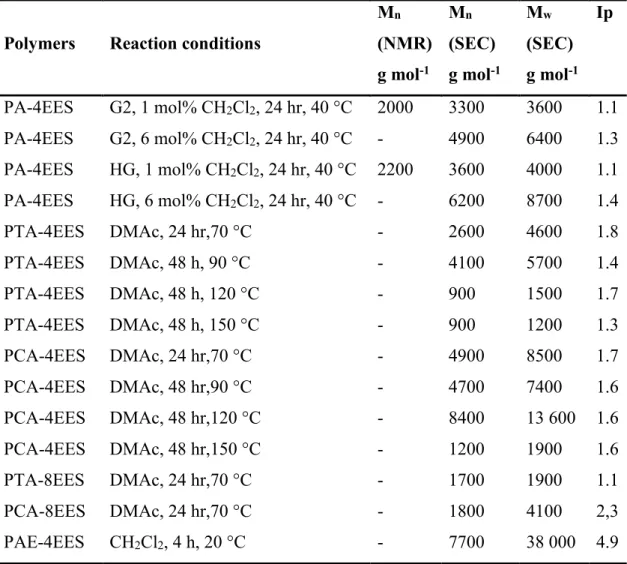
ruthénium vis-à-vis des oléfines en présence de groupements fonctionnels hétéroatomiques62 ... 18 Table 2.1: Molecular weights and dispersity of polymers synthesized by ADMET
and polycondensationa ... 56
Table 2.2: Proton chemical shifts (d) of the allyl group in cis- and trans
poly(etherethersulfones) obtained by polycondensation and by ADMET (major configuration trans) ... 57
Table 3.1: Monomer ratios used in the synthesis of poly(6EES-ran-4EEScb) ... 83 Table 3.2: Number molecular weight (Mn), degree of polymerization (DP) and
polydispersity index (Ip) of Poly(4EES-alt-tb), Poly(4EES-alt-cb) and PEES ... 85
Table 3.3: DSC and SEC data of copolymers synthesized with varying
6EES/4EEScb ratios ... 87
Table 3.4: Proposed assignment for the main MALDI-TOF fragments of the PEES
homopolymer ... 91
Table 3.5: Proposed assignment for the main MALDI-TOF fragments for the
poly(4EES-alt-cb) in the 1000 - 5000 g mol−1 range (only the most intense peaks are
reported in this Table) ... 92
Table 3.6: Proposed assignment for the main MALDI-TOF fragments for the
poly(6EES-ran-4EEScb) in the 1000 - 3500 g.mol−1 range (only the most intense
peaks are reported in this Table) ... 93
Table 3.7: Proposed assignment for additional MALDI-TOF fragments for the
poly(4EES-alt-cb) and poly(6EES-ran-4EEScb) in the 1000 - 4000 g mol−1 range .. 97 Table 3.8: Number molecular weight (Mn) and polydispersity index (Ip) of
poly(4EES-alt-cb) and poly(6EES-ran-4EEScb) copolymers before and after immersed in bleach ... 105
Table 4.1: Grafted and cross-linked molecules and their abbreviations ... 119 Table 4.2: Number molecular weights (Mn), degree of polymerization (DP) and
polydispersity index (Ip) of synthesized polyethersulfone (PES) and polyetherethersulfone (PEES) ... 127
Table 4.3: Number molecular weight, polydispersity index, glass transition
temperature and contact angles of copolymers and functionalized copolymers ... 129
Table 4.4: Carbon elementary analysis and solubility of copolymers cross-linked
with PEG2-dithiol and Pr-dithiol. ... 135
Table 4.5: Glass transition temperatures and contact angles of
Poly(6EES-ran-4EEScb) before and after surface cross-linking ... 138
Table A.2.1: Comparison of diffraction peak position for PES and polymers
x
Liste des schémas
Schéma 1.1 : Formule chimique du PES ... 1
Schéma 1.2 : Synthèse des PES par polysulfonylation utilisée par 3M Corporation12 3 Schéma 1.3 : Synthèse des PES par polyétherification utilisée par Union Carbide Corporation et ICI12... 4
Schéma 1.4 : Synthèse des PEES par polyétherification utilisée par Plastics division of ICI12 ... 4
Schéma 1.5 : Mécanisme de substitution nucléophile aromatique ... 5
Schéma 1.6 : Mécanisme radicalaire du DMPA26 ... 7
Schéma 1.7 : Mécanisme de la réaction thiol-ène clic18,25,27 ... 7
Schéma 1.8 : Catalyseurs de Grubbs utilisés pour l’ADMET... 19
Schéma 1.9: Polymérisation par métathèse des diènes acycliques (ADMET) ... 20
Schéma 1.10 : Mécanisme de polymérisation par métathèse des diènes acycliques (ADMET)69,70 ... 21
Schéma 1.11: Illustration de la polycondensation entre un bloc rigide et un segment flexible... 22
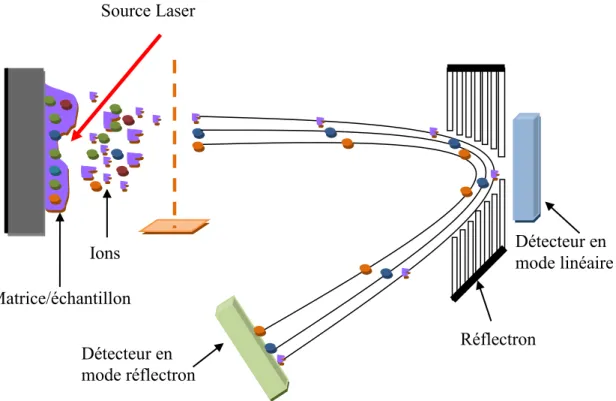
Schéma 1.12: Principe de fonctionnement d’un spectromètre de masse MALDI-TOF.72 ... 25
Scheme 2.1: Synthesis of monomer precursors: (a) APDS (4-ring) precursor and (b) HPSPPDS (8-ring) precursor ... 42
Scheme 2.2: Polymerization reactions: (a) acyclic diene metathesis polymerization (ADMET) of the APDS monomer, (b) polycondensation of HPDS with (Z) and dichlorobut-2-ene, (c) polycondensation of HPSPPDS with (Z) and (E)-1,4-dichlorobut-2-ene and (d) polycondensation with fumaryl chloride to insert ester linkages. ... 49
Scheme 3.1: Synthesis of random and alternate copolymers: a) Poly(4EES-alt-cb) and poly(4EES-alt-tb) alternate copolymers and b) Poly(6EES-ran-4EEScb) random copolymer (one pot polycondensation reaction) ... 82
Scheme 3.2: Repeat units and molar masses of various copolymers reported in the MALDI-TOF study ... 94
Scheme 4.1: Synthesis of 2-(2-(2-hydroxyethoxy)ethoxy)ethanethiol (PEG2-thiol)116 Scheme 4.2 : Polymers and copolymers used in this work... 117
Scheme 4.3: Thiol-ene click reactions onto poly(4EES-alt-cb) copolymer : a) PEG2 -thiol chain grafting and b) Pr-di-thiol and PEG2-dithiol chains cross-linking ... 120
Schéma 5.1 : Illustration de la possibilité d’une liaison intramoléculaire entre l’oxygène proche de la double liaison et le métal central du catalyseur2... 145
xi
Liste des figures
Figure 1.1 : Filtration du lait caillé pour la production du fromage ... 9 Figure 1.2 : Principe d’une membrane de filtration selon Prulho41 ... 10 Figure 1.3 : Images MEB en coupe plane (a) et transversale (b) d’une membrane
colmatée (agrégat de particules encerclé en vert) 50 ... 14 Figure 1.4 : Images MEB d’une coupe transversale d’une membrane de PES seul (a)
et d’un mélange PES/PAN dans un rapport massique 70/30 (d), telles que publiées par Amirilargani et al.57 ... 15 Figure 1.5 : Comparaison des masses molaires obtenues par ADMET avec les
catalyseurs de Grubbs deuxième génération et Hoveyda – Grubbs dans différents solvants63 ... 19 Figure 1.6: Composants basiques d’un spectromètre MALDI-TOF utilisable en mode
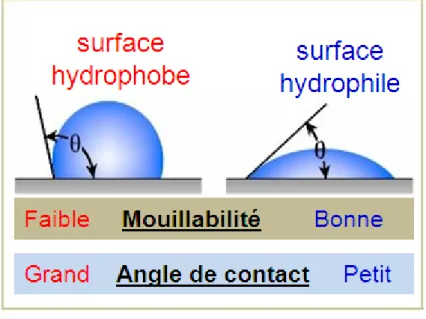
linéaire et mode réflectron72 ... 26 Figure 1.7: Mesure de l’angle de contact ... 28 Figure 1.8: Principe de mesure de l’angle de contact ... 29 Figure 2.1: 1H-NMR spectrum of the representative monomer and polymers obtained
by ADMET: (a) PA-4EES, Mn = 2200 g mol-1 and (b) enlargement showing
end-groups for PA-4EES with two different molecular weights and for the monomer. ... 54
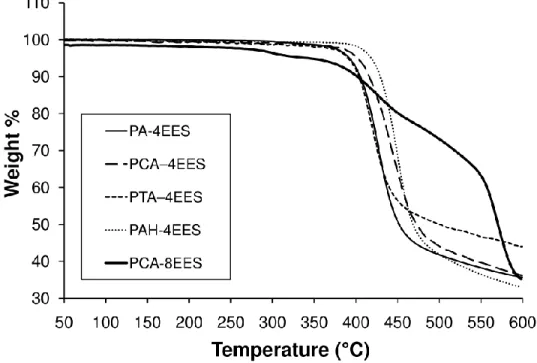
Figure 2.2: Thermal stability of representative 4-ring and 8-ring polymers as
determined by thermogravimetry. ... 58
Figure 2.3: Differential scanning calorimetry: (a) heating and cooling scans for
PA-4EES and (b) first heating scan for representative polymers ... 59
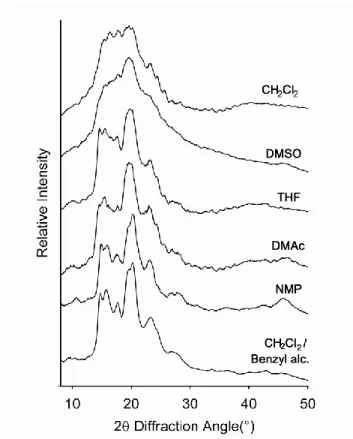
Figure 2.4: X-ray diffraction diagrams of PA-4EES as recrystallized by evaporation
from various solvents ... 63
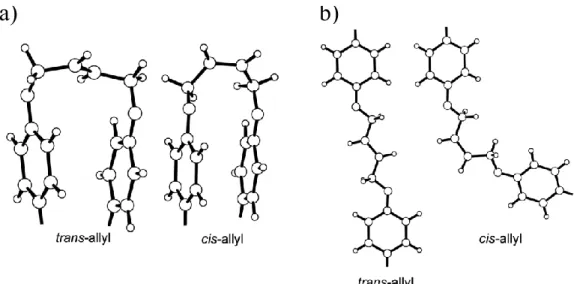
Figure 2.6: Molecular models of chain folding due to allyl groups: (a) chain fold
models and (b) extended chain conformation, showing deviation from linearity... 68
Figure 2.7: Investigation of the double melting behaviour of PA-4EES ... 69
a) Representative DSC scans of PA-4EES and b) X-ray diffraction diagrams as synthesized and after Annealing between Tm1 and Tm2 and rapid quenching ... 69 Figure 3.1: 1H-NMR spectra of poly(6EES-ran-4EEScb) random copolymers... 88 Figure 3.2: Representative MALDI-TOF mass spectrum of synthesized copolymers
a) PEES homopolymer b) Poly(4EES-alt-cb) and c) Poly(6EES-ran-4EEScb), ratio 70/30 ... 90
Figure 3.3: Thermogravimetric degradation curves of poly(4EES-alt-cb) (0/100),
PEES homopolymer (100/0) and random copolymers with varying 6EES/4EEScb ratios ... 100
Figure 3.4: DSC curves of poly(4EES-alt-cb) (0/100), PEES homopolymer (100/0)
and random copolymers with varying 6EES/4EEScb ratios ... 103
Figure 3.5: Changes in glass transition temperatures with varying 6EES weight % in
poly(6EES-ran-4EEScb) copolymers ... 104
Figure 3.6: FTIR spectra of poly(6EES-ran-4EEScb) copolymer before and after
xii
Figure 4.1: FTIR spectra of poly(4EES-alt-cb) and poly(4EES-alt-cb)-graft-PEG2: a)
from 700 to 1900 cm-1 and b) from 2500 to 4000 cm-1 ... 130 Figure 4.2: 1H-NMR spectra of Poly(4EES-alt-cb) and
Poly(4EES-alt-cb)-graft-PEG2 ... 131 Figure 4.3: FTIR spectra of Poly(6EES-ran-4EEScb) and
Poly(6EES-ran-4EEScb)-graft-PEG16 a) from 700 to 1900 cm-1 and b) from 2500 to 4000 cm-1 ... 133 Figure 4.4: 1H-NMR spectra of 4EEScb) and
Poly(6EES-ran-4EEScb)-graft-PEG16 ... 133 Figure 4.5: Contact angles of PES, PEES, alternate copolymer (Poly(4EES-alt-cb)),
and alternate copolymer after cross-linking or grafting ... 136
Figure 4.6: Contact angles of the random copolymer (Poly(6EES-ran-4EEScb)) before
and after grafting or cross-linking ... 137
Figure 4.7: FTIR spectra of Poly(6EES-ran-4EEScb) before and after
surface-cross-linking ... 139
Figure A.2.1: NMR spectra of 4,4’-bis(4-methoxyphenoxy) diphenyl sulfone (MPDS)
in CDCl3 ... 153
Figure A.2.2:NMR spectra of 4,4’-bis(4-hydroxyphenoxy) diphenyl sulfone (HPDS) in DMSO ... 154
Figure A.2.3: NMR spectra of 4,4’-bis(4-allyloxyphenoxy) diphenyl sulfone (APDS)
in CDCl3 ... 155 Figure A.2.4: 1H-NMR spectrum of a) (Z)-1,4-dichlorobut-2-ene in CDCl
3 and b)
(E)-1,4-dichlorobut-2-ene in CDCl3 ... 156 Figure A.2.5: NMR spectra of 4-fluoro-4’-hydroxy diphenyl sulfone (FHDS)... 157 Figure A.2.6: NMR spectra of 4-fluoro-4’-methoxy diphenyl sulfone (FMDS) ... 158
Figure A.2.7: NMR spectra of
4,4'-bis(4-(4-(4-methoxyphenylsulfonyl)phenoxy)phenoxy) diphenyl sulfone (MPSPPDS) in CDCl3 ... 159
Figure A.2.8: NMR spectra of
4,4'-bis(4-(4-(4-hydroxyphenylsulfonyl)phenoxy)phenoxy) diphenyl sulfone (HPSPPDS) in DMSO ... 160
Figure A.2.9: 1H-NMR spectrum of poly(allyl-co-ether ether sulfone ether)
(PA-4EES) in CDCl3 ... 161 Figure A.2.10: 1H-NMR of the 4-ring polymers obtained by polycondensation ... 165 Figure A.2.11: Comparison of PTA-4EES NMR spectra before and after heating,
showing the persistence of the trans signals ... 166
Figure A.3.1: Representative MALDI-TOF mass spectrum of
Poly(6EES-ran-4EEScb), ratio 50/50 ... 168
Figure A.3.2: Representative MALDI-TOF mass spectrum of
Poly(6EES-ran-4EEScb), ratio 60/40 ... 168
Figure A.3.3: Representative MALDI-TOF mass spectrum of
Poly(6EES-ran-4EEScb), ratio 80/20 ... 169
Figure A.3.4: Representative MALDI-TOF mass spectrum of
Poly(6EES-ran-4EEScb), ratio 90/10 ... 169
Figure A.4.1: NMR spectra of S-2-(2-(2-hydroxyethoxy)ethoxy)ethyl thioacetate in
xiii
Figure A.4.2: NMR spectra of 2-(2-(2-hydroxyethoxy)ethoxy)ethanethiol in
CDCl3 ... 171 Figure A.4.3: FTIR spectra of Poly(6EES-ran-4EEScb) and
Poly(6EES-ran-4EEScb)-graft-C8 a) from 700 to 1900 cm-1 and b) from 2500 to 4000 cm-1 ... 172 Figure A.4.4: 1H-NMR spectra of 4EEScb) and
Poly(6EES-ran-4EEScb)-graft-C8 ... 173 Figure A.4.5: FTIR spectra of Poly(4EES-alt-cb) and
Poly(4EES-alt-cb)-crosslink-Pr ... 174 a) from 700 to 1900 cm-1 and b) from 2500 to 4000 cm-1 ... 174 Figure A.4.6: FTIR spectra of Poly(4EES-alt-cb) and
xiv
Abréviations
Å : Ångström
ADMET : Polymérisation par métathèse des diènes acycliques (acyclic diene metathesis polymerization)
alt : Alternate
APDS : 4,4’-Bis(4-allyloxyphenoxy) diphenyl sulfone BBr3 : Tribromure de bore cb : cis but-2-ène CDCl3 : Chloroforme deutérié CHCl3 : Chloroforme CH2Cl2 : Dichlorométhane CH3I : Iodure de méthane Cl : Chlore C8 : Octane d : Doublet dd : Doublet de doublet DMAc : N,N-Diméthylacétamide DMF : N,N-Dimethyformamide DMPA : 2,2-diméthoxy-2-phénylacetophénone DMSO : Diméthylsulfoxyde
DMSO-d6 : Diméthylsulfoxyde deutérié DP : Degré de polymérisation
DSC : Calorimétrie différentielle à balayage ou analyse enthalpique différentielle
E-DCB : (E)-1,4-dichlorobut-2-ène EES : Éther éther sulfone EESE : Éther éther sulfone éther
EG : End-group
FHDS : 4-Fluoro-4’-hydroxy diphenyl sulfone FMDS : 4-Fluoro-4’-methoxy diphenyl sulfone
FTIR : Spectroscopie infrarouge à transformée de Fourier FTIR-ATR : Spectroscopie infrarouge par réflexion totale atténuée G2 : Catalyseur de Grubbs de deuxième génération (Grubbs
second generation catalyst)
H : Hydrogène ou proton
HCl : Acide chlorhydrique HG : Hoveyda–Grubbs catalyst
HPDS : 4,4’-Bis(4-hydroxyphenoxy) diphenyl sulfone
HPSPPDS : 4,4’-Bis(4-(4-(4-hydroxyphenylsulfonyl)phenoxy)phenoxy) diphenyl sulfone
I : Intensité
Ip : Indice de polydispersité
xv K2CO3 : Carbonate de potassium
KOH : Solution aqueuse d’hydroxyde de potassium
kV : kilovolt
Li : Lithium
m : Multiplet
M : Molaire
mA : milliampère
MALDI-TOF : Matrix-Assisted Laser Desorption Ionization –Time Of Flight
MEB : Microscopie Électronique à Balayage mg/mL : Milligramme par millilitre
MgSO4 : Sulfate de magnésium
MHz : Méga Hertz
mL : Millilitre
mmol : Millimole
Mn : Masse molaire moyenne en nombre
MPa : Mégapascal
MPDS : 4,4’-Bis(4-methoxyphenoxy) diphenyl sulfone
MPSPPDS : 4,4’-Bis(4-(4-(4-methoxyphenylsulfonyl) phenoxy)pentoxy) diphenyl sulfone
Mw : Masse molaire moyenne en poids
m/z : Ratio masse sur charge NaCl : Chlorure de sodium NaI : Iodure de sodium
NaOH : Hydroxyde de sodium
NaHCO3 : Bicarbonate de sodium
nm : Nanomètre
NMP : N-Méthyl-2-pyrrolidone
PA-4EES : Poly(allyl-co-ether ether sulfone ether )
PABr-4EES : Poly(brominated allyl-co-ether ether sulfone ether) PACl-4EES : Poly(chlorinated allyl-co-ether ether sulfone ether) PAE-4EES : Poly(trans-allyl-co-ether ether sulfone ester)
PAH-4EES : Poly(hydrogenated allyl-co-ether ether sulfone ether) PAN : Polyacrylonitrile
PCA-4EES : Poly(cis-allyl-co-ether ether sulfone ether)
PEG : Polyéthylène glycol
PEEK : polyétheréthercétone PEES : Polyétheréthersulfone PES : Polyéthersulfone
PPTA : Poly(para-phénylène térephthalamide) ppm : Partie par million
Pr-dithiol : Propanedithiol
PTA-4EES : Poly(trans-allyl-co-ether ether sulfone ether)
ran : Random
xvi
RMN 13C : Résonance magnétique nucléaire du carbone 13
RMN 1H : Résonance magnétique nucléaire du proton
s : Singulet
SEC : Chromatographie d’exclusion stérique SEM : Scanning Electron Microscopy
t : Triplet
tb : trans but-2-ène
Tg : Température de transition vitreuse TGA : Analyse thermogravimétrique Tm : Température de fusion
TMS : Tetraméthysilylane
UV : Ultraviolet
WAXS : «Wide Angle X-ray Scattering» ou diffraction des rayons X aux grands angles
xvii
Symboles
𝑑𝑠 : Densité du solvant g/cm3
𝑑𝑝 : Densité du copolymère en g/cm3
𝑀𝑐 : Masse molaire moyenne en nombre entre les ponts de réticulation 𝑀𝑠 : Masse molaire du solvant g/mol
𝑚𝑝 : Masse du copolymère avant gonflement
𝑚𝑡 : Masse du copolymère à l’équilibre après gonflement (copolymère +
solvant)
𝑅 : Constante des gaz parfaits 𝑇 : Température absolue
𝑉𝑠 : Volume molaire du solvant en cm3/mol
𝑉𝑝 : Fraction volumique du copolymère à l’équilibre après absorption
du solvant
𝑉𝑝𝑟 : Fraction volumique du copolymère réticulé
𝛽 : Constante de réseau 𝛿 : Paramètre de solubilité
𝜒 : Paramètre d’interaction solvant/copolymère 𝜒𝐷𝑆𝐶 : Taux de cristallinité obtenu par DSC
𝜒𝑋−𝑟𝑎𝑦 : Taux de cristallinité obtenu par diffraction des rayons X
𝜌 : Densité du copolymère g/cm3
θ : Thêta
% : Pourcentage
° : Degré
°C : Degré Celsius
°C/min : Degré Celsius par minute 𝛥𝐻 : Enthalpie de fusion
xviii
Dédicaces
Je dédie ce mémoire à :
Ma mère, qui a œuvré pour ma réussite, de par son amour, son soutien, tous les sacrifices consentis et ses précieux conseils, pour toute son assistance et sa présence dans ma vie, reçois à travers ce travail aussi modeste soit-il, l'expression de mes sentiments et de mon éternelle gratitude.
Mon père, qui peut être fier et trouver ici le résultat de longues années de sacrifices et de privations pour m'aider à avancer dans la vie. Puisse Dieu faire en sorte que ce travail porte son fruit ; Merci pour les valeurs nobles, l'éducation et le soutien permanent venu de toi.
Mes frères et sœurs (Jacqueline, Diory, Rose, Sobel, Mane, Mbalam, Watéo, Mame Coumba, Mame Latsouck et Marie Ngounda et à mes demi-frères et demi-sœurs (Diouly, Gnilane et Sara) qui n'ont cessé de m’encourager et d'être pour moi des exemples de persévérance et de courage.
La femme de ma vie, Salimata Ndiaye, mon âme sœur, la lumière de mon chemin. Ma vie à tes cotés est remplie de belles surprises. Tes sacrifices, ton soutien moral et matériel, tes encouragements sans cesse, ta gentillesse sans égal, ton profond attachement m'ont permis d’arriver au bout de ce travail.
xix
« Telle est bien la beauté et la
noblesse de la science : désir sans
fin de repousser les frontières du
savoir, de traquer les secrets de la
matière et de la vie sans idée
préconçue des conséquences
éventuelles. »
xx
Remerciements
Je souhaite adresser mes remerciements les plus sincères à toutes les personnes qui ont contribué de prêt ou de loin à la réussite de cette thèse.
Nulle œuvre n'est exaltante que celle réalisée avec un soutien moral et financier. D’abord, je remercie ma Directrice de thèse, la Professeure Josée Brisson, de m’avoir donné l’opportunité d’intégrer son groupe de recherche, de m’avoir soutenu et permis d’explorer le domaine fascinant de la synthèse des polymères et de leurs caractérisations. Vous ne cessiez pas de m’encourager, encore m’encourager, toujours m’encourager à aller jusqu’au bout de mes synthèses pour l’obtention de copolymères de hautes masses molaires. Vos nombreux conseils, votre imagination et votre énergie tout au long de ce travail ont été, pour moi, une véritable source de motivation afin de mener à bien ce projet. J'aimerais également lui dire à quel point j’ai apprécié sa grande disponibilité tout au long de cette thèse plus particulièrement durant les moments de correction des articles et de ce document. Enfin, j’ai été extrêmement sensible à ses qualités humaines, d'écoute et de compréhension tout au long de ce travail doctoral.
Je souhaite continuer à la côtoyer dans le futur aussi bien dans le cadre professionnel que personnel.
J’adresse également mes remerciements au Professeur Jean-François Morin pour ses conseils et pour m’avoir permis d’opérer les réactions thiol-ène clic dans son laboratoire, mais aussi, pour avoir accepté de faire partie des membres du jury.
Mes remerciements vont également à la Professeure Maria-Cornelia Iliuta pour avoir mis, à ma disposition, les équipements de son laboratoire et de m’aider à procéder aux mesures d’angles de contact.
Je sais infiniment gré au Professeur Jérôme Claverie de l’UQAM de s’être rendu disponible et d’avoir accepté la fonction d’examinateur externe pour cette thèse.
xxi
Je suis particulièrement reconnaissant au Professeur Peter McBreen de l’intérêt qu’il a porté à l’égard de ce travail en acceptant de faire partie du jury.
Mes remerciements vont également à Madame Plesu (TGA, DSC, SEC, Rayons X), Monsieur Audet (RMN), Monsieur Groleau (CHNS), Monsieur Paquet-Mercier (FTIR) et Madame Furtos de l’Université de Montréal (MALDI-TOF).
Je tiens à remercier vivement tous les membres du groupe de la Professeure Brisson : Huan Liang, Abdelkader Benhalima, Simon Provencher, François Hudon et Marianne P. Ouattara. Mention spéciale à Huan Liang, avec qui, j’ai mené des discussions enrichissantes en ce qui concerne nos projets. Je voudrais remercier particulièrement les étudiants stagiaires : Mikaël Leduc qui a participé à l’optimisation du choix du solvant utilisé pour la recristallisation des copolymères présentés dans le chapitre 2 et Jacob Dion Gagné, pour son aide à la préparation des films de polymère.
Enfin, ces remerciements ne peuvent s’achever sans une pensée particulière pour tous mes proches et amis qui m’ont toujours soutenu et encouragé dans les bons comme dans les moments plus difficiles. Merci à toutes et tous !
xxii
Avant-propos
Cette thèse a été rédigée sous la direction de Madame Josée Brisson, Professeure titulaire au département de chimie de l’Université Laval. En étroite collaboration avec ma directrice de recherche, j’ai joué un rôle de premier plan dans la synthèse et la caractérisation des copolymères ainsi que dans la rédaction des articles et de ce document.
Cette thèse comprend cinq chapitres. Le premier et le cinquième chapitre décrivent respectivement l’introduction générale et la conclusion générale. Les chapitres 2, 3, et 4 ont chacun fait l’objet d’un document sous forme d’article qui a été publié ou sera soumis pour publication dans une revue scientifique. Pour chacun de ces articles, j’ai œuvré comme auteur principal en procédant aux synthèses et à la majeure partie des caractérisations des copolymères, en rédigeant la première version des articles, en apportant les modifications suggérées par la professeure Brisson pour tous les articles, mais également, celles suggérées par les arbitres de l’article dans le cas du Chapitre 2.
Les co-auteurs de ces manuscrits ont largement contribué à leur réalisation en participant à l’optimisation de certaines méthodes de caractérisation ou en procédant à leur révision, en plus des conseils et des orientations. Tous mes remerciements à : Mikaël Leduc (Chapitre 2), qui a participé à l’optimisation du choix du solvant utilisé pour la recristallisation des copolymères.
Alexandra Furtos (Chapitre 3), qui nous a aidé dans l’enregistrement des spectres MALDI-TOF et a confirmé notre interprétation
Jean-François Morin (Chapitre 4), qui a proposé certaines voies ou conditions de synthèse, notamment pour les synthèses thiol-ène clic.
Maria Cornelia Iliuta (Chapitre 4), qui nous a assisté dans l’enregistrement des mesures d’angles de contact et dans leur interprétation.
xxiii
Hormis les articles scientifiques, ce travail a fait l’objet de plusieurs présentations dans des conférences nationales et internationales qui sont les suivantes:
A. Faye, J. Brisson, Synthesis and postfunctionalization of polyetherethersulfone-allyl copolymers for applications in membrane filtration, Sustainable Materials
Science and Technology, Paris, France, juillet 2015.
A. Faye, J. Brisson, Synthesis and crystallization control of polyetherethersulfone copolymers by regular insertion of an allyl functionality, High Polymer Forum,
Gananoque, Canada, juillet 2014.
A. Faye, J. Brisson, Synthesis Route for Crystalline Polyethersulfone Copolymers,
96th Canadian Chemistry Conference and Exhibition, Quebec, Canada, mai 2013.
A. Faye, J. Brisson, Synthesis of Polyethersulfone Copolymers via ADMET, High
1
Chapitre 1 : Introduction générale
Les polyéthersulfones (PES) sont des polymères amorphes de la famille des poly(arylène éther sulfone)s et dont la structure chimique est composée de noyaux aromatiques liés à des groupements sulfonyles (-SO2-) et éthers (-O-) (Schéma 1.1).
Les groupements phényles et sulfones sont responsables de la résistance à la chaleur et à l'oxydation, tandis que les éthers contribuent beaucoup à la flexibilité de la chaîne.
Schéma 1.1 : Formule chimique du PES
L’unité de répétition, bien qu’étant régulière, ne permet pas d’obtenir facilement des arrangements ordonnés en raison de l’alternance des groupements éther et sulfone, chacun ayant un angle de valence différent, ce qui nuit à un empilement de chaîne régulier.1,2 La forte polarité des liaisons sulfones conduit à un effet d’attraction
d'électrons qui délocalise les électrons π des noyaux aromatiques, ce qui a tendance à donner un caractère de double liaison aux liaisons C-S de la chaîne. Une telle délocalisation augmente considérablement la barrière de rotation autour des liaisons C-S et par conséquent la rigidité de la chaîne, 3 gênant ainsi leur repliement. Cette
rigidité intrinsèque de la chaîne a également pour conséquence de rendre élevées les températures de transition vitreuse (Tg) de ces matériaux (230 °C environ).4
D’autre part, l'angle de valence C-S-C est de 105° alors que celui entre C-O-C est de 121°.5 Cette différence substantielle dans les angles de liaison réduirait la densité
d’empilement des chaînes. Ceci entraîne une diminution de l'enthalpie de fusion et de la température de fusion (Tm).6 En conséquence, l'intervalle (Tm-Tg) est assez étroit
2
Dans cette même famille de polymères, on rencontre le polysulfone (PSF) et le poly(phényl sulfone) (PPSF) qui ont été commercialisés sous différents noms (voir le
Tableau 1.1)et le poly(éther éther sulfone) (PEES).
Tableau 1.1 : Famille des polyéthersulfones avec leurs abréviations, structures
chimiques, noms commerciaux, producteurs et années de synthèse1
Abréviations Structures chimiques Noms Producteurs Années
PES Victrex ICI 1972
PSF Udel UCC 1965
PPSF Radel UCC 1976
PEES - - -
1.1 Revue de la littérature sur la synthèse des PES
Les PES ont été synthétisés pour la première fois et de façon indépendante dans les années 1960 par trois (3) laboratoires différents que sont : 3M Corporation7 et Union
Carbide Corporation (UCC),8,9 tous deux basés aux États-Unis et le Plastics Division
of ICI10 basé au Royaume Uni. L’objectif était de développer des matériaux
thermoplastiques thermiquement stables répondant à des applications d'ingénierie.11,12
Deux principales méthodes ont été utilisées pour la synthèse des PES. 3M Corporation a synthétisé les PES par polysulfonylation du 4,4'-bis(chlorosulfonyl)diphényle éther avec l’oxydibenzène en utilisant une réaction de Friedel-Crafts,12 tel que montré dans le schéma 1.2, autrement dit en utilisant une
3
substitution électrophile aromatique.1 Cependant, cette méthode est peu sélective et
souffre d’une faible réactivité pour un tel substrat.13 Union Carbide Corporation,
quant à elle, a développé les PES par polyétherification en utilisant une réaction de
substitution nucléophile aromatique12 (Schéma 1.3). ICI a également utilisé la
substitution nucléophile aromatique pour la synthèse de ces polymères mais en
faisant réagir un sel de métal alcalin d’un composé 4-chloro-4’-hydroxy diphényl sulfone sur lui-même pour obtenir un PES (Schéma 1.3a) ou bien un diphénolate de métal alcalin avec un composé bis(4-chlorophényl) sulfone pour obtenir un PEES (Schéma 1.4), en utilisant un solvant polaire aprotique comme le diméthyle sulfoxyde (DMSO).1,6 Cependant, un léger excès de NaOH conduit à un clivage des chaînes du
polymère, ce qui entraîne l’obtention de polymères de faibles masses molaires.14 Par
la suite, des masses molaires élevées ont été obtenues en remplaçant le NaOH par le K2CO3 en présence d’un solvant polaire aprotique de haut point de fusion comme le
sulfolane ou le diphényle sulfone mais à une température très élevée (335 °C).14,15
4
Schéma 1.3 : Synthèse des PES par polyétherification utilisée par Union Carbide
Corporation et ICI12
Schéma 1.4 : Synthèse des PEES par polyétherification utilisée par Plastics division
of ICI12
Les solvants polaires aprotiques, en plus de faciliter la solubilité du polymère, permettent d’augmenter la nucléophilie de l’alcoolate en complexant les cations Na+
ou K+ si l’hydroxyde de potassium est utilisé à la place de l’hydroxyde de sodium,
augmentant ainsi le degré de dissociation.8 Les atomes d’halogène de ces composés
sont activés par le groupe sulfone (groupement fortement électro-attracteur) situé en position para par rapport à l’halogène.8
La principale méthode utilisée pour la synthèse des PES est donc la polycondensation par substitution nucléophile aromatique. Le mécanisme de substitution nucléophile aromatique est présenté dans le Schéma 1.5. Dans un premier temps, le nucléophile attaque le carbone porteur de l’halogène (C-X) activé par le groupement sulfone (groupement fortement électroattracteur). L’halogène X ne part pas directement mais il y a création d’un intermédiaire stabilisé par résonance appelé complexe de
5
Meisenheimer.12 La deuxième étape de réaction consiste à l’élimination du groupe
partant, X.
Les composés fluorés sont plus réactifs que les composés chlorés correspondants qui, eux, sont plus réactifs que leurs analogues bromés car plus l’halogène est électronégatif mieux il stabilise la charge négative de l’intermédiaire réactionnel (complexe de Meisenheimer). L’attaque du nucléophile, dans le cas des composés fluorés, est également favorisée par le caractère non volumineux (donc moins encombrant) des atomes de fluor et la forte polarisation du lien Cδ+-F δ- due à leur
forte électronégativité qui augmente le caractère électrophile de l’atome de carbone.12
Schéma 1.5 : Mécanisme de substitution nucléophile aromatique
1.2 Les réactions thiol-ène clic radicalaires
Le terme chimie clic, introduit en 2001 par Sharpless et al.,16 décrit des couples de
groupements fonctionnels réagissant rapidement et sélectivement l’un avec l’autre dans des conditions douces. Ces réactions chimiques ont pour caractéristiques d’être à la fois modulables, régiosélectives, efficaces donnant des produits facilement purifiables (isolation simple et non chromatographique de l’adduit obtenu) avec des rendements élevés.16,17
Le terme thiol-ène clic est utilisé pour désigner l'addition d'un thiol sur une liaison
ène (double liaison).18 Les réactions thiol-ène clic radicalaires sont des réactions
6
thiol-ène clic radicalaires ont l’avantage de combiner les attributs de la chimie clic et
d'une réaction photoamorcée (activation à des moments et des endroits spécifiques), ce qui fait qu’elles sont des méthodes intéressantes pour la synthèse chimique de matériaux avec des propriétés modulables.19,20 Ces réactions sont donc largement
utilisées dans les domaines des biosciences,21,22 de la chimie médicinale23 et de la
chimie des matériaux.24 Dans la chimie des matériaux polymères, elles sont utilisées
pour faire une polymérisation, une modification de surface, un greffage de molécules ou bien pour synthétiser des dendrimères.25 Comme pour tout procédé radicalaire, il
existe un certain nombre de moyens d'initiation des réactions thiol-ène clic. Ces méthodes d’excitation sont largement discutées par Hoyle et al.20 Nous nous
limiterons au procédé d'excitation par clivage homolytique d’un photoiniateur comme le 2,2-diméthoxy-2-phénylacetophénone (DMPA) qui est l’un des plus efficaces car le rendement quantique pour la production de radicaux réactifs est plus élevé.20 Par
irradiation avec une lampe à rayons ultraviolets (UV) de longueur d’onde 365 nm, le DMPA se clive facilement en générant deux radicaux A (radical benzoyle) et B (radical (diméthoxyméthyl) benzène) (Schéma 1.6). Le radicale B se réarrange pour former un radical méthyle et le benzoate de méthyle.20,26 Les radicaux A et méthyle
ont une affinité très grande pour l’hydrogène et donc peuvent facilement arracher un hydrogène d’un thiol donnant naissance à un radicale thiyle très réactif.27 Le radical
thiyle formé réagit ensuite avec la double liaison dans une configuration anti-Markovnikov pour donner un thiolalkyle radical. Ce dernier capte un hydrogène d’un thiol conduisant ainsi à la formation d’un thioéther et d'un nouveau radical thiyle qui peut réagir de nouveau avec une double liaison (Schéma 1.7).18,25,27
7
Schéma 1.6 : Mécanisme radicalaire du DMPA26
Schéma 1.7 : Mécanisme de la réaction thiol-ène clic18,25,27
1.3 Domaine d’application des PES
Les polyéthersulfones (PES) et polyétheréthersulfones (PEES), avec un éther de plus
(Tableau 1.1), sont des polymères qui suscitent un grand intérêt dans la fabrication de
dispositifs de haute technologie non seulement du fait de leur haute performance thermique, chimique et radiative6,28,29 mais également de la possibilité pour le
8
adapter à des besoins particuliers. Les dispositifs constitués par ces matériaux ont un excellent comportement mécanique face aux températures élevées, ils sont également très résistants aux chocs, au feu et à l’hydrolyse.30-32 La principale application de ces
polymères réside dans la fabrication de membranes pour la filtration. Les polyéthersulfones sont d’excellents candidats pour la fabrication de membranes pour la microfiltration ou l’ultrafiltration car :33,34
- ils permettent d’avoir une grande sélectivité de la membrane (taux de rejet élevé) et une bonne distribution de la taille des pores ;
- ils sont très résistants à l’oxydation par les désinfectants tels que les peroxydes ou l'hypochlorite souvent nécessaires pour le nettoyage des membranes après utilisation ;
- ils présentent un excellent comportement thermique, résistant jusqu’à 400 °C, avec des températures de transition vitreuse qui atteignent les 200 °C4 due à la rigidité
intrinsèque de la chaîne (présence de noyaux aromatiques)3,4,35 et peuvent être
utilisés sur un large domaine de pH ;
- ils possèdent des propriétés mécaniques intéressantes qui permettent de résister aux gradients de pression utilisés comme force motrice de transfert lors des opérations de filtration.
Les premières membranes à base de PES ont été obtenues avec le polysulfone (PSF) au cours des années 1960 pour une alternative aux membranes cellulosiques dans des procédés de séparation, en raison de leur résistance très élevée dans des conditions extrêmes de pH et une bonne stabilité thermique.36 De nos jours, les applications
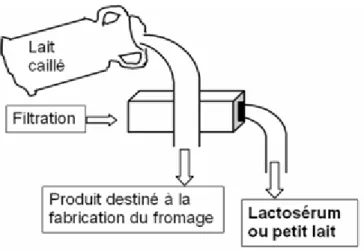
existantes se situent principalement dans la fabrication de membranes pour des filtres de seringue utilisés pour la filtration de solutions à l’échelle du laboratoire ou bien pour des applications dans le domaine industriel pour des membranes à fibres creuses. Dans l’industrie laitière, par exemple, ces membranes ont permis de valoriser le coproduit majeur dans la fabrication du fromage, le lactosérum communément appelé petit lait (Figure 1.1). Le lactosérum a été considéré pendant longtemps comme
9
déchet dans l’industrie fromagère, mais aujourd’hui, grâce à ces membranes, il est possible de le fractionner en plusieurs constituants individuels de haute qualité nutritive (concentrés de protéines, isolats de protéines, …).
Figure 1.1 : Filtration du lait caillé pour la production du fromage
(adapté à partir de la page web du Comité de défense du véritable camembert, http://veritable.camembert.free.fr/pages/Lait_traitements.htm, consultée le 17 janvier 2016)
On se sert également de ces membranes de PES pour la production industrielle d’eau potable, à travers un procédé sûr, efficace et rapide pour l'élimination des particules, de la turbidité et des micro-organismes présents dans l'eau.
Les deux niveaux de filtration membranaire les plus utilisés pour les PES sont la microfiltration et l’ultrafiltration.1,37,38
La microfiltration, pour laquelle la taille des pores de la membrane est de l’ordre du micromètre et se situant généralement entre 0,1 à 10 μm, permet d’éliminer les matières en suspension et de faire l’épuration bactérienne.
L’ultrafiltration, avec une taille des pores de la membrane variant de 1 à 100 nm, en plus de l’épuration bactérienne, permet d’éliminer les virus.
10
D’autre part, il est possible de moduler les propriétés de ces polymères pour les adapter à une application bien définie en greffant certains groupements sur la chaîne polymère.7,14 Les polyéthersulfones dont des groupements sulfones sont rajoutés sur
les cycles aromatiques sont utilisés comme membranes échangeuses d’ions dans les piles à combustible pour des applications dans le domaine du transport (véhicules, camions, autobus et locomotives) et l'électronique.39,40
Du fait de la résistance de ces matériaux à l’eau et à la vapeur, ils sont utilisés pour fabriquer des ustensiles de cuisson et du matériel médical (nébuliseurs et composants de dialyse).1 Ils ont aussi des applications dans le domaine nucléaire, des
télécommunications, des pièces automobiles ou aérospatiales pour l’isolation de câbles.14
1.3.1 Filtration membranaire
Une membrane de filtration est un matériau à perméabilité sélective qui permet de séparer des particules en solution en fonction de leur taille sous l'action d'une force motrice, le but étant de purifier un liquide ou de fractionner ou concentrer des particules. Les particules retenues au niveau de la surface de la membrane forment le rétentat tandis que celles qui la traversent représentent le perméat (Figure 1.2).
11
Il existe deux modes de filtration, les filtrations frontale et tangentielle, que l’on différencie selon l’orientation du flux d’alimentation.
En mode frontal (filtration la plus connue), le flux d’alimentation est perpendiculaire à la membrane alors que dans le cas d’une filtration tangentielle, le flux arrive parallèlement à la membrane. La tangentielle permet un colmatage moins rapide, mais elle est généralement réservée à la filtration de très petites particules.
La majorité des membranes polymères poreuses commercialisées sont élaborées via un procédé de séparation de phases. La séparation de phases (également appelée inversion de phase ou démixtion) résulte d'un changement d'état thermodynamique d'une solution de polymère initialement homogène. Le changement d'état thermodynamique peut être induit par différentes méthodes :42
- variation de la température ;
- intrusion d'un non-solvant dans une solution binaire polymère/solvant.
Tous les processus de séparation de phases sont basés sur les mêmes principes thermodynamiques. Dans tous les cas, le point de départ est une solution thermodynamiquement stable soumise ensuite à des conditions entraînant une démixtion telle qu'un abaissement de température ou l'intrusion d'un non-solvant. L'inversion de phase induit la création de deux phases : une phase pauvre et une phase riche en polymère qui croissent suivant des mécanismes de nucléation-croissance pour former l'architecture membranaire.42 Après démixtion liquide-liquide,
la phase riche en polymère se solidifie et constitue alors la matrice membranaire. La phase pauvre est éliminée par des lavages successifs et laisse place aux pores de la membrane.
1.4 Problématique
Les polyéthersulfones sont utilisés dans plusieurs domaines, cependant l’obtention de voies de synthèse permettant un meilleur contrôle de leur masse moléculaire, leur morphologie et leurs propriétés thermiques reste toujours un défi pour les chercheurs.
12
La polycondensation par substitution nucléophile aromatique est la principale méthode utilisée pour la synthèse des PES. Cette polycondensation est effectuée en système ouvert en déplaçant l'équilibre de la réaction par élimination de la petite molécule formée lors de la réaction. Cette élimination devient de plus en plus difficile au fur et à mesure que la réaction avance du fait de la vitesse de diffusion de ces petites molécules, ce qui rend peu probable les possibilités de contrôle de la masse molaire. Ce type de polymérisation ne permet pas, non plus, de contrôler la morphologie et les propriétés thermiques. Le contrôle de ces paramètres pourrait jouer un rôle déterminant dans l’amélioration des propriétés pour des applications déjà existantes, mais pourrait aussi permettre de répondre à des besoins additionnels, notamment la modulation des propriétés séparatrices des membranes.
La principale application des PES se situe dans la fabrication de membranes, cependant leur utilisation comme membranes est souvent limitée par leur caractère hydrophobe qui, par l’adsorption de particules au niveau de la surface, entraîne un encrassement de la membrane conduisant ainsi au colmatage.28,43 Le colmatage
résulte de l’accumulation des substances filtrées au niveau de la surface de la membrane ou à l’intérieur des pores et, entraîne une perte des performances des membranes. Les causes du colmatage des membranes à base de PES peuvent provenir de trois origines principales :44
- Le colmatage par adsorption : Il provient de la fixation de particules au niveau de la surface de la membrane et résulte en général des interactions entre les molécules notamment les protéines que contiennent les liquides filtrés et les surfaces hydrophobes de la membrane. Le degré d'adsorption dépend du type d'interaction tel que les liaisons hydrogène, les interactions dipolaires, les interactions de van der Waals, et les effets électrostatiques.45 Cependant, il a été
rapporté que les interactions hydrophobes sont le principal facteur renforçant l'adsorption des protéines sur la surface des membranes à base de polyéthersulfone.46 Quand une molécule de protéine est en contact avec la surface
d’une membrane hydrophobe, les molécules d'eau liées à la protéine vont se déplacer du fait des interactions hydrophobes. Ceci provoque une rupture de la
13
liaison entre la protéine et les molécules d’eau, induisant des changements de conformation dans la structure de la protéine, ce qui se traduit par une adsorption irréversible de la protéine sur la surface de la membrane.47,48
- La capture de particules : Elle intervient lors de la filtration uniquement et se caractérise par le blocage de particules dans les pores de la membrane par effet stérique sous l’effet de la force motrice.49
- La création de biofilms : Elle intervient lorsque des bactéries se développent à la surface de la membrane sous l’effet de conditions favorables à leur développement (température notamment), et en particulier dans les zones de faibles convections. Les bactéries sécrètent des exopolymères qui forment un film peu perméable recouvrant la surface de la membrane.
Des observations réalisées par le groupe de Qilin Li50 au microscope électronique à
balayage (MEB) ont permis de mettre en évidence la présence d’un agrégat de particules à la surface de la membrane après ajout de particules organiques dans les solutions filtrées (Figure 1.3). Ce dépôt de matières organiques, adhérant au matériau membranaire, induit des chutes importantes du flux de perméation et, en raison de leur croissance, il est difficile de les éliminer par la suite. Un rétrolavage à l’eau seulement n’est plus suffisante pour retrouver la perméabilité optimale de la membrane. Un nettoyage chimique est donc nécessaire. Par exemple, la soude caustique associée à de l’hypochlorite de sodium (NaClO/NaOH) permet de solubiliser la matière organique composée de groupement phénol ou carboxyle et dégrader les polysaccharides et protéines en sucres et composés aminés plus petits.51,52 Les lavages acides permettent d’éliminer des espèces cationiques.53
L’impact des lavages chimiques sur l’intégrité membranaire est encore peu étudié, cependant il a été montré qu’à long terme ces lavages chimiques peuvent entraîner une modification du matériau membranaire et aggraver le colmatage.54
14
Figure 1.3 : Images MEB en coupe plane (a) et transversale (b) d’une membrane
colmatée (agrégat de particules encerclé en vert) 50
Pour réduire cet effet, il est rapporté dans la littérature qu’il faudrait augmenter l’hydrophilicité de ces polymères pour améliorer les propriétés anti-adsorbantes des membranes, ce qui limitera considérable le colmatage et ainsi maintenir les performances de la membrane.48,55,56
Il est également rapporté que les membranes hydrophiles sont plus faciles à nettoyer que les membranes hydrophobes car l’adsorption devient faible et donc facile à enlever.
Une des stratégies visant à améliorer l'hydrophilicité de ces polymères est de les mélanger avec d’autres polymères hydrophiles comme les polyéthylènes glycols (PEG), mais cette méthode a des limites car à un certain rapport massique, la solution de polymère devient hétérogène conduisant à la séparation de phases lors de la fabrication de la membrane. Le groupe de Mohammadi57 a montré qu’en mélangeant
le PES avec le polyacrylonitrile (PAN) dans un rapport massique de 70/30, il apparaît deux couches au niveau de la membrane vue au microscope électronique à balayage (MEB) due à la séparation de phase lors de sa fabrication (Figure 1.4). Cette séparation modifie considérablement la structure de la membrane, comparée à celle du PES.
Coupe plane Coupe transversale
15
Figure 1.4 : Images MEB d’une coupe transversale d’une membrane de PES seul (a)
et d’un mélange PES/PAN dans un rapport massique 70/30 (d), telles que publiées par Amirilargani et al.57
Pour les piles à combustible, le rajout des groupements sulfones sur les noyaux aromatiques pose souvent un problème de stabilité. Zhang et al.40 ont rapporté qu’il
est généralement considéré que les polymères avec des groupes acides sulfoniques pendants ou des chaînes latérales sont plus stables à l'hydrolyse que ceux avec des groupes acides sulfoniques directement connectés sur le squelette des polymères.
I.5 Objectif du projet
Dans cette présente étude, notre objectif est de synthétiser les PES avec incorporation de segments flexibles comportant des doubles liaisons dans les chaînes du polymère pour contrôler :
- la cristallinité ;
- les températures de transition vitreuse ; - l’hydrophilicité des copolymères obtenus.
La modulation de la cristallinité est effectuée en introduisant, au sein de la chaîne, un groupement allyl flexible, de configuration cis ou de configuration trans. Ces segments flexibles pourraient provoquer un repliement de chaînes à l’image des travaux du groupe de Josée Brisson58 sur des copolymères rigides flexibles de Kevlar
où il est indiqué que la présence d’une chaîne flexible permet le repliement des chaînes de polymères rigides, mais pourraient aussi, si le bloc rigide est de taille assez faible, être incorporés au sein de l’unité de répétition et de la maille cristalline. Le
16
changement de configuration permettra alors d’obtenir une chaîne de symétrie et de conformation différentes, ce qui devrait provoquer le changement de cristallinité désiré.
Les températures de transition vitreuse sont contrôlées par la modulation du pourcentage de segment flexible incorporé dans les chaînes du polymère.
Les doubles liaisons incorporées sont utilisées pour une post-fonctionnalisation, permettant de contrôler l’hydrophilicité enfin d’adapter les propriétés des copolymères à des applications bien définies. Par exemple, pour lever les contraintes d’application des PES (leur caractère hydrophobe) dans les membranes de filtration, leur hydrophilicité est modulée en fonctionnalisant les copolymères obtenus à travers les doubles liaisons incorporées par le greffage de différentes molécules hydrophiles. L’ajout des segments flexibles permettra éventuellement d’améliorer la solubilité de ces matériaux et de faciliter leur mise en œuvre.59 Cependant, leur ajout provoque une
baisse des températures de transition vitreuse.59 C’est pourquoi la séquence, la taille
et la proportion de ces segments flexibles doivent être ajustées afin de minimiser leurs effets sur les propriétés thermiques des matériaux résultants.
Pour l’introduction des segments flexibles dans les chaînes du polymère, une méthodologie appropriée doit être utilisée pour arriver à l’objectif fixé. Deux approches différentes sont donc utilisées dans ce projet : la polymérisation par
métathèse des diènes acycliques (ADMET en anglais, Acyclic Diene Metathesis
Polymerization) et la polycondensation classique.
La polymérisation par métathèse des diènes acycliques (ADMET) permet d’obtenir des polymères de faibles polydispersités avec des doubles liaisons régulièrement réparties le long des chaînes du polymère.
La polycondensation, elle, permet d’obtenir directement des copolymères de configuration cis ou trans avec incorporation régulière ou aléatoire des doubles liaisons.
17
1.6 Méthodologie
1.6.1 Polymérisation par métathèse des diènes acycliques (ADMET)
Dans la science des matériaux, la métathèse des oléfines permet, entre autres, de faire des réactions de polymérisation par métathèse de diènes acycliques plus connues sous le nom de ADMET (en anglais : Acyclic Diene Metathesis Polymerization).60 Cesréactions de polymérisation sont rendues possibles par l’usage d’un certain type de catalyseurs carbéniques qui peuvent différer par la nature du métal central (titane, molybdène, tungstène, ruthénium).61 Cependant, un choix approprié du catalyseur est
important pour éviter les réactions secondaires indésirables qui peuvent avoir lieu entre le catalyseur et les groupements fonctionnels du milieu réactionnel. Ces derniers peuvent se lier avec le centre actif du métal et ainsi désactiver complètement le catalyseur.62 Le succès de la polymérisation par métathèse des oléfines repose donc
sur l’usage de catalyseurs qui réagissent préférentiellement avec des oléfines en présence de groupements fonctionnels hétéroatomiques.
Une étude permettant de suivre la réactivité des catalyseurs à base de titane, tungstène, molybdène et ruthénium vis-à-vis des oléfines en présence d’autres groupements fonctionnels a montré que ceux formés de ruthénium sont beaucoup plus sélectifs aux oléfines qu’aux autres groupements fonctionnels présents dans le milieu réactionnel.62
18
Tableau 1.2: Réactivité des catalyseurs à base de titane, tungstène, molybdène et
ruthénium vis-à-vis des oléfines en présence de groupements fonctionnels hétéroatomiques62
Titane Tungstène Molybdène Ruthénium
Acides Acides Acides Oléfines
Ordre de réactivité
des oléfines
Alcools, Eau Alcools, Eau Alcools, Eau Acides Aldéhydes Aldéhydes Aldéhydes Alcools, Eau
Cétones Cétones Oléfines Aldéhydes
Esters, Amides Oléfines Cétones Cétones
Oléfines Esters, Amides Esters, Amides Esters, Amides
De cette étude, dont les résultats sont résumés dans le Tableau 1.2, on conclut que les catalyseurs au titane, tungstène et molybdène sont plus disposés à réagir avec les groupements acides, alcools, eau, et aldéhydes qu’avec les oléfines alors que ceux à base de ruthénium sont plus sélectifs aux alcènes.
Hormis le choix du catalyseur, le choix d’un bon solvant s’impose pour cette polymérisation. Schulz et al.63 ont indiqué que la réussite de cette polymérisation
dépend de la capacité du solvant à : - initier le catalyseur ;
- augmenter la réactivité des espèces actives du catalyseur et du substrat ; - maintenir l’activité du catalyseur pour un temps plus ou moins long.
Ce groupe a effectué la polymérisation par métathèse des diènes acycliques dans différents solvants (Figure 1.5) en utilisant les catalyseurs de Grubbs deuxième génération et Hoveyda – Grubbs. L’étude a révélé que les réactions effectuées dans le dichlorométhane présentaient les masses molaires les plus élevées.
19
Figure 1.5 : Comparaison des masses molaires obtenues par ADMET avec les
catalyseurs de Grubbs deuxième génération et Hoveyda – Grubbs dans différents solvants63
Dans le cadre du présent projet, deux types de catalyseurs à base de ruthénium ont été utilisés : le Grubbs deuxième génération (G2) et le Hoveyda-Grubbs (HG) (Schéma
1.8). Ces catalyseurs sont, non seulement plus tolérants aux groupes fonctionnels
présents dans le milieu réactionnel, mais aussi plus actifs et plus stables en présence d’air et d’humidité.62,64-67 Le dichlorométhane a été sélectionné comme solvant.