HAL Id: dumas-01260202
https://dumas.ccsd.cnrs.fr/dumas-01260202
Submitted on 21 Jan 2016HAL is a multi-disciplinary open access
archive for the deposit and dissemination of sci-entific research documents, whether they are pub-lished or not. The documents may come from teaching and research institutions in France or abroad, or from public or private research centers.
L’archive ouverte pluridisciplinaire HAL, est destinée au dépôt et à la diffusion de documents scientifiques de niveau recherche, publiés ou non, émanant des établissements d’enseignement et de recherche français ou étrangers, des laboratoires publics ou privés.
maladie chez des patients avec PCR positive à
Pneumocystis jirovecii : une étude prospective
monocentrique
Thomas Fauchier
To cite this version:
Thomas Fauchier. Évaluation diagnostique et intérêt en pratique clinique de la PCR temps réel pour différencier colonisation et maladie chez des patients avec PCR positive à Pneumocystis jirovecii : une étude prospective monocentrique. Médecine humaine et pathologie. 2014. �dumas-01260202�
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 1
UNIVERSITÉ DE NICE-SOPHIA ANTIPOLIS
FACULTÉ DE MÉDECINE
____ Année 2014 N°
THESE
Présentée et soutenue publiquement : Le 13 octobre 2014
Par
Thomas FAUCHIER
Né le 07 octobre 1983 à Ollioules
Pour l'obtention du diplôme d'état de Docteur en médecine
Evaluation diagnostique et intérêt en pratique clinique de la
PCR temps réel pour différencier colonisation et maladie
chez des patients avec PCR positive à Pneumocystis jirovecii:
une étude prospective monocentrique.
Jury de thèse :
Président : Professeur Pierre MARTY Assesseurs :
Professeur Christian PRADIER Professeur Pierre Simon ROHRLICH Directeur de thèse : Docteur Christelle POMARES
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 3
UNIVERSITÉ DE NICE-SOPHIA ANTIPOLIS
FACULTÉ DE MÉDECINE
_________
Liste des professeurs au 1er novembre 2013 à la Faculté de Médecine de Nice
Doyen M. BAQUÉ Patrick
Assesseurs M. CARLES Michel
Mme BREUIL Véronique M. ESNAULT Vincent M. MARTY Pierre
Conservateur de la bibliothèque M. SCALABRE Grégory
Chef des services administratifs Mme CALLEA Isabelle
Doyens Honoraires M. AYRAUD Noël M. RAMPAL Patrick M. BENCHIMOL Daniel Professeurs Honoraires M. BALAS Daniel M. BLAIVE Bruno M. BOQUET Patrice M. BOURGEON André M. BOUTTÉ Patrick M. BRUNETON Jean-Noël Mme BUSSIERE Françoise M. CHATEL Marcel M. COUSSEMENT Alain M. DARCOURT Guy M. DELMONT Jean M. DEMARD François M. DOLISI Claude M. FREYCHET Pierre M. GÉRARD Jean-Pierre M. GILLET Jean-Yves M. GRELLIER Patrick M. HARTER Michel M. INGLESAKIS Jean-André M. LALANNE Claude-Michel M. LAMBERT Jean-Claude M. LAPALUS Philippe M. LAZDUNSKI Michel M. LEFEBVRE Jean-Claude M. LE BAS Pierre M. LE FICHOUX Yves M. LOUBIERE Robert M. MARIANI Roger M. MASSEYEFF René M. MATTEI Mathieu M. MOUIEL Jean Mme MYQUEL Martine M. OLLIER Amédée M. ORTONNE Jean-Paul M. SCHNEIDER Maurice M. TOUBOL Jacques
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 4 M. ZIEGLER Gérard
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 5
M.C.A. Honoraire Mlle ALLINE Madeleine
M.C.U. Honoraires M. ARNOLD Jacques M. BASTERIS Bernard
Mlle CHICHMANIAN Rose-Marie M. EMILIOZZI Roméo
M. GASTAUD Marcel M.GIRARD-PIPAU Fernand M. GIUDICELLI Jean M. MAGNÉ Jacques Mme MEMRAN Nadine M. MENGUAL Raymond M. POIRÉE Jean-Claude Mme ROURE Marie-Claire
PROFESSEURS CLASSE EXCEPTIONNELLE
M. AMIEL Jean Urologie (52.04)
M. BENCHIMOL Daniel Chirurgie Générale (53.02) M. CAMOUS Jean-Pierre Thérapeutique (48.04)
M. DARCOURT Jacques Biophysique et Médecine Nucléaire (43.01) M. DELLAMONICA Pierre Maladies Infectieuses ; Maladies Tropicales (45.03) M. DESNUELLE Claude Biologie Cellulaire (44.03)
Mme EULLER-ZIEGLER Liana Rhumatologie (50.01)
M. FENICHEL Patrick Biologie du Développement et de la Reproduction (54.05)
M. FRANCO Alain Gériatrie et Biologie du vieillissement (53.01) M. FUZIBET Jean-Gabriel Médecine Interne (53.01)
M. GASTAUD Pierre Ophtalmologie (55.02) M. GILSON Éric Biologie Cellulaire (44.03)
M. GRIMAUD Dominique Anesthésiologie et Réanimation Chirurgicale (48.01) M. HASSEN KHODJA Reda Chirurgie Vasculaire (51.04)
M. HÉBUTERNE Xavier Nutrition (44.04)
M. HOFMAN Paul Anatomie et Cytologie Pathologiques (42.03) M. LACOUR Jean-Philippe Dermato-Vénéréologie (50.03)
Mme LEBRETON Élisabeth Chirurgie Plastique, Reconstructrice et Esthétique (50.04)
M. MICHIELS Jean-François Anatomie et Cytologie Pathologiques (42.03) M. PRINGUEY Dominique Psychiatrie d'Adultes (49.03)
M. QUATREHOMME Gérald Médecine Légale et Droit de la Santé (46.03) M. SANTINI Joseph O.R.L. (55.01)
M. THYSS Antoine Cancérologie, Radiothérapie (47.02) M. VAN OBBERGHEN Emmanuel Biochimie et Biologie Moléculaire (44.01)
PROFESSEURS PREMIERE CLASSE
M. BATT Michel Chirurgie Vasculaire (51.04) M. BÉRARD Étienne Pédiatrie (54.01)
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 6 M. BERNARDIN Gilles Réanimation Médicale (48.02)
M. BOILEAU Pascal Chirurgie Orthopédique et Traumatologique (50.02) M. BONGAIN André Gynécologie-Obstétrique (54.03)
Mme CRENESSE Dominique Physiologie (44.02)
M. DE PERETTI Fernand Anatomie-Chirurgie Orthopédique (42.01) M. DRICI Milou-Daniel Pharmacologie Clinique (48.03)
M. ESNAULT Vincent Néphrologie (52-03) M. FERRARI Émile Cardiologie (51.02) M. GIBELIN Pierre Cardiologie (51.02)
M. GUGENHEIM Jean Chirurgie Digestive (52.02)
Mme ICHAI Carole Anesthésiologie et Réanimation Chirurgicale (48.01) M. LONJON Michel Neurochirurgie (49.02)
M. MARQUETTE Charles-Hugo Pneumologie (51.01)
M. MARTY Pierre Parasitologie et Mycologie (45.02) M. MOUNIER Nicolas Cancérologie, Radiothérapie (47.02)
M. MOUROUX Jérôme Chirurgie Thoracique et Cardiovasculaire (51.03) M. PADOVANI Bernard Radiologie et Imagerie Médicale (43.02)
M. PAQUIS Philippe Neurochirurgie (49.02) Mme PAQUIS Véronique Génétique (47.04)
M. RAUCOULES-AIMÉ Marc Anesthésie et Réanimation Chirurgicale (48.01) Mme RAYNAUD Dominique Hématologie (47.01)
M. ROBERT Philippe Psychiatrie d’Adultes (49.03) M. ROSENTHAL Éric Médecine Interne (53.01) M. SCHNEIDER Stéphane Nutrition (44.04)
M. TRAN Albert Hépato Gastro-entérologie (52.01)
PROFESSEURS DEUXIEME CLASSE
M. ALBERTINI Marc Pédiatrie (54.01) Mme ASKENAZY-GITTARD Florence Pédopsychiatrie (49.04) M. BAHADORAN Philippe Cytologie et Histologie (42.02)
M. BAQUÉ Patrick Anatomie - Chirurgie Générale (42.01) M. BARRANGER Emmanuel Gynécologie Obstétrique (54.03) M. BENIZRI Emmanuel Chirurgie Générale (53.02) Mme BLANC-PEDEUTOUR Florence Cancérologie – Génétique (47.02) M. BREAUD Jean Chirurgie Infantile (54-02) Mlle BREUIL Véronique Rhumatologie (50.01) M. CANIVET Bertrand Médecine Interne (53.01)
M. CARLES Michel Anesthésiologie Réanimation (48.01) M. CASSUTO Jill-Patrice Hématologie et Transfusion (47.01) M. CASTILLO Laurent O.R.L. (55.01)
M. CHEVALLIER Patrick Radiologie et Imagerie Médicale (43.02) M. DUMONTIER Christian Chirurgie plastique
M. FERRERO Jean-Marc Cancérologie ; Radiothérapie (47.02) M. FOURNIER Jean-Paul Thérapeutique (48-04)
M. FREDENRICH Alexandre Endocrinologie, Diabète et Maladies métaboliques (54.04)
Mlle GIORDANENGO Valérie Bactériologie-Virologie (45.01) M. GUÉRIN Olivier Gériatrie (48.04)
M. HANNOUN-LEVI Jean-Michel Cancérologie ; Radiothérapie (47.02) M. IANNELLI Antonio Chirurgie Digestive (52.02)
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 7 M. JOURDAN Jacques Chirurgie Thoracique et Cardiovasculaire (51.03) M. LEVRAUT Jacques Anesthésiologie et Réanimation Chirurgicale (48.01) M. PASSERON Thierry Dermato-Vénéréologie (50-03)
M. PICHE Thierry Gastro-entérologie (52.01)
M. PRADIER Christian Épidémiologie, Économie de la Santé et Prévention (46.01)
M. ROGER Pierre-Marie Maladies Infectieuses ; Maladies Tropicales (45.03) M. ROHRLICH Pierre Pédiatrie (54.01)
M. RUIMY Raymond Bactériologie-virologie (45.01)
M. SADOUL Jean-Louis Endocrinologie, Diabète et Maladies Métaboliques (54.04)
M. STACCINI Pascal Biostatistiques et Informatique Médicale (46.04) M. THOMAS Pierre Neurologie (49.01)
M. TROJANI Christophe Chirurgie Orthopédique et Traumatologique (50.02) M. VENISSAC Nicolas Chirurgie Thoracique et Cardiovasculaire (51.03) PROFESSEUR DES UNIVERSITÉS
M. SAUTRON Jean-Baptiste Médecine Générale
MAITRES DE CONFÉRENCES DES UNIVERSITÉS - PRATICIENS HOSPITALIERS
Mme ALUNNI-PERRET Véronique Médecine Légale et Droit de la Santé (46.03) M. AMBROSETTI Damien Cytologie et Histologie (42.02)
Mme BANNWARTH Sylvie Génétique (47.04)
M. BENOLIEL José Biophysique et Médecine Nucléaire (43.01) Mme BERNARD-POMIER Ghislaine Immunologie (47.03)
Mme BUREL-VANDENBOS Fanny Anatomie et Cytologie pathologiques (42.03) M. DELOTTE Jérôme Gynécologie-Obstétrique (54.03)
M. DOGLIO Alain Bactériologie-Virologie (45.01)
Mme DONZEAU Michèle Biologie du Développement et de la Reproduction (54.05)
M. FOSSE Thierry Bactériologie-Virologie-Hygiène (45.01) M. FRANKEN Philippe Biophysique et Médecine Nucléaire (43.01) M. GARRAFFO Rodolphe Pharmacologie Fondamentale (48.03) Mme HINAULT Charlotte Biochimie et biologie moléculaire (44.01) Mlle LANDRAUD Luce Bactériologie–Virologie (45.01)
Mme LEGROS Laurence Hématologie et Transfusion (47.01) Mme MAGNIÉ Marie-Noëlle Physiologie (44.02)
Mme MUSSO-LASSALLE Sandra Anatomie et Cytologie pathologiques (42.03) M. NAÏMI Mourad Biochimie et Biologie moléculaire (44.01) M. PHILIP Patrick Cytologie et Histologie (42.02)
Mme POMARES Christelle Parasitologie et mycologie (45.02)
Mlle PULCINI Céline Maladies Infectieuses ; Maladies Tropicales (45.03) M. ROUX Christian Rhumatologie (50.01)
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 8 M. TESTA Jean Épidémiologie Économie de la Santé et Prévention (46.01)
M. TOULON Pierre Hématologie et Transfusion (47.01) PROFESSEURS ASSOCIÉS
M. DIOMANDE Mohenou Isidore Anatomie et Cytologie Pathologiques M. HOFLIGER Philippe Médecine Générale
M. MAKRIS Démosthènes Pneumologie
M. PITTET Jean-François Anesthésiologie et Réanimation Chirurgicale Mme POURRAT Isabelle Médecine Générale
MAITRES DE CONFÉRENCES ASSOCIÉS
Mme CHATTI Kaouthar Biophysique et Médecine Nucléaire M. GARDON Gilles Médecine Générale
Mme MONNIER Brigitte Médecine Générale M. PAPA Michel Médecine Générale
PROFESSEURS CONVENTIONNÉS DE L’UNIVERSITÉ
M. BERTRAND François Médecine Interne
M. BROCKER Patrice Médecine Interne Option Gériatrie M. CHEVALLIER Daniel Urologie
Mme FOURNIER-MEHOUAS Manuella Médecine Physique et Réadaptation M. QUARANTA Jean-François Santé Publique
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 9
Remerciements :
A Monsieur le Professeur Marty,
Vous me faites l’honneur de présider le jury de cette thèse. Je vous remercie d'avoir accepté de juger mon travail.
Je vous remercie de m’avoir accepté dans votre stage en tant que hors-filière, d’avoir cru en un interne de santé publique, de m’avoir fait confiance pour mener à bien cette étude, et, dans une certaine mesure, de veiller à la transversalité des disciplines médicales. La santé publique doit être une discipline qui, par sa rigueur et sa méthode, doit aider les autres spécialités à effectuer des travaux scientifiques dans le but de faire avancer la recherche et la médecine.
Je vous remercie de contribuer à l’épanouissement intellectuel des internes de toute spécialité.
Sachez que je garde un excellent souvenir de mon passage dans votre service, si bien que je passe ma thèse avec vous !
Recevez ma plus grande considération. A Monsieur le Professeur Pradier,
Vous me faites l’honneur de votre participation au jury de cette thèse.
Je vous remercie d’évaluer la qualité de ce travail, en tant que professeur de Santé Publique.
Soyez assuré de ma profonde gratitude. A Monsieur le Professeur Rohrlich,
Vous me faites un grand honneur en siégeant dans ce jury.
Je vous remercie d'avoir accepté si spontanément de juger mon travail de thèse. Soyez assuré de ma sincère reconnaissance et de mon profond respect.
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 10
A Madame le Docteur Pomares,
Tu me fais l’honneur d’avoir été ma directrice de thèse.
Je te remercie de l’accueil que tu m’as fait dans votre service, il y a 3 ans de cela… Cela passe si vite !
Je te remercie d’avoir cru en moi et de m’avoir confié ce travail qui m’a suivi jusqu’au bout du monde, dans un lagon paradisiaque, et qui a continué sous la grisaille de Paris après une escale à Nice, pour aujourd’hui se présenter en tant que thèse de médecine. Merci pour tous tes conseils, pour nos heures de discussions téléphoniques et de réécriture !
Reçois ma plus grande considération. A Madame le Docteur Hasseine
Merci de m’avoir soutenu, de m’avoir expliqué les différentes techniques de mycologie (pas très évidentes !).
Sois assurée de ma sincère gratitude.
A Virginie, sans qui l’ébauche de cette thèse n’aurait pu voir le jour. Merci, un grand merci pour ton aide !!!!!
A mes Professeurs de Santé Publique, Messieurs Pradier, Quaranta et Staccini, pour la qualité de leur enseignement et leur pédagogie.
A Monsieur le Docteur Fosse, à Mesdames les Docteurs Berrouane et Veyres, pour votre gentillesse, votre disponibilité et votre compétence pour m’avoir fait aimer l’hygiène hospitalière … j’espère vous revoir bientôt.
A Madame le Docteur Mirabel, pour avoir cru en moi et m’avoir fait confiance, pour avoir fait la tournée des dispensaires de Nouvelle-Calédonie, et m’avoir aidé dans mon épanouissement personnel et professionnel.
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 11
Aux équipes du laboratoire de parasitologie-mycologie, équipe d’hygiène hospitalière Dr Gari-Toussaint, Dr Delaunay (aaaah… les punaises de lit… j’en ai rêvé !!!), à Mme Cassar, à Mme Degus. Votre gentillesse et votre accueil ont été très importants pour moi dans les services… la preuve par les gâteaux !! (Larmes !).
A l’équipe du DIM (la DIM TEAM), à nos discussions sur la nourriture (surtout après les repas… oui le codage c’était dur en postprandial), Dr Bourdais-Manonne, Dr Gycquel, Mmes Bloquet Rasson….
A l’ASSNC, Weena, Agnès, Claire, Dr Rouchon… aaah, les cocotiers, le lagon (soupir !) A tous mes amis de Nouvelle Calédonie, mes anciens co-internes : mes nièces, papa, maman, papy, mamy, à nos moments inoubliables sur le Caillou !!!
A tous mes co-internes de Santé Publique qui se reconnaitront.
A mes amis Co-internes de Nissa la Bella : Linda (mi- parisienne mi- niçoise), Christine, Caroline (ouais ouais ouais bien bien bien), Géraldine (et nos discussions très intéressantes à l’internat).
Et il n’y a pas que la médecine et les statistiques dans la vie…
A mes amis : Mickael, Lambert, Lilian, Célia, Constance, Canardia (où es-tu ?), Canard Xavier, Morgane, Valérie (le délire plein), Jérôme, Mickey, Poum-Poum.
A ma famille. Merci Papa et Maman de m’avoir soutenu dans ces années difficiles qu’est l’externat. Merci d’avoir cru en moi. Merci de votre amour et de me supporter depuis 30 ans…
A ceux qui n’en sont allés et ne sont plus là aujourd’hui pour me voir… A mes grands-parents, qui me manquent…
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 12
Table des matières
Abréviations ... 14
Introduction ... 15
Pathologie et espèce incriminée : ... 15
Historique : ... 15
Description initiale de la pathologie : ... 15
Pneumocystose chez le patient VIH : ... 16
Pneumocystose chez les non VIH après l’arrivée des trithérapies : ... 16
Découverte de patients ‘colonisés’ par Pneumocystis jirovecii ... 17
La colonisation asymptomatique remise en question : ... 17
Biologie du champignon : ... 17 Habitat : ... 17 Cycle du champignon : ... 18 Techniques diagnostiques : ... 19 Microscopie et coloration : ... 19 Immunofluorescence indirecte et PCR : ... 19 Techniques PCR utilisées : ... 20
Détection des β 1,3-D-glycanes sériques:... 20
Problématiques actuelles : ... 21 Problématique diagnostique : ... 21 Problématique clinique : ... 21 Problématique thérapeutique : ... 22 Objectifs de l’étude : ... 22 Matériel et Méthode ... 23 Type d’étude : ... 23 Critères d’inclusion : ... 23
Provenance des patients : ... 23
Modalité de recueil clinique : ... 24
Les données recueillies :... 24
Méthode de Polymerase Chain Reaction quantitative (qPCR) : ... 28
Définition du cycle seuil (CT) : ... 29
Méthode d’examen direct (microscopie) : ... 29
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 13
Relecture des dossiers : ... 30
Analyses statistiques : ... 30
Résultats. ... 31
Échantillon de l’étude avec l’ensemble des qPCR positives ... 32
Analyse du sous échantillon de patients avec Pneumocystose maladie PJP+ versus colonisation PJP-. ... 37
Les cycles seuils de la qPCR Pneumocystis : un outil pour distinguer Pneumocystose maladie (PJP+) et colonisation (PJP-) ... 46
Discussion ... 58
Critère principal de jugement ... 58
Critères secondaires de jugement : ... 60
Caractéristiques de l’échantillon qPCR+ :... 60
Forces et faiblesses de l’étude : ... 66
Puissance et implications pratiques : ... 67
Conclusion ... 68
Résumé ... 69
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 14
Abréviations
CHU : Centre hospitalier universitaire
CD4 : lymphocyte cluster de différenciation 4 CD8 : lymphocyte cluster de différenciation 8
Courbe ROC : courbes d’analyse de la sensibilité et de la spécificité d’un examen par rapport à un examen de référence.
CT : cycles de seuil
DIM : département d’informatique médical LBA : liquide broncho-alvéolaire
IC : intervalle de confiance IQR : intervalle interquartile
Odd (Côte) : rapport du nombre d’exposés sur le nombre de non exposés. Ex : rapport des PJP+ sur les PJP-.
Odds ratio (OR) : rapport des Odds (rapport des côtes).
Patient PJP- : patient du groupe considéré colonisé ou porteur Patient PJP+ : patient du groupe considéré malade
Patient VIH : patient souffrant du VIH
Patient non VIH : patient ne souffrant pas du VIH PCR : polymerase chain reaction
qPCR : PCR en temps réel
PJP : Pneumocystis jirovecii pneumonia : pneumocystose à Pneumocystis jirovecii SIDA : Syndrome de l’immunodéficience acquise
ROC : Receiver operating characteristic. VIH : virus de l’immunodéficience humain. VPN : valeur prédictive négative.
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 15
Introduction
Pathologie et espèce incriminée :
La pneumocystose (Pneumocystis jirovecii pneumonia ou PJP) est une pathologie respiratoire aiguë potentiellement mortelle en l’absence de traitement. L’agent pathogène incriminé est un champignon dénommé Pneumocystis jirovecii (ex carinii) (1) appartenant au règne des fungi. Cette pathologie touche exclusivement les patients immunodéprimés. Il n’est pas cultivable et son identification reste problématique, par méthode directe ou indirecte (2–5).
Historique :
Description initiale de la pathologie :
Décrit par Antonio Carini dans les poumons de rat en 1910, un an après la découverte du pathogène par Carlos Chagas, la communauté scientifique a baptisé ce pathogène
Pneumocystis carinii. Otto Jirovec a identifié ce micro-organisme dans l’espèce humaine
chez des enfants malnutris souffrant de pneumopathies interstitielles et l’a classé dans le règne des protozoaires(2). Aujourd’hui après l’analyse du génome, Pneumocystis est classé dans le règne des fungi et a été rebaptisé Pneumocystis jirovecii (3-4). Chaque espèce semble hôte-spécifique (5) et était jusqu’à peu de temps décrite uniquement chez les mammifères, notamment le rat (6) mais certaines études semblent contredire cette affirmation. On a ainsi pu détecter Pneumoctystis parmi les volailles et, si le champignon semble spécifique à l’espèce infectée, une étude a montré le passage d’un Pneumocystis humain à la volaille (7). Néanmoins, il n’y a pas eu de preuve de passage de Pneumocystis des animaux à l’Homme(7).
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 16
Pneumocystose chez le patient VIH :
D’épidémies localisées dans des collectivités d’enfants défavorisés dans les années 50 (1, 8), la maladie est devenue endémique avec l’épidémie de SIDA au début des années 80. Cette maladie se présentait alors chez de jeunes gens immunodéprimés par le VIH par une triade fièvre/dyspnée/toux, d’apparition frustre, d’évolution insidieuse et fatale sans traitement en quelques semaines (8). Le risque était particulièrement élevé lorsque le taux de lymphocytes sanguins CD4+ était en dessous de 200 éléments/mm3 (9). La PJP représentait la plus fréquente des maladies opportunistes classant les patients infectés par le VIH en stade SIDA (25 à 30% des cas (10,11)). Une étude a estimé l’incidence d’un premier épisode de PJP à 3,9 cas pour 1000 patients-années chez des patients VIH de 2003 à 2007 (12).
Pneumocystose chez les non VIH après l’arrivée des trithérapies :
Au cours des années 90, l’arrivée des trithérapies et une meilleure prise en charge des personnes séropositives a fait reculer cette pathologie souvent inaugurale de la phase SIDA(13,14), tout en restant la manifestation la plus fréquente (337 PJP sur 1510 cas de SIDA déclarés à l’Institut de veille sanitaire (InVS) soit 25% (15). En revanche, la mise sur le marché de chimiothérapies anti-cancéreuses plus agressives pour les cancers, les hémopathies malignes, les thérapies immunosuppressives pour des pathologies auto-immunes (15), ont fait émerger de nouveaux facteurs de risque de pneumocystose chez des patients historiquement non concernés par cette maladie (16-21). De plus, les syndromes décrits chez ces nouveaux immunodéprimés (patients non VIH) divergent de la pneumocystose habituellement décrite chez les patients VIH (22) avec une apparition brutale des symptômes, des désaturations plus fréquentes et une évolution rapide et fatale en l’absence de traitement (23). Ces symptômes peuvent être causés par une réaction immunitaire plus forte(24). Le nombre absolu de PJP dans la population non VIH n’est pas connu car il n’y a pas de système national de déclaration pour cette population (5), néanmoins des études ont montré une prévalence de 2 à 45% (25).
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 17
Découverte de patients ‘colonisés’ par Pneumocystis jirovecii
Dans les années 2000, de nouvelles techniques diagnostiques ont montré la présence de
Pneumocystis chez des individus immunocompétents(26) et chez des enfants (27,28).
La colonisation asymptomatique remise en question :
L’innocuité du pathogène chez des patients apparemment non immunodéprimés commence à être remis en question, notamment chez les nourrissons et la mort subite inexpliquée (29-31) ou les patients atteints de pathologies pulmonaires chroniques comme la broncho-pneumopathie obstructive (32-34), la sarcoïdose, la mucoviscidose (35,36) ou la dilatation des bronches (26,37). On retrouve même ce pathogène dans la population générale après autopsie (38). Les prévalences de la maladie dans différentes sous-populations commencent à être étudiées (29,39), ainsi certaines études ont montré une prévalence de 27% chez les sujets VIH en Afrique (40) et une étude chilienne a montré une prévalence de 83,5% chez les enfants victimes de mort inexpliquée du nourrisson (29) même si on n’a pu en démontrer la responsabilité (41). Les conséquences individuelles d’une colonisation par Pneumocystis restent mal évaluées par manque d’études suivies des sujets colonisés
Biologie du champignon :
Habitat :
Pneumocystis se développe dans les alvéoles pulmonaires en contact étroit avec les
pneumocytes de type I, d’où son nom, tout en restant extracellulaire (42). Les alvéoles pulmonaires sont les seuls lieux de multiplication connus. L’Homme infecté est son propre réservoir et la principale source de P.jirovecii (43). La transmission interhumaine en milieu hospitalier a été évoqué dans un contexte de cas groupés de PJP (44,45).
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 18
Cycle du champignon :
Le cycle de Pneumocystis jirovecii reste méconnu dans l’alvéole pulmonaire. Il existe des formes trophiques et des formes kystiques. Les kystes matures contiennent huit corps intrakystiques qui donnent des petites formes trophiques après libération et selon un cycle hypothétique. Ces formes trophiques sont très adhérentes entre elles ainsi qu’à la surface des pneumocystes de type I (42). Le schéma 1 présente une hypothèse de cycle. La paroi des prékystes intermédiaires, tardifs et matures, contient des β-1,3-D-glycanes (46).
Schéma 1 : cycle hypothétique de Pneumocystis jirovecii dans l’alvéole pulmonaire. Source :Le Gal S, Damiani C, Totet A, Nevez G. Pneumocystis : diagnostic biologique des infections à Pneumocystis jirovecii. EMC-Biologie médicale 2012 ;0(0) :1-8[Article 90-35-0098-A]
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 19
Techniques diagnostiques :
Microscopie et coloration :
La culture s’avérant impossible (39,47), le diagnostic s’est initialement fait par examen direct après prélèvement pulmonaire distal (examen microscopique après coloration de Giemsa, de Chalvardjian (Bleu de Toluidine O), ou de Gomori Gocrott). Ces différentes colorations présentent des avantages et des inconvénients : Giemsa permet de détecter les formes trophiques et kystiques alors que Chalvardjian ne permet d’observer que les formes kystiques (48) et Gomori Gocrott les formes kystes plus rapidement (49). En revanche, ces colorations très spécifiques permettent de diagnostiquer les pneumocystoses avec une charge fongique très élevée typique des patients VIH.
Immunofluorescence indirecte et PCR :
Au milieu des années 1980 la production d’anticorps monoclonaux spécifiques de
Pneumocystis a permis de développer des techniques d’immunodétection par
immunofluorescence indirecte (42,50,51) mais c’est surtout la polymerase chain reaction (PCR) qui a permis d’augmenter la sensibilité des examens en détectant la présence d’ADN de Pneumocystis jirovecii chez des patients immunocompétents apparemment sains (38,52). En effet, une méta-analyse de dix ans a trouvé une sensibilité de 99,1%, une spécificité de 92,6% sur des LBA (53). Si la PCR a permis l’identification de patients colonisés présentant ou non des symptômes pulmonaires, elle ne distingue pas une simple colonisation d’une véritable maladie (54). Cette méthode qualitative ne présageait pas non plus de la charge fongique allant de pair avec le statut colonisation ou maladie. En effet, plusieurs études démontrent que la charge fongique est corrélée au statut colonisation ou maladie (plus la charge fongique est élevée et plus la probabilité d’infection s’accroît) (55,56). Une nouvelle technique PCR quantitative en temps réel (qPCR) permet grâce à l’amplification au-delà d’une valeur appelée cycle de seuil (CT), valeur proportionnelle à la charge fongique, de quantifier la concentration fongique dans les prélèvements. Plusieurs études ont tenté d’obtenir des seuils de sensibilité et de spécificité en prenant
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 20
comme examen de référence la microscopie et surtout l’immunofluorescence indirecte pour distinguer la colonisation de la maladie en fonction de la charge fongique (56,57).
Techniques PCR utilisées :
x PCR conventionnelle : c’est une PCR qualitative : elle détecte la présence ou l’absence du pathogène recherché dans le prélèvement. Elle ne quantifie pas la concentration de l’agent recherché et ne peut déterminer une charge fongique. x PCR quantitative : real-time PCR ou PCR temps réel : c’est une PCR quantitative :
elle détecte l’absence ou la présence du pathogène recherché dans le prélèvement et amplifie au-delà d’un seuil le produit de la PCR. Ce signal seuil est appelé cycle seuil ou CT (Cycle thresold). Le moment d’apparition de ce cycle de seuil est dépendant de la quantité de matrice initialement présente dans l’échantillon amplifié. Le CT calculé est inversement proportionnel au logarithme décimal (log10) du nombre de copies initiales. Il apparaît toujours au cours de la phase exponentielle de la PCR. Elle permet donc une quantification. Dans la technique de PCR en temps réel, il existe plusieurs variantes utilisant différentes sondes. Dans notre cas, nous utilisons une sonde Taqman (hydrolyse des sondes) Détection des β 1,3-D-glycanes sériques:
La détection des β 1,3-D-glycanes sériques pour le diagnostic des infections fongiques profondes a été développée. Un taux supérieur à 80-100 pg/ml est en faveur d’une infection à Pneumocystis jirovecii si le patient ne présente pas d’autre infection fongique invasive (58,59). Cette méthode de référence reste en seconde intention après microscopie et PCR.
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 21
Problématiques actuelles :
Problématique diagnostique :
Plus la charge fongique est élevée, plus la probabilité d’avoir une PJP s’accroît. Néanmoins, la charge fongique chez les patients immunodéprimés non VIH avec PJP est plus basse que la charge fongique chez les patients VIH avec PJP et pourrait se confondre avec des colonisations (16).
Le diagnostic de colonisation et sa distinction de la maladie lorsqu’il existe une symptomatologie pulmonaire est une problématique pour le clinicien actuel. De plus, l’innocuité de la colonisation pourrait être remise en cause et nécessiter un diagnostic supplémentaire de ‘colonisation par Pneumocystis jirovecii à surveiller’, notamment chez les patients souffrants de pathologies pulmonaires chroniques ou immunodéprimés.
Problématique clinique :
La présentation clinique chez les patients malades présentant la maladie varie en fonction de la pathologie sous-jacente ; ainsi les patients VIH ont une présentation clinique différente des patients non VIH, du fait de la charge fongique et d’une réaction immunitaire plus sévère chez les patients non VIH. Les patients VIH ont une charge fongique plus importante avec une dyspnée progressive, une toux d’apparition insidieuse, une fièvre et une évolution frustre sur plusieurs semaines contrastant avec la présentation de la maladie chez les patients non VIH avec une charge fongique beaucoup plus faible, une dyspnée brutale avec désaturation rapide, une toux d’installation rapide pouvant être accompagnée de forte fièvre (5). De plus, la PJP peut être confondue avec d’autres pathologies respiratoires infectieuses ou inflammatoire comme des pneumopathies virales ou des pneumopathies de sensibilité ou médicamenteuses. Etablir des seuils de détection différents entre patients VIH et non VIH pourraient faciliter le diagnostic et améliorer la prise en charge des patients malades, notamment chez les patients non VIH chez qui la maladie demeure moins connue.
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 22
Problématique thérapeutique :
Alors que les patients VIH (60) et dans certains cas chez les patients non VIH (granulomatose de Wegener ou transplantés rénaux) disposent de recommandations (17,18,61) pour la prévention de la PJP, la prévention chez d’autres patients non VIH reste à définir (16,62,63), notamment chez les patients recevant une immunosuppression par corticoïdes (maladies auto-immunes, chimiothérapies) (64). De plus, plusieurs problèmes sont rencontrés à cause des molécules utilisées : la toxicité des traitements (sulfadiazine-trimethoprime et en second recours : pentadimine , clindamycine-primaquine ou atovaquone (65,66)) et l’émergence de résistance (16) préconisent une diminution des posologies des traitements (67)) ainsi qu’un meilleur diagnostic pour une meilleure prescription des molécules antipneumocystoses (39). Néanmoins, la question de traiter ou non les colonisations est posée car il semble que les colonisations ne soient pas sans risque (8,21,26).
Objectifs de l’étude :
Il y a plusieurs objectifs à différencier dans cette étude, l’objectif principal étant d’obtenir des valeurs de cycles de seuil (CT) pour distinguer la colonisation de la maladie. Nous avons voulu aussi décrire l’échantillon de patients avec qPCR positive et étudier ses caractéristiques. Les trois grands points sont définis ci-après :
-Description de l’échantillon des patients avec qPCR positif à Pneumocystis jirovecii par rapport à la décision clinique (valeur de référence).
-Critère principal : Obtenir des valeurs-seuils de cycles de seuil (CT) de la qPCR avec des sensibilités et spécificités pertinentes pour distinguer colonisation de la maladie chez des patients avec un lavage broncho-alvéolaire (LBA) positif pour Pneumocystis par la technique qPCR.
-Critère secondaire : Obtenir des valeurs-seuils de CT de la qPCR avec des sensibilités et spécificités pertinentes pour des patients suspects de pneumocystose en fonction de leur statut sérologique pour le VIH.
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 23
Matériel et Méthode
Type d’étude :
Il s’agissait d’une étude de cohorte prospective monocentrique non interventionnelle diagnostique en aveugle au Centre Hospitalier Universitaire de Nice (CHU), France. L’étude était en simple aveugle. L’inclusion a commencé au 1er avril 2008 pour se
terminer le 1er octobre 2013. La date de fin d’étude était le 1er janvier 2014, soit trois
mois après la date de fin d’inclusion.
Critères d’inclusion :
Les qPCR Pneumocystis étaient systématiquement réalisées sur tout prélèvement respiratoire (LBA, crachats, expectorations induites).
Nous avons inclus toutes les qPCR positives à Pneumocystis jirovecii.
Pour l’étude de la sensibilité et spécificité de la qPCR, seuls les liquides broncho-alvéolaires (LBA) ont été retenus : en effet, les LBA étaient les prélèvements les plus pertinents pour le diagnostic de PJP, notamment chez les patients VIH (68)
Provenance des patients :
Les patients provenaient des hôpitaux des Alpes-Maritimes et du Var-est, région Provence-Alpes-Côte-D’azur Est (PACA Est) pour laquelle le Centre Hospitalier Universitaire de Nice est au centre du réseau de soin. Les qPCR positives ont concerné les prélèvements des patients des hôpitaux du CHU de Nice (Alpes-Maritimes), le Centre Antoine Lacassagne (Nice, Alpes-Maritimes), le Centre hospitalier d’Antibes (Alpes-Maritimes) et le Centre hospitalier de Fréjus-Saint-Raphaël (Var). Seul le CHU de Nice disposait d’une technique de diagnostic par qPCR dans la région, ce qui fait que le CHU
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 24
de Nice avait l’exhaustivité des cas de colonisation ou de maladie à Pneumocystis de la région.
Modalité de recueil clinique :
L’identité du patient était connue grâce à un numéro d’identification donné par le logiciel de laboratoire GLIMS®. Par la suite, on recueillait les données cliniques, biologiques et radiologiques du patient avec le logiciel CLINICOM (INTERSYSTEM®). L’évolution et la décision clinique ont été recueillies grâces aux comptes rendus disponibles sur CLINICOM et les diagnostiques principaux et secondaires retenus par le département d’informatique médical (DIM).
Les données recueillies :
Une fiche de collecte était réalisée avec comme données recueillies : -le sexe, l’âge de la personne (date de naissance) et la date de prélèvement. -des données cliniques :
*le contexte clinique ayant motivé la recherche de Pneumocystis jirovecii (69) - fièvre
- dyspnée - toux,
- autres symptômes moins spécifiques comme hémoptysie, œdème aigu du poumon, etc.…
* antécédents médicaux à risque de pneumocystose, classées en 6 catégories. - pathologies immunodépressives
- auto-immunes - cancers
- hémopathies malignes, - statut sérologique VIH
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 25
- les autres comorbidités étaient répertoriées dans la catégorie « autre ». *le service demandeur
Les services demandeurs étaient soit des services du CHU, soit des services provenant d’hôpitaux extérieurs au CHU. Du fait de la complexité du prélèvement, le prélèvement respiratoire se faisait dans des services avec plateaux techniques adéquats (service de pneumologie ou de réanimation). Dans le cadre des autres services, les patients étaient transférés en ambulatoire dans les services de pneumologie afin de pratiquer le prélèvement.
Dans la fiche de collecte, le service demandeur restait le service pour lequel l’hospitalisation principale avait été demandée.
Pour plus de commodités, les services demandeurs ont été regroupés et classés dans 6 disciplines : - hématologie/cancérologie - réanimation - pneumologie - médecine interne - infectiologie
- les autres services étaient regroupés dans la catégorie « autre ».
*le traitement au long cours pour rechercher des traitements à risque (thérapies immunosuppressives) ou des traitements préventifs antipneumocystoses.
On considérait traitement au long cours tout traitement curatif, préventif ou prophylactique d’une pathologie chronique. Nous portions plus particulièrement notre attention sur les thérapies immunosuppressives (chimiothérapie, corticothérapie, immunothérapie) de pathologies chroniques (cancers, hémopathies malignes, maladies auto-immunes) ou les traitements antirétroviraux chez les patients VIH.
Il était également noté les mises sous traitement préventif par sulfadiazine-trimethoprime chez les patients immunodéprimés (immunodépression par le VIH, etc.). Nous avons considéré quatre classes thérapeutiques :
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 26
- antirétroviraux
- prévention antipneumocystose -autres traitements au long cours
Les combinaisons de ces associations thérapeutiques (bithérapies) étaient également étudiées.
*la décision clinique de considérer la qPCR positive comme Pneumocystose maladie ou comme simple colonisation à Pneumocystis jirovecii.
* Traitement curatif de l’épisode aigu :
On considérait comme traitement curatif le traitement principal entrepris pour l’épisode ayant motivé la demande de recherche de Pneumocystis :
- traitement par sulfadiazine-trimethoprime curative - traitement par antibiotique
- traitement par corticothérapie - autre traitement, etc…
Un traitement secondaire était inscrit en cas de corticothérapie associée à un traitement curatif de la pneumocystose dans le cas d’une pneumocystose grave (si Pression en oxygène<75mmHg nécessitant une ventilation invasive (70)).
*l’évolution
- favorable : amélioration ou amendement des symptômes ayant motivé la demande
- défavorable : passage à une chronicité des symptômes comme par exemple dans une pneumopathie d’hypersensibilité, une granulomatose, etc…
*le décès, sa date et sa cause et si le décès était imputable à l’épisode respiratoire ayant motivé la demande.
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 27
*radiologie : une imagerie médicale (radiographie, scanner, imagerie par résonnance magnétique) était systématiquement recherchée pour chaque patient inclus. On recherchait dans les comptes rendus d’imagerie les notions « d’opacité en verre dépoli » (71), la conclusion diagnostique du praticien radiologue était aussi prise en compte. *biologie :
- lymphopénie
- charge virale VIH en cas de séropositivité au VIH - taux de CD4
- le rapport CD4/CD8. Le rapport CD4/CD8 était exprimé en variable semi-quantitative avec trois seuils (<0,1, <1 et >1)
On prenait la valeur de ces variables à plus ou moins quinze jours date de la demande de recherche de Pneumocystis.
- résultat de la recherche de Pneumocystis :
- Examen direct microscopique par coloration de Charlvardjian et de May Grünwald Giemsa (MGG), technique qualitative.
- qPCR Pneumocystis. Précision du type de prélèvement (LBA, crachat ou expectoration induite) et de la valeur de cycle de seuil (CT).
*Recherche des perdus de vue :
En cas de perdu de vue, les services cliniques et les départements d’informatique médicaux (DIM) étaient contactés. La date de point choisi était de trois mois après la dernière inclusion, ce délai étant le délai de suivi retrouvé dans d’autres études cliniques pour cette pathologie (72) .
Pour tous les patients non décédés à la date de point, une date de dernière nouvelle ultérieure avait été recherchée.
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 28
Méthode de Polymerase Chain Reaction quantitative (qPCR) :
L’extraction des prélèvements respiratoires a été réalisée par le kit QIAamp® DNA mini-kit (Qiagen, Courtabœuf, France), selon le protocole ‘sang petit volume et fluides corporels’. Un volume de 2ml était extrait à chaque fois qu’il s’agissait d’un LBA. Lorsqu’il s’agissait d’autres prélèvements respiratoires, la totalité du prélèvement était prise. L’échantillon était centrifugé à 3000 tours/minute pendant cinq minutes. L’extraction était réalisée sur le culot. Enfin, le volume d’élution était de 100 μl.
Nous avons utilisé la qPCR de Meliani (73), servant de référence pour les qPCR. La cible amplifiée était le gène 1 de la sous unité large de l’ARN mitochondrial (mtLSUrRNA). Ce gène est la cible la plus fréquemment choisie pour le diagnostic de PJP (56,73,74) Les
amorces utilisées étaient les suivantes : PCW3 :
CTTAAAATAAATAATCAGACTATGTGCGATAAG et PCW4 :
GGAGCTTTAATTACTGTTCTGGGC. La sonde utilisée était une sonde Taqman (FAM6- AGATAGTCGAAAGGGAAC-TAMRA).
La qPCR était réalisée à partir 5 μl d’extrait d’ADN à partir des 100 μl auquel on ajoutait les réactifs de PCR : 2 μl Mix LC (Ligh cycler Fast Start DNA Master Hybrobes 10X, Roche Applied Science), 4μl de MgCl2 (25mM), 1 μl de chaque amorce (10 μM), 0.25 μl de la sonde (20 μM), 0.25 μl d’UNG (Uracyl DNA glycosylase, Invitrogen 1U/μl) et qsp H20 pour un volume final de 20μl.
Le protocole d’amplification sur Light Cycler 2.0 e comprend une étape d’activation de l’UNG à 50C° pendant deux minutes suivie d’une phase d’activation de la Taq polymérase de 10 min à 95°C puis la phase d’amplification de cinquante cycles :
- Dénaturation 10 s à 95°C - Hybridation 45 s à 60°C - Elongation 1 s à 72°C
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 29
Définition du cycle seuil (CT) :
Pour déterminer la positivité d’une PCR et/ou quantifier un échantillon par PCR en temps réel, on détermine le nombre de cycles à partir duquel le produit PCR est détectable.
Méthode d’examen direct (microscopie) :
L’examen direct était réalisé par la lecture au microscope d’étalement sur lame suite à la centrifugation par cytospin d’un culot du prélèvement. Les lames étaient colorées au May-Grünwald-Giemsa (MGG) et par la coloration de Chalvardjan (bleu de toluidine). Des kystes et des formes végétatives de Pneumocystis étaient recherchés. Les résultats étaient communiqués sous forme qualitative (positif ou négatif).
Etude réalisée en aveugle :
La décision clinique de considérer le patient en Pneumocystose maladie (PJP+) ou en colonisation à Pneumocystis (PJP-) était prise indépendamment du résultat quantitatif (cycle de seuil) de la qPCR. Le clinicien avait cependant la connaissance du résultat qualitatif (positif ou négatif).
Définition PJP+ :
Dans notre étude, la référence était constituée par la décision du clinicien qui considérait le patient en Pneumocystose maladie (PJP+) ou colonisation (PJP-). La caractéristique PJP+ était définie dans les comptes rendus médicaux par le diagnostic de pneumocystose plus un traitement antipneumocystose à dose curative (sulfadiazine-trimethoprime BACTRIM® ou atovaquone WELLVONE®).
La décision de considérer le patient en Pneumocystose maladie et de mettre un traitement anti Pneumocystis dépendait donc des antécédents du patient, du résultat de l’examen direct, du résultat qualitatif de la qPCR, de la symptomatologie, de la radiologie, des traitements au long cours, du degré d’immunodépression et de la présomption du clinicien.
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 30
Définition PJP- :
En cas de qPCR Pneumocystis positive, tout autre diagnostic, toute suspicion infirmée ou le maintien d’un traitement à dose préventive sans diagnostic de pneumocystose étaient considérés PJP-.
Relecture des dossiers :
A la date de l’arrêt de l’étude, tous les dossiers médicaux ont été revus afin de détecter les éventuels diagnostics réfutés a posteriori. Les diagnostics de PJP+ infirmés a
posteriori ont été reconsidérés PJP- et inclus dans les analyses statistiques et dans les
résultats comme PJP-.
Analyses statistiques :
Les analyses statistiques ont été faites par le logiciel S.A.S version 9.3. Tous les résultats ont été analysés avec un risque alpha de 0,05. Les variables quantitatives suivant une loi Normale ont été analysées avec des tests paramétriques (test de Student). Les variables quantitatives ne suivant pas une loi Normale ont été analysées par les tests de Mann Whitney. Pour les variables qualitatives, les tests du chi-deux et le test exact de Fisher ont été utilisés. Les analyses de survie utilisaient le modèle du Logrank. Les analyses univariées et multivariées ont été utilisées pour prendre en charge les facteurs de confusion éventuels et les Odds Ratio calculés dans cette occasion. Pour les sensibilités et spécificités, des seuils de CT ont été calculés grâce aux courbes ROC en prenant comme référence la décision clinique, la microscopie étant jugée trop peu sensible pour pouvoir servir de référence (75).
Les seuils de CT ont été déterminés pour obtenir des seuils de sensibilité et de spécificité de 80% pour chacun des sous-groupes.
Du fait de la rareté de la maladie, d’une incidence très faible et de données sur la colonisation peu informatives, nous n’avons pu calculer un nombre de sujets nécessaires avant de commencer l’étude. Mais nous avons réalisé une analyse intermédiaire en 2011 qui montrait des résultats significatifs concernant les groupes malades et non malades ce qui nous a fait poursuivre l’étude (22).
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 31
Résultats.
Le laboratoire de Parasitologie-Mycologie du Centre Hospitalier Universitaire de Nice a réalisé entre le 1er avril 2008 et le 1er octobre 2013 1964 qPCR correspondant à 986
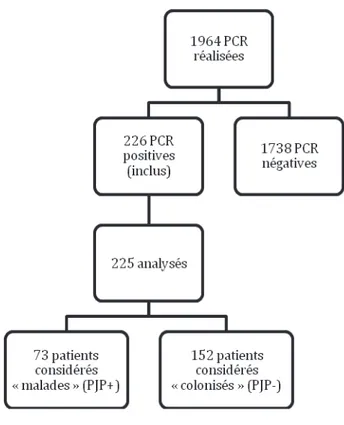
patients à la recherche de Pneumocystis jirovecii. Il y a eu 226 (11,5%) patients avec des qPCR positives (qPCR+) à Pneumocystis jirovecii. Un seul patient a été considéré perdu de vue et a donc été exclu. Soixante-treize patients (33,77%) dont les prélèvements étaient positifs ont été considérés selon les critères clinico-biologiques comme malades (PJP+).
Au laboratoire de Parasitologie-Mycologie du CHU de Nice, les infections fongiques invasives y compris les cas de PJP sont déclarés au RESSIF (Réseau de surveillance des infections fongiques invasives) géré par l’Institut Pasteur. A partir de ces fichiers, nous avons vérifié qu’aucun patient PJP+ n’a eu de qPCR négative.
Du fait des multiples paramètres de l’étude nous avons considéré plusieurs sous-échantillons qui seront détaillés par la suite :
- un sous-échantillon PJP+ versus PJP- pour comparer la population de patients en Pneumocystose maladie (PJP+) aux patients colonisés (PJP-).
- un sous-échantillon de patients PJP+ versus PJP- avec qPCR réalisée sur LBA pour comparer les valeurs des CT entre ces deux échantillons.
- un sous-échantillon de patients VIH versus non-VIH (autres comorbidités) avec qPCR réalisées sur LBA pour comparer les cycles de seuil entre ces sous-groupes parmi les échantillons de patients PJP+ et PJP-.
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 32
Figure 1 : Diagramme de flux de l’étude
Échantillon de l’étude avec l’ensemble des qPCR positives
Caractéristiques de l’échantillon avec qPCR Pneumocystis positive (qPCR+).
La description de l’échantillon des patients qPCR+ figure dans le tableau 1. L’échantillon de patients qPCR+ avait une nette prédominance masculine (sexe ratio 1,74) avec 143 individus de sexe masculin. L’âge moyen pour cet échantillon était de 59 ans et demi (Intervalle de confiance IC 95% [ 57,39 ; 61,91]).
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 33 Caractéristique de l’échantillon n, (%)
Effectif 225
Sexe Ratio 1,74 (143 hommes pour 82 femmes)
Age (moyenne, IC95%) 59,65[57,39;61,91]
Statut sérologique VIH positif 45 (19,91)
Si VIH positif: charge virale (médiane, IQR) 5,11 log10 [3,23 log10;6,99 ]
Lymphocytémie ( 22 données manquantes) hors aplasiques médiane, IQR 1000 [600; 1700]
Rapport CD4/CD8 (133 données manquantes) CD4 >1 CD4[0,1 ;1] CD4<0,1 40 (43,48) 30 (32,61) 22 (23,91) Services Pneumologie 63 (28,00) Infectiologie 39 (17,33) Réanimation 38 (16,89) Autres 36 (16,00) Médecine Interne 29 (12,89) Hématologie/Cancérologie 20 (8,89) Comorbidités Hémopathie maligne 47 (20,89) Maladies auto-immunes 43 (19,11)
VIH (si absence autres comorbidités)* 44 (19,56) (* 1 VIH classé en cancer)
Maladies respiratoires 37 (16,44)
Cancer 30 (13,33)
Autres 14 (6,22)
Transplantation 10 (4,44)
Tableau 1 : Description de l’échantillon de patient ayant une qPCR Pneumocystis positive.
Services demandeurs :
Une majorité (28,00%) de patients ayant une qPCR Pneumocystis positive venait des services de pneumologie des différents hôpitaux de la région, puis des services d’infectiologie (17,33%) et ensuite des services de réanimation (16,89%). En revanche, les services d’onco-hématologie étaient peu demandeurs. Ces résultats pouvaient s’expliquer par la facilité de certains services à effectuer plus de LBA que d’autres, car disposant d’un plateau technique adéquat (services de pneumologie ou de réanimation par exemple). De plus, les services de pneumologie et d’infectiologie pouvaient être plus
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 34
sensibles à la symptomatologie respiratoire (dyspnée et toux) d’autant plus chez des patients VIH dans les services d’infectiologie.
Immunodépression dans la population qPCR positives :
Quarante-cinq (19,92%) patients étaient séropositifs pour le VIH
(phase SIDA, maladie connue ou de découverte récente) avec une charge virale médiane de 5,11 log10. Deux autres catégories de patients ressortaient parmi les comorbidités : les hémopathies malignes (20,89%) et les pathologies auto-immunes (19,11%).
Les patients avec qPCR+ étaient immunodéprimés avec une lymphocytémie basse. Nous avons pu recueillir les rapports CD4/CD8 chez 92 sujets. Ce rapport était inférieur ou égal à 1 chez 56,52% des patients
Traitement au long cours et données manquantes :
L’ensemble des patients de l’échantillon qPCR+ souffrait de pathologies chroniques (comorbidités). La distribution des traitements pour ces pathologies chroniques se répartissait de la manière suivante :
- 73,98% prenaient des immunodépresseurs en monothérapie ou en association (corticothérapie, immunosuppresseurs, biothérapie)
- 13,82% avaient une thérapie antirétrovirale en cours
-4,07% une association d’immunosuppresseurs et une prévention antipneumocystose,
- et 1,63% une association d’antirétroviraux et de prévention antipneumocystose. Au total, six patients ont eu une qPCR positive malgré un traitement préventif contre la pneumocystose et ont été considérés PJP+ dans un premier temps (Tableau 2).
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 35
Contexte clinique
CT Microscopie Décès Remarque Statut final
Myosite 26 négatif non PJP+
Transplantation hépatique
26 négatif non PJP+
Mucoviscidose 25 négatif non PJP+
VIH stade SIDA absence positif non PJP+
BPCO 36 négatif non Diagnostic
réfuté a
posteriori
PJP-
Cirrhose 35 négatif non Diagnostic
réfuté a
posteriori
PJP-
Tableau 2 : Caractéristiques des six patients traités contre la pneumocystose malgré un traitement préventif.
Le patient avec myosite était sous immunosuppresseurs et corticoïdes et présentait une infection pulmonaire avec une lymphopénie à 1000 et un rapport CD4/CD8<1. Le patient s’est amélioré sous traitement curatif. Il n’y avait pas d’imagerie disponible. Le patient avec décompensation hépatique avait une cirrhose mixte et présentait une dyspnée, de la toux et une lymphopénie à 600/mm3. Son imagerie montrait un épanchement sans foyer de verre dépoli. Il était sous immunosuppresseurs et corticoïdes. Le patient s’est amélioré sous traitement curatif.
Le jeune patient ayant une mucoviscidose a présenté une décompensation respiratoire aiguë. Le patient s’est amélioré sous traitement curatif.
Le patient VIH était en phase SIDA (charge virale 4,5 log10) présentait une dyspnée et son imagerie montrait des foyers en verre dépoli diffus. Il avait un antécédent de pneumocystose.
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 36
Les deux patients réfutés étaient :
- un patient séropositif pour le VIH avec une charge virale indétectable mais lymphopénique à 1000/mm3, le diagnostic retenu était celui d’exacerbation de Bronchopneumopathie chronique obstructive (BPCO)
- un patient avec BPCO, lymphopénique à 700 présentant une dyspnée. Son diagnostic initial a été réfuté devant sa séronégativité pour le VIH, la microscopie
Pneumocystis négative et l’absence d’hémopathie maligne.
Pour cent deux patients ayant une qPCR positive, il n’était pas documenté de traitement au long cours. Parmi ces patients, vingt-six étaient séropositifs pour le VIH. Douze étaient sans traitement VIH (découverte de séroposivité VIH ou rupture de traitement). Neuf de ces douze patients étaient PJP+ et on a observé chez ces neuf patients sans traitement VIH deux décès.
Traitement curatif de l’épisode respiratoire à l’origine de la demande de recherche de Pneumocystis dans la population qPCR Pneumocystis positive :
Au niveau des traitements curatifs pour l’épisode respiratoire, nous avons pu recueillir 143 données. Il consistait en :
- 82 (57,34%) traitements par sulfadiazine-trimethoprime : - 73 chez les PJP+ soit 100% des PJP+
- 9 PJP- (5,92% des PJP-),
- 30,77% des patients avaient un traitement antibiotique autre (bêta-lactamines, fluoroquinolones…)
- 8,39% un traitement non anti-infectieux. - et 3,50% un traitement par corticoïdes,
Critères cliniques, paracliniques et biologiques de l’échantillon qPCR +.
Concernant les critères cliniques qui ont amené les cliniciens à effectuer un prélèvement pour le Laboratoire de Parasitologie-Mycologie, on retrouvait un épisode de fièvre chez 77 individus (34,22%), de toux chez 68 individus (30,22%) et de dyspnée chez 125
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 37
individus (55,56%). L’association de deux critères se retrouvait chez 76 individus (33,78%) et la triade fièvre-toux-dyspnée caractéristique de la Pneumocystose chez 27 individus (12,00%).
Nous avons pu recueillir les comptes rendus de 162 imageries avec 47,53% en aspect de verre dépoli, caractéristique non pathognomonique de la pneumocystose.
L’examen direct du prélèvement respiratoire montrait une positivité après coloration au Chalvardjan chez trente patients soit 13,33%. Ces 30 patients ont été considérés PJP+. Pour treize patients (5,78%) au moins deux qPCR Pneumocystis ont été réalisées à différents temps. Il a été constaté pour ces patients un changement de statut avec une qPCR positive qui se négative sur le prélèvement suivant et réciproquement sans différence statistique entre les patients malades et les patients colonisés. Ces données sont non contributives pour l’étude mais confirment le caractère réversible de la colonisation. Pour ces treize patients, cinq étaient PJP+ et huit étaient PJP-, sans différence significative.
Analyse du sous échantillon de patients avec Pneumocystose maladie PJP+ versus colonisation PJP-.
Il y avait ainsi 73 malades PJP+ et 152 non malades PJP- parmi les 225 qPCR
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 38
Figure2 : Répartition de l’échantillon qPCR+ en fonction de PJP+ et de PJP-
Caractéristiques des échantillons :
La description de l’échantillon figure dans le tableau 3. La prédominance masculine se retrouvait dans les deux groupes PJP+ et PJP- . En revanche, le groupe de patients malades PJP+ était significativement plus jeune (55,40 ans versus 61,70 ans, p=0,01). Le statut sérologique VIH était aussi significativement différent, les patients PJP+ étant plus à risque d’être séropositif au VIH (41,10% versus 9,87%, p<0,037 en régression logistique multivariée). Le statut sérologique VIH est donc un facteur de risque de PJP+. La charge virale était plus importante chez les PJP+ que chez les PJP- et la lymphocytémie était plus profonde chez les malades que chez les patients colonisés En régression logistique multivariée, un rapport CD4/CD8 fortement abaissé (inférieur à 0,1) était un facteur de risque de la pneumocystose, (régression logistique multivariée OR= 6,31, IC95% [1,92 ; 20,76], p=0,002) alors qu’avec un rapport CD4/CD8 compris entre 0,1 et 1, on avait qu’une tendance non significative (OR= 2,43, IC95% [0,92 ; 6,41], p=0,07).
En conclusion, deux facteurs de risques ont été identifiés : séropositivité VIH et rapport CD4/CD8<0,1.
225
qPCR+
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 39 Caractéristique de l’échantillon PJP+ n,(%) PJP- n,(%) P univarié Effectif 73 (32,44) 152 (67,56)
Sexe Ratio Homme/femme 1,92 1,66 0,63
Age (moyenne, IC95%) 55,40 [51,21; 59,58] 61,70 [59,04;64,38] 0,01 Statut sérologique VIH positif 30 (41,10) 15 (9,87) <10-3 Si VIH positif: charge virale (médiane, IQR) 5,71 log10 [5,31 log10;5,91 log10] 4,73 log10 [3,81 log10; 5 log10] 0,01
Lymphocytémie (22 données manquantes)
hors aplasiques médiane, IQR
800 (500 ; 1300) 1100 (700 ; 1800) 0,03
Rapport CD4/CD8 (133 données manquantes) CD4>1 CD4[0,1 ;1] CD4<0,1 CD4>1 CD4[0,1;1] CD4<0,1 0,003
14 (29,16)
17 (35,42) 17 (35,42) 26 (59,09) 13 (29,55) 5 (11,36)
Tableau 3 : Comparaison des caractéristiques des patients PJP+ et PJP-.
Saisonnalité de la pneumocystose :
Le laboratoire de parasitologie-mycologie du CHU de Nice étant le seul centre de la région à pratiquer des qPCR Pneumocystis et des examens directs à la recherche de
Pneumocystis jirovecii, nous avions l’exhaustivité des cas de pneumocystoses dans la
région de Nice. Nous avons pu alors étudier sur une période de cinq ans l’hypothèse d’un caractère saisonnier de la pneumocystose sans en montrer une tendance significative en analyse univariée ou multivariée.
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 40
Pathologies chroniques, traitements au long cours et services demandeurs :
L’ensemble de ces données sont décrites dans le tableau 4.
Caractéristique de l’échantillon PJP+ n,(%) PJP- n,(%) p univarié Services <10-4 Infectiologie 20 (27,40) 19 (12,50) Médecine Interne 18 (24,66) 11 (7,24) Réanimation 10 (13,70) 28 (18,42) Hématologie/Cancérologie 10 (13,70) 10 (6,58) Pneumologie 8 (10,96) 55 (36,18) Autres 7 (9,59) 29 (19,08) Comorbidités <10-4
VIH (si absence autres comorbidités)* 30 (41,10) 14 (9,21) Hémopathie maligne 19 (26,03) 28 (18,42) Maladies auto-immunes 11 (15,07) 132 (21,05) Cancer 6 (8,22) 24 (15,79) Transplantation 3 (4,11) 7 (4,61) Maladies respiratoires 3 (4,11) 34 (22,37) Autres 1 (1,37) 13 (8,55)
Traitements au long cours (102 données manquantes) 46 77 =0,06 Association d’immunosuppresseurs 34 (76,09) 56 (72,73) Traitement antirétroviral 6 (13,04) 11 (14,29) Traitement préventif de la pneumocystose 1 (2,17) 0 (0,00) Autres traitement en monothérapie 0 (0,00) 5 (6,49) Association Immunosuppresseurs et prévention pneumocystose 2 (4,34) 4 (6,49)
Association antiVIH et prévention pneumocystose
2 (4,34) 0 (0,00)
Association autres traitements et prévention pneumocystose
1 (2,17) 1 (1,62)
Total prévention pneumocystose
Université Nice Sophia Antipolis©, Faculté de Médecine 13/10/2014 Page 41
Tableau 4 : Comparaison des pathologies chroniques, traitements au long cours et services demandeurs entre les patients PJP+ et PJP-. Les valeurs des p univariés sont données par catégories (Services, Comorbidités et Traitements au long cours) et non pour les sous-catégories.
Services demandeurs :
Alors qu’on s’attendait à une côte (Odd) de 1 pour 2 dans les services (73 PJP+ pour 152 PJP-, soit 1PJP+ pour 2 PJP-), on constatait une distribution différente (p=0.001) au sein des services étudiés. Ces résultats suggéraient une différence entre la demande des services demandeurs de qPCR qui s’avérait positive à la présence de Pneumocystis
jirovecii (qPCR+) et le fait d’être malade (PJP+) : les services de pneumologie avaient
moins de risque d’avoir un patient malade (PJP+) avec une qPCR+ ( Odd de 1 pour 7), tout comme la réanimation (Odd de 1 pour 3), alors que les services d’infectiologie et d’hématologie/cancérologies avaient un Odd de 1 pour 1 et que la médecine interne avait un Odd inversé de 1,63 pour 1. Ces résultats suggéraient qu’il existait des services ‘à risque’ où en cas de qPCR positive, la pneumocystose était plus probable du fait des facteurs de risques des patients hébergés. Les services à risque décrits ci-avant accueillaient des patients immunodéprimés avec maladies auto-immunes sous corticothérapies, des patients sous chimiothérapies pour cancers ou hémopathies malignes ou des patients séropositifs au VIH. Ces patients étaient à haut risque de pneumocystose à cause de leur immunodépression. Au contraire, certains services comme la pneumologie qui accueillaient des patients avec des pathologies respiratoires diverses non corrélées à de l’immunodépression étaient moins à risque.
Comorbidités :
Les pathologies chroniques pour lesquelles les patients pouvaient avoir ou non un traitement au long cours, immunodépresseurs ou préventif de la PJP, constituaient les comorbidités du patient. La distribution de ces comorbidités était significativement différente entre les malades PJP+ et les non-malades PJP- (p<10-4). Seule la comorbidité VIH ressortait comme facteur de risque de pneumocystose comme décrit dans le