Profils en acides gras, abondance de composés volatils et propriétés
sensorielles du lait de vaches recevant de la fléole des prés sous forme de foin,
d’ensilage ou de pâturage
Mémoire
Marie-Pier Villeneuve
Maîtrise en sciences animales
Maître ès sciences (M.Sc.)
Québec, Canada
iii
Résumé
Afin d’évaluer l’effet du type de fourrage utilisé dans la ration sur la flaveur ainsi que sur le profil en acides gras et en composés volatils du lait, des vaches laitières ont reçu une ration à base de fléole des prés sous forme de foin, d’ensilage ou de pâturage. Le rapport acide palmitique sur acide oléique fût inférieur pour le lait issu du traitement pâturage comparativement aux autres traitements. Le type de fourrages a également affecté les teneurs en acides gras, alcools, aldéhydes, cétones, lactones et terpènes du lait. Des panélistes ont été en mesures de différencier les laits des traitements foin et pâturage. Les résultats de cette expérience montrent que les profils en acides gras et en composés volatils des sécrétions lactées peuvent être modulés par le type de fourrage servi aux vaches et que ces changements influencent les propriétés sensorielles du lait.
v
Table des matières
Résumé ... iii
Table des matières ... v
Liste des tableaux ... vi
Liste des figures ... vii
Liste des abréviations et des sigles ... ix
Remerciements ... xi
Avant-propos ... xiii
Chapitre 1. ... 1
Introduction ... 1
Chapitre 2 ... 5
Revue des travaux antérieurs ... 5
2.1. Alimentation et composition du lait ... 5
2.2. Composés volatils retrouvés dans le lait via la consommation de fourrages ... 6
2.3. Principaux constituants et composés volatils ayant un impact sur la flaveur du lait ... 9
2.4. Impacts des traitements thermiques sur les composés volatils retrouvés dans le lait ... 18
2.5. Impact des méthodes d’analyses sur les composés volatils retrouvés dans le lait ... 22
2.6. Étude des composés volatils retrouvés dans le lait ... 31
2.7. Analyses sensorielles, seuils de perception et dégustation de lait ... 38
Liste des ouvrages cités ... 41
Chapitre 3 ... 47
Milk volatile organic compounds and fatty acid profile in cows fed timothy as hay, pasture, or silage ... 47
Interpretive summary ... 48
Abstract ... 49
Introduction ... 50
Materials and methods ... 51
Results and discussion ... 56
Conclusion ... 63
Acknowledgement ... 63
References ... 65
Chapitre 4 ... 81
Liste des tableaux
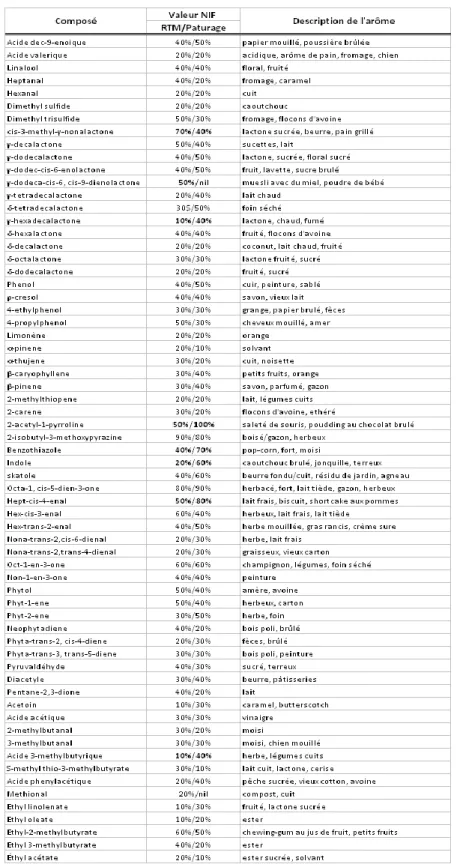
Tableau 2.1. Valeur NIF (nasal impact frequency) des composés identifiés par chromatographie en phase gazeuse avec olfactomètre (GC-O) et provenant du lait de vaches ayant consommé une ration totale mélangée (RTM) ou du pâturage, avec la description aromatique.. ... 35 Tableau 2.2. Abondances relatives moyennes (mg/kg, ± erreur type de la moyenne) des composés volatils identifiés dans le lait de vaches Holstein ayant consommées des rations à base de pâturage ou une RTM (tiré de Croissant et al., 2007). ... 37 Table 3.3. Chemical composition of the three experimental timothy forage types ... 69 Table 3.4. Body weight, forage intake, milk yield, and milk composition in Holstein cows fed timothy hay, pasture, or silage ... 70 Table 3.5. Fatty acid profile of milk fat of Holstein cows fed timothy hay, pasture, or silage ... 71 Table 3.6. Milk volatile organic compounds in Holstein cows fed timothy as hay, pasture, or silage. ... 74 Table 3.7. Results of the triangle tests comparing milks from cows fed silage or pasture with milk from cows fed hay ... 76 Table 3.8. Average rankings of 1 to 3 given by 30 assessors for the intensity of global, sweet, and grassy flavors of milk from Holstein cows fed timothy hay, pasture, or silage ... 77
vii
Liste des figures
Figure 2.1. Analyse en composantes principales des composés volatils retrouvés dans du lait pasteurisé à différentes températures (77, 79, 82 et 85°C) et analysés aux jours 0, 7, 10 et 13 après la pasteurisation (Source : Gandy et al., 2008). ... 21 Figure 3.2. The ratio of 16:0 to c9 18:1 fatty acids in milk fat of Holstein cows fed timothy hay, pasture, or silage. SEM = 0.34. a, b Bars with uncommon superscripts are different at P < 0.01. ... 79
ix
Liste des abréviations et des sigles
°C : degré Celsius
ADF : (acid detergent fiber) fibre au détergent acide
AEDA : (aroma extraction dilution analysis) analyse de dilution et extraction d’arôme BW : (body weigh) poids corporel
C : carbone
CLA : acides linoléiques conjugués CP : (crude protein) protéine brute d : (day) jour
DIM : (days in milk) jour en lactation DM : (dry matter) matière sèche
DMI : (dry matter intake) matière sèche ingérée DVB : Divinylbenzene
FA : (fatty acid) acide gras
FCM : (fat corrected milk) lait corrigé pour sa teneur en matière grasse g : gramme
g/L : gramme/litre
GC : (gaz chromatography) chromatographie en phase gazeuse
GC-FID : (gaz chromatography –flame ionisation detector) chromatographie en phase gazeuse jumelée à un détecteur à ionisation de flamme
GCMS : (gaz chromatography mass spectrometry) chromatographie en phase gazeuse avec spectromètre de masse
GC-O : (gaz chromatography-olfactometry) chromatographie en phase gazeuse avec olfactomètre HRGC : (high resolution gaz chromatography) chromatographie en phase gazeuse à haute résolution
HS-SPME : (headspace solid phase micro extraction) micro-extraction en phase solide configuration ‘headspace’
kg : kilogramme mg : milligramme MS : matière sèche
NDF : (neutral detergent fiber) fibre au détergent neutre NEL : (net energy of lactation) énergie nette de lactation
NIF : (nasal impact frequency) fréquence de détection nasale PA : polyacrylate
PDMS : polydimethylsiloxane RTM : ration totale mélangée
SPME : (solid phase micro extraction) micro-extraction en phase solide TMR : (total mixed ration) ration totale mélangée
VOC : (volatile organic compounds) composés organiques volatils α : alpha
β : bêta γ : gamma ω-3 : oméga 3 ω-6 : oméga 6
xi
Remerciements
Cette expérience a été financée par le programme de Chaire Industrielle du Conseil de Recherches en Sciences Naturelles et en Génie du Canada (Ottawa, ON, Canada) avec la contribution de Novalait inc. (Québec, QC, Canada), des Producteurs laitiers du Canada (Ottawa, ON, Canada), de la Fédération des producteurs de lait du Québec (Longueuil, QC, Canada), du Ministère de l’Agriculture, des Pêcheries et de l’Alimentation du Québec (Québec, QC, Canada) et de Valacta (Sainte-Anne-de-Bellevue, QC, Canada). Les auteurs souhaitent également remercier le personnel du Centre de recherche en sciences animales de Deschambault pour leur collaboration durant la phase expérimentale. Nous remercions aussi Gabrielle St-Pierre et Micheline Gingras, du Département des sciences animales de L’Université Laval, pour leur aide lors des analyses de laboratoire.
xiii
Avant-propos
L’idée de réaliser un projet de maîtrise a d’abord fait surface lors d’un stage professionnel réalisé en 2008 dans un centre de recherche. Ayant toujours aimé appendre, j’ai trouvé fascinant de découvrir le monde de la recherche qui rallie rigueur et sciences.
J’ai terminé mon bac au printemps 2009 et l’envie d’entreprendre des études supérieures était toujours présente. J’ai finalement décidé de communiquer avec Rachel Gervais, que j’avais croisée à quelques reprises lors de ma dernière session et qui m’avait parlé d’une Chaire de recherche sur la composition du lait qui serait bientôt mise sur pied avec le Dr Yvan Chouinard. Je me souviens très bien de m’être rendue au Pavillon Paul-Comtois pour rencontrer Rachel. C’était inévitable; son charisme, sa personnalité authentique et sa grande générosité m’ont pratiquement convaincue. Je suis donc allé rencontrer Yvan Chouinard qui m’avait déjà enseigné un cours de nutrition animale. Je savais que le Dr Chouinard était un enseignant qui connaissait très bien sa matière, mais j’étais loin de me douter que j’allais rencontrer un chercheur si intelligent et dévoué, et qu’il allait devenir mon directeur de recherche. Avec le Dr Chouinard, j’ai appris à pousser davantage mes réflexions afin de m’assurer de toujours bien comprendre l’origine des phénomènes observés et par le fait même, j’ai développé ma curiosité scientifique. J’ai été inspirée de travailler auprès d’un chercheur faisant preuve de beaucoup d’humilité et d’humanité, en plus d’être animé d’une passion aussi remarquable pour son métier.
Le projet, portant sur l’influence du type de fourrage sur les flaveurs du lait, exigeait d’abord d’identifier quels facteurs alimentaires pouvaient avoir un impact sur les propriétés du lait. Il fallait également obtenir de l’information sur les méthodes possibles d’analyse des composés aromatiques volatils contenus dans le lait. Une revue de littérature sur le sujet est présentée dans le deuxième chapitre de ce mémoire. Le chapitre trois contient l’article scientifique dans lequel nous décrivons l’expérience que nous avons réalisée. Cet article a été réalisé avec la collaboration d’Yvan Chouinard, professeur titulaire, Rachel Gervais, professeure adjointe et Yolaine Lebeuf, Professionnelle de recherche au Département des sciences animales de l’Université Laval. Gaëtan Tremblay, chercheur scientifique chez Agriculture Agroalimentaire Canada, Jean-Christophe Vuillemard, professeur titulaire au Département des sciences des aliments et de nutrition et Jacinthe Fortin, chercheure au Centre de recherche et de développement sur les aliments d’Agriculture et
Agroalimentaire Canada ont également contribué à cet article qui sera soumis pour publication en 2013 dans le Journal of Dairy Science. La mise en forme et les abréviations utilisées dans ce dernier chapitre respectent donc les exigences de ce journal.
Je tiens à remercier Yolaine Lebeuf et Micheline Gingras pour leur précieuse aide lors des analyses en laboratoire ainsi que pour le temps qu’elles ont accordé à étudier l’analyse d’échantillons de lait avec le GCMS. Je veux également remercier toute l’équipe du Centre de recherche en sciences animales de Deschambault et plus particulièrement Marie-Ève, André et Philippe, pour leur collaboration et tout le plaisir que nous avons eu lors de la phase expérimentale du projet. Merci à Gabrielle St-Pierre et Leacady Saliba pour leur aide. Un merci spécial à Marie-Pierre Dallaire, également étudiante à la maîtrise, qui est passé d’une collègue de travail à une précieuse amie et ce, en m’accompagnant lors de toutes les étapes que l’on doit franchir lorsqu’on entreprend des études supérieures.
Pour terminer, j’aimerais remercier mes parents, qui ont toujours cru en moi et m’ont supporté tout au long de mes études. Merci aussi à ma petite sœur, pour son positivisme et son soutien. Finalement, merci à mon conjoint, qui m’a encouragé dès le début à réaliser ce projet et qui a été présent à toutes les étapes. C’est grâce à vous tous et à la lueur de fierté que je vois dans vos yeux que j’ai toujours envie de continuer et de me dépasser…
Mario, Pierrette, Cassandra et Jasmin, je vous dédie ce mémoire…
1
Chapitre 1.
Introduction
Les consommateurs sont de plus en plus soucieux de la qualité des aliments qu’ils ingèrent. Les caractéristiques nutritionnelles, microbiologiques et sensorielles revêtent une grande importance dans la sélection d’un produit plutôt qu’un autre. En ce sens, la flaveur d’un aliment, ainsi que son apparence et sa texture, sont considérés comme déterminants dans le choix effectué par le consommateur pour un produit particulier (d’Acampora et al., 2007).
Sur le plan physiologique, l’odeur d’un aliment est perçue par le nez, avant la prise en bouche, alors que l’arôme est perçu par les voies rétro nasales lorsque l’aliment se trouve dans la cavité buccale (Molimard et al., 1997). Ce sont ces phénomènes, combinés au goût de l’aliment, qui définissent le concept de flaveur. La perception de la flaveur est généralement due à la présence de molécules volatiles présentes à de très faibles concentrations (Molimard et al., 1997).
La perception sensorielle du lait est étroitement liée à ses caractéristiques ou propriétés physiques. L’émulsion de globules de gras dans la phase aqueuse de protéines colloïdales procure un agréable goût en bouche (Marsili, 2003). Des composés volatils y sont présents à de faibles concentrations (Marsili, 2003). Les protéines, les lipides et les glucides contenus dans le lait sont des précurseurs de composés aromatiques volatils (Alvarez, 2009). Par exemple, la matière grasse du lait peut intervenir directement dans la flaveur ou agir à titre de précurseur de plusieurs composés aromatiques tels que les acides gras, les cétones, les alcools, les lactones et les esters (Molimard et al., 1997). Le lait contient de nombreux composés volatils ayant diverses origines et pouvant influencer sa flaveur.
Il est connu que la race de l’animal, son stade de lactation, son âge et son alimentation peuvent influencer la composition du lait. D’ailleurs, plusieurs chercheurs se sont attardés à l’effet de l’alimentation des animaux sur les caractéristiques du lait produit. Mais généralement, on a investigué l’effet de différents types de régime sur les teneurs en composantes majeures du lait, soit les protéines et la matière grasse. Beaucoup moins d’études ont porté sur l’impact de l’alimentation des animaux sur la flaveur du lait produit.
Or, les études complétées ont démontré que l’alimentation des vaches laitières est susceptible de modifier de façon significative les propriétés sensorielles des laits crus (Dubroeucq et al., 2002; Marsili, 2003). Les composés à l’origine des flaveurs peuvent être transférés dans le lait de la vache via l’inhalation, la digestion et les gaz du rumen (Shipe et al., 1962; Morgan et Pereira, 1962). Le principal facteur pouvant changer la concentration en composés volatils dans le lait s’avère donc être l’alimentation des animaux.
Toutefois, plusieurs facteurs rendent difficile l’identification des composés volatils ayant un rôle de premier plan dans la formation de la flaveur du lait. Tout d’abord, il y a moins de composés volatils dans le lait que dans d’autres produits laitiers tels que le beurre ou le fromage (Bendall, 2001). De plus, certains de ces composés possèdent un faible seuil de détection sensorielle (Marsili, 2003) et sont présents dans le lait à des concentrations auxquelles il est très difficile de les quantifier. Cela complique la compréhension exacte de leur rôle dans la flaveur globale du lait. Un autre élément qui complique la compréhension de la formation des flaveurs dans le lait est que la plupart des composés aromatiques présents peuvent être produits par deux ou même plusieurs voies (Marsili, 2003). Par exemple, les productions de méthyl-cétone, d’alcool secondaires et de lactones dans le lait peuvent provenir de réactions microbiennes aussi bien que de traitements à température élevée (Marsili, 2003). En ce sens, le type, l’intensité et la durée des traitements thermiques appliqués au lait (ex. pasteurisation) ont aussi un impact sur sa teneur en composés volatils. Des réactions chimiques ou une détérioration microbiologique peuvent aussi avoir lieu lors de l’entreposage du lait.
3
Ultimement, les méthodes d’extraction et d’analyse des composés volatils sont multiples et diffèrent énormément dans la littérature, ce qui complique la comparaison des résultats obtenus.
Nous avons émis l’hypothèse que le type de fourrage utilisé dans la ration des vaches laitières a une influence sur la flaveur du lait. Le but de notre expérience était d’étudier l’effet du type de fourrage de fléole des prés, soit le foin, l’ensilage et le pâturage, consommé par les vaches laitières, sur les composés volatils retrouvés dans le lait, la production laitière et la composition du lait en acides gras.
5
Chapitre 2
Revue des travaux antérieurs
2.1. Alimentation et caractéristiques sensorielles du lait
Certains aliments de la vache tels que les sous-produits de la betterave et les crucifères sont reconnues pour conférer des flaveurs indésirables au lait (Urbach, 1990). Parallèlement, de nombreuses observations ont été faites relativement à l’effet, parfois cité comme indésirable, de la consommation d’herbe sous forme de pâturage sur la flaveur des produits laitiers (Urbach, 1990). Toutefois, les effets de la nature des fourrages et de leurs méthodes de conservation sur la flaveur du lait produit restent peu connus.
Verdier-Metz et al. (1998) ont comparé les fromages fabriqués à partir du lait de vaches recevant du fourrage récolté dans une même parcelle et le même jour mais servis sous forme de foin ou d’ensilage. Les deux fourrages consommés étaient d’excellente qualité. Outre le fait que le fromage fabriqué avec le lait des vaches ayant reçu de l’ensilage était plus jaune (dus à une plus grande concentration en carotènes dans l’ensilage), il était également plus amer (Verdier-Metz et al., 1998). Les autres propriétés sensorielles étaient relativement comparables pour les deux types de fromages produits. D’autres études ont été menées afin d’analyser l’impact de la source de fourrages sur les propriétés des fromages ou du beurre obtenus, mais très peu se sont attardé aux effets pouvant être perçus sur le lait frais.
En effet, peu de chercheurs ont tenté d’identifier les caractéristiques précises qui différencient les laits provenant de vaches nourries de différents régimes alimentaires. Dans l’étude de Dubroeucq et al. (2002), des tests triangulaires ont permis de distinguer des laits provenant de vaches nourries de
rations à base de pâturage et des laits issus de vaches recevant des rations à base de foin ou des régimes riches en concentrés. Environ la moitié des dégustateurs ont également différencié des laits provenant de vaches nourries d’un régime à base d’ensilage d’herbe plutôt qu’à base de foin. Les auteurs affirment donc que des ensilages d’herbes bien conservés et distribués dans de bonnes conditions peuvent être à l’origine de modifications des caractéristiques sensorielles des laits (Dubroeucq et al, 2002). En outre, les différences observées entre les laits provenant d’animaux nourris aux pâturages et ceux provenant de vaches recevant une ration à base de foin ou de concentrés seraient liées soit aux profils en acides gras du lait de pâturage, ce dernier étant plus riches en acides gras à chaînes polyinsaturés, ou seraient attribuables aux composés volatils retrouvés dans le lait de pâturage (Dubroeucq et al, 2002).
2.2. Composés volatils retrouvés dans le lait via la consommation de fourrages
Les espèces fourragères peuvent contenir plus d’une dizaine de composés volatils de diverses natures chimiques (Kalač, 2011). D’ailleurs, dans certaines régions d’Europe, on vise à utiliser certains composés volatils comme «marqueurs» afin de retracer le type de fourrage consommé par les vaches laitières, puisque ces composés peuvent être transférés dans le lait et ultimement, dans les fromages produits. Des études spécifiques ont été réalisées, au cours des dernières années, afin d’analyser les effets de la diversité botanique des fourrages sur les caractéristiques sensorielles de divers types de fromages produits. Les terpènes notamment, pourraient être utilisés comme paramètre de traçabilité pour du lait ou des produits laitiers d’origine contrôlée.
Les principaux composés volatils retrouvés dans les fourrages peuvent être divisés en plusieurs groupes, selon leur structure chimique. Par exemple, il y a les hydrocarbures, les terpènes, les alcools, les aldéhydes, les cétones, les acides, les esters et les composés soufrés (Kalač, 2011). Certains de ces composés proviennent directement des plantes, alors que d’autres sont produits s’il y a étiolement, lors du séchage ou lors de la fermentation des ensilages (Kalač, 2011).
7
Depuis plusieurs années, l’utilisation d’ensilage dans la ration des vaches est souvent associée à la présence de flaveurs indésirables dans le lait cru. L’étude menée par Shipe et al. (1962) a permis de conclure qu’une grande variété de composés présents dans les ensilages pouvaient être transférés dans le lait par les voies respiratoires aussi bien que par l’absorption dans le système digestif (Shipe et al., 1962). Ces chercheurs ont également démontré que les flaveurs étaient transmises plus rapidement lorsqu’elles étaient inhalées. Des aliments tels que les ensilages fermentés, la luzerne (en herbe ou en foin) et le foin de trèfle seraient reconnu comme pouvant causer des flaveurs indésirables dans le lait (Marsili, 2003). Certaines des molécules contribuant à ces flaveurs indésirables ont d’ailleurs été identifiées (Marsili, 2003). Par exemple, de la luzerne fraîchement coupée contiendrait des teneurs élevées en trans-2-hexanal, trans-3-hexanal et trans-3-hexenol, ce qui procurerait un goût d’herbe au lait (Marsili, 2003).
D’autres auteurs attribuent le ‘goût d’étable’ dans le lait frais à la présence d’acides gras à faible poids moléculaires, à des composés hétérocycliques azotés, à des phénols, des lactones, des dérivés du phytol ou des acétones, ainsi qu’à des produits carbonylés volatils (Alvarez, 2009). Il y a donc plusieurs composés volatils qui peuvent influencer la flaveur du lait. Notons que les composés aromatiques retrouvés dans le lait peuvent provenir directement de l’alimentation, mais ils peuvent également être produits dans le rumen lors du processus de fermentation.
Dans l’étude de Krizsan et al. (2007), 24 ensilages à faible teneur en matière sèche (213 ± 17,6 g/kg MS) et de différentes qualités de fermentation ont été analysés pour quantifier les composés volatils présents et faire un lien avec leur ingestion. Ces ensilages étaient principalement constitués de fléole des prés (Phleum pratense L.) et de fétuque des prés (Festuca elatior auct. Amer). On a identifié et quantifié treize esters, cinq aldéhydes, trois alcools et un sulfure (Krizsan et al., 2007). On a retrouvé du méthanol et de l’éthanal à des concentrations respectivement comparables et légèrement plus élevées en moyenne dans l’herbe comparativement à l’ensilage (Krizsan et al., 2007). Cela indique que la présence de ces composés n’est pas uniquement due à la fermentation (Krizsan et al., 2007). La pectine est la source majeure de méthanol dans la nature et la libération de ce dernier résulte de
l’activité des enzymes pectiques retrouvées dans les plantes, les bactéries, les levures et les champignons (Krizsan et al., 2007). En effet, le méthanol est relâché à partir de la pectine, alors que l’éthanol est produit à partir des glucides fermentescibles. Les alcools primaires seraient formés par la réduction de leur aldéhydes respectifs (Toso et al., 2002). Les autres alcools proviendraient du catabolisme des acides aminés (Kalač, 2011). La concentration moyenne en propanal était également plus élevée dans l’herbe que dans l’ensilage. On a retrouvé de l’éthanol dans les fourrages, mais dans cette étude, Krizsan et al. (2007) n’ont pas trouvé de réponse claire quant à l’origine de l’éthanal et de l’éthanol retrouvé dans l’herbe.
Plusieurs composés volatils peuvent être transférés dans le lait cru ou dans le lait transformé de bonne qualité ayant une flaveur dite « normale ». Par exemple, l’acétone et le 2-butanone seraient les deux molécules présentes en plus grande concentration et pourraient potentiellement provenir de l’alimentation des animaux (Marsili, 2003). Les toluènes et les limonènes seraient présents à l’état de trace seulement et proviendraient de la dégradation de la β-carotène et des fourrages, respectivement (Marsili, 2003). L’hexanal serait aussi présent à l’état de trace et proviendrait de l’auto-oxydation de l’acide linoléique (Marsili, 2003). On constate, avec ces différentes études, que l’alimentation a bel et bien un effet sur le profil des composés volatils retrouvés dans le lait, ces derniers pouvant contribuer à la flaveur du lait.
Selon MacGibbon et Taylor, (2006), les familles de composés volatils qui contribueraient significativement à la flaveur du lait seraient les acides gras, les aldéhydes, les lactones et les méthyl-cétones. Day (1966) a, quant à lui, identifié les acides gras, les aldéhydes, les alcools, les lactones, les cétones, les hydrocarbures et les esters comme étant les familles de composés volatils les plus importantes contribuant à la flaveur du lait. La prochaine section sera donc consacrée à une revue des principales familles de composés volatils retrouvées dans le lait, et documentées dans la littérature.
9
2.3. Principaux constituants et composés volatils ayant un impact sur la flaveur du lait
La matière grasse du lait joue un rôle de premier plan en ce qui a trait aux propriétés organoleptiques des produits laitiers. En effet, les lipides subissent de nombreuses réactions telles que l’hydrolyse, l’auto-oxydation, la décarboxylation, la déshydratation, la réduction et l’estérification. Ces réactions libérent différents composés aromatiques qui peuvent avoir un impact sur les qualités organoleptiques du lait. Plusieurs composés sont libérés dont les acides gras, les alcools, les aldéhydes, les esters, les hydrocarbures, les cétones et les lactones. Nous allons donc nous attarder à ces familles chimiques, ainsi qu’aux composés soufrés et aux terpènes, composés généralement cités dans la littérature ou auxquels certains chercheurs se sont intéressés dans les dernières années.
2.3.1 Acides gras
Plus de 400 acides gras ont été identifiés dans la matière grasse du lait (MacGibbon et Taylor, 2006). Spécifions qu’il existe deux types d’acides gras soit les acides gras saturés, comprenant uniquement des liaisons simples, et les acides gras insaturés, à l’intérieur desquels certains atomes d’hydrogène sont manquant ce qui génère la présence d’une ou plusieurs double(s) liaison(s). Les acides gras que l’on dit polyinsaturés comprennent plusieurs doubles liaisons.
Les acides gras du lait proviennent de deux sources différentes. Les acides gras à chaînes courtes et moyennes (C4 à C14) sont synthétisés dans la glande mammaire alors que les acides gras à longue chaîne (18 carbones et plus) sont prélevés dans le plasma sanguin et proviennent de l’alimentation ou des réserves adipeuses de l’animal. Les acides gras à 16 carbones proviennent de l’une ou l’autre des deux sources (MacGibbon et Taylor, 2006). Par exemple, l’acide α-linolénique (18:3 cis-9, cis-12, cis-15) et l’acide linoléique (18:2 cis-9, cis-12) sont deux acides gras polyinsaturés que l’on retrouve en grande quantité dans l’herbe fraîche (Boufaïed et al., 2003; Jenkins et al., 2008). Ces acides
doivent être ingérés par la vache afin d’être sécrétés dans le lait. L’alimentation de la vache revêt donc une grande importance en ce qui a trait à la composition en acides gras insaturés du lait.
Dans les pays à climat tempéré, l’herbe fraîche contient de 1 à 3 % d’acides gras et est riche en acide linolénique (Doreau et al., 2005). L’espèce, le stade de développement, la température et l’intensité de la lumière sont tous des facteurs expliquant les variations de concentration en lipides observés dans les plantes. Dans l’herbe fraîche, l’acide α-linolénique représente de 50 à 75 % des acides gras totaux (Boufaïed et al., 2003; Elgersma et al., 2006). Les lipides qui constituent les végétaux ne sont toutefois pas statiques et leur dégradation à l’intérieur même de la plante par des lipases est probable et normale. Mais ces processus n’ont pas d’influence notable sur les profils en acides gras dans les plantes. Les plus grandes modifications de la fraction lipidique ont plutôt lieu lors de la sénescence de la plante, lors de la pâture ou lors de la conservation (Elgersma et al., 2006).
Modifier l’alimentation des vaches, directement à la ferme, est le moyen le plus rapide et le plus efficace pour contrôler et moduler le profil et la teneur en matière grasse du lait (Chilliard et al., 2000). De plus, la composition en acides gras du lait peut affecter non seulement ses qualités organoleptiques, mais également ses propriétés nutritionnelles (Chilliard et al., 2000). Plusieurs études ont démontré, au cours des dernières années, les propriétés intéressantes de certains acides gras tels que les ω-3 (spécialement l’acide α-linolénique) et les acides linoléiques conjugués (CLA) notamment dans la prévention du cancer, de l’obésité et de l’athérosclérose (Chilliard et al., 2000). Les acides α-linolénique et linoléique sont les principaux acides gras, respectivement des familles ω-3 et ω-6, qu’on retrouve dans le lait (Slots et al., 2008). C’est pourquoi plusieurs études ont été réalisées afin de moduler et d’optimiser la composition en acides gras des produits laitiers soit, en diminuant la proportion d’acides gras saturés et en augmentant la proportion d’acides gras insaturés, principalement ceux de la famille des ω-3.
11
La quantité d’acide α-linolénique dans le lait serait légèrement plus élevée lorsque les vaches reçoivent des rations à base d’herbe plutôt qu’à base d’ensilage de maïs, l’herbe verte étant la principale source d’acide α-linolénique (Chilliard et al., 2001). Des rations à base d’herbe ou d’ensilage ont également été comparées et il a été observé que sous forme d’herbe, un mélange de graminées et de luzerne permet de produire un lait plus riche en acides gras mono- et polyinsaturés (Morel et al., 2006). De plus, le lait produit contenait des concentrations significativement plus élevées en acide linoléique et en acide α-linolénique (Morel et al., 2006). Lorsque les rations contiennent plus de 58 % d’ensilage d’herbe, cela entraîneraient une augmentation de l’acide myristique et de l’acide palmitique mais diminueraient la proportion d’acide oléique, d’acide linoléique et d’acide α-linolénique, comparativement au lait produit lorsque les animaux consomment de l’herbe au pâturage (Chilliard et al., 2000). Selon Chilliard et al. (2001) du côté de la France, c’est principalement au printemps et à l’automne que la teneur en acides gras de l’herbe est la plus élevée. Il est donc possible d’établir un lien entre la mise au pâturage des animaux et la forte augmentation de la teneur en acide linolénique observée dans le lait, ces derniers pouvant alors représenter jusqu’à 2,5 % des acides gras totaux du lait (Decaen et Ghadaki, 1970). Par contre, des teneurs moins élevées en acide linolénique (maximum 1 %) ont aussi été observés dans d’autres études pour des vaches alimentées au pâturage, ce qui pourrait être expliqué par un stade de développement plus avancé des plantes pâturées (Chilliard et al., 2001). Par ailleurs, Shingfield et al. (2005) ont démontré que le lait contiendrait une plus grande proportion d’acides gras polyinsaturés lorsque la ration est constituée principalement de foin plutôt que d’ensilage. Les observations varient dans la littérature relativement à la teneur en acides gras polyinsaturés retrouvés dans le lait de vaches selon le type de fourrages consommé. Or, il faut noter qu’en plus d’apporter des acides gras polyinsaturés, les fourrages procurent aussi des fibres qui favorisent un pH près de la neutralité et rendent ainsi optimales les conditions pour les microorganismes dans le rumen. Ces derniers vont hydrolyser les lipides et hydrogéner les acides gras qui s’y retrouvent via l’alimentation. Initialement, les lipides ingérés par la vache sont en grande partie des glycolipides, des phospholipides et des triacylglycérols tous riches en acides linoléique et α-linolénique (MacGibbon et Taylor, 2006). Les lipides seront hydrolysés dans le rumen pour libérer des acides gras non estérifiés. Ensuite, ces derniers sont assujettis au processus de biohydrogénation par les microorganismes du rumen (MacGibbon et Taylor, 2006). Donc, des acides gras essentiels tels que l’acide linoléique et l’acide
α-linolénique sont hydrogénés en acides gras monoinsaturés généralement d’isomère trans ainsi qu’en acide stéarique saturé 18:0 (Doreau et al., 2005).
Il est également connu que les acides gras retrouvés dans le lait peuvent avoir un impact sur la flaveur. Par exemple, à de faibles concentrations, l’acide butyrique et l’acide caproïque ont été identifiés comme composés clefs dans la flaveur du lait (MacGibbon et Taylor, 2006). Par contre, lorsque présents en grandes concentrations, ils sont associés à la formation de flaveurs indésirables. Comme mentionné précédemment, les lipides du lait sont également assujettis à plusieurs réactions. Bendall (2001) mentionne que des études ont montré des taux d’oxydation plus rapides pour les acides gras ayant un degré d’insaturation élevé (Cho et al., 1987). Il a donc anticipé dans son étude que dans le lait frais, l’oxydation de l’acide α-linolénique aurait un plus grand impact sur la flaveur que l’oxydation d’autres acides gras tels que l’acide linoléique ou l’acide oléique. En effet, les résultats de son étude démontrent que les produits de l’oxydation de l’acide linolénique (octa-1, cis-5-dien-3-one, hept-cis-4-enal et hex-cis-3-enal) ont été davantage décelés dans le lait que les produits de l’oxydation de l’acide linoléique (oct-1-en-3-one et non-1-en-3-one) (Bendall, 2001). Donc, si on assume que le lait de vaches nourries au pâturage contient généralement davantage d’acide linolénique, il pourrait ainsi être plus susceptible à l’oxydation. En ce sens, une augmentation de la quantité d’acides gras insaturés dans le lait serait en lien avec une augmentation de la quantité de produits de l’oxydation de l’acide linolénique et ces produits pourraient avoir un impact sur la flaveur du lait. De plus, lorsqu’on augmente la quantité d’acides gras insaturés du lait, le point de fusion de la matière grasse diminue et le lait présente une teneur en gras liquide plus importante, ce qui peut également avoir un impact sur l’aspect physico-chimique du lait et ultimement, sur sa flaveur.
2.3.2 Aldéhydes
Les aldéhydes peuvent provenir des lipides (aldéhydes à chaînes droites tels que l’isobutanal, le pentanal, l’hexanal et le nonanal) ou de la dégradation des acides aminés (composés à chaînes ramifiées tels que le 2-methylbutanal et le 3-methylbutanal) (Toso et al., 2002). La plupart des
13
aldéhydes provenant des lipides contribueraient à former l’agréable arôme herbacé du lait (Moio, 1993). Par contre, à concentrations plus élevées, ils procurent une forte et désagréable odeur de suif (Moio et al., 1993). La plupart des aldéhydes retrouvés dans les produits laitiers proviennent de l’oxydation des lipides (Day, 1966). Par exemple, le pentanal et l’hexanal peuvent être présents dans le lait cru mais peuvent également être induits via l’oxydation des lipides par la lumière (Calvo et de la Hoz, 1992). Dans l’étude de Toso et al. (2002), l'hexanal fût l’aldéhyde retrouvé en plus grande quantité dans le lait des vaches alimentées avec de l’ensilage d’herbe. Parallèlement à ce résultat, selon Marsili (2003), l’hexanal serait aussi présent à l’état de trace dans le lait et proviendrait de l’auto oxydation de l’acide linoléique. En effet, les précurseurs les plus importants pour la formation des aldéhydes sont les acides gras insaturés dont les acides oléique, linoléique, linolénique et arachidonique. Gaspardo et al. (2009), ont aussi mesuré une grande quantité d'hexanal comparativement aux autres composés volatils dans le lait. Dans le lait pasteurisé, l’hexanal fût également identifié comme étant un important composé volatil, avec son odeur d’herbe (Moio et al., 1994).
2.3.3 Esters
Les esters peuvent être formés dans la glande mammaire lors de l’estérification des alcools et acides gras à courte chaîne (Moio et al. 1993). Dans leur étude de 1993, Moio et al. ont comparés les composés volatils précurseurs de la flaveur du lait cru de bovins, d’ovins, de caprins et de bufflesses. Pour les bovins, les esters représentaient la plus importante classe de composés, comprenant près de la moitié de la fraction volatile neutre. Les esters éthyliques des acides butanoïque, hexanoïque, octanoïque et décanoïque furent les principaux retrouvés (Moio et al., 1993).
Les esters butyrate d'éthyle et hexanoate d'éthyle sont les substances les plus odorantes retrouvées dans des laits crus bovins avec une odeur fruitée (Moio et al., 1994; Marsili, 2003). Les composés aromatiques les plus puissants dans le lait cru seraient d’ailleurs principalement des esters (Friedrich et Acree, 1998). On note cependant que les esters ne sont généralement pas détectés dans le lait pasteurisé puisqu’ils sont perdus lors du chauffage et de la transformation (Moio et al., 1994 ; Marsili,
2003). Des traitements à température élevée (environ 100ºC) provoquent la volatilisation ou l’hydrolyse des esters éthyliques et ultimement, la formation de méthyl-cétones (Moio et al., 1994).
Dans l’étude de Gaspardo et al. (2009), les esters furent la deuxième famille de composés volatils retrouvés en plus grande proportion. Ces concentrations d’esters élevées dans le lait pourraient être reliées à l’entreposage à des températures froides avant l’échantillonnage. En effet, comme l’explique Nursten (1997), durant cette période, les alcools sont en partie estérifiés avec des acides volatils et convertis en propyles et en esters éthyliques à partir de l’activité enzymatique des bactéries lactiques.
2.3.4 Cétones
Les cétones sont généralement présents sous forme de méthyl-cétones et proviennent des acides gras libres qui sont d’abord oxydés en β-cétoacides qui subissent ensuite une décarboxylation en méthyl-cétones (Moio et al., 1993). Similairement à ce qui a été évalué dans d’autres études sur la fraction volatile du lait (Toso et al., 2002), les cétones furent la plus abondante famille de composés identifiés avec l’acétone et le 2-butanone comme principaux constituants dans l’étude de Gaspardo et al. (2009). D’ailleurs, l’acétone et le 2-butanone seraient les cétones présentes en plus grande concentration dans le lait cru et pourraient potentiellement provenir de l’alimentation des animaux (Gordon et Morgan, 1972; Marsili, 2003).
Dans l’étude de Mounchili et al. (2005), les analyses statistiques suggèrent que le butane-2-one ainsi que le sulfure de diméthyle (un composé soufré) seraient des marqueurs de flaveurs reliés à l’alimentation. Les résultats de l’étude démontrent également qu’il y a une augmentation de la teneur en propane-2-one et en butane-2-one dans le lait de vaches ayant consommé de l’ensilage juste avant la traite et que le lait obtenu avait des défauts de flaveur pouvant être caractérisé par un ‘goût d’étable’ (Mounchili et al., 2005).
15 2.3.5 Lactones
Les lactones sont reconnues pour leur arôme sucré semblable à la pêche ou à la noix de coco (Moio et al., 1993). Dans l’étude de Moio et al. (1993), seulement la δ-déca-lactone et la δ-dodécalactone ont été détectées, en très faible quantité, dans le lait cru de bovin, ovin, caprin et de bufflesse. Le peu de molécules identifiées pourrait être attribué à la technique d’analyse utilisée au moment de l’étude (nous reviendrons sur les méthodes d’analyses un peu plus loin). Notons qu’un pH plus faible du rumen, lorsque les vaches reçoivent une ration riche en concentrés par exemple, pourrait favoriser la production de lactone (Bendall, 2001).
2.3.6 Composés soufrés
Dans l’étude de Moio et al., (1994), le sulfone de diméthyle et les esters furent les composés retrouvés en plus grandes quantités dans le lait cru. Dans le lait pasteurisé, ce sont le sulfone de diméthyle et le pentanal qui furent retrouvés en plus grandes quantités. Dans l’étude de Moio et al. (1996), le sulfone de diméthyle, un composé soufré, était présent dans le lait de brebis alimentées au pâturage, et ce, à des concentrations dix fois plus grandes que dans le lait provenant d’une ration à base de grain. Toutefois, le sulfone de diméthyle a un très faible impact sur l’odeur dans un lait qui a été chauffé (Moio et al., 1994).
Lorsque les vaches consomment des aliments comme de la luzerne, la quantité de sulfure de diméthyle augmente dans le lait (Urbach, 1990). À de faibles concentrations, le sulfure de diméthyle et le sulfone de diméthyle contribuent à la flaveur normale du lait cru. Par contre, lorsqu’ils se retrouvent en forte proportion, ils peuvent causer des problèmes d’odeur (Urbach, 1990; Moio et al., 1996). Il serait alors possible que le sulfure de diméthyle soit oxydé en sulfone de diméthyle via l’oxysulfure de diméthyle. En fait, le sulfure de diméthyle est un produit de la dégradation de la méthionine et est reconnu pour sa contribution au goût dit normal du lait, ou pour sa contribution à la formation de flaveurs indésirables lorsque présent à concentrations élevées. Le sulfure de diméthyle
possède un faible seuil de détection olfactive et de minimes changements de concentration peuvent modifier l’arôme du lait (Gordon et Morgan, 1973).
2.3.7 Alcools
Les alcools primaires peuvent être formés par la réduction de leurs aldéhydes respectifs et sont présents en faibles quantités dans le lait (Moio et al., 1993). Dans des conditions normales, la contribution des alcools à la flaveur du lait est donc généralement négligeable (Forss, 1979). Dans l’étude de Gaspardo et al. (2009), les chercheurs ont évalué la fraction de composés volatils retrouvés dans le lait et la concentration en alcool y était faible. Les composés les plus abondants étaient le 1-propanol, l’éthanol et le méthanol (Gaspardo et al., 2009).
Il est connu que les ensilages n’ayant pas bien fermenté peuvent transmettre des flaveurs indésirables dans le lait. Des problèmes de flaveurs associés aux aliments ingérés par les animaux ont également été détectés dans le lait de troupeaux ayant apparemment consommé des ensilages d’herbes de bonne qualité. En ce sens, Gordon et Morgan (1972) ont identifiés l’éthanol comme un des principaux composés volatils dans le lait ‘teinté ’ par l’alimentation des animaux. Randby et al. (1999) ont vérifié si l’ajout d’éthanol pur à la ration, soit dans l’ensilage, pouvait influencer la composition et la flaveur du lait. Les concentrations utilisées dans cette étude représentaient des proportions qu’il est possible de retrouver dans des ensilages bien fermentés, soient 600 g/jour. Un maximum de 0,2 à 0,3 % de l’éthanol ingéré s’est retrouvé dans le lait (Randby et al., 1999). Cette teneur, avec une concentration maximale de 180 mg/kg dans le lait, ne peut toutefois pas expliquer à elle seule la flaveur indésirable associée à ce lait. Il faut considérer la contribution de l’éthanol, mais également celle des produits de son métabolisme. Par exemple, la concentration d’acétone dans le lait peut doubler lorsqu’il y a ingestion d’éthanol. Dans cette étude, on rapporte que les changements observés dans la composition du lait suite à l’ingestion d’éthanol sont similaires à ceux observés lorsque l’animal fait de l’acétonémie (c.-à-d. augmentation de la concentration en gras, en acétone et en acides gras libres). Par contre, le processus physiologique et biochimique responsable de
17
l’apparition de flaveurs indésirables dans le lait lorsque les vaches ingèrent de l’éthanol ne sont pas encore bien compris (Randby et al., 1999).
Dans du lait cru issus de vaches recevant trois types de rations, Toso et al. (2002) ont identifié différents alcools. L’éthanol et le 3 methyl-1-butanol étaient les plus abondants. D’autres alcools, tels que l’éthanol, le 1-pentanol, le 1-octen-3-ol, le 1-octanol, le dodécanol, le tétradécanol et le pentanol, ont été identifiés dans du lait pasteurisé (Toso et al., 2002).
2.3.8 Terpènes
Les terpènes sont un vaste groupe de métabolites secondaires des plantes, dérivant d’unités isoprènes (C5) (Kalač, 2011). Les monoterpènes (C10), les sesquiterpènes (C15) et les caroténoïdes (C40) passent facilement des fourrages au lait avec seulement quelques altérations mineures (Kalač, 2011). Les terpènes sont retrouvés en plus grande quantité dans le lait d’animaux ayant ingéré des fourrages riches en dicotylédones plutôt que des fourrages riches en graminées (Bugau et al., 2001) ou une ration à base de concentrés (Moio et al., 1996).
Certains auteurs, principalement français, ont donc proposé d’utiliser les terpènes comme marqueurs afin de retracer les laits associés à différentes régions et par le fait même, différents types de pâturages. La concentration en terpènes dans les fourrages dépend principalement de leur composition botanique (Martin et al., 2005). Par exemple, les fourrages riches en graminées sont pauvres en terpènes alors que les fourrages provenant de pâturages de hautes altitudes et comprenant plusieurs espèces de dicotylédones ont une teneur en terpènes plus élevée (Mariaca et al., 1997; Bugaud et al., 2001). La concentration en terpènes augmenterait avec la maturité des fourrages et elle diminuerait au cours de la récolte et de l’entreposage (Martin et al., 2005).
Dubroeucq et al. (2002) ont comparés des laits issus de différentes rations et malgré qu’un passage des terpènes des plantes au lait fût observé, la concentration en terpène dans le lait était relativement très faible (7-10 %). Le fourrage utilisé contenait de nombreuses espèces riches en terpènes, mais ces plantes ont été servies sous forme séchée et le séchage des plantes serait à l’origine d’une volatilisation importante des terpènes.
2.4. Impacts des traitements thermiques sur les composés volatils retrouvés dans le lait
Initialement, lorsque les chercheurs ont étudié la flaveur du lait, ce fût pour identifier les composés chimiques responsables de flaveurs indésirables (‘oxydés’ ou ‘rances’) pouvant parfois être présentes (Marsili, 2003). La provenance de plusieurs composés volatils responsables de flaveurs indésirables a d’ailleurs été élucidée. Des défauts de qualité peuvent se former suite à l’exposition du lait à de la lumière provenant des fluorescents dans les supermarchés, et ce, même s’il se trouve à l’intérieur de bouteilles de polyéthylène de densité élevée (Marsili, 2003). Le lait est alors plus vulnérable à la formation de flaveurs indésirables que l’on dit ‘induites par la lumière’ (Marsili, 2003). Ce processus serait divisé en deux étapes. En premier lieu, la dégradation d’acides aminés soufrés provenant des protéines du lactosérum donnerait un goût de brûlé au lait dans les premiers jours (Marsili, 2003). Après deux jours passés sur les tablettes, un goût de métal ou de carton se développerait et resterait dans le lait (Marsili, 2003). Ce goût serait associé à la formation d’aldéhydes (surtout le pentanal et l’hexanal), d’alcools, d’hydrocarbures et de cétones (1-hexen-3-one et 1-n(1-hexen-3-onen-3-(1-hexen-3-one) lors de réactions d’oxydation des lipides (Marsili, 2003). Le matériel d’emballage peut aussi être directement responsable de la formation de flaveurs indésirables dans le lait. Par ailleurs, comme le lait est un excellent milieu de croissance pour les microorganismes, certaines flaveurs indésirables peuvent aussi apparaître suite à une contamination post-pasteurisation par des bactéries psychotropes (Marsili, 2003).
19
La flaveur du lait peut donc être influencée par l’alimentation ou le métabolisme de la vache, ainsi que par des microorganismes et leurs enzymes durant l’entreposage. Or, la flaveur du lait peut également être modifiée lors des traitements thermiques (Calvo et de la Hoz, 1992). L’intensité de la flaveur ainsi produite dépend de l’intensité du traitement appliqué, incluant la température atteinte, la durée du traitement et la méthode de chauffage.
Une étude récente indique que la pasteurisation peut modifier la flaveur du lait en lui donnant un goût de ‘cuit’ ou de ‘chauffé’, surtout lorsque le produit vient tout juste de subir le traitement (Alvarez, 2009). L’intensité de cette flaveur indésirable diminuerait durant l’entreposage (Alvarez, 2009).
L’étude de Bendall (2001), dans laquelle on a identifié une soixantaine de composés volatils, a été réalisée sur du lait ayant été préalablement pasteurisé. Au contraire, Hettinga et al. (2007) ont analysé du lait n’ayant subi aucun traitement. Des laits crus de vaches ayant reçu différentes rations à base d’ensilage (55 %) et de concentrés (45 %) et sans défaut de qualité ont été analysés et on a retrouvé systématiquement sept composés volatils (Hettinga et al., 2007).
Les composés aromatiques formés lors de traitements thermiques peuvent provenir des protéines du lait (Calvo et de la Hoz, 1992). Dans l’étude de Calvo et de la Hoz (1992), les auteurs expliquent que les composés aromatiques peuvent être formés à partir du relâchement de composés sulfhydriles durant la dénaturation des protéines du lactosérum ou des protéines contenues dans la membrane des globules de gras. C’est ce qui permettrait de former différents composés soufrés. Toutefois, les auteurs mentionnent que la concentration en certains composés soufrés se verrait diminuer lorsque l’intensité des traitements thermiques appliqués serait trop grande. Le lactose, le glucose et le galactose peuvent aussi être précurseurs de composés aromatiques durant les traitements thermiques, entre autres par le biais d’interactions avec des acides aminés et autres composés azotés lors de la réaction de Maillard. L’application de traitements thermiques peut également conduire à la formation de composés à partir des lipides. Par exemple, dans les laits chauffés, des
méthyl-cétones, des lactones et des aldéhydes sont formés à partir du gras du lait (Calvo et de la Hoz, 1992).
Outre le procédé utilisé, la température à laquelle est réalisé le traitement peut aussi avoir un impact. Gandy et al. (2008) ont réalisé une étude dans le but de cibler les effets de différentes températures de pasteurisation sur les caractéristiques sensorielles, les composés volatils et la durée de vie du lait. Ils ont utilisé du lait standardisé à 2 % et pasteurisé à 77, 79, 82 et 85 ºC. Une analyse en composante principale a permis d’établir des liens entre la présence de certains composés volatils et la température de chauffage (figure 1). On a aussi analysé l’effet des jours passés après la pasteurisation sur les composés volatils présents dans le lait.
Les résultats indiquent que 37,5 % de la variation est expliquée par la composante 1 (horizontale) alors que 18,2 % de la variation est expliquée par la composante 2 (verticale). Le jour de la pasteurisation, soit le jour 0 (d0 dans la figure), le traitement à 77°C (77d0) était hautement corrélé avec la présence d’hydroxylamine, de phénol et d’acide butanoïque dans le lait alors que sept jours après le traitement, il était davantage relié à celle du limonène, de l’heptanol et du nonane (Gandy et al., 2008). D’autres molécules étaient associées aux autres traitements, mais l’élément principal qui ressort de cette analyse est que les échantillons de lait peuvent être facilement différenciés, à partir de leurs composés volatils, surtout aux jours 0 et 7 (Gandy et al., 2008). Beaucoup moins de composés volatils étaient présents dans le lait 10 et 13 jours après la pasteurisation. Cela implique que les composés volatils qui se développent après les traitements de pasteurisation se dégradent par la suite.
21
Figure 2.1. Analyse en composantes principales des composés volatils retrouvés dans du lait pasteurisé à différentes températures (77, 79, 82 et 85°C) et analysés aux jours 0, 7, 10 et 13 après la pasteurisation (Source : Gandy et al., 2008).
Dans des laits ayant subi un traitement thermique, les composés soufrés tels que le sulfure d’hydrogène, le méthanethiol, le disulfure de carbone, le sulfure de diméthyle, le disulfure de diméthyle et le trisulfure de diméthyle seraient libérés des groupes sulfhydriles des protéines du lactosérum, principalement de la β-lactoglobuline, et seraient responsables de la flaveur ‘cuite’ (Simon et Hansen, 2001). Pourtant, dans l’étude de Pereda (2007) où on a analysé des laits ayant subi une homogénéisation à ultra-haute pression ou une pasteurisation à haute température, on a seulement identifié le sulfure de diméthyle. Cela pourrait être dû à la méthode d’extraction utilisée, la micro-extraction en phase solide (SPME), qui ne serait pas assez sensible pour permettre l’identification de composés soufrés à de très faibles concentrations (Pereda, 2007). De récents travaux, réalisés par Havemose et al. (2007), ont montré que la SPME serait une méthode appropriée pour étudier les modifications d’oxydation dans lait, mais qu’elle ne serait pas assez sensible pour détecter des composés présents à faible concentration tels que les composés soufrés. Nous y reviendrons dans la section sur les techniques d’analyse.
Il est également possible que d’autres procédés de transformation aient un impact sur le profil des composés volatils du lait. En effet, après une homogénéisation sans pasteurisation, les lipases naturelles du lait causent une lipolyse dans le lait cru et libèrent ainsi des acides gras libres (Hettinga et al., 2007). Ces derniers vont ensuite former des aldéhydes et des cétones (Hettinga et al., 2007).
2.5. Impact des méthodes d’analyses sur les composés volatils retrouvés dans le lait
L’analyse des flaveurs des produits laitiers exige plusieurs étapes afin de pouvoir identifier des centaines de composés aromatiques ayant différentes volatilités, polarités et concentrations (McGorrin, 2007). La méthodologie employée pour analyser les composés volatils qui se retrouvent dans le lait est un élément important à prendre en considération lorsqu’on compare des données. En effet, il existe plusieurs méthodes pour extraire et analyser les composés aromatiques et il est
23
primordial d’en tenir compte puisqu’elles ne sont pas toutes aussi performantes les unes que les autres, et sont utilisées pour divers substrats.
L’analyse des composés volatils retrouvés dans les produits laitiers comprend une étape d’isolation ou d’extraction, suivie d’une étape d’identification chimique (McGorrin, 2007). Les composés extraits sont séparés dans une colonne capillaire avec une phase gazeuse et l’identification se fait généralement à l’aide de la chromatographie en phase gazeuse et de la spectrométrie de masse (GC-MS). L’étape de préparation des échantillons pour isoler les composés volatils du lait est probablement la plus difficile du processus d’analyse.
2.5.1 Méthodes d’extraction
Des teneurs importantes en lipides, protéines et glucides dans le lait rendent difficiles la séparation des composés aromatiques si l’on se base uniquement sur les propriétés générales telles que la polarité ou la volatilité (Friedrich et Acree, 1998). Il existe différentes méthodes pour isoler les composés des produits laitiers telles que la distillation sous vide (‘high vacuum distillation’), l’extraction à l’aide de solvant (‘solvent extraction’), l’échantillonnage ‘headspace’ en équilibre (‘static headspace’), l’échantillonnage ‘headspace’ dynamique (‘dynamic headspace sampling’ ou ‘purge and trap’) ou la microextraction en phase solide (‘solid-phase microextraction, SPME’) (McGorrin, 2007). Un échantillonnage par ‘dynamic headspace’ peut prendre environ une à deux heures, ce qui représente un temps d’analyse relativement long (Pillonel et al., 2001). La SPME s’avère être une méthode de choix pour sa rapidité, son faible coût, sa facilité d’utilisation et son automatisme (Pillonel et al., 2001).
2.5.1.1 La micro-extraction en phase solide (SPME)
Avec les méthodes conventionnelles, des composés peuvent être perdus durant les étapes d’extraction et de concentration (Stashenko et Martinez, 2007). La SPME est une technique
relativement récente développée pour l’isolation et la concentration des composés volatils, semi-volatils ou non semi-volatils des aliments (McGorrin, 2007).Cette méthode combine l’échantillonnage des composés volatils, leur extraction, leur concentration et leur injection pour la chromatographie en une seule technique. C’est à l’aide d’une fibre que sont absorbés et concentrés les composés volatils (McGorrin, 2007).
Le premier dispositif de SPME a été développé par Arthur et Pawliszyn (1990) en guise de technique de préconcentration pour l’analyse des polluants dans l’eau. Dans les dernières années, la SPME est devenue une méthode populaire et son utilisation s’est répandue à divers secteurs d’études. La SPME peut être effectuée dans un mode d’extraction direct (immersion de la fibre) ou via une configuration ‘headspace’ (HS/SPME) (Pillonel et al., 2001). Dans le premier cas, la fibre est plongée directement dans l’échantillon d’où les composés seront extraits (Pillonel et al., 2001). Dans le mode HS/SPME, les composés à analyser doivent d’abord diffusés de la matrice vers l’air puis de l’air jusqu’au revêtement de la fibre (Pillonel et al., 2001). Dans le cas d’analyses de composés volatils provenant de matrices complexes telles que les aliments, il est préférable d’utiliser la méthode HS/SPME étant donné le plus grand risque d’endommager la fibre. D’ailleurs la HS/SPME est la méthode la plus couramment utilisée notamment pour sa haute sélectivité et parce que l’absence de contact avec l’échantillon prévient la contamination et/ou la décomposition du revêtement de la fibre (Stashenko et Martinez, 2007). Elle est également considérée comme la technique idéale pour l’analyse d’échantillons biologiques puisqu’elle réduit les interférences avec les composés volatils ayant une masse moléculaire importante telles que les protéines, ce qui permet d’obtenir des extraits plus ‘propres’ (Mounchili et al., 2005).
Il est possible d’améliorer la cinétique de l’extraction en agitant et/ou en augmentant la température d’extraction. Par contre, élever la température d’échantillonnage peut aussi diminuer la quantité de composés extraits (Pillonel et al., 2001). Il est important que la procédure d’isolation employée donne un produit représentatif de l’échantillon que l’on souhaite analyser. C’est pourquoi le choix d’une méthode de préparation des échantillons appropriée est primordial.
25 2.5.1.1.1 Types de fibre
Afin de réaliser la SPME, plusieurs fibres composées de différentes épaisseurs de films et de matériel de revêtement peuvent être utilisées. La fibre utilisée aura un impact sur la sélectivité des composés lors de l’extraction. Lors du choix de la fibre, il faut tenir compte de la polarité, de la volatilité et du poids moléculaire des composés analysés (McGorrin, 2007).
Selon Pillonel et al. (2001) les revêtements de fibres peuvent être classés en deux groupes :
- ceux comprenant une seule couche de polymères liquides purs (polydimethylsiloxane (PDMS) ou polyacrylate (PA)),
- ceux qui contiennent un film mixte de polymères liquides et de particules solides (Carboxen-PDMS, Divinylbenzene (DVB)-(Carboxen-PDMS, Carbowax-DVB et DVB-carboxen-PDMS).
Voici une brève description ainsi que les particularités de chacune de ces fibres.
1- PDMS : Ce revêtement de fibre est fortement hydrophobe et non-polaire. Il a été développé à l’origine pour extraire les polluants d’échantillons liquides (Pillonel et al., 2001). La fibre est de type absorbant et a une forte capacité pour cloisonner les composés volatils à partir d’une phase liquide, et elle est plus appropriée pour les substances à analyser non polaires (McGorrin, 2007). La fibre est très sensible aux composés non-polaires et insensible aux composés polaires (Stashenko et Martinez, 2007).
2- PA : Le revêtement est plus polaire que le PDMS (Pillonel et al., 2001). Il est utilisé pour l’extraction de composés polaires tels que les acides gras et les composés soufrés réduits (Pillonel et al., 2001).
3- Car/PDMS : Le carboxen est un revêtement constitué de molécule de carbone avec des macro, meso et micropores. Il est généralement utilisé en combinaison avec le PDMS, améliorant alors l’extraction des petites molécules (Pillonel et al., 2001).
4-DVB-PDMS : Le DVB contient de plus grands pores que le carboxen et est donc plus adapté pour l’extraction de plus grosses molécules (Müller et al., 1997). Pour certaines applications dans des produits laitiers, ces fibres seraient capables d’extraire des composés volatils ayant un point d’ébullition élevé (McGorrin, 2007).
5- DVB/Carboxen/PDMS : Le carboxen permet de capter les petites molécules et le DVB, les plus grosses. La désorption est aussi facilitée avec cette configuration. Ces fibres sont toutefois difficiles à produire et sont parfois livrées avec des défauts (fissures dans le revêtement). Pour certaines applications dans des produits laitiers, elles seraient capables d’extraire des composés volatils à point d’ébullition élevé (McGorrin, 2007).
6- Carbowax/DVB : Il s’agit de la fibre la plus polaire du groupe de films mixtes.
La polarité de la fibre aurait seulement un effet minimal sur l’extraction de molécules à faible poids moléculaire alors que la porosité et l’épaisseur du film auraient une plus grande influence sur l’extraction des petites molécules (Pillonel et al., 2001).
27 2.5.1.1.2 Conditions d’échantillonnage
À température ambiante, les techniques d’immersion et le ‘headspace’ sont meilleurs pour les composés non polaires alors que les mêmes techniques, utilisées avec un chauffage, sont les plus appropriées pour extraire les composés polaires (Pillonel et al., 2001).
L’ajout de sel dans les échantillons à analyser pourrait augmenter la teneur en composés extraits, peu importe si il s’agit du mode immersion ou du ‘headspace’ (Pillonel et al., 2001). Il y a quatre types de comportements observés suite à l’ajout de sel :
l’extraction augmente avec l’augmentation de la concentration de sel;
l’extraction augmente initialement et cesse d’augmenter à une certaine concentration de sel; l’extraction augmente initialement et décroit avec l’augmentation de la concentration de sel; l’extraction diminue avec l’augmentation de la concentration en sel.
En général, on peut dire que l’ajout de sel améliore considérablement le taux d’extraction des composés polaires comme l’isopropylamine, l’isopropanol, l’acide carboxylique et les phénols (Pillonel et al., 2001). L’effet serait beaucoup plus faible pour les molécules moins polaires telles que le benzène, toluène, éthylbenzène et xylène. Il y aurait d’autres applications pour l’acétaldéhyde, les terpénoïdes, les amines aromatiques et les produits de la réaction de Maillard (Pillonel et al., 2001).
2.5.1.1.3 Reproductibilité
La méthode SPME est simple et requiert peu de matériel (échantillon). Elle est peu coûteuse, sélective et sensible (Stashenko et Martinez, 2007). Mentionnons que la détérioration rapide du revêtement de la fibre nécessite de prendre certaines précautions (utilisation de standards) pour les études à long terme (Pillonel et al., 2001). Certains facteurs tels que la température de l’échantillon (40-50 degrés C), le temps d’exposition de la fibre (5-30 min) et le ratio du volume de l’échantillon par rapport au volume d’headspace dans le flacon peuvent aussi influencer la sensibilité ainsi que la reproductibilité de l’isolation des composés volatils (McGorrin, 2007). L’agitation à l’aide d’une barre magnétique peut aussi avoir un impact en accélérant le transfert des composés volatils de l’échantillon à la fibre (McGorrin, 2007).
2.5.1.1.4 Méthode de quantification et d’identification
Le développement de la chromatographie en phase gazeuse a permis aux chimistes de séparer, quantifier et identifier les composés qui constituent les odeurs (Delahunty et al., 2006). Généralement, le chromatographe est jumelé à un détecteur, soit un spectromètre de masse ou à un détecteur à ionisation de flamme, afin d’identifier les composés (Delahunty et al., 2006).
Pour être détecté par une chromatographie en phase gazeuse jumelée à la spectrométrie de masse (GC-MS), les composés aromatiques doivent être présents dans l’aliment à une concentration égale ou supérieure à 10-5 g/L (Friedrich et Acree (1998). Se basant sur leurs connaissances en chimie des arômes, Friedrich et Acree (1998) mentionnent que seulement une petite fraction des composés volatils présents dans les aliments joue un rôle significatif dans la perception de l’odeur globale.
29
Or, savoir si un composé est présent à une concentration donnée ou non ne permet pas de conclure qu’il est perceptible (Delahunty et al., 2006). C’est pourquoi certains laboratoires utilisent la chromatographie en phase gazeuse jumelée à un olfactomètre (GC -O). Dans ce cas, c’est le système olfactif humain qui permet l’identification des odeurs via un dispositif installé sur le GC.
2.5.1.2 La chromatographie en phase gazeuse jumelée à un olfactomètre (GC-O)
La perception de composés volatils par le nez de l’humain dépend de la libération des composés de leur matrice (ex : le lait) et des propriétés odorantes du mélange de composés (d’Acampora et al., 2007). Seulement une petite proportion du grand nombre de composés volatils retrouvés au sein d’une matrice va contribuer à la flaveur globale (Van Ruth, 2001; d’Acampora et al., 2007). De plus, ces molécules ne contribuent pas de manière équivalente à la flaveur globale d’un échantillon. Il existe une différence importante entre la concentration et l’intensité aromatique d’un composé (d’Acampora et al., 2007). C’est ce qui a amené les chercheurs à se pencher sur la question de la détermination de la contribution de chaque constituant sur la flaveur globale d’un produit (d’Acampora et al., 2007). Globalement, l’importance sensorielle d’un composé dans le lait peut se résumer par la concentration à laquelle on le retrouve et des limites de détection du nez humain (d’Acampora et al., 2007). Parallèlement, il faut tenir compte des interactions imprévisibles entre les molécules odorantes et les autres constituants du lait tels que les lipides, les protéines, les glucides, et les minéraux (d’Acampora et al., 2007). La GC-O s’avère donc être l’outil approprié puisqu’elle procure une analyse instrumentale jumelée à une analyse sensorielle (d’Acampora et al., 2007).
La description du premier chromatographe couplé à un olfactomètre afin de ‘renifler ’ les ‘effluents ’ pour déterminer l’activité volatile des odeurs fût publiée en 1964 par Fuller et al. (d’Acampora et al., 2007). Le but de la GC-O est de déterminer l’activité odorante des composés volatils se trouvant dans un échantillon et d’attribuer une importance relative à chacun d’entre eux (Delahunty et al., 2006). Ainsi, pour chaque composé séparé qui arrive du GC, l’évaluateur peut détecter le composé,