Université de Lille
Année Universitaire 2018/2019
Faculté de Pharmacie de Lille
MEMOIRE
POUR LE DIPLOME D'ETUDES SPECIALISEES DE PHARMACIE
Soutenu publiquement le 27 septembre 2019 Par M. DUBREUCQ Vincent
Conformément aux dispositions réglementaires en vigueur tient lieu de
THESE EN VUE DU DIPLOME D’ETAT DE DOCTEUR EN PHARMACIE _____________________________
Harmonisation de l'utilisation des solutions verrous à base d'urokinase en hémodialyse au sein du GHT de l'Artois.
_____________________________ Membres du jury :
Président : Monsieur le Professeur Nicolas SIMON Professeur des Universités
Faculté de Pharmacie - Université de Lille
Pharmacien, Praticien Hospitalier - Centre Hospitalier Universitaire de Lille
Assesseurs :
Monsieur le Docteur Bruno FRIMAT
Maître de Conférences Associé en Pharmacie Clinique Faculté de Pharmacie - Université de Lille
Pharmacien, Praticien Hospitalier - Centre Hospitalier de Lens
Monsieur le Docteur Aurélien MARY Maître de Conférences des Universités
UFR de Pharmacie - Université de Picardie Jules Verne
Pharmacien, Praticien Hospitalier - Centre Hospitalier Universitaire Amiens Picardie
Monsieur le Docteur Linh BUI
Université de Lille Faculté de Pharmacie de Lille Année Universitaire 2018/2019
MEMOIRE
POUR LE DIPLOME D'ETUDES SPECIALISEES DE PHARMACIE
Soutenu publiquement le 27 septembre 2019 Par M. DUBREUCQ Vincent
Conformément aux dispositions réglementaires en vigueur tient lieu de
THESE EN VUE DU DIPLOME D’ETAT DE DOCTEUR EN PHARMACIE _____________________________
Harmonisation de l'utilisation des solutions verrous à base d'urokinase en hémodialyse au sein du GHT de l'Artois.
_____________________________ Membres du jury :
Président : Monsieur le Professeur Nicolas SIMON Professeur des Universités
Faculté de Pharmacie - Université de Lille
Pharmacien, Praticien Hospitalier - Centre Hospitalier Universitaire de Lille
Assesseur(s) :
Monsieur le Docteur Bruno FRIMAT
Maître de Conférences Associé en Pharmacie Clinique Faculté de Pharmacie - Université de Lille
Pharmacien, Praticien Hospitalier - Centre Hospitalier de Lens
Monsieur le Docteur Aurélien MARY Maître de Conférences des Universités
UFR de Pharmacie - Université de Picardie Jules Verne
Pharmacien, Praticien Hospitalier - Centre Hospitalier Universitaire Amiens Picardie
Monsieur le Docteur Linh BUI
Université de Lille
Président : Jean-Christophe CAMART
Premier Vice-président : Damien CUNY
Vice-présidente Formation : Lynne FRANJIÉ
Vice-président Recherche : Lionel MONTAGNE
Vice-président Relations Internationales : François-Olivier SEYS Directeur Général des Services : Pierre-Marie ROBERT Directrice Générale des Services Adjointe : Marie-Dominique SAVINA
Faculté de Pharmacie
Doyen : Bertrand DÉCAUDIN
Vice-Doyen et Assesseur à la Recherche : Patricia MELNYK Assesseur aux Relations Internationales : : Philippe CHAVATTE Assesseur à la Vie de la Faculté et aux
Relations avec le Monde Professionnel : Thomas MORGENROTH Assesseur à la Pédagogie : Benjamin BERTIN
Assesseur à la Scolarité : Christophe BOCHU
Responsable des Services : Cyrille PORTA
Liste des Professeurs des Universités - Praticiens Hospitaliers
Civ. NOM Prénom Laboratoire
Mme ALLORGE Delphine Toxicologie
M. BROUSSEAU Thierry Biochimie
M. DÉCAUDIN Bertrand Pharmacie Galénique
M. DEPREUX Patrick ICPAL
M. DINE Thierry Pharmacie clinique
Mme DUPONT-PRADO Annabelle Hématologie
M. GRESSIER Bernard Pharmacologie
M. LUYCKX Michel Pharmacie clinique
M. ODOU Pascal Pharmacie Galénique
M. STAELS Bart Biologie Cellulaire
Faculté de Pharmacie de Lille
3, rue du Professeur Laguesse - B.P. 83 - 59006 LILLE CEDEX ( 03.20.96.40.40 - ! : 03.20.96.43.64
Liste des Professeurs des Universités
Civ. NOM Prénom Laboratoire
M. ALIOUAT El Moukhtar Parasitologie
Mme AZAROUAL Nathalie Physique
M. BERTHELOT Pascal Onco et Neurochimie
M. CAZIN Jean-Louis Pharmacologie – Pharmacie clinique
M. CHAVATTE Philippe ICPAL
M. COURTECUISSE Régis Sciences végétales et fongiques
M. CUNY Damien Sciences végétales et fongiques
Mme DELBAERE Stéphanie Physique
M. DEPREZ Benoît Lab. de Médicaments et Molécules
Mme DEPREZ Rebecca Lab. de Médicaments et Molécules
M. DUPONT Frédéric Sciences végétales et fongiques
M. DURIEZ Patrick Physiologie
M. FOLIGNE Benoît Bactériologie
M. GARÇON Guillaume Toxicologie
Mme GAYOT Anne Pharmacotechnie Industrielle
M. GOOSSENS Jean François Chimie Analytique
M. HENNEBELLE Thierry Pharmacognosie
M. LEMDANI Mohamed Biomathématiques
Mme LESTAVEL Sophie Biologie Cellulaire
M. LUC Gerald Physiologie
Mme MELNYK Patricia Onco et Neurochimie
M. MILLET Régis ICPAL
Mme MUHR – TAILLEUX Anne Biochimie
Mme PAUMELLE-LESTRELIN Réjane Biologie Cellulaire
Mme PERROY Anne Catherine Législation
Mme ROMOND Marie Bénédicte Bactériologie
Mme SAHPAZ Sevser Pharmacognosie
M. SERGHERAERT Eric Législation
Mme SIEPMANN Florence Pharmacotechnie Industrielle
M. SIEPMANN Juergen Pharmacotechnie Industrielle
M. WILLAND Nicolas Lab. de Médicaments et Molécules
Liste des Maîtres de Conférences - Praticiens Hospitaliers
Civ. NOM Prénom Laboratoire
Mme BALDUYCK Malika Biochimie
Mme GARAT Anne Toxicologie
Mme GOFFARD Anne Bactériologie
M. LANNOY Damien Pharmacie Galénique
Mme ODOU Marie Françoise Bactériologie
Liste des Maîtres de Conférences
Civ. NOM Prénom Laboratoire
Mme ALIOUAT Cécile Marie Parasitologie
M. ANTHERIEU Sébastien Toxicologie
Mme AUMERCIER Pierrette Biochimie
Mme BANTUBUNGI Kadiombo Biologie cellulaire
Mme BARTHELEMY Christine Pharmacie Galénique
Mme BEHRA Josette Bactériologie
M BELARBI Karim Pharmacologie
M. BERTHET Jérôme Physique
M. BERTIN Benjamin Immunologie
M. BLANCHEMAIN Nicolas Pharmacotechnie industrielle
M. BOCHU Christophe Physique
M. BORDAGE Simon Pharmacognosie
M. BOSC Damien Lab. de Médicaments et Molécules
M. BRIAND Olivier Biochimie
M. CARNOY Christophe Immunologie
Mme CARON Sandrine Biologie cellulaire
Mme CHABÉ Magali Parasitologie
Mme CHARTON Julie Lab. de Médicaments et Molécules
M CHEVALIER Dany Toxicologie
M. COCHELARD Dominique Biomathématiques
Mme DANEL Cécile Chimie Analytique
Mme DEMANCHE Christine Parasitologie
Mme DEMARQUILLY Catherine Biomathématiques
M. DHIFLI Wajdi Biomathématiques
Mme DUMONT Julie Biologie cellulaire
Mme DUTOUT-AGOURIDAS Laurence Onco et Neurochimie
M. EL BAKALI Jamal Onco et Neurochimie
M. FARCE Amaury ICPAL
Mme FLIPO Marion Lab. de Médicaments et Molécules
Mme FOULON Catherine Chimie Analytique
M. FURMAN Christophe ICPAL
Mme GENAY Stéphanie Pharmacie Galénique
M. GERVOIS Philippe Biochimie
Mme GOOSSENS Laurence ICPAL
Mme GRAVE Béatrice Toxicologie
Mme GROSS Barbara Biochimie
M. HAMONIER Julien Biomathématiques
Mme HAMOUDI Chérifa Mounira Pharmacotechnie industrielle
Mme HANNOTHIAUX Marie-Hélène Toxicologie
Mme HELLEBOID Audrey Physiologie
M. HERMANN Emmanuel Immunologie
M. KAMBIA Kpakpaga Nicolas Pharmacologie
M. KARROUT Youness Pharmacotechnie Industrielle
Mme LALLOYER Fanny Biochimie
M. LEBEGUE Nicolas Onco et Neurochimie
Mme LECOEUR Marie Chimie Analytique
Mme LEHMANN Hélène Législation
Mme LELEU-CHAVAIN Natascha ICPAL
Mme LIPKA Emmanuelle Chimie Analytique
Mme MARTIN Françoise Physiologie
M. MOREAU Pierre Arthur Sciences végétales et fongiques
Mme MUSCHERT Susanne Pharmacotechnie industrielle
Mme NIKASINOVIC Lydia Toxicologie
Mme PINÇON Claire Biomathématiques
M. PIVA Frank Biochimie
Mme PLATEL Anne Toxicologie
M. POURCET Benoît Biochimie
M. RAVAUX Pierre Biomathématiques
Mme RAVEZ Séverine Onco et Neurochimie
Mme RIVIERE Céline Pharmacognosie
Mme ROGER Nadine Immunologie
M. ROUMY Vincent Pharmacognosie
Mme SEBTI Yasmine Biochimie
Mme SINGER Elisabeth Bactériologie
Mme STANDAERT Annie Parasitologie
M. TAGZIRT Madjid Hématologie
M. VILLEMAGNE Baptiste Lab. de Médicaments et Molécules
M. WELTI Stéphane Sciences végétales et fongiques
M. YOUS Saïd Onco et Neurochimie
M. ZITOUNI Djamel Biomathématiques
Professeurs Certifiés
Civ. NOM Prénom Laboratoire
M. HUGES Dominique Anglais
Mlle FAUQUANT Soline Anglais
M. OSTYN Gaël Anglais
Professeur Associé - mi-temps
Civ. NOM Prénom Laboratoire
M. DAO PHAN Hai Pascal Lab. Médicaments et Molécules
M. DHANANI Alban Droit et Economie Pharmaceutique
Maîtres de Conférences ASSOCIES - mi-temps
Civ. NOM Prénom Laboratoire
M. BRICOTEAU Didier Biomathématiques
Mme CUCCHI Malgorzata Biomathématiques
M. FRIMAT Bruno Pharmacie Clinique
M. GILLOT François Droit et Economie pharmaceutique
M. MASCAUT Daniel Pharmacie Clinique
M. ZANETTI Sébastien Biomathématiques
AHU
Civ. NOM Prénom Laboratoire
Mme DEMARET Julie Immunologie
Mme HENRY Héloïse Biopharmacie
Faculté de Pharmacie de Lille
3, rue du Professeur Laguesse - B.P. 83 - 59006 LILLE CEDEXTel. : 03.20.96.40.40 - Télécopie : 03.20.96.43.64 http://pharmacie.univ-lille2.fr
L’Université n’entend donner aucune approbation aux opinions
émises dans les thèses ; celles-ci sont propres à leurs auteurs.
TABLE DES MATIERES
TABLE DES MATIERES ... 7
REMERCIEMENTS ... 8
LISTE DES ABBREVIATIONS ... 10
LISTE DES FIGURES ... 11
LISTE DES TABLEAUX ... 12
INTRODUCTION ... 13
1) Généralités, contexte et objectifs ... 14
1.1 Généralités ... 14
1.1.1 Insuffisance rénale et hémodialyse ... 14
1.1.2 Différentes voies d'abord vasculaires ... 15
1.1.2.1 FAV ... 16
1.1.2.2 PAV ... 17
1.1.2.3 CVC ... 17
1.1.3 Complications et dysfonctionnements liés au cathéter ... 18
1.1.4 Solutions verrous ... 19 1.1.4.1 L'héparine sodique ... 19 1.1.4.2 Le citrate de sodium ... 20 1.1.4.3 La taurolidine ... 20 1.1.4.4 L'urokinase ... 21 1.1.4.4 L'altéplase ... 21 1.2 Contexte ... 21
1.2.1 Hémodialyse dans le GHT de l'Artois ... 21
1.2.2 Répartition des consommations des solutions verrous en 2018 ... 22
1.2.3 Pratiques de prescriptions des solutions verrous dans le GHT de l'Artois ... 24
1.3 Objectifs de l'étude ... 25
2) Matériel et Méthode ... 26
2.1 Mise en place de l'étude ... 26
2.2 Critères d'inclusion ... 26
2.3 Critères d'évaluation ... 27
2.4 Recueil des données ... 28
2.5 Analyse des données ... 29
3) Résultats ... 30
3.1 Description de la population de l'étude ... 30
3.2 Description des caractéristiques de la population ... 30
3.3 Description des séances de dialyse ... 33
3.3.1 Nombre de séances ... 33
3.3.1.1 Description globale ... 33
3.3.1.2 Description par patient ... 34
3.3.2 Solutions verrous utilisées ... 34
3.3.2.1 Répartition globale ... 34
3.3.2.2 Répartition par patient ... 35
3.3.2.3 Schémas d’utilisation des solutions verrous ... 37
3.3.3 Efficacité des séances ... 38
3.3.4 Dysfonctionnements ... 40
4) Discussion ... 44
4.1 Description de la population de l'étude ... 44
4.2 Description des séances de dialyse ... 45
4.3 Elaboration d'un arbre décisionnel ... 49
4.4 Perspectives ... 54
CONCLUSION ... 55
BIBLIOGRAPHIE ... 56
REMERCIEMENTS
A Monsieur le Professeur Nicolas SIMON,
Je vous remercie de me faire l’honneur de présider ce jury et de juger ce travail. Veuillez trouver ici l'expression de mon profond respect et de toute ma considération.
A Monsieur le Docteur Bruno FRIMAT,
Je vous remercie de m'avoir fait l’honneur d'accepter de m'encadrer et de me confier ce travail. Merci pour votre professionnalisme, votre implication, votre soutien et vos précieux conseils. C'est un honneur sincère de pouvoir travailler à vos côtés.
A Monsieur le Docteur Aurélien MARY,
Je vous remercie de me faire l’honneur de juger ce travail.
Soyez assuré de ma reconnaissance et de mon profond respect.
A Monsieur le Docteur Linh BUI,
Je vous remercie d'avoir accepté de faire partie de ce jury. Merci pour votre implication dans ce travail et vos conseils.
Veuillez croire au témoignage de mon profond respect et de mes sincères remerciements.
A l'ensemble des pharmaciens et des équipes pharmaceutiques
lensoises,
Vous m'avez accueilli en tant qu'externe et transmis votre passion pour la pharmacie hospitalière, vous m'avez retrouvé et accompagné en tant qu'interne durant 4 semestres enrichissants sur tous les points, et je suis heureux de pouvoir désormais poursuivre mon chemin à vos côtés en tant que pharmacien.
Merci à tous pour votre aide, votre encadrement, vos précieux conseils et votre bonne humeur quotidienne.
A l'ensemble des pharmaciens rencontrés au cours de mon
internat,
Je vous remercie pour la transmission de vos connaissances et de vos conseils. Merci à tous pour ces bons moments partagés au cours de ces 4 années.
A ma famille,
A Alice,
Merci pour ton attention, ta présence, ton soutien et tes encouragements de tous les jours. Une nouvelle vie commence désormais pour nous : je suis heureux de pouvoir avancer à tes côtés.
A mes parents,
Merci de m'avoir soutenu quotidiennement et fait confiance tout au long de mes études. Merci d'avoir toujours cherché le meilleur pour ma réussite : je ne serais pas là aujourd'hui sans vous.
A Céline, François et Maël,
Merci pour votre présence, votre joie et vos rires: je suis heureux de partager tous ces bons moments avec vous.
A mes amis,
Merci à l'ensemble de mes co-internes (Aline, Clémence, Fanny, Gabrielle, Laurine, Lucie, Marie, Valentine, Edouard, Mathieu, Matthieu, William et tous les internes du CHU) pour ces moments d'entraide, d'amitié et de bonne humeur.
Merci à mes trois confrères d'officine, Anaïs, Léa et Julien, sans qui mes années d'étude n'auraient pas été si joyeuses et agréables.
LISTE DES ABBREVIATIONS
AIT : Accident Ischémique Transitoire AVC : Accident Vasculaire Cérébral
BPCO : Broncho-Pneumopathie Chronique Obstructive CDL : Centre de Dialyse du Lensois
CHB : Centre Hospitalier de Béthune CHL : Centre Hospitalier de Lens
COMEDIMS : Commission des Médicaments et des Dispositifs Médicaux Stériles. CVC : Cathéter Veineux Central
CVT : Cathéter Veineux Tunnelisé DFG : Débit de Filtration Glomérulaire
DIM : Département de l'Information Médicale
EHPAD : Etablissement d'Hébergement pour Personnes Agées Dépendantes EPO : Erythropoïétine
FAV : Fistule Artério-Veineuse
GCS : Groupement de Coopération Sanitaire GHT : Groupement Hospitalier de Territoire IDE : Infirmier Diplômé d'Etat
IMC : Indice de Masse Corporelle MCO : Médecine Chirurgie Obstétrique MRC : Maladie Rénale Chronique ND : Non Disponible
NYHA : New York Heart Association PAV : Pontage Artério-Veineux
REIN : Réseau Epidémiologie Information Néphrologie SAP : Seringue Auto-Pulsée
SAS : Syndrome d'Apnées du Sommeil SMR : Service Médical Rendu
TIH : Thrombopénie Induite par l'Héparine USLD : Unité de Soins Longue Durée
LISTE DES FIGURES
Figure n°1 : Représentation du circuit d'hémodialyse ... 15 Figure n°2 : Représentation d'une fistule artério-‐veineuse ... 16 Figure n°3 : Représentation schématique d'un Cathéter Veineux Central Tunnelisé par voie jugulaire interne droite ... 18 Figure n°4 : Répartition des consommations 2018 des solutions verrous en
hémodialyse au CHL et au CHB ... 23 Figure n°5 : Répartition des coûts 2018 des solutions verrous en hémodialyse au CHL et au CHB ... 23 Figure n°6 : Détail de la partie de l'arbre décisionnel de prescription des solutions verrous en l'absence de contre indication de l'héparine ... 50 Figure n°7 : Détail de la partie de l'arbre décisionnel de prescription des solutions verrous en cas de contre indication de l'héparine ... 52
LISTE DES TABLEAUX
Tableau n°1 : Répartition des capacités d'accueil des quatre établissements du GHT de l'Artois ... 22 Tableau n°2 : Répartition des consommations et des coûts des solutions verrous en hémodialyse au CHL et au CHB en 2018 ... 22 Tableau n°3 : Répartition des patients inclus dans l'étude selon la structure
d'origine ... 30 Tableau n°4 : Nombre de comorbidités cumulées par patient ... 30 Tableau n°5 : Description des éléments de caractérisation de la population en effectif et en pourcentage ... 32 Tableau n°6 : Description des variables quantitatives de la population de l'étude ... 33 Tableau n°7 : Répartition des séances d'hémodialyse étudiées dans l'étude selon leur hôpital de réalisation ... 33 Tableau n°8 : Description statistique du nombre de séances de dialyse par patient ... 34 Tableau n°9 : Nombre de séances de dialyse par patient ... 34 Tableau n°10 : Description en nombre et en pourcentage des séances de dialyse réalisées avec chaque solution verrou ... 35 Tableau n°11 : Description par patient du nombre de séances de dialyse réalisées avec chaque solution verrou ... 36 Tableau n°12 : Description des schémas d’utilisation des solutions verrous par patient ... 37 Tableau n°13 : Description des marqueurs d'efficacité de la séance n+1 en regard de la solution verrou utilisée lors de la séance n ... 38 Tableau n°14 : Description des marqueurs d'efficacité de la séance n+2 en regard de la solution verrou utilisée lors de la séance n ... 39 Tableau n°15 : Description des marqueurs d'efficacité de la séance n+3 en regard de la solution verrou utilisée lors de la séance n ... 40 Tableau n°16 : Description par patient des solutions verrous utilisées avant
dysfonctionnement ... 41 Tableau n°17 : Description des solutions verrous utilisées chez les patients sans survenue de dysfonctionnement ... 43
INTRODUCTION
La maladie rénale chronique, caractérisée par l'altération du fonctionnement des reins, nécessite une prise en charge au long cours, qui peut aboutir, à son stade terminal, à la mise en place d'un traitement de suppléance tel que l'hémodialyse. Ce terme regroupe l'ensemble des méthodes d'épuration du sang utilisant une circulation sanguine extra-corporelle. Un abord vasculaire fonctionnel étant nécessaire à la bonne épuration sanguine, le recours à un cathéter veineux central peut devenir indispensable. Pour éviter la survenue de complications liées à l'obstruction de cathéter, des solutions verrous anticoagulantes sont utilisées entre chaque séance de dialyse. Il n'existe pas de consensus bien établi sur les critères de choix des différents verrous. Entre empirisme médical et profils de patients très variés, une réelle hétérogénéité existe. Ce travail a pour but d'analyser les règles d'utilisation des différentes solutions verrous anticoagulantes au sein des deux services d'hémodialyse du Groupement Hospitalier de Territoire de l'Artois pour aboutir à une harmonisation et une sécurisation des pratiques. Un accent particulier est porté sur l'utilisation des verrous à base d'urokinase globalement peu étudiés et dotés d'un véritable potentiel iatrogène. En phase préliminaire à ce travail, il a paru essentiel d'étudier les caractéristiques de notre population cible pour étayer les critères clefs guidant les options retenues dans la conception de notre arbre décisionnel.
1) Généralités, contexte et objectifs
1.1 Généralités
1.1.1 Insuffisance rénale et hémodialyse
Les reins sont des organes vitaux qui assurent des fonctions primordiales pour l'organisme telles que la filtration et l'épuration de déchets toxiques, la régulation de l'eau et des minéraux, ainsi que la sécrétion d'hormones (rénine, angiotensine, EPO, calcitriol...). On parle de maladie rénale chronique (MRC) en cas d'altération d’apparition lente et progressive : ces fonctions ne sont alors plus assurées. La MRC se définit par la présence, pendant plus de trois mois, d'une diminution du débit de filtration glomérulaire (DGF) inférieur à 60 ml/min/1,73m2 ou de marqueurs d'atteinte rénale (protéinurie, albuminurie, hématurie, leucocyturie...). (1) Une classification de la MRC est établie en 5 stades, selon la valeur du DFG. (2) Lorsque le DFG présente une valeur inférieure à 15 ml/min/1,73m2, le stade 5 de la MRC, appelé insuffisance rénale chronique terminale, est atteint. A ce stade, la mise en place d'un traitement de suppléance commence à être envisagée afin de compenser les défaillances de ces fonctions rénales. Les traitements de suppléance, dont la prévalence nationale ne cesse de croître et qui était de 1294 par million d’habitants en 2017, sont d'une part la transplantation rénale à partir d'un donneur décédé ou vivant, et d'autre part la dialyse. Au 31 décembre 2017, ont été dénombrés 87 275 personnes en traitement de suppléance dont 47 985 (55 %) en dialyse (51,5% en hémodialyse et 3,5% en dialyse péritonéale) et 39 288 (45 %) porteuses d’un greffon rénal fonctionnel. (3) A la différence de la dialyse péritonéale qui utilise le péritoine comme membrane de filtration, l'hémodialyse regroupe les modalités d'épuration extra-rénale ayant recours à une circulation sanguine extra-corporelle et basées sur des échanges au travers d'une membrane semi-perméable. Ces échanges s'effectuent au travers de cette membrane entre le sang du patient et le dialysat, solution stérile composée d'eau ultra-pure et de minéraux.
La séance de dialyse nécessite la présence de différents éléments indispensables à son bon déroulement.
Tout d'abord, un abord vasculaire fonctionnel est nécessaire puisqu'il permet de dériver le sang du patient vers une circulation extra-corporelle afin de pouvoir y être épuré.
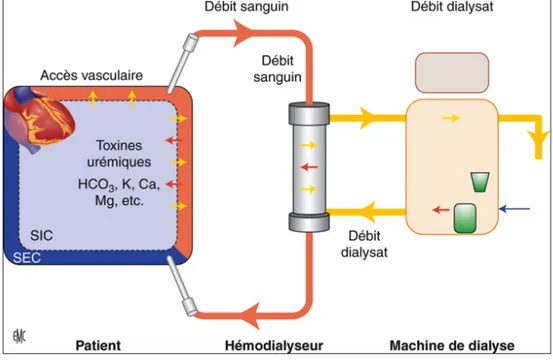
Puis, le générateur de dialyse, qui permet aussi de contrôler le bon déroulement de la séance, assure quant à lui la production continue de dialysat et la circulation du sang dans la circulation extra-corporelle. Le sang du patient circule de l'abord vasculaire jusqu'au dialyseur dans une tubulure qu'on appelle ligne artérielle, afin de pouvoir y être épuré. Le sang y circule dans un sens et le dialysat dans l'autre : des échanges au niveau de sa membrane semi-perméable peuvent alors s'effectuer entre les deux compartiments.
Enfin le sang dépourvu de ses déchets toxiques peut ensuite regagner le patient au niveau de son abord vasculaire, par l'intermédiaire de la ligne veineuse. (4) (5)
La figure n°1 représente schématiquement ce circuit d'hémodialyse. (5)
Figure n°1 : Représentation du circuit d'hémodialyse
1.1.2 Différentes voies d'abord vasculaires
Un abord vasculaire de qualité est indispensable pour pouvoir y faire des branchements répétés au long cours, lors des séances d'hémodialyse et doit permettre d'obtenir un débit sanguin suffisant (300ml/min) pour assurer l'efficacité des séances. (6) (7)
Il existe trois types d'abord vasculaire utilisés en hémodialyse : la fistule artério-veineuse (FAV), le pontage artério-veineux (PAV) prothétique et le cathéter veineux central (CVC).
1.1.2.1 FAV
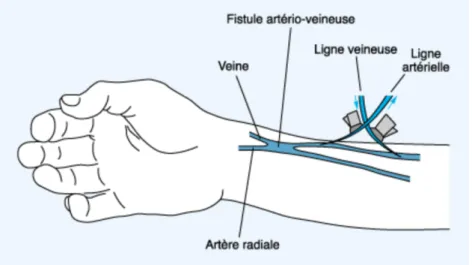
La FAV, bien que nécessitant un délai d'attente avant son usage, est l'abord vasculaire de premier choix en hémodialyse de par son efficacité, sa longévité et le moindre risque de complications. (8) Il s'agit d'un abord natif, généralement réalisé au niveau de l'avant bras, sous anesthésie locale, crée par l'anastomose d'une veine à une artère, comme représenté sur la figure n°2. (9)
Figure n°2 : Représentation d'une fistule artério-veineuse
Il existe différents types de FAV selon leur localisation et les veines et artères utilisées dont les principales sont :
-la fistule radio-céphalique distale, réalisée en première intention, mettant en communication la veine céphalique et l'artère radiale,
-la fistule radio-céphalique moyenne ou haute, lorsque la fistule distale n'est pas réalisable,
-la fistule ulno-basilique distale au niveau du poignet, faisant communiquer la veine basilique et l'artère ulnaire,
-la fistule brachio-céphalique, permettant la communication entre la veine céphalique et l'artère brachiale. (10)
La communication entre les secteurs veineux et artériel permet la dilatation des vaisseaux, l'épaississement de leur paroi et l'augmentation du débit sanguin permettant d'obtenir un débit important au niveau de la FAV. Cependant, la FAV n'est pas utilisable en situation d'urgence puisque la cicatrisation de l'anastomose et la dilatation de la veine artérialisée nécessitent un délai de plusieurs semaines. (6) (11)
1.1.2.2 PAV
Le PAV, bien que se compliquant plus rapidement d'une sténose veineuse, représente une alternative à la FAV en cas d'absence de veine susceptible d'être artérialisée. Une prothèse est alors interposée entre une artère et une veine profonde permettant ainsi les ponctions. (7)
1.1.2.3 CVC
Enfin, la troisième alternative est le recours à un cathéter veineux central, utilisé en situation d'urgence lorsque la création d'une FAV ou d'un PAV n'a pas pu être anticipée ou lorsque leur création ou utilisation est impossible.
On distingue les cathéters non tunnelisés mis en place en situation d'urgence des cathéters tunnelisés utilisés préférentiellement et pouvant être laissés en place au long cours. (12)
L'utilisation d'un cathéter tunnelisé permet ainsi de réduire le risque infectieux par éloignement du point de ponction du site d'insertion veineux et d'effectuer des séances de dialyse en attendant la maturation d'une fistule ou d'un pontage artério veineux ou la réalisation d'une greffe rénale. Mais il s'agit également d'une voie d'abord de choix dans certaines situations telles que l'impossibilité de réaliser un abord artério-veineux (espérance de vie limitée, risque de décompensation cardiaque, capital vasculaire épuisé) ou l'impossibilité de l'utiliser (thrombose). Ainsi le recours aux cathéters veineux centraux tunnelisés est fréquent dans la prise en charge globale d'une population de patients dialysés. Ces cathéters veineux tunnelisés existent principalement sous deux formes distinctes: soit de bi-cathéters indépendants dits de "Canaud", soit d'un cathéter bi-lumière. Ils sont introduits sous échoguidage la plupart du temps dans la veine jugulaire droite et leurs extrémités placées à la jonction entre la veine cave supérieure et l'oreillette droite, comme représenté sur la figure n°3. Outre le site d'insertion jugulaire utilisé en première intention en raison d'une meilleure qualité d'épuration et d'un moindre risque de complications, le site fémoral peut être choisi notamment en cas d'instabilité cardiopulmonaire. Enfin, la voie sous-clavière peut être utilisée en dernière intention (6) (7) (11) (13) (14)
Figure n°3 : Représentation schématique d'un Cathéter Veineux Central Tunnelisé par voie jugulaire interne droite
1.1.3 Complications et dysfonctionnements liés au cathéter
La première complication liée au cathéter est le risque infectieux allant jusqu'à entraîner son ablation. Ainsi l'application stricte des règles d'hygiène lors de la manipulation des cathéters est primordiale pour éviter leur survenue.
Des dysfonctionnements liés au cathéter peuvent également survenir. Le dysfonctionnement d'un cathéter de dialyse se définit comme l'impossibilité de maintenir un débit sanguin suffisant, fixé usuellement à 300ml/min, nécessaire au bon déroulement de la séance de dialyse, induisant une mauvaise épuration sanguine. (15)
Ces dysfonctionnements présentent deux types d'origine :
-une origine mécanique, d'apparition précoce liée à une mauvaise position de l'extrémité du cathéter lors de sa pose ou à une coudure du cathéter. Ce type de dysfonctionnements nécessite alors une intervention afin de le repositionner de façon adéquate ou en cas d'échec de procéder à son ablation et à une pose d'un autre cathéter.
-une origine thrombotique, d'apparition plus tardive liée à la présence d'un thrombus dans le cathéter obstruant sa lumière interne, ou d'une sténose de la veine. (11) Ces dysfonctionnements d'origine thrombotique font l'objet de mesures préventives systématiques en fin de séance de dialyse, à savoir le rinçage des voies veineuses et artérielles avec du NaCl 0,9% au débranchement du cathéter, l'instillation d'une solution verrou dans les deux branches du cathéter qui va rester en place durant
toute la période interdialytique, la fermeture des embouts du cathéter par des bouchons stériles ainsi que la réalisation d'un pansement occlusif. (16)
Cette solution verrou, instillée à chaque fin de séance, est alors retirée avant de débuter la séance suivante. Afin d'éviter au maximum son passage systémique, le volume de verrou utilisé doit être adapté au cathéter de chaque patient en fonction de son volume interne et donc de son diamètre et de sa longueur. (17)
Outre ces mesures préventives, si un dysfonctionnement d'origine thrombotique apparaît en cours de séance, différentes mesures correctives peuvent être envisagées :
-un rinçage des voies veineuses et artérielles du cathéter avec une solution de Chlorure de Sodium isotonique,
-une inversion des lignes : le circuit du sang est alors inversé entre les lignes artérielle et veineuse. Cette mesure peut être efficace en cas de fonctionnalité conservée d'une branche du cathéter par rapport à l'autre,
-le recours à un fibrinolytique en cours de séance tel que l'altéplase ou l'urokinase afin de procéder à une tentative de reperméabilisation du cathéter veineux tunnelisé.
1.1.4 Solutions verrous
L'instillation d'une solution verrou dans les deux branches du cathéter veineux central tunnelisé constitue un élément primordial de la prévention du risque de survenue de dysfonctionnements et de complications.
Différentes solutions existent sur le marché, elles ont cependant la particularité de ne pas toutes avoir le même statut : certaines solutions ont le statut de dispositif médical tandis que d'autres sont des médicaments. Leurs critères d'évaluation sont donc différents ce qui ne simplifie pas les comparaisons.
La principale propriété recherchée est leur activité anticoagulante afin d'éviter la formation d'un thrombus de fibrine au niveau du cathéter, même si certaines solutions présentent d'autres propriétés non négligeables telles que des activités antibactériennes ou encore la lutte contre l'installation du biofilm sur le CVT, qui joue un rôle important dans le dépôt de fibrine dans le CVT favorisant sa thrombose.
1.1.4.1 L'héparine sodique
L'héparine sodique est un médicament de la classe des héparines non fractionnées (HNF), elle présente une activité anticoagulante directe par fixation sur l'antithrombine. Cette fixation augmente considérablement l'activité inhibitrice de l'antithrombine sur la thrombine (FIIa) mais aussi sur le FXa et tous les facteurs
activés de la coagulation. L'héparine sodique utilisée en solution verrou se présente sous forme d'un flacon de 5ml contenant 25000UI, soit une concentration de 5000UI/ml.
Il s'agit d'une solution verrou utilisée de façon courante même si certains éléments pourraient en limiter son utilisation tels que le risque de passage systémique malgré son utilisation en verrou et le risque de complications hémorragiques associées à son utilisation. (17) (18) De même, tout antécédent de TIH contre indique son utilisation. (19) Enfin, l'héparine ne présente pas d'activité antimicrobienne, elle stimulerait même l'activité du biofilm. (20)
1.1.4.2 Le citrate de sodium
Plusieurs références de solutions verrous se composent de citrate de sodium à 4%, telles que: CITRALOCK®, CITRAFLOW®, DURALOCK®. Elles se présentent sous forme de seringues pré-remplies, et possèdent toutes le même statut de dispositif médical de classe IIb. Le citrate de sodium possède une activité anticoagulante de par sa fixation au calcium ionisé l'empêchant alors d'intervenir dans la cascade de la coagulation.
Le citrate de sodium se présente à la fois seul, mais certaines références de solutions verrous l'associent à d'autres molécules.
1.1.4.3 La taurolidine
La taurolidine est un dérivé de la taurine, agissant grâce à la formation de groupements N-methylol qui se fixent sur la paroi bactérienne et la détruisent entraînant une activité anti-bactérienne.
La taurolidine 1,35%, ne possédant pas d'activité anticoagulante, se retrouve toujours associée dans les solutions verrous :
-avec le citrate de sodium 4% dans le TAUROLOCK® qui se présente sous forme d'ampoules sécables de 3 ou de 5ml,
-avec le citrate de sodium 4% et l'héparine sodique 500UI/ml dans le TAUROLOCK HEP® 500, qui se présente sous forme d'ampoules sécables de 5ml,
-avec le citrate de sodium 4% et l'urokinase 25000UI dans le TAUROLOCK U® 25000, qui se présente par l'association d'un flacon d'urokinase 25000UI et d'une ampoule de 5ml de TAUROLOCK® : en effet, le TAUROLOCK U® s'obtient par dissolution de la poudre lyophilisée d'urokinase à l'aide des 5ml de TAUROLOCK®. L'ensemble de ces références possède le statut de dispositif médical de classe III.
1.1.4.4 L'urokinase
L'urokinase 100000UI est un médicament de la classe des fibrinolytiques dont le nom commercial est l'ACTOSOLV®. Il s'agit d'un activateur du plasminogène, d'origine humaine : elle provoque une activation de la fibrinolyse par transformation du plasminogène en plasmine. L'ACTOSOLV se présente sous forme de poudre pour solution injectable à reconstituer avec 2ml d'eau ppi. Ce médicament est indiqué dans la restauration de la perméabilité des cathéters veineux centraux et de dialyse, en cas d'obstruction liée à un thrombus en formation ou récemment formé, avec un SMR de niveau important.
Son utilisation en tant que solution verrou en hémodialyse est donc une utilisation hors AMM.
1.1.4.4 L'altéplase
L'altéplase 2mg est un médicament de la classe des fibrinolytiques dont le nom commercial est l'ACTILYSE®. Il s'agit d'une glycoprotéine qui, après liaison à la fibrine, induit la transformation du plasminogène en plasmine entraînant alors la fibrinolyse. Ce médicament dosé à 2mg est indiqué dans le traitement thrombolytique des cathéters veineux centraux occlus y compris ceux utilisés en hémodialyse, avec un SMR de niveau important.
Son utilisation en tant que solution verrou en hémodialyse est donc une utilisation hors AMM.
1.2 Contexte
1.2.1 Hémodialyse dans le GHT de l'Artois
Le GHT de l'Artois est composé par les quatre établissements suivants : le Centre Hospitalier de Lens (CHL) qui est l'établissement support du GHT, le Centre Hospitalier de Béthune (CHB), le Centre Hospitalier d'Hénin-Beaumont et le Centre Hospitalier de La Bassée. Leurs capacités d'accueil respectives sont détaillées dans le tableau n°1. (21)
Capacitaire MCO Psychiatrie SSR EHPAD USLD Total Lits Places HDJ Centre Hospitalier de Lens 605 98 0 120 823 165 Centre Hospitalier de Béthune 359 0 38 130 527 94 Centre Hospitalier d'Hénin-Beaumont 49 90 50 190 379 59 Centre Hospitalier de La Bassée 0 0 84 80 164 33
Tableau n°1 : Répartition des capacités d'accueil des quatre établissements du GHT de l'Artois
Cependant, l'activité d'hémodialyse est présente uniquement au sein de deux d'entre eux : le Centre Hospitalier de Lens et le Centre Hospitalier de Béthune. Le pôle d'excellence néphrologique étant situé à Béthune.
Le service d'hémodialyse du Centre Hospitalier de Lens, appelé Centre de Dialyse du Lensois (CDL), est organisé sous forme d'un Groupement de Coopération Sanitaire (GCS) entre le Centre Hospitalier de Béthune, le Centre Hospitalier de Lens et l'Hôpital privé de Bois-Bernard, et comporte 18 postes. Il est partagé entre une activité publique avec les médecins du Centre Hospitalier de Béthune (les lundi, mercredi et vendredi) et une activité privée avec les médecins de l'Hôpital privé de Bois-Bernard (les mardi, jeudi et samedi). Si le personnel médical change en fonction des journées, le personnel soignant est une seule et même équipe de statut public. Il s'agit donc d'un exemple de montage particulier de partenariat public-privé.
Le service d'hémodialyse du Centre Hospitalier de Béthune comporte quant à lui 22 postes avec une seule et même équipe publique.
1.2.2 Répartition des consommations des solutions verrous en 2018
Les consommations 2018 des solutions verrous pour les services d'hémodialyse du Centre Hospitalier de Lens et du Centre Hospitalier de Béthune sont détaillées dans le tableau n°2.Année 2018 héparine sodique 25000UI/5ml
CITRALOCK®
4% TAUROLOCK HEP® 500 TAUROLOCK U® 25000 ACTOSOLV® 100000UI CHL Consommation 1740 0 145 585 34
Coût TTC 3535,31 € 0 € 1392 € 20358 € 2196,35 €
CHB Consommation 1890 185 320 0 304
Coût TTC 3840,08 € 266,40 € 3072 € 0 € 19638 €
Tableau n°2 : Répartition des consommations et des coûts des solutions verrous en hémodialyse au CHL et au CHB en 2018
Quatre solutions verrous sont référencées au Centre Hospitalier de Lens : l'héparine sodique 25000UI/5ml, le TAUROLOCK HEP® 500, le TAUROLOCK U® 25000, et l'ACTOSOLV® 100 000UI.
Au total, sur l'année 2018, le service d'hémodialyse du Centre Hospitalier de Lens a consommé 2504 solutions verrous pour un coût TTC de 27481,66€.
Si 70% des consommations sont représentées par l'héparine sodique, 82% des coûts sont liés à l'utilisation des présentations à base d'urokinase.
Parallèlement, quatre solutions verrous sont également référencées au Centre Hospitalier de Béthune : l'héparine sodique 25000UI/5ml, le CITRALOCK® 4%, le TAUROLOCK HEP® 500, et l'ACTOSOLV® 100 000UI.
Sur l'année 2018, le service d'hémodialyse du Centre Hospitalier de Béthune a consommé 2699 solutions verrous pour un coût TTC de 26814,48€. L'ACTOSOLV® 100 000UI utilisé à 11% représente à lui seul 73% du coût global des solutions verrous référencées.
Figure n°4 : Répartition des consommations 2018 des solutions verrous en hémodialyse au CHL et au CHB
Figure n°5 : Répartition des coûts 2018 des solutions verrous en hémodialyse au CHL et au CHB 70% 6% 23% 1% héparine sodique 25000UI/5ml TAUROLOCK HEP® 500 TAUROLOCK U® 25000 ACTOSOLV® 100000UI 70% 7% 12%
11% héparine sodique 25000UI/5ml
CITRALOCK 4% TAUROLOCK HEP® 500 ACTOSOLV® 100000UI 13% 5% 74%
8% héparine sodique 25000UI/5ml
TAUROLOCK HEP® 500 TAUROLOCK U® 25000 ACTOSOLV® 100000UI 14% 1% 12% 73% héparine sodique 25000UI/5ml CITRALOCK 4% TAUROLOCK HEP® 500 ACTOSOLV® 100000UI CHL CHB CHL CHB
Les consommations de solutions verrous au CHL et au CHB semblent donc montrer des pratiques hétérogènes au sein du GHT de l'Artois. Il nous a paru important de comprendre quels sont les niveaux d'hétérogénéité (pratique, protocole, différence de recrutement etc...)
1.2.3 Pratiques de prescriptions des solutions verrous dans le GHT de
l'Artois
Au CHB et dans le secteur public du CHL, le choix de la solution verrou à instiller dans les branches du CVC s'effectue par le néphrologue sans protocole existant. En effet, seul un protocole d'utilisation de l'urokinase en cas de cathéter obstrué est rédigé. Il consiste, devant l'absence de risque hémorragique (ponction récente, intra-musculaire, soins dentaires, chirurgie récente, ulcère digestif..), en la prescription d'une seringue électrique (SAP) d'urokinase à poser sur la branche défectueuse du cathéter, afin de la désobstruer tout en évitant l'envoi d'embol dans la circulation veineuse. Une SAP composée d'une ampoule d'ACTOSOLV® 100 000UI diluée dans 20mL de NaCl 0,9% est alors adaptée par l'intermédiaire d'un prolongateur à la branche du cathéter concernée et est administrée sur 20 minutes à un débit de 60ml/h.
Dans la partie privée du CHL, un protocole d'utilisation des solutions verrous pour les cathéters d'hémodialyse est rédigé. Il décrit le citrate 4% (CITRAFLOW® 4%) présenté sous forme de seringue pré-remplie comme verrou de 1ère intention à poursuivre au long cours en l'absence de survenue de dysfonctionnement. Si un dysfonctionnement de cathéter se présente, l'utilisation d'ACTILYSE® 2mg est préconisée, en répartissant 1mg par branche de cathéter. Cependant, une distinction est faite entre l'obstruction partielle ou complète du cathéter. Si l'obstruction est partielle, un recours à un verrou court d'ACTILYSE® 2mg sur 30 minutes est recommandé. Si elle est complète, selon l'avis du néphrologue, il est décrit soit l'utilisation d'un verrou court d'ACTILYSE® 2mg sur 60 minutes d'une part, soit d'autre part l'utilisation d'un verrou court d'ACTILYSE® 2mg sur 30 minutes et ensuite de deux injections lente de 0,3ml de sérum physiologique suivies chacune de 10 minutes de repos, avant de procéder à l'aspiration de l'ensemble. Enfin, quelque soit le type d'obstruction, le protocole recommande l'utilisation d'un verrou d'ACTILYSE® 2mg à la fin de la séance au cours de laquelle l'obstruction s'est présentée restant en place jusqu'à la séance de dialyse suivante, à partir de laquelle
le verrou de première intention à base de citrate 4% sera repris. Le verrou d' ACTILYSE® 2mg sera alors répété une fois par mois. Cependant, en pratique, l'ensemble de ce protocole n'est pas applicable devant l'absence de référencement du citrate 4% et de l'ACTILYSE 2mg au CHL.
1.3 Objectifs de l'étude
Devant ces pratiques hétérogènes, marquées par des référencements différents, mais aussi par des utilisations pas ou partiellement protocolées, un travail sur le bon usage des solutions verrous dans le GHT de l'Artois semble nécessaire.
Les objectifs de ce travail sont d'une part de caractériser la population de patients hémodialysés dans le GHT, chez lesquels les solutions verrous sont utilisées, et d'autre part d'aboutir à une uniformisation et une protocolisation de l'utilisation de ces solutions verrous en hémodialyse à l'échelle du GHT de l'Artois, en définissant avec précision la place des verrous à base d'urokinase (TAUROLOCK U® et ACTOSOLV® 100 000UI).
2) Matériel et Méthode
2.1 Mise en place de l'étude
Après prise de contact avec le néphrologue responsable des unités de Lens et de Béthune, il a été décidé que le travail serait piloté par un binôme pharmacien - néphrologue. La première phase observationnelle constituait en une analyse détaillée des pratiques d'utilisation des solutions verrous par les soignants, avec l'implication des cadres de santé respectifs des deux unités.
Puis, dans un second temps, une première réunion pluridisciplinaire s'est effectuée le mercredi 16 janvier 2019, réunissant tous les interlocuteurs concernés par cette problématique, à savoir l'ensemble de l'équipe médicale du service d'hémodialyse du Centre Hospitalier de Béthune, les cadres de santé des deux unités, ainsi que des pharmaciens des Centres Hospitaliers de Béthune et de Lens. Cette réunion avait pour objectif de présenter le contexte, d'exposer les objectifs et de définir la méthodologie de l'étude pour y parvenir. Un groupe de travail pluridisciplinaire, constitué de 6 médecins néphrologues, d'un IDE, d'un interne en pharmacie et des cadres de santé, s'est alors formé. Une supervision était assurée par le néphrologue responsable d’unité et un pharmacien praticien. Il a été décidé d'effectuer une étude observationnelle rétrospective sur l'année 2018. La population de l'étude a donc ensuite été ciblée, et les critères d'évaluation ainsi que la méthode de recueil ont été définis. Au cours de cette étude 6 réunions ont été organisées, le reste de la communication s'étant effectuée par échanges de mails ou de téléphones avec les professionnels de santé présents sur les deux centres hospitaliers.
2.2 Critères d'inclusion
Les patients inclus dans l'étude respectent les critères d'inclusion suivants :
- patient hémodialysé au cours de l'année 2018 (du 01/01/2018 au 31/12/2018) dans les services d'hémodialyse des Centres Hospitaliers de Béthune et de Lens (patients issus de la filière privée et publique)
- patient ayant un cathéter veineux jugulaire tunnelisé comme voie d'abord utilisé lors de la séance d'hémodialyse.
Tout patient respectant ces deux critères a été inclus dans l'étude.
Outre la période de l'étude, limitée uniquement aux séances de l'année 2018, le principal critère d'exclusion des patients hémodialysés dans le GHT de l'Artois est l'utilisation d'une FAV comme voie d'abord.
2.3 Critères d'évaluation
Cette étude présente trois volets distincts.
-Dans le premier volet, il a été réalisé une caractérisation de la population par des critères définis par le groupe de travail. Ces critères incluaient à la fois des données générales sur la population (âge, sexe, durée moyenne de séance, traitement par EPO) mais aussi la présence ou non de comorbidités (diabète, insuffisance respiratoire chronique, insuffisance cardiaque, insuffisance coronarienne, cancer, cirrhose...).
-Dans le deuxième volet, outre le recueil des solutions verrous utilisées après chaque séance de dialyse, il a été effectué un recueil de données d'efficacité et de dysfonctionnement des séances.
Le débit de circulation sanguine extracorporelle et l'index Kt/V des séances, marqueurs de la fonctionnalité du cathéter et de l'efficacité des séances, ont été recueillis pour chaque séance. L'index Kt/V correspond à la dose normalisée de dialyse qui est le paramètre d’épuration le plus facile à quantifier directement, avec K : la clairance de l’urée du dialyseur (ml/min), t : la durée de la séance de dialyse (min) et V : le volume de diffusion de l'urée (ml). Il exprime le rapport de volume épuré à celui de l'eau totale du patient. Une épuration efficace est alors définie par une valeur de Kt/V ≥1,2. (22)
Dans une optique de comparaison d'efficacité des différentes solutions verrous, il a été décidé de lier ces deux marqueurs d'efficacité au verrou utilisé. Cependant, ne connaissant pas la durée et ou le délai d'impact d'une solution verrou sur l'efficacité des séances de dialyse suivantes, le groupe de travail a décidé d'évaluer l'index Kt/V et le débit sanguin des séances n+1, n+2 et n+3 en regard de la solution verrou utilisée lors de la séance n.
Enfin, les dysfonctionnements des séances, mis en évidence par l’utilisation d’urokinase en verrou en cours de séance et par le changement de cathéter consécutif à une origine thrombotique, ont également été répertoriés.
Dans le but d'observer l'influence des solutions verrous sur la survenue de ces dysfonctionnements, le groupe de travail, a décidé de procéder à une étude rétrospective des solutions verrous utilisées sur une période fixée à un mois avant la survenue de chaque dysfonctionnement.
Le groupe de travail a également défini un indicateur permettant de refléter la place des solutions verrous à base d'urokinase : le rapport U/V, avec U : le nombre de séances avec utilisation de verrous à base d'Urokinase (TAUROLOCK U® et ACTOSOLV®) et V : le nombre de séances total quelque soit le Verrou utilisé.
Il a alors été décidé collégialement de calculer ce rapport U/V sur la période d'un mois avant la survenue de chaque dysfonctionnement et de le comparer de façon empirique au rapport U/V calculé sur l'ensemble de l'année 2018 chez les patients n'ayant présenté aucun dysfonctionnement.
-Dans un troisième volet, suite aux phases préliminaires de caractérisation de la population et des séances de dialyse, il a été mis en place un travail sur l'harmonisation et l'optimisation de la stratégie d'anticoagulation des solutions verrous, en se basant sur les pratiques mises en évidence, et aboutissant à la rédaction d'un protocole sous forme d'arbre décisionnel de choix des solutions verrous. Ce protocole validé par l'équipe médicale publique du GHT de l'Artois, sera également validé institutionnellement à l'échelle du GHT, par présentation en COMEDIMS. Bien qu'une organisation locale des COMEDIMS ait été conservée dans chaque établissement, elles disposent d'une coordination à l'échelle du GHT validée en collège médical. En effet, des réunions pré-COMEDIMS sont réalisées entre les coordinateurs locaux. Ces réunions permettent d'évoquer les ordres du jour respectifs des 4 COMEDIMS du GHT en ciblant des sujets communs, d'échanger sur les thèmes déjà abordés dans les différents établissements et dans ce cas de procéder au partage des documents existants. Les supports documentaires (ordre du jour, diaporamas présentés et compte rendus) sont également uniformisés.
2.4 Recueil des données
Toutes les données ont été recueillies dans les dossiers médicaux des patients répondant aux critères d'inclusion cités précédemment. Cette étude a ainsi fait l'objet d'une déclaration par l'intermédiaire du médecin du DIM du GHT de l'Artois dans le cadre de l’application du nouveau règlement européen sur la protection des données à caractère personnel.
Les données ont été anonymisées, chaque patient ayant été associé à un numéro au fur et à mesure des inclusions.
Le recueil des données de caractérisation de la population de l'étude a été réalisé grâce aux fiches NEPHRONOR. En effet, ces fiches sont complétées systématiquement pour chaque patient par les néphrologues, à l'initiation du traitement (Annexe n°1 : Fiche Nouveau Patient NEPHRONOR), puis au cours du suivi au minimum une fois par an.
Le deuxième volet de l'étude, nécessitant un recueil des caractéristiques de toutes les séances de dialyse pour chaque patient, s'est effectué grâce aux données retranscrites sur les fiches de séance ainsi que sur les fiches DIALIN (Annexe n°2 : Fiche de surveillance des abords de séance).
2.5 Analyse des données
Après la mise en place de cette étude et la phase de recueil des données, 5 réunions ont été organisées, lors desquelles les données recueillies ont été présentées et discutées au groupe de travail afin d'obtenir un consensus.
Après avis du laboratoire de biostatistique de la faculté de pharmacie de Lille, le groupe de travail a décidé de se limiter à une analyse descriptive des données. En effet, les effectifs inclus ne permettent pas d'exploitation statistique des données. Les résultats seront alors présentés, selon les variables, par leur médiane, moyenne, écart type, valeur minimale ou maximale, effectif ou fréquence.
3) Résultats
3.1 Description de la population de l'étude
Au total, 38 patients issus des différents services d'hémodialyse du GHT de l'Artois ont répondu aux critères d'inclusion de notre étude, selon la répartition suivante :
Hôpital patients inclus Nombre de CH LENS PUBLIC 7 CH LENS PRIVE 16 CH BETHUNE 15
Total 38
Tableau n°3 : Répartition des patients inclus dans l'étude selon la structure d'origine
Le code couleur employé sur le tableau n°3, à savoir le bleu pour la partie publique du Centre Hospitalier de Lens, le rouge pour la partie privée du Centre Hospitalier de Lens et le vert pour le Centre Hospitalier de Béthune, sera utilisé lors de la présentation de l'ensemble des résultats de l'étude.
Ainsi, sur la population totale de l'étude, 23 patients ont été pris en charge au Centre Hospitalier de Lens, à savoir : 7 dans la partie publique (patients n°1 à 7) et 16 patients dans la partie privée (patients n°8 à 23) soit respectivement 42% et 18% de la population, et 15 patients ont été traités au Centre Hospitalier de Béthune (patients n°24 à 38) représentant 40% de notre population étudiée.
3.2 Description des caractéristiques de la population
Dans un premier temps, l'ensemble des critères de caractérisation de la population est présenté par patient dans le tableau de recueil. (Annexe n°3)
Tableau n°4 : Nombre de comorbidités cumulées par patient
Patient 1 2 3 4 5 6 7 8 9 10 11 12 13 Nombre de comorbidités 6 2 3 7 1 3 4 6 1 7 3 3 2 Patient 14 15 16 17 18 19 20 21 22 23 24 25 26 Nombre de comorbidités 8 1 5 5 5 6 2 3 6 3 2 3 2 Patient 27 28 29 30 31 32 33 34 35 36 37 38 Nombre de comorbidités 0 4 3 0 3 8 4 4 2 3 4 4
Le tableau n°4 représente le nombre de comorbidités cumulées par patient parmi : IMC>25kg/m2, diabète, tabagisme, insuffisance respiratoire chronique ou BPCO, oxygénothérapie ou assistance ventilatoire, SAS, IC, insuffisance coronarienne, infarctus du myocarde, arythmie, anévrisme de l'aorte abdominale, AOMI, AVC, AIT, cancer ou hémopathie évolutif, cirrhose et handicap. La présence des comorbidités varie selon les patients : on note leur absence chez les patients n°27 et 30, alors que les patients n°14 et 32 en possèdent 8.
La synthèse de ces éléments de caractérisation est récapitulée dans le tableau n°5. Notre population d'étude est ainsi constituée de 18 hommes (47%) et de 20 femmes (53%). Parmi les principales comorbidités, on note une forte proportion de diabétiques (63%) dont 58% sous insuline, une population en insuffisance cardiaque à 53% dont 55% sont au stade III ou IV de la classification fonctionnelle de la NYHA, une population en insuffisance coronarienne à 24%, et près de 29% présentent un trouble du rythme cardiaque.
Nous retrouvons également 2 patients cirrhotiques, 4 patients atteints d'un cancer évolutif ou d'une hémopathie maligne, 10 patients atteints d'artériopathie des membres inférieurs. 5 patients ont des antécédents d'AIT ou d'AVC et 7 présentent une insuffisance respiratoire chronique ou sont sous assistance respiratoire.
De même, de façon plus globale, 28 patients sur 38, soit 74% de la population étudiée, ont au moins une pathologie cardiovasculaire (pathologie coronarienne, insuffisance cardiaque, troubles du rythme, artérite des membres inférieurs et/ou antécédents d’AVC ou d’AIT).
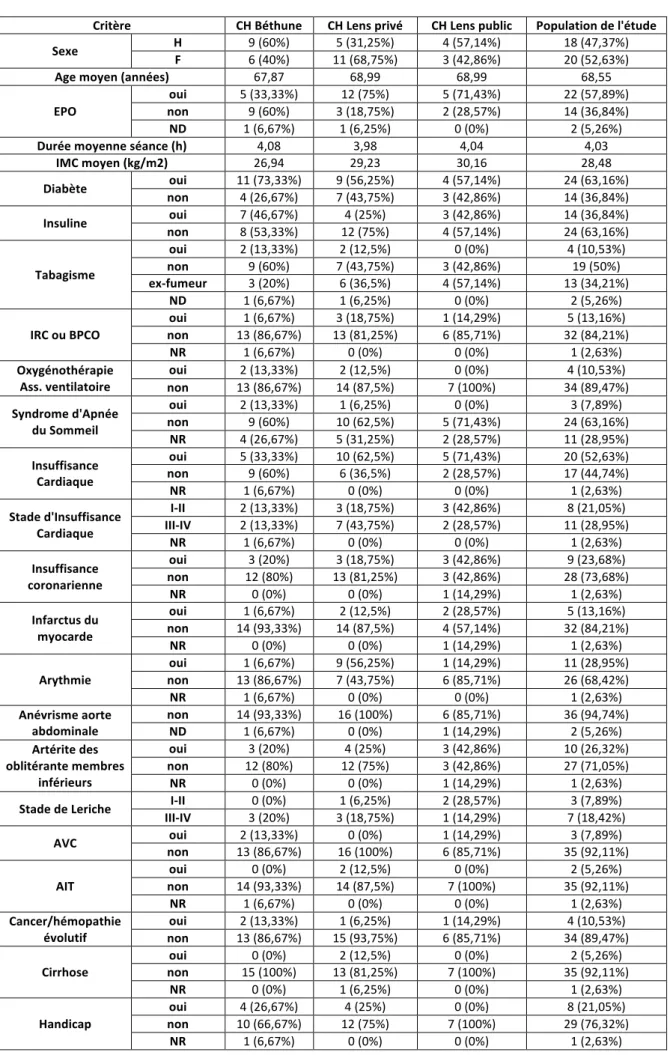
Tableau n°5 : Description des éléments de caractérisation de la population en effectif et en pourcentage
Critère CH Béthune CH Lens privé CH Lens public Population de l'étude
Sexe H F 9 (60%) 6 (40%) 11 (68,75%) 5 (31,25%) 4 (57,14%) 3 (42,86%) 18 (47,37%) 20 (52,63%)
Age moyen (années) 67,87 68,99 68,99 68,55
EPO
oui 5 (33,33%) 12 (75%) 5 (71,43%) 22 (57,89%)
non 9 (60%) 3 (18,75%) 2 (28,57%) 14 (36,84%)
ND 1 (6,67%) 1 (6,25%) 0 (0%) 2 (5,26%)
Durée moyenne séance (h) 4,08 3,98 4,04 4,03
IMC moyen (kg/m2) 26,94 29,23 30,16 28,48
Diabète non oui 11 (73,33%) 4 (26,67%) 9 (56,25%) 7 (43,75%) 4 (57,14%) 3 (42,86%) 24 (63,16%) 14 (36,84%)
Insuline oui 7 (46,67%) 4 (25%) 3 (42,86%) 14 (36,84%) non 8 (53,33%) 12 (75%) 4 (57,14%) 24 (63,16%) Tabagisme oui 2 (13,33%) 2 (12,5%) 0 (0%) 4 (10,53%) non 9 (60%) 7 (43,75%) 3 (42,86%) 19 (50%) ex-‐fumeur 3 (20%) 6 (36,5%) 4 (57,14%) 13 (34,21%) ND 1 (6,67%) 1 (6,25%) 0 (0%) 2 (5,26%)
IRC ou BPCO
oui 1 (6,67%) 3 (18,75%) 1 (14,29%) 5 (13,16%) non 13 (86,67%) 13 (81,25%) 6 (85,71%) 32 (84,21%) NR 1 (6,67%) 0 (0%) 0 (0%) 1 (2,63%) Oxygénothérapie Ass. ventilatoire oui 2 (13,33%) 2 (12,5%) 0 (0%) 4 (10,53%) non 13 (86,67%) 14 (87,5%) 7 (100%) 34 (89,47%) Syndrome d'Apnée du Sommeil oui 2 (13,33%) 1 (6,25%) 0 (0%) 3 (7,89%) non 9 (60%) 10 (62,5%) 5 (71,43%) 24 (63,16%) NR 4 (26,67%) 5 (31,25%) 2 (28,57%) 11 (28,95%) Insuffisance Cardiaque oui 5 (33,33%) 10 (62,5%) 5 (71,43%) 20 (52,63%) non 9 (60%) 6 (36,5%) 2 (28,57%) 17 (44,74%) NR 1 (6,67%) 0 (0%) 0 (0%) 1 (2,63%) Stade d'Insuffisance Cardiaque I-‐II 2 (13,33%) 3 (18,75%) 3 (42,86%) 8 (21,05%) III-‐IV 2 (13,33%) 7 (43,75%) 2 (28,57%) 11 (28,95%) NR 1 (6,67%) 0 (0%) 0 (0%) 1 (2,63%) Insuffisance coronarienne oui 3 (20%) 3 (18,75%) 3 (42,86%) 9 (23,68%) non 12 (80%) 13 (81,25%) 3 (42,86%) 28 (73,68%) NR 0 (0%) 0 (0%) 1 (14,29%) 1 (2,63%) Infarctus du myocarde oui 1 (6,67%) 2 (12,5%) 2 (28,57%) 5 (13,16%) non 14 (93,33%) 14 (87,5%) 4 (57,14%) 32 (84,21%) NR 0 (0%) 0 (0%) 1 (14,29%) 1 (2,63%) Arythmie oui 1 (6,67%) 9 (56,25%) 1 (14,29%) 11 (28,95%) non 13 (86,67%) 7 (43,75%) 6 (85,71%) 26 (68,42%) NR 1 (6,67%) 0 (0%) 0 (0%) 1 (2,63%) Anévrisme aorte abdominale non 14 (93,33%) 16 (100%) 6 (85,71%) 36 (94,74%) ND 1 (6,67%) 0 (0%) 1 (14,29%) 2 (5,26%) Artérite des oblitérante membres inférieurs oui 3 (20%) 4 (25%) 3 (42,86%) 10 (26,32%) non 12 (80%) 12 (75%) 3 (42,86%) 27 (71,05%) NR 0 (0%) 0 (0%) 1 (14,29%) 1 (2,63%)
Stade de Leriche I-‐II 0 (0%) 1 (6,25%) 2 (28,57%) 3 (7,89%)
III-‐IV 3 (20%) 3 (18,75%) 1 (14,29%) 7 (18,42%) AVC oui 2 (13,33%) 0 (0%) 1 (14,29%) 3 (7,89%) non 13 (86,67%) 16 (100%) 6 (85,71%) 35 (92,11%) AIT oui 0 (0%) 2 (12,5%) 0 (0%) 2 (5,26%) non 14 (93,33%) 14 (87,5%) 7 (100%) 35 (92,11%) NR 1 (6,67%) 0 (0%) 0 (0%) 1 (2,63%) Cancer/hémopathie évolutif oui 2 (13,33%) 1 (6,25%) 1 (14,29%) 4 (10,53%) non 13 (86,67%) 15 (93,75%) 6 (85,71%) 34 (89,47%) Cirrhose oui 0 (0%) 2 (12,5%) 0 (0%) 2 (5,26%) non 15 (100%) 13 (81,25%) 7 (100%) 35 (92,11%) NR 0 (0%) 1 (6,25%) 0 (0%) 1 (2,63%) Handicap oui 4 (26,67%) 4 (25%) 0 (0%) 8 (21,05%) non 10 (66,67%) 12 (75%) 7 (100%) 29 (76,32%) NR 1 (6,67%) 0 (0%) 0 (0%) 1 (2,63%)
Le tableau n°6 fait un focus sur les éléments de description des variables quantitatives suivantes : âge, IMC et durée de séance.
Médiane Moyenne Ecart type Minimum Maximum Age (années) 69 68,5 11,9 38 88 IMC (kg/m2) 27,4 28,5 5,8 18,2 40,1 Durée séance (h) 4 4 0,4 2 5
Tableau n°6 : Description des variables quantitatives de la population de l'étude
L'âge des patients pris en compte en début d'année 2018 varie de 38 à 88 ans, avec une médiane de 69 ans, ainsi qu'une moyenne et un écart type respectivement de 68,5 et 11,9 ans.
Leur IMC moyen est de 28,5 kg/m2 avec un écart type de 5,8 kg/m2. Sa médiane est de 27,4 kg/m2, avec des valeurs s'échelonnant de 18,2 à 40,1 kg/m2.
En ce qui concerne la séance de dialyse proprement dite, l'ensemble des patients inclus dans l'étude possède un rythme de 3 séances par semaine, avec une durée moyenne et médiane de 4heures par séance.
3.3 Description des séances de dialyse
3.3.1 Nombre de séances
3.3.1.1 Description globaleLes 38 patients inclus ont cumulé sur l'ensemble de l'année 2018 un nombre total de 2581 séances d'hémodialyse avec un cathéter veineux jugulaire tunnelisé comme voie d'abord. Ces séances ont été réalisées dans les différents services d'hémodialyse du GHT de l'Artois selon la répartition suivante:
Hôpital Nombre de Séances Pourcentage de séances CH LENS PUBLIC 818 31,69
CH LENS PRIVE 1086 42,08
CH BETHUNE 677 26,23
Total 2581
Tableau n°7 : Répartition des séances d'hémodialyse étudiées dans l'étude selon leur hôpital de réalisation
Ainsi, sur les 2581 séances d'hémodialyse étudiées, 1904 ont été réalisées au Centre Hospitalier de Lens, à savoir : 1086 dans la partie privée et 818 dans la partie