HAL Id: hal-01732902
https://hal.univ-lorraine.fr/hal-01732902
Submitted on 14 Mar 2018HAL is a multi-disciplinary open access
archive for the deposit and dissemination of sci-entific research documents, whether they are pub-lished or not. The documents may come from teaching and research institutions in France or abroad, or from public or private research centers.
L’archive ouverte pluridisciplinaire HAL, est destinée au dépôt et à la diffusion de documents scientifiques de niveau recherche, publiés ou non, émanant des établissements d’enseignement et de recherche français ou étrangers, des laboratoires publics ou privés.
Elaboration d’un programme d’éducation thérapeutique
du diabète de type 2 adapté au milieu carcéral
Camille Herbourg
To cite this version:
Camille Herbourg. Elaboration d’un programme d’éducation thérapeutique du diabète de type 2 adapté au milieu carcéral. Sciences pharmaceutiques. 2013. �hal-01732902�
AVERTISSEMENT
Ce document est le fruit d'un long travail approuvé par le jury de
soutenance et mis à disposition de l'ensemble de la
communauté universitaire élargie.
Il est soumis à la propriété intellectuelle de l'auteur. Ceci
implique une obligation de citation et de référencement lors de
l’utilisation de ce document.
D'autre part, toute contrefaçon, plagiat, reproduction illicite
encourt une poursuite pénale.
Contact : ddoc-thesesexercice-contact@univ-lorraine.fr
LIENS
Code de la Propriété Intellectuelle. articles L 122. 4
Code de la Propriété Intellectuelle. articles L 335.2- L 335.10
http://www.cfcopies.com/V2/leg/leg_droi.php
UNIVERSITE DE LORRAINE
2013
_________________________________________________________
FACULTE DE PHARMACIE
ELABORATION D’UN PROGRAMME
D’EDUCATION THERAPEUTIQUE DU
DIABETE DE TYPE 2 ADAPTE AU MILIEU
CARCERAL
THESE
Présentée et soutenue publiquement Le 08/03/2013,
pour obtenir
Le Diplôme d'Etat de Docteur en Pharmacie
par Camille HERBOURG
née le 17 janvier 1989, à Laxou (54)
Membre du jury
Président du jury : Monsieur Pierre LABRUDE, professeur des Universités
Membres du jury : Mademoiselle Laëtitia ALBERTINI, pharmacien hospitalier au CH saint-Charles de Toul,
Monsieur Philip BÖHME, médecin diabétologue au CHU de Brabois Madame Sandrine BRESCIANI, médecin coordonateur des UCSA
2 UNIVERSITÉ DE LORRAINE FACULTÉ DE PHARMACIE Année universitaire 2012-2013 DOYEN Francine PAULUS Vice-Doyen Francine KEDZIEREWICZ
Directeur des Etudes Virginie PICHON
Président du Conseil de la Pédagogie Bertrand RIHN
Président de la Commission de la Recherche Christophe GANTZER
Président de la Commission Prospective Facultaire Jean-Yves JOUZEAU
Responsable de la Cellule de Formations Continue et Individuelle Béatrice FAIVRE
Responsable ERASMUS : Francine KEDZIEREWICZ Responsable de la filière Officine : Francine PAULUS Responsables de la filière Industrie : Isabelle LARTAUD,
Jean-Bernard REGNOUF de VAINS Responsable du Collège d’Enseignement
Pharmaceutique Hospitalier : Jean-Michel SIMON
Responsable Pharma Plus E.N.S.I.C. : Jean-Bernard REGNOUF de VAINS Responsable Pharma Plus E.N.S.A.I.A. : Bertrand RIHN
3 DOYENS HONORAIRES Chantal FINANCE Claude VIGNERON PROFESSEURS EMERITES Jeffrey ATKINSON Gérard SIEST Claude VIGNERON
PROFESSEURS HONORAIRES MAITRES DE CONFERENCES HONORAIRES
Roger BONALY Monique ALBERT
Pierre DIXNEUF Gérald CATAU
Marie-Madeleine GALTEAU Jean-Claude CHEVIN
Thérèse GIRARD Jocelyne COLLOMB
Maurice HOFFMANN Bernard DANGIEN
Michel JACQUE Marie-Claude FUZELLIER
Lucien LALLOZ Françoise HINZELIN
Pierre LECTARD Marie-Hélène LIVERTOUX
Vincent LOPPINET Bernard MIGNOT
Marcel MIRJOLET Jean-Louis MONAL
François MORTIER Dominique NOTTER
Maurice PIERFITTE Marie-France POCHON
Janine SCHWARTZBROD Anne ROVEL
Louis SCHWARTZBROD Maria WELLMAN-ROUSSEAU
ASSISTANT HONORAIRE Marie-Catherine BERTHE Annie PAVIS
4
Faculté de Pharmacie Présentation
ENSEIGNANTS Section CNU* Discipline d'enseignement
PROFESSEURS DES UNIVERSITES - PRATICIENS HOSPITALIERS
Danièle BENSOUSSAN-LEJZEROWICZ 82 Thérapie cellulaire
Chantal FINANCE 82 Virologie, Immunologie
Jean-Yves JOUZEAU 80 Bioanalyse du médicament
Jean-Louis MERLIN 82 Biologie cellulaire
Alain NICOLAS 80 Chimie analytique et bromatologie
Jean-Michel SIMON 81 Economie de la santé, Législation pharmaceutique
PROFESSEURS DES UNIVERSITES
Jean-Claude BLOCK 87 Santé publique
Christine CAPDEVILLE-ATKINSON 86 Pharmacologie
Pascale FRIANT-MICHEL 85 Mathématiques, Physique
Christophe GANTZER 87 Microbiologie
Max HENRY 87 Botanique, Mycologie
Pierre LABRUDE 86 Physiologie, Orthopédie, Maintien à domicile
Isabelle LARTAUD 86 Pharmacologie
Dominique LAURAIN-MATTAR 86 Pharmacognosie Brigitte LEININGER-MULLER 87 Biochimie
Pierre LEROY 85 Chimie physique
Philippe MAINCENT 85 Pharmacie galénique
Alain MARSURA 32 Chimie organique
Patrick MENU 86 Physiologie
Jean-Bernard REGNOUF de VAINS 86 Chimie thérapeutique
Bertrand RIHN 87 Biochimie, Biologie moléculaire
5
Béatrice DEMORE 81 Pharmacie clinique
Nathalie THILLY 81 Santé publique
MAITRES DE CONFÉRENCES
Sandrine BANAS 87 Parasitologie
Mariette BEAUD 87 Biologie cellulaire
Emmanuelle BENOIT 86 Communication et santé
Isabelle BERTRAND 87 Microbiologie
Michel BOISBRUN 86 Chimie thérapeutique
François BONNEAUX 86 Chimie thérapeutique
Ariane BOUDIER 85 Chimie Physique
Cédric BOURA 86 Physiologie
Igor CLAROT 85 Chimie analytique
Joël COULON 87 Biochimie
Sébastien DADE 85 Bio-informatique
Dominique DECOLIN 85 Chimie analytique
Roudayna DIAB 85 Pharmacie clinique
Joël DUCOURNEAU 85 Biophysique, Acoustique
Florence DUMARCAY 86 Chimie thérapeutique
François DUPUIS 86 Pharmacologie
Faculté de Pharmacie Présentation
ENSEIGNANTS (suite) Section CNU* Discipline d'enseignement
Raphaël DUVAL 87 Microbiologie
Béatrice FAIVRE 87 Hématologie
Adil FAIZ 85 Biophysique, Acoustique
6 Caroline GAUCHER-DI STASIO 85/86 Chimie physique, Pharmacologie
Stéphane GIBAUD 86 Pharmacie clinique
Thierry HUMBERT 86 Chimie organique
Frédéric JORAND 87 Environnement et Santé
Olivier JOUBERT 86 Toxicologie
Francine KEDZIEREWICZ 85 Pharmacie galénique
Alexandrine LAMBERT 85 Informatique, Biostatistiques
Faten MERHI-SOUSSI 87 Hématologie
Christophe MERLIN 87 Microbiologie
Blandine MOREAU 86 Pharmacognosie
Maxime MOURER 86 Chimie organique
Francine PAULUS 85 Informatique
Christine PERDICAKIS 86 Chimie organique
Caroline PERRIN-SARRADO 86 Pharmacologie
Virginie PICHON 85 Biophysique
Anne SAPIN-MINET 85 Pharmacie galénique
Marie-Paule SAUDER 87 Mycologie, Botanique
Gabriel TROCKLE 86 Pharmacologie
Mihayl VARBANOV 87 Immuno-Virologie
Marie-Noëlle VAULTIER 87 Mycologie, Botanique
Emilie VELOT 86 Physiologie-Physiopathologie humaines
Mohamed ZAIOU 87 Biochimie et Biologie moléculaire
Colette ZINUTTI 85 Pharmacie galénique
PROFESSEUR ASSOCIE
Anne MAHEUT-BOSSER 86 Sémiologie
PROFESSEUR AGREGE
Christophe COCHAUD 11 Anglais
7 80ème et 85ème : Sciences physico-chimiques et ingénierie appliquée à la santé
81ème et 86ème : Sciences du médicament et des autres produits de santé 82ème et 87ème : Sciences biologiques, fondamentales et cliniques
32ème : Chimie organique, minérale, industrielle
8
S
ERMENT DES
A
POTHICAIRES
j
e jure, en présence des maîtres de la Faculté, des conseillers de l’ordre des pharmaciens et de mes condisciples :Ð
’ honorer ceux qui m’ont instruit dans les préceptes de mon art et de leur témoigner ma reconnaissance en restant fidèle à leur enseignement.Ð
’exercer, dans l’intérêt de la santé publique, ma profession avec conscience et de respecter non seulement la législation en vigueur, mais aussi les règles de l’honneur, de la probité et du désintéressement.Ð
e ne jamais oublier ma responsabilité et mes devoirs envers le malade et sa dignité humaine ; en aucun cas, je ne consentirai à utiliser mes connaissances et mon état pour corrompre les mœurs et favoriser des actes criminels.Q
ue les hommes m’accordent leur estime si je suis fidèle à mes promesses.Q
ue je sois couvert d’opprobre et méprisé de mes confrères si j’y manque.9 « LA F AC UL TE N’E N TE N D DON NE R A U CUNE A PP R OB A TI ON, NI
IMP RO B A TIO N A UX OP I N ION S E M ISE S D AN S L E S THE SE S, CE S OP IN I ON S D OI VE NT E T RE C ON SI DE RE E S C O MME PRO PRE S A LE U R AU TE U R » .
10
REMERCIEMENTS
A mon Président de Jury,
Monsieur Pierre LABRUDE, Professeur des Universités, Faculté de Pharmacie de Nancy,
Qui m’a fait l’honneur d’accepter la présidence de cette thèse. Sincères remerciements.
A ma directrice de thèse,
Mademoiselle Laëtitia ALBERTINI,
Pharmacien hospitalier à l’hôpital Saint-Charles de Toul,
Je te remercie de m’avoir proposé et de m’avoir fait confiance pour ce sujet. Merci de m’avoir suivie et apporté tous tes conseils précieux dans son écriture. Encore une fois, merci.
Aux membres du jury,
Monsieur Philip BOHME,
Médecin diabétologue au CHU de Brabois,
Médecin coordonateur de la Maison du Diabète de Nancy,
Qui m’a fait l’honneur d’être membre du jury et de superviser ma thèse.
Je vous remercie de votre accueil et de celle de votre équipe à la Maison du Diabète de Nancy.
11 Madame Sandrine BRESCIANI,
Médecin coordonateur des UCSA de Toul et Ecrouves,
Merci de nous avoir permis de réaliser ce programme au sein des prisons de Toul et Ecrouves ; je vous remercie de m’avoir suivie et d’être membre du jury.
Sincères remerciements.
A toutes les personnes que j’ai rencontrées au centre de détention de Toul,
Je vous remercie pour l’accueil que vous m’avez réservé au sein de votre équipe. Merci de m’avoir suivie durant l’évolution de ma thèse.
Sincères remerciements.
A mes parents,
Et plus particulièrement ma maman qui m’a soutenue pendant toutes mes études. Merci d’avoir été présente dans les moments de doute et à la veille de tous mes examens.
Je vous aime.
A mon frère,
Pour tous les bons moments passés ensemble.
A mon oncle et ma tante,
Je vous remercie de m’avoir écoutée tout au long de mes 6 années d’études.
A ma grand-mère,
Aux membres de ma famille que je n’ai pas cités, Un clin d’œil aux « dindes »,
Grand merci à vous 6, vous avez su rendre mes études inoubliables et remplies de souvenirs. J’espère que notre amitié n’est qu’à son début.
12
A Caro, ma binôme de TP, et nos longues nuits de travail sur nos rapports en 2ème et 3ème
année.
A Lucie et Markus, sans vous la 1ère année aurait été beaucoup plus difficile ; je vous souhaite
13
SOMMAIRE
LISTE DES ABBREVIATIONS………17
INTRODUCTION………...18 1ère PARTIE : LE DIABETE DE TYPE 2 I. EPIDEMIOLOGIE ... 21 1. INTERNATIONALE ... 21 2. FRANCAISE ... 22 3. EN PRISON ... 22 II. ETIOLOGIE ... 23 III. PHYSIOPATHOLOGIE ... 23 1. MECANISME DE L’INSULINORESISTANCE ... 24 2. L’HYPERINSULINISME ... 25 3. L’INSULINODEFICIENCE ... 26 IV. DEPISTAGE ... 26 1. DEPISTAGE GENERALISE ... 26
2. PREMIER DEPISTAGE A L’ENTREE EN DETENTION ... 27
V. DIAGNOSTIC ... 28
VI. PREDISPOSITIONS AU DIABETE DE TYPE 2 ... 29
1. INFLUENCE DE L’ENVIRONNEMENT ... 29
2. UNE PART DE GENETIQUE…... 29
VII. DES COMPLICATIONS EVITABLES ... 30
1. MICROANGIOPATHIE DIABETIQUE ... 32
a. La neuropathie ... 32
b. La rétinopathie ... 33
c. La néphropathie ... 35
2. LA MACROANGIOPATHIE DIABETIQUE ... 36
3. LES COMPLICATIONS INFECTIEUSES ... 38
4. COMPLICATIONS METABOLIQUES AIGÜES ... 38
a. L’acidocétose diabétique ... 38
14
c. L’hypoglycémie ... 41
VIII. TRAITEMENT DU DIABETE DE TYPE 2 : LES ANTIDIABETIQUES ORAUX ... 42
1. LES BIGUANIDES ... 42
2. LES SULFAMIDES HYPOGLYCEMIANTS ... 44
3. LES GLINIDES ... 44
4. LES INHIBITEURS DES α-GLUCOSIDASES ... 45
5. LES GLIPTINES ET ANALOGUES DU GLP-1 ... 45
a. Rappels ... 45
b. Les gliptines : inhibiteurs de DPP4 ... 46
c. Analogues du GLP-1 ... 46
6. ET L’INSULINE ? ... 47
7. STRATEGIE THERAPEUTIQUE ... 48
8. MEDICAMENTS DISPONIBLES A L’UCSA DE TOUL ... 49
IX. LE PROBLEME DE L’OBSERVANCE ... 50
1. ENQUETE SUR L’OBSERVANCE AUX ADO ... 50
2. ENQUETE SUR L’OBSERVANCE A L’INSULINE... 51
2ème PARTIE : L'EDUCATION THERAPEUTIQUE DU PATIENT I. HISTORIQUE DE L’EDUCATION THERAPEUTIQUE DU PATIENT ... 54
II. HISTORIQUE DE L’EDUCATION THERAPEUTIQUE DU DIABETE ... 55
III. DEFINITION ET BUTS DE L’ETP ... 55
IV. DIFFERENTES MODALITES D’EDUCATION THERAPEUTIQUE ... 57
V. LES 4 ETAPES DE L’EDUCATION DU PATIENT ... 58
1. ELABORER UN DIAGNOSTIC EDUCATIF ... 58
a. Fonction pour le patient ... 59
b. Fonction pour le soignant ... 59
2. DEFINIR UN PROGRAMME PERSONNALISE D’ETP ... 59
3. MISE EN ŒUVRE DE SEANCES D’ETP ... 61
a. Les séances collectives ... 61
b. Avantages et inconvénients de l’enseignement en groupe ... 62
c. Les séances individuelles ... 62
15
e. Alternance de séances collectives et individuelles ... 63
4. L’EVALUATION DES COMPETENCES ... 64
VI. RESUME DES 4 ETAPES DE L’ETP ... 65
VII. A QUI PROPOSER UNE EDUCATION THERAPEUTIQUE ? ... 666
3ème PARTIE : ELABORATION D'UN PROGRAMME ADAPTE AU MILIEU CARCERAL I. JUSTIFICATION DE L’ETUDE ... 68
II. MATERIEL & METHODE ... 68
1. APPELLATION DU PROGRAMME ... 68 2. POPULATION ... 69 3. ENVIRONNEMENT ... 69 4. L’EQUIPE MEDICALE ... 69 5. METHODES ... 70 a. Contrat ... 70
b. Fiche de diagnostic educatif ... 70
c. Questionnaires de motivation ... 71
d. Formation(s) de l’équipe infirmier(es) ... 72
e. Liaison avec la maison du diabète et de la nutrition de Nancy ... 73
f. Programmes personnalisés ... 74
g. Planning des seances d’etp ... 75
h. Aide apportée par les auxiliaires vidéo de Toul ... 75
i. Déclaration a l’agence régionale de sante ... 76
III. CONGRES SNPHPU AJACCIO ... 76
4ème PARTIE : RESULTATS DU PROGRAMME ETADIAP I. PREPARATION DES SEANCES D’EDUCATION THERAPEUTIQUE ... 78
1. REPARTITION DES TRAITEMENTS ... 78
2. DIAGNOSTICS EDUCATIFS ... 79
3. NOUVEAUX ARRIVANTS ... 80
4. DONNEES BIOLOGIQUES AVANT LES SEANCES D’ETP ... 80
16
II. DEROULEMENT DES SEANCES D’ETP ... 82
1. TABLEAU DE PRESENCE DES PERSONNES DETENUES EN FONCTION DES SEANCES ... 82
2. SEANCE 1 : EXPLICATIONS DE LA MALADIE ET COMPLICATIONS ... 82
3. SEANCE 2 : L’INSULINE ... 82
4. SEANCE 3 : LES ANTIDIABETIQUES ORAUX ... 83
5. SEANCE 4 : LE PIED DIABETIQUE ... 83
6. SEANCE 5 : DIABETE ET ALIMENTATION ... 83
III. CREATION D’UN LIVRET PATIENT ... 84
IV. RESULTATS BIOLOGIQUES APRES ETP ... 85
1. HbA1c ET GLYCEMIE ... 85
V. CONCLUSION ET PERSPECTIVE ... 86
REFERENCES BIBLIOGRAPHIQUES………144
LISTE DES FIGURES……….148
17
LISTE DES ABREVIATIONS
ALD : Affection de Longue Durée HAS : Haute Autorité de Santé
OMS : Organisation Mondiale de la Santé
ALFEDIAM : Association de Langue Française pour l’Etude du DIAbète et des Maladies métaboliques
SFD : Société Francophone du Diabète
ANAES : Agence Nationale d’Accréditation et d’Evaluation de la Santé ADA : American Diabetes Association
UCSA : Unité de Consultations et de Soins Ambulatoires
DCCT: The Diabetes Control and Complications Trial Research Group INPES : Institut National de Prévention et d’Education pour la Santé ADO : AntiDiabétiques Oraux
ETP : Education Thérapeutique du Patient MDN 54: Maison du Diabète et de la Nutrition HDL : High Density Lipoprotein
IMC : Indice de Masse Corporel MHD : Mesures hygiéno-Diététiques IAG : Inhibiteur des α-Glucosidases
IST : Infections Sexuellement Transmissibles NC : Non Communiqué
IDE : Infirmière Diplômée d’Etat
SNPHPU : Syndicat National des Pharmaciens Praticiens Hospitaliers et Praticiens Hospitaliers Universitaires
18
INTRODUCTION
De nombreux faits divers défrayent régulièrement la chronique dans le milieu carcéral (suicides, violences…). Ces dernières années, plusieurs accidents survenus dans la prise en charge des personnes détenues diabétiques ont été dévoilés.
En 2008, Monsieur R.M, 19 ans, était placé dans une cellule disciplinaire de la maison d’arrêt de Mulhouse(1). Diabétique, il s’est injecté une surdose d’insuline et a sombré dans un coma
profond. Le jeune homme aurait été victime d’une « crise » d’hypoglycémie. Plus de douze heures se seraient écoulées, selon la plaignante, entre le début de la « crise » et le transfert à l’hôpital. Ses parents ont porté plainte pour non assistance contre l’administration pénitentiaire. En février 2011, un non-lieu a été prononcé pour l’administration de la prison de Mulhouse.
Monsieur K.N, 26 ans, diabétique insulino-dépendant, détenu à la prison de Toulon, a été retrouvé mort, le 24 août 2000 au matin, dans la cellule 315 de la prison de Toulon(2). Le
médecin légiste, après autopsie du corps, a conclu que le décès était survenu après un coma hypoglycémique.
Parallèlement, les programmes d’éducation thérapeutique diabétique se multiplient de plus en plus depuis plusieurs années dans le monde mais également en France. Cependant, ces programmes ne sont que très peu développés en milieu carcéral.
Qu’en est-il des patients diabétiques incarcérés ?
L’objectif de notre étude est de transmettre aux patients une meilleure connaissance de leur maladie et de leurs médicaments mais également de leur permettre de mieux vivre avec celle-ci.
19
Dans une première partie, nous nous intéresserons au diabète de type 2 et ses particularités de prise en charge en prison, ses complications et ses traitements.
Nous aborderons également l’avancée de l’éducation thérapeutique dans cette maladie chronique et son intérêt, particulièrement, pour les personnes incarcérées.
Dans une seconde partie, nous présenterons l’étude que nous avons développée, les méthodes et le matériel utilisés ainsi que les objectifs attendus.
Dans une troisième partie, nous exposerons les résultats de notre programme d’éducation thérapeutique diabétique de type 2 adapté au centre de détention de Toul (54).
20
1
ère
PARTIE :
21
I. EPIDEMIOLOGIE
1. INTERNATIONALE
Par l’absence de symptômes immédiats, le diabète de type 2 anciennement appelé diabète non insulino-dépendant, a une prévalence difficile à établir mais il est certain que le nombre de patients atteints croit d’année en année dans tous les pays du monde.
Selon le rapport de la SFD (Société Francophone du Diabète), anciennement appelée ALFEDIAM, de 2008, le diabète de type 2 représente plus de 90 % de l’ensemble des diabétiques(4).
Aujourd’hui, on dénombre environ 175 millions de patients diabétiques de type 2 sur le plan mondial (figure 1). Et ce chiffre est estimé à passer à 300 millions en 2025 soit une augmentation de plus de 71,5%.
22
La prévalence1 du diabète non insulinodépendant fluctue d’un pays à un autre, on constate
qu’elle est plus élevée en Chine, en Inde et aux Etats-Unis.
Des études ont montrées qu’il n’y a pas de différences significatives de prévalence entre les femmes et les hommes.
2. FRANCAISE
Différentes enquêtes menées ces 20 dernières années en Belgique, en France et dans le Grand Duché de Luxembourg montrent que la prévalence du diabète diagnostiqué dans chacun des trois pays est proche de 3%(6).
En France, c'est l'Alsace qui détient le plus grand nombre de diabétiques de type 2 avec une prévalence dans cette région de 6,5%.
Le diabète de type 2 est au premier rang des déclarations ALD et des causes d’hospitalisation en Lorraine et représente 1500 décès par an.
3. EN PRISON
En France, on dénombre 191 prisons regroupant 66 445 personnes détenues, nouveau « record » au dernier recensement de mars 2012. Le nombre de personnes détenues atteint un nouveau record en France.(7)
Le nombre de personnes détenues diabétiques insulinotraités ou non est encore mal connu. Une équipe dijonnaise a réalisé un questionnaire qu’elle a ensuite envoyé à l’ensemble des centres de détention français pour estimer la prévalence du diabète insulinotraité.
23
Cent soixante trois questionnaires ont été envoyés, cent treize ont été retournés complétés. Parmi toutes ces prisons, 60% ont déjà eu à prendre en charge un patient diabétique insulinotraité ; avec une moyenne d’âge de 44 ans(8).
II. ETIOLOGIE
Le diabète de type 2 est une maladie chronique, qui touche en général les plus de 40 ans et qui résulte de la conjonction de plusieurs facteurs de risque et d’environnement ; au premier rang de celles-ci, les modifications des comportements alimentaires avec la consommation excessive de sucres rapides et de graisses saturées, le vieillissement des populations ainsi que la sédentarité et l’absence d’activités physiques régulières semblent être les causes d’apparition d’un diabète de type 2.(5)
III. PHYSIOPATHOLOGIE
Le pancréas est constitué d’îlots de Langerhans, ceux-ci étant composé de 4 types cellulaires principaux : les cellules β (celles qui nous intéressent dans le diabète de type 2), les cellules α, δ et PP(9). Ces cellules produisent respectivement l’insuline, le glucagon, la somatostatine et le polypeptide pancréatique ; à l’état physiologique, la glycémie est tenue en équilibre grâce à l’adaptation des sécrétions d’insuline et des sécrétions de glucagon (figure 2). Le glucagon avec son action opposée à celle de l’insuline permet l’hydrolyse du glycogène hépatique en glucose ceci concourant à l’augmentation de la glycémie.
24 Figure 2 : Mécanisme de maintien de l'équilibre glycémique
L’anomalie métabolique fondamentale du diabète non insulino-dépendant est l’insulinorésistance des tissus périphériques (foie, muscles et tissus adipeux). Cette phase est accompagnée d’une hypersécrétion insulinique pour compenser. La dernière étape est l’insulinodéficience qui apparait 10 à 20 ans après le début de la maladie.
1. MECANISME DE L’INSULINORESISTANCE
L’insulinorésistance se traduit par une diminution de l’efficacité de l’insuline (figure 3) sur ses tissus cibles, et plus particulièrement le tissu musculaire(10). En effet, un excès de graisses au niveau du tissu adipeux viscéral libère une grande quantité d’acides gras libres dans la circulation sanguine. Ceux-ci sont responsables d’une synthèse hépatique accrue de triglycérides et favorise la néoglucogénèse hépatique.
Au niveau musculaire, une compétition entre ces acides gras libres et le glucose se met en place. Les acides gras libres sont plus facilement oxydés et sont donc dégradés en priorité. La
25
glycémie reste stable et de plus cette oxydation préférentielle entraine une production d’acétyl CoA qui inhibe en retour les enzymes de la glycolyse.
Figure 3 : Mécanisme de l'insulinorésistance(10)
2. L’HYPERINSULINISME
L’insulinorésistance est responsable de l’absence de diminution de la glycémie. Pour se défendre, l’organisme réagit en augmentant la production d’insuline par le pancréas permettant d’obtenir une réponse quantitativement normale.
26
3. L’INSULINODEFICIENCE
Après de nombreuses années de « contrôle », le pancréas cesse de sécréter les quantités nécessaires d’insuline ce qui entraine une remontée de la glycémie supérieure à 1,20 g/L à jeun. On parle alors d’insulinopénie.
IV. DEPISTAGE
1. DEPISTAGE GENERALISE
Selon une définition stricte de l’ADA (American Diabetes Association), le dépistage correspond à la découverte de patients asymptomatiques(11). En revanche, la découverte de
patients avec des symptômes correspondrait à une démarche de diagnostic. Mais selon l’OMS, cette définition s’élargit et concerne aussi bien les cas de patients asymptomatiques que les cas symptomatiques non décelés.
Aujourd’hui, le dépistage devient systématique dans des contextes d’obésité, d’hérédité ou de risques cardiovasculaires.
Selon le rapport de l’ANAES de février 2003, le dépistage du diabète de type 2 concerne toutes personnes de plus de 45 ans ayant au moins un des facteurs de risques suivants(11) :
- Découverte antérieure d’une glycémie à jeun perturbée ou d’une intolérance au glucose
- Origine non caucasienne et/ou migrant
- Excès pondéral (IMC > 27 kg/m² chez l’homme et 26 kg/m² chez la femme) - Hypertension artérielle (> 140/90)
- HDL < ou = 0.35 g/L et/ou triglycérides > ou = 2 g/L et/ou dyslipidémie traitée - Diabète familial au premier degré
27
- Femme ayant fait un diabète gestationnel ou ayant accouché d’un enfant de plus de 4kg
- Sujet en situation de précarité (SDF...)
Le dépistage s’effectue par un test de glycémie à jeun. Un test positif donne une glycémie > 1,26 g/L. un second test devra alors être réalisé pour confirmer les premiers résultats.
En cas de résultat négatif, le test devra être répété tous les 3 ans et un suivi plus rapproché sera mis en place en cas de présence d’un ou plusieurs facteurs de risques.
2. PREMIER DEPISTAGE A L’ENTREE EN DETENTION
La loi n° 94-43 du 18 janvier 1994, publiée par le Haut Comité de la santé publique sur la santé en milieu carcéral, a profondément modifié le principe de prise en charge des personnes détenues à leur entrée en centre de détention(12). Cette loi a permis de déléguer cette prise en
charge au service public hospitalier.
La circulaire du 8 décembre 1994 a émis comme but de donner à la population carcérale une qualité et une continuité des soins analogues à celles offertes à l’ensemble de la population.
Des Unités de Consultations et de Soins Ambulatoires ont été créées. Ceci a permis de proposer à chaque nouvel arrivant, un dépistage plus complet, une prise en charge et un suivi médical tout au long de son incarcération.
Prévue par l’article D285 du Code de procédure pénale, cette première visite (la seule obligatoire tout au long de la détention) doit être effectuée dans des délais les plus brefs et a pour objectif de « déceler toute affection de nature contagieuse ou évolutive qui nécessiterait des mesures d’isolement ou de soins urgents ».
28
Le dossier médical, constitué par l’infirmier(ère), comporte des recherches sur des antécédents de maladie ou des pathologies en cours de traitement (VIH, hépatite B et C) ainsi qu’un premier bilan psychologique de l’incarcération. Ensuite, sont effectuées des mesures biologiques (albuminurie, glycosurie, cétonurie) et biométriques (poids, taille, pression artérielle), une visite médicale et un bilan dentaire ; ainsi qu’une radiographie pulmonaire permettant le dépistage de la tuberculose(13).
V. DIAGNOSTIC
Un sujet non diabétique a une glycémie qui fluctue entre 0,7 à 0,8 g/L tout en ne dépassant pas 1,0 g/L à jeun et 1,4 g/L dans les périodes postprandiales.
Le diagnostic positif d’un diabète de type 2, selon le rapport de l’OMS (Organisation Mondiale de la Santé) de 1999 et celui de l’ANAES de janvier 1999, se base sur :
- Une glycémie à jeun (au moins 8 heures de jeûne) > 1,26 g/L ou 7 mmoles/L à deux reprises
- Ou une glycémie > 2 g/L ou 11 mmoles/L à n’importe quelle heure de la journée. Si le résultat de l’examen glycémique se situe entre 1 g/L et 1,25 g/L, le diagnostic d’un diabète de type 2 ne peut être posé mais on supposera légitimement une intolérance au glucose pouvant évoluer vers un diabète de type 2. Il sera alors nécessaire de mettre en place des mesures de prévention comme une activité physique et/ou une modification de l’alimentation.
29
VI. PREDISPOSITIONS AU DIABETE DE
TYPE 2
1. INFLUENCE DE L’ENVIRONNEMENT
La sédentarité, les mauvaises habitudes alimentaires (consommation excessive de sucres rapides et/ou de graisses saturées) ainsi qu’une obésité androïde2, également appelé obésité abdominale sont les trois causes responsables du déclenchement du processus de résistance à l’insuline.
Cependant, on ne peut pas imputer entièrement aux facteurs environnementaux et personnels, le développement d’un diabète de type 2.
En effet, on a constaté que certaines familles étaient dites « diabétiques » par la présence de nombreux diabétiques au sein de la même famille tandis que d’autres sont totalement épargnées de cette maladie. Il est donc légitime de parler d’un caractère génétique dans le développement d’un diabète de type 2(10).
2. UNE PART DE GENETIQUE…
L’existence d’un terrain génétique doit être évoquée mais il est encore difficile aujourd’hui de déterminer exactement quels sont les gènes véritablement impliqués.
Dans le développement du diabète de type 2, on parle de gènes de susceptibilité ou de prédisposition ; en effet, ces gènes ne sont ni nécessaires (certains diabétiques de type 2 ne l’ont pas), ni suffisants (les facteurs environnementaux jouent un rôle très important comme décrit précédemment).
30
Ces gènes prédisposent donc à la maladie mais ne conduisent pas inéluctablement à l’apparition d’un diabète.(10)
L’institut Pasteur de Lille a créé une banque d'ADN de familles diabétiques. Celle-ci regroupe les dons de plus de 2500 individus, issus de plus de 450 familles et permet d’identifier un maximum de ces gènes.
A travers les travaux de nombreuses équipes réparties dans le monde entier, plusieurs gènes ont été identifiés comme augmentant les risques de diabète. L’exemple du gène de la
glycogène synthase a été mis en évidence dans plusieurs études.
Ce gène code une enzyme participant au métabolisme du glucose. Cette enzyme permet l’ajout et la fixation de nouveaux résidus de glucose à une molécule de glycogène, forme de stockage du glucose au niveau hépatique et musculaire. Il apparait que cette enzyme a une activité diminuée chez les patients diabétiques de type 2.
D’autres gènes semblent être liés à l’apparition d’un diabète non insulino-dépendant et sont en cours de recherche.
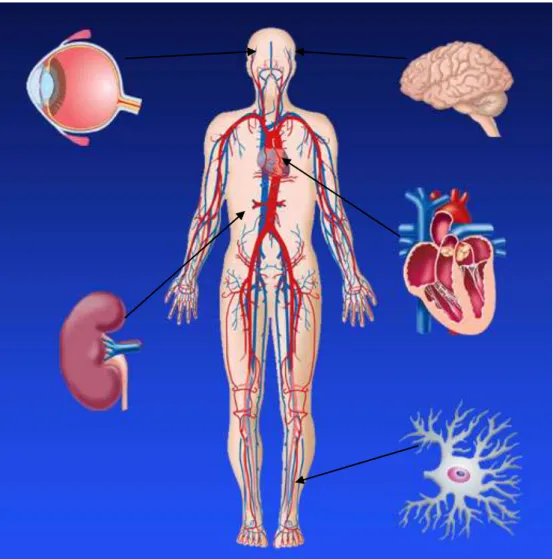
VII. DES COMPLICATIONS EVITABLES
Le diabète de type 2 est une maladie chronique qui peut entrainer des complications (figure 3) si ce dernier n’est pas bien pris en charge(14).
Quatre complications :
- La microangiopathie (atteinte des artérioles et capillaires) - La macroangiopathie
31
- Les complications infectieuses
- Les complications métaboliques aigües
32
1. MICROANGIOPATHIE DIABETIQUE a. La neuropathie
Elle touche aussi bien les diabétiques insulinodépendants que les diabétiques non insulinodépendants. Il s’agit d’une atteinte des nerfs périphériques.
L’existence d’une hyperglycémie chronique dans l’apparition d’une neuropathie a été révélée par une étude du DCCT : The Diabetes Control and Complications Trial Research Group(15).
Cette étude concerne des patients indemnes de neuropathie lors de leur inclusion dans l’étude ; puis leur suivi sous insulinothérapie intensive pendant 5 ans. On note une diminution de 69% de l’apparition de neuropathie chez ces patients en comparaison à des diabétiques sous insulinothérapie conventionnelle (1 à 2 injections d’insuline par jour).
En dehors de ces données, on constate à l’inverse qu’environ 50% des patients (quel que soit leur diabète et leur équilibre glycémique) ne présentent pas d’évolution vers une neuropathie clinique.
Ceci suggère la participation d’autres facteurs dissociables de l’état d’hyperglycémie chronique comme des facteurs héréditaires (mère et/ou père atteints de diabète associé à une neuropathie). On constaterait notamment une prévalence importante de neuropathie dans certaines populations : indienne, nord-africaine.
La clinique se manifeste par : des troubles sensitifs :
- Paresthésies
- Douleurs musculaires
33
- Douleurs d’allure névralgique
Des troubles moteurs (dont la fréquence est inférieure à celle des troubles sensitifs) :
- Paralysies
- Atrophie de certains muscles Une aréflexie achilléenne bilatérale
b. La rétinopathie
Complication la plus silencieuse du diabète, la rétinopathie touche, dans les pays développés, 2% de la population diabétique.
Elle se traduit par une baisse de l’acuité visuelle et même de cécité, cette complication est corrélée à un mauvais équilibre glycémique.
Les premiers signes d’une baisse d’acuité visuelle témoignent déjà de lésions avancées de la rétinopathie.(16)
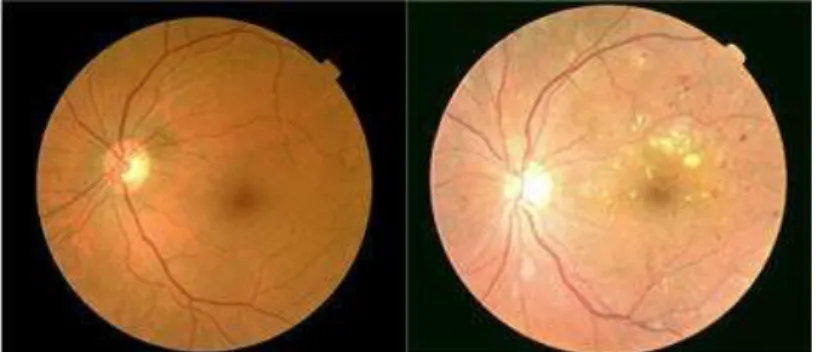
Le diagnostic s’effectue sur un fond d’œil (figure 5) réalisé annuellement parfois complétée par une angiographie rétinienne.
Un suivi régulier des patients atteints de diabète de type 1 et 2, tous les ans, est donc indispensable pour surveiller et éviter ces complications. On estime qu’au bout de 20 ans 33% des diabétiques de type 2 seront atteint d’une rétinopathie diabétique.
Figure 5 : A gauche, un fond d'œil normal, à droite un fond d'œil avec rétinopathie évoluée.
34
Le dépistage d’une rétinopathie s’effectue selon le mode suivant : (16)
Figure 6 : dépistage d'une rétinopathie (16)
La rétinopathie évolue sur deux modes différents :
- L’ischémie se traduit par l’apparition d’hémorragies intra-rétiniennes (petits points rouges sur l’examen de fond d’œil) mais également par l’apparition de néo-vaisseaux intra rétiniens menaçant de se rompre à tout moment et de provoquer des hémorragies.
35
- L’œdème maculaire se développe par accumulation de sang ou de liquide dans la macula, responsables de lésions des cellules visuelles ; le premier symptôme sera une diminution de l’acuité visuelle.
L’hypertension artérielle est un facteur aggravant de rétinopathie diabétique. c. La néphropathie
L’atteinte du rein, et plus spécifiquement du glomérule rénal, dans le diabète de type 2 est beaucoup moins fréquente que les complications vues précédemment.
Chaque rein est composé d’environ 1200000 glomérules ; ceux-ci ont un rôle important dans la filtration du sang, le passage de l’eau et des composés de faibles poids moléculaires dans le tube urinifère. Une grande partie de ceux-ci est réabsorbé, le reste forme l’urine.
Lorsque le glomérule est atteint, on parle de glomérulopathie. On remarque alors une augmentation de l’albumine dans les urines, qui au fur et à mesure s’accentue et signe la baisse d’activité de filtration du rein.
On parle alors d’insuffisance rénale. Le diagnostic s’établit sur la mesure de l’urée et de la créatinémie et du calcul de la clairance rénale.
Tableau I : Classification de la maladie rénale chronique d'après ANAES 2002
Stades Définitions DFG (ml/min/1,73 m²)
1 Maladie rénale chronique avec DFG ≥ 60 ≥ 60
2 IRC modérée 30-59
3 IRC sévère 15-29
36
2. LA MACROANGIOPATHIE DIABETIQUE
A l’inverse de la microangiopathie, on appelle macroangiopathie, l’atteinte des artères. Il s’agit de l’athérosclérose. Ce n’est pas le diabète qui est responsable de l’apparition de l’athérosclérose mais celui-ci accentue les facteurs de risque déjà présents chez le sujet atteint (hypercholestérolémie, hypertension artérielle, dyslipidémie). L’athérosclérose est définie comme un dépôt de plaques lipidiques sur les parois d’une artère formant l’athérome, bouchant au fur et à mesure la lumière de cette artère.
Les artères les plus couramment touchées sont celles du cœur, des membres inférieurs et du cou. Chaque localisation est responsable d’une complication particulière.
Dans l’évolution de la plaque d’athérome, le plus dangereux est d’aboutir à son détachement ; l’infiltration de monocytes dans le sous-endothélium de l’artère, se différenciant ensuite en macrophages et se multipliant entrainent une réaction inflammatoire et la fragilisation de la plaque ; s’en suit une fracture en multiples morceaux pouvant migrer vers d’autres localisations. (Figure 7)
37
Figure 7 : évolution d'une plaque d'athérome (17)
Au niveau du cœur, ce sont les artères coronaires qui sont impliquées ; ceci pourra entrainer de l’angor voire un infarctus du myocarde. Au niveau des jambes, le risque d’artériopathie des membres inférieurs est à craindre ; les premiers symptômes débutent par une réduction du périmètre de marche due à des douleurs ressenties dans les mollets ; les complications peuvent aller jusqu’à la gangrène et l’amputation. Concernant les carotides, le danger est l’accident vasculaire cérébral (AVC) amenant parfois de graves conséquences (hémiplégie, troubles de la déglutition…).
38
3. LES COMPLICATIONS INFECTIEUSES
On estime à près de 10000 le nombre d’amputations par an dues au diabète. Plus de la moitié de ces amputations pourraient être évitées. Ces complications infectieuses touchent plus particulièrement les pieds.
Ceci a valu la désignation de « pied du diabétique », toute infection des pieds d’un patient atteint de diabète de type 1 ou 2 ; il est donc nécessaire de dépister les diabétiques à risque podologique élevé.
Quels sont les diabétiques à risque ?
Comme décrit auparavant, la neuropathie diabétique est responsable d’une perte de sensibilité au niveau des pieds, facteur de risque d’une non prise en charge d’une plaie ou d’une blessure. L’infection est donc souvent soignée tardivement et peut amener à des complications.
L’artériopathie des membres inférieurs a une part importante dans la survenue et la non guérison des plaies ; en effet, la cicatrisation d’une blessure nécessite un apport en oxygène 20 fois plus important que pour le maintien du tissu cutané. Mécanisme qui ne peut pas être mis en jeu lorsqu’une artériopathie existe. Le risque final de ces infections est l’amputation.
4. COMPLICATIONS METABOLIQUES AIGÜES
a. L’acidocétose diabétique
Egalement appelé coma acidocétosique, l’incidence annuelle de cette complication est d’environ 4%.
Dans les conditions normales, lors d’un jeûne, le déclenchement de voies métaboliques permet à l’organisme de puiser dans ses réserves et de fournir l’énergie nécessaire au fonctionnement de ses organes. Le cœur, par exemple, utilise les acides
39
gras provenant du tissu adipeux et les corps cétoniques produits par leur métabolisme hépatique ; le cerveau, utilise la néoglucogénèse.
Ce mécanisme tend à faire augmenter la quantité de corps cétoniques présents dans l’organisme ; ceux-ci réalisent une insulinosécrétion basale. Cette sécrétion d’insuline freine en retour le mécanisme de lipolyse et donc la production de corps cétoniques.
Chez le patient diabétique, l’insulinosécrétion basale ne peut pas se faire et le taux d’acides gras est alors 2 à 4 fois plus élevé. Un cercle vicieux se met alors en place puisque ces acides gras seront oxydés en Acétyl-Coenzyme A, qui synthétisera de nouveau des corps cétoniques.
Les deux principaux corps cétoniques retrouvés sont l’acide acéto-acétique (décarboxylé en acétone) et l’acide β-hydroxybutyrique. On parle alors de cétose.
40 Figure 8 : L'acidoacétose diabétique
Le traitement immédiat de l’acidocétose est l’administration d’insuline à doses modérées, de l’ordre de 10 unités/heure, ceci jusqu’à rétablissement des valeurs biologiques.
41 b. Le coma hyperosmolaire
A 95%, il est retrouvé chez les diabétiques de type 2. Il s’agit d’une déshydratation massive (déclenchée par des diarrhées, vomissements, la prise de diurétiques ou de corticoïdes) associée à une osmolarité > 350 mmoles/L.
L’hyperglycémie initiale entraine une polyurie, qui n’est pas compensée par des apports hydriques suffisants ; une hypovolémie apparait, et évolue vers une insuffisance rénale dite fonctionnelle.
c. L’hypoglycémie
Cette complication du traitement est fréquente avec certains antidiabétiques oraux (ADO) et peut entrainer de graves conséquences. La principale famille mise en cause est celle des sulfamides hypoglycémiants.
On parle d’hypoglycémie diabétique lorsque la glycémie est à < 0,70 g/L(18).
Il est possible qu’aucune gêne ou symptôme ne soit ressentis par le patient, la glycémie peut alors descendre à 0,50 g/L, on parle d’hypoglycémie non ressentie.
Les prodromes d’une hypoglycémie sont neurovégétatifs : sensation de jambes en coton, vertiges, bâillements, troubles de la vue, sensation de perte de connaissance imminente. Notre organisme réagit en libérant des hormones qui ont pour mission de déstocker le glucose au niveau du foie ; ces hormones auront des effets négatifs sur le muscle cardiaque ce qui ajoutera des perturbations comme des palpitations, des tremblements, une tachycardie.
Aux UCSA de Toul et Ecrouves le protocole de prise en charge est le suivant : - Chez un patient conscient et capable de déglutir :
Administration de 3 ou 4 morceaux de sucre ou une brique de jus de fruit. S’agissant de sucres rapides, la remontée de la glycémie est rapide. Afin de consolider cet état, il est
42
nécessaire d’administrer 30 minutes à 1 heure plus tard, un sucre lent tel que du pain, des céréales…
- Chez un patient non conscient et incapable de déglutir :
Une injection IV de 2 à 4 ampoules de glucose hypertoniques à 30% suivie d’une perfusion de glucose à 5 ou 10%.
Du glucagon en IM ou en sous-cutané peut être injecté chez le diabétique insulinodépendant (le glucagon est une hormone hyperglycémiante).
VIII. TRAITEMENT DU DIABETE DE TYPE 2 :
LES ANTIDIABETIQUES ORAUX
En première intention des mesures hygiéno-diététiques sont tout d’abord mises en place. Après 6 mois, si la glycémie ne se rectifie pas, un traitement par antidiabétique oral sera mis en place.
1. LES BIGUANIDES
Le seul représentant actuel en France est la metformine (Glucophage®500 – 850 – 1000 mg, Stagid®700 mg)
Il a comme propriétés de faire diminuer la néoglucogénèse hépatique et d’augmenter l’utilisation périphérique du glucose par le foie et le muscle squelettique.
Cet ADO est utilisé en première intention lors de l’instauration d’un traitement antidiabétique chez le diabétique de type 2.
43
La metformine peut être utilisée seule ou en association avec d’autres ADO. Initialement, le traitement débute par une posologie de 500 mg ou 850 mg de chlorhydrate de metformine 2 à 3 fois par jour, administrée au cours ou à la fin des repas.
Au bout de 10 à 15 jours, la posologie sera adaptée en fonction de la glycémie.
La metformine étant éliminée par le rein, une adaptation des doses en fonction de la fonction rénale du patient sera nécessaire ainsi qu’un contrôle régulier de celle-ci.
La dose maximale recommandée de metformine est de 3 grammes par jour, en trois prises distinctes.
L’alcool est déconseillé car il existe un risque majoré d’acidose lactique lors d’intoxication alcoolique aigue.
Lors de la nécessité d‘injection de produits de contraste iodés, il est nécessaire d’arrêter le traitement avant l’examen et celui-ci ne pourra être réintroduis que 48 heures après. En effet, l’injection peut entrainer une insuffisance rénale pouvant être responsable d’une accumulation de metformine.
Les effets indésirables les plus souvent rapportés sont les troubles digestifs (nausées, vomissements, diarrhées, douleurs abdominales er perte d’appétit). Dans la majorité des cas, ces effets indésirables régressent après quelques semaines de traitement. Pour minorer ces troubles digestifs, il est recommandé de prendre le comprimé de metformine pendant un repas. Une perturbation du goût peut également se manifester.
44
2. LES SULFAMIDES HYPOGLYCEMIANTS
Glimépiride (Amarel®), glibenclamide (Daonil® 5mg et 1,25 mg, Hémi-Daonil®2,5 mg), gliclazide (Diamicron®).
Les sulfamides agissent sur la libération d’insuline par le pancréas en augmentant sa sécrétion.
Le traitement débute initialement par une dose de ½ comprimé par jour. L’administration s’effectue généralement avant le petit déjeuner.
En entretien, la posologie maximale est de 3 comprimés par jour, en 2 à 3 prises distinctes.
Le miconazole en voie générale ou buccale peut être responsable d’une augmentation de l’effet hypoglycémiant. L’ensemble des formes de phénylbutazone majorent également le risque hypoglycémiant, il est donc préférable de choisir un autre anti-inflammatoire. L’association avec l’alcool entraine un effet antabuse (chaleur, rougeur, vomissement…) et augmente le risque hypoglycémique.
Le principal effet indésirable retrouvé avec les sulfamides hypoglycémiants est le risque d’hypoglycémie.
3. LES GLINIDES
Le seul représentant actuel commercialisé en France est le répaglinide (Novonorm®0,5 – 1 – 2 et 4 mg)
Il s’agit d’une classe pharmacologique beaucoup moins courante. Ils ont le même mode d’action que les sulfamides hypoglycémiants. Ils peuvent être utilisés seuls ou en association avec la metformine.
45
La dose initiale lors de l’instauration d’un traitement est de 0,5 mg et sera augmentée si besoin 1 à 2 semaines après. L’administration est préprandiale.
La dose maximale par jour est de 16 mg. La dose unitaire ne doit pas dépasser 4 mg. Le principal effet indésirable est le risque d’hypoglycémie.
4. LES INHIBITEURS DES α-GLUCOSIDASES
Le seul représentant actuel est l’acarbose (Glucor® 50 et 100 mg).
Ils diminuent l’hyperglycémie post-prandiale par inhibition des α-glucosidases intestinales. Le traitement initial est de 1 comprimé de 50 mg 3 fois par jour, celui-ci pourra être augmenté à 100 mg 3 fois par jour en fonction des paramètres glycémiques.
L’administration s’effectue avant les principaux repas.
Un inconfort intestinal ainsi que des diarrhées et des douleurs abdominales sont fréquemment rapportés.
5. LES GLIPTINES ET ANALOGUES DU GLP-1
a. Rappels
Suite à l’arrivée du bol alimentaire, les cellules de l’intestin libérent des facteurs peptidiques, GLP-1 et GIP. Ceux-ci augmentent de manière importante la réponse insulinique lorsque la glycémie est élevée.
Mais un système enzymatique dégrade rapidement ces peptides, les DPP4 (dipeptidyl peptidase 4) d’où une demi-vie très courte de 2 minutes.
46 b. Les gliptines : inhibiteurs de DPP4
Leur administration permet d’augmenter les taux de GLP-1 et GIP d’où une augmentation de la sécrétion d’insuline.
Deux représentants existent :
- Sitagliptine (Januvia®100 mg) - Vildagliptine (Galvus®100 mg)
Figure 9 : Action des gliptines
La dose usuelle de ce médicament est de 100 mg une fois par jour.
c. Analogues du GLP-1
Deux médicaments injectables en sous-cutanée :
- Exenatide (Byetta®10 µg/40mL – 5 µg/20 mL), naturellement résistant aux DPP4 - Liraglutide (Victoza®6 mg/mL), composé de synthèse résistant aux DPP4.
47
Leurs demi-vies fluctuent entre 2 et 3 heures.
Exenatide est instauré pendant 1 mois à la posologie de 5µg, au petit déjeuner et au diner. Cette dose peut par la suite être montée à 10µg deux fois par jour. Une posologie unique supérieure à 10µg/jour n’est pas recommandée. Un intervalle de 6 heures entre les deux injections est à respecter.
Liraglutide est initié à une posologie de 0,6 mg/jour pour limiter les problèmes
gastro-intestinaux. Après une semaine de traitement, la dose sera augmentée à 1,2 mg. Une posologie unique supérieure à 1,8 mg n’est pas recommandée.
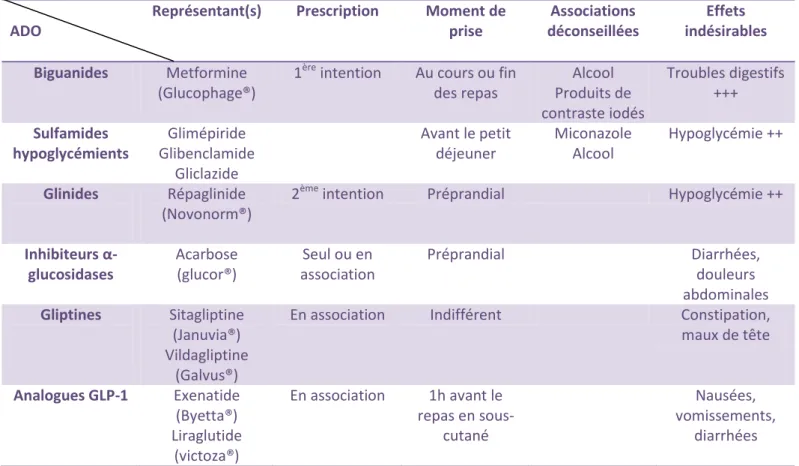
Tableau II: Récapitulatif des différents ADO disponibles ADO
Représentant(s) Prescription Moment de
prise Associations déconseillées Effets indésirables Biguanides Metformine (Glucophage®)
1ère intention Au cours ou fin
des repas Alcool Produits de contraste iodés Troubles digestifs +++ Sulfamides hypoglycémients Glimépiride Glibenclamide Gliclazide Avant le petit déjeuner Miconazole Alcool Hypoglycémie ++ Glinides Répaglinide (Novonorm®)
2ème intention Préprandial Hypoglycémie ++
Inhibiteurs α-glucosidases Acarbose (glucor®) Seul ou en association Préprandial Diarrhées, douleurs abdominales Gliptines Sitagliptine (Januvia®) Vildagliptine (Galvus®)
En association Indifférent Constipation,
maux de tête Analogues GLP-1 Exenatide (Byetta®) Liraglutide (victoza®) En association 1h avant le repas en sous-cutané Nausées, vomissements, diarrhées 6. ET L’INSULINE ?
La mise en place d’une thérapie par insuline lors d’un diabète de type 2 est le dernier recours pour équilibrer la glycémie. L’histoire naturelle de la maladie amène au bout de plusieurs
48
années, à l’apparition d’une insulinopénie. Les médicaments insulinosécréteurs ne sont donc plus d’aucun secours. L’injection d’insuline devient alors le seul moyen de contrôler la glycémie.
L’insuline fait diminuer à long terme le risque de développer des complications vasculaires, cardiologiques ou neurologiques.
7. STRATEGIE THERAPEUTIQUE
Tableau III : Stratégie thérapeutique du diabète de type 2
MHD : Mesures Hygiéno-Diététiques IAG : Inhibiteur des α-Glucosidases
49
8. MEDICAMENTS DISPONIBLES A L’UCSA DE TOUL
Les UCSA des centres de détention de Toul et Ecrouves sont rattachés à l’Hôpital Saint Charles de Toul ; les médicaments antidiabétiques disponibles pour l’UCSA sont donc ceux du livret de l’Hôpital (19). En cas de prescription d’un médicament qui n’est pas inscrit au
livret de l’hôpital, le pharmacien propose un équivalent de la même classe pharmacologique ou fait une commande exceptionnelle.
Tableau IV : ADO disponibles au livret du médicament du CH Saint Charles de Toul
ANTIDIABETIQUES ORAUX INSULINE
- Diamicron 30 mg - Insuline lantus 100 UI/mL OPTISET - Glimépiride 1 mg - Insuline levemir FLEXPEN
- Glimépiride 2 mg - Insuline novomix 30 FLEXPEN - Glimépiride 3 mg - Insuline novorapid FLEXPEN - Glimépiride 4 mg - Insuline umuline profil 30 PEN - Hémidaonil - Insuline insulatard FLEXPEN - Daonil 5 mg - Insuline umuline rapide Fl 10 mL - Glucophage 1000 mg - Glucophage 850 mg - Glucor 100 mg - Glucor 50 mg - Glucovance 500 mg / 5 mg - Novonorm 0,5 mg - Novonorm 1 mg - Januvia 100 mg
50
IX. LE PROBLEME DE L’OBSERVANCE
Selon Hippocrate : « les malades mentent souvent lorsqu’ils disent prendre leurs médicaments».
« L’observance au traitement est le degré de concordance entre le comportement d’un individu (prise de médicament, suivi d’un régime, modification du mode de vie), et la prescription médicale ».
1. ENQUETE SUR L’OBSERVANCE AUX ADO
Le service d’endocrinologie, diabétologie et maladies métaboliques du centre hospitalier universitaire IBN Sina de Rabbat au Maroc a réalisé une enquête, sur l’observance de 106 patients, aux ADO.
106 diabétiques de type 2 ont été suivis dont 62 femmes et 44 hommes. Le questionnaire se base sur la qualité de l’observance médicamenteuse ainsi que sur les causes de la mauvaise observance.
Résultats : 58 patients ont une bonne observance soit 55%,48 patients ont une mauvaise observance.
Parmi les 48 patients ayant une mauvaise observance, les causes de celle-ci ont été répertoriées :
51 0,00% 5,00% 10,00% 15,00% 20,00% 25,00% 30,00% 35,00% 40,00% 45,00% 50,00%
Graphique 1 : Causes de mauvaises observances des patients sous ADO
2. ENQUETE SUR L’OBSERVANCE A L’INSULINE
Une étude menée en 2007 auprès de 8926 personnes diabétiques tirées au sort a permis de mettre en évidence le problème de l’observance dans le traitement par insuline de leur diabète(15).
Ces patients étaient âgés d’au moins 18 ans ; un auto-questionnaire leur a alors été distribué composé de six questions.
4277 personnes ont répondu au questionnaire soit environ 48 %.
Le bilan de la bonne observance thérapeutique a été étudiée chez 237 patients diabétiques de type 1 ; la moyenne d’âge était de 42 ans.
Les auteurs montrent :
52
- Une observance moyenne dans 55% des cas soit 130 patients, - Une mauvaise observance dans 17% des cas soit 40 patients.
Après analyse de chaque cas, les facteurs associés à une mauvaise observance étaient par ordre croissant d’importance :
- Des recommandations pour le diabète trop lourde - Des difficultés financières
- Un indice de masse corporel (IMC) > 30 - Un âge < 25 ans
- Une mauvaise prise en charge par le médecin traitant
La conclusion de ces deux études va permettre d’adapter la prise en charge des patients atteints de diabète de type 2 traité par ADO et/ou insuline à travers un programme d’accompagnement et pourquoi pas d’éducation thérapeutique …
53
PARTIE 2:
L’EDUCATION THERAPEUTIQUE
DU PATIENT
54
I. HISTORIQUE DE L’EDUCATION
THERAPEUTIQUE DU PATIENT
Les années 1980 et suivantes, ont confirmées par de nombreuses études l’importance des projets d’ETP ; dans le cadre du diabète une diminution de 80% des comas et de 75% des amputations chez les patients malades valident ces hypothèses.(20)
En février 2001, le ministère chargé de la santé, représenté par Bernard KOUCHNER élabore le Plan National d’éducation pour la Santé.(20) Il s’agit du premier plan qui aborde l’éducation
thérapeutique du patient. Il développe l’ETP selon 3 grands axes :
- L’élaboration de modalités de financement spécifiques pour le diabète et l’asthme - La formation et la recherche
- Son intégration dans la procédure d’accréditation des établissements de santé.
En 2002, dans son rapport sur la santé en France, la Haut Comité de santé publique consolide l’importance de l’élaboration des projets d’éducation thérapeutique : « c’est la personne, dans sa singularité et sa globalité, qui est l’objet d’attention des soignants et non plus seulement l’organe atteint ».
Enfin la loi du 4 mars 2002 crée l’Institut National de Prévention et d’Education pour la Santé (INPES) responsable des missions dans l’éducation thérapeutique(20).
Entre 2002 et 2006, cette thématique est élargie dans des programmes nationaux portant sur l’asthme, la broncho-pneumopathie chronique obstructive (BPCO), le diabète, l’hépatite C et l’obésité.
En Avril 2007, la HAS donne l’impulsion à l’ETP en éditant le premier guide méthodologique. En Mars 2009, la loi Hôpital, patients, santé, territoire (HPST) inscrits l’ETP
55
dans le code de la Santé Publique. En Juin 2009, le manuel V2010 de certification des établissements de santé établit l’ETP comme un des critères de certification (critère 23.a) (21).
Aujourd’hui, les diplômes universitaires d’éducation thérapeutique du patient se multiplient.
II. HISTORIQUE DE L’EDUCATION
THERAPEUTIQUE DU DIABETE
La première grande étude est celle de Leona Miller(22) (1887-1981) en 1972 réalisé dans un
collectif de 6000 patients diabétiques au Los Angeles County Hospital.
Deux ans d’éducation thérapeutique aux malades ont permis de faire baisser fortement la morbidité.
L’apprentissage aux diabétiques, de leur pathologie, de leur traitement, a fait diminuer la durée de leur hospitalisation passant de 5,7 jours à 1,4 jours par an. Les consultations pour l’apparition de complications, comme les lésions infectieuses des membres inférieurs, sont passées de 320 à 40 par semaine.
Cette étude a permis de mettre en évidence la nécessité des programmes d’éducation thérapeutique chez les patients diabétiques.
III. DEFINITION ET BUTS DE L’ETP
Selon le rapport de l’OMS-Europe publiée en 1996, Therapeutic Patient
56
Disease, l’éducation du patient ou ETP « vise à aider les patients à acquérir ou maintenir les
compétences dont ils ont besoin pour gérer au mieux leur vie avec une maladie chronique. Elle fait partie intégrante et de façon permanente de la prise en charge du patient. Elle comprend des activités organisées, y compris un soutien psychosocial, conçues pour rendre les patients conscients et informés de leur maladie, des soins, de l’organisation et des procédures hospitalières, et des comportements liés à la santé et à la maladie. Ceci a pour but de les aider (ainsi que leur entourage) à comprendre leur maladie et leur traitement, collaborer ensemble et assumer leurs responsabilités dans leur propre prise en charge, dans le but de les aider à maintenir et améliorer leur qualité de vie. » (23)
Les finalités spécifiques de l’ETP sont : (figure 9)(24)
- l’apprentissage ou le maintien de compétences d’autosoins (soulager les symptômes, prendre en compte les résultats d’une autosurveillance, réaliser des gestes techniques et de soins…)
- l’acquisition de compétences d’adaptation (se connaitre soi-même, développer une réflexion critique, prendre des décisions et résoudre un problème…)
57
IV. DIFFERENTES MODALITES
D’EDUCATION THERAPEUTIQUE
58
V. LES 4 ETAPES DE L’EDUCATION DU
PATIENT
Selon la HAS, voici les différents éléments sur lesquels s’appuyer pour réaliser un programme d’éducation thérapeutique.
1. ELABORER UN DIAGNOSTIC EDUCATIF
Le diagnostic éducatif est une démarche d'identification des besoins du patient.(26)
Première étape d'une démarche d’éducation personnalisée, ce moment d'écoute est au service d'un cheminement pédagogique. Les informations utiles de la vie du patient : repères biomédicaux, environnement, activités, représentations, vécu, projets, sont prises en compte en vue de l'élaboration d'un programme éducatif personnalisé.
Ce diagnostic est un support d'entretien. Document à la disposition des soignants, il récapitule les paramètres renseignés au cours de la mise en place du suivi d'un patient, "au fil de l'eau". Il est composé de 4 grandes parties :
- Environnement professionnel, social et familial (peu développé dans notre situation « environnement carcéral ».)
- Situation affective et relationnelle, vécu du diabète - Compréhension et représentations vis à vis du diabète - Projets du patient
59
Les facteurs liés à la personne et ceux liés son environnement, et leur interaction mutuelle, sont donc pris en compte tout au long de la démarche éducative.
a. Fonction pour le patient
Cette narration lui permet de visualiser où il en est par rapport à sa maladie, de donner du sens à ce qu’il sait.
Cette phase peut faire émerger sa propre demande et a pour fonction d'engager sa motivation. Ce moment le positionne en tant qu'acteur, en coopération avec ses soignants.
b. Fonction pour le soignant
Cet entretien lui permet d’apprécier ce que sait le patient, d'identifier les représentations et les difficultés à prendre en compte, les atouts sur lesquels s'appuyer. Il peut proposer au patient un accompagnement éducatif adapté à ses besoins. Ceci peut le conduire à ajuster sa proposition thérapeutique.
La dernière page, est consacrée à la synthèse du diagnostic éducatif ; il s’agit d’une formulation écrite par le soignant, datée ; elle n'est pas confidentielle, et se partage avec lui.
2. DEFINIR UN PROGRAMME PERSONNALISE D’ETP
Le diagnostic éducatif va permettre la formulation des attentes du patient, les compétences qu’il souhaite acquérir ou celles qu’il souhaite développer.
Comme décrit auparavant, les compétences d’autosoins et d’adaptation sont majoritairement développées.