HAL Id: tel-01776877
https://hal.univ-lorraine.fr/tel-01776877
Submitted on 24 Apr 2018HAL is a multi-disciplinary open access
archive for the deposit and dissemination of sci-entific research documents, whether they are pub-lished or not. The documents may come from teaching and research institutions in France or abroad, or from public or private research centers.
L’archive ouverte pluridisciplinaire HAL, est destinée au dépôt et à la diffusion de documents scientifiques de niveau recherche, publiés ou non, émanant des établissements d’enseignement et de recherche français ou étrangers, des laboratoires publics ou privés.
toxico-pharmacologique de substances naturelles
hépatotropes
Pierre-Yves Arvis
To cite this version:
Pierre-Yves Arvis. Utilisation des hépatocytes en culture pour le criblage toxico-pharmacologique de substances naturelles hépatotropes. Médecine humaine et pathologie. Université Paul Verlaine - Metz, 1989. Français. �NNT : 1989METZ004S�. �tel-01776877�
AVERTISSEMENT
Ce document est le fruit d'un long travail approuvé par le jury de
soutenance et mis à disposition de l'ensemble de la
communauté universitaire élargie.
Il est soumis à la propriété intellectuelle de l'auteur. Ceci
implique une obligation de citation et de référencement lors de
l’utilisation de ce document.
D'autre part, toute contrefaçon, plagiat, reproduction illicite
encourt une poursuite pénale.
Contact : ddoc-theses-contact@univ-lorraine.fr
LIENS
Code de la Propriété Intellectuelle. articles L 122. 4
Code de la Propriété Intellectuelle. articles L 335.2- L 335.10
http://www.cfcopies.com/V2/leg/leg_droi.php
Thèse de Doctorat de l'Universlté de lletz llention .Scfences - option Toxicologie
UIILTSAII(DII DBS NBPâ'TOGYTBS BIf GULÎI,NE P(,t'R LB GR.TBI.AGB IOXrCO-PA.â'nI|.â'COL('GTQUB
DB SUBSÎAITGBS TTâ'II'N,ELLBS EBPAIOIN.OPBS
présentée et soutenue publiquenent le 4 iuillet 1989 par : Plerre-Yves ARUIS
Jtlembres du jury :
J.M. PELT, Professeur (Président du iury) A.l,l. BATT, Professeur (Rapporteur) J. FLEURENTIN, l'laître de conférences - D. GOUY, Docteur Vétérinaire (rapporteur)
F. l'lORTIER, Professeur (Directeur de thèse) J.J. SERRAN0, Professeur (Rapporteur)
Êo.^-
l't-
t"-S*
ô 11'^
hèo*,
T\û-
tÀLi^
tt
tr-- e
{*a-
[o. À-,*.,*i*
Je voudrais remercier:
Monsieur le Professeur J-M. PELT,
Président de l'lnstitr! Européen d'Ecologie et Directeur du laboratoire de Biologie Végétale et flarrygognosie du Centre des Sciences de l'Environnernent à Meu, pour m'avoir accuèilfi avec bienveillance dans son équipe au sein de laquelle ces travaux ont débulé et pour avoir accepté de présider ce jury.
Monsieur h Prcfesseu F. MORTIER,
Professeur de Pharmacognosie à la Faculté des Sciences Pharmaceutiques et Biologiques de Nancy I, pour avoir dirigé ce travail et m'avoir apporté compétences et soutien dans lès bons comme dans les mauvais moments.
Mademoiselle le Professeur A-M. BATT,
Professeur de Toxicologie à la Faculté des Sciences Pharmaceutiques et Biologiques de Nancy I, qui m'a "initié" aux processus de la lipoperoxidation dans son enseignement du D.EA. de Toxicologie de Metz, pour avoir accepté de juger ce mémoire et d'en être rapporteur.
Monsieur le Docteur D. GOljY,
Directeur du Service Commun de Toxicologie du Centre de Recherches Sanoli à Montpellier, qui a accepté de faire partie de ce jury et d'être rapporteur de ce mânoire en dépit de sès lourdes tâches.
Monsieur le Docteur J. FLEURENTIN,
Président de la Société Française d'Ethnopharmacologie et Maitre de Conference au laboratoire de Biologie Végétale et Pharmacognosie du Centre des Sciences de l'Environnement à Metz, pour m'avoii bien souvent eclairé par ses conseils et pour sa participation à ce jury.
Monsieur le Prcfesenr J-J. SERRANO.
Professeur de Pharmacodynamie à la'Faculté de Pharmacic de Montpellier, d'avoir répondu favorablement à notre invitation et pour l'honneur qu'il nous fait en faiiant partie de ce jury et d'avoir acæpté d'êtrc rapporteur.
aidé au cours de ces années :
* Au CenÈre des Sciences de I'Environnement à Met,z
Mademoiselle le Professeur P.. VASSEUR gui a toujours trouvé des noments pour me conseiller et me faire profit,er de ses
conpétences.
Monsieur le Docteur P. LEHR pour sa contribution aux essais de m i c r o s c o p i e é l e c t r o n i q : e à : b a l a y a g e .
Monsieur le Professeur J-C BLOCK, pour son sens. aigr de Ia c r i t i g u e p o s i t i v e .
L ' é g r r i p e d e s c o l l è g u e s T h é s a r d s d e l a P h a r m a c o . , I e " p e t i t " À l a i n ROLIÂND, Dominigrre BEAUX, Claire HOEFFÎ.ER, Marie-Claire I"ANHERS, Annett,e LEXA et Michel JOYEUX gui continue à malt,raiter les
h é p a t o c y t e s .
Les collègues Thésard,s des autres labos avec une ment,ion
particulière à Véronigr.re THARREÀU et, Jean-Pierre FIÂMBEÀU dont I ' a m i t i . é f u t s o u v e n t u n s e c o u r s .
Les membres permanents gui par leur gentillesse savent, créer un e s p r i t f a m i l i a l .
* Au Service Conmun de Toxicologie de SAI{OFI Recherches à M o n t p e l l i e r M o n s i e u r I e D o c t e u r P . V I C g u i a t o u j o u r s s u s e r e n d r e d i s p o n i b l e e t m e p r o d i g u e r s e s c o n s e i l s é c l a i r é s p o u r g u e c e t r a v a i l a b o u t i s s e . M a d e m o i s e l L e l e D o c t e u r N . B I C H E T g u i m ' a e n s e i g n é l ' a r t . e t l a m a n i è r e d e c u L t i v e r l e s c e l l u l e s e t d e l e s s o u m e t t r e a u x p i r e s s é v i c e s .
L'égr:ipe de Ia Section de Toxj-co-génétigue Monigue BONNERY, Catherine COHEN-SOLÀL, Anne-Françoise PELLOUX et Nathalie RÂOUST.
Monsieur le Doct,eur-Ingénieur B. BASUYAUX et ses techniciennes à gr:i 1'ont doit Ia mise au. poinÈ et la réalisat,ion des dosages de l ' a l b u r n i n e .
Les dj-fférents membres des sections du Servj,ce de Toxicologie dont bon nombre d'ent,re eux ont apport,é leur contribut,ion à ces Èravaux.
Madarne René RÂMUAI.DE avec guri j' ai longtemps partagé son bureau e t q u i n ' a b e a u c o u p d o n n é p a r s e s c o n s e i l s e t s o n a m i t , i é .
Je réserverais une place t,oute particulière à Patrice E'RÂNCOUR, p o u r g u i l e s e n s a i g u d e l ' a n i t i é p a s s e a u d e l a de tous les
AVAI{Î PROPOS.
1. INIRODUCTION.
2. AlrÀrYsE BrBLrOGRAPtlrQUe.
2L. LES MODEI.ES TOXICO-PHARMACOLOGf QUES in tritro.
22. LES HEPATOTOXIQUES.
22L. LE IETRACHLORURE DE CARBONE.
222 . tA D-GAI.ACTOSAI,IINE .
23. LES HEPATOTROPES.
3. MATERIEL ET METHODES.
31. PREPARATIONS DES EXTRAITS DE PLÀNTES.
311. EXTRÀITS AQUEUX BRUTS D' Eupatorium canna.blnun. 3 L 1 1 . L ' , E X T R À r r E 5 L 4 L - 3 4 .
3 L I 2 . L ' E X T R À I T R T ] . 0 9 6 .
3L2. EXTRÀIT PURIFIE DE SiJybum matlanum
32. PREPARÀTION DES HEPATOCYTES lN VJËTO ET TRAITEMENTS. 32T. HEPÀÎOCYTES DE RÀÎ EN SUSPENSION. 3 2 I L . M E T H O D E D ' O B T E N T I O N . 3 2 L 2 . T E S T S D E C Y T O T O X I C I T E . 3 2 L 3 . T E S T S D E P R O T E C T I O N . 32131 . TRAITEMENT SIMULTAI{E. 32L32. TRÀITEMENT PREVENTIF.
322. HEPATOCYTES DE RÀT EN CULTURE PRIMAIRE. 3 2 2 L . M E T H O D E D ' O B T E N T I O N . 3 2 2 2 . T E S T S D E C Y T O T O X I C I T E . PAGES { 6 1 n 1 1 2 L 2 6 3 4 3 4 3 4 3 4 3 4 ? 6 3 6 3 5 ? Â 3 7 3 8 3 8 3 8 3 9 3 9 T V
3222L. I{ETITODE CIÀSSTQUE.
32222. MICROMETHODE.
3223. ÎESTS DE PROTECTION.
3223L. ÎRAITEMENT S IMI'LTANE .
32232. TRÀITEMENT PREX/ENTTF.
323 . IIEPATOCYTES IiUMATNS EN CULTURE PRIMAIRE.
3 2 3 t . M E T H O D E D , O B T E N T I O N .
3232. TESTS DE CYTOIOXTCITE.
3233. TESTS DE PROTECTION.
33. DOSAGES BIOCHIMIQUES ET COLORIMETRIQUES.
331. TEST D'EXCLUSION DU BLEU TRYPAÀI.
332. DOSAGES ENZYMATIQUES.
332L. ITEPÀTOCYTES EN SUSPENSION.
3322. HEPAÎOCYTES EN CULTURE PRIMAIRE.
333. DOSÀGES DES PROTEINES TOTAI.ES
3331. METHODE DE COLORÀTION DE LOWRY.
3332. METIIODE DE COLORÀTION AU BLEU DE COOMASSIE.
334. TEST DE COLORATION AU ROUGE NEUTRE.
3 3 5 . T E S T D E C O L O R À T T O N A U M T T .
3 3 6 . D O S A G E D E L , A I B U M I N E .
3361. DOSAGE DE L,ATBUMINE DE RLT.
3362. DOSAGE DE L'A].BUMINE HU}4AINE.
34 . OBSERVATIONS CYTOMORPHOLOGTQUES .
3 4 1 . M T C R O S C O P T E P H O T O N T Q U E .
342. MTCROSCOPIE ETECTRONIQUE.
342T. MICROSCOPIE ELECTRONIQUE A BALAYAGE.
3422. MICROSCOPIE ELECTRONIQUE A TRNiISMISSION.
35. ATATYSES STATISTIQUES DES RESUI.TATS .
4 0 4 L 4 t 4 L 4 L 4 2 4 2 4 2 4 3 4 5 4 5 4 6 4 6 ^ 1 4 8 4 8 4 9 5 0 5 2 5 3 ( ? 5 5 5 8 5 8 q o 5 9 6 0 o t
'4L.
CYTOTOXICITE DE 2 PRODUITS DE REFERENCE :
LE TETRACHLORT'RE DE CARBONE ET I,A D-GAI.ACTOSAMINE.
41I. IIEPAÎOCYTES DE RA.T EN SUSPENSION.
4111. EFFET/DOSE DU CC14 DUR,A}TT 30 MINUTES.
4TL2. CINEITQUE D,ÀCTION TOXTQUE DU CC14 8MM.
4113. INTERÀCTIONS ENTRE LE CC14 ET 2 TTERS SOL\TAI\TTS.
41131. INTERACTTON ENTRE LE CCI4 ET L'ETHANOL.
4LT32. INTERACTION ENTRE LE CC14 ET LE DMSO.
4L2. HEPATOCYTES DE RAT EN CUT"TURE PRIMAIRE.
4 L 2 t . C Y T O T O X T C T T E D U C C 1 4 .
4L22. CYTOTOXICITE DE LA D-GAIÀCTOSAI'{INE.
U.22I. CYTOTOXICITE DTRECTE DE LÀ D-GAJ"ÀCTOSAI4INE.
4L222. INFLUENCE DU SERUM DE \ÆÂU SUR LA
CYTOTOXTCITE DIRECTE DE IÂ D-GAIÂCTOSAMINE.
4t223. CYTOÎOXICITE RETARDEE DE I.A D.GAI"ACTOSAI,IINE .
413. HEPATOCYTES HUMAINS EN CULTURE PRIMAIRE : CYTOTOXICITE RETARDEE DE I"A D.GAI.ÀCTOSA}'IINE.
42. RECHERCHE D'UNE E\ÆNTUEIJLE CYTOTOXICITE DES EXTRAITS DE PIÂ}ITE iN VitTO DÀI{S LES I{EPATOCYTES EN CULTURE.
42T. HEPATOCYTES DE RAT EN SUSPENSION.
4 2 L L . C Y T O T O X I C I T E D E L , E X T R À I Î E 5 1 4 ] . - 3 4 .
4 2 L 2 . C Y T O T O X I C I T E D E L , E X T R À I T R T 1 . 0 9 6 .
422. HEPATOCYTES DE RÀT EN CULTURE PRIMAIRE.
4 2 2 L . M O D E L E C L A S S I O U E . 4 2 2 L L . C Y T O T O X I C I T E D'EUPATOIRE : 4 2 2 L 2 . C Y T O T O X T C T Î E 4222. MICROMETHODE. 4 2 2 2 L . C Y T O T O X I C I T E EXTRÀIIS AQUEUX 5 1 4 1 - 3 4 e t R T 1 0 9 6 . LA SILIMARINE. D E S Ër DE 5 3 6 3 6 3 6 9 7 4 8 2 9 0 9 0 9 5 9 5 Y I 9 9 1 ô C
r r 0
r 1 0 1 ' t ^ L t 2 1 1 4 1 1 4 1 L 4 1 1 9 1 , 2 5 L25 D E L , E X T R À I T E 5 1 4 1 - 3 4 .4 2 2 2 2 . C Y T O T O X I C I T E D E L ' E X T R À T T R Î 1 . 0 9 6 . 423 . ITEPATOCYTES ITU}4ÀINS EN CULTURE PRIMATRE.
4 2 3 L . C Y T O T O X I C I T E D E t ' E X T R A I I E 5 1 . 4 1 - 3 4 . 4232. CYTOTOXICITE DE L'EXIRAIT RT 1.096.
43. INFLUENCE DES EXTRÂfTS D'Eupatorium cannabinum L. SUR I.A CYTOTOXICITE DE 2 PRODUITS DE REFERENCE : LE TETRACI{LORURE DE CARBONE ET I.A D.GAI.ACTOSÀI,IINE. 431. TIEPATOCYTES DE RAT EN SUSPENSION.
4311. INFT.UENCE DE L'EXTRAII E 5141.3A SUR I',A TOXICTTE DU CC14 EN TR.AITET4ENT SIMULIAIIE DURÀNT 30 MINUTES.
43!2. INFT.UENCE DE L'EXTRAIT RT 1096 SUR IÂ TOXICTTE DU CC14 EN TRAITEMENT SIMULTAI{E DURÂNT 60 MINUTES.
4313. INFLUENCE DE L'EXTRÀIT E 51.41-3À SUR IÀ ÎOXICITE DU CC14 EN TRAIÎEMENT PRSVENTIF. 43T4. INFLUENCE DE L'EXTRAIT RT 1096 SUR T.A
TOXICITE DU CCI4 EN TRAITEMENT PREVENTIF. 432. HEPATOCYTES DE RAl EN CULTURE PRIMAIRE.
4 3 2 L . I N F L U E N C E D E L ' E X T R À I T R T 1 0 9 6 S U R I Â
TOXICITE DU CCI4 EN TRAITEMENT PREVENTIF. 4322. INFLUENCE DES EXTBAITS E 5141-3À eT RT 1096
SUR IÂ TOXICTTE DE I,A D-GAI.ACTOSÀI,TINE EN TRAITEMENT S IMULTÂÎ.TE .
433. HEPATOCYTES HUMAINS EN CULTURE PRIMAIRE :
INFLUENCE DE L'EXÎRAIT E 51.41-3A SUR I"A TOXICITE DE IÀ D-GAIÂCTOSÀI,IINE EN IRAITEMENT SIMULTÀI{E.
5 . D T S C U S S T O N .
51 . JIISTIFICATION DU CHOIX DES ESPECES ET DES MARQUEURS. 5 ] . 1 . I . E S E S P E C E S .
5L2. LES MARQUEURS DE LÀ CYTOTOXTCITE. 52. CYTOTOXICITE DES PRODUITS DE REFERENCE.
52T. LE TETRÀCHLORURE DE CARBONE. 522. I"A D-GAI.ACTOSAI{INE. L 3 3 1 4 0 1 4 0 r . 4 5 1 - 5 0
r.50
L 5 0 L52 L 5 4r . 5 0
L 6 2 L O Z L 6 4 t 6 ' 7 L 7 3 L 7 4 L 7 4 L 7 5 L 7 8 L'7 9 t8254. RECITERCIIE D, UN EFFET HEPATOTROPE DES D' EI'PÀTOIRE. 6. CONCLUSToN. 1 . B I B L I O G R A P H I E . 8 . AI{NEXES. EXTRAITS 1 , 8 I 1 9 3 L 9 8 2 t 2
Ficn:re I : METABOLISI4E DE LA Fiqure 2 : STRUCTURE CHIMIQUE F i n r r r a ? . êëlJÉs-Ficrure 4 :
EFFET DU CCL4 SUR I.A FUTTE DE L'ENZYME LDH DAI{S DE RAT EN SUSPENSION TRAITES DURANT 30 MINUTES.
F i . r r r r a c . ÈÆÈry
EFFET DU CCL4 SUR LA FUITE DE L' ENZYME GPT DÀÀTS DE RÂT EN SUSPENSION TRÂITES DURANT 30 MINUTES.
F i m r r a R .
ÈSLlg
EFFET DU CCL4 SUR LA FUITE DE L,ENZYME GOT DAÀTS DE RÀT EN SUSPENSION ÎRAITES DURA\TT 30 MINUTES.
F i q u r e 7 :
EFFET DU CCL4 8 MM SUR I,A FUITE DE L, ENZYME LDH HEPAÎOCYTES DE RÀT EN SUSPENSION TRÀTTES DURÂNT
F i a u r e 8 :
EFFET DU CCL4 8 MM SUR I,A FUITE DE L'ENZYME GPT HEPATOCYTES DE RÀT EN SUSPENSION TRÀTTES DURANT
Fiqure 9 :
EFFET DU CCL4 8 MM SUR LA FUITE DE L,ENZYME GOT HEPATOCYTES DE RÀT EN SUSPENSION TRAITES DURÀNT
IITDE:( DES TIGI'RES
PAGES
2 3
D-GAT.ÀCTOSÂI,1INE .
3 5
DES ISOMERES COMPRIS DAI\TS I,A SILYMÀRINE.
4 4
PROTOCOLES D'ETUDE DES SUBSTAIICES CYTOTOXIQUES OU HEPAÎOTROPES POWAIIT ETRE TESTEES DÀI{S LES MODELES D,HEPATOCYTES. EN CULTURE.
F i q u r e 1 0 :
EFFET DE L' INTERÂCTION ENTRE LE CCL4 L, ENZYME LDH DAI{S LES HEPATOCYTES DE DURÀNT 30 MINUTES. b J LES HEPATOCYTES o o LES HEPATOCYTES o / tES HEPÀTOCYTES 7 0 DANS LES 1 . 2 0 M T N U T E S . ' 7 L DAI{S tES L z O M I N U T E S . 7 2 DÂNS LES I 2 O M I N U T E S . 1 1
ET L'ETHÀNOL SUR LA FUITE DE RÀT EN SUSPENSION TRÀITES
EFFET DE L' INTERÀCTION ENTRE LE CCL4 L, ENZYME GPT DAT{S LES HEPÀTOCYTES DE DURANT 30 MINUTES.
F i q u r e 1 2 :
EFFET DE L' INTERÀCTION ENTRE LE' CCL4 L, ENZYME GOT DAI{S LES HEPATOCYTES DE DURÂNT 30 MTNUTES.
F i q u r e 1 3 :
EFFET DE L, INTERÀCTION ENTRE LE CCL4 L' ENZYME LDH DA}TS LES TTEPATOCYTES DE DURÀNT 30 MINUTES.
F i o u r e L 4 :
EFFET DE L, INTERÀCTION ENTRE LE CCL4 L' ENZYME GPT DAÀIS tES HEPATOCYTES DE DURANT 30 MTNUTES.
h ' r m l r ê | \ èël*lt!g
EFFET DE L, INTERÀCTTON ENTRE LE CCL4 ET L,ENZYME GOT DANS LES HEPAÎOCYTES DE RAT DURANT 30 MINUTES
Fiqure l- 6 :
EFFET DU CCL4 SUR IÂ FUITE DE L'ENZYME LDH DE RÂT EN CULTURE PRIMA]RE TRAITES DURÀNT
ET L'ETHÀNOL SUR I.A FUITE DE RAT EN SUSPENSION TRÀITES
7 9
ET L'ETHÀNOL SUR I.,A FUTTE DE RÀT EN SUSPENSION TRAITES
8 5
ET LE DMSO SUR T.À FUITE DE RÂT EN SUSPENSION TRÀITES
8 6
ET LE DMSO SUR I,A FUTTE DE RÀT EN SUSPENSION TRÀITES
8 7 LE DMSO SUR T.A FUITE DE
EN SUSPENSION TRAITES
A <
Y L
DAI\TS LES HEPÀÎOCYTES 6 0 M I N U T E S .
9 2
DAI\IS LES HEPATOCYTES 5 0 M I N U T E S .
9 3
DA}TS LES HEPÀTOCYTES 6 0 M I N U T E S .
F i c r u r e L 7 :
EFFET DU CCL4 SUR I,A FUITE DE RÀT EN CULTURE PRIMA]RE
F i c r u r e 1 8 :
EFFET DU CCL4 SUR LÀ FUITE DE RÀÎ EN CULTURE PRIMAIRE D E L , E N Z Y M E G P T TRAITES DURÀNT D E L , E N Z Y M E G O T TRÀITES DURANT
r 0 0
F i q u r e 1 9 :EFFET RETARDE DE IÂ D-GAT,ACTOSAI4INE SUR LA FUITE DE L' ENZYME LDH DAI\TS LES HEPAÎOCYTES DE RÀT EN CULTURE PRIMAIRE DURÀNT 96
L 0 3
EFFEÎ RETARDE DE i,A D-GAIÂCTOSA}4INE SUR I.À FUITE DE L'ENZYME LDH DA}TS LES HEPAÎOCYTES DE RAT EN CULTURE PRIMÀIRE DURANÎ 72
HEURTS
1,0 6 Ficrure 21 :
EFFET RETARDE DE IÀ D-GAI,ACTOSÂI4INE SUR IÂ FUITE DE L' ENZYME LDH DAI\TS LES IIEPAIOCYTES IiU}4AINS EN CULTURE PRIMATRE DURANT 96
HEURES
F i c r u r e 2 2 : L 0 8
EFFET RETARDE DE IÂ D.GAIÀCTOSA!4INE SUR IÂ SECRETION D'A.LBUMTNE DAÀTS tES HEPAÎOCYTES HUI'IAINS EN CULTURE PRIMATRE DURÀNT 96
HEURES.
Ficrure 23 120
EFFET DE LA SILTMÀRINE SUR IÂ FUITE DE LDH DAI,IS LES IIEPÀTOCYÎES DE RAT EN CULTURE PRIMAIRE TRATTES DURANT 24 HEURES.
L 2 l F i q u r e 2 4 :
EFFET DE I"A SILYI,TARINE SUR I,A FUTTE DE LDH DA}TS LES HEPATOCYTES DE RÀT EN CULTURE PRII4ÀIRE TRÀITES DURÂNT 24 HEURES
F i q u r e 2 5 z L 2 2
EFFET DE i SILYMARINE SUR IÀ FUITE DE GPT DA}IS LES HEPAÎOCYTES DE RÀT EN CULTURE PRI}4AIRE TRÀITES DUBANT 24 HEURES.
F i q u r e 2 6 z L 2 3
EFFET DE I.A SILYMARINE SUR ],À FUITE DE GOT DANS LES HEPATOCYTES DE RÀT EN CULTURE PRI}4AIRE TRAITES DURANT 24 HEURES.
F i c r u r e 2 7 z L 2 7
EFFET DE L'EXTRAIT E 514].-3A SUR LÀ FUITE DE LDH DA}TS LES HEPATOCYTES DE RÀT EN CULTURE PRIMAIRE EN MICROMETHODE ÎRÀITES DURÂNT 24 HEURES.
F i q u r e 2 8 z L 2 . 8
EFFET DE L' EXTRÂIT E 5141..3À SUR LÀ COLORATION DES LYSOSOMES PAR LE ROUGE NEUTRE DANTS LES HEPATOCYTES DE RAl EN CULTURE PRIMAIRE EN MICROMETHODE TRAITES DURÀNT 24 HEURES.
t29 F i o u r e 2 9 :
EFFET DE L,EXTRAIT E 5141-3À SUR LA CAPACITE DE REDUCTION DU MTT PAR LES MITOCHONDRIES DA}TS LES HEPATOCYTES DE RAT EN CULTURE PRII4AIRE EN MICROMETHODE ÎRÀTTES DURÀNT 24 HEURES.
EFFET DE L'EXTR,AIT E 51.41-3À SUR LA QUAI{TITE DE PROTEINES TOTAJ.ES DAÀIS LES HEPATOCYTES DE RÀT EN CULTURE PRIMAIRE EN MICROMETHODE ÎRÀITES DURÀNT 24 HEURES.
F i c r u r e 3 1 : 1 3 1
EFFET DE L,EXTRÀIT E 5141.-3À SUR I"A CÂPACITE DE SYNTHESE D, À].BUMINE DA}TS LES HEPATOCYTES DE RÂÎ EN CUTTURE PRIMAIRE EN MICROMETHODE TRÀITES DURANT 24 HEURES.
F i q u r e 3 2 : 1 3 4 EFFET DE L' EXTR.AIT RT HEPATOCYTES DE RÂT EN DURANT 24 HEURES. k l m t F â !+lg
1096 SUR I.A FUITE DE LDH DAITS LES
CULTURE PRIMAIRE EN MICROMETHODE TRÂITES
1 ? q
EFFET DE L'EXTRÀIT RT 1.096 sUR I,A COLORATION DES LYSOSOI4ES PAR LE ROUGE NEUTRE DANS LES HEPATOCYTES DE RÀÎ EN CULÎURE PRIMAIRE EN MICROMETHODE TRAITES DURÀNT 24 HEURES.
F i q u r e 3 4 : 1 3 6
EFFET DE L'EXTRATT RT ].096 SUR I"A CAPACITE DE REDUCTION DU MTT PAR LES MITOCHONDRIES DA}TS LES HEPATOCYTES DE RÀT EN CULTURE PRIMAIRE EN MICROMETHODE TRÀITES DURÀNT 24 HEURES.
É r i , ^ r r r r a ? q
Èé:trry 1 ? ?
EFFET DE L'EXTRÂTT RT 1096 SUR LA QUANTITE DE PROTEINES TOTÀIES DÀI{S LES ITEPATOCYTES DE RAT EN CUT.TURE PRI},IAIRE EN MICROMETHODE TRAITES DURÀNT 24 HEURES.
F i q u r e 3 5 :
r 3 8
EFFET DE L,EXTRÀIT RT 1096 SUR LA CAPACITE DE SYNTHESE D'AI,BUMINE DN{S LES TTEPAÎOCYTES DE RÀT EN CULTURE PRIMAIRE EN MICROMETHODE TRATTES DURANT 24 HEURES.
F i c r u r e 3 ? : L 4 L
EFFET DE L,EXTRÀIT E 51.41.-34 SUR I,A FUITE DE LDH DÀNS LES HEPATOCYTES HUMAINS EN CULTURE PRTMAIRE DURANT 72 HEURES.
F i q u r e 3 8 :
EFFET DE L'EXTRÀIT E 51.41.34 SUR LA FUITE DE GPT DÀI{S LES HEPATOCYTES HUMAINS EN CULTURE PRIMAIRE DURÀNT 72 HEURES.
Ficrure 3 9 : EFFET DE L,EXTRAIT I{EPÀTOCYTES ITUMAINS F i q u r e 4 0 : EEFET DE L,EXTRAIT HEPÀTOCYTES HUMAINS F i $ : r e 4 L :
E 5141-3A SUR I.A FUITE DE GOT DAI{S LES EN CULTT'RE PRIMAIRE DURANT 12 HEURES.
RT 1.096 SUR IÀ FUITE DE LDTi DÀbIS tES EN CULTURE PRIMAIRE DURANT 24 TIEURES .
L43
L 4 6
L47
1 4 8 EFFET DE L'EXTRAIT RT 1096 SUR I"A FUITE DE GPT DAITS LES
HEPATOCYTES HUMAINS EN CULTURE PRTMAIRE DURÀNT 24 HEURES.
Ficrure 42 :
EFFET DE L,EXTRÀIT RT 1096 SUR I,A FUITE DE GOT DANS LES HEPATOCYTES HUMAINS EN CULTURE PRI}'IAIRE DURÀNT 24 HEURES.
F i q u r e 4 3 :
INFLUENCE DU TEMPS DE PRETRÂ]TEMENT PAR L,EXTRÀIT E 5141-34 SUR LA FUITE DE L,ENZYME LDH INDUÎTE PAR LE CCL4 8 MM/DMSO DÀI{S LES HEPATOCYTES DE RAT EN SUSPENSION INTOXIQUES DURANT 30 MINUTES.
F i q u r e 4 4 : r 3 0
INFLUENCE DU TEMPS DE PRETRÀITEMENT PÀR L,EXTARIT E 514].-3À SUR LÀ FUTTE DE L,ENZYME GPT INDUTTE PAR LE CCL4 8 MM/DMSO DÀ}TS LES ITEPATOCYTES DE RAT EN SUSPENSION INTOXIQUES DURANT 30 MINUTES.
F i q u r e 4 5 :
INFLUENCE DU TEMPS DE PRETRÂITEMENT PAR L'EXTARIT E 5].41.-3À SUR IÀ FUITE DE L,ENZYME GOT INDUITE PAR LE CCL4 8 MM/DMSO DANS LES HEPATOCYTES DE RÀT EN SUSPENSION INTOXTQUES DURÀNT 30 MINUTES.
F i q u r e 4 5 : 1 6 8
INFLUENCE DE L'EXTRAIT E 51.41..3À EN TRAITEMENT SIMULTAATE SUR IÂ FUITE DE L, ENZY}ÎE LDH INDUITE PAR I.A D-GATACTOSA}4INE 5 MM DAI{S LES HEPATOCYTES HU},IAINS EN CULTURE PRI}4AIRE DURANT 72 HEURES.
F i q u r e 4 7 :
r_59
INFLUENCE DE L, EXTRÀIT E 5].41-3A EN TRÀITEMENT SIMTILTAIIE SUR LA FUITE DE L' ENZYME GPT INDUITE PAR LA D-GA.LACTOSÀMINE 5 MM DAITS LES HEPATOCYTES HUI,IAINS EN CULTURE PRIMAIRE DURANT 72 HEURES.
F i q u r e 4 8 : L 7 0
INFLUENCE DE L,EXTRAIT E 5T41-3A EN TRAITEMENT SIMULTANE SUR LA FUITE DE L, ENZYME GOT INDUITE PÀR I.A D-GA].ACTOSAT4INE 5 MM DAÀIS LES HEPATOCYTES HUMAINS EN CULTURE PRIMAIRE DURÀNT 72 HEURES.
TITRAGE DE L,A}TIICORPS POLYCLONAI ANTI-AIBUMTNE DE RAÎ.
F i q u r e 5 0 . 2 2 2
DROITE SIAI{DARD D'ETAJ.ONNAGE DE L,A^LBUMINE DE RÀT.
F i q u r e 5 L : 2 2 3
DROITES STAI{DARDS D'ETAI.ONNAGE DE L'ALBUMINE DE RÀT.
Ficrure 52 : 224
DROITES STâTiTDARDS D,ETAI.ONNAGE DE. L'A.LBUMINE DE RÂT.
Ficrure 53 . 230
TITRÀGE DE L, A}TTICORPS POLYCLONÀL AI{TT-AJ.BUMINE TIUMAINE.
Ficrure 54 : 23L
Sebleell-L :
HEPATOCYTES TSOLES ET LEURS LIMITES. T a b l e a u I I : ETFET DU CCL4 SUR ITEPAIOCYTES DE RÂT T a b l e a u f l f : EFFET DU CCT4 8 LES HEPAÎOCYTES Tableau IV :EN CUI.ÎURE LES MODELES - tEI'RS
i FUITE DES ENZYMES LDH, GPT ET GOT DA}TS EN SUSPENSION TRAIÎES DURANT 30 MINUTES.
IITDEX DES' trABI.EAT'X
PAGES 9 P O S S I B I L I T E S 6 8 LIJù ? ?
FUITE DES ENZYMES LDH, GPT ET GOT DAI{s SUSPENSION TRAITES DURÀNT T2O MINUTES. 8 0 I"A EN mM DE SUR RÀT
EFFET DE L' INTERÀCTTON ENTRE LE CCLA ET L'ETIIÀNOL SUR LA FUITE DES ENZYMES LDH, GPT ET GOT DA}TS tES HEPATOCYTES DE RAT EN SUSPENSION TRAITES DURÀNT 30 MINUTES.
T a b l e a u V : 8 1 :
VALEURS THEORIQUES CAI,CULEES PAR MODELISATION AU MOYEN D'UNE
REGRESSION MULTIPLE POUR LA MESURE DE LA FUTTE DES ENZYMES LDH ET GPT PROVOQUEE PAR L, INTERÀCTION ENTRE tE CCL4 ET L'ETHÀNOL DAIIS LES HEPAÎOCYTES DE RAT EN SUSPENSION TRÀITES DURAITT 30 MINUTES.
T a b l e a u V I : 8 8
EFFEÎ DE L' INTERACTION ENTRE LE CCL4 ET LE DMSO SUR I.A FUITE DES ENZYMES LDH, GPT ET GOT DÀ\TS LES HEPATOCYTES DE RÀT EN SUSPENSION TRAITES DURÀNT 30 MINUTES.
T a b l e a u V I I : 8 9
VA]..EURS THEORIQUES CA]"CULEES PAR MODELISAÎION AU MOYEN D'UNE
REGRESSION MULTIPLE POUR LÀ MESURE DE IÀ FUITE DES ENZY}4ES LDH ET GPT PROVOQUEE PÀR L' INTERACTION ENTRE LE CCL4 ET LE DMSO DÂT,IS LES HEPATOCYTES DE RAT EN SUSPENSION TRAIÎES DURANT 30 MINUTES.
T a b l e a u V I I I z 9 4
EFFET DU CCL4 SUR IÀ FUITE DES ENZYMES LDH, GPT ET GOT DAI.IS LES HEPATOCYTES DE RAT EN CULTURE PRTMAIRE TRAITES DURÀNT 60 MTNUTES.
EFFET DIRECÎ DE IÀ D.GAI.ACTOSAN{INE SUR tA FUITE DES ENZYMES LDH, GPl ET GOT DÀI{S LES HEPAÎOCYTES DE-RÀT EN CULÎURE PRTMATRE
ÎRÀIÎES DURANT 24 TIEURES.
T a b l e a u X : 9 8
INFLUENCE DU SERUM DE \ÆÀU NOTI\EAU NE SUR tA CYTOTOXTCTTE DIRECTE DE I,A D-GAJ.ACTOSAI,IINE DAI\TS LES TiEPATOCYTES DE RAT EN CULTURE PRIMÀTRE TRAITES DURANT 29 HEURES.
1 0 4 EFFET RETARDE DE I"A D-GÀJ.ACTOSAMINE SUR IÂ FUITE DE L' ENZYME LDIT DAI\IS LES HEPATOCYTES DE RÀÎ EN CULTURE PRIMAIRE DUR.AÀIT 72 HEURES.
l a b l e a u X I I I : 1 0 7
EFFET RETARDE DE LA D-GAJ,ACTOSAI,IINE SUR i FUITE DE L' ENZYME LDH DA}IS LES HEPATOCYTES ITUMAINS EN CULTURE PRIMAIRE DURANT 96
IIEURES .
T a b l e a u X I :
EFFET RETARDE DE IÂ D-GAI.ACTOSA.MINE SUR DA}IS LES HEPATOCYTES DE RAT. EN CULTURE
T a b l e a u X f I :
l a b l e a u X I V :
EFEET RETARDE DE IÂ D-GAIACTOSA}4INE SUR DÂ}IS LES HEPATOCYTES HUMAINS EN CULTURE HEURES.
Tableau XV :
1 ô 1
I V I
IÂ FUTÎE DE L' ENZY}4E LDII PRIMAIRE DURANT 96 HEURES.
1 ô O
IÀ SECRETTON D' ATBUMINE PRTMAIRE DURÀNT 95
E F F E T D E L ' E X T R À T T E 5 1 4 1 . 3 À S U R L A F U I T E D E S E N Z Y M E S GOT DANS LES HEPATOCYTES DE RAl EN SUSPENSION TRAITES M I N U T E S . Tableau XVI : 1 1 1 5 À 4 L D H , G P T E T DURÀNT 30 L 1 3 EFFET DE L',EXTRÀIÎ RT L096 SUR LÀ FUrTE DES ENZYMES LDH, GpT ET GOT DAIIS tES HEPAÎOCYTES DE RAT EN SUSPENSION TRAITES DURÀNT 60 M I N U T E S .
Tableau XVTI : L L 5
E F F E T D E S E X T R A T T S E 5 1 4 1 - 3 A E T R T 1 0 9 6 S U R L A F U I T E D E S E N Z Y M E S LDH, GPT ET GOT DAI\TS LES HEPAÎOCYTES DE RAT EN CULTURE PRIMAIRE TRATTES DURÀNT 24 HEURES.
lableau XVïff : LL7
OBSERVATIONS EN MICROSCOPIE ETECTRONTQUE A TRANSMISSION DE I.A CYTOTOXICITE DES EXTRLITS E 51.41..34 ET RÎ T096 DANS LES
HEPATOCYTES DE RAT EN CUTTURE PRIMAIRE TRAITES DURANT 24 IIEURES.
T a b l e a u X f X :
EFFET DE IÂ SILYMARINE DAI{S LES IiEPÀTOCYTES DE ITEURES.
Tableau XX :
E F F E T D E L , E X T R A I T R T T O 9 5 S U R I Â F U ] T E D E S GOT DAITS LES HEPAÎOCYTES HU}4AINS EN CULTURE HEURES .
Tableau XXIV :
L24 FU]TE DES ENZYI4ES LDH, GPT ET GOT
CUT,TURE PRIMATRE TRATTES DURANT 24 SUR Ï.A'
RÀT EN
L32
EFFET DE L,EXTRÀIT E 5].4]..34 SUR LES I1EPATOCYTES DE RÀT EN CUIJÎURE PRIMAIRE EN MICROMETHODE TRÀIÎES DURÂNT 24 HEURES.
labJæasiXl
:
1 3 9EFFET DE L,EXTB.AIT RT 1096 SUR LES HEPAÎOCYTES DE RAT EN CULTURE PRTMATRE EN MICROI4ETHODE TRAITES DURANT 24 HEURES.
T a b l e a u X X f f :
EFEET DE L'EXTRAIT E 51.41-3A SUR I"A FUTTE DES ENZYMES GOT DA}IS LES HEPATOCYTES HU},TÀINS EN CUT.TURE PRT},IAIRE HEURES. T a b I e a U X X T I I : L 4 4 L D H , G P T E T DURÀNT 72 L 4 9 ENZYMES LDH, GPT ET PRIMAIRE DURÀNT 24 t 5 r
INFTUENCE DE L'EXTRAIT E 5141.-34 SUR LÀ FUITE DES ENZYMES LDH, GPT ET GOT INDUITE PAR LE CCL4 4 mM / DMSO DAI{S LES HEPATOCYTES DE RÀT EN SUSPENSION EN TRÂTTEMENT SIMULTAITE DURÀNT 30 MTNUTES.
Tableau XXV : I 5 J
INFLUENCE DE L,EXTRAIT RT 1096 SUR I"A FUrTE DES ENZYMES LDH, GPT ET GOT INDUTTE PAR LE CCL4 TO mM / ETIIÀITOL DA}TS LES HEPATOCYTES DE RAT EN SUSPENSION EN TRÀITEMENT SIMULTAIVE DURÂNT 50 MINUTES.
Tableau X)fi/r . 159
INFLUENCE DU TEMPS DE PRETRÀITEMENT PAR L'EXTRAIT E 5141.3A SUR LÀ FUITE DES ENZYMES LDH, GPT ET GOT INDUITE PAR LE CCL4 I mM / DMSO DAI{S LES HEPATOCYTES DE RÀÎ EN SUSPENSION INTOXIQUES DURÀNT 3 0 M I N U T E S .
INFLUENCE DE L'EXTRÀIÎ E 5141-3A EN PREÎRÀITEMENT DE 30 MINUTES SUR I"A FUITE DES ENZYMES LDH, GPT ET GOT INDUITE PAR LE CCL4 8 mM / DMSO DAI{S LES HEPATOCYTES DE RAT EN SUSPENSION INTOXIQUES
DURANT 30 MINUTES.
Tableau H(V'fIf : 1 6 l
INFT.UENCE DE L'EXTRÀIT RT 1096 EN PRETRÀITEMENT DE 30 MINTITES SUR I.A FUITE DES ENZYMES LDH, GPT ET GOT INDUITE PAR LE CCL4 8 MM / DMSO DA}TS LES HEPATOCYTES DE RAT EN SUSPENSION INTOXTQUES DURÀNT 3 0 M I N U T E S .
!able.as-X&[X :
L 6 3INFLUENCE DE L'EXTRAIT RT 1.096 EN PRETRÀITEMENT DE 29 HEURES SUR LÀ FUITE DES ENZYMES LDH, GPT ET GOT INDUITE PAR LE CCL4 L0 mM / DMSO DANS LES HEPATOCYTES DE RÀT EN CULTURE PRIMAIRE INTOXIOUES DURANT 60 MINUTES.
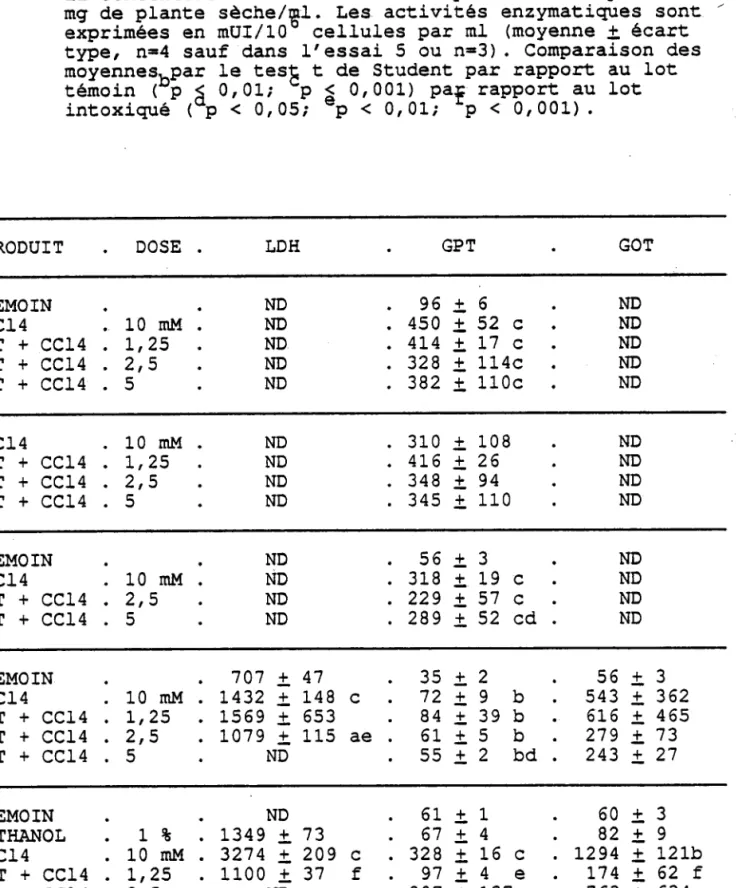
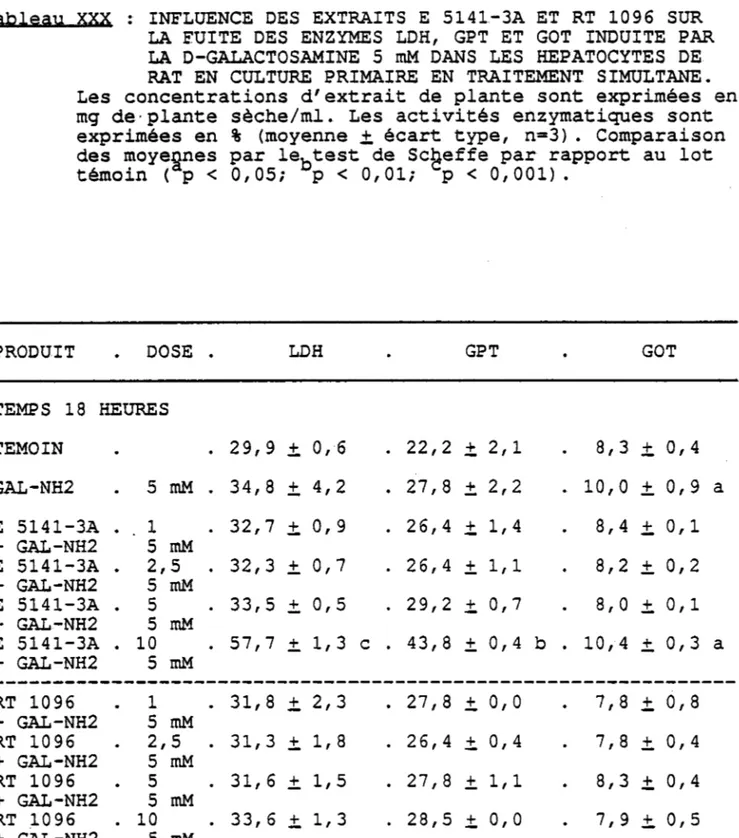
Tableau XXX .
INFLUENCE DES EXTRAITS E 5141-3A ET RT 1-096 SUR I,A FUTTE DES ENZY}4ES LDH, GPT ET GOT INDUITE PAR LA D-GAIACTOSAI4INE 5 mM DÀITS LES HEPATOCYTES DE RAl EN CULTURE PRIMAIRE EN TRÀITE}dENT
SIMULTÀ.NE.
Tableau XXXI : L 7 L
INFLUENCE DE L'EXTRÀIT E 514].-3À EN ÎRATTEMENT SIMULTÀ}TE SUR LA FU]TE DES ENZYMES tDH, GPT ET GOT INDUTTE PÀR I*A D-GÂI.ÀCTOSÀI,1TNE 5 mM DÀIVS LES HEPATOCYTES HUMAINS EN CULTURE PRIMAIRE DURÀNT 72 HEURES.
T a b l e a u X X X I T :
SYNTHESE COMPÀRÀTIVE DE L'EFFET DE 2 CA}INAE}INUM L. SUR DIFFERENTS MODELES CULTURE.
T a b l e a u X X X I I I :
r 8 7
EXTRAITS AQUEUX D' EUPATORITJM IN VITRO D' HEPATOCYTES ENr92
INFLUENCE DES EXTRÀITS ÀQUEUX BRUTS D'EUPATOIRE E 51.41-3À ET RT ].096 SUR L' INTOXICAÎION PAR DES MOLECULES DE REFERENCE
D,HEPAÎOCYTES ISOLES EN CULTURE SELON DIVERS MODELES.
Tableau XXXIV z 233
RECHERCHE DE IÀ DL 50 DE L'EXTRAIT E 5141-3A CHEZ LA SOURIS MALE.
Tableau X (V z 234
RECHERCHE DE LA DL 50 DE L'EXTRÂIT E 5141-34 CHEZ LA SOURIS FEMELE.
Tab,Ieau XX)fi/f :
RECTTERCHE DE LÀ DL 50 DE L'EXTRAIT RT ].096
W :
RECHERCHE. DE IÂ DL 50 DE L'EXTRÀIT RT ],096
235
CHEZ TÂ SOURIS I4ÀtE
-2 ] 6
AI,IM = Aut,orisation de mise sur Ie narché LDH = Lact,at,e déshydrogénase
GPt = Glutamat,e pyruvate transani.nase (ou A-LAT) GOT = Glutarnate oxaloacétate transaminase (ou ASAT) DMSO = Diméthylsulfoxyde CC14 = Îét,raclrLorure de carbone GaI-NH2 = D-gafactosamine MDA = Malonaldéhyde MTT = (3- (4, 5-dimet,hylt,hiazoL-2-u1) -2, 5 diphenyltet,razolj.r:rn bromide) RN = Rouge neutre
SAB = Sérum albumi-ne bovine
l4FO = système Mixt,e function oxyd,ase UTP = Uridine triphosphate
RIA = Radio Immuno Assay
CE 50 = Concentrat,ion provoguant 50 * de I'effet, D L 5 0 = d o s e l é t , a l e 5 0
QSP = Quantité suffisanÈe pour I . P . = I n t r a p é r i t o n é a l e u I = microlitre m l = n i l l i l i t r e m U f = rnilli u n i t é i n t e r n a t i o n a l e m M = millimolaire m g P S / m l = m i l l i g r a m m e d e p l a n t e s è c h e p a r m i l l i l i t r e DO = Densité optigue n = nombre d'échantillons p a i l o t p = risgue de première espèce ND = non dét,erminé
À\râl[':f PnoPos
Le travaj.l gue nous présent,ons dans cet exposé concrétj-se une collaboration entre Ie laborat.oire de Biologie Végétale et, Pharmacognosi.e du Centre des Sciences de l'Environnement à Metz, dirigé par Ie Professeur J-M PELT, Ie Laboratoire de P h a r m a c o g n o s i e d e l a F a c u 1 t é d e s S c i e n c e s B i o l o g i g u e s e t , Pharmaceutigr:es de Nancy l, dirigé par le Professeur F MORTIER et Ie groupe industriel SAÀIOFI (Centre de Recherches de Montpellier dirigé par Ie Professeur J-P CAI$O) .
Une partie des expériences, faisant suit,e au travail grre nous avons présenté et sout,enu publiquement pour l'obt,ention du D . E . A . d e T o x i c o l o g i e d e I ' U n i v e r s i t é d , e M e t , z I e 2 5 s e p t e m b r e 1 9 8 5 , a é t é r é a 1 i s é e d a n s l e L a b o r a t o i r e d e B i o l o g i e V é g é t , a l e e t Pharmacognosie du Centre des Sciences de I'Environnement à Metz d u r a n t l ' a n n é e f 9 8 6 . U n e d e u x i è m e p a r t i e d e s e x p é r i e n c e s a é t é r é a l i s é e a u c o u r s d e s a n n é e s 1 9 8 7 e t , L 9 8 8 d a n s I e l a b o r a t o i r e d e loxico-génét,igue dirigé par le Docteur N BICHET, laboratoire qtli fait partie du service commun de Toxicologie du centre SANOFI Recherches à Montpellier alors dirigé par Ie Docteur P VIC et a u j o u r d ' h u i d i r i g é p a r le Docteur D GOUY.
C e t r a v a i l c o n s t i t u e u n e a p p r o c h e n o u v e l l e p o u r l ' é t , u d e de plant,es médicinales au moyen de test,s jn vitro sur hépatocytes en culture. Il vient compléter des résultat,s obt,enus par des m é t , h o d e s to x i c o - p h a r m a c o l o g i g u e s " c l a s s i q u e s " j n vivo, reconnues e t d é t e r m i n a n t e s p o u r l ' a u t o r i s a t i o n d e m i s e s u r I e m a r c h é d e s p é c i a l i t é s p h a r m a c e u È i q u e s n o u v e l l e s .
1. INTRODUCTTON.
Pour permettre la nise sur le marChé dtun nouveau médicament, à dês fins thérapeutigrres chez l'homme, le législateur doit. Statuer notalûnent, sur un dossier t,oxicologigue et pharmacologiqrre faisant partie du dossier d'aut,orisation de mise èur le rnàrcfré (AI'!M) . La commercialisation de préparations d,'origines naturelles devra elle aussi s'appuyer sur des t,ests expérimentaux afin de prouver leur innocuit,é et, démontrer leur aclivité. Ceci doit fournir rnat,ière à la const,itution d'un doss j-er d,' zu,!!t simplif ié pour la mise sur le marchê d'un phyt,omédicament (\ERÂIN 1988) .
Les modè1es toxico-pharmacologigr.res in vivo représentent la dénarche "classique" et sont toujours déterminants pour I'ÀllM de nouveaux produits maj.s ils nécessitent des manipulat,ions nombreuses pas tou jours prédict j.ves et des invest,issement,s
financiers irnportant,s. La toxicologie et la pharmacologie s, orientent, acluellement de plus en plus vers les technigues in vlgto sur les organes isolés comme sur les modèles de cult,ures de c e l l u l e s . L e s r a i s o n s e n s o n t à l a f o i s é t h i q u e s , s c i e n t , i f i $ : e s , économigr:es et politiques.
Alors gue ces dernières années iI ét,ait évogué Ie terme de méthodes jn vit,ro alternatj,ves ou substitutives, iI est ar:jourd, hui préférable de parler de rnéthodes complémentaires
( G R E E N L 9 8 8 ) .
Les rnéÈhodes in vitro sur cultures de celLules sonÈ p1ut,ôt, adapÈées et réservées au criblage précoce des molécules - ( s c r e e n i n g -
p o u r l e s a n g l o s a x o n s ) c a r e l l e s p r é s e n t e n t , l e s avantages suivants sur les méthodes jn vlvo :
r a p i d i t é .
p ô s s i b i l i t , é d ' u t i l i s e r d e p e t i t e s g r : a n t i t é s d e s u b s t a n c e s à t , e s t , e r .
p o s s i b i l i t , é d e d i s p o s e r d ' u n g r a n d n o m b r e d ' é c h a n t i l l o n s à p a r t , i r d ' u n m ê m e a n i m a l .
coùt inférieur aux méthodes in vivo.
( G R I S I T A M e Ë a L . L 9 7 8 , G R E I M 1 9 8 0 , K L A S S E N e t S T À C E Y L 9 8 2 , K R À C K e Ë a I . . 1 9 8 3 , B E N F O R D e t , H U B B A R D 1 9 8 7 ) .
C e t , r a v a i l s ' i n s c r i t d a n s I a c o n t i n u i t , é d e s r e c h e r c h e s menées au Laboratoire de Biologie Végétale et Pharmacognosie du Cent,re des Sciences de 1'Environnenent, à Metz con joint,ement associé au Laboratoire de Pharmacognosie de Ia Faculté des Sciences Biologiques et, Pharmaceutigrres de Nancy I. Ces recherches ont pour but d'infirmer ou de confirmer au moyen de tests scientifigr.res, les propriétés pharmacologigr.res d'ext,raits d e p l a n t e s r é p u t é e s a c t i v e s s e l o n I ' a n a l y s e d e s d o n n é e s ernpiligr.res recueillies généralement sur le terrain. L'un des axes d e r e i h e r c h e s r e p o s e s u r l a m i s e e n é v i d e n c e d ' a c t i v i t é s h é p a t , o t r o p e s d e p l a n t e s m é d i c i n a l e s ( F L E U R E N T I N e Ë a L . 1 9 8 6 , H O E F L E R e Ë a I , . 1 9 8 7 ) .
2
Le fole est l'organe le plus act,if d'un point de vue biochimigue pour le néta.bolisme des substances endogènes . et, exogènes-(xénôbiot,igrres). Son rôIe est essentiel dans Ie maintien d,e I'homéostasie biologigrre de I'organisme. Il intervient dans Itactivation et, la détoxification des sr:bstances chimigues. Les hépatocytes gui sont des cellules Parenchpnateusesr représentent, environ 70 t du nornbre t,ota1 des cellules de cet organe et' en assurent les fonctions essentielles.
Le dysfonctionnement de ces celluLes peut être provoqué par différént,s tyPes d'at't,eint,es : t,oxigrlgs, virales, méAicamenteuses ou inrnunoallergigr:es (PERRISSOUD 19e1) .
Envj.ron 600 préparat,ions commetciales d'origine nat,urelle proposant une act,ivit,é hépatotrope sont, dénombrées au niveau rnonOiat. Cependant, les informations scient,ifiques prouvant
I r e f f i c a c i È é d e c e s p l a n t e s s o n t p e u f r é g u e n t e s e t i n s u f f i s a n t e s ( L A N D A eÊ aL.L986) .
Parmi différentes plantes communes en Europe, Eupat,orium cannabittum L. (Ast,eraceae) est bien connue depuis I'antiguité pour Ses applications dans les EraiEements des ict,ères, des ènotécystitel et des plaies. Un extrait agueux brut, d'Eupatoire
(EP 1.001) dont, la préparat,ion galénigr:e a ét,é réalisé par SAIIOFI Recherches à Toulouse suivant les indications des fabricat,ions t,raditionnelles, a montré un effet cholérét,igue eL des propriét'és hépat,ot.ropes sur plusieurs modèles pharmacologigr.res chez I'animal e n t i e r ( L i l ( À eË aJ,.1988' LEXA-ROBIN 1988) .
* * *
Le t,ravail de recherches gr-ri nous a été confié consiste en Ia rnise au point, de méthodes in vitro adaptées au criblage de substances naturelles hépatotropes. Ces mét,hodes de criblage in vitro sur des hépatocytes en culture, doj-vent êt,re performantes' r a p i d e s , r e p r o d u c t , i b l e s e t l e s p l u s p r é d j . c t i v e s p o s s i b l e s .
A ces fins, une applicatj-on a ét,é conduit,e sur 2 extraj-t,s agueux bruts d'Eupat,orium cannabinum L. (Àsteraceae) réaLisés par SAI{OFI Recherches : I'extrait, E 514L-34 préparé conformément aux données ernpirigues et l'ext,rait RT 1096 réalisé suivant un procédé pilote semi-industriel devant about,ir à la production et â t a c o m m e r c i a l i s a È i o n d ' u n e s p é c i a l i t , é p h a r m a c e u t i g u e .
Après avoir rnis au point un rnodèIe de culture d , h é p a t o c y t e s d e r a t e n s u s p e n s i o n ( A R V I S 1985) dans. le b u t d e conduire des expériences à court terme, les résult,ats posit,ifs obtenus alors nous ont encouragé à poursuivre ce travail. Cette s u i t e f a i t I ' o b j e t , d e l a p r é s e n È a t , i o n d e c e m é m o i r e . N o u s e n décrirons naintenant tes points clés et, Ie détail des adresses sera accessible au lecteur dans Ie sommaire.
L e t r a v a i l e x p é r i m e n t , a l s ' a r È i c u l e e n t r o i s p a r t i e s d ' i m p o r t a n c e c o m p a r a b l e . C e t t e " t , r i c h o t o m i e " r e p r é s e n t e . Ies phasês essentielles du cheminement de I'approche méthodigue
nécessaj.re à 1'édification de modè]es toxico-pharmacologiques susceptibles de mettre en évidence les vertues hépatotropes de su.bst,ances nouvelles .
La première paftie consj.dère les tests prat,i$rés sur des produits t,oxigues de référence : le tétrachlorure de carbone (utiJ.isé pour des expériences à court t,erne) et ' Ia D-galactosanine (ut,ilisée pour des expériences à long t,erme) . Cette paft,le ét,ait, indispensable car il faut disposer de bons nodèIes cytotoxigrres si l'on veut pouvoir ensuj-t,e cribler des sr:.bstances hépatotropes. L'arborescence des t,ravaux gui ont, pu être réalisés est la suivant,e :
. . TETRACHLORURE HEPATOCYTES . . CUf,tUnn . SUSPENSTON DE CARBONE. . . . CULTURE PRIMAIRE
. .D.GAT.ÀCTOSAI4INE . .CULTURE PRTMAIRE
La seconde part,j.e considère les t,ests de recherche d'une cytotoxicité de subst,ances nat,urelles : deux ext,raits agueux brut,s d'Eupat,orium canna-binum L. (Asteraceae) et un extraj-t purifié de Silybun marlanum (Àsteraceae). La recherche d'une é v e n t u e l l e c y t o t , o x i c i t , é d e s s u b s t a n c e s n o u v e l l e s , g u ' e l l e s s o i e n t d ' o r i g i n e n a t , u r e l l e o u d e s y n t h è s e , ê t s u r t o u t s i e l - l e s s o n t supposées présenter des vertues hépatot,ropes, est une précaut,ion élément,aire et indispensable si l'on désire pouvoir donner une suite favorable au développement, d'un produit nouveau. Cette réflexj.on constiÈue le fondement, des études toxicologigues demandées dans Ie dossier d'expert,ise pour I'AI4M dans leguel l ' i n n o c u i t é d u p r o d u i t d o i t ê t r e d é r n o n t , r é e . L ' a r b o r e s c e n c e d e s travaux gr:i ont pu être réa1isés est Ia suivante :
. . S U S P E N S I O N
TTEPAÎOCYTES. .
..cr,AssrQUE
PRIMÀIRE. . :4
La troisième part,ie considère les t,ests prat'igués pour Ia recherche d'éventuelles act,ivit,és hépatot,ropes de deux extraits aqueux brut,s d'Eupatorium canna.binum L. (Asteraceae) vis à vis des sr:bstances toxigues de référence ayant fait l'ob jet, de la première partie i. e. le t,étrachlorure de carbone (pour les tests â court terme) et Ia D-galactosamine (pour les tests à long terme). Les activités hépaÈotropes ont, été recherchées soj.t lors de traitements simuLtanés soit lors de t,rait,ement,s prévent,ifs. L'arborescence des t,ravaux qul ont, pu êt,re réalisés est la suivante : . . SIMULTANE TETRACHT.ONùNE Og CARBONE . . S U S P E N S I O N . ..SIMULTAÀIE. .D-GALACIOSAI4TNE . .PNEVENTIF. . . .TETRÀCHLORURE DE CÀRBONE
Les tests gue nous avons developpés onu ut,ilisé non seulement plusieurs t,ypes de rnodèIes de culture d'hépat,ocytes de rat mais encore des hépatocytes humains en cult,ure primaire.
N o u s a v o n s u t i l i s é l e m o d è I e d ' h é p a t o c y t e s d e r a t e n s u s p e n s i o n d a n s l e s é t u d e s à c o u r È t e r m e . L e s h é p a t o c y t e s d e r a t en culture primaire ont servi de nodèIe expérimental dans les é t u d e s à m o y e n t e r m e ( 2 4 h e u r e s ) e t l o n g t e r m e ( 3 à 4 j o u r s ) . Nous avons prat,igr:é deux types de modèles : soit, un modèIe de c u l t u r e p r i m a i r e " c l a s s i q u e " s o i t , u n m o d è I e d e m j - c r o c u l t u r e . C e dernier nodèIe d'hépaÈocytes en microculture fait, actuellement l ' o b j e t , d ' u n e é t u d e m u l t i c e n t r i g u e d e v a l i d a t i o n d a n s u n progranme de la CommunauÈé Economique Européenne. Enfin, 1'usage des hépatocyt,es humains a été réservé à des tests en culture p r i m a i r e " c l a s s i q u e " .
Les points majeurs du plan de thèse sont les suivant,s : a) Une introduction gui per-met' 'de définir Ie contexte gui a motivé ce travail ainsi gue son déroulement.
b) Une "analyse bibliographigrre* coutte pour comparer. les différent,s modètes in vit,ro, indiquer les caract,éristiques principales du mode d'action des produits héPatotoxigues de iefgrence çlue nous avons utilisés et gr:elqres données sur les su.bstances -hépat,otropes d'origine naturelles ayant' fait I'ob jet d ' é t u d e s s u r l e s h é p a t o c y t e s i s o l é s .
c) Une paltj.e matériel et méthodes la plus complète possible ?€in $te le lecteur intéressê puisse éventuellement y trouver matière à const,ruire d'autres recherches.
d) Une part,ie "résultats" construite en suivant Ie Plan de travail présenté précédenmeRt et q:i est const,ituée d'éIéments biochimiques essent,iels représentant des marçlueurs de la c y t o t o x i C i t g t e l s g u e : I e t , e s t d e v i a b i l i t é a u b l e u T r y p a n , .les dôsages enzymat,içIues de LDH, GPf ou GOT, Ie dosage des protéines tot,ales (méthode de Lowry et, méthode bio-rad) r les test,s fonctionnels des lysosomes (rouge neut,re) - des mitochondries
(MTT) du rét,iculum endoplasmi,gue (syntTrèse et sécret,ion d'albumine) et comptétée par des observations cyt,omorphologigues en microsCopie optigue à cont,raste de phase et en microscopie élect,ronigue à balayage et à transmission
e ) U n e d i s c u s s i o n g é n é r a t e r e p r e n a n t l a s y n t , h è s e . d e s r é s u l t a t , s e t y apportant, une analyse critique comparée.
- 6
2 . AI\TAT,YSE BIBLTOGRÂPTIIQUE
2t- tEs MODELES TOXICO-PIIARMACOLOGTQUES ln vitzo'
L ' h é p a e o c y t e r e p r ê s e n t , e à l ' é c h e l l e c e l l u l a i r e , I ' u n i t é fonctionnelle du foie.
Depuls ces 20 dernières années, de nombreuses néthodes ont ét,é proposées pour isoler les hépatocyt,es de diverses espèces animales. Les résultat,s décriËs sont très varia.bles quant aux r e n d e m e n t s ( g u a n t i È é de cellules i s o l é e s ) , à l a v i a b i l i t é d e s dits hépatocytes ainsi qu'au maintlen de leurs fonct,ions spécifi+res. Au regard de la chronoLogj-er. d'énormes progrès gnt été eCaOfis dans le sens d'une constante amélioration gr:antit,ative d'une part et gualit,ative d'aut,re part'.
plusieures épogr:es margr:ent les évolutions techniqres de Ia préparat,ion des hépatocytes isolés.
La fin des années 50 marque l'épogr:e "pionniers" pour laguelle iI convient de cit,er les travaux de IIOWARD eË aJ'. (L961) ' HO!{ARD et pESCH (1968) qui introduisent Ia t,echnigue de dissociation du foie par un système enzymatigue. Cette t,echnigue est reprise et, anréliorée par les travaux de BERRY et FRIEND (1969) gui const,ituent, encore aujourd'hui la rnéthode princeps de référence gr:i introduisit, la perfusion du foie par une solut,ion de collagénase et, hyaluronldase.
Les années 70 marquent, I'épogrre de l'amélioration du rendement et de Ia gualité des hépatocytes. On peut citer les travaux de SCHREIBER et SCHREIBER (1973) ' BERRY (1974) | BERRY et WERNER
( L 9 1 4 ) , K R E B S e t a l , . ( L 9 7 4 ) , W A G L E e t T N G E B R E T S E N ( L 9 7 5 ) , J E E J E E B H O Y E I P H I L L T P S ( T 9 7 6 ) , F R Y E Ë A . I . ( L 9 7 6 1 , B E R R Y ( ] . 9 7 6 ) . C C sont surtout les travaux de SEGLEN (I9'7 6) qui représent,èrent, une forrnidable progression méthodologigr:e en introduisant la p e r f u s i o n i n s i t u p a r I a c o l l a g é n a s e s e u l e a v e c r e c i r c u l a t i o n d u Iigr:ide dissociateur et optimisation des conditions expériment,al,es permett,ant, d'obt,enir ainsi un rendement importanc e t u n e v i a b i l i t é é I e v é e . L ' o b t e n t i o n d ' h é p a t o c y t e s i s o l é s à partir de tranche de foie à encore ses protagonistes (BELLEMANN e r a l , . ( L 9 7 7 ) , G U S T A V S O N e t , M O R I À N D ( 1 9 8 0 ) ).
Au cours des années 80, Ies aut,eurs se préoccupent, surt,out de l ' a m é l i o r a t i o n d e s c o n d i t i o n s d e c u l t u r e e t , d e s p e r f o r m a n c e s b i o c h i m i g r : e s d e s h é p a t o c y t e s i s o l é s . L e s p r o p o s i t i o n s s o n t nombreuses et, variées et, l'on peut citer certains t,ravaux comme c e u x d e C À R L S E N e Ë a J . . ( 1 9 8 1 ) , C R E S T O e Ë a | . ( 1 9 8 1 ) , S T O J A I . T O V e t M A J T ( I C - S I N G H ( L 9 8 2 ) , G R E E N C T A J . . (1 9 8 3 ) , Q U E R Â L E Ë A T . ( L 9 8 4 ) , [ { A r { G e t a J - . (1 9 8 5 ) .
En fait, iI exj.ste à peut près autant de technigues aux variat,ions subtiles gue de laborat,oires et d'auteurs qui u t i l i s e n t c e s m o d è l e s d ' h é p a t o c y t e s i s o l é s e n c u l t u r e m a j . s c e
sont, surtout, les travaux de BERRY et, FRIEND (1969) puis de SEGLEN (L976) qt.ri const,it,uent, Ies pu^blicat,ions princeps auxgrrelles la majorité des auteurs se réfèrent.
D e p u i s g u e l g r r e s a n n é e s , L ' u t i l i s a t i o n d ' h é p a t o c y t e s humains est devenue accessible aux chercheurs et les travaux de GUGI'EN-GUILLOUZO et aJ,. (L982) sont, à not,re connaissance les p r e m i è r e s i n f o r m a t i o n s g u i p r ô n e n t I a q r a l i t é s u r c e m o d è l e .
Au cours des 10 d,ernières années, une part de plus en plus important,e a été réservée aux Suspensions d'hépatocytes i s o l é s p à r p e r f u s i o n e n z F n a t i g u e ( G U I L L O U Z O 1 9 8 6 ) .
Les suspensions d'hépat,ocytes isolés offrent, 1'avant,age de constj.tuer une population de cellules homogène et d'exprimer des act,ivités fonctionnelles comparables à celles préserrtes chez I , a n i m a l e n t , i e r . E n o u t , r e , i f e s l p o s s i b l e d ' a n a l y s e r d e n o m b r e u x paremèt,res à partir de Ia suspension cellulaire initiale (BAUR et
a J , . 1 9 7 5 ) .
La cytot,oxicit,é est habituellernent appréciée par la mesure de la viabilité cellulaire au moyen du test, classigue de coloration au bleu Trypan et par la mesure de l'acÈivité d, enzymes int,ra-cellulaires libérées dans Ie milieu d' incubat,ion. La meéure de Ia lacticodéshydrogénase (I,DH) apparaj.t, êt,re la plus représent,ative des enzymes relargruées dans le milieu afin de grràntifier les dornmages occasionnés à la membrane plasmigue dg" hépatocyt,es t,raités par les subst,ances à tester. Récemment' la mesure âe I'act,ivité de la LDH int,ra-cellulaire a ét,é proposée conme index de cytot,oxicité dans Ie modèIe des hépatocytes de rat e n c u l t u r e p r i m a i r e ( C H À O e Ë a J , . 1 9 8 8 ) .
Pour certains auteurs, iI est souhait,able de choisir des act,iviÈês nétabotigues de Ia cellule corune critère d'éval-uation de la cytot,oxicité. La mesure de ta gr:ant,it,é d' al-bumlne sécrètée atteste du bon fonctionnemenÈ des hépatocytes fraichement, isolés e n s u s p e n s i o n e t e n c u l t u r e p r i m a i r e ( G U I L L O U Z O L 9 8 6 ) .
Les hépatocytes fraichement, isolés ont, été largement u t i l i s é s c o m m e s y s t è m e d ' é v a l u a t i o n d ' u n e c y t , o t o x i c i t é d e s xénobiotigrres (KI,AASSEN et STACEY L982, KRACK et aJ'. L983) . Géneralement, les composés gr:i nécessitent, une activaÈion m é t a b o l i g u e p o u r e x e r c e r l e u r e f f e t , i n d u i s e n t u n e t o x i c i t é c o m p a r a b l e à c e l l e o b s e r v é e c h e z l ' a n i m a l . T Y S O N e Ë a l . . ( 1 9 8 0 ) o n t testé de nombreux composés et ont montré grre seuLement 2 d'entre eux donnaient des résuJ.tats différents de ceux décrits in vivo.
Les hépatocytes fraichement isolés en suspension ont une durée de vie brève et ne peuvent donc être utilisés pour l'étude des effets chronigues ou à long terme des comPosés h é p a t o t o x i g r r e s . D e t e l l e s é t u d e s p e u v e n t s ' e n v i s a g e r s i l ' o n a reèours à des cultures primai.res (MacQUEEN et, WILLIAI4S L982) . Toutefois, il faut rappeler grre les enzymes du métabolj-sme des xénobiot,igues sont légèrement, altérées dans les cultures p r i m a i r e s . L a b a i s s e b r u t , a l e d u t a u x d e c y t o c h r o m e P 4 5 0 e t d e
I, activit,é de plusieurs enzymes intervenant dans Ie métabolisme des xénobiotigr:es après 1 à 2 jours de culture ne reflèt.e plus ce gni se passe jn vivo (GUGUEN-GUILLOUZO et GUILLOUZO l-983) .
Ceci expligrre pourgr:oi les études de t'oxiciÈé sur hépat,ocytes de rongieurs sont généralement, limitées à 48 heures.
I t e s t p o s s i b l e d e p a l l i e r c e t t e d i m i n u t i o n d e s caractéristigues foncÈionnelles des hépat,ocytes et de Ia compenser par un choix judicieux d'un milieu de culture a p p i o p r i é , p a r f o i s " d o p é " p a r I ' a j o u t , d e c o f a c t e u r s . L e m a i n t i e n correct des caract,éristigues initiales des hépatocytes peut être p r o l o n g é p a r I ' a j o u t d e s é r u m d e v e a u n o u v e a u n é o u f o e t a l , d r i n s u l i n e , d ' h y d r o c o r t i s o n e , d e d e x a m é t h a s o n e , d e g l u c a g o n o u d, acide aminolévrtlinigue grri sont des précurseurs des voi-es de
I
biosynthèses de certaines fonct,ions essent,ielles (DICH ex aJ-. f 9 8 8 i . L e t r a i t e m e n t d e s b o i t e s d e P é t , r i p a r u n e s o l u t i o n d e collagène afin de constituer une pellicu1e au fond des boit'es avant-la mise en culture des hépatocytes, favorise I'att,achement, des cellules au support et stabilise les fonctions biochimiques
(MICHÀtOPOUT.OS et PITOT 1975) .
L'addition de diméthylsulfoxide (DMSO) à 2* ou de phénobarbital, pourrait également rnaintenir le taux correct de èertaines enzymes impliqr:ées dans le nét'abolj.sme des x é n o b i o t , i g r . r e s ( I s o M e t , a ! . 1 9 8 5 , M Y A Z Â K I e t a l - 1 9 8 5 ) .
LtutiU.sation de co-cultures associant, des hépat,ocytes à des cellules épithéliales senrble représenter un sysÈème performant dans Iàs études à long terme (supérieurgs à 10 jours) ê e t o n B E G U E e t a l . ( 1 9 8 4 ) , G U G U E N - G U I L I J O U Z O e t a l . . ( L 9 8 3 ) .
Enfin, Ia possiJcilit,é de pouvoir disposer au jourd'hui drhépatocytes hunains en culture primaire représenterait la situâtion- la plus favorable pour ét,a^blir des comparaisons ln vlvo/in vitro gtri soient les plus prédictives de la sit,uation chez l,homme. Cependant, les "opportunités" qui permet,t,ent, aux chercheurs d'avoir accès à des foies humains sains issus généralement de personnes accidentées ne t,rouvant pas de receveur greffable conservent un caractère assez exceptionnel
En revanche, le développement récent de cultures primaires d,, hépat,ocytes humaj.ns issus de biopsies prélevées chez àes patients càncéreux est en cours de validation dans Ie Service de l,tpX du Centre SAÀIOFI Recherches à Montpellier. SÀf\fOFI collabore avec les organismes publics (INSERM U L28 et V 2'78) p o u r I ' o p t i m i s a t i o n d e I a t e c h n i g u e d ' o b t , e n t i o n e È d e ôonservation des hépat,ocyt,es humaj,ns et sur la régUlation des
enzymes de phase I impligtlés dans I'oxydation des principes a c t i f s . P a r a i l l e u r s , u n e c o n v e n t i o n e s t s i g n é e e n t r e l e g r o u p e SAIVOFI et l'INSERM pour la constitut,ion d'une bangue nationale drhépatocytes humains cryocongelés (FABRE conmun. personnelle) .
Les avant,ages eÈ les inconvénients systèmes sont résumés dans Ie t,ableau I.
&bJ.eE rJ : ItrEPATOCYTES ISOLES EN CULTURE - LES MODELES - LEttRS POSSIBTLITES ET LEURS LI!{ITES.
. HEPTAOC:IrES EII SUSPEU5IOT . HEPÀIOCIIITE8 tr[ CU&1!RE PRII'IAIRE
fup. druÈlllr.Èlon . qnaÀquat.hrutrr . 2l à {8 h.uaat' vglt Plualaust Joutt èv.c . dm cotect.uar..g pluebunr rodatl ca . co-qrl,Eu8a
c'raoG'8''G1qu"
: :i.*i:î HIî'T
: il:îf#Tî::iil:':."
, BdEa.û. pfe[f$r. po.ai!L. . rÔprrÔr lgrÔr qurlquo hlunr dl a1ro ra , drrr À la prap.srtloa . cul'Èu8.
Àv.1t.q.. - prÉp.nÊlon !rctl.' rapldr . - trat boanor coDdlEldlt pàyrloloElquu , pu dr consaalaaÈl'on pæ drr - réorg$ttrrlon oor?bologlqua.È
, ûl,ct'o-orgatrlner à c!âlndla . rtructurala .n Eottæouch. plocho dtr Èlrru , doac rÈôrllItÔ conrttllÔr . hépatlqur
, [rtr non obJ,lgrtotra . - æfoarÈ.loo d. coûtrcts .lntor-crllulalnr
: ;.:î:.:ïîli'i:f
: :',T.ïT:i::ilffL
rtuur..cr
, (.ary!.. dr pha.. ll . (ldr E o la vtto, : ii.:';T'!n Ylv,,l
racon'ônrrat'
: ;iï::ï:T:i-'s'dult
: "#ï':ï.1;iï.i:i"iÏi:i"*'
. - E.PlodqctlblllÈÔ d.r . ttarll.! . ra.ultrlt lraelblcr À la (tdq qÈ.r trl vlvpl . qurll,ta dr. praprtattont .s . du donn.u8t 0
22. LES HEPATOTOXIQUES.
Les dysfonctionnement,s du foie provogués par des produits chimigues ont, été reconnus comme un problèrne toxicologigue depuis environ L00 ans d'après ZIMI{ERI'141'I (1978)
-Une re\ le très complète et bien documentée, classant les subst,ances hépatot,oxiques selon
a) les alt,érat,ions morphologigues et fonctionnelles
b ) l e s a l t , é r a t i o n s c h i m i g r : e s ( n é c r o s e , s t , é a t o s e , c h o l e s t ' a s e intra-hépatigr.re et, hépatite virale)
c ) s i . t e s c e l l u l a i r e s o u o r g a n i t e s c i b l e s
d) mécanismes d'action toxigr.re (accumulat,ion lipidigue, synthèse prot,éigr:e, peroxydat,ion Iipidj.gr:e, nécrose' cholest,ase,
c i r r h o s e , c a r c i n o g é n è s e )
e ) f a c t e u r s i n f l u a n t s l ' i n t o x i c a t i o n h é p a t i g u e
(biotransformaÈion des t,oxigues, glut,athion, alt,ération du flux sangruin hépatigr-re, potentialisation de l'hépatotoxicité) a é t é r é c e m m e n t , é t a b l i e p a r P L A À ( f 9 8 6 ) .
Afin d,e construire des mod.è.l,es permett,ant, de cribler d.es s u b s t a n c e s s u s c e p t i b l e s d ' a i d e r I e f o i e à p r é s e r v e r s o n i n t é g r i t é métaboligr.re et f onct,ionnelle (substances hépatotropes ) , Ie toxicologrue devra avant tout déterminer des conditions d r i n t o x i è a t i o n p a r d e s s u b s t , a n c e s h é p a t o t o x i g u e s d e r é f é r e n c e .
I I d i s p o s e p o u r c e l a d ' u n g r a n d n o m b r e d e m o l é c u l e s p o u v a n t produiré une ou des perturbat,ions dans Ia cellu1e hépatigue
(népatocyte) . La longue expérience acgrrise gràce aux expérimentations sur I'anirnal offre aux chercheurs un choix assez l a i g e d e s u b s t a n c e s a g r e s s i v e s . L e s i n t o x i c a t i o n s p e u v e n t ê t r e m o d u l é e s s o i t e n f o n c t i o n d e I a d o s e d a n s I e c a s d e s
intoxications aigues soit, en fonction du t,emps dans le cas des intoxicat,ions répétées ou chronigr:e.s et entrainent respectivement u n e n é c r o s e , u n e s t é a t o s e o u u n e c i r r h o s e p a r e x e m p l e .
D a n s l e s e x p é r i e n c e s i n v i t , t o , l e m o d è l e d e c u L t u r e d e s h é p a t o c y t e s ( e n suspension ou en culture primaire) l i m i t , e l e s p o é s i b i l j - t , é s o f f e r t e s a u c h e r c h e u r . E n e f f e t , l e c h o i x d u t , o x i g u e âe référence est imposé par Ie type de modèle de cult,ure e s s e n t i e l l e r n e n t à c a u s e d e I a v a r i a b l e t e m p s ( v o i r t a b l e a u I ) . L a s u r v i e b r è v e d e s h é p a t o c y t e s e n s u s p e n s i o n i m p o s e l e c h o i x d ' u n t o x i g u e a y a n t u n m o d e d ' a c Ë i o n r a p i d e a l o r s q u e l e s h é p a t o c y t q s en cutgurè primaire donnent, accès à une palette plus riche de s u b s t a n c e s t o x i q u e s d e r é f é r e n c e s a n s g u e l e t e m p s d ' u t i l i s a t , i o n d e s c u l t u r e s n e r e p r é s e n t e u n e r é e l l e c o n t r a i n t e .
A i n s i , p o u r l e s e x p é r i e n c e s s u r I e m o d è I e d e s h é p a t o c y t e s en suspension, nous avons sélectionné Ie tétrachlorure de carbone
( C C 1 4 ) p a r m i l e s d i f f é r e n t s a g e n t s t o x i g l r e s c a r i I e s t f a c i l e m e n t disponible et son action toxigue in vitro est rapide conrme nous a t I ô n s 1 ' e x p o s e r d a n s l a s u i t , e . S o n u t i l i s a t i o n d a n s l e s expérimentat,ions in vivo prat,iguées depuis plusieurs années au 1 a Ë o r a t o i r e I a i s s a i e n t p r é s a g e r d e I a p o s s i b i l i t é d ' é t a b l i r ensuite des comParaisons in vivo/in vitto.
Pour les expériences sur les modèles d'hépatocyt'es en culture primaire, la D-galactosamine a ét,é choisj.e conme su.bstance t,oxigue d,e référence, son mode d'actj'on différent' de celui du CC14 devant apporter des informat,ions complénentaires.
22L. I.E TETRACIILORURE DE CÀRBONE.
Cet,te molécu]e appartient, à Ia fanille des agents toxigr.res dj.rect,s gr:i pal déf init,ion entrainent des lésions àrgatij.q,r"s avanÈ dtentràj.ner des lésions méta.boligues. Ils sont' caiactérisés par leur rapidit,é d'act,ion et' provoguenÈ ténératement uàe hépatite aigue dont, les lésions sont dose dépendantes (PI"AÂ L98 6)
Les hépatotoxigues direct,s sont rapidemenÈ élininés par l,anirnal ett cot rs d'exp-érinent,ation. 0n peut, citer parml ceux-ci ie pfrosphore blanc, le chloroforme et surtout, le tétrachlorure de carËone- (CCI4) qui sert classigrrement, de modèle expérinental pour r J f r o a u i i e , s e l o n ! a d o s e , d e s l é s i o n s d e t y p e n é c r o s e o u s t ê a t o s e ( P E R R I S S O U D L 9 8 1 , P T , À A f 9 8 6 ) .
Différentes substances hépatotoxigr.res ont, en commun la caract,éristiqr:e de nécessiter une act,ivat,ion mét,aboligue Par un systène enzymatigr.re de telle sort,e gue Ie dérivé produit'. soit p i " " a c t i f â t s e r v e d e s u p p o r t à I ' h é P a t o t o x i c i t é . L e s t , o x i q u e s àppartenant à cett,e êlasse et frégr:ement utilj-sés en p[à6""oIogie sont le bromobenzène, la dirnéthylniÈrosamine, i , a l c o o l a i t y f i q u e , l e t é t r a c h l o r u r e d e c a r b o n e , I e t h i o a c é t , a n i d e et le paracetarnof . Le CC14 est cert,ainement l'agent hépatotoxigue l e p l u s é t u d i é e t , l e p l u s u t i t i s é p o u r é v a l u e r l ' e f f e t , p r o t e c t , e u r a e è u o s t a n c e s h é p a t o t i o p e s ( I Â N S e t , a 1 . . 1 9 8 0 , P E R R I S S O U D L 9 8 1 - ) .
L e s p r i n c i p a l e s r a i s o n s p o u r l e s g r . r e l l e s _ le CCI4 a ét,é t r è s é t , u d i é l e p o s e n t s u r l e s f a i t s g u ' i l e s t - f a c i l e d e s e I e p r o c u r e r s o u s f ô r m e p u r e e t , g u ' i l - p r o d u i t d e s a l t é r a t i o n s d u f o i e àans d,e nombreuses êspèces dont la souris, Ie taE, le lapin et
I ' h o m m e ( S L A T E R f9 8 4 b )
Force est de const,ater gue les mécanismes gui expligr]ent Ia t,oxicit,é du CCl4 aussi bien in vivo gu' jn vitro sont nombreux e t , v a r i é s . L a c o n n a i s s a n c e d e c e s m é c a n i s m e s d ' a c t ' i o n e s t directement corrélable aux moyens nis en oeuvre pour appréhender I e s v o i e s n é t a b o l i g u e s i n c r i m i n é e s .
Une monogràphie des conségrrences générales du CCI4 sur les voies métaboligrres ainsi qu'une re\ re import,ante sur la biotransformation des hydrocarbones halogénés a ét,é décriÈe par AIIDERS (1984) . Cependant, la lipoperoxydation représent,e. Ie phénomène majeur de f impact, du CCI4 sur le foi9. Depuis-environ bO ans de trés nombreux èhercheurs se sont, penchés sur l'étude de
ce t,oxigrre et certains articles de synt'!!9e constituent des réfêrences de base très document,ées (RECKNÀGEL et GHOSHAT L966, RECKNAGEL L967, RECKNAGEL er GLENDE f9?3, RECKNAGEL eË al..L97'7, s L a t g n 1 9 ? 9 , 3 1 , a t e n t g g 2 , B R I D G E S e t a 1 , . 1 9 8 3 , R E C K N A G E L 1 9 8 3 , S L A T E R ! 9 8 4 a , B A C O N e t a 1 . . 1 9 8 6 ' P L A A 1 9 8 6 ) .
L 2
L e s o r i n c i o e s d e l a l j . n o p e r o x v d a t i o n :
Le CC14 est. mét,abolisé par réduct,ion éIéct,ronigue 91!11Vsée Àpe"ifiq,,rement par Ie cytôchrome P 450 (NOGUCHf et al'.1982) - La ièactiori produil un radiàal trichlorornéthyl ('CC13)
C C 1 4 + e - ' c c 1 3 + cl
E n p r é s e n c e d r o x y g è n e m o l é c u l a i r e , I a p l u p a r t . d e s r a d i c a u x ' C C 1 3 réalissent pour iormer le radical libre t,richlorométhylperovy
t ' o ô c c r f ) ( p  c x g n e Ê a 1 , . 1 9 ? 8 ) . C e r a d i c a L b e a u c o u p p l u s r é a c t i f gue le ( iCCL3) est, responsable de l'at,tague d'un groupement fràiiryiÀ".' situé entre dêux doubles. Iiaisons - dans une chaine âf ipi..tiq,.re d,'un acide gras _ polyinsaturé. Des acides gras pàfvi"""iurés ent,rent dans Ia composition des phospholipides iremËranaires et, ainsi s'initie le processus de lipoperoxydation: iileign 1984a) . Il en d,écouJ.e une suit,e de rêactions chimigues cornplexes grri mènent à la décomposition des acides gras p o t y i n s a t u r é s ( P O R T E R 1 9 8 4 , S I  T E R f 9 8 4 b ) .
Le processus se déroule en 3 Phases : - phase d'initiation
Les molécu1es d,acj.de gras potyinsat,urés (ÀGPI) sont at,taquées préférent,j.ellement par le radicaux libres au nj.veau des atomes àrhydrogène de groupernents méthylènes (CH^) sit'ués ent,re deux d o u b l e s l i a i s o n s C : C . z
- phase de ProPagation
A p r è s I ' a t t a g u e d e I ' A G P I p a r I e r a d i c a l l i b r e ( ' C C f 3 ) i l s e fôrrne imrnédiâtemenÈ un radical libre lipidigue ( 'L) avec déplacement, d,un électron du radical libre par résonnance. ceiui-ci réagit t,rès rapidement avec I',oxygène moléculaire pour f o r m e r u n r a d i c a l l i b r e l i p o p e r o x y ( ' O O L ) .
Au niveau des lipoprotéines de Ia nenbrane cellulaire, Ies cÀaines d, acide graê qui constituent les phospholipides sont, très À C r o i t e m e n t j u x t à p o s é s . A i n s i r u n r a d i c a l l i b r e l i p o p e r o x y . s i t u é sur une cnàine d'un acide gras phospholipidigue réagit en arrachant un hyd.rogène du méthylène de I'acide gras polyinsaturé v o i s i n , à t ' o i i g i À e d ' u n h y d r o p e r o x y d e l i p i d i g t - r e ( L O O H ) et, d'un n o u v e a u r a d i c à I l i b r e t i p i d i g u e ( ' t ) . C e p h é n o m è n e autocatalytigrre peut se propager théorigrrement de proche en p r o c h e .
. O O L + LH - phase t,erminale
Elle correspond à l'inact,ivation des radicaux libres pouf about'ir à Ia produètion d'une molécule stable gr:i peut être obt'enue de p l u s i e u r s f a ç o n ( P R Y O R 1 9 7 6 )