la
première partie
de la thèse
123
CHAPITRE IV : OXYDATION STATIQUE
304L.
125 SOMMAIRE
IV.1. Introduction ... 126
IV.2. Caractérisation des couches de passivation ... 127
IV.2.1. Exposition en milieu vapeur (400°C – 500h) d’une plaquette polie miroir 127 IV.2.2. Exposition en milieu vapeur (400°C – 500h) d’une plaquette rectifiée ... 133
IV.2.3. Exposition en milieu REP (340°C – 500h) d’une plaquette polie miroir .. 137
IV.2.4. Exposition en milieu REP (340°C – 500h) d’une plaquette rectifiée ... 139
IV.2.5. Synthèse : ... 141
IV.3. Etude de la réactivité de la surface en milieu REP à 340°C ... 143
IV.3.1. Effet de la préparation de surface sur la cinétique de croissance de la couche d’oxyde…… ... 143
IV.3.2. Pénétrations intergranulaires d’oxydes ... 147
IV.3.3. Bilan de l’influence de l’état de surface ... 152
IV.4. Comparaison des produits de corrosion milieu vapeur/milieu REP ... 154
126
IV.1. Introduction
Ce chapitre présente la réactivité de surface des matériaux de l’étude dans le cadre de la problématique de la corrosion sous contrainte. Les matériaux utilisés dans les réacteurs à eau pressurisée sont résistants à la corrosion généralisée dans un environnement REP, en milieu primaire. Cette résistance est due à la présence d’une fine couche d’oxyde appelée ‘couche de passivation’ ou ‘couche passive’. Cependant, l’altération locale des propriétés de la couche passive peut induire une sensibilisation à la corrosion localisée du matériau. Cette altération peut être due à une attaque chimique (cas de la corrosion par piqûres causée généralement par l’action de certaines espèces chimiques telles que les ions chlorures) ou à une sollicitation mécanique (corrosion sous contrainte). L’endommagement par corrosion sous contrainte est considéré comme une dégradation inhérente à l’état passif du matériau. Il est donc primordial de caractériser cette couche passive par une étude complète de l’oxydation statique des nuances de l’étude en particulier de l’acier inoxydable 304L. L’étude de l’oxydation de la nuance A-286 sera réalisée dans le chapitre suivant, dans le cadre de l’étude des interactions entre la localisation de la déformation plastique dans des bandes de déformation et le film passif. Cette étude sur l’oxydation a pour objectif :
d’appréhender les mécanismes se produisant en surface lors de la formation du film passif sur cette nuance lorsqu’elle est immergée en milieu nominal REP. Nous étudions la nature des couches formées, leur composition chimique ainsi que l’évolution des éléments chimiques tels le chrome et l’oxygène du substrat vers le film passif.
d'étudier l’influence des modifications microstructurales se produisant sous la couche d’oxyde.
d’étudier l’effet de l’état de surface sur la nature et sur la cinétique des produits de corrosion formés. Rappelons que l’état de surface en service est un état brut d’usinage ou un état de rectification mécanique pour la finition de la visserie. A contrario pour les études de CSC en laboratoire, l’état de surface des éprouvettes est généralement poli miroir, dans le but de découpler l’effet de l’état de surface des mécanismes intrinsèques conduisant à la fissuration par CSC. Un des objectifs de cette étude est de quantifier l’impact de l’état de surface sur la croissance de la couche d’oxyde, et ainsi valider un état de surface pour les essais de CSC. Deux états de surface ont été étudiés : (i) un état rectifié, (ii) un état de surface poli miroir après usinage par électroérosion.
L’étude évaluera également l’effet accélérant d’un milieu de type vapeur d’eau par rapport à un milieu REP nominal, et la représentativité des produits de corrosion formés dans ce milieu par rapport à un milieu nominal REP.
Le chapitre est structuré comme suit :
dans un premier temps, nous caractérisons la couche de passivation formée lors de l’oxydation successivement en milieu vapeur à 400°C et en milieu REP à 340°C de plaquettes d’acier inoxydable 304L avec deux états de surface différents : un état de surface rectifié et un état poli miroir après usinage par électroérosion. Ensuite, l’étude de
127
la réactivité de surface de l’acier exposé en milieu REP à 340°C est abordée avant d’établir la comparaison des produits de corrosion formés en milieu vapeur par rapport au milieu REP.
IV.2. Caractérisation des couches de passivation
Dans le but de caractériser les produits de corrosion obtenus, une approche multi échelle a été mise en place : la microscopie optique (MO), la microscopie électronique à balayage (MEB) et la Microscopie Electronique à Transmission (MET) couplée à la spectroscopie EELS (spectroscopie de pertes d’électrons) ont été utilisées. Les observations ont été réalisées sur des échantillons polis miroir après usinage par électroérosion (voir la procédure de préparation dans le chapitre 2) et des échantillons rectifiés, exposés en milieu vapeur à 400°C pendant 500h ou en milieu REP simulé à 340°C pendant 500h. Les résultats sont présentés pour les deux milieux de l’étude.
IV.2.1.
Exposition en milieu vapeur (400°C – 500h) d’une
plaquette polie miroir
Dans cette première étude, toute la démarche de caractérisation est détaillée. Une vue générale de la surface obtenue au microscope optique (Figure IV-82) montre des inhomogénéités de la couche d'oxyde sur la surface de l'échantillon. En effet, l’oxydation de la phase ferrite δ en forme de radeaux est différente de celle de la matrice austénitique. Cette inhomogénéité de comportement entre les deux phases résulte d’une cinétique d’oxydation variable entre la ferrite δ et l’austénite γ. Le mécanisme d’oxydation semble être favorable à l’austénite γ car la couche d'oxyde est plus dense et plus compacte que pour la ferrite δ. L'oxydation est un phénomène lié à la diffusion des espèces anioniques impliquées dans les réactions électrochimiques, du matériau vers le milieu, ou à la diffusion de ces espèces de la couche d'oxyde vers la solution et parallèlement de la solution vers le métal. Lorsque deux phases de compositions chimiques différentes sont présentes dans le matériau, la concentration en espèces anioniques impliquées dans les réactions électrochimiques est également variable d’une phase à l’autre. Cela peut expliquer que la cinétique d'oxydation soit différente à la surface de ces deux phases, d’où une oxydation préférentielle de l’une des phases (austénite γ dans notre cas).
128
Figure IV-82 : Oxydation du 304L en milieu vapeur (400°C, 500h) a) Image en microscopie optique de la surface d’une plaquette polie miroir b) zoom sur une zone montrant une interface ferrite δ / austénite γ. Afin de compléter les observations réalisées en microscopie optique, les couches d’oxyde ont été caractérisées au MEB/FEG. Une image de la surface réalisée en électrons secondaires est présentée sur la Figure IV-83, où l’hétérogénéité d’oxydation constatée entre les deux phases est confirmée. Deux zones d'oxydation (identifiées A et B) sont très clairement distinguées. L’analyse chimique en EDX de ces deux zones a permis de montrer que la zone oxydée B correspond à la ferrite δ car le pourcentage atomique de Cr augmente dans cette zone tandis que le pourcentage atomique de Ni est divisé par 2 par rapport à la zone oxydée A correspondant à l’austénite γ.
A B
Figure IV-83 : Images en électrons secondaires des zones d’oxydation préférentielle. La zone A avec une plus grande densité d’oxydes correspond aux grains d’austénite γ, tandis que la zone B est identifiée comme
étant de la ferrite δ.
Cependant, même si une variation de la densité des cristallites a été constatée pour les zones A et B, la morphologie du film semble identique : une première couche compacte constituée de petites cristallites nanométriques, sur laquelle sont déposées, de manière
a) b)
129
hétérogène, des cristallites dont la taille varie de 400 à 600 nm. Ces cristallites appartenant à la couche externe sont facettées et de morphologie polyédrique comme le montre une image obtenue à plus fort grandissement de la zone A sur la Figure IV-84.
Figure IV-84 : Oxydation du 304L en milieu vapeur (400°C, 500h) .Image en électrons secondaires de l’oxyde de surface d’une plaquette polie. Zoom de la zone A de la Figure IV-2.
La proportion de ferrite dans le matériau étant relativement faible (entre 2,5 et 6% selon la technique d’observation utilisée), les observations ont été réalisées sur la phase austénitique. Afin de caractériser plus finement la couche d’oxyde (nature, composition chimique), des analyses MET ont été effectuées en coupe transverse de l’échantillon. Une vue en coupe de la surface oxydée est présentée sur la Figure IV-85 .
Figure IV-85 : Oxydation du 304L en milieu vapeur (400°C, 500h). Plaquette polie miroir. Image en champ clair de la coupe transverse de la couche d’oxyde.
Cette couche d’oxyde est constituée de gros cristallites (pointés 1 et 2 sur la Figure IV-85 de composition EDX (90% at Fe, 6% at Cr et 4% at Ni) dont la taille peut atteindre le micromètre. Ces cristallites ont une forme facettée comme observées au MEB (Figure IV-84). Une étude par diffraction électronique (Figure IV-86) sur deux de ces cristallites montre que ce sont des cristallites de magnétite (groupe d’espace : Fd-3m, a= 8.41 Å). La mesure des distances inter-réticulaires et des angles entre les plans confirment une phase magnétite.
Cristallites facettées et de morphologie polyédrique
130
Figure IV-86 : Images en champ clair de cristallites de magnétite associées aux diagrammes de diffraction. De plus, une analyse en mode STEM EELS sur ces mêmes cristallites (pointé 1 et 2 de la Figure IV-85) montre une signature au seuil L2,3 du Fe et au seuil K de l’oxygène (Figure
IV-87) parfaitement superposable aux seuils du Fer et de l’oxygène de la magnétite Fe3O4
(Fe2+ Fe3+2O4) de référence.
Figure IV-87 : Spectres EELS en mode STEM (nanosonde) au seuil L 2,3 du Fer (à gauche) et au seuil K de l’oxygène (à droite) obtenues sur les cristallites (pointés 1 et 2 de la Figure IV-85). Les spectres des deux
pointées sont identiques.
La couche d’oxyde est également constituée de cristallites de plus petites tailles variant de10 à 25 nm et dont la composition, mesurée par EDX, est 70% at. Fe, 27% at. Cr et 3% at. Ni (pointés 3, 4 et 5 sur la Figure IV-85). Ces cristallites forment une couche plus compacte que la magnétite et sont de forme non facettée. L’étude en STEM EELS sur ces petites cristallites a montré des positions en énergie et une signature au seuil L2,3 du Fer
et au seuil K de l’oxygène qui sont modifiées par rapport aux signatures de la magnétite de référence (Figure IV-88).
700 705 710 715 720 725 730 Fe1_Magnetite
Energy Loss (eV) 520 530 540 550 560 570 580
O1_Magnetite
131
Figure IV-88 : Spectres EELS a) au seuil L2,3 du Fer, b) au seuil K de l’oxygène et c) au seuil L2,3 du chrome effectués sur des cristallites non facettées (pointés 3, 4 et 5 de la Figure IV-85). Les spectres du fer et de
l’oxygène sont associés avec ceux de la magnétite Fe3O4 de référence pour comparaison tandis que les spectres du chrome sont associés aux références du Cr4+ (CrO2) et du Cr3+ (Cr2O3).
La position en énergie du fer correspond à la signature du fer au degré d’oxydation +2. Le seuil K de l’oxygène ne présente pas de décalage en énergie. Néanmoins le premier pic à 531 eV présente une surface différente montrant un environnement chimique différent de l’oxygène dans la structure. Pour ce qui concerne le seuil L2,3 du chrome, la
position en énergie est comparable à celle du chrome au degré d’oxydation +3. Par contre les structures fines (allure de la courbe) de ces cristallites au seuil L2,3 du Cr sont
différentes de celles de Cr2O3 (Figure IV-88). On peut conclure que la composition des
cristallites est très proche du spinelle Fe2+Cr3+2O4.
Au voisinage de l’interface oxyde/substrat, la concentration en Cr augmente dans l’oxyde jusqu’à atteindre 50% at. Cet oxyde n’est pas homogène en épaisseur sur toute la surface (pointés 6 et 7 de la Figure IV-85) étudiée. Nous observons une bande d’oxyde sous les cristallites de magnétite d’environ 100 nm d’épaisseur (pointé 7 de la Figure IV-85) qui est riche en chrome (50% at Cr). Cette bande, observée en haute résolution, présente une très fine recristallisation. L’analyse EELS effectuée sur cet oxyde (pointés 6 et 7 de la
520 530 540 550 560 570
O-K
Energy Loss (eV)
Fe
3O4
part non facettée
700 705 710 715 720 725 730 735 740
Fe-L2,3
Energy Loss (eV)
Fe
3O4
Part non Fac
b) a)
570 575 580 585 590 595 600
EELS-Cr-L 2,3
Pertes d'énergie (eV) Cr
2O3 CrO
2 Part non facettée
132
Figure IV-85) montre les mêmes spectres EELS que pour les petites cristallites non facettés c’est à dire une couche dont la composition serait proche du spinelle Fe2+Cr3+2O4
et non du composé Cr2O3.
De plus, l’analyse EFTEM (Figure IV-89) (Energy Filtered Transmission Electron Microscopy) sur cette zone perturbée montre, en filtrant au seuil du fer et du chrome, un important enrichissement de cette interface en chrome. Le filtrage au seuil K de l’oxygène nous montre que cette couche appartient bien à l’oxyde.
Figure IV-89 : EFTEM sur la zone perturbée située au niveau des cristallites 3, 4, 5 de la Figure IV-85. a) Fe : jaune – Cr : bleu b) carte de l’oxygène.
Si on s’intéresse maintenant au substrat, celui-ci ne présente aucune déformation comme le montre la Figure IV-85. En effet, la préparation de surface crée généralement à la surface de l’échantillon une modification de l’état de contraintes et génère donc des amas de dislocations en extrême surface, de la recristallisation dynamique et dans certains cas de finition par usinage, de la martensite de déformation. Dans notre cas, la finition de la préparation réalisée par OPS (polissage à l’oxyde de silicium) a permis de s’affranchir de cet écrouissage de surface. L’analyse EDX montre lorsqu’on s’éloigne de l’oxyde un appauvrissement en nickel et un enrichissement en chrome sur une épaisseur d’environ 1 m. On retrouve la composition classique de l’acier à 1,5 m de profondeur
.
133
Nature Formule spinelle Epaisseur Remarque
Couche externe
Magnétite Fe3O4 jusqu'à
1µm Type Fe2+Fe3+2O4 spinelles (Fe,Ni)Crtype
2O4 10 - 25 nm
Plus riche en chrome que Fe3O4 et moins
que les spinelles de la couche interne. Non facettée
Couche
interne spinelles (Fe,Ni)Crtype 2O4 -
Fine couche riche en Cr (100nm d'épaisseur)
Substrat austénitiques Grains - - Enrichissement en chrome en s'éloignant non déformé, pas de recristallisation de l'oxyde sur 1µm
Tableau IV-10 : Résumé des résultats de caractérisation de la couche d’oxyde obtenue après exposition 500h de la nuance 304L avec un état de surface poli miroir en milieu vapeur à 400°C.
IV.2.2.
Exposition en milieu vapeur (400°C – 500h) d’une
plaquette rectifiée
Soit S0 la surface moyenne de telle sorte que h0 = 0 (Figure IV-90), nous définissons :
l’intérieur des stries lorsque h1 – h0 > 0
l’extérieur des stries lorsque h1 – h0 < 0
Figure IV-90 : Représentation schématique des stries de rectification et de la rugosité de surface Une vue d’ensemble en microscopie optique de la couche d’oxyde (Figure IV-91) montre la présence de cristallites ainsi que de stries de rectification. Les différences de hauteur d’une strie à l’autre en surface font qu’il est difficile d’obtenir une image nette en profondeur (dans la strie) et en hauteur (sur la strie). Sur cette figure à faible grandissement, nous notons une oxydation différente de celle observée sur l’échantillon poli, avec une réactivité variable le long de la rugosité de surface. Le focus est effectué à l’intérieur de la strie afin de mettre en évidence la faible densité de cristallites.
134
Figure IV-91 : Oxydation du 304L en milieu vapeur (400°C, 500h). Plaquette rectifiée. Image en microscopie optique.
L’image obtenue au MEB (Figure IV-92) de la surface du matériau montre la forte rugosité de surface et la présence de cristallites non uniformément réparties sur la surface.
Figure IV-92 : Oxydation du 304L en milieu vapeur (400°C, 500h). Plaquette rectifiée Image en électrons secondaires (MEB ) présentant l’oxydation en surface l’échantillon.
La couche d'oxyde présente, comme pour l’échantillon poli, une structure duplex (Figure IV-93), elle est constituée d'une couche externe (cristallites facettées micrométriques) et d'une couche interne plus dense et compacte. La couche d'oxyde semble moins dense à l’intérieur des stries de rectification, qu’à l’extérieur.
Figure IV-93 : Oxydation du 304L en milieu vapeur (400°C, 500h). Plaquette rectifiée. Image en électrons secondaires (MEB) de la couche d’oxydes en dehors des stries de rectification.
135
Une étude en MET d’une coupe transverse de la couche d’oxyde permet de visualiser et d’étudier l’oxyde ainsi que l’interface oxyde/substrat.
Une vue générale de l’oxyde est représentée sur la Figure IV-94 a). La Figure IV-94 b) indique une zone agrandie (indiquée par des pointillés) de la vue d’ensemble.
Figure IV-94 : Oxydation du 304L en milieu vapeur (400°C, 500h). Plaquette rectifiée. a) Image en champ clair de la couche d’oxyde b) zoom sur une zone d’intérêt représentée par un rectangle en pointillés. L’oxyde est constitué de grosses cristallites dispersées sur l’ensemble de la surface. Leur taille est de l’ordre de 300 à 500 nm. L’analyse EDX effectuée sur ces gros cristallites montre une composition chimique en % at de 91-94% Fe, 4-7% Cr et 1-2% Ni. Un diagramme de diffraction obtenue sur la cristallite représentée sur la Figure IV-95 est indexé selon l’axe de zone [011] de la magnétite Fe3O4 (Fd- 3m de paramètre de maille a=
8,41 Å) (Figure IV-95).
Figure IV-95 : Oxydation du 304L en milieu vapeur (400°C, 500h). Plaquette rectifiée. Image en champ clair d’une cristallite de magnétite associée à son diagramme de diffraction.
L’oxyde est également constitué de cristallites de plus petite taille (Figure IV-94 a)) qui forment une couche compacte de l’ordre de 50 nm d’épaisseur. La composition chimique, déterminée par EDX, de ces cristallites est de 65% Fe, 26% Cr et 8% Ni. Ces cristallites sont plus riches en chrome et nickel que la magnétite. Les analyses EELS sont comparables à celles réalisées sur les petits cristallites non facettés de l’échantillon 304L poli. _ 022 _ 022 _ 111 _ 111 _ 111 __ 111 _ _ 200 200 _ 311 _ 311 _ _ [011] _ 022 _ 022 _ 022 _ 022 _ 111 _ 111 _ 111 _ 111 _ 111 __ 111 __ 111 _ _ 111 _ _ 200 200 _ 200 _ 311 _ 311 _ 311 _ _ 311 _ _ [011]
136
Une très fine couche (de 5 à 10 nm) (Figure IV-94 b)) est visible dans les zones les plus fines de la lame. Cette couche analysée par EDX montre un enrichissement important en chrome (46% Fe, 49% Cr et 5% Ni).
De plus, l’étude EELS sur le seuil L2,3 du Fer, du Cr et au seuil O-K confirme des
signatures comparables au composé (Fe,Ni)Cr2O4. Ces cristallites sont donc des spinelles
de type FeCr2O4 riches en chrome. L’étude effectuée en EFTEM (Figure IV-96) sur cette
fine couche montre en filtrant au seuil du chrome et de l’oxygène un enrichissement en chrome de cette interface. Le filtrage au seuil K de l’oxygène nous montre que cette couche appartient bien à l’oxyde.
Figure IV-96 : Image filtrée sur le seuil du chrome et de l’oxygène montrant la fine couche riche en chrome d’interface avec le substrat (EFTEM)
Le substrat présente une surface perturbée sous l’oxyde (Figure IV-97) ne montrant pas d’enrichissement en chrome. Il s’agit d’une recristallisation sous forme de petits grains (taille de grains de l’ordre de 100 nm) sur 1,5 μm de profondeur. Un diagramme de diffraction effectué sur ce substrat et représenté sur la Figure IV-97 est constitué d’anneaux concentriques qui sont caractéristiques d’une zone finement cristallisée. Les distances interréticulaires mesurées (2Å, 1,78 Å, 1,1 Å, 0,9 Å et 0,8 Å) sont celles du fer austénitique de paramètre de maille a=3,60 Å.
Figure IV-97 : Image en champ clair de la couche d’oxyde et diagramme de diffraction du substrat déformé sous l’oxyde.
137
Les résultats de cette partie de l’étude sont récapitulés dans le Tableau IV-11.
Nature Formule spinelle Epaisseur Remarque
Couche externe
Magnétite Fe3O4 300 -
500nm Type Fe2+Fe3+2O4 spinelles (Fe,Ni)Crtype
2O4 50nm
Plus riche en chrome que Fe3O4 et moins
que les spinelles de la couche interne.
Couche
interne spinelles (Fe,Ni)Crtype 2O4 5 - 10 nm Couche interne riche en Cr
Substrat austénitiques Grains - -
Présence d'une zone recristallisée (Taille des grains 100nm) sur 1,5µm en profondeur. Composition chimique
proche de celle de la matrice Tableau IV-11 : Résumé des résultats de la caractérisation de la couche d’oxyde obtenue après exposition
500h de la nuance 304L avec un état de surface rectifié en milieu vapeur à 400°C.
En conclusion, pour l’oxydation en milieu vapeur, la couche d’oxyde est plus épaisse pour les échantillons polis que pour les échantillons rectifiés. De plus, la couche protectrice riche en chrome peut atteindre 100nm d’épaisseur pour les échantillons polis alors que pour les échantillons rectifiés, elle est de l’ordre de 5 à 10nm.
Nous allons caractériser à présent la nature de la couche d’oxyde développée lors de l’exposition en milieu primaire REP. Ces conclusions seront d’autant plus intéressantes qu’elles donnent une indication sur les couches passives protectrices se formant au niveau des internes de cuve en acier inoxydable dans les REP.
IV.2.3.
Exposition en milieu REP (340°C – 500h) d’une
plaquette polie miroir
Les observations en MO montrent des hétérogénéités d’oxydation (Figure IV-103 b)). Ces hétérogénéités étant en rapport avec la ferrite δ, les prélèvements des lames MET servant à la préparation des coupes transverses ont été réalisées au niveau des zones homogènes de la plaquette oxydée représentatives de l’état d’oxydation général de la matrice austénitique.
La Figure IV-98 montre la couche d’oxyde formée en milieu simulé REP. La structure duplex de l’oxyde est identifiée, avec la couche d’oxyde externe constituée des cristallites facettées, déposées sur une couche d’oxyde interne plus compacte et de faible épaisseur.
138
Figure IV-98 : Oxydation du 304L en milieu primaire REP (340°C, 500h). Plaquette polie miroir. Image en champ clair de la couche d’oxyde.
La couche d’oxyde externe est constituée de grosses cristallites dispersées à la surface et de composition chimique proche de celle de la magnétite Fe3O4 (jusqu’à 75% at de fer,
16% at de Cr et 9% at de Ni). Ces cristallites de magnétite sont peu nombreuses et leur taille peut atteindre 1µm. La plupart des cristallites déposées en surface ont une composition chimique proche de la spinelle (Fe,Ni)Cr2O4 et de taille variant de 50 à
100nm. Ces cristallites de type Fe,Ni(Cr)2O4 (de composition chimique 75% at. Fe, 15%
at Cr, 10% at Ni) sont enrichies en Ni et Cr par rapport aux grosses cristallites de magnétite.
Ces cristallites sont déposées sur la couche compacte d’oxyde riche en chrome. L’épaisseur de cette couche est inhomogène en épaisseur et varie de 50 à 200nm. La teneur en chrome dans cette couche varie entre 40% et 55% at.
Au niveau du substrat, au voisinage de l’interface substrat/oxyde, un enrichissement important de nickel jusqu’à 40% at. (appauvrissement en chrome) est observé sur une profondeur de 100nm. Grâce aux analyses EDX, nous avons montré que l’épaisseur de cette couche de substrat enrichie en nickel est par endroit deux fois plus importante que la couche compacte riche en chrome. La présence de nano grains allongés dans le substrat à une profondeur voisine de 400 – 500nm est montrée sur la Figure IV-99. Le cliché de diffraction associé confirme la recristallisation de cette zone en sous couche du substrat.
Figure IV-99 : Oxydation du 304L en milieu primaire REP (340°C, 500h). Plaquette polie miroir .Image en champ clair de la coupe transverse du substrat montrant la présence de nano grains allongés dans le
139
Dans le Tableau IV-12, sont résumés les résultats de la caractérisation de la couche d’oxyde obtenue.
Nature Formule spinelle Epaisseur Remarque
Couche externe
Magnétite Fe3O4 jusqu'à 1µm Très peu nombreux, quelques cristallites seulement
spinelles (Fe,Ni)Crtype
2O4 50 - 100nm
Plus représentatives de la couche d'oxyde externe
Couche
interne spinelles (Fe,Ni)Crtype 2O4 > 50nm fine couche riche en Cr
Substrat austénitiques Grains - -
Présence d'une zone recristallisée (grains allongés de 100nm d'épaisseur) sur 500nm en
profondeur. Enrichissement en Ni d’abord puis composition chimique proche de celle de
la matrice
Tableau IV-12 : Résumé des résultats de la caractérisation de la couche d’oxyde obtenue après exposition 500h de la nuance 304L avec un état de surface poli miroir en milieu REP à 340°C.
IV.2.4.
Exposition en milieu REP (340°C – 500h) d’une
plaquette rectifiée
La dernière étape de cette phase de caractérisation consiste à analyser la couche d’oxyde formée sur la plaquette avec un état de surface rectifié et exposée en milieu REP à 340C° pendant 500h.
Les images obtenues au MO (Figure IV-103) montrent une oxydation qui semble uniforme le long des stries de rectification.
Une vue générale de la coupe transverse de cette couche d’oxyde est présentée sur la
Figure IV-100. Très peu de cristallites sont observées en surface. Celles qui sont
observées (Figure IV-101) ont été identifiées comme étant de la magnétite Fe3O4 par
l’intermédiaire des clichées de diffraction qui leur sont associés. Leurs tailles varient de 300 à 700nm.
Figure IV-100 :Oxydation du 304L en milieu primaire REP (340°C, 500h). Plaquette rectifiée. Image en champ clair de la couche d’oxyde.
140
Figure IV-101 : Oxydation du 304L en milieu primaire REP (340°C, 500h). Plaquette rectifiée Image en champ clair d’une cristallite de magnétite Fe3O4 et le cliché de diffraction observé.
Des cristallites de plus petites tailles (20 à 40 nm) sont dispersées autour des grosses cristallites. Cependant, ces cristallites de composition chimique moyenne 57% at. Fe, 35% at. Cr et 8% at. Ni sont enrichies en chrome et nickel et appauvries en fer par rapport aux cristallites de magnétite, ce qui suggère les spinelles de type Fe,Ni(Cr)2O4.
Ces cristallites sont dispersées sur une fine couche d’oxyde interne, épaisse de 10nm et enrichie en chrome. Le pourcentage en chrome peut atteindre 55% atomique. Enfin, sous la couche d’oxyde au voisinage de l’interface oxyde / métal de base, le substrat présente une couche constitués de nanograins sur une profondeur de 1,5µm. L’interface oxyde/substrat présente un enrichissement en nickel (jusqu’à 15%) accompagné d’un appauvrissement en chrome dont la teneur passe à 18% (contre près de 50% dans la couche interne), mais le substrat reprend rapidement la composition chimique de l’austénite.
Les résultats de la caractérisation de la couche d’oxyde sont résumés dans le Tableau IV-13 :
Nature Formule
spinelle Epaisseur Remarque
Couche externe
Magnétite Fe3O4 300 - 700nm Très peu nombreux, quelques cristallites seulement
spinelles (Fe,Ni)Crtype
2O4 20 - 40nm
Plus représentatives de la couche d'oxyde externe
Couche
interne spinelles
type
(Fe,Ni)Cr2O4 10nm fine couche riche en Cr (10 nm)
Substrat austénitiques Grains - -
Présence d'une zone recristallisée sur 1,5µm en profondeur. Faible enrichissement en Ni
sur quelques nanomètres, mais la composition chimique se rapproche très vite
de celle de la matrice Tableau IV- 13: Résumé des résultats de la caractérisation de la couche d’oxyde obtenue après exposition
500h de la nuance 304L avec un état de surface rectifié en milieu REP à 340°C.
En conclusion, pour les échantillons exposés en milieu REP, la couche d’oxyde est plus épaisse pour les échantillons polis que les échantillons rectifiés. La couche protectrice riche en chrome peut atteindre 100 nm pour les échantillons polis alors que son épaisseur est seulement de 10 nm pour les échantillons rectifiés. Ces conclusions sont cohérentes avec celles tirées des analyses en milieu vapeur.
141
IV.2.5.
Synthèse :
Dans cette partie, la nature de la couche de corrosion développée lors de l’exposition pendant 500h en milieu vapeur (400°C) et en milieu simulé REP (340°C) est caractérisée. Afin de tester la réactivité de surface dans les deux milieux, deux états de surface différents sont testés : la moitié des échantillons prévus pour la caractérisation sont polis miroir et l’autre moitié finie par rectification. Les principaux résultats sont les suivants :
En milieu vapeur comme en milieu REP, la couche d’oxyde présente un caractère duplex : une couche d’oxyde externe et une couche d’oxyde interne.
a) La couche externe est constituée de cristallites facettées polyédriques de magnétite Fe3O4 et de cristallites de taille moins importante de type
(Fe,Ni)Cr2O4. Elle est poreuse et peu protectrice. En milieu vapeur, l’épaisseur
moyenne de cette couche est plus importante que celle mesurée en milieu REP. En milieu REP, les cristaux de magnétite sont moins nombreux et dispersés sur la couche d’oxyde interne. La couche d’oxyde externe est enrichie en Fer pour les gros cristallites de magnétite, puis appauvrie en Fer et enrichie en Nickel et Chrome pour les spinelles par rapport aux cristallites de magnétite. b) La couche d’oxyde interne est quant à elle plus compacte et donc moins poreuse que la couche externe. Son observation à haute résolution dans le cas des échantillons oxydés en milieu vapeur montre qu’elle est constituée de nano cristallites qui ont été identifiées comme étant des spinelles de type FeCr2O4
grâce à une analyse EELS. Dans le cas des échantillons oxydés en milieu REP, la couche d’oxyde interne étant très fine, les éléments la constituant ne sont pas précisément définis. Cependant, les analyses EDS montrent que la concentration en chrome atteint 55% at et que la couche interne est moins riche en nickel que la couche externe. La concentration en fer et oxygène est également plus faible. L’épaisseur de la couche est inhomogène et varie de 75 à 100nm dans le cas des échantillons oxydés en milieu vapeur et de 10 à 50 nm pour les échantillons oxydés en milieu REP. Cette couche est également nommée couche d’interface car elle se situe entre la couche d’oxyde externe et le métal de base. De plus, nous rappelons que l’interface oxyde externe / oxyde interne représente l’ancienne interface métal de base / environnement.
Cette structure duplex de l’oxyde formée sur un acier inoxydable en milieu aqueux à haute température (entre 200 et 400°C) a été mise en évidence par de nombreuses études (Robertson 1989; Aaltonen, Mäkelä et al. 1998; Stellwag 1998; Ziemniak and Hanson 2002; Terachi, Fujii et al. 2005; Lozano-Perez, D. W. Saxey et al. 2010). Ils confirment la présence dans la couche d’oxyde externe de magnétite et de spinelles pouvant contenir du chrome et du nickel (selon la composition de l’alliage) tandis que la couche interne est enrichie en chrome et constituée de spinelle riche en chrome. En milieu vapeur, Stellwag et al (Stellwag 1998) et Warzee et al (Warzee 1965) ont également mis en évidence cette configuration de la couche d’oxyde ainsi que les éléments la constituant.
Dans le cas des échantillons rectifiés (oxydés en milieu vapeur et REP), la zone située sous la couche d’oxyde au voisinage de l’interface oxyde / métal est recristallisée et constituée de nanograins dont la composition chimique est enrichie en nickel par rapport au métal de base. Elle peut s’étendre jusqu’à 1,5 µm (cas des échantillons usinés). Cette zone recristallisée est inexistante pour
142
l’échantillon poli et oxydé en milieu vapeur, et peu étendue (500nm au maximum) pour l’échantillon poli et oxydé en milieu REP. Il apparaît que plus la préparation est fine, et moins la zone recristallisée et étendue. Une préparation de surface sévère développe l’écrouissage de surface, d’où la présence de la zone recristallisée, et dans certains cas de martensite d’écrouissage.
Les couches d’oxyde caractérisées dans cette l’étude sont schématisées sur la Figure IV-102.
Figure IV-102 : Représentation schématique de la couche d’oxyde formée sur les plaquettes de 304L a) polies miroir et exposées en milieu vapeur 400°C pendant 500h b) Rectifiées et exposées en milieu vapeur à 340°C pendant 500h c) polies miroir et exposée en milieu REP simulé à 340°C pendant 500h d) Rectifiées et
exposées en milieu REP simulé à 340°C pendant 500h.
a) b) c) d) Fe3O4 Spinelle de type (Fe, Ni)Cr2O4 1µm 100nm Fe3O4 Spinelle de type (Fe, Ni)Cr2O4 500nm 5 - 10nm 500nm Zr=1,5µm Zr = 400 – 500nm Quelques cristallites Fe3O4 (Taille maximale 1µm)
Spinelles de type (Fe,Ni)Cr2O4
(50 - 100nm)
50nm en moyenne 200nm par endroits)
Spinelles (Fe, Ni)Cr2O4
(300 - 700nm)
Petites cristallites enrichies en Fer (25 et 50nm).
10nm Zr =1,5µm
143
IV.3. Etude de la réactivité de la surface en milieu
REP à 340°C
IV.3.1.
Effet de la préparation de surface sur la cinétique de
croissance de la couche d’oxyde
Le but de cette partie est d’évaluer le rôle de l’état de surface sur les caractéristiques de la couche d’oxyde en milieu primaire REP. L’influence de l’état de surface est étudiée en oxydant dans un même milieu des plaquettes avec deux niveaux d’écrouissage très différents : les échantillons polis de telle sorte que sur une épaisseur initiale de 2mm, 250µm de matière sont enlevés de part et d’autre afin de réduire au mieux l’écrouissage initial et les échantillons dont la finition correspond à un usinage par rectification. Nous mettons en évidence les modifications suivantes entre les échantillons polis et finis par rectification :
- En termes de morphologie des oxydes
Les images au microscope optique ont été réalisées sur les échantillons polis et rectifiés, avant et après l’essai de corrosion en milieu REP (Figure IV-103). L’aspect des échantillons après exposition est relativement différent entre l’échantillon poli et celui rectifié. En dehors de la présence de stries de rectification résultant de la finition de l’usinage, la couleur de la couche d’oxyde formée n’est pas la même. En effet, les échantillons rectifiés exposés en milieu simulé REP sont d’aspect sombre et de couleur plutôt marron, laissant paraître les stries d’usinage alors qu’un oxyde plus coloré (bleuâtre) parsemé de petites tâches oranges s’est formé sur les échantillons polis. La couleur bleue provient d’interférences sur l’épaisseur de la couche d’oxyde, ce qui indique la présence d’un oxyde très fin (d’épaisseur inférieure à 200nm). Quant à l’oxyde formé sur les échantillons rectifiés, la couleur indiquerait la présence probable d’un oxyde de fer. L’analyse MET réalisée dans la section précédente confirme ces hypothèses.
144
Figure IV-103 : Image au microscope optique des plaquettes de 304L a) polie miroir avant exposition en milieu b) après exposition en milieu REP à 340°C pendant 500h c) rectifiée avant exposition en milieu d)
rectifiée après exposition en milieu REP à 340°C pendant 500h.
L’étude des couches d’oxyde au MET ont permis de préciser les modifications structurales ou chimiques induites par l’état de surface Ces modifications (ou similitudes) sont décrites ci-dessous.
- En termes de structure cristallographique
La nature duplex de la couche d’oxyde est observée pour les deux états de surface : une couche d’oxyde externe constitué de cristaux de magnétite Fe3O4 et de
spinelles de type FeCr2O4 observés sur les échantillons polis et rectifiés. Dans le
cas des échantillons rectifiés, les cristaux de magnétite sont peu nombreux et dispersés en surface. Lorsque ces échantillons rectifiés sont exposés en milieu REP, les cristaux semblent moins géométriques et plus ancrés dans la couche d’oxyde interne. A certains endroits de la surface, la couche d’oxyde est même dépourvue de la couche d’oxyde externe. Cela montrerait que soit l’oxyde interne est très peu adhérent, soit les mécanismes impliquant le développement de l’oxyde externe sont ralentis sur ce type de surfaces écrouies.
L’épaisseur moyenne de la couche d’oxyde externe formée en milieu REP sur une surface polie est deux fois plus importante que celle formée sur une surface usinée. Le comportement de la couche d’oxyde externe est modifié en présence d’une surface rectifiée.
une couche d’oxyde interne compacte, riche en chrome et constituée de nanocristallites de type (Fe,Ni)Cr2O4 pour les échantillons rectifiés (identifiés par
EELS) et polis (pas identifiés mais suggérés par l’analyse chimique). L’épaisseur de la couche d’oxyde est inhomogène quelque soit l’état de surface de la plaquette. De fait, l’épaisseur moyenne de la couche lorsque l’échantillon est immergé en milieu REP, est de l’ordre de 100nm pour l’échantillon poli et 50 nm pour l’échantillon rectifié soit deux fois plus développé en l’absence d’écrouissage de surface.
Ainsi, les couches d’oxyde formées sur les échantillons polis sont très similaires en terme de structure cristallographique aux couches formées sur les échantillons rectifiés. Les cinétiques de croissance des couches d’oxyde sont plus rapides pour les plaquettes polies
d) c)
145
miroir car les épaisseurs obtenues sont doublées en milieu REP et 10 fois plus importantes en milieu vapeur.
- Structures en sous couche
La caractérisation de la zone sous la couche d’oxyde est importante dans la mesure où cette zone fournit des indications intéressantes concernant les circuits de diffusion empruntés par les espèces entrant en jeu lors des réactions électrochimiques conduisant à la formation du film de passivation. De plus, cette zone donne des informations sur les éventuelles pénétrations d’oxyde et leur localisation en sous couche.
La caractérisation menée sur les coupes transverses des échantillons polis et rectifiés a montré la présence en sous couche d’une zone perturbée, recristallisée constituée de grains, de forme allongée (sauf pour l’échantillon poli et oxydé en milieu vapeur). Les diagrammes de diffraction constitués d’une série de cercles concentriques confirment la présence de cette zone non structurée, constituée de nano grains austénitiques (Figure IV-97, Figure IV-99, Figure IV-100). Pour rappel, la taille moyenne des grains initiaux de la nuance 304L identifiée au chapitre III est de 27µm.
Cette zone recristallisée a été mise en évidence sur les échantillons rectifiés oxydés en milieu vapeur et REP sur une profondeur de 1,5µm dans le substrat. Concernant les plaquettes polies, la zone recristallisée est observée seulement sur les échantillons oxydés en milieu REP, mais est trois fois moins profonde que pour les échantillons rectifiés.
Cette couche de recristallisation serait donc favorisée par l’état de surface écroui induit par la rectification. Pour valider cet effet intrinsèque de l’état de surface, la surface de l’échantillon rectifié a été caractérisée, et nous montrons la présence d’une couche de nanograins d’1 μm d’épaisseur et l’absence d’oxygène dans cette couche de surface. La Figure IV-104 montre une micrographie représentative de la zone en sous surface d’une plaquette rectifiée. Cette zone est effectivement peu structurée, constituée d’amas de dislocations désordonnées et de nanograins comme indiqué sur la Figure IV-104. Le diagramme de diffraction associé montre des anneaux plus ou moins bien résolus, caractéristiques de cette zone fortement perturbée, à petits grains. Les distances inter-réticulaires mesurées 2,05Å, 1,78Å, 1,43Å, 1,23Å, 1,07Å correspondent respectivement aux plans (111), (020), (-211), (022), (311) du fer cubique face centré austénitique.
Figure IV-104 : Image en champ clair de la surface d’une plaquette rectifiée non oxydée et le cliché de diffraction associé à la zone fortement perturbé en sous surface.
146
Figure IV-105 : Image en champ clair de la surface d’une plaquette rectifiée non oxydée. Présence de nanograins bien définis.
Nous pouvons conclure que cette zone recristallisée provient de la préparation de surface et n’est pas une conséquence de l’environnement d’exposition.
De ce fait, la recristallisation en surface est la résultante des contraintes induites par la préparation de surface (lors de l’usinage ou même du polissage mécanique mis en place). Ainsi, avant exposition au milieu, la quantité des joints de grain disponibles comme court- circuit de diffusion n’est pas identique d’un échantillon à l’autre et cela conduit donc à penser qu’il existe une prédisposition, en fonction de l’état de surface, à développer une couche d’oxyde plus ou moins épaisse.
En accord avec nos observations, quelques études ont mis en avant la recristallisation du métal sous la couche d’oxyde en relation avec l’état de surface. Dans le cas de deux séries d’échantillons en 316L prélevées dans des réacteurs en service en milieux REB (Réacteur à Eau Bouillante) et REP (Réacteur à Eau Pressurisée), Bruemmer et al (Bruemmer 2008) indiquent la présence d’oxydation au niveau des joints de grain fortement déformés lors de la préparation de surface, localisés en sous couche au niveau de la structure recristallisée. Cette oxydation interne et intergranulaire est associée à l’endommagement par IGSCC (corrosion sous contrainte intergranulaire) de ces composants, à savoir l’enveloppe de cœur et la tuyauterie en milieu REB ou des doigts de gant d’instrumentation du pressuriseur en milieu REP. Les caractérisations au MET réalisées dans le cadre de cette étude ont montré que la zone recristallisée observée en sous couche est constituée de grains fins et allongés, avec une forte densité de dislocation au voisinage de la surface. Selon les auteurs, les gradients de déformation locaux en sous couche induits par la préparation de surface, identifiés par analyse EBSD, conduisent aux conditions de recristallisation adéquates. Cette microstructure recristallisée est donc corrélée à un phénomène d’oxydation intergranulaire à travers la nanostructure. Carette et al (Carrette 2002) ont également observé cette zone recristallisée sur un alliage 600 oxydé en milieu REP.
Nous avons aussi observé au niveau du substrat pour des échantillons oxydés en milieu REP un enrichissement du volume en nickel sur 100nm pour l’échantillon poli et 30nm pour l’échantillon rectifié. Cet enrichissement en Ni est accompagné d’un appauvrissement en Cr jusqu’à 10% (moins que la teneur du métal de base) dans le
147
substrat, immédiatement sous la couche d’oxyde. Cet appauvrissement en chrome de la matrice en sous couche serait elle le résultat des processus de formation de pénétrations d’oxyde aux joints de grain ? La sensibilité de l’analyse EDS au MET ne permet pas de détecter l’atome d’oxygène. Le chapitre suivant est dédié à l’étude de ces pénétrations d’oxyde intergranulaires par la technique SIMS.
IV.3.2.
Pénétrations intergranulaires d’oxydes
Afin de déterminer la présence d’éventuelles pénétrations d’oxydes en sous couches, nous caractérisons les profils de concentration de différents éléments chimiques, entrant en jeu dans les réactions électrochimiques de corrosion. Pour cela, des analyses par la méthode SIMS inverse ont été réalisées sur deux séries de plaquettes en 304L ayant été exposées en milieu primaire simulé REP. Les plaquettes de la première série ont été polies miroir, les plaquettes de la 2ème série sont finies par rectification. Les profils des
éléments étudiés sont les suivants :
- 16O élément essentiel lorsqu’on caractérise les effets de l’oxydation.
- Le suivi du signal 12C permet le traçage des divers carbures que nous pouvons rencontrer dans la matrice. L’échantillon oxydé étant collé contre le porte échantillon du côté oxyde avec une colle GATAN, le signal du carbone délimite donc la couche d’oxyde. Il sera choisi comme étant le signal de référence.
- Les profils des oxydes de type 56Fe16O, 52Cr16O, sont définis car nous nous intéressons aux éléments majeurs composant le substrat soit le Fe et le Cr, qui s’oxydent en sous couche, et éventuellement à leur localisation.
- Le profil de l’oxyde d’aluminium est considéré, car dans ces conditions thermodynamiques (dans l’eau à haute température), l’aluminium est très réactif avec l’oxygène et est préférentiellement oxydé.
Les Figure IV-106 et Figure IV-107 représentent l’évolution des intensités des signaux des différents éléments cités ci-dessus en fonction de la profondeur d’analyse, en partant du métal de base jusqu’à l’oxyde pour une plaquette polie et une plaquette rectifiée.
148
Figure IV-106 : Profils de concentration d’éléments chimiques du métal de base vers la couche définies sur une plaquette polie exposée en milieu simulé REP.
1,00E+01 1,00E+02 1,00E+03 1,00E+04 1,00E+05 1,00E+06 1,00E+07 1,00E+08 2 4 6 8 10 12 14 16 In te n si té d u s ig n al (c /s ) Profondeur d'abrasion (µm) 12C 16O 27Al16O 52Cr16O 56Fe16O
Figure IV-107 : Profils de concentration d’éléments chimiques du métal de base vers la couche définies sur une plaquette rectifiée exposée en milieu simulé REP
L’allure générale des profils de concentration obtenus sur tous les échantillons polis et rectifié suit une évolution en deux temps :
- Durant l’abrasion du métal de base, les intensités des signaux sont stabilisées autour de valeurs moyennes représentatives de la concentration moyenne de
1,0E+01 1,0E+02 1,0E+03 1,0E+04 1,0E+05 1,0E+06 1,0E+07 1,0E+08 1,0E+09 12 14 16 18 20 22 In te n si té d u s ig n al (c /s ) Profondeur d'abrasion (µm) 12C 16O 27Al16O 52Cr16O 56Fe16O 921nm
Zone affectée par l’oxydation
Zone recristallisée en sous couche (500nm) Sens de l’abrasion Oxyde d’aluminium Surface de l’oxyde externe 300nm Métal de base
Zone affectée par l’oxydation
Métal de base
Oxyde d’aluminium
Présences d’oxydes ou d’oxygène dissous sous la
couche d’oxyde
Zone recristallisée en sous couche (1,5µm)
Présences d’oxydes ou d’oxygène dissous sous la
149
l’élément dans l’alliage. Rappelons que les signaux obtenus sont calculés en moyennant l’intensité sur une aire de 140µm². Lors de la traversée du faisceau source dans le métal de base, le signal recueilli (en intensité et forme) dépend du positionnement spatial des défauts, de pollutions ou d’éventuels précipités secondaire présents dans le volume étudié, de la présence ou pas d’îlots d’oxyde présents dans la nuance. Ainsi, entre l’échantillon poli et rectifié, les intensités des signaux diffèrent car la répartition des objets dans le volume étudié n’est pas identique. Cependant, les valeurs moyennes des intensités des signaux pour le même élément restent du même ordre de grandeur.
- Lorsque le faisceau d’ions primaires atteint l’interface métal / oxyde, les intensités des signaux augmentent brusquement au fur et à mesure que la couche d’oxyde est traversée. De plus, la modification des rendements d’abrasion obtenus dans la couche d’oxyde conduisent à une modification du signal du carbone, signe que le faisceau traverse la couche d’oxyde (Voir Figure IV-107). La couche d’oxyde étant directement liée à la colle, le décollement brutal du signal du carbone correspond donc à l’arrivée du faisceau dans la couche d’oxyde.
- Etant donné que le porte cible sur lequel sont disposés les échantillons à analyser est en silicium, l’analyse est stoppée lorsque le signal du silicium augmente de manière significative.
Le faisceau traverse le métal de base et débouche sur la couche d’oxyde. Les signaux obtenus par éléments chimiques permettent d’obtenir des informations sur la nature et la succession des divers types d’oxydes internes présents dans le métal de base, ainsi que sur l’épaisseur de la couche d’oxyde.
Dans le cas de l’échantillon poli (Figure IV-106), le signal de l’oxyde est relativement
constant et stabilisé dans le métal de base, excepté au niveau de la singularité du profil détectée à 17µm de la surface bombardée. Le signal de l’oxyde d’aluminium est calqué sur celui de l’oxygène et présente la même singularité. Ces deux profils indiquent donc qu’il s’agirait d’un oxyde d’aluminium isolé et non connecté à la couche d’oxyde. Le signal d’oxygène décolle donc dès 18,6µm et la surface de l’oxyde est estimée localisée à 18,9µm. Le retard de 300nm du signal de l’oxygène sur celui du carbone est interprété comme étant la présence d’oxygène dissous et / ou la présence de pénétration d’oxydes intergranulaires connectés à la couche. Cependant pour avoir la confirmation qu’il s’agit bien de pénétration d’oxydes et de découpler ce phénomène des deux autres cités précédemment, il est nécessaire d’observer les cartographies de ces éléments au même niveau que les profils par l’imagerie en mode RAE (Resistive Anode Encoder). Cette zone de 300nm serait donc en amont de la couche d’oxyde de surface et coïnciderait avec la zone constituée de nanograins recristallisée en sous couches.
Dans le but de confirmer la présence de pénétrations d’oxyde intergranulaire, les cartographies en mode imagerie direct de différents éléments (16O, 27Al16O, 52Cr16O, 56Fe16O) ont été réalisées à deux différentes profondeurs : à 14µm, une zone située dans
le métal de base, à 17µm une zone proche de la singularité correspondant à l’oxyde d’aluminium et à 19µm très près de la zone où l’intensité du signal de l’oxygène est perturbée.
Oxydation statique 304L
150
14µm 17µm 19µm
Figure IV-108 : Cartographies en imagerie direct des éléments chimiques oxygène (16C) et des
oxydes d’aluminium, chrome et de fer (27Al16O, 52Cr16O, 56Fe16O) à une profondeur de 14 µm
(images à gauche), 17µm (au centre) et une profondeur de 19 µm (image à droite).
16
O
52Cr
16O
52Cr
16O
56Fe
16O
56Fe
16O
40
μm
40 μm
16O
40 μm
40
μm
40
μm
40
μm
40
μm
40
μm
151
Sur la Figure IV-108, les cartographies élémentaires RAE des éléments observés à une profondeur de 14µm ne montrent aucun signal prépondérant, conformément aux profils de diffusion présentés en Figure IV-106. Lorsque l’on progresse en profondeur dans le métal de base à 17µm, les profils de diffusion de l’oxygène et de l’oxyde d’aluminium présentent une singularité. Les cartographies RAE élémentaires à 17µm de l’élément 16O
et de l’oxyde d’aluminium montrent que le signal est plus intensifié qu’à 14 ou 19µm sur certaines zones et confirment la présence de cet oxyde. Notons que les intensités des signaux des oxydes de chrome et de fer sur les cartographies à 17µm sont peu intenses. Enfin à 19µm dans la zone d’oxydation perturbée, les cartographies élémentaires de l’élément 16O et des oxydes 52Cr16O, 56Fe16O montrent la présence d’oxydes enrichis en fer
et chrome en sous couche dans le substrat.
Concernant l’échantillon rectifié (Figure IV-107), les singularités au niveau des profils de l’oxyde d’aluminium et de l’oxygène indiquent également la présence d’oxydes isolés dans le métal de base. Cependant, aux environs de l’interface métal / oxyde, le signal de l’oxygène est légèrement perturbé et déconnecté du signal du carbone, cela permet de définir une zone de 921 nm indiquant la présence d’oxygène dissous et / ou la présence de pénétration d’oxydes intergranulaires connectés à la couche. De plus, nous observons que la zone recristallisée, plus en profondeur dans le métal de base que pour l’échantillon poli miroir, est à cheval sur la zone de 921 nm. La présence de recristallisation hors de la zone oxydée dans le métal de base peut expliquer la perturbation du signal d’oxygène en avant de la zone affectée par l’oxydation.
Il ressort que plus la zone recristallisée est profonde et plus l’oxygène dissous et / ou les pénétrations d’oxydes intergranulaire se sont localisés sur une zone plus étendue (3 fois plus importante sur l’échantillon rectifié que poli). La zone recristallisée semble donc favoriser le développement des pénétrations d’oxydes en sous couche.
Le rôle de la zone recristallisée pour le développement des pénétrations d’oxydes que nous mettons en évidence à partir des interprétations des analyses SIMS sont cohérentes avec celles reportées par Bruemmer et al (Bruemmer 2008). Cette situation est schématisée sur la
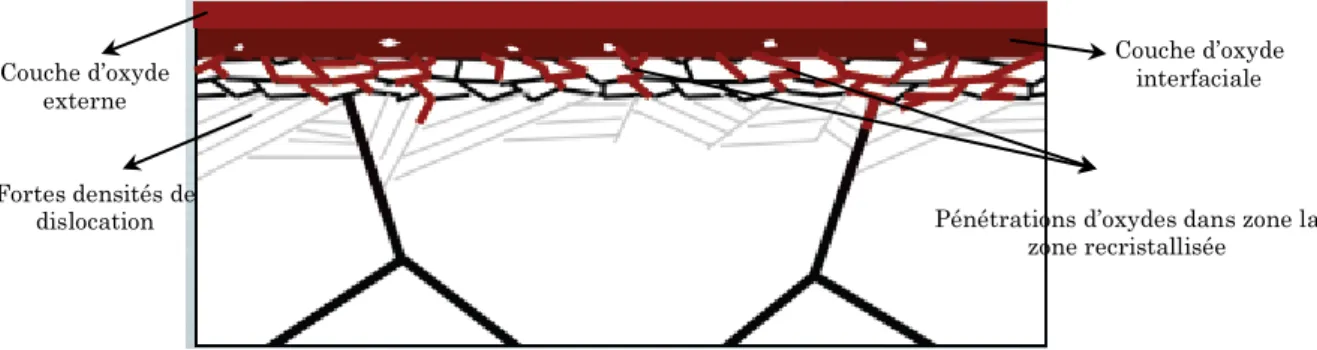
Figure IV-109. L’auteur indique, sur cette figure, que l’oxydation intergranulaire lors de la durée de service de la pièce, se produit à travers une partie de la zone constituée de nanograins recristallisés. Notons aussi la présence d’une zone à forte densité de dislocations en sous couche.
Figure IV-109 : Schéma représentatif des microstructures en subsurface pour la nuance 316 L écrouie, oxydé en milieu LWR. L’accent est mis sur la zone recristallisée sous la couche d’oxyde interne, présentant
des pénétrations d’oxyde, et sur les amas de dislocation. (Bruemmer 2008)
Couche d’oxyde externe
Couche d’oxyde interfaciale
Pénétrations d’oxydes dans zone la zone recristallisée Fortes densités de
152
IV.3.3.
Bilan de l’influence de l’état de surface
Cette partie a mis en évidence le rôle important occupé par la préparation de surface dans le développement de la couche d’oxyde en milieu REP comme en milieu vapeur d’eau à haute température.
En comparant des analyses effectuées sur l’acier 304L poli et rectifié en milieu vapeur et REP simulé, les points suivants ressortent :
- Les modifications induites par une préparation de surface induisant un fort taux d’écrouissage (voir les amas de dislocation près de la surface sur la Figure IV-104) sont très significatives. L’épaisseur de la couche d’oxyde formée sur un échantillon poli est 2 fois plus importante que celle développée sur un échantillon rectifié en milieu REP. Cette observation est en accord avec les travaux de Tapping et al (Tapping, Davidson et al. 1986) sur des aciers inoxydables exposés en milieu aqueux à haute température. La tendance est similaire pour la couche protectrice enrichie en chrome : elle atteint 100nm d’épaisseur pour les échantillons polis alors qu’elle n’est que de 10nm pour les échantillons rectifiés. Ces observations donnent une première indication selon laquelle la cinétique de diffusion des espèces impliquées dans les réactions électrochimiques (Cr3+)
est plus rapide lorsque l’échantillon est poli.
- Dans les deux cas, la couche d’oxyde de configuration duplex est constituée de magnétite Fe3O4 et de spinelles de type (Fe,Ni)Cr2O4, dispersées à la surface de la couche
d’oxyde interne enrichie en chrome. Cette couche interne serait constituée de nano spinelles de type (Fe,Ni)Cr2O4. La modification induite par la préparation de surface
n’est donc liée qu’à la cinétique de croissance de la couche d’oxyde (ralentie par l’écrouissage de surface).
- L’écrouissage de surface résultant de la préparation de surface conduit à la modification de la microstructure de la zone en sous surface de la couche d’oxyde. Il s’agit de la recristallisation dynamique en grains fins allongés de 100 nm d’épaisseur dont la profondeur est directement liée à la préparation de surface. En effet, pour les échantillons polis, cette zone est inexistante (échantillon exposé en milieu vapeur) ou fine (500nm pour l’échantillon exposé en milieu simulé REP) tandis que lorsque la surface est rectifiée, la zone recristallisée est plus épaisse (1,5µm pour les échantillons exposés en milieu REP simulé ou vapeur et 1µm pour l’échantillon exposé sous air). D’après les analyses SIMS, cette zone est sujette à la présence d’oxygène dissous / pénétrations intergranulaires connectées à la couche d’oxyde sur 300nm pour l’échantillon poli et 921nm pour l’échantillon rectifié. Les mêmes observations ont été réalisées par Bruemmer (Bruemmer 2008) qui indique que la préparation de surface (une rectification comme un polissage mécanique grossier) produit d’importantes modifications en sous couche, incluant la génération de fortes densités de dislocations, des transformations de phases en particulier l’émission de la phase martensitique (pas observée dans le cadre de notre étude) et la recristallisation des grains en surface (voir Figure IV-109)
153 Ces conclusions suggèrent que :
La couche de recristallisation contribue donc au ralentissement de la cinétique de corrosion, et indirectement à la diffusion des ions impliquées dans les réactions électrochimiques tels les ions Cr3+, Fe3+, Fe2+ du métal vers l’interface. Ainsi, une
couche barrière freine la progression des ions vers le milieu. Cette couche ralentissant les ions métalliques a été identifiée comme étant la couche d’oxyde interne qui est généralement compacte et dont la croissance gouverne la croissance de la couche d’oxyde totale. Plus les grains sous la couche d’oxyde sont petits, plus les sites de germination de l’oxyde interne sont nombreux et plus les joints de grains sont nombreux, plus la couche d’oxyde interne est compacte et protectrice. La couche d’oxyde totale est d’autant plus fine. Ces joints en sous couche constituent donc des courts circuits de diffusion pour la formation de la couche d’oxyde et l’hypothèse posée est que les joints de grains constituent des courts circuits crédibles pour la diffusion des espèces de corrosion. Cette conclusion est en accord avec le modèle d’oxydation de Robertson [4] basé sur la diffusion des espèces à travers les joints de grains de la couche d’oxyde interne (anciennement joints de grain du métal).
En confirmant la présence de pénétrations d’oxyde dans la zone recristallisée à nanograins, l’hypothèse posée est la suivante : le réservoir de cations disponibles dans le métal de base contribuerait non seulement à la formation des oxydes présents au niveau des joints de grains, mais également à la formation de la couche d’oxyde. La formation des oxydes intergranulaires est basée sur la diffusion des atomes d’oxygène issus de la dissociation de la molécule H2O (le
milieu) à haute température aux joints de grain. Elle a été étudiée par divers auteurs qui ont posé un certain nombre d’hypothèses permettant d’expliciter ces phénomènes en faisant fi des approches classiques de diffusion non applicables dans ces conditions, c'est-à-dire la diffusion des espèces de corrosion en milieu confiné, le long des joints de grain. Cependant, ces études indiquent que ce mécanisme est corrélé à la déchromisation du métal de base. En effet, la quantité d’ions chrome disponibles pour la formation de la couche d’oxyde interne en présence de la zone de recristallisation est mois importante que lorsque cette couche recristallisée est absente ou moins(ou lorsqu’elle est moins étendue). En général, les études de caractérisation en laboratoire sont réalisées sur des échantillons polis afin de découpler les effets de l’écrouissage de surface des mécanismes effectifs se produisant durant la corrosion des aciers inoxydables. Cependant, il faut garder à l’esprit qu’en conditions réelles de fonctionnement des réacteurs, les constituants présents dans les internes de cuve ne sont pas polis et que les couches d’oxydes formées dans ces conditions sont plus fines que celle développées lors des essais en laboratoire. Cela expliquerait, en partie, que les temps de CSC soient beaucoup plus courts en laboratoire que pour les composants industriels. En partie, car les essais en laboratoire peuvent également être accélérés par les conditions expérimentales mises en œuvre.
154
IV.4. Comparaison des produits de corrosion
milieu vapeur/milieu REP
Cette partie mène une étude comparative des couches d’oxydes passives développées en milieu vapeur et REP simulé dans des conditions de tests sensiblement équivalentes. L’objectif étant d’apporter des éléments de compréhension sur les mécanismes de formation de la couche d’oxyde, tout en vérifiant l’effet accélérant du milieu vapeur sur la cinétique d’oxydation de la nuance d’acier inoxydable 304L.
La structure bi-couche observée sur l’échantillon oxydé en phase vapeur est identique à celle identifiée sur les échantillons caractérisés en milieu REP. Dans les deux cas, l’oxyde externe est constitué de cristallites de magnétite et de spinelles de fer, enrichis en chrome par rapport à la magnétite tandis que l’oxyde interne, compacte et peu poreux est constitué de nano cristallites de spinelles de chrome. Le milieu vapeur testé reproduit la même couche d’oxyde formée en milieu REP au niveau de la configuration des couches (couche interne compacte et cristallites riche en fer déposées sur cette couche) et de leur composition.
La cinétique d’oxydation en milieu REP est cependant moins rapide que celle de l’acier en milieu vapeur, étant donné que la couche de passivation formée pendant une exposition de 500h en milieu vapeur à 400°C est en moyenne dix fois plus épaisse que celle formée suite à une exposition de 500h en milieu simulé REP à 340°C. La densité des cristallites de magnétite constituant la couche d’oxyde externe est également plus importante sur les échantillons exposés en milieu vapeur.
Afin de découpler l’effet de la température sur la croissance de la couche d’oxyde de celle de l’environnement, des échantillons rectifiés ont été recuits sous air à 400°C pendant 500h. Les caractéristiques de l’oxyde formé sous air sont similaires à celles de celui développé en milieu aqueux (voir Figure IV-110), l’épaisseur de la couche d’oxyde étant en moyenne de 30nm, soit une couche d’oxyde aussi fine que celle observée sous eau à 340°C. Sous la couche d’oxyde, le substrat présente une couche de nanograins d’épaisseur 1 μm et contient de l’oxygène en volume jusqu’à 500nm d’épaisseur.
Cette expérience indique que dans cette gamme de température [340°C – 400°C], l’effet de la température semble négligeable dans la comparaison eau / vapeur en terme d’épaisseur de la couche d’oxyde formée.
Figure IV-110 : Image en champ clair de la section transverse d’une plaquette rectifiée et oxydée sous air à 400°C pendant 500h.