MINISTERE DE L’ENSEIGNEMENT SUPERIEUR ET DE LA RECHERCHE SCIENTIFIQUE UNIVERSITE AKLI MOHAND OULHADJ – BOUIRA
FACULTE DES SCIENCES DE LA NATURE ET DE LA VIE ET DES SCIENCES DE LA TERRE DEPARTEMENT DE BIOLOGIE
Réf : ……./UAMOB/F.SNV.ST/DEP.BIO/2018
MEMOIRE DE FIN D’ETUDES
EN VUE DE L’OBTENTION DU DIPLOME MASTER
Domaine : SNV Filière : Sciences Biologiques
Spécialité : Biotechnologie Microbienne
Présenté par :
AOUADI Hadjira & KADDOUR Houria
Thème
Cinétique de destruction des micro-organismes par
microonde et ultrason, cas d’étude : Boues résiduaires
de station d’épuration de la ville de Bouira
Soutenu le : 02/ 07 / 2018
Devant le jury composé de :
Nom et Prénom Grade
M. REMINI Hocine MCB Univ. de Bouira Président
M. DAHMOUNE Farid MCA Univ. de Bouira Promoteur
Mlle.ADEL Khadidja doctarante Univ. deBouira Co-Promotrice
M. RAI Abdelwahab MAB Univ. de Bouira Examinateur
Remerciements
Louanges à Allah le miséricordieux le très miséricordieux qui nous a aidé tout au long de notre vie, nous remercions pour sa bienveillance, la patience et le courage qu’il nous a accordé
Nous remercions nos parents pour leur patience, générosité ; qui nous ont toujours souhaité beaucoup de motivation, d’encouragements et surtout pleins de bonheurs.
Nous remerciements s’adressent aux honorables membres du jury, M. Hocine REMINI et M. Abedelwahab RAI, de nous avoir fait le grand honneur d’accepté d’évaluer notre travail.
Nous tenons à remercier sincèrement M. Farid DAHMOUNE qui fut pour nous un encadreur attentif et disponible malgré ses nombreuses charges. Sans son accompagnement ce mémoire n’aurait jamais vu le jour. Sa compétence, sa rigueur scientifique et sa clairvoyance nous ont beaucoup aidées dans notre parcours. Il a été et restera un modèle exemplaire dans notre formation.
Nous remercions notre co-promotrice Mm. Khadidja ADEL pour son aide et sa gentillesse. Nous souhaitons aussi adresser nos remerciements les plus sincères aux M. Amine
BELBAHI et M. Amine NOUAL, pour leurs aides.
Nous adressons nos remerciements à tous les enseignants qui ont contribué à notre formation. Nous recommandons nos plus cordiaux remerciements à tous nos proches et amis, qui nous ont toujours soutenu et encouragé au cours de la réalisation de ce mémoire.
Un merci symboliquement à Alexandra Elbakyan, qui a fondé le moteur de recherche scientifique Sci-Hub, permettant la libre diffusion des connaissances scientifiques.
Enfin, nos remerciements s’adressent à toutes les personnes qui ont contribué de près ou de loin à la réalisation de ce travail ou qui nous encouragé et soutenu à tout moment
Liste des figures
Figure 1 : Représentation des champs constitués d’une onde électromagnétique………...5
Figure 2 : Les mécanismes de chauffage par micro-ondes………...6
Figure 3 : Micro-onde et interaction avec la matière………....6
Figure 4 : Domaines de fréquence des sons……….……….……8
Figure 5 : Principe de la cavitation……….………....…10
Figure 6 : Simulation décrivant l’inactivation microbienne en utilisant le modèle du Mafart et al. (2002) pour le paramètre de forme………..12
Figure 7 : Lit de séchage des boues d’épuration dans la STEP de Bouira……….….17
Figure 08 : Les dilutions décimales préparées à partir de la solution mère……….18
Figure 09 : Échantillons du 1er essai……….……...20
Figure10 : Échantillons du 2eme essai………..20
Figure 11 : Échantillons du 1er essai………....21
Figure 12 : Échantillon de 2eme essai………...22
Figure 13 : Nombre de la FAMT et la flore fongique obtenues à la dilution 10-4……….…..24
Figure 14 : Cinétiques d’inactivation des populations de la flore fongique et de FMAT par microonde. Comparaison des valeurs expérimentales et celles simulées en utilisant le modèle de Weibull (―)………...32
Figure n°15 : Cinétiques d’inactivation des populations de la flore fongique et de FMAT par microonde. Comparaison des valeurs expérimentales et celles simulées en utilisant le modèle de Weibull (―)………..………..….33
Figure n°16 : Cinétiques d’inactivation des populations de la flore fongique et de FMAT assisté par Ultrason. Comparaison des valeurs expérimentales et celles simulées en utilisant le modèle de Weibull (―)………34
Figure n° 17 : Comparaison du traitement assisté par micro-onde et du traitement à l’ultrason………...………35
Liste des tableaux
Tableau I : Liste de microorganismes pathogènes présents dans la boue………...14 Tableau II : Liste des produits utilisés...……...15 Tableau III : Liste des appareils utilisés………..….16 Tableau IV : Réduction de la charge de FAMT et la flore fongique après traitement assisté
par micro-onde (essai 1)………25
Tableau V : Réduction de la charge de FAMT et la flore fongique après traitement assisté
par micro-ondes (essai 2)………..…26
Tableau VI : Réduction de la FAMT et la flore fongique de l’essai 01 après exposition au
bain à ultrasons………...………..…29 Tableau VII : Réduction de la flore fongique et la FMAT de dilution 10 -4 après traitement par ultrason………...30
Tableau VIII : Valeurs des paramètres cinétiques de l'inactivation de FMAT et la flore
fongique par micro-onde (essai 1)……….………...31
Tableau IX : Valeurs des paramètres cinétiques d’'inactivation de FMAT et de la flore
fongique par microonde (essai 2) ……….…32
Tableau X : Valeurs des paramètres cinétiques d’inactivation de la et de la flore fongique
par
Liste des abréviations
MO : Micro-onde US : Ultrason
FMAT : Flore mésophile aérobie totale KHz : kilo hertz
MHz : Méga hertz GHz : Giga hertz Ev : Electron volte
MVS : Matière Volatile Sèche MST : Matière Solide Totale Kpa : Kilopascal
SNV-ST : Science de la Nature et de la Vie-Science de la Terre STEP : Station d’Epuration des Eaux Usées
ONA : Office national d’assainissement UFC : Unité Formant Colonie
RMSE : Racine de la moyenne des carrés des écarts (Root Mean Squared Error) Symboles grecs
α Paramètre d’échelle du modelé de Weibull β Paramètre de forme du modèle de Weibull
Table des Matières
Liste des abréviationsListes des figures Listes des tableaux
Introduction ………...………...…1
Chapitre I : Revue Bibliographique 1. Destruction des microorganismes……...………...3
1. 1. Facteurs influençant la destruction microbienne ………...3
2. Destruction microbienne par micro-onde et ultrason………...…...….… 4
2 .1. Destruction microbienne par micro-onde………..………..4
2.1.1. Les micro-ondes et le spectre électromagnétique …...………....4
2.1.2. Principes de chauffage par micro-onde…...……....……….…5
2.1.3. Effet sur les microorganismes…………...………...………...7
2.2. Destruction microbienne par ultrason………...………....7
2.2.1. Définition………...……….……….7
2.2.2. Cavitation………...………..8
2.2.3. Paramètres influençant la cavitation. ………...…………...8
2.2.4. Effet sur les microorganismes………...………...9
3. Microbiologie prévisionnelle………...…………....11
3.1. Modélisation de destruction microbienne…………..… ..………..……….11
3.1.1. Modélisation primaire………..………...……….11
4. Microorganismes et les boues résiduaires ……….…………..…...….. 12
4.1. Microorganismes des boues………...……….….……..13
Chapitre II : Matériel et Méthodes 1. Cadre et objectifs ………...………...………..15
2. Equipement et produits utilisés………...….15
3. Préparation de l’échantillon………...………...16
3.1. Prélèvements et transport de l’échantillon………..…...………..…..16
5.1. Estimation de la charge microbienne initiale (la FAMT et la flore fongique).…..18
6. Traitement de l’échantillon……….……...…………..19
6.1. Traitement assisté par micro-onde…...……….………..……….. 19
6.2. Traitement assisté par ultrason………...………..………..…………21
7. Analyse microbiologique après traitement…………...………...…..…..22
7.1. Dénombrement de la flore mésophile aérobie totale et la flore fongique...…...22
8. Expression et analyse des résultats ……...………..23
Chapitre III : Résultats et discussion 1. Estimation de la charge microbienne initiale avant traitement ………..…...….24
2. Traitement assisté par micro-onde………...………...24
3. Traitement assisté par ultrasons……….……….…29
4. Modélisation de destruction microbienne……….…..….31
4.1. Cinétique de destruction par microonde………....……33
4.2. Cinétique de destruction par ultrason……….………33
5. Comparaison entre traitement assisté par microonde et ultrason………... 34 Conclusion et perspectives
Références Bibliographiques Annexes
Introduction
Les microorganismes ont été la première forme de vie sur terre ils regroupent les bactéries, les levures, les champignons, les algues et les protozoaires. Ces êtres vivants sont des ubiquitaires qui colonisent tous les milieux. Ils sont indispensables à l’homme et à l’environnement (1). Cependant, il existe des formes pathogènes qu’il est nécessaire de traiter et d’éliminer.
Par ailleurs, plusieurs techniques ont été développées dans le but de détruire ou d’inhiber les micro-organismes et leurs toxines. Il s’agit des méthodes de traitement thermique (pasteurisation..) et athermique (utilisation des produits chimique, fumigation etc). Cependant, ces traitements altèrent parfois les produits sur lesquels ils sont utilisés et présentent un danger pour l’homme et l’environnement ; par conséquent, il est indispensable de chercher des techniques de traitement alternatives qui détruisent les micro-organismes et qui soient sans conséquences négatives sur l’environnement et la santé humaine (2).
Parmi ces techniques de destruction des microorganismes innovantes, on cite les méthodes ondulaires à savoir les microondes et les ultrasons. Ces dernières sont des méthodes physiques, visant à remplacer les traitements chimiques, offrant ainsi une meilleure image de préservation du naturel.
L’efficacité de ces méthodes dans la destruction des microorganismes, a été démontrée par de nombreuses études publiées (3-5). En effet, ces études montrent que les micro-ondes et les ultrasons peuvent induise une réduction significative jusqu’à l’élimination des bactéries. Une panoplie travaux a été menée sur de multiples microorganismes, décrivant une efficacité similaire de ces méthodes contre divers agents pathogènes.
Ces techniques pourraient bien être utilisées pour l’élimination les microorganismes pathogènes des boues résiduaires issues de l’épuration des eaux usées qui en sont très chargées. Ces boues devenant très vite envahissantes par manque d’espace (environ 1200 tonnes/mois de matière sèche), vu que la seule solution consiste à les laisser sécher au niveau de la station. De ce fait, il est indispensable de trouver une solution pour éliminer ces résidus dans les conditions les plus économiques tout en respectant les contraintes liées à la protection de l’environnement et de l’hygiène publique.
Introduction
Le travail que nous présentons est une étude préliminaire sur la cinétique de destruction des microorganismes. Cette étude vise à mettre en évidence l’efficacité des techniques assistée par microonde et ultrason sur la destruction des micro-organismes des boues résiduaires de la station d’épuration des eaux usées de Bouira. Ces techniques peuvent constituer au futur, une alternative propre pour le traitement des boues et la fabrication à partir de ces dernières d’engrais biologique de haute valeur.
Dans ce contexte, le présent manuscrit est scindé sur trois principaux chapitres :
Le premier étant la partie bibliographique en décrivant quelques généralités nécessaires à la compréhension du sujet ;
Le second chapitre traite du matériel utilisé et le protocole expérimental que nous avons mené ;
Le troisième chapitre annonce les résultats et discussion des résultats obtenus, et termine par une conclusion générale en évoquant les résultats prépondérants de cette présente investigation.
Chapitre I Revue Bibliographique
1. Destruction des microorganismes
La destruction microbienne est un phénomène mettant en jeu des réactions complexe et diverses, selon la nature de l’agent antimicrobien utilisé. Ces réactions dépendent essentiellement du microorganisme, de son état physiologique, du temps et de la dose du traitement utilisée (concentration d’un produit chimique, température, énergie d’une radiation) (7).
1.1. Facteurs influençant la destruction microbienne Nature et état du micro-organisme
Les espèces microbiennes ne sont pas toutes sensibles pareillement à l’action de l’agent antimicrobien ; ce dernier est caractérisé par son spectre d’activité qui est plus ou moins large en fonction de l’activité vis-à-vis des différentes molécules biologiques.
L’état physiologique de la bactérie joue aussi un grand rôle : les micro-organismes sont plus sensibles en phase exponentielle qu’en phase stationnaire (8, 9) .
Nature de l’agent antimicrobien
Les différents agents ont une efficacité et un spectre d’activité variables. Pour les agents physiques, l’activité microbicide augmente souvent avec la dose alors que pour les agents chimiques, les effets seront d’abord bactériostatiques puis bactéricides (8).
Rôle de l’environnement
L’environnement peut influencer considérablement l’efficacité des agents antimicrobiens physiques ou chimiques. Pour les agents chimiques, la solubilité dans l’eau est un facteur déterminant. Parmi les principaux facteurs jouant un rôle, on peut signaler : le pH du milieu, la turbidité, la viscosité, la dureté de l’eau, et les matières organiques (8).
Chapitre I Revue Bibliographique
2. Destruction microbienne par micro-ondes et ultrasons
En matière de procédés de destruction microbienne, il existe plusieurs processus tels que les procédés thermiques, les procédés athermiques (haute pression, champ électrique pulsé, ultrason, etc.).
Dans cette étude on s’est intéressé à la destruction microbienne par micro-onde et ultrason, qui seront présentés avec plus de détail dans la partie qui suit.
2.1. Destruction microbienne par micro-onde
2.1.1. Les micro-ondes et le spectre électromagnétique
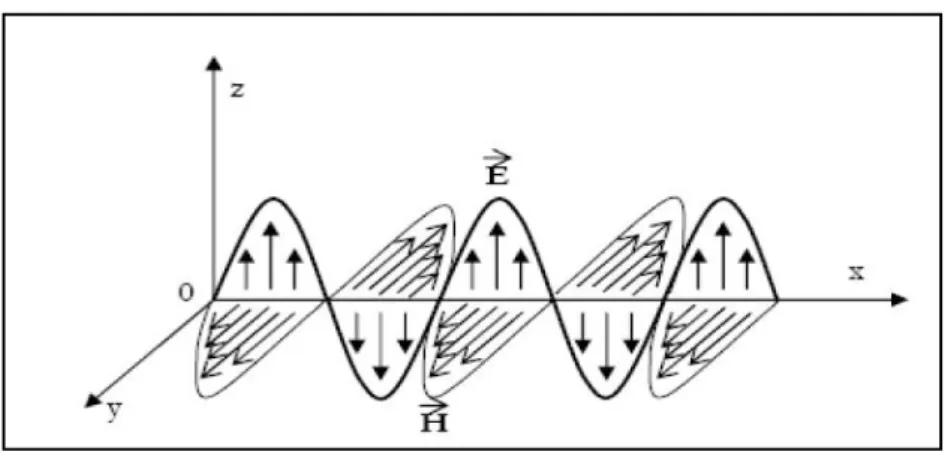
Les micro-ondes sont des ondes radio électromagnétiques qui se trouvent dans une bande de fréquence de 300 MHz à 300 GHz (5) avec une longueur d'onde allant d'environ 1m à 1 mm, la fréquence la plus utilisée est de 2450 MHz (10), L'énergie des micro-ondes est une forme de radiation non ionisante qui est générée par plusieurs types de dispositifs, le plus souvent est le magnétron (10, 11), l'énergie des micro-ondes est de 1,2 x 10-5 eV, alors que l'énergie nécessaire pour rompre les liaisons d’hydrogènes est de 5,2 Ev (12). Les micro-ondes comprennent deux constituants (Figure n°1) : un champ magnétique et un champ électrique orienté perpendiculairement les uns aux autres et qui propageant dans un milieu matériel ou dans le vide (13).
Chapitre I Revue Bibliographique
Figure n°1: Représentation des champs constitués d’une onde électromagnétique (13). E : Champ électrique variable de l’onde électromagnétique suivant l’axe OZ,
H : Champ magnétique variable de l’onde électromagnétique suivant l’axe OY. L’axe OX
représente la direction de propagation de l’onde dans le vide.
2.1.2. Principes de chauffage par micro-ondes
Les mécanismes de chauffage par micro-onde sont classés en deux types : la rotation des molécules dipolaires et la polarisation ionique (14). .
Le premier mécanisme inclus la rotation dipolaire, dans un champ électrique alternatif, les molécules dipolaires sont incapables de suivre les oscillations rapides du champ. La chaleur est générée rapidement en raison de la friction moléculaire interne(5, 15). Certains matériaux diélectriques tels que l'eau contiennent des dipôles permanents qui tentent à réorienter sous l'influence d'un champ alternatif, causant ainsi une orientation de polarisation (16).
Le deuxième mécanisme inclus la polarisation des ions à la suite du mouvement d'avant en arrière des molécules ioniques qui tentent de s'aligner avec le champ électrique oscillant
Chapitre I Revue Bibliographique
Figure n°2 : Les mécanismes de chauffage par micro-ondes (17)
Lorsqu’une matière est irradiée par une onde électromagnétique, différents types d'interactions sont possibles (Figure n°3).
L’onde est réfléchie et le matériau est dit opaque ;
L’onde travers le matériau sans perdre d’énergie et le matériau dit transparent ;
L’onde est absorbée, C’est l’absorption de l’énergie des microondes qui est à l’origine du chauffage diélectrique (18, 19).
Figure n°3 : Micro-onde et interaction avec la matière (18).
La capacité d'un matériau à absorber l’énergie de micro-onde est régie par son facteur de dissipation, qui est le rapport entre le facteur de perte diélectrique et la constante diélectrique du matériau.
micro-Chapitre I Revue Bibliographique
Par conséquent, un matériau avec un facteur de dissipation élevé est facilement chauffé par micro-ondes (14).
2.1.3. Effet sur les microorganismes
Beaucoup de recherches sont réalisées sur l’effet des micro-ondes sur les microorganismes. Deux mécanismes sont proposés pour l'inactivation des micro-organismes par micro-ondes
(20) :
Le premier mécanisme indique que les micro-ondes inactivent les microorganismes entièrement par la chaleur par des mécanismes comparables à d'autres processus provoqués par la chaleur, tels que la dénaturation des enzymes, des protéines, des acides nucléiques, ou d'autres composants vitaux, ainsi que des perturbations des membranes cellulaire (12).
Le second mécanisme implique des effets non thermiques. L’éventualité d’effets non thermiques des micro-ondes demeure un sujet controversé (21).
Les chercheures observent que les microorganismes irradiés par micro-onde sont détruits à des températures inférieures à leur « Thermal Death Point » et montrent des dommages plus importants que les cellules traitées par chauffage conventionnel à des températures similaires (22).
Les auteurs ont suggéré que l’effet athermique des micro-ondes est lié au changement des structures protéiques en modifiant la direction des réactions biochimiques (23).
2.2. Destruction par ultrason 2.2.1. Définition
L’ultrason est une onde vibrationnelles acoustique de pression dont la fréquence se situe entre 16 KHz et 10 MHz. C’est-à-dire entre les domaines des sons audibles (16 Hz-16 kHz) et des hyper-sons (> 10 MHz) (Figure n°4) (3).
Cette onde est caractérisée par :
Sa fréquence (hertz ou cycle par seconde), c'est-à-dire le nombre de cycle passant en un point fixe par unité de temps.
Son amplitude, qui correspond à la différence maximale entre la dépression et la compression, son unité est le mètre (m) (24).
Chapitre I Revue Bibliographique
Figure n°4 : Domaines de fréquence des sons (25).
L’ultrason utilisé pour la destruction microbienne, est situé dans une gamme de fréquence allant de 20 à 100 KHz, et ayant des intensités acoustiques supérieures à 10 W/m2(24).
2.2.2. Cavitation
Il est généralement reconnu que les effets majeurs des ultrasons sont dus au phénomène de cavitation (26). La cavitation est définie de manière générale comme étant l’ensemble des phénomènes liés à la formation, la croissance et l’effondrement (collapse) de microbulles ou cavités se produisant à des intervalles de temps très courts (10-3 s) et libérant une quantité importante d’énergie (27) .
2.2.3. Paramètres influençant la cavitation
Les principaux facteurs qui influencent la cavitation sont :
Puissance
Il s’agit là du paramètre qui a l’effet le plus marqué, une puissance minimale est requise pour observer le phénomène de cavitation, connue sous le nom de seuil de Blake (seuil de cavitation), déterminé à partir de la pression hydrostatique du milieu en fonction du rayon du noyau de cavitation. Elle dépend également de l’impédance acoustique du milieu, qui augmente lorsque le milieu entre en cavitation (28).
Fréquence
Un autre effet important à prendre en considération est la fréquence appliquée. Lorsque la fréquence appliquée augmente, la production et l’intensité de la cavitation dans un liquide diminuent. À haute fréquence (>1 MHZ), les cycles sont très rapides et le temps en pression négative (zone de raréfaction) est trop court pour engendrer la croissance de la bulle de cavitation (29).
Chapitre I Revue Bibliographique
Température
La température du solvant peut jouer un double rôle lorsque celui-ci est soumis aux ultrasons. L’augmentation de la température diminue la solubilité des gaz dans les liquides, etaugmente la tension de vapeur du solvant, donc le seuil de cavitation est abaissé (30).
Nature du solvant
Une faible viscosité et tension superficielle du solvant permettent d’abaisser le seuil de cavitation, parce que les forces de cohésion sont moindres. En revanche, une forte pression de vapeur implique une vaporisation importante dans la bulle lors de la phase de dépression, sa condensation amortie l’implosion, limitant ainsi les énergies mises en jeu
(28).
Gaz
Lorsque la quantité de gaz dissoute augmente, les échanges de gaz à travers la bulle sont favorisés, et la cavitationaugmente. Par contre, l’intensité de l’implosion diminue (24).
2.2.4. L’effet de l’ultrason sur les microorganismes
Le premier effet antimicrobien du traitement par ultrason est attribué à la cavitation acoustique intracellulaire qui provoque un amincissement des membranes cellulaires, un réchauffement localisé et la production des radicaux libres (4, 31) .
Pendant le processus de sonication, des ondes longitudinales sont créées lorsqu'une onde sonore rencontre un milieu liquide, créant ainsi des cycles de compression et d'expansion alternées (32).
Ces cycles de changement de pression provoquent une cavitation et des bulles de gaz se forment dans le milieu. Ces bulles ont une plus grande surface pendant le cycle d'expansion, ce qui augmente la diffusion de gaz, provoquant l'expansion de la bulle. On atteint un point où l'énergie ultrasonore fournie n'est pas suffisante pour retenir la phase vapeur dans la bulle ; par conséquent, une condensation rapide se produit. Les molécules condensées entrent en collision violemment, créant des ondes de choc. Ces ondes de choc créent des régions de très hautes températures et pressions, pouvant atteindre 5500°C et 50.000 kPa (Figure n°5) (33).
Les changements de pression résultant de ces implosions sont l'effet bactéricide principal dans les ultrasons. Les zones chaudes peuvent tuer certaines bactéries, mais elles sont très localisées et n'affectent pas une zone suffisamment étendue (33).
Chapitre I Revue Bibliographique
Figure n°5 : Principe de la cavitation (34)
Le deuxième effet antimicrobien de l’ultrason provient de l’effet chimique. En effet, dans la littérature il a été mentionné que la sonolyse utilisant une unité d’ultrasons de 20 kHz améliore l'inactivation des micro-organismes en raison des mécanismes antimicrobiens des radicaux hydroxyles (35-37). Des études antérieures ont montré que l’ultrason génère une augmentation de la température à un niveau localisé à l'intérieur d'une bulle effondré qui engendre des radicaux hydroxyles primaires (38-40). En outre, il a été rapporté que les réactions impliquant un transfert d'électron unique sont accélérées dans les applications ultrasoniques (41) .
Tous les effets chimiques de la cavitation comprennent la génération des radicaux libres qui impliquent un transfert d'électron unique pendant la phase de refroidissement d’atomes d'hydrogène et les radicaux hydroxyles se recombinent pour former du peroxyde d'hydrogène (H2O2) ayant des propriétés bactéricides importantes (42). À la fin de ces
réactions successives, la quantité de radicaux libres augmente. De plus, le radical hydroxyle (OH-) est capable de réagir avec le squelette sucre-phosphate de la chaîne d’ADN provoquant une sécession des liaisons ester-phosphate et des cassures dans l'ADN microbien double brin (43).
Chapitre I Revue Bibliographique
3. Microbiologie prévisionnelle
La microbiologie prévisionnelle est une discipline qui vise à développer des modèles mathématiques permettant de prévoir les aptitudes de croissance, survie ou décroissance des populations microbiennes dans les aliments en fonction des facteurs environnementaux influents (65).
La modélisation mathématique d’un comportement bactérien se déroule généralement en deux étapes :
La première étape est la modélisation primaire et consiste à décrire l’évolution du comportement microbien en fonction du temps avec un modèle cinétique. Les paramètres issus des modèles primaires permettent ensuite de procéder à la modélisation secondaire, qui correspond à la description de l’effet des facteurs environnementaux (température, pH, acides, aw, CO2, etc.) sur les paramètres du modèle primaire (44). Seule
la modélisation primaire sera abordée dans cette partie de la bibliographie.
3.1. Modélisation de destruction microbienne 3.1.1. Modélisation primaire
Modèles basés sur la distribution de Weibull
Le modèle de Weibull énoncé en 1951 par Waloddi Weibull est une loi de probabilité. Initialement, ce modèle a été développé pour décrire la défaillance d’un système donné soumis à une contrainte au cours du temps (45). En Microbiologie, cette distribution de la durée de vie a été d’abord employée pour décrire l’inactivation bactérienne due à stress thermique(46, 47).
Selon les travaux de Pelag et cole (2000), la distribution de la résistance au stress au sein de la population bactérienne suit une distribution de Weibull.
L’évolution de la population durant l’application d’un stress peut être alors décrite par :
𝑵 𝑵𝟎= 𝐞𝐱𝐩[− ( 𝒕 𝜶) 𝜷 ] (1)
α et β sont les deux paramètres de la distribution des thermorésistances. α est appelé paramètre d’échelle (caractérisé par le temps) et β est le paramètre de forme. Mafart et al. (2002) ont reparamétré ce modèle sous une forme plus intéressante dont les paramètres ont
Chapitre I Revue Bibliographique
une signification pratique pour l’inactivation des microorganismes : où α est appelé le temps de la première réduction décimale et β qui décrit la forme des courbes :
𝒍𝒐𝒈𝑵 = 𝒍𝒐𝒈𝑵𝟎− ( 𝒕 𝜶)
𝜷
(2)
Lorsque β <1 la courbe est concave, lorsque β >1 la courbe est convexe et lorsque la courbe est log-linéaire β =1 (Figure n°6) (48).
Figure n°6 : Simulation décrivant l’inactivation microbienne en utilisant le modèle du
Mafart et al. (2002) pour le paramètre de forme (48).
4. Microorganismes et les boues résiduaires
Les boues sont définies par le Comité Européen de Normalisation (CEN) comme «un mélange d'eau et de matières solides, séparé par des procédés naturels ou artificiels des divers types d'eau qui le contiennent» (49).
En fonction des processus de traitement d’épuration des eaux usées, quatre grandes Catégories de boues peuvent être distinguées (50) :
Les boues primaires qui proviennent du traitement primaire des eaux usées par décantation,
Les boues biologiques, biomasse en excès provenant du traitement biologique secondaire. Elles sont aussi appelés boues secondaires ou boues activées.
Chapitre I Revue Bibliographique
Les boues mixtes, mélange de boues primaires et de boues biologiques. Elles proviennent de la totalité de la station.
Les boues physico-chimiques, provenant de la décantation après traitement avec un réactif.
4.1. Microorganismes des boues
Les boues d’épuration contiennent de nombreux micro-organismes ayant un potentiel pathogène plus ou moins élevé. Ces organismes appartiennent à quatre catégories différentes d’êtres vivants (Bactéries, parasites, champignons, virus) qui proviennent en majorités des excréments humains ou animaux et qui se retrouvent dans les eaux usées de départ. (51) (Tableau n°I).
Chapitre I Revue Bibliographique
Tableau n° I : Liste de microorganismes pathogènes présents dans la boue (52).
Bactéries Fungi Parasites Virus
Aeromonas hydrophila Bacillus anthracis Brucella abortus Brucella melitensis Brucella suis Campylobacter jejuni Clostridium spp Escherichia coli Coxiella burnetiid Erysipelopetrix rhusiopathiae Legionella pneumophila Leptospira interrogans Listeria monocytogenes Mycobacteries atypiques Mycobacterium avium Mycobacterium bovis Mycobacterium paratuberculosis Pseudomonas aeruginosa Pseudomonas pseudomallei Pseudomonas pseudomallei Salmonella spp Shigella sp Staphylococcus spp Streptococcus spp Yersinia enterocolitica Levures Candida Cryptococcus Trichospohora Moisissures Aspergillus Phialophora Geotrichum Trichophyton Epodermophyton Protozoaires Cryptosporidium sp Giardia intestinalis Entamoeba histolytica Balantidium coli Toxoplasma gondi Helminthes Ascaris lumbricoides Trichuris trichiura Toxocara sp Taenia sp Hymenolepis Coronavirus Enterovirus Herpesvirus Parvovirus Rotavirus Poxvirus Togavirus
Chapitre II Matériel et Méthodes
1. Cadre et objectifs
L’objectif de ce chapitre est de décrire l’échantillon étudié et de présenter tous les protocoles et les techniques utilisés au cours de ce travail.
Compte tenu de l’évolution des techniques de destruction microbienne, et que l’impact de ces traitements sur les microorganismes diffère d’une technique à une autre, nous avons essayé à travers ce travail de vérifier l’efficacité des deux traitements innovants qui sont : la micro-onde et l’ultrason sur la flore mésophile aérobie totale et la flore fongique de la boue d’épuration.
L’étude a été réalisée au niveau du laboratoire de la faculté SNV-ST de l’université de Bouira, durant une période de 3 mois (Mars- Mai).
2. Équipements et produits utilisés
Les produits et les milieux utilisés dans cette présente étude sont listés dans le tableau suivant :
Tableau II : Liste des produits utilisés
La composition de ces milieux de culture est représentée dans l’annexe I.
Produit
Eau distillée Eau physiologique
Utilisation
Préparation des milieux de culture Préparation des dilutions
Milieux Utilisation
Gélose nutritive Gélose sabouraud
Dénombrement de la FAMT
Chapitre II Matériel et Méthodes
Les différents équipements utilisés sont listés dans le tableau suivant :
Tableau III : Liste des appareils utilisés.
Appareils Référence
Balance de precision KERN 440-35N
Hotte de protection microbiologique
Cruma, CRFL2
Etuve memmert
Autoclave DaiHan, WAC – 80, korai
Mortier IKA A11 BASIC, Germany
Micro-onde LG (MS2535GISW)
Bain ultrasound J.P.SELECTA, s.a
Vortex Venticell
Bain marie Nuve bath
pH meter METTLER TOLEDO
3. Préparation de l’échantillon
3.1. Prélèvements et transport de l’échantillon
Un échantillon homogène et composite a été réalisé à partir de différents prélèvements effectués sur différents endroits et profondeurs sur le lit de séchage de la station d’épuration des eaux usées de la ville de Bouira, qui cumule des boues de différentes périodes (Figure n° 07).
Les prélèvements ont été effectués dans des sacs en plastique stériles et conservés à une température de +4°C/ +6°C.
Chapitre II Matériel et Méthodes
Figure n°7: Lit de séchage des boues d’épuration dans la STEP de Bouira.
4. Les flores microbiennes étudiées La flore mésophile aérobie totale
La flore mésophile aérobie totale est l'ensemble des micro-organismes aptes à se multiplier à l'air aux températures moyennes, plus précisément ceux dont la température optimale de croissance est située entre 25 et 40°C (66).
La flore mésophile aérobie totale (FMAT) est utilisée comme un indicateur de pollution global (66).
La flore fongique
La flore fongique comprend les levures et les moisissures.
- Levure : Micro-organisme aérobie, mésophile qui se développe à 25°C, en formant des
colonies présentant le plus souvent un contour régulier et une surface plus au moins convexe (68).
- Moisissure : Micro-organisme aérobie, mésophile filamenteux qui développe
habituellement des propagules ou des germes plats ou duveteux ou des colonies présentant souvent des fructifications colorées et des formes de sporulation (68).
Chapitre II Matériel et Méthodes
5. Procédures expérimentales et analytiques
5.1. Estimation de la charge microbienne initiale (la FAMT et la flore fongique)
Préparation de la solution mère et les dilutions décimales
Un échantillon de boue de 01 g a été pesé, puis mis aseptiquement dans un tube à essai stérile contenant 9 ml d’eau physiologique stérile donnant la solution mère « dilution 10-1
», la solution a été homogénéisée à l’aide d’un vortex. Par la suite, différentes dilutions du 10-2 jusqu’à 10-4 sont préparées, bien homogénéisées pendant 5 à 10 secondes avec l’eau physiologique stérile (67) (Figure n°8).
Figure n°08 : Les dilutions décimales préparées à partir de la solution mère. Ensemencement et incubation
Chaque dilution a été ensemencée en surface avec 0,1 ml de suspension, la FMAT a été ensemencée sur la gélose nutritive et la flore fongique sur Sabouraud.
Les boites ont été ensuite incubées à 22 et 25 °C pendant 3 et 5 jours pour les FAMT et la flore fongique respectivement.
Lecture
Un comptage du nombre de colonies microbiennes par boite de Pétri a été effectué en retenant juste les boites contenants entre 30 et 300 colonies pour la FAMT et 15 à 150
Chapitre II Matériel et Méthodes
Le nombre global de micro-organismes est déterminé par l’application de la loi : 𝑵 = 𝒄
𝑫𝑽 Où :
C : moyenne du nombre de colonies dans les deux boites. V : volume ensemencé.
D : dilution à partir de laquelle les dénombrements sont obtenus.
Le nombre N est exprimé en unités formant colonies par millilitre ou gramme de boue (UFC/ml) (8, 53).
Cette loi est appliquée pour l’interprétation de toutes les analyses bactériologiques qui suivent dans cette étude.
6. Traitement de l’échantillon
6.1. Traitement assisté par micro-onde
Dans cette étude, le traitement a été réalisé à l’aide d’un micro-onde domestique, ayant
une cavité de dimensions de 22.5 × 37.5 × 38.6 cm et une fréquence de fonctionnant de 2,45 GHz, fonctionne a des puissances allant de 100 a 1000 Watts . Pour les cinetiques de destruction, des essais ont été realisès comme suit :
1er essai
Un échantillon de 50 g de boue a été mis aseptiquement dans un bécher stérile de 500ml contenant 450ml d’eau physiologique, broyé à l’aide d’un bras mortier et homogénéisé par des rotations manuelles, ensuite ce volume est réparti à raison de 50 ml dans des flacons de 180 ml (Figure n° 19). Par la suite ces dernières ont été traitées par micro-onde en les plaçant dans sa cavité et en exposant chacun à l’irradiation d’une des puissances 400, 600 ,800 et 1000 W pendant des durées de temps variables : 3, 5, 7, 10, 12, 15, 18, 20, 22, 25 minutes successives.
Chapitre II Matériel et Méthodes
Figure n°09 : Échantillons du 1er essai.
2eme essai
Trois échantillons de boue de 100 g ont été pesés et misent aseptiquement dans des béchers stériles de 500 ml (Figure n° 10). Le mélange a été irradié à des puissances de 300, 600 et 900 W pendant des durées de temps variables : 3, 5, 7, 10, 12, 15, 18, 20, 22 et 25 minutes successives.
Figuren°10 : Échantillons du 2eme essai.
Après le traitement par micro-onde, les échantillons ont été retirés et recouverts avec du papier aluminium désinfecté puis refroidi à température ambiante (14).
Une dilution décimale de 10-1 a été préparée à partir de 1 g de boue traitée de chaque
Chapitre II Matériel et Méthodes
6.2. Traitement assisté par ultrason
Le traitement sonore de notre échantillon a été réalisé à l’aide d’un bain ultrason
(Ultrasonic Cleaner Set, WUC-A10 H). L’appareil fonctionne à une fréquence de 40 KHz avec une puissance de 523W. Pour les cinetiques de destruction, des essais ont été realisés comme suit :
1er essai
Un échantillon de 011g de boue a été pesé et mis aseptiquement dans un bécher stérile de 0111 ml contenant 501 ml d’eau physiologique puis broyé à l’aide d’un bras mortier et homogénéisé par des rotations manuelles, un volume de 60 ml a été réparti en 06 tubes à essai en verre (10 ml/ tube). Par la suite ces dernières ont été exposés au bain ultrason, à de température de 45°C pendant des durées de temps variable : 05, 20, 30, 40, 50, 65 min (Figure n° 11).
Figure n°11 : Échantillons du 1er essai.
2eme essai
Une dilution de 10-4 a été préparée à partir d’un échantillon de 1g de boue diluée avec 9ml d’eau physiologique, la dilution a été préparée en triple (Figure n° 12).
Chapitre II Matériel et Méthodes
Les tubes de la dilution 10-4 ont été exposé à des températures de 30, 45, 60 °C pendant des
durées de temps variables 5, 20, 30, 40, 50, 65 et 90 minutes.
Figure n° 12 : Échantillon de 2eme essai.
7. Analyse microbiologique après traitement
Dans cette partie nous avons soumis les échantillons ayant subi le traitement à l’analyse microbiologique en vue de montrer l’impact des micro-ondes et des ultrasons sur la réduction de la charge microbienne.
7.1. Dénombrement de la flore mésophile aérobie totale et la flore fongique Ensemencement et incubation
À partir de chaque échantillon traité, 0.1 ml de suspension a été étalé en surface sur :
Une boite de Pétri contenant de la gélose nutritive.
Une boite de Pétri contenant Sabouraud.
Les boites ont été ensuite incubées à 22 et 25 °C pendant 3 et 5 jours pour les FAMT et la flore fongique respectivement
Lecture
Un comptage du nombre de colonies microbiennes a été effectué en prenant en considération juste les boites contenants entre :
30 et 300 colonies pour FAMT ;
Chapitre II Matériel et Méthodes
Les résultats sont exprimés en unités formant des colonies par millilitre ou gramme de boue (UFC/ml).
8. Expression et analyse des résultats
Le traitement de nos résultats a été réalisé par deux méthodes :
Calcul de taux de réduction
La charge microbienne restante après exposition en % = (moyenne de charge obtenue à chaque temps et puissance /nombre de la charge initiale) × 100%.
La réduction en 100% = 100 – charge microbienne restante après exposition en%.
Modélisation de la cinétique d'inactivation
La diminution de la population survivante de N (t) par traitement micro-onde et ultrason est décrite par le modèle Weibull (Équation 2). Cette équation a été déjà détaillée dans la section (section 3.3.1).
Estimation des paramètres
Les paramètres du modèle Weibull (Équation 2) ont été ajustées en utilisant le Toolbox « cftool » de Matlab (version 7, The Math Works Inc, Natick, MA, Etats-Unis).
Chapitre III Résultats et Discussion
Dans ce chapitre sont présentés les résultats du traitement de la biomasse des boues obtenues par les deux méthodes : micro-onde et ultrason.
La première partie portera sur la validation de l’efficacité des différentes méthodes de traitement utilisées et la seconde partie qui suit est consacrée à la modélisation des cinétiques de destruction microbienne.
1. Estimation de la charge microbienne initiale avant traitement : La FMAT et la flore fongique :
La charge initiale de la FMAT et la flore fongique présente dans la boue d’épuration prélevée sur le lit de séchage de la station d’épuration de la ville de Bouira est de 11,1.1010
et 10,5.1010 UFC/ml respectivement (Figure n° 13).
Figure n°13 : Charge de la FMAT et la flore fongique avant le traitement.
2. Traitement assisté par micro-onde :
Après traitement des solutions préparées à partir de la boue avec différents temps et puissances micro-onde, nous avons enregistré une diminution dans la charge de la FMAT et la flore fongique, comme le montre le tableau n° IV.
Chapitre III Résultats et Discussion
Tableau IV : Réduction de la charge de FMAT et de la flore fongique après le traitement
assisté par micro-ondes (essai 01).
Puissance (W)
400 600 800 1000
Temps (min) FMAT F.F FMAT F.F FMAT F.F FMAT F.F
3 Ind 14.8 Ind 9.6 Ind 6.9 Ind 5
5 Ind 8.6 Ind 6.9 Ind 3.9 Ind 3.3
7 Ind 7.2 Ind 4.7 Ind 3.1 Ind 2.4
10 Ind 6.8 Ind 1.8 29.8 2 17.4 1.7 12 20 6.6 20.2 1.6 16.2 1.9 7.4 1.6 15 18 6.4 13.2 1.5 5 1.5 3.8 0 18 16.2 5 10.7 0 3.8 0 0 0 20 15 4.1 7.6 0 0 0 0 0 22 13.4 3.4 4.2 0 0 0 0 0 F.F : Flore fongique Ind : indénombrable
Les charges microbiennes sont exprimées en UFC* 10 3/ ml
La réduction de la FMAT n’est pas significative après l’exposition aux puissances 400 et 600W pendant 10 min et aux puissances 800 et 1000W pendant 7 min, vu que les boites restent indénombrables (Annexe II). En revanche, une réduction remarquable a été enregistrée à l’irradiation 400 et 600 W après 12 min et qui est estimée de 99,99 %. Et vraisemblablement pour le traitement au traitement d’exposition aux puissances 800 et 1000 W après 10 min. Une destruction totale est obtenue après le 18 et 20 min du
Chapitre III Résultats et Discussion
Concernant la flore fongique, une réduction de 99.99 % est obtenue après 3 min d’exposition au micro-onde pour toutes les puissances appliquées. La destruction totale (100 %) n’est obtenue qu’après 18 min à 600 et 800 W et après 15 min à 1000 W.
Quant au traitement de la boue sèche par 300, 600 et 900 W, le résultat obtenu montre une diminution de la charge de la FMAT et de la flore fongique (Tableau n° V).
Tableau V : Réduction de la charge de FMAT et de la flore fongique après traitement
assisté par micro-ondes (essai 2).
Puissance (W)
300 600 900
Temps (min) FMAT F.F FMAT F.F FMAT F.F
3 Ind Ind Ind Ind Ind 14.3
5 Ind Ind Ind Ind Ind 3.7
7 Ind 8.7 Ind 6.4 Ind 2.9
10 Ind 7.2 Ind 5.1 Ind 2.1
12 Ind 6.8 Ind 4.3 23.7 1.6 15 Ind 6.1 30 3 5.9 0 18 30 3 22 2.6 5.6 0 20 25.3 2.8 20 1.7 0 0 22 24 1.9 17.8 0 0 0 22 15.1 0 12.3 0 0 0 25 12.5 0 9 0 0 0 Ind : indénombrable
Chapitre III Résultats et Discussion
La réduction de la FMAT après 15, 12 et 10 min d’exposition aux puissances 300, 600, et 900W respectivement n’est pas statistiquement significative, vu que les boites restent indénombrables, il atteint 99.99 % après 18 min d’exposition à 300 W, 15 min après l’exposition à 600 W et 12 min après l’exposition à 900 W. La destruction totale (100%) est obtenue à la puissance 900 W après une durée d’exposition de 20 min.
Concernant la flore fongique la réduction n’est pas significative lorsque la boue a été irradiée aux puissances 300 et 600 W pendant 5 min et à 900 W pendant 3 min, il atteint 99.99 % après 7 min d’exposition aux puissances 300 et 600 W et après 5 min à 900 W. La destruction totale (100%) était obtenue aux puissances 600 et 900 W après 22 min et 18 min respectivement. (Annexe II).
Les résultats obtenus à partir de ces expériences, ont indiqué que dans tous les échantillons, la destruction des microorganismes augmente avec les puissances et la durée d’exposition aux micro-ondes.
Nous avons obtenu une réduction complète des microorganismes sur des temps de contact courts, lorsque la boue était irradiée à des niveaux de puissance micro-ondes plus élevés, une entrée de puissance élevée entraîne une élévation rapide de la température intracellulaire ce qui engendre la destruction microbienne.
Lorsque la boue était irradiée à des niveaux de puissance plus bas ; la destruction était ralentie, les puissances basses n’engendrent pas une augmentation de la température à des valeurs de destruction qu’après des durées d’exposition prolongées.
L'augmentation de la destruction des microorganismes avec l'augmentation de l'énergie des micro-ondes peut être attribuée à l’augmentation à la fois de l'effet thermique (température) et de l'intensité du rayonnement électromagnétique (effet non thermique), qui sont tous deux les mécanismes par lesquels les micro-organismes sont détruits pendant le traitement par micro-ondes ; cependant, l'effet thermique est connu pour être le principal mécanisme par lequel la destruction survient (54).
L'effet thermique provoque la rupture des cellules microbiennes quand l'eau est rapidement chauffée au point d'ébullition par la rotation des molécules dipolaire sous un champ électromagnétique oscillant (54, 55), L’effet athermique des micro-ondes est lié au
Chapitre III Résultats et Discussion
changement des structures protéiques en divisant différemment les ions et en modifiant la direction des réactions biochimiques (23) .
Les microorganismes ne répondent pas de la même manière au radiation des micro-ondes, la réduction de la flore fongique était plus rapide que celle de la flore aérobie ce qui confirme que les champignons sont plus sensibles à l’irradiation de micro-ondes que les bactéries (56).
Ce résultat est cohérant avec ceux Wainwright et al. (1980) et Ferriss et al. (1980) et Speir et al. 1986 qui ont testé l’effet des micro-ondes sur les microorganismes du sol et ont trouvés que les champignons sont les plus sensibles (56-59).
Nous avons remarqué une différence entre le 1er essai qui a été réalisé en milieu liquide et le 2ème essai qui a été réalisé à sec, la destruction était meilleure dans le milieu liquide ou la boue absorbe mieux l’irradiation des micro-ondes donc mieux chauffée grâce aux propriétés diélectriques de l’eau.
Dans un environnement sec, l'effet germicide du rayonnement des micro-ondes a été significativement diminué et produit seulement après une période prolongée d'irradiation, probablement en raison d'une transformation plus basse d’énergie des micro-ondes en chaleur (69).
Yoonkyung Kang et al. (2014) ont testé l'effet germicide de l'irradiation des micro-ondes sur les spores fongiques (ex. Cladosporium herbarum et Fusarium solani), les bactéries végétatives et les spores bactériennes (ex., Bacillus subtilis), ils ont travaillé dans des milieux liquides et secs, ils ont trouvé que la température des milieux liquides était généralement plus élevée que celle des milieux secs. En outre, l'effet germicide semble être plus fort dans les milieux liquides. Par conséquent, ils ont conclu que la différence de température est liée à la différence de la teneur entre les milieux liquides et secs (60). Notre résultat est en accord avec ceux obtenus par Mawioo et al. (2017) qui ont traité 04 types de boues, ces derniers possèdent des teneurs différentes en eau. Ils ont conclu que plus la teneur en eau est élevée plus la boue sera chauffée rapidement et la destruction sera meilleure (14).
Chapitre III Résultats et Discussion
3. Traitement assisté par ultrason :
Le traitement de la solution mère a montré une diminution de la flore Aérobie Mésophile Totale et la flore fongique. Les résultats sont représentés dans le tableau n° VI.
Tableau VI : la charge de la FMAT et la flore fongique de l’essai 01 après l’exposition au
bain à ultrason.
Temps (min) Flores Microbiennes
FMAT Flore fongique
20 Indénombrable Indénombrable
30 Indénombrable Indénombrable
40 Indénombrable Indénombrable
65 Indénombrable Indénombrable
Les résultats obtenus montrent que :
L’exposition de la solution mère aux ultrasons n’a induit aucun changement significatif dans la charge de la FMAT et de la flore fongique, où on n’a pas observé une diminution de la charge initiale après traitement à courte durée.
Le traitement par ultrasons à longue durée (65 min) a engendré une légère diminution, vu que la charge de la FMAT et de la flore fongique est restée indénombrable (Annexe V).
Ces résultats sont compatibles avec les travaux de Brokman et al. (2010) et Dewil et al. (2006). Bien que leurs études aient utilisé des échantillons et des germes différents et un appareil à ultrason plus performant (61, 62).
L’étude de Brokman et al. (2010) a montré que la sonotrode à ultrasons n’a pas grand effet sur les micro-organismes après un traitement de courte durée et à faible intensité (61).
Dewil et al. (2006) ont obtenu la même efficacité dans les conditions déjà citées. La charge
initiale, la durée et l’intensité sont fortement liées entre elles et nécessitent un équilibrage lors de l’irradiation ultrasonore (62).
Chapitre III Résultats et Discussion
Lors du traitement de la dilution 10-4, la charge de survie de FMAT et la flore fongique
sont représenté dans le tableau suivant.
Tableau VII : Réduction de la flore fongique et la FMAT après traitement par ultrason.
Température (°C)
30 45 60
Temps (min) FMAT F.F FMAT F.F FMAT F.F
5 9 1.5 6.6 1.7 10.5 6.6 20 3 0 6.5 1.5 10 4.6 30 0 0 3 0 5 3.6 40 0 0 0 0 4.5 3.2 50 0 0 0 0 3.5 1.7 65 0 0 0 0 0 0 90 0 0 0 0 0 0 F.F : Flore fongique
Les charges microbiennes sont exprimées en UFC* 106/ ml.
Les résultats obtenus montrent qu’à la dilution 10-4 au traitement à ultrasons avec variation
de la température 30, 45 et 60°C. Nous avons constaté une destruction totale de la FMAT après 30, 40,65 min à 30,45 et 60°C respectivement (Annexe IV).
Les résultats montrent que l’augmentation de la température diminue l’efficacité des ultrasons, certains auteurs Guerrero et al. (2001); Herceg et al. (2012) ont suggéré que l'efficacité du traitement par ultrasons dans la destruction des bactéries par cavitation pourrait être minimisée avec une augmentation de la température. Ce fait pourrait être probablement le résultat d'un effet thermique accru qui masque l'effet de sonication, et / ou une diminution dans la violence de l'implosion en raison de l'augmentation de la pression
Chapitre III Résultats et Discussion
Dans le cas de la flore fongique, le traitement par ultrasons avec variation de la température de la dilution 10-4, les résultats obtenus sont plus significatifs, nous avons
enregistré une destruction totale de la flore fongique après 20, 30, 65 min à 30, 45, 65°C. Chemat et al. (2011) ont rapporté que plus la cellule est grande plus l’effet des ultrasons est meilleur, ce qui est expliqué par l’augmentation de la surface de contact des vibrations des ondes avec la cellule (26).
Les différents profils de charge de la FMAT et la flore fongique après traitement par micro-onde et ultrason sont représentés dans l’annexe III, V.
4. Modélisation de la destruction microbienne : 4.1. Cinétique de destruction par microonde :
Paramètres et qualité d’ajustement :
Les paramètres estimés du modèle Weibull lorsque la boue a été traitée en solution sont résumés dans le tableau ci-dessous.
Tableau VIII : Valeurs des paramètres de cinétiques d’inactivation de FMAT et de la flore
fongique par micro-onde.
La qualité d’ajustement de chaque cinétique a été représentée par les coefficients de détermination, d’ajustement et RMSE. Regardant le tableau n°VIII, les valeurs de ces paramètres statistiques (R2 allant 0,86 à 0,99 ; RMSE proche de la valeur 0) sont
α(s) β R2 RMSE
Puissance (W)
FMAT FF FMAT FF FMAT FF FMAT FF
400 4174 2214 0.52 1.26 0.93 0.84 0.06 0.08
600 1302 917.5 1.64 1.12 0.97 0.92 0.07 0.12
800 977.6 1137 2.04 0.69 0.86 0.97 0.17 0.05
Chapitre III Résultats et Discussion
hautement satisfaisantes. Les cinétiques de destruction expérimentale et celles prédites obtenues à différentes puissances et durées de traitement sont présentés dans la figure n°14.
Figure n°14 : Cinétiques d’inactivation des populations de la flore fongique et de FMAT
par microonde. Comparaison des valeurs expérimentales (400W, 600W, 800W et
1000W) et celles simulées en utilisant le modèle de Weibull (―).
Les paramètres d’ajustement lorsque la boue a été traitée à sec sont présentés dans le tableau ci-dessous.
Tableau IX : Valeurs des paramètres de cinétiques d’inactivation de FMAT et de la flore
fongique par micro-onde (boue sèche).
α (s) β R2 RMSE
FMAT FF FMAT FF FMAT FF FMAT FF
300W 2059 1516 2.40 2.50 0.98 0.96 0.03 0.05
600W 2063 1488 1.71 1.35 0.96 0.97 0.05 0.03
Chapitre III Résultats et Discussion
Les résultats obtenus nous amènent à conclure que les cinétiques de destruction sont bien présentées par le modèle du Weibull avec un R2 minimal de 0,83 et maximal de 0,98, ainsi
que tous les RMSE présentent des valeurs inferieures à 0.23 ce qui signifie que l’erreur moyenne entre les valeurs expérimentales et prédites est proche de 0. La figure n°15 présente les cinétiques de survie de la FMAT et la flore fongique expérimentale et les celles prédites obtenues à différentes puissances et durées de traitement.
La sensibilité thermique de la flore fongique et la FMAT est quantifiée par les valeurs des temps de réduction décimale α présentés dans le tableau IX.
Figure n°15 : Cinétiques d’inactivation des populations de la flore fongique et de FMAT
par microonde. Comparaison des valeurs expérimentales ( 300W, 600W et 900W) et celles simulées en utilisant le modèle de Weibull (―).
4.2. Cinétique de destruction par ultrason :
Paramètres et qualité d’ajustement :
Les cinétiques de destruction de la FMAT et de Flore fongique ont été bien représentées. Comme le montrent les valeurs de R2 déterminés pour chaque température et chaque flore, la qualité d’ajustement est très bonne. Le R2 minimum rencontré est de 0.911. Ainsi que le
RMSE < 0.081(tableau X), ce qui signifie que l’erreur moyenne entre les valeurs expérimentales et prédites est proche à 0.
(Nous notons que les paramètres du modèle n’ont pas été estimés pour la flore fongique traitée par ultrason à 30 °C. à cause du manque des donnés parce que nous avons enregistré une destruction totale juste après 20 min).
Chapitre III Résultats et Discussion
Tableau X : Valeurs des paramètres cinétiques d’inactivation de FMAT et de la flore
fongique par ultrason.
ND : Non déterminé
La figure n°16 présente la cinétique de survie de la flore fongique et de FMAT.
Figure n°16 : Cinétiques d’inactivation des populations de la flore fongique et de FMAT
assisté par Ultrason. Comparaison des valeurs expérimentales (˜ 30°C, 45°C et 60°C) et celles simulées en utilisant le modèle de Weibull (―).
5. Comparaison du traitement assisté par micro-onde et du traitement à l’ultrason
L’analyse des donnés révèle que le traitement assisté par micro-onde est le plus adéquat pour la destruction de la flore microbienne des boues (Figure n° 17), vu qu’on a obtenu une destruction de 99,9% à des courtes durés, contrairement aux ultrasons qui n’ont pas induit une diminution significative sur la solution mère traitée.
Cependant lors du traitement des dilutions réalisées à partir de la solution mère par
ultrason, nous avons enregistré un changement dans la charge des microorganismes traduit
Paramètres α (s) β RMSE R2
Températures F.F FMAT F.F FMAT F.F FMAT F.F FMAT
30 °C ND 1328 ND 6.811 ND ND ND ND
45°C 6226 2442 0.02 2.24 ND 0.006 0.99 0.99
Chapitre III Résultats et Discussion
ondes comme la meilleure technique pour l’hygiénisation des boues des STEP afin de les valorisées.
Figure n° 17 : Comparaison du traitement assisté par micro-onde et du traitement à l’ultrason
de la flore fongique (a) et de la FMAT (b).
0 0,5 1 1,5 2 2,5 3 3,5 4 4,5 5 12 17 22 27 Log N ( UF C/ g) Temps (mn) Traitement Microonde Traitement Ultrason (a) 0,0 0,5 1,0 1,5 2,0 2,5 3,0 3,5 4,0 4,5 0 20 40 60 80 100 LogN( UF C/ g) Temps (min) Traitement Microonde Traitement Ultrason (b)
Conclusion et perspectives
Conclusion et perspectives
Dans cette présente étude nous avons exploré l’influence des traitements micro-ondes et ultrasons sur la destruction de la FAMT et de la flore fongique présentent dans la boue d’épuration des STEP, en vue de l’obtention d’une cinétique de destruction simulée avec le modèle de Weibull, et de connaitre la meilleure méthode de traitement de ce type de déchet dans le contexte de la protection de l’environnement et la valorisation des boues résiduaires.
Le traitement par micro-ondes a été réalisé sur deux échantillons de boue liquide et sèche, la destruction a été meilleure dans le milieu liquide, une destruction de 100% a été obtenue aux puissances 800 et 1000 W après 20 min et 18 min respectivement pour la FMAT et après 18 min à 600 et 800 W et 15 min à 1000 W pour la flore fongique.
Cependant, la tendance a été renversé dans le cas du traitement assisté par ultrason le traitement par ultrasons, la réduction de la charge de la FAMT a été engendrée après une forte dilution et une durée d’exposition plus longue. La variation de la température dans le traitement de des échantillons dilués, indique que l’augmentation de la température diminue l’efficacité des ultrasons et la destruction totale de la FAMT est obtenue après 30, 40, 60 min à 30,45, 60°C respectivement.
A la lumière de ces résultats, nous concluons que ces deux traitements appliqués ont un effet significatif sur les deux flores de la boue étudiée. Néanmoins, les micro-ondes ont un effet plus efficace que celui des ultrasons par conséquent, ce traitement pourrait être qualifié comme un traitement environnemental alternatif.
Toutefois, il serait souhaitable de compléter ce travail par :
D’autres investigations notamment sur l’effet de ces techniques sur les différentes souches qui se trouvent dans la boue ;
Optimisation du traitement assisté par microonde/ultrason ;
Couplage microonde à l’ultrason afin de booster le traitement ;
Références Bibliographiques
1. Alnnasouri M. Etude du développement de biofilms dans des réacteurs de traitement d'eau: éditeur inconnu. Université de limoges; 2010, 172p.
2. Levy C. Principaux facteurs influençant l'efficacité de la lumière pulsée pour la décontamination des microorganismes pathogènes et d’altération des denrées alimentaires: Université d'Avignon; 2010,1992p.
3. Veillet S. Enrichissement nutritionnel de l'huile d'olive: entre tradition et innovation: Université d'Avignon; 2010,153p.
4. Fellows P. Properties of foods and processing theory. Food Processing Technology. 2000.
5. Ahmed J, Ramaswamy HS. Microwave pasteurization and sterilization of foods. Food Science And Technology-New York-Marcel Dekker-. 2004;167:691.
6. Leveau J-Y, Larpent J-P, Bouix M. Sécurité microbiologique des procédés alimentaires. Techniques de l'ingénieur Bioprocédés. 2001(F1120).
7. Dupin H, Cuq J-L, Malewiak M-I, Leynaud-Rouaud C, Berthier A-M. Alimentation et nutrition humaines ESF Editeur ed. Paris1992; 1533p.
8. Guiraud J-P. Microbiologie alimentaire Paris2012. 66-69p.
9. Lansing-M Prescott, John Harley, Klein D-A. Microbiologie. Paris2003. 1184 p. 10. Chandrasekaran S, Ramanathan S, Basak T. Microwave material processing—a review. AIChE Journal. 2012;58(2):330-63.
11. Janković SM, Milošev MZ, Novaković ML. The effects of microwave radiation on microbial cultures. Hospital Pharmacology-International Multidisciplinary Journal. 2014;1(2):102-8.
12. Heddleson RA, Doores S. Factors affecting microwave heating of foods and microwave induced destruction of foodborne pathogens–a review. Journal of Food Protection. 1994;57(11):1025-37.
13. Wakim LH. Effet d'un chauffage micro-ondes et conventionnel sur la thermorésistance d'une Salmonelle traitée dans un produit à basse activité d'eau. Conséquences sur la qualité du produit: ENSIA; 2008.
14. Mawioo PM, Garcia HA, Hooijmans CM, Velkushanova K, Simonič M, Mijatović I, et al. A pilot-scale microwave technology for sludge sanitization and drying. Science of the Total Environment. 2017;601:1437-48.
15. Singh R. Heating Mechanism of Microwave. International Journal for Exchange of Knowledge. 2014:43.