ﺎﻨﺘﻤﻠﻋ ﺎﻣ ﻻﺇ ﺎﻨﻟ ﻢﻠﻋ ﻻ ﻚﻧﺎﺤﺒﺳ
ﻢﻴﻜﳊﺍ ﻢﻴﻠﻌﻟﺍ ﺖﻧﺃ ﻚﻧﺇ
:ﺔﻳﻵﺍ :ﺓﺮﻘﺒﻟﺍ ﺓﺭﻮﺳ
31
MOHAMMED V DE RABAT
FACULTE DE MEDECINE ET DE PHARMACIE - RABAT
DOYENS HONORAIRES :
1962 – 1969 : Professeur Abdelmalek FARAJ 1969 – 1974 : Professeur Abdellatif BERBICH 1974 – 1981 : Professeur Bachir LAZRAK 1981 – 1989 : Professeur Taieb CHKILI
1989 – 1997 : Professeur Mohamed Tahar ALAOUI 1997 – 2003 : Professeur Abdelmajid BELMAHI 2003 - 2013 : Professeur Najia HAJJAJ – HASSOUNI
ADMINISTRATION :
Doyen
Professeur Mohamed ADNAOUI
Vice-Doyen chargé des Affaires Académiques et estudiantines
Professeur Brahim LEKEHAL
Vice-Doyen chargé de la Recherche et de la Coopération
Professeur Toufiq DAKKA
Vice-Doyen chargé des Affaires Spécifiques à la Pharmacie
Professeur Jamal TAOUFIK
Secrétaire Général
1 - ENSEIGNANTS-CHERCHEURS MEDECINS ET PHARMACIENS
PROFESSEURS :
DECEMBRE 1984
Pr. MAAOUNI Abdelaziz Médecine Interne – Clinique Royale
Pr. MAAZOUZI Ahmed Wajdi Anesthésie -Réanimation
Pr. SETTAF Abdellatif Pathologie Chirurgicale
NOVEMBRE ET DECEMBRE 1985
Pr. BENSAID Younes Pathologie Chirurgicale
JANVIER, FEVRIER ET DECEMBRE 1987
Pr. LACHKAR Hassan Médecine Interne
Pr. YAHYAOUI Mohamed Neurologie
DECEMBRE 1989
Pr. ADNAOUI Mohamed Médecine Interne –Doyen de la FMPR
Pr. OUAZZANI Taïbi Mohamed Réda Neurologie
JANVIER ET NOVEMBRE 1990
Pr. HACHIM Mohammed* Médecine-Interne
Pr. KHARBACH Aîcha Gynécologie -Obstétrique
Pr. TAZI Saoud Anas Anesthésie Réanimation
FEVRIER AVRIL JUILLET ET DECEMBRE 1991 Pr. AZZOUZI Abderrahim Anesthésie Réanimation- Doyen de FMPO
Pr. BAYAHIA Rabéa Néphrologie
Pr. BELKOUCHI Abdelkader Chirurgie Générale
Pr. BENCHEKROUN Belabbes Abdellatif Chirurgie Générale
Pr. BENSOUDA Yahia Pharmacie galénique
Pr. BERRAHO Amina Ophtalmologie
Pr. BEZAD Rachid Gynécologie Obstétrique Méd. Chef Maternité des
Orangers
Pr. CHERRAH Yahia Pharmacologie
Pr. CHOKAIRI Omar Histologie Embryologie
Pr. KHATTAB Mohamed Pédiatrie
Pr. SOULAYMANI Rachida Pharmacologie- Dir. du Centre National PV Rabat Pr. TAOUFIK Jamal Chimie thérapeutique V.D à la pharmacie+Dir. du CEDOC +
DECEMBRE 1992
Pr. AHALLAT Mohamed Chirurgie Générale Doyen de FMPT
Pr. BENSOUDA Adil Anesthésie Réanimation
Pr. CHAHED OUAZZANI Laaziza Gastro-Entérologie
Pr. CHRAIBI Chafiq Gynécologie Obstétrique
Pr. EL OUAHABI Abdessamad Neurochirurgie
Pr. FELLAT Rokaya Cardiologie
Pr. GHAFIR Driss* Médecine Interne
Pr. JIDDANE Mohamed Anatomie
Pr. TAGHY Ahmed Chirurgie Générale
Pr. ZOUHDI Mimoun Microbiologie
MARS 1994
Pr. BENJAAFAR Noureddine Radiothérapie
Pr. BEN RAIS Nozha Biophysique
Pr. CAOUI Malika Biophysique
Pr. CHRAIBI Abdelmjid
Endocrinologie et Maladies Métaboliques Doyen de la
FMPA
Pr. EL AMRANI Sabah Gynécologie Obstétrique
Pr. EL BARDOUNI Ahmed Traumato-Orthopédie
Pr. EL HASSANI My Rachid Radiologie
Pr. ERROUGANI Abdelkader Chirurgie Générale – Directeur du CHIS-Rabat
Pr. ESSAKALI Malika Immunologie
Pr. ETTAYEBI Fouad Chirurgie Pédiatrique
Pr. HASSAM Badredine Dermatologie
Pr. IFRINE Lahssan Chirurgie Générale
Pr. MAHFOUD Mustapha Traumatologie – Orthopédie
Pr. RHRAB Brahim Gynécologie –Obstétrique
Pr. SENOUCI Karima Dermatologie
MARS 1994
Pr. ABBAR Mohamed* Urologie Directeur Hôpital My Ismail Meknès
Pr. ABDELHAK M’barek Chirurgie – Pédiatrique
Pr. BENTAHILA Abdelali Pédiatrie
Pr. BENYAHIA Mohammed Ali Gynécologie – Obstétrique Pr. BERRADA Mohamed Saleh Traumatologie – Orthopédie Pr. CHERKAOUI Lalla Ouafae Ophtalmologie
Pr. LAKHDAR Amina Gynécologie Obstétrique
Pr. MOUANE Nezha Pédiatrie
MARS 1995
Pr. ABOUQUAL Redouane Réanimation Médicale
Pr. AMRAOUI Mohamed Chirurgie Générale
Pr. BARGACH Samir Gynécologie Obstétrique Pr. DRISSI KAMILI Med Nordine* Anesthésie Réanimation
Pr. EL MESNAOUI Abbes Chirurgie Générale
Pr. ESSAKALI HOUSSYNI Leila Oto-Rhino-Laryngologie
Pr. HDA Abdelhamid* Cardiologie Inspecteur du Service de Santé des FAR Pr. IBEN ATTYA ANDALOUSSI Ahmed Urologie
Pr. OUAZZANI CHAHDI Bahia Ophtalmologie
Pr. SEFIANI Abdelaziz Génétique
Pr. ZEGGWAGH Amine Ali Réanimation Médicale
DECEMBRE 1996
Pr. AMIL Touriya* Radiologie
Pr. BELKACEM Rachid Chirurgie Pédiatrie
Pr. BOULANOUAR Abdelkrim Ophtalmologie
Pr. EL ALAMI EL FARICHA EL Hassan Chirurgie Générale
Pr. GAOUZI Ahmed Pédiatrie
Pr. MAHFOUDI M’barek* Radiologie
Pr. OUZEDDOUN Naima Néphrologie
Pr. ZBIR EL Mehdi* Cardiologie DirecteurHôp.Mil. d’Instruction Med V Rabat
NOVEMBRE 1997
Pr. ALAMI Mohamed Hassan Gynécologie-Obstétrique
Pr. BEN SLIMANE Lounis Urologie
Pr. BIROUK Nazha Neurologie
Pr. ERREIMI Naima Pédiatrie
Pr. FELLAT Nadia Cardiologie
Pr. KADDOURI Noureddine Chirurgie Pédiatrique
Pr. KOUTANI Abdellatif Urologie
Pr. LAHLOU Mohamed Khalid Chirurgie Générale
Pr. MAHRAOUI CHAFIQ Pédiatrie
Pr. TOUFIQ Jallal Psychiatrie Directeur Hôp.Ar-razi Salé
Pr. YOUSFI MALKI Mounia Gynécologie Obstétrique
NOVEMBRE 1998
Pr. BENOMAR ALI Neurologie Doyen de la FMP Abulcassis
Pr. BOUGTAB Abdesslam Chirurgie Générale
Pr. ER RIHANI Hassan Oncologie Médicale
Pr. BENKIRANE Majid* Hématologie
JANVIER 2000
Pr. ABID Ahmed* Pneumo-phtisiologie
Pr. AIT OUAMAR Hassan Pédiatrie
Pr. BENJELLOUN Dakhama Badr.Sououd Pédiatrie
Pr. BOURKADI Jamal-Eddine Pneumo-phtisiologie Directeur Hôp. My Youssef Pr. CHARIF CHEFCHAOUNI Al Montacer Chirurgie Générale
Pr. ECHARRAB El Mahjoub Chirurgie Générale
Pr. EL FTOUH Mustapha Pneumo-phtisiologie
Pr. EL MOSTARCHID Brahim* Neurochirurgie
Pr. MAHMOUDI Abdelkrim* Anesthésie-Réanimation
Pr. TACHINANTE Rajae Anesthésie-Réanimation
Pr. TAZI MEZALEK Zoubida Médecine Interne
NOVEMBRE 2000
Pr. AIDI Saadia Neurologie
Pr. AJANA Fatima Zohra Gastro-Entérologie
Pr. BENAMR Said Chirurgie Générale
Pr. CHERTI Mohammed Cardiologie
Pr. ECH-CHERIF EL KETTANI Selma Anesthésie-Réanimation
Pr. EL HASSANI Amine Pédiatrie - Directeur Hôp.Cheikh Zaid
Pr. EL KHADER Khalid Urologie
Pr. EL MAGHRAOUI Abdellah* Rhumatologie
Pr. GHARBI Mohamed El Hassan Endocrinologie et Maladies Métaboliques
Pr. MDAGHRI ALAOUI Asmae Pédiatrie
Pr. ROUIMI Abdelhadi* Neurologie
DECEMBRE 2000
Pr.ZOHAIR ABDELLAH * ORL
Pr. BALKHI Hicham* Anesthésie-Réanimation
Pr. BENABDELJLIL Maria Neurologie
Pr. BENAMAR Loubna Néphrologie
Pr. BENAMOR Jouda Pneumo-phtisiologie
Pr. BENELBARHDADI Imane Gastro-Entérologie
Pr. BENNANI Rajae Cardiologie
Pr. BENOUACHANE Thami Pédiatrie
Pr. BEZZA Ahmed* Rhumatologie
Pr. BOUCHIKHI IDRISSI Med Larbi Anatomie
Pr. BOUMDIN El Hassane* Radiologie
Pr. CHAT Latifa Radiologie
Pr. DAALI Mustapha* Chirurgie Générale
Pr. DRISSI Sidi Mourad* Radiologie
Pr. EL HIJRI Ahmed Anesthésie-Réanimation
Pr. EL MAAQILI Moulay Rachid Neuro-Chirurgie
Pr. EL MADHI Tarik Chirurgie-Pédiatrique
Pr. EL OUNANI Mohamed Chirurgie Générale
Pr. ETTAIR Said Pédiatrie - Directeur Hôp. d’EnfantsRabat
Pr. GAZZAZ Miloudi* Neuro-Chirurgie
Pr. HRORA Abdelmalek Chirurgie Générale
Pr. KABIRI EL Hassane* Chirurgie Thoracique Pr. LAMRANI Moulay Omar Traumatologie Orthopédie
Pr. LEKEHAL Brahim Chirurgie Vasculaire Périphérique
Pr. MAHASSIN Fattouma* Médecine Interne
Pr. MEDARHRI Jalil Chirurgie Générale
Pr. MIKDAME Mohammed* Hématologie Clinique
Pr. MOHSINE Raouf Chirurgie Générale
Pr. NOUINI Yassine Urologie - Directeur Hôpital Ibn Sina
Pr. SABBAH Farid Chirurgie Générale
Pr. SEFIANI Yasser Chirurgie Vasculaire Périphérique Pr. TAOUFIQ BENCHEKROUN Soumia Pédiatrie
DECEMBRE 2002
Pr. AL BOUZIDI Abderrahmane* Anatomie Pathologique
Pr. AMEUR Ahmed * Urologie
Pr. AMRI Rachida Cardiologie
Pr. AOURARH Aziz* Gastro-Entérologie
Pr. BAMOU Youssef * Biochimie-Chimie
Pr. BELMEJDOUB Ghizlene* Endocrinologie et Maladies Métaboliques
Pr. BENZEKRI Laila Dermatologie
Pr. BENZZOUBEIR Nadia Gastro-Entérologie
Pr. BERNOUSSI Zakiya Anatomie Pathologique
Pr. BICHRA Mohamed Zakariya* Psychiatrie
Pr. CHOHO Abdelkrim * Chirurgie Générale
Pr. CHKIRATE Bouchra Pédiatrie
Pr. EL ALAMI EL Fellous Sidi Zouhair Chirurgie Pédiatrique
Pr. EL HAOURI Mohamed * Dermatologie
Pr. FILALI ADIB Abdelhai Gynécologie Obstétrique
Pr. HAJJI Zakia Ophtalmologie
Pr. IKEN Ali Urologie
Pr. JAAFAR Abdeloihab* Traumatologie Orthopédie
Pr. KRIOUILE Yamina Pédiatrie
Pr. MABROUK Hfid* Traumatologie Orthopédie
Pr. MOUSSAOUI RAHALI Driss* Gynécologie Obstétrique
Pr. OUJILAL Abdelilah Oto-Rhino-Laryngologie
Pr. RACHID Khalid * Traumatologie Orthopédie
Pr. RAISS Mohamed Chirurgie Générale
Pr. RGUIBI IDRISSI Sidi Mustapha* Pneumo-phtisiologie
Pr. RHOU Hakima Néphrologie
Pr. SIAH Samir * Anesthésie Réanimation
Pr. THIMOU Amal Pédiatrie
JANVIER 2004
Pr. ABDELLAH El Hassan Ophtalmologie
Pr. AMRANI Mariam Anatomie Pathologique
Pr. BENBOUZID Mohammed Anas Oto-Rhino-Laryngologie
Pr. BENKIRANE Ahmed* Gastro-Entérologie
Pr. BOULAADAS Malik Stomatologie et Chirurgie Maxillo-faciale
Pr. BOURAZZA Ahmed* Neurologie
Pr. CHAGAR Belkacem* Traumatologie Orthopédie
Pr. CHERRADI Nadia Anatomie Pathologique
Pr. EL FENNI Jamal* Radiologie
Pr. EL HANCHI ZAKI Gynécologie Obstétrique
Pr. EL KHORASSANI Mohamed Pédiatrie
Pr. EL YOUNASSI Badreddine* Cardiologie
Pr. HACHI Hafid Chirurgie Générale
Pr. JABOUIRIK Fatima Pédiatrie
Pr. KHARMAZ Mohamed Traumatologie Orthopédie
Pr. MOUGHIL Said Chirurgie Cardio-Vasculaire
Pr. OUBAAZ Abdelbarre * Ophtalmologie
Pr. TARIB Abdelilah* Pharmacie Clinique
Pr. TIJAMI Fouad Chirurgie Générale
Pr. ZARZUR Jamila Cardiologie
JANVIER 2005
Pr. ABBASSI Abdellah Chirurgie Réparatrice et Plastique Pr. AL KANDRY Sif Eddine* Chirurgie Générale
Pr. ALLALI Fadoua Rhumatologie
Pr. AMAZOUZI Abdellah Ophtalmologie
Pr. AZIZ Noureddine* Radiologie
Pr. BAHIRI Rachid Rhumatologie Directeur Hôp. Al Ayachi Salé
Pr. BARKAT Amina Pédiatrie
Pr. BENYASS Aatif Cardiologie
Pr. DOUDOUH Abderrahim* Biophysique
Pr. EL HAMZAOUI Sakina * Microbiologie
Pr. HAJJI Leila Cardiologie (mise en disponibilité
Pr. HESSISSEN Leila Pédiatrie
Pr. JIDAL Mohamed* Radiologie
Pr. LAAROUSSI Mohamed Chirurgie Cardio-vasculaire
Pr. LYAGOUBI Mohammed Parasitologie
Pr. RAGALA Abdelhak Gynécologie Obstétrique
Pr. SBIHI Souad Histo-Embryologie Cytogénétique
AVRIL 2006
Pr. ACHEMLAL Lahsen* Rhumatologie
Pr. AKJOUJ Said* Radiologie
Pr. BELMEKKI Abdelkader* Hématologie
Pr. BENCHEIKH Razika O.R.L
Pr. BIYI Abdelhamid* Biophysique
Pr. BOUHAFS Mohamed El Amine Chirurgie - Pédiatrique
Pr. BOULAHYA Abdellatif* Chirurgie Cardio – Vasculaire. Pr. CHENGUETI ANSARI Anas Gynécologie Obstétrique
Pr. DOGHMI Nawal Cardiologie
Pr. FELLAT Ibtissam Cardiologie
Pr. FAROUDY Mamoun Anesthésie Réanimation
Pr. HARMOUCHE Hicham Médecine Interne
Pr. HANAFI Sidi Mohamed* Anesthésie Réanimation
Pr. IDRISS LAHLOU Amine* Microbiologie
Pr. JROUNDI Laila Radiologie
Pr. KARMOUNI Tariq Urologie
Pr. KILI Amina Pédiatrie
Pr. KISRA Hassan Psychiatrie
Pr. KISRA Mounir Chirurgie – Pédiatrique
Pr. LAATIRIS Abdelkader* Pharmacie Galénique
Pr. LMIMOUNI Badreddine* Parasitologie
Pr. MANSOURI Hamid* Radiothérapie
Pr. OUANASS Abderrazzak Psychiatrie
Pr. SAFI Soumaya* Endocrinologie
Pr. SEKKAT Fatima Zahra Psychiatrie
Pr. SOUALHI Mouna Pneumo – Phtisiologie
Pr. TELLAL Saida* Biochimie
Pr. ZAHRAOUI Rachida Pneumo – Phtisiologie
DECEMBRE 2006
Pr SAIR Khalid Chirurgie générale Dir. Hôp.Av.Marrakech
OCTOBRE 2007
Pr. ABIDI Khalid Réanimation médicale
Pr. ACHACHI Leila Pneumo phtisiologie
Pr. ACHOUR Abdessamad* Chirurgie générale
Pr. AIT HOUSSA Mahdi * Chirurgie cardio vasculaire
Pr. AMHAJJI Larbi * Traumatologie orthopédie
Pr. AOUFI Sarra Parasitologie
Pr. BAITE Abdelouahed * Anesthésie réanimation Directeur ERSSM
Pr. BALOUCH Lhousaine * Biochimie-chimie
Pr. BOUTIMZINE Nourdine Ophtalmologie
Pr. CHERKAOUI Naoual * Pharmacie galénique
Pr. EHIRCHIOU Abdelkader * Chirurgie générale
Pr. EL BEKKALI Youssef * Chirurgie cardio-vasculaire
Pr. EL ABSI Mohamed Chirurgie générale
Pr. EL MOUSSAOUI Rachid Anesthésie réanimation
Pr. EL OMARI Fatima Psychiatrie
Pr. GHARIB Noureddine Chirurgie plastique et réparatrice
Pr. HADADI Khalid * Radiothérapie
Pr. ICHOU Mohamed * Oncologie médicale
Pr. ISMAILI Nadia Dermatologie
Pr. KEBDANI Tayeb Radiothérapie
Pr. LALAOUI SALIM Jaafar * Anesthésie réanimation
Pr. LOUZI Lhoussain * Microbiologie
Pr. MADANI Naoufel Réanimation médicale
Pr. MAHI Mohamed * Radiologie
Pr. MARC Karima Pneumo phtisiologie
Pr. MASRAR Azlarab Hématologie biologique
Pr. MRANI Saad * Virologie
Pr. OUZZIF Ez zohra * Biochimie-chimie
Pr. RABHI Monsef * Médecine interne
Pr. RADOUANE Bouchaib* Radiologie
Pr. SEFFAR Myriame Microbiologie
Pr. SEKHSOKH Yessine * Microbiologie
Pr. SIFAT Hassan * Radiothérapie
Pr. TABERKANET Mustafa * Chirurgie vasculaire périphérique
Pr. TACHFOUTI Samira Ophtalmologie
Pr. TAJDINE Mohammed Tariq* Chirurgie générale
Pr. TANANE Mansour * Traumatologie-orthopédie
Pr. TLIGUI Houssain Parasitologie
Pr. TOUATI Zakia Cardiologie
DECEMBRE 2008
Pr TAHIRI My El Hassan* Chirurgie Générale
MARS 2009
Pr. ABOUZAHIR Ali * Médecine interne
Pr. AGADR Aomar * Pédiatrie
Pr. AIT ALI Abdelmounaim * Chirurgie Générale Pr. AIT BENHADDOU El Hachmia Neurologie
Pr. AKHADDAR Ali * Neuro-chirurgie
Pr. ALLALI Nazik Radiologie
Pr. ARKHA Yassir Neuro-chirurgie Directeur Hôp.des Spécialités
Pr. BELYAMANI Lahcen* Anesthésie Réanimation
Pr. BJIJOU Younes Anatomie
Pr. BOUHSAIN Sanae * Biochimie-chimie
Pr. BOUI Mohammed * Dermatologie
Pr. BOUNAIM Ahmed * Chirurgie Générale
Pr. BOUSSOUGA Mostapha * Traumatologie-orthopédie
Pr. CHTATA Hassan Toufik * Chirurgie Vasculaire Périphérique
Pr. DOGHMI Kamal * Hématologie clinique
Pr. EL MALKI Hadj Omar Chirurgie Générale
Pr. EL OUENNASS Mostapha* Microbiologie
Pr. ENNIBI Khalid * Médecine interne
Pr. FATHI Khalid Gynécologie obstétrique
Pr. HASSIKOU Hasna * Rhumatologie
Pr. KABBAJ Nawal Gastro-entérologie
Pr. KABIRI Meryem Pédiatrie
Pr. KARBOUBI Lamya Pédiatrie
Pr. LAMSAOURI Jamal * Chimie Thérapeutique
Pr. MARMADE Lahcen Chirurgie Cardio-vasculaire
Pr. MESKINI Toufik Pédiatrie
Pr. MESSAOUDI Nezha * Hématologie biologique
Pr. MSSROURI Rahal Chirurgie Générale
Pr. NASSAR Ittimade Radiologie
Pr. OUKERRAJ Latifa Cardiologie
Pr. RHORFI Ismail Abderrahmani * Pneumo-Phtisiologie
OCTOBRE 2010
Pr. ALILOU Mustapha Anesthésie réanimation
Pr. AMEZIANE Taoufiq* Médecine Interne
Pr. BELAGUID Abdelaziz Physiologie
Pr. CHADLI Mariama* Microbiologie
Pr. CHEMSI Mohamed* Médecine Aéronautique
Pr. DAMI Abdellah* Biochimie- Chimie
Pr. DARBI Abdellatif* Radiologie
Pr. DENDANE Mohammed Anouar Chirurgie Pédiatrique
Pr. EL HAFIDI Naima Pédiatrie
Pr. EL KHARRAS Abdennasser* Radiologie
Pr. EL MAZOUZ Samir Chirurgie Plastique et Réparatrice
Pr. EL SAYEGH Hachem Urologie
Pr. ERRABIH Ikram Gastro-Entérologie
Pr. LAMALMI Najat Anatomie Pathologique
Pr. MOSADIK Ahlam Anesthésie Réanimation
Pr. MOUJAHID Mountassir* Chirurgie Générale
Pr. NAZIH Mouna* Hématologie
DECEMBRE 2010
Pr.ZNATI Kaoutar Anatomie Pathologique
MAI 2012
Pr. AMRANI Abdelouahed Chirurgie pédiatrique
Pr. ABOUELALAA Khalil * Anesthésie Réanimation
Pr. BENCHEBBA Driss * Traumatologie-orthopédie
Pr. DRISSI Mohamed * Anesthésie Réanimation
Pr. EL ALAOUI MHAMDI Mouna Chirurgie Générale Pr. EL KHATTABI Abdessadek * Médecine Interne Pr. EL OUAZZANI Hanane * Pneumophtisiologie
Pr. ER-RAJI Mounir Chirurgie Pédiatrique
Pr. JAHID Ahmed Anatomie Pathologique
Pr. MEHSSANI Jamal * Psychiatrie
Pr. RAISSOUNI Maha * Cardiologie
* Enseignants Militaires FEVRIER 2013
Pr.AHID Samir Pharmacologie
Pr.AIT EL CADI Mina Toxicologie
Pr.AMRANI HANCHI Laila Gastro-Entérologie
Pr.AMOR Mourad Anesthésie Réanimation
Pr.AWAB Almahdi Anesthésie Réanimation
Pr.BELAYACHI Jihane Réanimation Médicale
Pr.BELKHADIR Zakaria Houssain Anesthésie Réanimation
Pr.BENCHEKROUN Laila Biochimie-Chimie
Pr.BENKIRANE Souad Hématologie
Pr.BENNANA Ahmed* Informatique Pharmaceutique
Pr.BENSGHIR Mustapha * Anesthésie Réanimation
Pr.BENYAHIA Mohammed * Néphrologie
Pr.BOUATIA Mustapha Chimie Analytique et Bromatologie Pr.BOUABID Ahmed Salim* Traumatologie orthopédie
Pr BOUTARBOUCH Mahjouba Anatomie
Pr.CHAIB Ali * Cardiologie
Pr.DENDANE Tarek Réanimation Médicale
Pr.DINI Nouzha * Pédiatrie
Pr.ECH-CHERIF EL KETTANI Mohamed Ali Anesthésie Réanimation Pr.ECH-CHERIF EL KETTANI Najwa Radiologie
Pr.EL FATEMI NIZARE Neuro-chirurgie
Pr.EL GUERROUJ Hasnae Médecine Nucléaire
Pr.EL JAOUDI Rachid * Toxicologie
Pr.EL KABABRI Maria Pédiatrie
Pr.EL KHANNOUSSI Basma Anatomie Pathologique
Pr.EL KHLOUFI Samir Anatomie
Pr.EL KORAICHI Alae Anesthésie Réanimation
Pr.EN-NOUALI Hassane * Radiologie
Pr.ERRGUIG Laila Physiologie
Pr.FIKRI Meryem Radiologie
Pr.GHFIR Imade Médecine Nucléaire
Pr.IMANE Zineb Pédiatrie
Pr.IRAQI Hind Endocrinologie et maladies métaboliques
Pr.KABBAJ Hakima Microbiologie
Pr.KADIRI Mohamed * Psychiatrie
Pr.MAAMAR Mouna Fatima Zahra Médecine Interne
Pr.MEDDAH Bouchra Pharmacologie
Pr.MELHAOUI Adyl Neuro-chirurgie
Pr.MRABTI Hind Oncologie Médicale
Pr.NEJJARI Rachid Pharmacognosie
Pr.OUBEJJA Houda Chirugie Pédiatrique
Pr.OUKABLI Mohamed * Anatomie Pathologique
Pr.RAHALI Younes Pharmacie Galénique
Pr.RATBI Ilham Génétique
Pr.RAHMANI Mounia Neurologie
Pr.REDA Karim * Ophtalmologie
Pr.REGRAGUI Wafa Neurologie
Pr.RKAIN Hanan Physiologie
Pr.ROSTOM Samira Rhumatologie
Pr.ROUAS Lamiaa Anatomie Pathologique
Pr.ROUIBAA Fedoua * Gastro-Entérologie
Pr SALIHOUN Mouna Gastro-Entérologie
Pr.SAYAH Rochde Chirurgie Cardio-Vasculaire
Pr.SEDDIK Hassan * Gastro-Entérologie
Pr.ZERHOUNI Hicham Chirurgie Pédiatrique
AVRIL 2013
Pr.EL KHATIB MOHAMED KARIM * Stomatologie et Chirurgie Maxillo-faciale
MAI 2013
Pr.BOUSLIMAN Yassir Toxicologie
MARS 2014
Pr. ACHIR Abdellah Chirurgie Thoracique
Pr.BENCHAKROUN Mohammed * Traumatologie- Orthopédie
Pr.BOUCHIKH Mohammed Chirurgie Thoracique
Pr. EL KABBAJ Driss * Néphrologie
Pr. EL MACHTANI IDRISSI Samira * Biochimie-Chimie
Pr. HARDIZI Houyam Histologie- Embryologie-Cytogénétique
Pr. HASSANI Amale * Pédiatrie
Pr. HERRAK Laila Pneumologie
Pr. JANANE Abdellah * Urologie
Pr. JEAIDI Anass * Hématologie Biologique
Pr. KOUACH Jaouad* Gynécologie-Obstétrique
Pr. LEMNOUER Abdelhay* Microbiologie
Pr. MAKRAM Sanaa * Pharmacologie
Pr. OULAHYANE Rachid* Chirurgie Pédiatrique
Pr. RHISSASSI Mohamed Jaafar CCV
Pr. SABRY Mohamed* Cardiologie
Pr. SEKKACH Youssef* Médecine Interne
Pr. TAZI MOUKHA Zakia Gynécologie-Obstétrique
AVRIL 2014
PROFESSEURS AGREGES :
DECEMBRE 2014
Pr. ABILKASSEM Rachid* Pédiatrie
Pr. AIT BOUGHIMA Fadila Médecine Légale
Pr. BEKKALI Hicham * Anesthésie-Réanimation
Pr. BENAZZOU Salma Chirurgie Maxillo-Faciale
Pr. BOUABDELLAH Mounya Biochimie-Chimie
Pr. BOUCHRIK Mourad* Parasitologie
Pr. DERRAJI Soufiane* Pharmacie Clinique
Pr. DOBLALI Taoufik* Microbiologie
Pr. EL AYOUBI EL IDRISSI Ali Anatomie
Pr. EL GHADBANE Abdedaim Hatim* Anesthésie-Réanimation
Pr. EL MARJANY Mohammed* Radiothérapie
Pr. FEJJAL Nawfal Chirurgie Réparatrice et Plastique
Pr. JAHIDI Mohamed* O.R.L
Pr. LAKHAL Zouhair* Cardiologie
Pr. OUDGHIRI NEZHA Anesthésie-Réanimation
Pr. RAMI Mohamed Chirurgie Pédiatrique
Pr. SABIR Maria Psychiatrie
Pr. SBAI IDRISSI Karim* Médecine préventive, santé publique et Hyg.
AOUT 2015
Pr. MEZIANE Meryem Dermatologie
Pr. TAHRI Latifa Rhumatologie
JANVIER 2016
Pr. BENKABBOU Amine Chirurgie Générale
Pr. EL ASRI Fouad* Ophtalmologie
Pr. ERRAMI Noureddine* O.R.L
Pr. NITASSI Sophia O.R.L
JUIN 2017
Pr. ABI Rachid* Microbiologie
Pr. ASFALOU Ilyasse* Cardiologie
Pr. BOUAYTI El Arbi* Médecine préventive, santé publique et Hyg.
Pr. BOUTAYEB Saber Oncologie Médicale
Pr. EL GHISSASSI Ibrahim Oncologie Médicale
Pr. OURAINI Saloua* O.R.L
Pr. RAZINE Rachid Médecine préventive, santé publique et Hyg.
Pr. ZRARA Abdelhamid* Immunologie
2 - ENSEIGNANTS-CHERCHEURS SCIENTIFIQUES
PROFESSEURS/Prs. HABILITES
Pr. ABOUDRAR Saadia Physiologie
Pr. ALAMI OUHABI Naima Biochimie-chimie
Pr. ALAOUI KATIM Pharmacologie
Pr. ALAOUI SLIMANI Lalla Naïma Histologie-Embryologie
Pr. ANSAR M’hammed Chimie Organique et Pharmacie Chimique
Pr .BARKIYOU Malika Histologie-Embryologie
Pr. BOUHOUCHE Ahmed Génétique Humaine
Pr. BOUKLOUZE Abdelaziz Applications Pharmaceutiques Pr. CHAHED OUAZZANI Lalla Chadia Biochimie-chimie
Pr. DAKKA Taoufiq Physiologie
Pr. FAOUZI Moulay El Abbes Pharmacologie
Pr. IBRAHIMI Azeddine Biologie moléculaire/Biotechnologie
Pr. KHANFRI Jamal Eddine Biologie
Pr. OULAD BOUYAHYA IDRISSI Med Chimie Organique
Pr. REDHA Ahlam Chimie
Pr. TOUATI Driss Pharmacognosie
Pr. ZAHIDI Ahmed Pharmacologie
Mise à jour le 10/10/2018 Khaled Abdellah
A ma très chère grande mère
A cette douce personne qui m’a toujours montré la meilleure des voix,
j’aurai aimé partager ce moment avec toi, j’aurai aimé te voir sourire une
dernière fois, j’aurai aimé me blottir entre tes bras une dernière fois , mais
hélas dieux on a décidé autrement , je prie le tout puissant pour
t’accueillir dans son paradis éternelle.
A ma mère lala Boumalek Fatima
Tu représentes pour moi le symbole de la bonté par excellence, la source de
tendresse et l’exemple du dévouement qui n’a pas cessé de m’encourager et
de prier pour moi.
Ta prière et ta bénédiction m’ont été d’un grand secours pour mener à
bien mes études.
Aucune dédicace ne saurait être assez éloquente pour exprimer ce que tu
mérites pour tous les sacrifices que tu n’as cessé de me donner depuis ma
naissance, durant mon enfance et même à l’âge adulte.
Tu as fait plus qu’une mère puisse faire pour que ces enfants suivent le
bon chemin dans leur vie et leurs études.
Je te dédie ce travail en témoignage de mon profond amour. Puisse Dieu,
le tout puissant, te préserver et t’accorder santé, longue vie et bonheur.
A mon père que dieux ait pitié de son âme Baaddouch mouhamed
Aucun mot ne pourra exprimer ma grande tristesse en ton absence…
Ton visage gai et souriant…
Ta tendresse infinie…
Et ton amour incomparable…
Resteront à jamais gravés dans mon cœur…
Je te remercie pour tous les beaux moments que nous avons partagé en
famille…
Je te remercie pour m’avoir appris à prendre des décisions dans la vie…
Je te remercie pour ton grand amour…
Tu me manques beaucoup papa…
J’aurai aimé que tu sois à mes côtés ce jour…
Mais le destin en a décidé autrement…
J’espère que tu es fier de moi papa…
Je t’aime…
A mes freres
Said Baaddouch ,abedali Baaddouch, mustapha Baaddouche
Aucune dédicace ne pourrait traduire ma gratitude et ma profonde
reconnaissance et mon amour. Je vous dédie ce travail comme témoignage
de mon respect et mon amour éternel.
A ma grande sœur Khadija Baaddouch et rekayia Baaddouch
Ma meilleure amie ma confidente Les mots ne pourraient guère exprimer
l’attachement, l’amour et l’affection que je porte pour toi. Mon ange
gardien et mon fidèle compagnon dans les moments les plus délicats de
cette vie. Tu as toujours cru en moi, tu as su me redonner du courage
dans les moments les plus difficiles, je t’aime ma sœur.
A ma famille ben lmouden et Boumalek
Je vous dédie ce travail modeste pour exprimer ma gratitude
A mes amis Yassine Merjan , faycal benssassi ,Hamid maydoun,Anas
Moukhlisse.khalid,hakim…etc
Grace à vous les difficultés de la vie m’ont paru facile, grâce a vous j’ai
regagné le sourire quand j’étais mal, grâce à vous j’ai su supporter toutes
A mon oncle Haj mouhamed boumalek et son marie lala keltoum
Veuillez trouver dans ce modeste travail l’expression de mon affection la
plus sincère .
A ma deuxieme mere
Madam derii Aicha et latifa habach .
Vous images et vous sourire étaient et resterez toujours devant mes yeux.
J’aurais tant souhaité vous avoir à mes côtés, mais Dieu en a voulu
autrement.
A mon amie Oumaima Elmidaoui
Ma meilleure amie, ma sœur nulle mots ne saurait exprimer ce que je
ressens, tu as toujours été là pour moi et moi pour toi, on a escaladé les
marches de la réussite pas à pas, on trébuchait, on tombait certes mais il
y avait toujours ta main tendue envers moi qui me soutenait qui me
redonnait cette joie de vivre,
Je te serai à tous jamais reconnaissant.
A mon ami et frère yassine
Depuis le premier jour j’ai su que tu seras mon compagnon d’arme, ta
sagesse, ta tendresse, et ton sens d’amitié m’ont redonné fois en ce monde,
j’espère qu’on sera les meilleurs amis pour toujours dans cette vie et la
prochaine
A Notre Maître et Président de Thèse
Monsieur Mimoun ZOUHDI
Professeur de Microbiologie
Vous nous avez fait le grand honneur d’accepter la présidence du jury de
cette thèse et nous vous remercions de la confiance que vous avez bien
voulu témoigner.
Nous avons eu de la chance de compter parmi vos étudiants et de profiter
de l’étendue de votre savoir. Nous ne saurons jamais vous exprimer notre
profonde gratitude.
Vos remarquables qualités humaines et professionnelles ont toujours
suscité notre profonde admiration.
Nous vous prions de trouver dans ce travail le témoignage de notre
reconnaissance et l’assurance de nos sentiments respectueux.
A Notre Maître et Rapporteur de Thèse
Monsieur Yassine SEKHSOKH
Professeur de Microbiologie
Nous tenons à vous déclarer nos remerciements les plus sincères pour
avoir accepté de diriger ce travail et avoir vérifié à son élaboration avec
patience et disponibilité.
Votre dévouement au travail, votre modestie et votre gentillesse imposent
le respect et représentent le modèle que nous serons toujours heureux de
suivre. Mais au-delà de tous les mots de remerciements que nous vous
adressons, nous voudrons louer en vous votre amabilité, votre courtoisie et
votre générosité. Ce fut très agréable de travailler avec vous pendant cette
période.
Puisse ce travail être à la hauteur de la confiance que vous nous avez
accordée.
A Notre Maître et Juge de Thèse
Monsieur Ahmed GAOUZI
Professeur de Pédiatrie
Nous sommes très heureux de l’honneur que vous nous faites en
acceptant de juger notre travail.
Votre présence est pour nous, l’occasion de vous exprimer notre
admiration de votre grande compétence professionnelle et de votre
généreuse sympathie.
A Notre Maître et Juge de Thèse
Madame Saida TELLAL
Professeur de Biochimie
Vous nous faites un immense plaisir en acceptant de juger notre thèse.
Qu’il nous soit permis de témoigner à travers ces quelques lignes notre
admiration à la valeur de votre compétence, votre rigueur ainsi que votre
gentillesse, votre sympathie et votre dynamisme qui demeureront pour
nous le meilleur exemple.
Que ce travail soit une occasion de vous exprimer notre gratitude, de
respect et d’admiration les plus sincères.
Abréviations
A/E : Attachement/Effacement ADN : Acide désoxyribonucléique ADN : Acide désoxyribonucléique
AEEC : Attaching and Effacing E. coli
Afssa : Agence française de sécurité sanitaire
ANSES : Agence nationale de la sécurité sanitaire de l’alimentation, de l’environnement et du travail
ARN : Acide ribonucléique
AST3 : Appareil de sécrétion de type III
CNR :Centre national de référence
EA : Éthanolamine
ECP : E. coli common pilus
EHEC : Escherichia.coli entérohémorragique ELISA : Enzyme-linked Immunosorbent Assay
EPEC : Escherichia.coli entéropathogène Gb3 : Globotriasoylcéramide
Gb4 : Globotétraosylcéramide
HCP : Hemorrhagic coli pilus
HPA : Hydroxypropionaldehyde
InVS : Institut national de Veille Sanitaire
LEE : Locus d’effacement des entérocytes
LPS : Lipopolysaccharide
MLVA : Multiple locus variable number
ORF : open reading frame
PCR : Réaction de polymerisation en chaîne (Polymerase Chain Reaction). PTT : Purpura thrombotique thrombocytopénique
RE : Réticulum endoplasmique
rRNA :Ribosomal ribonucleic acid
SHU : Syndrome Hémolytique et Urémique SNC : Systhéme nerveuxcentrale
STEC : Escherichia.coli producteur de Shiga toxines Stx : Gène codant la Shiga-toxine
TIAC : Toxi-infection alimentaire collective
Liste des figures
Figure 1: Représentation schématique de la structure d‘E. coli ... 9 Figure 2: Induction de la production des Shiga-toxines Stx1 et Stx2, adaptée de Mellies &
Lorenzen (2014) ... 11
Figure 3: Structure (A) et mode d’action des Shiga-toxines (B) , adaptée de Bryan et al.
(2015); Melton-Celsa (2014). La toxine Stx, composée d’une sous-unité A et d’un pentamère de sous-unités B, se fixe au récepteur Gb3 et est internalisée dans l’endosome. Le complexe Stx/Gb3 migre par un transport rétrograde vers l’appareil de Golgi puis le réticulum endoplasmique dans lequel le peptide A1 est libéré pour atteindre les ribosomes et engendrer un arrêt de la synthèse protéique ... 13
Figure 4: Organisation génétique du locus d‘effacement des entérocytes (Ritchie and
Waldor, 2005) ... 15
Figure 5: Représentation schématique de l‘assemblage du système de sécrétion de type III
chez les EPEC (Sekiya et al., 2001) ... 18
Figure 6: Représentation schématique du système de sécrétion de type III , exprimé par les
EHEC et C. rodentium (Pallen et al., 2005) ... 18
Figure 7: Mécanisme de pathogénicité des E. coli entéropathogènes et entérohémorragiques (Croxen and Finlay, 2010) ... 19
Figure 8: Mode de transmission des EHEC à partir du réservoir animal, adaptée de
Fairbrother et al. (2006)[116]. La transmission des EHEC par l’alimentation représente la principale source d’infection pour l’Homme. La transmission entre personnes qui peut être observée en milieu familial ainsi que le contact direct entre l’Homme et les animaux de la ferme constituent également des sources d’infection ... 30
Figure 9: Surveillance du SHU chez les enfants de moins de 15 ans en France en 2015. ... 35 Figure 10: Répartition départementale des souche de EHEC isolées en 2017 (n=250) sur le
Figure 11: Principales étapes du processus infectieux des E. coli enterohémorragiques. ... 42 Figure 12: Adhésion des EHEC aux cellules épithéliales intestinales et formation des
lésions A/E ... 43
Figure 13: Diagnostic d’une infection à EHEC ... 51 Figure 14: Principe de mise en évidence des EHEC dans les selles ... 53 Figure 15: Aspect des colonies d' Escherichia coli O157 : H7 Colonies sorbitol – sur
milieu SMAC – céfixime-tellurite ; à gauche, d' Escherichia coli sorbitol positif à droite ... 54
Figure 16: Pulsotypes d’E. coli O104:H4 [digestion enzymatique par NotI] ... 55 Figure 17: Biopsie colique d’un patient porteur d’une infection à Escherichia coli 0157 :
Liste des tableaux
Tableau I: Résumé des principales épidémies à EHEC dans le monde entre 1998-2014 ... 6 Tableau II: Principaux critères biochimiques différentiels des espèces du genre
Escherichia (d‘après Grimont, 1987) ... 8
Tableau III: Protéines sécrétées par le système de sécrétion de type III par les E.coli
O157:H7 et leurs activités (d‘après Stevens and Frankel, 2014) ... 16
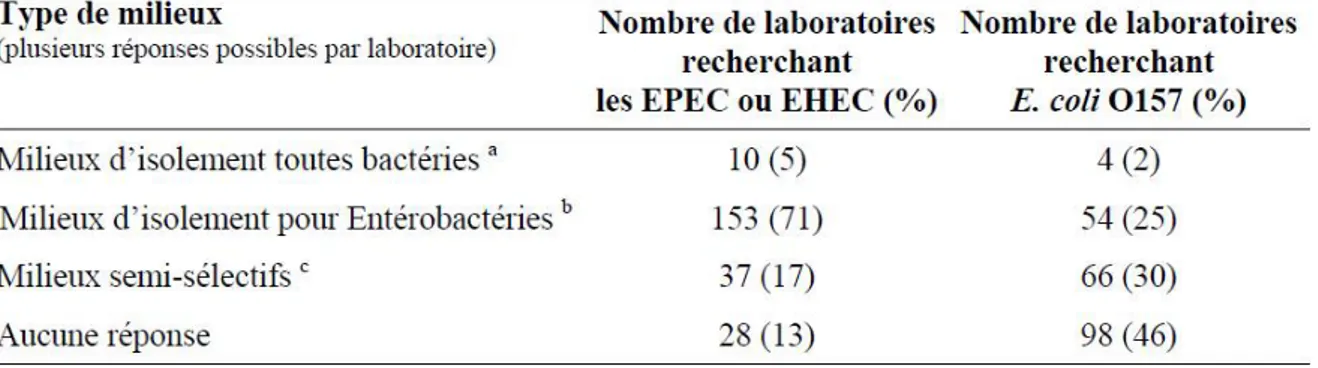
Tableau IV: Milieux utilisés pour la recherche des EPEC ou EHEC et pour la recherche de
E. coli O157 par les 215 laboratoires répondants... 26
Tableau V : Pathovar entérique : résultats des experts ... 28 Tableau VI : Nombre (%) de TIAC déclarées par danger, en fonction du niveau
d’identification de l’agent et del’aliment, et nombre de TIAC retenues pour l’analyse sur la période 2006-2015 ... 32
Tableau VII: Séquences des amorces nucléotidiques permettant la détection spécifique des
I. Introduction ...2 II. Historique d’Escherichia coli entérohémorragique ...4 III. Epidémiologie ...8
1. Agent pathogène EHEC ...8 1.1 Taxonomie ...8 1.2 Morphologie ...9 1.3 Facteurs de virulence des EHEC ...9 1.3.1 Shiga-toxines ... 10 1.3.1.1 Phages stx ... 10 1.3.1.2 Structure et mode d’action des Shiga-toxines ... 12 1.3.1.3 Sous-types de Shiga-toxines ... 14 1.3.2 Locus d’effacement des entérocytes ... 15 1.4 Autres facteurs de virulence potentiels des EHEC ... 23 1.4.1 Plasmide de virulence des EHEC ... 23 1.4.2 îlots génomiques ... 25 1.5 Caractères culturaux ... 25 1.6 Caractères Biochimiques ... 27 1.7 Caractères antigéniques ... 27 2. Réservoir et modes de transmission ... 29 3. Réceptivité et et Facteurs favorisants ... 31 4. Aspects épidémiologiques ... 34 5. Répartition géographique ... 37
IV. Physiopathologie des infections à Escherichia coli entérohémorragique ... 42
2. Action des Shiga-toxines au niveau des cellules cibles ... 44 3. Rôle des Shiga-toxines dans la physiopathologie du SHU . ... 44
V. Aspects cliniques ... 47
1. Colite hémorragique ... 47 2. Syndrome hémolytique et urémique (SHU) ... 47 3. Purpura Thrombotique Thrombocytopénique (PTT) ... 48
VI. Diagnostic ... 51
1. Prélèvements ... 52 2. Culture ... 52 2.1 Isolement et caractérisation des souches EHEC de sérotype O157:H7 ... 53 2.2 Isolement et caractérisation des souches EHEC de sérotype non O157 ... 54 3. Mise en évidence des toxines et des gènes de virulence. ... 55 3.1 Effet cytopathogène ... 55 3.2 Méthodes moléculaires ... 56 3.3 Tests immunologiques ... 57 3.4 Diagnostic sérologique des infections à EHEC... 57 3.5 Mise en évidance des autres pathovars d’Escherichia coli ... 58
VII. Traitement... 60 VIII. Prévention ... 71 Conclusion ... 73 Résumés ... 75 Références ... 79
1
2
I. Introduction
Escherichia coli est un Bacille à Gram négatif, aéro-anaérobie facultatif, oxydase négative, mesurant de 2 à 4 μm de long et d’un diamètre d’environ 0,6 μm. E. coli est une bactérie normalement présente parmi la microflore digestive de l’Homme et des animaux à sang chaud. Mais certaines souches d’E. coli sont pathogènes car elles ont acquis des facteurs de virulence. Sur la base des signes cliniques observés chez les malades, les souches d’E. coli pathogènes sont regroupées en pathovars (ou pathotypes) parmi lesquels les E. coli entérohémorragiques ou EHEC (enterohemorrhagic E. coli) [1]. La virulence des EHEC est étroitement liée a la production d'une toxine appelee shigatoxine (Stx). Bien qu'associée le plus souvent a de nombreux autres facteurs de virulence, notamment ceux caractéristiques des E. coli enteropathogenes (EPEC) dont le gène eae du locus LEE (locus of enterocytes effacement), seule la mise en évidence de la toxine ou de ces gènes permet d'affirmer que l'on est en présence d'un EHEC. [2]
Les EHEC sont responsables chez l’homme de troubles variés allant d’une simple diarrhée aqueuse bénigne à une colite hémorragique pouvant évoluer vers des formes graves telles que le syndrome hémolytique et urémique (SHU) chez les jeunes enfants et le purpura thrombotique thrombocytopénique chez l’adulte. Le réservoir de ces bactéries est majoritairement le tube digestif des ruminants : la transmission à l’homme se fait principalement par la consommation d’aliments insuffisamment cuits (viande de boeuf notamment), l’eau contaminée, le contact direct avec des animaux ou avec des personnes infectées.[3]
Enfin, en raison de l'origine le plus souvent alimentaire des infections a EHEC, de leur évolution parfois fatale et de leur risque potentiellement epidemique, la detection d'EHEC, en particulier lorsqu'ils sont responsables de SHU, peut conduire a la mise en œuvre d'une enquête diligentée par l'InVS afin d'identifier la source de contamination.[4]
Notre travail consistera dans une première partie a développer l’épidémiologie d’E.coli entérohémorragique, Nous traitons dans une deuxième partie le diagnostic, traitement et prévention.
3
Historique d’Escherichia coli
entérohémorragique
4
II. Historique d’Escherichia coli entérohémorragique
La bactérie Escherichia coli a été décrite pour la première fois en 1885 après avoir été isoléedans des selles de nourrissons par l’allemand Theodor Escherich. Son nom actuel lui est ensuite donné en 1919 par Castellani et Chambers [5].
Des souches particulières d’Escherichia coli pathogènes ont été décrites pour la première fois en 1982, lors de deux épidémies survenues aux Etats-Unis (dans l’Oregon puis trois mois plus tard dans le Michigan) suite à la consommation de hamburgers contaminés et insuffisamment cuits. Les patients atteints présentant une colite hémorragique, ces souches particulières ont été dénommées Escherichia coli entérohémorragiques (EHEC).[6]
En 1983 Karmali a mit en évidence dans des selles d’enfants atteints du syndrome hémolytique et urémique (SHU) des souches d’E. Coli produisant une toxine active sur les cellules Véro (cellules de rein de singe vert d’Afrique), appelée vérotoxine ou Shiga toxine .parmi ces souches on trouve l’E .coli O157 :H7. [7] [8]
En 1985, la relation entre la présence d’E. coli O157:H7 produisant des Shiga-toxines dans les selles d’enfants et les signes cliniques, i.e. les colites hémorragiques et le SHU, est établie. [8]
Ainsi, deux observations microbiologiques et cliniques clés, l’une basée sur une bactérie E. coli de sérotype rare et l’autre basée sur la production d’une cytotoxine spécifique, ont conduit à la reconnaissance d’une nouvelle classe d’agents pathogènes entériques responsable d’une maladie caractérisée par des signes intestinaux et rénaux. [9]
la toxiinfection en 1996 au Japon, provoquée par une souche STEC O157:H7 à partir de jeunes pousses de radis, qui avait causé près de 10000 malades et 12 décès.[10] Des viandes hachées en France ont été à l’origine d’infections par Escherichia coli O157:H7, en mars 2008 puis en juillet 2011.les aliments en cause contaminateurs de cette bactérie redoutable sont très divers dans le monde. l’E. Coli O104:H4 (E.coli entérohémorragique (EHEC) est une autre souche, redoutable, décelée en juin 2011, jugulée en juillet, 2011, décelée en Europe du Nord - Allemagne), puis en France.[11][12]
5
une épidémie a frappé l’Allemagne (3 816 cas de colite hémorragique, 54 décès, 845 SHU dont une centaine chez des enfants)et à une moindre échelle en France 7 étaient due à un E. coli rare, 0104 :H4, particulièrement virulent car producteur de Stx, résistant aux antibiotiques et entéroagrégant.[13][14]
En Allemagne, une épidémie de grande ampleur a été rapportée suite à la consommation de graines germées contaminées par E. coli O104 :H4. Il s’agissait d’une souche pathogène émergente considérée comme non pathogène selon la définition de l’Anses. Peu de temps après (en juin 2011), quinze cas de SHU ou de diarrhée sanglante ont été signalés en France. Des graines germées contaminées par la même souche d’E. coli O104 :H4 étaient à l’origine de la contamination.[14]
Des infections humaines causées par des souches de STEC sont signalées dans le monde entier. à la fois en tant que cas sporadiques et associés à une éclosion. La notification de Les infections par des STEC humains sont obligatoires dans la plupart des États membres de l’UE. En 2015, 5901 cas d'infection par les STEC ont été confirmés dans l'UE.[15]
6
7
8
III. Epidémiologie
1. Agent pathogène EHEC
1.1 Taxonomie
Les E. coli sont des bacilles à Gram négatif appartenant à la famille des Enterobacteriaceae. Ce sont des bactéries aérobies anaérobies facultatives, mésophiles et asporulées se développant sur des milieux pauvres, fermentant les nitrates et ne possédant pas d‘oxydase . [17]
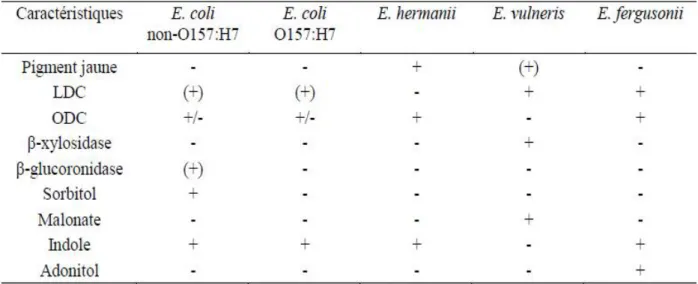
Commensale, E. coli est l‘espèce prédominante de la flore aéroanaérobie facultative du tube digestif des mammifères à sang chaud tel que l‘Homme. Cette bactérie est l‘une des premières colonisatrices du tractus gastro-intestinal du nouveau-né. Son implantation dans les premières heures suivant l‘accouchement, notamment au niveau du côlon est maintenue durant toute la vie du sujet. D‘autres espèces appartenant au genre Escherichia ont été décrites dans la littérature.[18] Il s‘agit d‘Escherichia albertii ; E. fergusonii ; E. hermannii et E vulneris. Elles se différencient par leurs capacités métaboliques (Tableau II).
Tableau II: Principaux critères biochimiques différentiels des espèces du genre Escherichia (d‘après Grimont, 1987). [17]
(+) positif pour la majorité des souches ; +/- positif ou négatif selon les souches ; LC Lysine Décarboxylase, ODC Ornithine Décarboxylase.
9
1.2 Morphologie
Escherichia coli ou colibacille est une bactérie asporulée mesurant 2 à 4 μ de long sur 0,4 à 0,6 μ de large. C’est une bactérie fine et allongée à extrémités arrondies, mobile grâce à une ciliature péritriche. Ce germe non exigeant, sur gélose ordinaire donne des colonies lisses, brillantes et homogènes.[19]
Figure 1: Représentation schématique de la structure d‘E. coli.[19]
1.3 Facteurs de virulence des EHEC
La virulence des EHEC est associée à la présence de toxines appelées Shiga-toxines (Stx) et à la présence du gène eae, responsable des lésions d’attachement-effacement au niveau du côlon et du caecum. [20]
La liste des facteurs de virulence et des mécanismes impliqués dans le pouvoir pathogène des souches EHEC n’est pas encore complètement connue. En effet, bien que la production de Stx et la colonisation de la muqueuse colique soient nécessaires, elles ne sont pas suffisantes pour induire maladie chez l’homme. De nombreux autres facteurs de virulence potentiels ont été décrits [20] [21] [22].6
10
1.3.1 Shiga-toxines
Les Shiga-toxines (Stx) sont considérées comme le principal facteur de virulence des EHEC. Les toxines Stx sont également connues sous le nom de Vérotoxines en raison de leur cytotoxicité sur les lignées cellulaires Vero dérivant de cellules épithéliales rénales de singe africain. La pathogénicité des EHEC dépend de la production des toxines Stx qui sont responsables des effets cliniques, notamment les colites hémorragiques et le SHU. Les toxines Stx sont des exotoxines présentant une parenté avec la toxine produite par Shigella dysenteriae de type I. Elles ont été classées en deux groupes majeurs : Stx1 et Stx2. Pour chaque groupe de toxine Stx, plusieurs variants ont été identifiés.[23]
1.3.1.1 Phages stx
Les gènes stx, codant les Shiga-toxines, sont portés sur un opéron localisé sur le génome d’un phage inductible et lysogénique similaire au bactériophage λ, appelé phage stx. Les gènes codant Stx1 et Stx2 sont portés par des phages distincts ayant un processus d’induction similaire. [24]
Au stade lysogénique, le phage stx est intégré dans le chromosome bactérien sous la forme d’un prophage et l’expression des gènes stx est inhibée. Dans le chromosome bactérien, les phages stx peuvent s’insérer au niveau d’un site préférentiel unique ou d’autres sites d’intégration secondaires.[25] Dans certaines conditions, le prophage est induit (stade lytique) et les gènes portés par le phage sont exprimés. Ainsi, l’expression des gènes stx est sous le contrôle du promoteur du phage et de l’antiterminateur Q [26] [27].
L’induction des prophages stx, et donc la production de Stx, est contrôlée par des molécules signal, dont RecA, un régulateur du système SOS (Figure 2).[24]
11
Figure 2: Induction de la production des Shiga-toxines Stx1 et Stx2, adaptée de Mellies & Lorenzen (2014).[24]
Par exemple, lors d’une infection chez l’Homme, un stress oxydatif qui survient au niveau de l’intestin participe à l’activation de RecA et donc à l’induction des prophages stx [28]
Le traitement des infections humaines à EHEC par des antibiotiques ciblant la synthèse d’ADN peut avoir de graves conséquences cliniques en raison de l’effet de certains antibiotiques sur l’induction du phage stx et la production de Stx. [29]
Par ailleurs, l’adrénaline, la noradrénaline ou l’auto-inducteur 3 (AI-3), une molécule du quorum sensing produite par les bactéries du microbiot intestinal, activent RecA par un mécanisme dépendant du système Qse (qorum sensing E. coli) [30] [31]
D’autres facteurs comme la carence en fer et la présence d’éthanolamine peuvent favoriser l’expression des gènes stx1 et stx2, respectivement. [32] [24]
Le prophage stx au stade lysogénique module l’expression de certains gènes de la bactérie hôte, comme par exemple une augmentation de l’expression de gènes impliqués dans la mobilité ou l’inhibition de l’expression de l’appareil de sécrétion de type III .[33] [34]
12
Cette inhibition est due à une région régulatrice présente sur le génome du phage stx et principalement retrouvée chez les souches de sérogroupe O157 isolées de cas cliniques. Chez les souches O157, la présence d’une région codant pour l’antiterminateur transcriptionnel Q933 a été associée à une expression élevée des gènes stx [35] .
De plus, les phages stx peuvent réguler différentes étapes de l’interaction des EHEC avec l’épithélium intestinal, comme l’augmentation de l’expression de la nucléoline, un des récepteurs de l’intimine.[36]
Les phages stx représentent des éléments génétiques mobiles et sont considérés comme vecteurs des gènes stx. La transmission des phages stx peut avoir lieu au cours du transit intestinal mais aussi dans l’eau, les aliments, via les fèces ou encore les biofilms.[37] [38]
1.3.1.2 Structure et mode d’action des Shiga-toxines
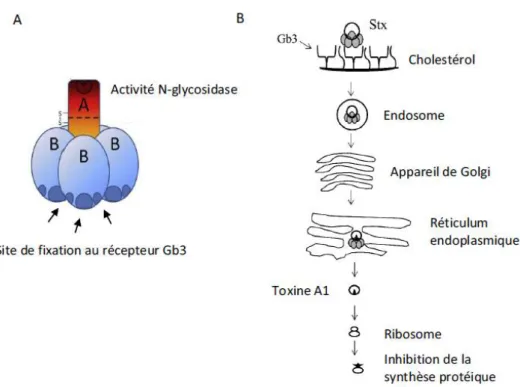
Les toxines Stx sont composées d’une sous-unité A liée de façon non covalente à 5 unités B identiques formant un pentamère (protéine de type AB5) (Figure 3). La sous-unité A est composée de deux parties, A1 et A2, reliées entre elles par un pont disulfure. Le peptide A1 possède l’activité enzymatique N-glycosidase alors que les sous-unités B permettent l’interaction de la toxine avec son récepteur, le globotriaosylcéramide Gb3 présent à la surface des cellules endothéliales de l’intestin, du rein et du cerveau chez l’homme.[39]
Pour exercer son activité N-glycosidase, le peptide A1 doit être libéré dans le cytosol de la cellule cible. Bien que la protéine Stx2 ne présente que 60% d’homologie avec Stx1, les deux toxines ont un mode d’action identique.[40] [41]
13
Figure 3: Structure (A) et mode d’action des Shiga-toxines (B) , adaptée de Bryan et al. (2015); Melton-Celsa (2014). La toxine Stx, composée d’une unité A et d’un pentamère de
sous-unités B, se fixe au récepteur Gb3 et est internalisée dans l’endosome. Le complexe Stx/Gb3 migre par un transport rétrograde vers l’appareil de Golgi puis le réticulum endoplasmique dans lequel le peptide A1 est libéré pour atteindre les ribosomes et engendrer un arrêt de la
synthèse protéique.[42]
Au niveau du site de colonisation intestinal des EHEC, les toxines Stx sont relarguées lors de la lyse bactérienne et rejoignent la circulation sanguine par translocation des cellules épithéliales intestinales, dépourvues de Gb3, du pôle apical vers le pôle basal sans activité cytotoxique. Les toxines Stx atteignent les cellules endothéliales cibles du côlon, du rein et du cerveau et se fixent sur le récepteur Gb3.[43]
14
Il existe deux sites de fixation de la sous-unité B qui ont une forte affinité avec le récepteur Gb3 alors que le troisième site de fixation semble être important pour le recrutement des récepteurs à la surface des cellules. Après fixation de la toxine au récepteur Gb3, le complexe Stx/Gb3 est internalisé dans la cellule cible par un mécanisme d’endocytose puis fusionne avec l’endosome (Figure 3). Le complexe rejoint l’appareil de Golgi puis le réticulum endoplasmique (RE) par un transport rétrograde.[41]
Dans le RE, le pont disulfure entre les peptides A1 et A2 est réduit et seul le peptide A1 est libéré et quitte le RE pour atteindre l’enveloppe nucléaire puis les ribosomes cibles (Figure 3). L’activité N-glycosidase du peptide A1 retire un résidu adénine de l’ARN ribosomique 28S du ribosome 60S, ce qui entraine la dissociation du ribosome avec le facteur d’élongation 1, conduisant à l’inhibition de la synthèse protéique.[44] Il a également été montré que les toxines Stx sont capables d’induire l’apoptose de différents types cellulaires.[45]
1.3.1.3 Sous-types de Shiga-toxines
Comme indiqué ci-dessus, deux grands groupes de toxines, Stx1 et Stx2, et de nombreux variants ont été identifiés. Ils se distinguent par leur différence d’activité biologique, de réactivité immunologique, de reconnaissance de leur récepteur au niveau des cellules cibles et de leur capacité à être activés par l’élastase du mucus intestinal.[46]
En 2012, Scheutz et al. ont développé un système basé sur les séquences des toxines Stx afin de standardiser la nomenclature des différents variants.[47] Le groupe des toxines Stx1 inclut les variants Stx1a, Stx1c et Stx1d, alors que celui des toxines Stx2 est plus hétérogène et comprend les variants Stx2a, Stx2b, Stx2c, Stx2d, Stx2e, Stx2f et Stx2g. Le type de variant reflète à la fois l’origine des souches et leur pouvoir pathogène. Certains variants semblent associés à des hôtes spécifiques et pourraient influencer directement la virulence des souches.[48]
Par exemple, les variants Stx2a, Stx2c et Stx2d ont été fréquemment associés à des souches hautement pathogènes et à l’apparition du SHU, alors que les variants Stx1 et Stx2e, Stx2f et Stx2g sont plus rarement impliqués dans des cas d’infections humaines . Les différents profils des variants de Stx sont considérés comme un facteur prédictif de la sévérité des infections à EHEC.[49]
15
1.3.2 Locus d’effacement des entérocytes
Ce LEE est un îlot de pathogénicité de 35,6 kb. Il est constitué de cinq opérons polycistroniques (LEE1 à 5) codant pour 41 ORF et notamment pour une intimine, codé par le gène eae (« E. coli attaching and effacing ») et son récepteur Tir (« translocated intimin 58 receptor ») (LEE5 ; Figure 4). En plus d‘être présent dans le génome chromosomique des STEC potentiellement pathogènes, ce LEE est retrouvé chez plusieurs bactéries entéropathogènes tels que les EPEC, Citrobacter rodentium ou Escherichia albertii.[50]
Figure 4: Organisation génétique du locus d‘effacement des entérocytes (Ritchie and Waldor, 2005).[51]
Les gènes sep (« secretion of E. coli protein »), esc (« E. coli secretion »).(36) et esp (« EPEC-secreted protein ») retrouvés dans les LEE1, LEE2 et LEE3 codent pour un système de sécrétion de type III (SSTT). Le LEE1 contient le gène « LEE encoded regulator » (ler) codant pour une protéine se fixant à l‘ADN et qui est le régulateur principal de l‘expression des autres LEE. Le SSTT est impliqué dans la translocation d‘effecteurs, majoritairement codés par les gènes du LEE4, dans la cellule hôte (Tableau 3).[52]
16
Tableau III: Protéines sécrétées par le système de sécrétion de type III par les E.coli O157:H7 et leurs activités (d‘après Stevens and Frankel, 2014).[52]
17
L‘expression de chaque opéron de ce LEE est inactivée de manière constitutive par la fixation d‘une protéine H-NS (« Histone-like protein ») sur le site de fixation de l‘ARN polymérase. La fixation de la protéine Ler (LEE1) à la protéine H-NS active l‘expression des opérons. Le SSTT est assemblé (Figure 5)[53], EspA permet l‘élongation de la seringue de l‘injectisome (SSTT) jusqu‘à la membrane de la cellule eucaryote. EspB et EspD transloquent ensuite à travers cette seringue moléculaire pour former un port d‘ancrage du SSTT dans la membrane de la cellule cible qui relie la bactérie à la cellule hôte (Figure 6).[54]
18
Figure 5: Représentation schématique de l‘assemblage du système de sécrétion de type III chez les EPEC (Sekiya et al., 2001). [53]
Figure 6: Représentation schématique du système de sécrétion de type III , exprimé par les EHEC et C. rodentium (Pallen et al., 2005).[54]
19
Grâce au SSTT ainsi formé, les protéines Tir sont ensuite transférées dans le cytoplasme
de la cellule cible. Elles sont insérées dans la membrane plasmique eucaryote et servent de récepteurs aux intimines exprimées à la surface de la membrane externe bactérienne et codées par le gène eae. L‘association entre ces deux protéines permet la mise ien place d‘une relation très rapprochée entre la bactérie et sa cible. Cet attachement permet le recrutement, par l‘intermédiaire des récepteurs Tir, de protéines eucaryotes qui induisent des réarrangements du cytosquelette et forment un « piédestal » d‘actine autour de la bactérie, créant ainsi une niche pour le développement du pathogène. La formation de ce piédestal crée le phénotype d‘effacement des microvillosités des cellules endothéliales du côlon à l‘origine des diarrhées aqueuses (lésion d‘attachement/effacement [A/E], Figure 7) [55]
Figure 7: Mécanisme de pathogénicité des E. coli entéropathogènes et entérohémorragiques (Croxen and Finlay, 2010).[55]
20
La colonisation du tube digestif est une étape majeure de la physiopathologie des EHEC. Les EHEC mettent notamment en place des lésions A/E analogues à celles décrites chez les EPEC (Figure 7). Néanmoins, contrairement aux EPEC qui colonisent l‘intestin grêle, les lésions A/E des STEC se concentrent au niveau de l‘épithélium folliculaire des plaques de Peyer.[56] Différents variants du gène eae existent.[57] Il semblerait que ces variants soient impliqués dans le tropisme cellulaire. En effet, les souches d‘EPEC sont capables de coloniser et d‘établir des lésions A/E au niveau de l‘intestin grêle, tandis que les EHEC sont retrouvés au niveau de l‘iléon terminal et du côlon, notamment à proximité des plaques de Peyer. Or il a été démontré qu‘une souche EHEC O157:H7 inactivée pour le gène eae-gamma et trans-complémentée pour le gène eae-alpha, communément retrouvé chez les EPEC, était capable de coloniser le côlon et l‘intestin grêle de porcs gnotobiotiques, à l‘instar des souches EPEC.[58]
D‘autres facteurs d‘adhésion potentiels ont été décrits chez les STEC. Le génome de la souche SAKAI O157:H7 contient au moins 16 groupes de gènes codant pour des adhésines fimbriaires. Ces gènes sont également retrouvés chez des souches non-O157, même si certains ne semblent pas être totalement fonctionnels. Cependant, l‘hypothèse de transcomplémentation des différents loci exprimant ces adhésines potentielles a été émise.[59] Parmi ces autres facteurs d‘adhésion, nous pouvons citer le gène saa (« STEC autoagglutinating adhesin ») codant pour une adhésine non fimbriaire auto-agglutinante. Ce gène a notamment été retrouvé chez des souches d‘EHEC eae négatives et isolées de cas humains.[60]
L‘adhésine EfaI est impliquée dans l‘adhésion in vitro de STEC à des cellules cibles [61, 62] Ce gène efaI présente 99,9% d‘homologie avec le gène lifA (pour « lymphocyte inhibitory factor A ») codant pour une lymphotoxine présente chez les souches EPEC.[62 ,63]
La protéine ToxB, impliquée dans l‘adhésion des souches EHEC O157:H7 sur des cellules Caco-2 in vitro favorise la sécrétion des protéines par le SSTT.[64 ,65] Cette protéine présente des homologies avec la toxine B de Clostridium difficile.[66,67]
21
Le facteur d‘adhésion Lpf (pour « long polar fimbriae ») semble être impliqué dans l‘adhésion des souches O157:H7.[68,69] Ces Lpf sont néanmoins présents chez de nombreuses souches d‘E. coli, notamment pathogènes, et ne semblent donc pas être spécifiques des EHEC.[70] Des gènes chromosomiques [71] et des îlots génomiques.[72] codant potentiellement pour d‘autres adhésines fimbriaires ont également été mis en évidence (sfa, stp et stc, OI-1 et OI- 47) mais leur rôle dans la pathogénie des EHEC reste à déterminer. Les « bundle-forming pilus » jouent un rôle dans l‘adhésion des EHEC aux cellules cibles.[55]
Une protéine de la membrane externe bactérienne, Iha (pour « IrgA homologue adhesin»), proche de la protéine IrgA (« Iron-regulated gene homologue A ») de Vibrio cholerae, a été identifiée. Iha confère aux bactéries un phénotype d‘adhésion diffuse sur des cellules HeLa en culture.[73] Les autres facteurs d’adhésion des EHEC non codés par le LEE : Chez les EHEC, de nombreuses adhésines fimbriaires et non fimbriaires contribuent à l’adhésion, à l’établissement et à la persistance de l’infection.[74] Différentes adhésines fimbriaires ont été décrites:
+ Le fimbriae Lpf (Long polar fimbriae) contribue à l’adhésion des EHEC aux cellules épithéliales intestinales, au niveau des cellules M ,[75] mais aussi aux protéines de la matrice extracellulaire comme la fibronectine, la laminine et le collagène de type IV.[76] Comme l’intimine, ce fimbriae semble influencer le tropisme cellulaire pour l’épithélium associé aux plaques de Peyer. [75 ,77]
+ Le pilus ECP (E. coli common pilus) et les fimbriae F9, ELF (E. coli laminin-binding-fimbriae) et Sfp (Sorbitol-fermenting fimbriae protein) permettent l’adhésion des EHEC aux cellules épithéliales in vitro.[74,78] De plus, le pilus ECP et les fimbriae F9 et ELF sont également capables d’interagir avec des protéines de la matrice extracellulaire. Il a également été montré que le pilus ECP et le fimbriae Sfp étaient exprimés dans des conditions limitées en oxygène, conditions retrouvées dans le tube digestif.[74,79]
+ Le pilus de type IV HCP pour « hemorrhagic coli pilus » est impliqué dans l’adhésion des EHEC à de nombreux types cellulaires ainsi que dans l’invasion des cellules épithéliales, l’hémagglutination des érythrocytes, la formation de biofilm et la réponse pro-inflammatoire. Ces propriétés suggèrent que ce pilus contribue non seulement à la virulence, la survie et la transmission des EHEC mais aussi l’inflammation causée par les EHEC.[80,81]
![Tableau I: Résumé des principales épidémies à EHEC dans le monde entre 1998-2014.[16]](https://thumb-eu.123doks.com/thumbv2/123doknet/15058509.697959/46.892.108.779.145.1026/tableau-résumé-principales-épidémies-ehec-monde.webp)
![Figure 1: Représentation schématique de la structure d‘E. coli.[19]](https://thumb-eu.123doks.com/thumbv2/123doknet/15058509.697959/49.892.199.691.349.589/figure-représentation-schématique-structure-coli.webp)

![Figure 4: Organisation génétique du locus d‘effacement des entérocytes (Ritchie and Waldor, 2005).[51]](https://thumb-eu.123doks.com/thumbv2/123doknet/15058509.697959/55.892.106.790.381.508/figure-organisation-génétique-locus-effacement-entérocytes-ritchie-waldor.webp)
![Tableau III: Protéines sécrétées par le système de sécrétion de type III par les E.coli O157:H7 et leurs activités (d‘après Stevens and Frankel, 2014).[52]](https://thumb-eu.123doks.com/thumbv2/123doknet/15058509.697959/56.892.109.788.167.1035/tableau-protéines-sécrétées-système-sécrétion-activités-stevens-frankel.webp)

![Figure 7: Mécanisme de pathogénicité des E. coli entéropathogènes et entérohémorragiques (Croxen and Finlay, 2010).[55]](https://thumb-eu.123doks.com/thumbv2/123doknet/15058509.697959/59.892.118.786.472.855/figure-mécanisme-pathogénicité-coli-entéropathogènes-entérohémorragiques-croxen-finlay.webp)