N°2017ANTI0230
Description des données comparatives démographiques,
biologiques, échocardiographiques et angiographiques des
infarctus du myocarde de type 1 et de type 2
THESE
Présentée et soutenue publiquement, pour la Faculté de Médecine Hyacinthe BASTARAUD des Antilles, au CHU de St Antoine à Paris
Et examinée par les Enseignants de la dite Faculté et de l’Assistance Publique des Hôpitaux Parisiens (APHP)
Pour obtenir le grade de DOCTEUR EN MEDECINE
Par Sébastien POUY
Examinateurs de la thèse : M. Aron Ariel COHEN Professeur
Président de thèse M. Laurent FELDMAN Professeur
M. Denis DUBOC Professeur M. Jocelyn INAMO Docteur M. Stéphane EDERHY Docteur
TABLES DES MATIERES
Remerciements ... 6
Liste universitaire des Antilles ... 7
Dédicaces ... 14
Abréviations ... 16
Revue de la littérature ... 17
1. Définitions ... 18
a. Définition universelle de l’infarctus du myocarde... 18
b. Définition de l’IDM de type 2 (2007) ... 18
c. Définition de l’IDM de type 2 (2012) ... 20
d. Définition de l’IDM de type 2 (2013) ... 21
e. Définition du NIMI ... 21
2. Description des données démographiques des IDM de type 2 ... 23
3. Facteurs déclenchants des IDM de type 2 ... 27
4. Atteinte coronaire chez les patients admis pour un IDM de type 2 ... 28
5. Prise en charge des IDM de type 2 ... 30
a. Prise en charge non invasive ... 30
b. Prise en charge invasive ... 32
6. Pronostic des IDM de type 2 ... 33
INTRODUCTION ... 38
METHODES ... 39
1. Population de l’étude ... 39
2. Classification des patients ... 39
3. Détermination du diagnostic final ... 40
4. Dosage de la troponine Ic ... 40
5. Analyse statistique ... 41
RESULTATS ... 42
1. Population de l’étude ... 42
2. Caractéristiques cliniques et paracliniques des IDM de ... 44
types 1 et 2 ... 44
3. Facteurs déclenchants des IDM de type 2 ... 48
4. Caractéristiques cliniques et paracliniques des IDM de 2 en fonction de la présence ou de l’absence de coronaropathie sous-jacente ... 49
5. Facteurs prédictifs de la présence ou de l’absence de lésions coronaires d’un IDM de type 2 ... 53
6. Facteurs déclenchants des IDM de type 2 en fonction de la présence ou de l’absence de coronaropathie sous-jacente... 54
DISCUSSION ... 55
CONCLUSION ... 58
SERMENT D’HIPPOCRATE ... 62
LETTRE MANUSCRITE D’AUTORISATION DE SOUTENANCE ... 64
AUTORISATION DE SOUTENANCE HORS SUBDIVISION ... 65
Remerciements
Je remercie le Professeur Ariel COHEN, PU-PH, chef de service en cardiologie au CHU de Saint Antoine, de m’avoir confié ce travail. Toujours disponible et à l’écoute malgré ses hautes fonctions, il m’aura guidé tout au long de ce travail.
Je ne remercierai jamais assez les Professeurs Denis DUBOC, PU-PH et chef de service en cardiologie au CHU de Cochin, et Laurent FELDMAN, PU-PH au CHU de Bichat, d’avoir accepté d’intégrer le jury de cette thèse. C’est un grand honneur pour moi.
Je remercie également le Docteur Stéphane EDERHY, PH au CHU de Saint Antoine, sans qui je n’aurais pu réaliser cette thèse. Médecin mais aussi scientifique dans l’âme, il a su m’aviser, me prodiguer des conseils astucieux et m’encadrer sans relâche. Je le respecte tant sur le plan humain que médical.
Bien entendu, je n’oublie pas Madame Sylvie LANG, statisticienne à Saint Antoine, qui a réalisé entièrement la partie statistique de ce travail. Un grand merci Sylvie.
De même, je suis extrêmement reconnaissant de l’aide apportée par Madame Clarisse BARILLE, secrétaire du Pr Ariel COHEN. Clarisse a été particulièrement réactive pour les tâches administratives avant de me proposer une précieuse relecture.
Enfin, je remercie le Docteur Jocelyn INAMO, MCU-PH, Directeur du DES de cardiologie Antilles-Guyane et chef de service en cardiologie au CHU de Martinique, de m’avoir soutenu pendant mon internat de cardiologie. Il a tout mis en œuvre afin que mon cursus se déroule toujours de manière optimale.
Liste universitaire des Antilles
Le Président de l'Université des Antilles : Jacky NARAYANINSAMY Doyen de la Faculté de Médecine : Raymond CESAIRE
Vice-Doyen de la Faculté de Médecine: Suzy DUFLO Professeurs des Universités - Praticiens Hospitaliers Bruno HOEN
Maladies Infectieuses
CHU de Pointe-à-Pitre /ABYMES
Pascal BLANCHET Chirurgie Urologique
CHU de Pointe-à-Pitre /ABYMES
André-Pierre UZEL Chirurgie Orthopédique et Traumatologie
CHU de Pointe-à-Pitre /ABYMES
Pierre COUPPIE Dermatologie CH de Cayenne
Thierry DAVID Ophtalmologie
CHU de Pointe-à-Pitre /ABYMES
Suzy DUFLO ORL – Chirurgie Cervico-Faciale
CHU de Pointe-à-Pitre /ABYMES
Eustase JANKY Gynécologie-Obstétrique
CHU de Pointe-à-Pitre /ABYMES
François ROQUES Chirurgie Thoracique et Cardiovasculaire CHU de Martinique
Jean ROUDIE Chirurgie Digestive CHU de Martinique
Jean-Louis ROUVILLAIN
Chirurgie Orthopédique CHU de Martinique
André CABIE Maladies Infectieuses CHU de Martinique
Philippe CABRE Neurologie CHU de Martinique
Raymond CESAIRE Bactériologie-Virologie-Hygiène option virologie CHU de Martinique
Professeurs des Universités - Praticiens Hospitaliers
(Suite)
Maryvonne DUEYMES-BODENES Immunologie CHU de Martinique
Régis DUVAUFERRIER Radiologie et imagerie Médicale
CHU de Martinique
Annie LANNUZEL Neurologie
CHU de Pointe-à-Pitre /ABYMES
Louis JEHEL Psychiatrie Adulte
CHU de Martinique
Mathieu NACHER Epidémiologie, Economie de la Santé et Prévention CH de Cayenne
Guillaume THIERY Réanimation
CHU de Pointe-à-Pitre /ABYMES Magalie DEMAR - PIERRE Parasitologie et Infectiologue CH de Cayenne
Vincent MOLINIE Anatomie Cytologie Pathologique CHU de Martinique
Philippe KADHEL Gynécologie-Obstétrique
CHU de Pointe-à-Pitre /ABYMES
Michel DEBANDT Rhumatologie CHU de Martinique
Jeannie HELENE-PELAGE Médecine Générale
CHU de Pointe-à-Pitre / Cabinet libéral
CHU de Martinique
Mehdi MEJDOUBI Radiodiagnostic et imagerie Médicale CHU de Martinique
Rémi NEVIERE Physiologie CHU de Martinique
Christian SAINTE-ROSE Radiodiagnostic et imagerie Médicale CHU de Martinique
Professeurs Associés de Médecine Générale
Franciane GANE-TROPLENT Médecine générale
Maîtres de Conférences des Universités - Praticiens Hospitaliers
Christophe DELIGNY Médecine Interne
CHU de Martinique
Jocelyn INAMO Cardiologie
CHU de Martinique
Fritz-Line VELAYOUDOM épse CEPHISE Endocrinologie
CHU de Pointe-à-Pitre
Marie-Laure LALANNE-MISTRIH Nutrition
CHU de Pointe-à-Pitre
Sébastien BREUREC Bactériologie &Vénérologie
CHU de Pointe-à-Pitre
Narcisse ELENGA Pédiatrie
CH de Cayenne
Moana GELU-SIMEON Gastroentérologie hépatologie
CHU de Pointe-à-Pitre
Chefs de Clinique des Universités - Assistants des Hôpitaux
BANCEL Paul ORL/Chirurgie maxillo-faciale
CHU de Pointe-à-Pitre
BORJA DE MOZOTA Daphné Gynécologie-Obstétrique CHU de Pointe-à-Pitre
DARCHE Louis Chirurgie Digestive et Viscérale CHU de Martinique
DE RIVOYRE Benoit Ophtalmologie
CHU de Pointe-à-Pitre
DEBBAGH Hassan Chirurgie thoracique
CHU de Martinique
DOURNON Nathalie Maladies infectieuses
CHU de Pointe-à-Pitre
GALLI-DARCHE Paola Neurologie
CHU de Martinique
GHASSANI Ali Gynécologie-Obstétrique
CHU de Pointe-à-Pitre
JACQUES-ROUSSEAU Natacha Anesthésie-Réanimation CHU de Pointe-à-Pitre
MARY Julia Rhumatologie
CHU de Martinique
MOINET Florence Rhumatologie-médecine interne
Chefs de Clinique des Universités – Médecine Générale
CARRERE Philippe
Médecine Générale
CHU de Pointe-à-Pitre / Cabinet
PLACIDE Axiane Médecine Générale
CHU de Martinique / Cabinet
MONFORT Astrid Cardiologie
CHU de Martinique
MOUREAUX Clément Urologie
CHU de Pointe-à-Pitre
NABET Cécile Parasitologie et Mycologie
CH de Cayenne
PARIS Eric Réanimation
CHU de Pointe-à-Pitre
PIERRE-JUSTIN Aurélie Neurologie
CHU de Pointe-à-Pitre
SAJIN Ana Maria Psychiatrie
CHU de Martinique
SEVERYNS Mathieu Chirurgie orthopédique
NIEMETZKI Florence Médecine Générale CH de Cayenne / Cabinet
MOUNSAMY Josué Médecine Générale
CHU de Pointe-à-Pitre / Cabinet
Professeurs Emérites
CHARLES-NICOLAS Aimé Psychiatrie Adulte
CHU de Martinique
Georges JEAN-BAPTISTE Rhumatologie
CHU de Martinique
Serge ARFI Médecine interne
CHU de Martinique
Bernard CARME Parasitologie
Dédicaces
A Haylie ma fille, que j’aime plus que tout au monde.
A Sokhna ma femme, qui m’a soutenu lors de ce retour drastique en médecine. Elle m’aura mis dans les meilleures conditions pour rédiger cette thèse.
A mes grand-parents, déjà partis, que je porte profondément dans mon cœur.
A mes parents, pour leur soutien inconditionnel. Sans eux, ces longues études n’auraient pas été possibles.
A ma grande sœur Christine (ma marraine !) et mon grand frère James (frérot le balltrapper), qui ont suivi ce parcours atypique dans les plus brefs détails. J’espère qu’ils ont compris que je ne suis ni endocrinologue ni dermatologue !
A toute ma famille de Sorde et mamie Huguette : je crois que je mérite de nombreux cannelés !
A Michel, Lydie, Mathieu et Magali : ma seconde famille
A ma belle-famille que j’adore, qui m’épate et dont je suis extrêmement fier : Fanta, la créatrice du bijou de ma vie, Fara, une des rares personnes qui aiment m’écouter à la guitare, Mourtada le patron, Lakhat le Wesley Snipes sénégalais, Cheikh, Falilou comme mon fils, Thiam le papa, Laure, Claudie, Ilan, Oran, Sylvie et Daniel.
A tous mes amis : Sophie, ma meilleure amie depuis la petite section (et Arnaud son mari), mon meilleur ami Flo depuis le CP, dont j’ignore toujours en quoi consiste son métier (et Nantz sa femme, la photographe de génie !), Stéphane le beau gosse (et July), Fred l’homme élastique, Elo la femme de l’homme élastique, Yann le BG et Caro, Thibaut et Cécilia, Sylvain et Ingrid, Abeni et Mathieu le couple « chirurgical », Emilie et Sepp le Teddy Riner du Stato, Odile, Brieg, François, Alysée et Boris le navigateur. Amis et co-internes, par ordre de rencontre : Dimitri, Salomé, Tito, Noëlle, Véro, Philippe, Gus, Alex, Titi, Gweno, PAC, Geoffroy, Jeanne, Sophie C, L.A, Léandre, Sophie P, Thomas, Baptiste, Tanissia, Sara, Sanae, Alexis, Laura, Vuty, Pascal, Louis, Jean Leopold, Mikael, Audrey, Pauline, Androula, Edem, Laura, Elisa, Bettia, Audrey, Jules, Pierre, Adeline et Yannick.
Assistants et chefs de cliniques qui m’ont stimulé : Marie-Elodie, Delphine, Julien F, Jean-Louis, Cyrille, Marie, Etienne, Ciham, Arnaud, Marion, Yann, Jeremy, Virginie, les deux Guillaume K et DV, Julien A, Fabien le canadien, Ludivine et Leila !
Sans oublier Julien Fabre, enseignant par excellence, Andréa Rami une cardiologue en or, Fabrice Démonière, rythmologue et ami cher, ainsi que le Dr Philippe Cohen-Tenoudji et ses collaborateurs (notamment Eric Charet le Montpelliérain fan de sport) mes futurs formateurs en angioplastie.
Abréviations
ACR : Arrêt Cardio-Respiratoire AOMI : Artériopathie oblitérante des membres inférieurs
ATL : Angioplastie Trans-Luminale BBG : Bloc de Branche Gauche BPCO : Bronchopneumopathie chronique obstructive
CPK-MB : Créatine Phosphokinase-MB DFG : Débit de Filtration Glomérulaire ECG : Electrocardiogramme
ETT : Echocardiographie Trans-Thoracique
FA : Fibrillation Atriale FEVG : Fraction d’Ejection du Ventricule Gauche
FC : Fréquence cardiaque Hb : Hémoglobine
HR : Hazard Ratio
HTA : Hypertension Artérielle HVG : Hypertrophie Ventriculaire Gauche
IDM : Infarctus Du Myocarde
MACE : Major Adverse Cardiac Events NIMI : Non Ischemic Myocardial Injury (lésions coronaires non ischémiques) O2 : Dioxygène
OMS : Organisation Mondiale de la Santé
OR : Odds Ratio
PAC : Pontage Aorto-Coronaire PAD : Pression Artérielle Diastolique PAS : Pression Artérielle Systolique SCA ST+ : Syndrome Coronaire aigue avec sus-décalage du segment-ST SpO2 : Saturation percutanée en Oxygène
T1MI : IDM de type 1 T2MI : IDM de type 2
TSV : Tachycardie Supra-Ventriculaire TV : Tachycardie Ventriculaire
Revue de la littérature
Cette revue de littérature sur les études de l’infarctus du myocarde de type 2 reprend les définitions, l’incidence, les données démographiques, les facteurs déclenchants, l’atteinte coronaire, la prise en charge et la mortalité de l’IDM de type 2.
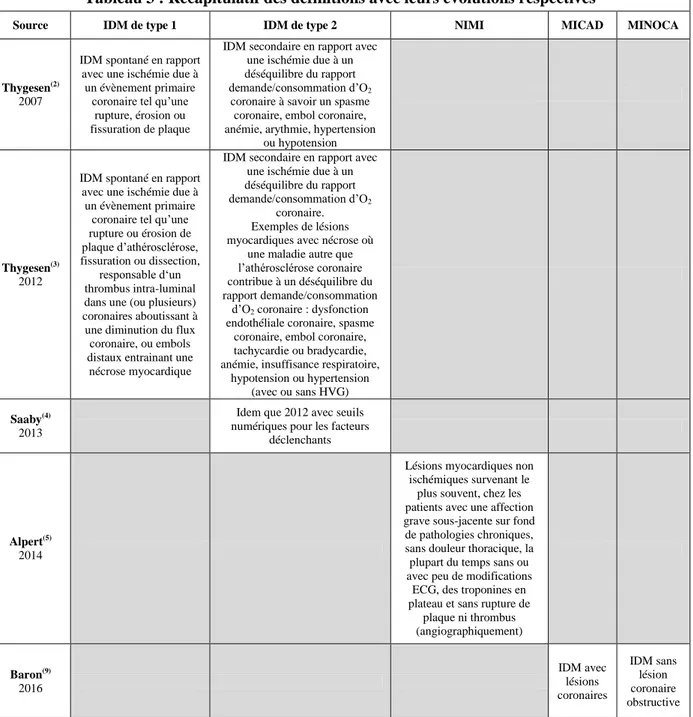
Entre 2007 et 2016, vingt-six études ont été publiées (Figure 1).
0 1 2 3 4 5 6 7 8 9 10 2007 2008 2009 2010 2011 2012 2013 2014 2015 2016
1. Définitions
a. Définition universelle de l’infarctus du myocarde
La définition de l’infarctus du myocarde (IDM) a largement évolué depuis sa première version, proposée par l’Organisation Mondiale de la Santé en 1960, résumant alors l’IDM à un « déséquilibre entre apports et demandes en oxygène au niveau du myocarde ».
La mise à disposition de biomarqueurs cardiaques signant de manière sensible et spécifique la nécrose myocytaire (troponine I/T, conventionnelle puis ultrasensible) a permis au cours des dernières années d’affiner la définition de l’IDM intégrant à la fois les données cliniques, de l’électrocardiogramme et de la biologie.
En 2000, un consensus entre les sociétés européenne et américaine de cardiologie(1) a précisé les critères définissant un IDM récent évolutif. Il s’agissait d’une cinétique d’élévation de la troponine I ou T (augmentation brutale puis diminution brutale) ou des CPK-MB, associée à au moins un des critères suivants :
symptômes cliniques évoquant une ischémie myocardique
apparition d’une onde Q de nécrose / modifications électriques à l’ECG (sus ou sous-décalage du segment ST)
intervention coronaire
b. Définition de l’IDM de type 2 (2007)
En 2007, Thygesen(2) et al. ont proposé une définition plus complexe et précise de l’IDM (Tableau 1), tenant compte en partie des différents mécanismes pouvant aboutir à
une nécrose myocardique. Ainsi, cette conférence de consensus distingue 5 entités différentes (IDM de type 1 à 5).
La définition de l’IDM de type 1 a été retenue comme une nécrose myocytaire due à un évènement primaire coronaire tel qu’une rupture, érosion ou fissuration de plaque. L’IDM de type 2 a été défini comme IDM secondaire en rapport avec une ischémie due à un déséquilibre du rapport demande/consommation d’O2 coronaire à savoir un spasme coronaire, embol coronaire, anémie, arythmies, hypertension ou hypotension.
Les autres sous-types d’IDM sont détaillés dans le tableau 1.
Tableau 1 : Définition initiale des 5 sous-types d’IDM en 2007(2)
Type 1 : IDM spontané en rapport avec une ischémie due à un évènement primaire coronaire tel qu’une rupture, érosion ou fissuration de plaque
Type 2 : IDM secondaire en rapport avec une ischémie due à un déséquilibre du rapport demande/consommation d’O2 coronaire à savoir un spasme coronaire, embol coronaire, anémie, arythmies, hypertension ou hypotension
Type 3 : ACR ou mort subite, accompagné de symptômes suggérant une ischémie myocardique et d’un sus-décalage du segment ST (également nouveau BBG) ; ou preuve d’un thrombus frais intra-coronaire à l’angiographie ou à l’autopsie (le décès doit avoir lieu avant la réalisation de la biologie ou la positivité des biomarqueurs dans le sang)
Type 4a : IDM associé à une intervention coronaire percutanée
Type 4b : IDM secondaire à une thrombose de stent documentée par angiographie ou autopsie
c. Définition de l’IDM de type 2 (2012)
En 2012, Thygesen(3) précise les définitions de chaque sous-type. Cela concerne essentiellement les IDM de types 1 et 2 (Tableau 2). Les mécanismes aboutissant à un déséquilibre du rapport demande/consommation d’O2, tels que la dysfonction endothéliale, l’insuffisance respiratoire, l’hypertension avec ou sans HVG et les bradycardies (en opposition aux tachycardies) sont précisés.
Tableau 2 : Précisions en 2012 par Thygesen des IDM de types 1 et 2(3)
Type 1 : IDM spontané en rapport avec une ischémie due à un évènement primaire coronaire tel qu’une rupture ou érosion de plaque d’athérosclérose, fissuration ou dissection responsable d‘un thrombus intra-luminal dans une (ou plus) coronaires aboutissant à une diminution du flux coronaire, ou embols distaux entrainant une nécrose myocardique
Type 2 : IDM secondaire en rapport avec une ischémie due à un déséquilibre du rapport demande/consommation d’O2 coronaire
Exemple de lésions myocardiques avec nécrose où une maladie autre que l’athérosclérose coronaire contribue à un déséquilibre du rapport demande/consommation d’O2 coronaire, tel que une dysfonction endothéliale coronaire, spasme coronaire, embol coronaire, tachycardie ou bradycardie, anémie, insuffisance respiratoire, hypotension ou hypertension (avec ou sans hypertrophie ventriculaire gauche)
d. Définition de l’IDM de type 2 (2013)
En 2013, Saaby(4) a proposé de préciser la définition de l’IDM de type 2 en appliquant des seuils précis numériques aux causes possibles, afin de normaliser la définition ou lever certains critères subjectifs. Exemples de ces critères numériques : pour l’anémie, le taux d’hémoglobine doit être inférieur à 8,9 g/dl chez les hommes et 8,1 g/dl chez les femmes, pour la fréquence respiratoire seuil de tachypnée à 20/mn, durée d’une TV > 20 mn, fréquence ventriculaire d’une TSV > 150/mn avec durée > 20 mn, bradycardie nécessitant un pacemaker, choc avec oligurie < 30 cc/h, etc.
A ce jour, ces critères n’ont pas été communément admis : difficulté d’application en pratique et rationnel physiopathologique sous-jacent arbitraire.
e. Définition du NIMI
En 2014, Alpert(5) propose une définition pour les NIMI (Non Ischemic Myocardial Injury, à savoir les lésions myocardiques non ischémiques) : elles surviennent, le plus souvent, chez les patients avec une affection grave sous-jacente sur fond de pathologies chroniques, sans douleur thoracique, la plupart du temps sans ou avec peu de modifications électrocardiographiques, une cinétique d’élévation de troponine en plateau, sans rupture de plaque ni thrombus à la coronarographie.
Ci-dessous les dates importantes des travaux (Figure 2) avec un récapitulatif des définitions (Tableau 3).
Saaby : seuils numériques pour les IDM
type 2 2000 2007 2012 2013 2014 OMS (<2000) Alpert : affine la définition de l’IDM Thygesen : Introduction des 5 sous-types d’IDM Thygesen : Précise les 5 sous-types d’IDM Alpert : Définit les NIMI
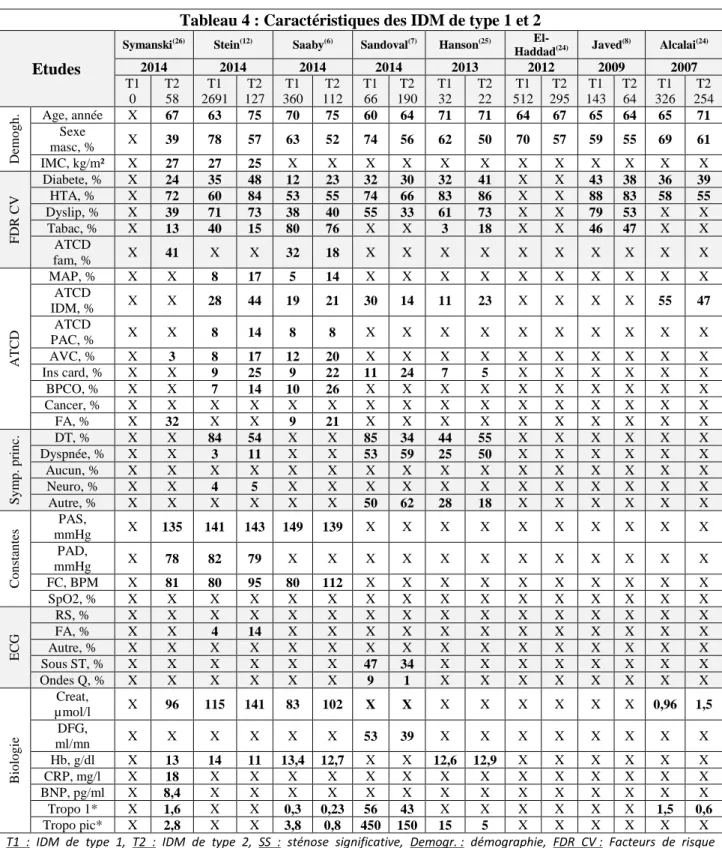
Tableau 3 : Récapitulatif des définitions avec leurs évolutions respectives
Source IDM de type 1 IDM de type 2 NIMI MICAD MINOCA
Thygesen(2)
2007
IDM spontané en rapport avec une ischémie due à un évènement primaire
coronaire tel qu’une rupture, érosion ou fissuration de plaque
IDM secondaire en rapport avec une ischémie due à un déséquilibre du rapport demande/consommation d’O2
coronaire à savoir un spasme coronaire, embol coronaire, anémie, arythmie, hypertension
ou hypotension
Thygesen(3)
2012
IDM spontané en rapport avec une ischémie due à un évènement primaire
coronaire tel qu’une rupture ou érosion de plaque d’athérosclérose, fissuration ou dissection,
responsable d‘un thrombus intra-luminal dans une (ou plusieurs) coronaires aboutissant à une diminution du flux
coronaire, ou embols distaux entrainant une nécrose myocardique
IDM secondaire en rapport avec une ischémie due à un déséquilibre du rapport demande/consommation d’O2
coronaire. Exemples de lésions myocardiques avec nécrose où
une maladie autre que l’athérosclérose coronaire contribue à un déséquilibre du rapport demande/consommation
d’O2 coronaire : dysfonction endothéliale coronaire, spasme
coronaire, embol coronaire, tachycardie ou bradycardie, anémie, insuffisance respiratoire,
hypotension ou hypertension (avec ou sans HVG)
Saaby(4)
2013
Idem que 2012 avec seuils numériques pour les facteurs
déclenchants
Alpert(5)
2014
Lésions myocardiques non ischémiques survenant le
plus souvent, chez les patients avec une affection grave sous-jacente sur fond de pathologies chroniques, sans douleur thoracique, la plupart du temps sans ou avec peu de modifications
ECG, des troponines en plateau et sans rupture de
plaque ni thrombus (angiographiquement) Baron(9) 2016 IDM avec lésions coronaires IDM sans lésion coronaire obstructive
IDM : Infarctus du Myocarde, NIMI : Non Ischemic Myocardial Injury, MICAD : Myocardial Infarction with Obstructive Coronary Artery Disease, MINOCA : Myocardial Infarction with Non-Obstructive Coronary Arteries, HVG : Hypertrophie ventriculaire Gauche, O2 : di-oxygène
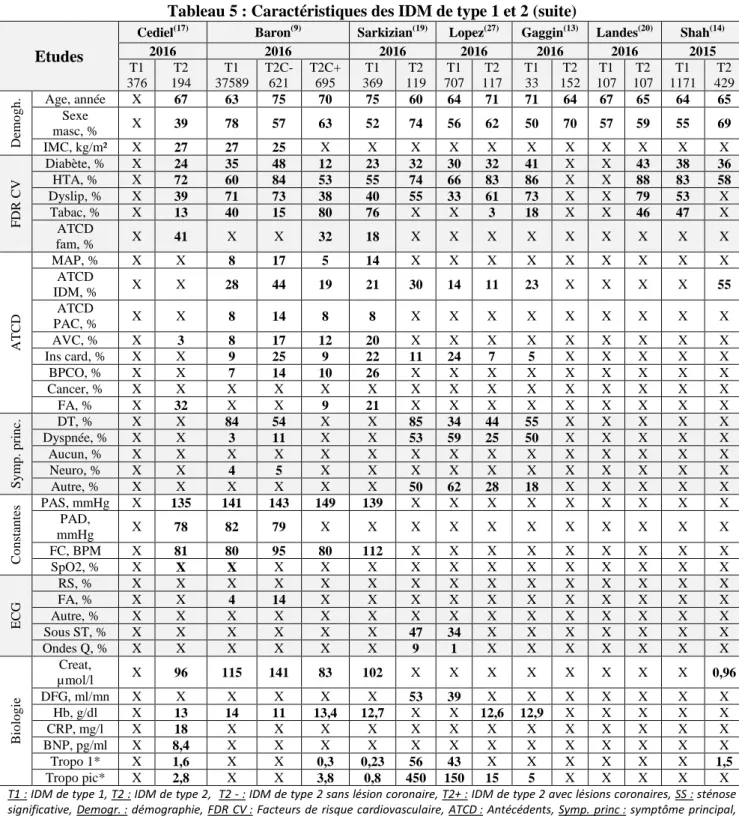
2. Description des données démographiques des IDM de type 2 Seize études, publiées entre 2007 et 2014 (tableaux 4 et 5), ont analysé les caractéristiques de base des patients admis pour un IDM de type 1 et de type 2, permettant d’isoler, pour chacune de ces deux entités, certaines données constantes d’une étude à l’autre.
L’interprétation de ces études reste cependant difficile tant la méthodologie (étude rétrospective versus prospective), la définition retenue pour identifier les patients admis pour un IDM de type 2 peut varier de manière importante d’une étude à l’autre.
Dans sept études rétrospectives, identifiant la population d’IDM de type 2 à partir d’un dosage positif de la troponine I ou T et d’une adjudication du type d’IDM a posteriori, la fréquence des IDM de type 2 au sein des patients admis pour un IDM varie de 2 à 30 % (Saaby(6) 2014, Sandoval(7) 2014, Javed(8) 2009, Baron(9) 2015, Morrow(10) 2009, Melberg(11) 2010 et Stein(12) 2014). A l’opposé, dans les deux seules études prospectives, l’incidence des IDM de type 2 varie de 3,5 % dans l’étude TRITON TIMI 38 (Morrow(10) 2009) et 12,2 % dans l’étude CASABLANCA (Gaggin(13) 2017).
L’incidence des IDM de type 2 comparativement aux IDM de type 1 est plus faible au sein des patients âgés de moins de 75 ans (60 vs 124 pour 100 000 patients) et est plus élevée au sein des patients âgés de 75 ans et plus (1008 vs 750 pour 100 000 patients) (Shah(14) 2015).
La méta-analyse de Gupta(15) publiée en 2017 montre que les patients admis pour un IDM de type 2 (comparativement aux patients admis pour un IDM de type 1) sont plus âgés (74 ans vs 69,8 ans), présentent un score GRACE à l’admission plus élevé, sont plus fréquemment de sexe féminin (46 % vs 32,7 %), présentent plus de facteurs de risque cardio-vasculaire, dont le diabète (29,2 % vs 25,6 %) et l’HTA (60,4 % vs 52 %).
Les comorbidités sont aussi plus fréquemment observées au sein des patients admis pour un IDM de type 2 comparativement aux patients admis pour un IDM de type 1, notamment l’insuffisance rénale (35 % vs 13,2 %) et les antécédents d’insuffisance cardiaque (21 % vs 10 %). Au plan biologique, les patients admis pour un IDM de type 2 ont des taux de troponine plus faibles, d’hémoglobine plus bas, mais des taux de CRP plus élevés (Gupta(15) 2017), que les patients admis pour un IDM de type 1.
En conclusion, la fréquence des IDM de type 2 est difficile à évaluer car dépend fortement de la méthodologie de l’étude. Les IDM de type 2 sont plus âgés, plutôt des femmes, avec un risque cardiovasculaire similaire aux types 1. Les IDM de type 2 se présentent aux urgences plutôt pour un symptôme autre qu’une douleur thoracique (surtout dyspnée), plus en arythmie (ECG), avec une biologie globalement plus sévère (anémie, insuffisance rénale, taux de BNP plus élevés). Seule la troponine semble moins élevée.
Ci-dessous les tableaux récapitulatifs des données démographiques de la littérature, entre 2007 et 2014 (Tableau 4) et de 2015 à 2016 (Tableau 5).
Tableau 4 : Caractéristiques des IDM de type 1 et 2
Etudes
Symanski(26) Stein(12) Saaby(6) Sandoval(7) Hanson(25)
El-Haddad(24) Javed(8) Alcalai(24)
2014 2014 2014 2014 2013 2012 2009 2007 T1 0 T2 58 T1 2691 T2 127 T1 360 T2 112 T1 66 T2 190 T1 32 T2 22 T1 512 T2 295 T1 143 T2 64 T1 326 T2 254 De m o g h . Age, année X 67 63 75 70 75 60 64 71 71 64 67 65 64 65 71 Sexe masc, % X 39 78 57 63 52 74 56 62 50 70 57 59 55 69 61 IMC, kg/m² X 27 27 25 X X X X X X X X X X X X F DR CV Diabete, % X 24 35 48 12 23 32 30 32 41 X X 43 38 36 39 HTA, % X 72 60 84 53 55 74 66 83 86 X X 88 83 58 55 Dyslip, % X 39 71 73 38 40 55 33 61 73 X X 79 53 X X Tabac, % X 13 40 15 80 76 X X 3 18 X X 46 47 X X ATCD fam, % X 41 X X 32 18 X X X X X X X X X X ATCD MAP, % X X 8 17 5 14 X X X X X X X X X X ATCD IDM, % X X 28 44 19 21 30 14 11 23 X X X X 55 47 ATCD PAC, % X X 8 14 8 8 X X X X X X X X X X AVC, % X 3 8 17 12 20 X X X X X X X X X X Ins card, % X X 9 25 9 22 11 24 7 5 X X X X X X BPCO, % X X 7 14 10 26 X X X X X X X X X X Cancer, % X X X X X X X X X X X X X X X X FA, % X 32 X X 9 21 X X X X X X X X X X S y m p . p ri n c. DT, % X X 84 54 X X 85 34 44 55 X X X X X X Dyspnée, % X X 3 11 X X 53 59 25 50 X X X X X X Aucun, % X X X X X X X X X X X X X X X X Neuro, % X X 4 5 X X X X X X X X X X X X Autre, % X X X X X X 50 62 28 18 X X X X X X Co n sta n tes PAS, mmHg X 135 141 143 149 139 X X X X X X X X X X PAD, mmHg X 78 82 79 X X X X X X X X X X X X FC, BPM X 81 80 95 80 112 X X X X X X X X X X SpO2, % X X X X X X X X X X X X X X X X ECG RS, % X X X X X X X X X X X X X X X X FA, % X X 4 14 X X X X X X X X X X X X Autre, % X X X X X X X X X X X X X X X X Sous ST, % X X X X X X 47 34 X X X X X X X X Ondes Q, % X X X X X X 9 1 X X X X X X X X Bio lo g ie Creat, µmol/l X 96 115 141 83 102 X X X X X X X X 0,96 1,5 DFG, ml/mn X X X X X X 53 39 X X X X X X X X Hb, g/dl X 13 14 11 13,4 12,7 X X 12,6 12,9 X X X X X X CRP, mg/l X 18 X X X X X X X X X X X X X X BNP, pg/ml X 8,4 X X X X X X X X X X X X X X Tropo 1* X 1,6 X X 0,3 0,23 56 43 X X X X X X 1,5 0,6 Tropo pic* X 2,8 X X 3,8 0,8 450 150 15 5 X X X X X X
T1 : IDM de type 1, T2 : IDM de type 2, SS : sténose significative, Demogr. : démographie, FDR CV : Facteurs de risque cardiovasculaire, ATCD : Antécédents, Symp. princ : symptôme principal, ECG : électrocardiogramme, Sexe masc : sexe masculin, HTA : Hypertension artérielle, Dyslip : dyslipidémie, ATCD fam : antécédents familiaux, MAP : maladie athéromateuse périphérique, IDM : Infarctus du myocarde, PAC : Pontage aorto-coronaire, Ins card : insuffisance cardiaque, AVC : Accident vasculaire cérébral, BPCO : Bronchopneumopathie chronique obstructive, FA : Fibrillation atriale, DT : douleur thoracique, PAS :
pression artérielle systolique, PAD : pression artérielle diastolique, FC : Fréquence cardiaque, SpO2 : Saturation percutanée en
oxygène, RS : Rythme sinusal, creat : créatinine, DFG : débit filtration glomérulaire, Hb : Hémoglobine, CRP : protéine C réactive,
Tableau 5 : Caractéristiques des IDM de type 1 et 2 (suite) Etudes
Cediel(17) Baron(9) Sarkizian(19) Lopez(27) Gaggin(13) Landes(20) Shah(14)
2016 2016 2016 2016 2016 2016 2015 T1 376 T2 194 T1 37589 T2C- 621 T2C+ 695 T1 369 T2 119 T1 707 T2 117 T1 33 T2 152 T1 107 T2 107 T1 1171 T2 429 De m o g h . Age, année X 67 63 75 70 75 60 64 71 71 64 67 65 64 65 Sexe masc, % X 39 78 57 63 52 74 56 62 50 70 57 59 55 69 IMC, kg/m² X 27 27 25 X X X X X X X X X X X F DR CV Diabète, % X 24 35 48 12 23 32 30 32 41 X X 43 38 36 HTA, % X 72 60 84 53 55 74 66 83 86 X X 88 83 58 Dyslip, % X 39 71 73 38 40 55 33 61 73 X X 79 53 X Tabac, % X 13 40 15 80 76 X X 3 18 X X 46 47 X ATCD fam, % X 41 X X 32 18 X X X X X X X X X ATCD MAP, % X X 8 17 5 14 X X X X X X X X X ATCD IDM, % X X 28 44 19 21 30 14 11 23 X X X X 55 ATCD PAC, % X X 8 14 8 8 X X X X X X X X X AVC, % X 3 8 17 12 20 X X X X X X X X X Ins card, % X X 9 25 9 22 11 24 7 5 X X X X X BPCO, % X X 7 14 10 26 X X X X X X X X X Cancer, % X X X X X X X X X X X X X X X FA, % X 32 X X 9 21 X X X X X X X X X S y m p . p ri n c. DT, % X X 84 54 X X 85 34 44 55 X X X X X Dyspnée, % X X 3 11 X X 53 59 25 50 X X X X X Aucun, % X X X X X X X X X X X X X X X Neuro, % X X 4 5 X X X X X X X X X X X Autre, % X X X X X X 50 62 28 18 X X X X X Co n sta n tes PAS, mmHg X 135 141 143 149 139 X X X X X X X X X PAD, mmHg X 78 82 79 X X X X X X X X X X X FC, BPM X 81 80 95 80 112 X X X X X X X X X SpO2, % X X X X X X X X X X X X X X X ECG RS, % X X X X X X X X X X X X X X X FA, % X X 4 14 X X X X X X X X X X X Autre, % X X X X X X X X X X X X X X X Sous ST, % X X X X X X 47 34 X X X X X X X Ondes Q, % X X X X X X 9 1 X X X X X X X Bio lo g ie Creat, µmol/l X 96 115 141 83 102 X X X X X X X X 0,96 DFG, ml/mn X X X X X X 53 39 X X X X X X X Hb, g/dl X 13 14 11 13,4 12,7 X X 12,6 12,9 X X X X X CRP, mg/l X 18 X X X X X X X X X X X X X BNP, pg/ml X 8,4 X X X X X X X X X X X X X Tropo 1* X 1,6 X X 0,3 0,23 56 43 X X X X X X 1,5 Tropo pic* X 2,8 X X 3,8 0,8 450 150 15 5 X X X X X
T1 : IDM de type 1, T2 : IDM de type 2, T2 - : IDM de type 2 sans lésion coronaire, T2+ : IDM de type 2 avec lésions coronaires, SS : sténose significative, Demogr. : démographie, FDR CV : Facteurs de risque cardiovasculaire, ATCD : Antécédents, Symp. princ : symptôme principal, ECG : électrocardiogramme, Sexe masc : sexe masculin, HTA : Hypertension artérielle, Dyslip : dyslipidémie, ATCD fam : antécédents familiaux, MAP : maladie athéromateuse périphérique, IDM : Infarctus du myocarde, PAC : Pontage aorto-coronaire, Ins card : insuffisance cardiaque, AVC : Accident vasculaire cérébral, BPCO : Bronchopneumopathie chronique obstructive, FA : Fibrillation atriale, DT : douleur thoracique, PAS : pression artérielle systolique, PAD : pression artérielle diastolique, FC : Fréquence cardiaque, SpO2 : Saturation percutanée
en oxygène, RS : Rythme sinusal, creat : créatinine, DFG : débit filtration glomérulaire, Hb : Hémoglobine, CRP : protéine C réactive, Tropo 1 : 1ère troponine dosée, Tropo pic : pic de troponine. (*) : unités différentes pour la troponine
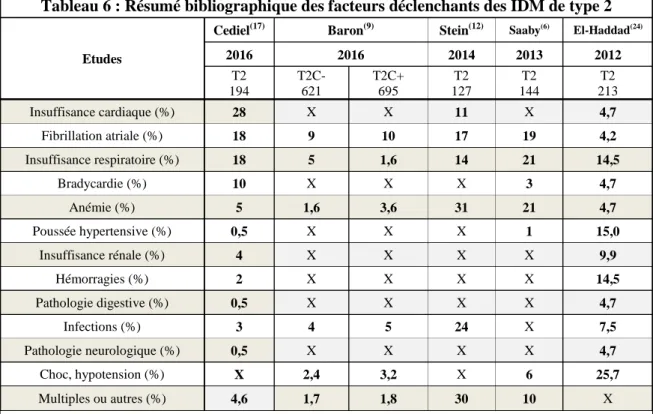
3. Facteurs déclenchants des IDM de type 2 Dans l’étude de Saaby(16)
publiée en 2013, les causes des IDM de type 2 étaient dominées par l’anémie (20 %), la détresse respiratoire (20 %) et les tachycardies supraventriculaires d’une durée > 20 mn (20 %).
L’étude de Stein(12)
menée en 2014 a montré que 31 % des facteurs déclenchants des IDM de type 2 étaient une anémie, 24 % un sepsis et 17 % de la fibrillation atriale. Cediel(17) a noté que 28 % des facteurs déclenchants étaient représentés par l’insuffisance cardiaque, 18 % par la fibrillation atriale, 18 % par l’insuffisance respiratoire et 10 % par des épisodes de bradycardie.
Les données bibliographiques des facteurs déclenchants sont récapitulées ci-dessous (Tableau 6).
Tableau 6 : Résumé bibliographique des facteurs déclenchants des IDM de type 2
Etudes
Cediel(17) Baron(9) Stein(12) Saaby(6) El-Haddad(24)
2016 2016 2014 2013 2012 T2 194 T2C- 621 T2C+ 695 T2 127 T2 144 T2 213 Insuffisance cardiaque (%) 28 X X 11 X 4,7 Fibrillation atriale (%) 18 9 10 17 19 4,2 Insuffisance respiratoire (%) 18 5 1,6 14 21 14,5 Bradycardie (%) 10 X X X 3 4,7 Anémie (%) 5 1,6 3,6 31 21 4,7 Poussée hypertensive (%) 0,5 X X X 1 15,0 Insuffisance rénale (%) 4 X X X X 9,9 Hémorragies (%) 2 X X X X 14,5 Pathologie digestive (%) 0,5 X X X X 4,7 Infections (%) 3 4 5 24 X 7,5 Pathologie neurologique (%) 0,5 X X X X 4,7 Choc, hypotension (%) X 2,4 3,2 X 6 25,7 Multiples ou autres (%) 4,6 1,7 1,8 30 10 X
T1 : IDM de type 1, T2 : IDM de type 2, T2 - : IDM de type 2 sans lésion coronaire, T2+ : IDM de type 2 avec lésions coronaires, SS : sténose significative. NB : les données sont en pourcentage
4. Atteinte coronaire chez les patients admis pour un IDM de type 2 L’atteinte coronaire documentée par la coronarographie reste, elle aussi, difficile à quantifier au sein des patients admis pour un IDM de type 2, et difficilement comparable à celle des patients admis pour un IDM de type 1, tant le recours à la coronarographie n’est pas systématique dans la population admise pour un IDM de type 2 (Baron(9) 2016 et Stein(12) PLOS 2014).
Plusieurs études décrivent les atteintes coronaires au sein des patients présentant un IDM de type 2 (Stein(12), Shah(14) 2015, Saaby(16) 2013, Javed(8) 2009 et Baron(9) 2016). La proportion de patients bénéficiant d’une coronarographie au décours d’un IDM de type 2 varie dans ces études de 8 % (Shah(14) 2015) à 50 % (Javed(8) 2009).
La proportion de patients admis pour un IDM de type 2 présentant une lésion coronaire jugée significative définie par une sténose coronaire > 50 % variait dans ces études de 29 % (Spatz(18) 2015) à 78 % (Javed(8) 2009).
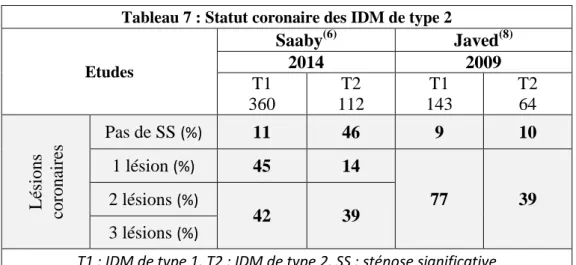
L’étude de Saaby(6)
en 2014 a montré que lespatients admis pour un IDM de type 2 ne présentaient pas de lésion coronaire significative dans 45 % des cas, contre seulement 12 % des patients admis pour un IDM de type 1 (p < 0,001). Pour les patients admis pour un IDM de type 2, l’atteinte coronaire était considérée comme monotronculaire dans 19 % des cas et dans 45 % des cas pour les patients présentant un IDM de type 1 (p = 0,008). L’atteinte était jugée bi ou tritronculaire dans 35,5 % des cas pour les IDM de type 2 contre 44 % pour les IDM de type 1 (p = 0,38). Les lésions isolées du tronc commun étaient notées chez 10 % des patients admis pour un IDM de type 2 et 6 % des IDM de type 1 (p = 0,43).
Gaggin(13) a aussi documenté le statut coronaire des IDM de type 2, en incluant tous les patients de son centre (ville de Boston) ayant bénéficié, soit d’une coronarographie (avec ou sans angioplastie), soit d’une artériographie périphérique (1251 patients au total). Douze pourcents de cette population ont présenté un IDM de type 2 dans l’année, soit 152 patients, parmi lesquels 25 % présentaient des lésions tritronculaires sévères (sténose > 70 %) et 47 % bitronculaires sévères.
Les tableaux récapitulatifs des lésions coronaires dans la littérature sont présentés ci-dessous (Tableaux 7 et 8).
Tableau 7 : Statut coronaire des IDM de type 2
Etudes Saaby(6) Javed(8) 2014 2009 T1 360 T2 112 T1 143 T2 64 Lé sions cor ona ir es Pas de SS (%) 11 46 9 10 1 lésion (%) 45 14 77 39 2 lésions (%) 42 39 3 lésions (%)
T1 : IDM de type 1, T2 : IDM de type 2, SS : sténose significative
Tableau 8 : Statut coronaire des IDM de type 2 (suite) Etudes
Baron(9) Sarkizian(19) Gaggin(13)
2016 2016 2016 T1 37589 T2C- 621 T2C+ 695 T1 369 T2 119 T1 33 T2 152 Lé sions cor ona ir es Pas de SS (%) X 100 X X 13 X X 1 lésion (%) 43 X 40 X X X X 2 lésions (%) 27 X 22 X X 56 45 3 lésions (%) 29 X 38 X X 21 23
T1 : IDM de type 1, T2 : IDM de type 2, T2 - : IDM de type 2 sans lésion coronaire, T2+ : IDM de type 2 avec lésions coronaires, SS : sténose significative
5. Prise en charge des IDM de type 2
Les études récentes ont démontré une grande hétérogénéité de la prise en charge, tant sur le plan des traitements administrés que du recours à l’opacification coronaire.
a. Prise en charge non invasive
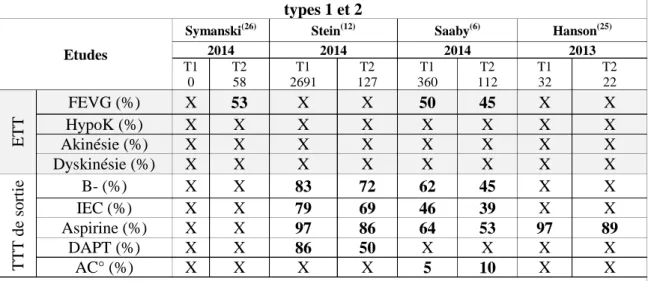
D’un point de vu médicamenteux, les patients admis pour un IDM de type 1 sortaient plus sous aspirine que les types 2 (90 % vs 49 %), plus sous clopidogrel (80 % vs 14 %) et bêtabloquants (76 % vs 36 %) (Tableaux 9 et 10).
Tableau 9 : Caractéristiques échocardiographiques et traitements de sortie des IDM de types 1 et 2
Etudes
Symanski(26) Stein(12) Saaby(6) Hanson(25)
2014 2014 2014 2013 T1 0 T2 58 T1 2691 T2 127 T1 360 T2 112 T1 32 T2 22 ETT FEVG (%) X 53 X X 50 45 X X HypoK (%) X X X X X X X X Akinésie (%) X X X X X X X X Dyskinésie (%) X X X X X X X X TT T de so rt ie B- (%) X X 83 72 62 45 X X IEC (%) X X 79 69 46 39 X X Aspirine (%) X X 97 86 64 53 97 89 DAPT (%) X X 86 50 X X X X AC° (%) X X X X 5 10 X X
T1 : IDM de type 1, T2 : IDM de type 2, FEVG : Fraction d’éjection ventriculaire gauche, HypoK : hypokinésie, TTT : traitement, B- : bêtabloquants, IEC : Inhibiteur de l’Enzyme de Conversion, DAPT : double anti-aggrégation plaquettaire, AC° : anticoagulation, ETT : échocardiographie transthoracique
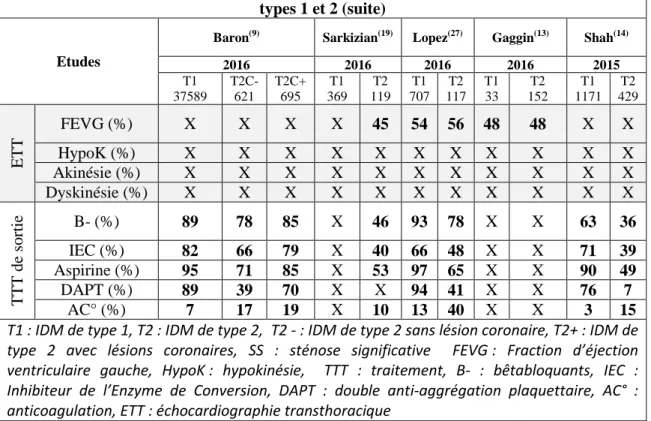
De même, selon, Sarkizian(19) et Cediel(17), les IDM de type 2 bénéficient également de moins d’échocardiographies que les types 1, respectivement 44 % contre 86 % et 41 % contre 95 %.
Tableau 10 : Caractéristiques échocardiographiques et traitements de sortie des IDM de types 1 et 2 (suite)
Etudes
Baron(9) Sarkizian(19) Lopez(27) Gaggin(13) Shah(14)
2016 2016 2016 2016 2015 T1 37589 T2C- 621 T2C+ 695 T1 369 T2 119 T1 707 T2 117 T1 33 T2 152 T1 1171 T2 429 ETT FEVG (%) X X X X 45 54 56 48 48 X X HypoK (%) X X X X X X X X X X X Akinésie (%) X X X X X X X X X X X Dyskinésie (%) X X X X X X X X X X X TT T de so rt ie B- (%) 89 78 85 X 46 93 78 X X 63 36 IEC (%) 82 66 79 X 40 66 48 X X 71 39 Aspirine (%) 95 71 85 X 53 97 65 X X 90 49 DAPT (%) 89 39 70 X X 94 41 X X 76 7 AC° (%) 7 17 19 X 10 13 40 X X 3 15
T1 : IDM de type 1, T2 : IDM de type 2, T2 - : IDM de type 2 sans lésion coronaire, T2+ : IDM de type 2 avec lésions coronaires, SS : sténose significative FEVG : Fraction d’éjection ventriculaire gauche, HypoK : hypokinésie, TTT : traitement, B- : bêtabloquants, IEC : Inhibiteur de l’Enzyme de Conversion, DAPT : double anti-aggrégation plaquettaire, AC° : anticoagulation, ETT : échocardiographie transthoracique
b. Prise en charge invasive
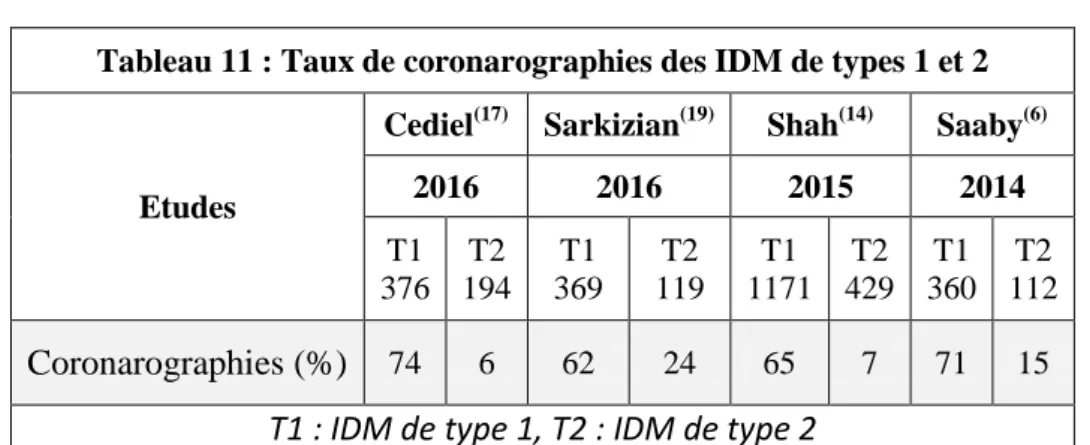
Les taux des coronarographies des IDM de types 1 et 2 sont résumés dans le Tableau 11.
Dans l’étude de Saaby(16)
, seuls 15 % des IDM de type 2 ont eu une angiographie coronaire contre 71 % des IDM de type 1.
Shah(14) en 2015 a montré que 7 % des IDM de type 2 avaient une coronarographie contre 65 % pour les IDM de type 1. A noter que 4 % des NIMI avaient une coronarographie.
En 2016, Sarkizian(19) retrouve que 5 % des IDM de type 2 ont eu une coronarographie contre 62 % pour les IDM de type 1.
Dans l’étude de Cediel(17)
en 2016, environ 6 % des IDM de type 2 avaient une coronarographie contre 74 % pour les IDM de type 1.
Tableau 11 : Taux de coronarographies des IDM de types 1 et 2
Etudes
Cediel(17) Sarkizian(19) Shah(14) Saaby(6)
2016 2016 2015 2014 T1 376 T2 194 T1 369 T2 119 T1 1171 T2 429 T1 360 T2 112 Coronarographies (%) 74 6 62 24 65 7 71 15
6. Pronostic des IDM de type 2
Dix études ont évalué le pronostic à court et moyen terme des patients admis pour un infarctus de type 2. Neuf de ces 10 études ont fait l’objet d’une méta-analyse (Gupta(15)) incluant 25 872 patients parmi lesquels 2 683 (10 %) étaient admis pour un infarctus de type 2 (Tableau 12).
Comparativement aux patients admis pour un IDM de type 1, les patients diagnostiqués avec un infarctus de type 2 présentaient une mortalité cardiovasculaire :
intra-hospitalière de 15 % contre 4,7 % (p < 0,00001) à 30 jours de 17,6 % contre 5,3 % (p < 0,0001) à 1 an de 27 % contre 13 % (p < 0,01)
Le Tableau 13 résume les données de la littérature concernant la mortalité.
Le pronostic au-delà de 1 an après une admission pour un IDM de type 2 a été décrit par Landes(20), et a montré qu’il n’y avait aucune différence significative sur les MACE entre les populations d’IDM de types 1 et 2. En revanche, la mortalité toute cause (en comparaison aux IDM de type 1), était significativement différente entre les deux populations (HR = 2,08 [1,14-3,81]).
Gaggin(13) a étudié les facteurs prédictifs indépendants du taux de mortalité des IDM de type 2 et a montré qu’un âge avancé, une pression artérielle systolique plus basse, un antécédent de coronaropathie, une insuffisance cardiaque, une BPCO, un antécédent de diabète, l’utilisation de dérivés nitrés, une glycémie élevée, le NT-proBNP et la cystatine C étaient associés à un pronostic péjoratif dans cette population.
Tableau 12 : Récapitulatif des mortalités intra-hospitalières, à 30 jours et à un an des études analysées par Gupta(15)
Item Etudes
IDM de Type1 IDM de Type 2 Poids
(%) RR IC à 95% Décès Total Décès Total M or talité in tr a -h osp italièr e Javed(8) 2009 15 143 9 64 18,1 0,75 0,34-1,61 Saaby(6) 2014 25 360 23 119 38,9 0,36 0,21-0,61 Sandoval(7) 2014 0 10 1 22 1,1 0,70 0 ,03-15,77 Stein(12) 2014 113 2691 15 127 41,8 0,36 0,21-0,59 Total (IC à 95%) 3204 332 100 0,41 0,30-0,57 Total évènements 154 48 M or talité à 30 jours Landes(20) 2015 3 107 17 106 7 0,17 0,05-0,58 Saaby(6) 2014 33 360 28 119 47,9 0,39 0,25-0,62 Stein(12) 2014 132 2691 17 127 45,1 0,37 0,23-0,59 Total (IC à 95%) 3158 352 100 0,36 0,26-0,49 Total évènements 168 62 M or talité à 1 an Baron(9) 2016 2361 17488 346 1403 56,9 0,55 0,50-0,60 Lopez(27) 2016 102 707 27 117 4,1 0,63 0,43-0,91 El-Haddad(24) 2012 28 512 84 295 9,5 0,19 0,13-0,29 Saaby(6) 2014 60 360 52 119 6,9 0,38 0,28-0,52 Shah(14) 2015 187 1171 134 429 17,4 0,51 0,42-0,62 Stein(12) 2014 220 2691 30 127 5,1 0,35 0,25-0,48 Total (IC à 95%) 22929 2490 100 0,49 0,45-0,53 Total évènements 2958 673
IDM : Infarctus du myocarde, RR : Risque relatif, IC : Intervalle de confiance. Les chiffres dans le tableau correspondent aux événements
Dans une étude récente incluant près de 4100 patients, Nestelberger(21) a montré l’impact que pouvait avoir la définition retenue pour catégoriser un IDM de type 2 sur le pronostic.
Ainsi lorsque l’on applique à cette population la définition universelle 2007 et 2012 pour identifier un IDM de type 2, la mortalité à 90 jours des IDM de type 2 selon la classification 2012 était de 0 % contre 3,6 % pour les IDM de type 2 selon la définition 2007 (p = 0,003)
Tableau 13 : Taux de mortalité des grandes études sur les IDM de type 2 Auteurs Effectifs d’IDM de type 2 Mortalité (comparée aux IDM de type 1) Remarques El Haddad(24) 2012 295 A 12 mois : RR = 6,9 (p < 0,001)
Pour le sexe féminin : RR = 1,9 ; [1,25 – 2,81] Hanson(25) 2013 22 Intra-hospitalière : 16 % vs 5 %, p = 0,38 Péri-opératoire Saaby(6) 2014 112
Suivi médian de 2,1 ans : 48 % vs 25,6 %
Après ajustement, facteurs déclenchants associés à cette surmortalité : l’âge et le choc hémodynamique Baron(21) 2016 T2- : 621 T2+ : 695 Mortalité à 4 ans :
- Avec lésions coronaires : HR = 1,72 ; [1,45 - 2,03] Après ajustement : HR = 0,76 ; [0,61-0,94] - Sans lésion coronaire : HR = 1,14 [0,84 - 1,55]
- Comparaison entre les 37 589 IDM de type 1 avec lésions coronaires et les 695 IDM de type 2 avec lésions coronaires
- Comparaison entre les 2 912 IDM de type 1 sans lésion coronaire et les 621 IDM de type 2 sans lésion coronaire Cediel(17) 2016 194 Taux de décès à 24 mois : IDM de type 2 = 39,7 % NIMI = 40 % IDM de type 1 = 19,7 % En multivarié :
- IDM de types 2 vs les IDM de types 1 : HR 1,41 ; p = 0,038 - NIMI versus les IDM de types 1 : HR = 1,54 ; p = 0,002
T2 : IDM de type 2 sans lésion coronaire, T2+ : IDM de type 2 avec lésions coronaires, RR : Risque relatif, HR : Hazard Ratio, IDM : Infarctus du myocarde, NIMI : lésions myocardiques non ischémiques
Dans une revue de littérature, Mihatov(22) a décrit le pronostic et les évènements des IDM de type 2 comparés aux IDM de type 1. Sur 100 patients/années, les IDM de type 2 présentaient significativement plus de MACE, un taux plus élevé de mortalité (toute cause ou cardiovasculaire), plus d’insuffisance cardiaque et d’arythmies. Il n’y avait pas de différence significative pour les récidives d’IDM, les atteintes périphériques et les évènements neurologiques.
L’objectif de cette thèse, sous forme d’article, sera de comparer les données démographiques, biologiques, échocardiographiques ainsi qu’angiographiques des patients admis pour un IDM de type 1 et de type 2 au CHU de SaintAntoine.
INTRODUCTION
La nouvelle définition universelle de l’infarctus du myocarde, établie en 2007(2), puis en 2012(3), a permis de préciser et d’affiner la définition de l’IDM de type 2.
L’IDM de type 2 est secondaire à une ischémie myocardique résultant d’une inadéquation entre la demande myocardique en O2 et les apports, en l’absence de rupture de plaque ou de thrombose coronaires. Les mécanismes physiopathologiques qui soutiennent cette entité sont variables et multiples. Ainsi, une dysfonction endothéliale, un spasme coronaire, une embolie coronaire, un épisode de tachycardie ou de bradycardie, une anémie, une hypotension artérielle ou une hypertension artérielle sont autant de mécanismes, suspectés ou avérés, pouvant entrainer un IDM de type 2. Il peut survenir en outre, aussi bien sur terrain préalable de coronaropathie sous-jacente ou en l’absence d’atteinte coronaire documentée.
L’objectif de cette étude est d’analyser les données comparatives démographiques, biologiques, échocardiographiques ainsi qu’angiographiques entre les IDM de type 1 et de type 2.
METHODES
1. Population de l’étude
L’ensemble des patients ayant bénéficié d’une coronarographie au CHU Saint Antoine, entre le 1er janvier 2015 et le 31 décembre 2016, a été évalué.
Les patients présentant un dosage de troponine négatif ont été exclus. Les patients admis pour un IDM de type 3 à 5 (selon la définition universelle de l’IDM de 2012) ont été exclus de cette analyse, ainsi que les patients admis pour une embolie pulmonaire, une cardiomyopathie de Tako-Tsubo ou une myocardite aigue.
Les données démographiques, biologiques, électrocardiographiques, échocardiographiques et angiographiques ont été collectées de manière rétrospective à partir des compte-rendus hospitaliers informatisés.
2. Classification des patients
La définition universelle de 2012 a été utilisée pour classer les patients(3). L’IDM de type 1 est un infarctus du myocarde spontané en rapport avec une rupture de plaque, ulcération, érosion ou dissection responsable de la formation d’un thrombus frais intra-luminal dans une ou plusieurs coronaires, ayant comme conséquence une diminution du flux via l’obstruction ou d’embols distaux induisant une nécrose myocardique. L’IDM de type 2 provient d’un déséquilibre entre demande et apport en O2 au niveau myocardique, qu’il y ait ou non des lésions coronaires sous-jacentes, avec un facteur déclenchant contribuant à ce déséquilibre (dysfonction endothéliale, spasme coronaire, embols coronaires, tachycardies, bradycardies, anémie, détresse respiratoire, hypotension, hypertension avec ou sans hypertrophie ventriculaire gauche). Les IDM de
type 3 sont secondaires aux ACR dont la cause probable est un IDM, les types 4 post-angioplastie (4a : post-post-angioplastie immédiat diagnostiqué par une augmentation de la troponine ; 4b : thromboses de stents) et les types 5 post-PAC.
Les NIMI (Non Ischemic Myocardial Injury) représentent des lésions myocardiques non ischémiques survenant chez les patients avec une affection grave sous-jacente sur fond de pathologies chroniques, sans douleur thoracique, la plupart du temps sans ou avec peu de modifications électrocardiographiques, une cinétique d’élévation de troponine en plateau, sans rupture de plaque, ni thrombus à la coronarographie
3. Détermination du diagnostic final
Chaque compte-rendu médical était analysé de manière indépendante par deux cardiologues afin de déterminer le type d’IDM (1 ou 2), en fonction des données cliniques, électrocardiographiques, biologiques et angiographiques. Etaient considérées comme significatives les lésions coronaires entrainant une réduction du diamètre luminal de plus de 50 % lors de la réalisation de la coronarographie(6) (16) (19).
L’adjudication du facteur déclenchant était réalisée à partir des données disponibles dans le compte-rendu médical. En l’absence de facteur déclenchant identifié, le patient était classé comme IDM de type 2 s’il ne présentait pas de critères permettant de retenir le diagnostic d’IDM de type 1, 3, 4, ni d’un NIMI.
4. Dosage de la troponine Ic
Le seuil de positivité pour la troponine Ic était de 0,15 ng/ml, correspondant au 99ème percentile de l’échantillon contrôle de référence.
5. Analyse statistique
Pour les comparaisons de populations, les tests du Chi2 et de Fischer ont été utilisés. Les résultats sont présentés par effectifs/pourcentages, moyennes/écart-types, ou médianes/interquartiles.
La régression logistique a été utilisée pour analyser les paramètres en rapport avec la présence de maladie coronaire : vérification de la "normalité" (et modification des variables pour qu'elles suivent une loi normale et soient pertinentes d'un point de vue clinique), régression logistique univariée et multivarié (seules les variables ayant un p < 0,2 ont été utilisées dans le modèle multivarié) et élimination pas à pas par la méthode inversée (dite « backward »).
RESULTATS
1. Population de l’étude
De janvier 2015 à décembre 2016, 881 patients du service de cardiologie de l’Hôpital Saint Antoine ont bénéficié d’une coronarographie (Figure 1). Parmi eux, 251 patients (28 %) avaient un dosage de troponine positif (> à 0,15 ng/ml). Rétrospectivement, ont été exclus dix patients (1,1 %) admis pour un syndrome coronaire aigu avec sus décalage du segment ST, 3 patients (0,3 %) admis pour un IDM de type 3, 50 patients (5,6 %) pour un IDM de type 4 et sept patients (0,8 %) pour un IDM de type 5.
De même, deux patients (0,2 %) pris en charge pour une embolie pulmonaire, 10 patients (1,1 %) pour une cardiomyopathie Tako-Tsubo, et 3 patients (0,3 %) admis pour une myocardite ont été également exclus. Dix-huit patients (2 %) ont été en outre exclus de cette étude pour des raisons diverses [2 (0,2 %) pour données incomplètes, 9 (1 %) patients ayant bénéficié de 2 coronarographies au cours de la période d’analyse, 1 (0,1 %) patient admis pour une ablation de TV, 6 (0,7 %) patients n’ayant pas eu de dosage de troponine]. La population finale de l’étude était donc constituée de 148 patients dont 52 patients (35 %) classés comme IDM de type 1 et 96 patients (65 %) classés comme IDM de type 2.
881 patients ayant bénéficié d’une coronarographie au CHU de Saint Antoine entre janvier 2015 et décembre 2016
251 patients avec une troponine positive
630 troponines négatives
52 IDM de type 1 96 IDM de type 2
103 exclusions : IDM de type 3 : 3 IDM de type 4 : 50 IDM de type 5 : 7 SCA ST+ : 10 Embolies pulmonaires : 2 Syndrome de Tako-Tsubo : 10 Myocardites : 3 Données incomplètes : 2 Pas de troponine dosée : 6 Doublons : 9
Ablation de TV : 1
2. Caractéristiques cliniques et paracliniques des IDM de types 1 et 2
Le tableau 1 détaille les données comparatives des patients admis pour un IDM de type 1 et de type 2.
La comparaison des 2 populations d’IDM montre qu’il n’existait pas de différence significative entre les 2 groupes sur l’âge, le sexe, l’IMC, ni les facteurs de risque cardiovasculaire. Les patients admis pour un IDM de type 2 souffraient plus d’AOMI (7,7 % vs 21,1 %, p = 0 ,036). Bien que plus fréquent dans la population admise pour un IDM de type 2, les antécédents d’insuffisance cardiaque et de pontages aorto-coronaires n’étaient pas significativement différents entre les 2 populations. Seuls les antécédents de FA étaient plus fréquemment représentés au sein des patients admis pour un IDM de type 2 (9,6 % vs 24 %, p = 0,033).
La présentation clinique à l’admission était significativement différente entre les 2 groupes. Les patients admis pour un IDM de type 2 consultaient plus fréquemment pour une dyspnée (45,8 % vs 13,5 % pour les types 1, p < 0,001), moins souvent pour une douleur thoracique (21,9 % vs 76,9 %, p < 0,001), étaient plus tachycardes (89 BPM vs 78 BPM, p = 0,0053) et plus hypoxiques (96 % vs 98 %, p = 0,009).
Les anomalies ECG étaient significativement différentes entres les 2 groupes. Les patients avec un IDM de type 2 présentaient plus fréquemment une FA à l’admission (16,7 % vs 1,9 %, p = 0,001). Les patients admis pour un IDM de type 2 présentaient des altérations plus marquées de la fonction rénale avec un DFG plus bas que les patients du groupe IDM de type 1 (63 ml/mn vs 85 ml/mn, p = 0,0056), un taux d’hémoglobine plus bas (13 g/dl vs 14,1 g/dl, p = 0,0007), un taux plus élevé de CRP (17 mg/L vs 3,7 mg/L) et du BNP (401 pg/ml vs 166 pg/ml). En revanche, le niveau de
troponine I mesuré à l’admission était plus bas dans le groupe IDM de type 2 comparativement au groupe IDM de type 1.
La FEVG était plus altérée dans le groupe IDM de type 2 (50 % vs 60 %, p = 0,0002). Les atteintes coronaires étaient significativement différentes entre les 2 groupes.
Soixante-trois pourcents des patients du groupe IDM de type 2 et 3,8 % des patients du groupe IDM de type 1 ne présentaient pas d’atteinte coronaire. Parmi les IDM de type 1, 50 % présentaient une atteinte coronaire monotronculaire, 30,8 % une atteinte bitronculaire et 15,4 % une atteinte tritronculaire. Par contre, chez les patients diagnostiqués avec un IDM de type 2, environ 37 % présentaient des lésions coronaires
[une (ou plus) coronaire avec une sténose d’au moins > 50 %)].
A la sortie, les patients du groupe IDM de type 2 recevaient moins fréquemment un traitement bêtabloquant (64,8 % vs 87,5 %), autant de bloqueurs du système rénine- angiotensine ou d’anti-aldostérone, moins d’aspirine (98 % vs 51,7 %) ou de double anti-aggrégation plaquettaire (22 % vs 79,6 %), mais recevaient plus fréquemment un traitement anticoagulant (39,6 % vs 18,8 %, p = 0,009).
Tableau 1 : Comparaison des données démographiques, biologiques, échocardiographiques ainsi qu’angiographiques entre les IDM de type 1 et de type 2
Population de l’étude IDM type 1
n = 52 (35 %)
IDM de type 2
n = 96 (65 %) p Données démographiques
Age (années, +/- EC) 65 ± 14 68 ± 13 0.0591
Sexe féminin (n, %) 20 (38.5) 32 (33.3) 0.533
IMC (kg/m², +/- EC) 25.9 (23.0-29.8) 25.4 (22.7-28.6) 0.6665 Facteurs de risque cardiovasculaire
Diabète (n, %) 17 (32.7) 30 (31.3) 0.857 Hypertension (n, %) 27 (51.9) 57 (59.4) 0.382 Dyslipidémie (n, %) 25 (48.1) 40 (41.7) 0.453 Tabagisme (n, %) 24 (46.2) 50 (52.1) 0.491 Hérédité coronaire (n, %) 6 (11.5) 5 (5.2) 0.195 Antécédents Atteinte périphérique (n, %) 4 (7.7) 20 (21.1) 0.036 Infarctus du myocarde (n, %) 5 (9.6) 13 (13.5) 0.485 Pontage aorto-coronaire (n, %) 1 (1.9) 10 (10.4) 0.06 Angioplastie (n, %) 3 (5.8) 10 (10.4) 0.34
Accident Vasculaire Cérébral (n, %) 4 (7.7) 17 (17.7) 0.096
Insuffisance cardiaque (n, %) 3 (5.8) 16 (16.7) 0.058 BPCO (n, %) 6 (11.5) 12 (12.5) 0.864 Cancer (n, %) 6 (11.5) 20 (20.8) 0.156 Fibrillation atriale (n, %) 5 (9.6) 23 (24.0) 0.033 Symptôme principal Douleur thoracique (n, %) 40 (76.9) 21 (21.9) <0.0001 Dyspnée (n, %) 7 (13.5) 44 (45.8) Asymptomatique (n, %) 0 7 (7.3) Lipothymie, syncope (n, %) 1 (1.9) 10 (10.4) Autre (n, %) 4 (7.7) 14 (14.6) Examen clinique PAS (mmHg, ± EC) 144 (129-157) 130 (120-154) 0.0756 PAD (mmHg, ± EC) 82 (73-92) 79 (67-90) 0.3208
Fréquence Cardiaque (BPM, ± EC) 78 (69-88) 89 (74-109) 0.0061 Saturation percutanée en O2* en %
(moyenne, +/- EC) 98 (96-100) 96 (93-99) 0.009 Post-opératoire immédiat, % 0 (0) 4 (4,2) 0,298 ECG Rythme sinusal (n, %) 51 (98.1) 71 (74.0) 0.001 FA (n, %) 1 (1.9) 16 (16.7) Autre (n, %) 0 9 (9.4)
Sous-ST ou ondes T négatives (n, %) 24 (46.2) 48 (50.0) 0.731
Ondes Q (n, %) 13 (25.0) 10 (10.4) 0.031
Biologie
Créatinine en µM (moyenne, ± EC) 82 (65-92) 93 (78-116) 0.0007 Clairance rénale en ml/min (moyenne, ± 85 (57-116) 63 (46-89) 0.0056
Hémoglobine en g/dl (moyenne, ± EC) 14.1 (13.2-15.1) 13.0 (11.4-14.4) 0.0007 CRP en mg/l (moyenne, ± EC) 3.7 (3.0-11.0) 17.0 (4.0-41.0) 0.0001 BNP en pg/ml (moyenne, ± EC) 166 (43-288) 401 (147-938) 0.0001 Troponine n°1 en ng/ml (moyenne, ± EC) 0.58 (0.15-2.20) 0.36 (0.17-0.86) 0.2006 Troponine n°2 en ng/ml (moyenne, ± EC) 1.70 (0.56-4.35) 0.43 (0.23-1.25) 0.0001 Echocardiographie
FEVG en % (moyenne, ± EC) 60 (50-60) 50 (30-60) 0.0002
Hypokinésie (n, %) 8 (15.4) 47 (49.0) <0.0001
Akinésie (n, %) 19 (36.5) 26 (27.1) 0.264
Dyskinésie (n, %) 4 (7.7) 10 (10.4) 0.771
Coronarographie
Pas de lésion significative (n, %) 2 (3.8) 60 (63)
<0.0001
Monotronculaire (n, %) 26 (50.0) 17 (18.1)
Bitronculaire (n, %) 16 (30.8) 8 (8.5)
Tritronculaire (n, %) 8 (15.4) 9 (9.6)
Atteinte d’un PAC (n, %) 0 (0) 2 (2.1)
Traitement médical à la sortie
Bêtabloquants (n, %) 42 (87.5) 59 (64.8) 0.005
IEC ou ARAII (n, %) 33 (68.8) 63 (69.2) 0.999
Aspirine (n, %) 48 (98.0) 47 (51.7) <0.0001
Double anti-aggrégation plaquettaire (n, %)
39 (79.6) 20 (22.0) <0.0001
Anticoagulants (n, %) 9 (18.8) 36 (39.6) 0.009
IMC : Indice de masse corporelle, BPCO : Bronchopneumopathie chronique obstructive, PAC : Pontage Aorto-Coronaire, PAD : Pression Artérielle Diastolique, PAS : Pression Artérielle Systolique, CRP : Protéine C réactive, BNP : Peptide Natriurétique, FEVG : Fraction d’Ejection du Ventricule Gauche, IEC : Inhibiteurs de l’Enzyme de Conversion, ARAII : antagoniste de l’Angiotensine II.
Les résultats sont présentés par nombre (n) et pourcentage (%), moyenne +/- écart-type (EC) et médiane (25è – 75è percentile) en adéquation avec le type de variable
3. Facteurs déclenchants des IDM de type 2
Les principaux facteurs déclenchants identifiés dans le groupe IDM de type 2 (Tableau 2) étaient les troubles du rythme supraventriculaire (23 %), une détresse respiratoire (19 %) et l’insuffisance cardiaque (15 %). A noter que l’anémie représentait 7 % des facteurs déclenchants et le sepsis 4 %. Les mécanismes multiples représentaient un patient sur quatre.
Tableau 2 : Facteurs déclenchants des IDM de type 2
Facteurs déclenchants IDM de type 2 n = 96 (65 %)
Anémie (n, %) 7 (7)
Tachyarythmie (n, %) 22 (23)
Détresse respiratoire (n, %) 18 (19)
Décompensation cardiaque (n, %) 15 (15)
Infection (autre que pulmonaire) (n, %) 4 (4)
Choc ou hypotension (n, %) 4 (4)
Mécanismes multiples (n, %) 26 (27)
4. Caractéristiques cliniques et paracliniques des IDM de 2 en fonction de la présence ou de l’absence de coronaropathie sous-jacente
Le Tableau 3 détaille les données comparatives entre les IDM de type 2, en fonction de la présence ou de l’absence de coronaropathie sous-jacente.
La comparaison des données démographiques des deux populations de patients d’IDM de type 2 avec et sans atteinte coronaire montre que les patients avec atteinte coronaire étaient plus âgés, plus fréquemment diabétiques ou hypertendus, et présentaient plus d’antécédents de cardiopathie ischémique (angioplastie coronaires ou IDM).
La présentation clinique, les données de l’examen clinique et de l’ECG n’étaient pas significativement différentes entre les 2 groupes.
Les patients du groupe IDM de type 2 avec atteinte coronaire présentaient une altération plus marquée de la fonction rénale, un taux d’hémoglobine et de CRP plus bas que les patients indemnes d’atteinte coronaire. Les deux sous-groupes avaient un niveau comparable de taux de troponine I. En revanche, le taux de BNP était significativement plus élevé dans le groupe avec atteinte coronaire.
D’un point de vue échocardiographique, les patients du groupe IDM de type 2 avec lésions coronaires avaient en moyenne une FEVG plus altérée (39 % vs 53 %, p = 0,01). Parmi les 36 patients (37 %) des IDM de type 2 avec coronaropathie sous-jacente, 17 (47,2 %) étaient monotronculaires, 8 (22,2 %) bitronculaires et 9 (25 %) tritronculaires. A la sortie d’hospitalisation, les IDM de type 2 avec lésions coronaires recevaient significativement plus d’aspirine (84,4 % vs 33,9 %, p < 0,0001) et de double anti-agrégation plaquettaire (50 % vs 6,8 %, p < 0,0001). Il n’y avait pas de différence significative sur le niveau d’anticoagulation curative entre les 2 groupes. En outre, les