HAL Id: tel-01180203
https://hal.archives-ouvertes.fr/tel-01180203
Submitted on 24 Jul 2015HAL is a multi-disciplinary open access
archive for the deposit and dissemination of sci-entific research documents, whether they are pub-lished or not. The documents may come from teaching and research institutions in France or abroad, or from public or private research centers.
L’archive ouverte pluridisciplinaire HAL, est destinée au dépôt et à la diffusion de documents scientifiques de niveau recherche, publiés ou non, émanant des établissements d’enseignement et de recherche français ou étrangers, des laboratoires publics ou privés.
Devenir des polluants métalliques associés aux sédiments
contaminés dans un cours d’eau en relation avec la
dynamique sédimentaire
Mathilde Zebracki
To cite this version:
Mathilde Zebracki. Devenir des polluants métalliques associés aux sédiments contaminés dans un cours d’eau en relation avec la dynamique sédimentaire. Chimie. UNIVERSITE PARIS-SUD XI, 2008. Français. �tel-01180203�
UNIVERSITE PARIS-SUD XI
E.D. RA YONNEMENTSETENVIRONNEMENT
THESE
pour
obtenir le grade de
DOCTEUR
Chimieprésentée
et soutenuepubliquement
par
Mathilde ZEBRACKI
le 23
juin 2008
Devenir
des
polluants
métalliques associés
auxsédiments contaminés dans
un coursd'eau
enrelation
avec
la
dynamique
sédimentaire
Directeurdethèse(LSCE) :Philippe BONTE
EncadrantEcole desMines: Claire ALARY
JURY Eric SIMONI Daniel THEVENOT Jean-Claude FISCHER Olivier RADAKOVITCH JanuszDOMINIK Président Rapporteur Rapporteur Examinateur Examinateur
REMERCIEMENTS
Les travaux présentés dans ce manuscrit ont pour l'essentiel été réalisés au Centre
National de Recherche sur les Sites et Sols Pollués (CNRSSP). Le CNRSSP était alors un
Groupement d'Intérêt Public (GIP) né d'un partenariatentredifférentes institutions et sociétés privées et situé sur le centre de recherche de l'Ecole des Mines à Douai. Ses priorités de
recherche concernaient la caractérisation, la mobilité et l'impact des polluants dans
l'environnement. Créé enmai 1996, le CNRSSPne survivrapasàsondixième anniversaireet
leGIP entrera enliquidation administrativeenjanvier2007.
Je remercie Pascal Oustrière, Directeur du CNRSSP, et Agnès Laboudigue, Directrice
scientifique, pour m'avoir accueillie au laboratoire en 2004. Je souhaite exprimer toute ma
reconnaissance à Jean-PaulMonory, liquidateur du GIP, dont le soutienauraétéprécieux.
Pour mener à bien ce travail de thèse,j'ai bénéficié de l'encadrement scientifique de
Philippe Bonté (LSCE), Directeur de thèse, et de Claire Alary (ENSM Douai), encadrante au
CNRSSP. Je leur sais gré de leur investissement et de leur accompagnement tout au long de
cette aventureintellectuelle ethumaineunique.
Je remercie Messieurs Jean-Claude Fischer (USTL) et Daniel Thévenot (CEREVE),
rapporteurs, pour leur regard éclairé et leurs critiques constructives, Messieurs Janusz
Dominik (Institut Forel) etOlivier Radakovitch (CEREGE), examinateurs, pour leur attention
et l'intérêt qu'ilsont portés à cetravail et,enfin, Eric Simoni (IPNO) d'avoir accepté d'être le
président de jury.
Je souhaite exprimer ma profonde gratitude envers tous ceux et toutes celles qui ont
contribué àl'aboutissement decetravail. Ungrand merci...
à Vincent Ledoux de la Société des Eaux de Douai, au personnel des Voies
Navigables de France et de la Communauté d'Agglomération du Douaisis pour
l'ensemble des informations transmises ;
au personnel des départements de l'Ecole des Mines pour sa disponibilité et son
soutientechnique ;
à toute l'équipe du LSCE pour son accueil chaleureux, son soutien technique et
analytique,enparticulier Irène, Marie-Françoise,etAlain ;
tous les cneursspiens et cneursspiennes dont l'esprit d'équipe est inoubliable et
dont le talent collectif peut transformer une coupure de courant électrique en
véritable carnaval, et avec dans le rôle des carnavaleux...Manon, Géraldine,
Stéphanie, Isabelle, Valérie & Valérie, Caroline, Laurence & Laurence, Gwen,
Mélanie,Philippe, Terence,Virginie, Bertrand, Vasilica, Florent, Cindy.
Je salue mes compagnons d'étude, de gloire, de fortune et de voyage aux Mines de
Douai : Guilaine, Philippe, Christophe & Christophe, Simon, Samira, Paul, Mohamad,
Amine, Guillaume.
Il est des régions qui méritent d'être traversées sans quoi on ne connaît pas l'histoire d'un pays. Le ch'Nord en fait résolument partie. Merci à tous ceux et toutes celles qui m'ont
permis d'y faireuntiot trou etde m'y sentir bien. C'est uneexpérience dont le souvenir m'est particulièrement agréable. Et,jesais..., je sais quebeaucoupontveillé surmoi...
TABLE DES MATIERES
INTRODUCTION 19
1 SYNTHESEBIBLIOGRAPHIQUE 23
1.1 LESMETAUX DANSLESYSTEMEAQUATIQUE 23
1.1.1 Originedes métaux dans les milieuxaquatiques 24
1.1.1.1 Naturelle 24
1.1.1.2. Anthropique 26
1.1.2 Distribution des métaux dans les milieuxaquatiques 27
1.1.2.1 Dansl'eau 27
1.1.2.2 Dans les sédiments 29
1.1.3 Réactivitédes métaux dans les sédiments 32
1.1.3.1 Spéciation chimique:méthodes 32
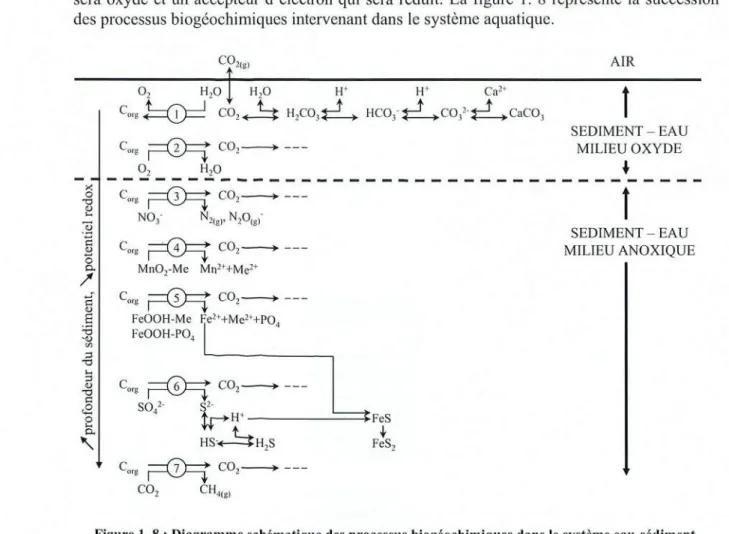
1.1.3.2 Mécanismes de fixation 34
1.2 Transfertdes métauxal'interfaceeau-sediment 37
1.2.1 Dansunsédimentnonperturbé 38
1.2.1.1 Diagenèse des sédiments 38
1.2.1.2 Diffusion à l'interface eau-sédiment 42
1.2.2 Dansunsédimentperturbé. 46
1.2.2.1 Etudesenmilieu naturel 46
1.2.2.2 Etudesaulaboratoire 47
1.2.2.3 Revue desprincipaux mécanismes 48
1.3 Rolede ladynamique sedimentaire.Utilisationdes traceurs environnementaux. 52
1.3.1 Les processussédimentaires 53
1.3.1.1. Lasédimentation 53
1.3.1.2. La remiseensuspension/l'érosion 54
1.3.2 Lestraceursradioactifsenvironnementaux 57
1.3.2.1. Différentesorigines 57
1.3.2.2. Détermination des activités dans les matrices naturelles 62
1.3.2.3. Notion detraçage 62 1.3.2.4 Applications 63 1.4 Conclusions 66 2 MATERIELS ET METHODES 69 2.1 Contextedel'etude 69 2.2 Presentationde laScarpe 70 2.2.1 Situationgéographique 70
2.2.2 Descriptiondu bassinversant 71
2.2.3 Leseauxdesurface 73
2.2.4 Secteurétudié 74
2.2.4.1 Sources depollutionlocales 74
2.2.4.2 Hydrologie 78
2.3 Choixdes sites de prelevement.Rappeldes objectifs 80
2.3.1 Carottage 80
2.3.2 Suivideterrain 80
2.3 prelevementet echantillonnage des solides 83
2.3.1 Sédiments 83
2.3.2 Matièresensuspension 86
2.4 Traitementetanalyse des échantillons solides 87
2.4.1 Mesuredemassevolumique 87
2.4.2 Distributiongramilométriquepargranulométrielaser 88
2.4.2.1 Principe 88
2.4.2.2 Manipulation 89
2.4.2.3 Influence des ultrasons 89
2.4.3 Activitésdesradionuclides émetteursgamma 90
2.4.3.1 Principe de laspectrométriegamma 91
2.4.3.2 Manipulation 92
2.4.4 Activitésdes radionuclides émetteursalpha 92
2.4.4.1 Principe de laspectrométriealpha 92
2.4.4.2 Manipulation 93
2.4.5 Dosagedes métauxetmajeursparICPAES 93
2.4.5.3 Dosagede la fraction pseudo-totale
2.4.5.4 Dosage de la fraction réactive desmétaux
2.4.6 MesuredesteneursenC, N, S
2.4.6.1 Dosage du carbone organique total
2.4.6.2 Dosage de l'azote
2.4.6.3 Dosage du soufre total
2.5 Analysedes eaux interstitielles
2.5.1 Echantillonnage desmétauxcontenusdansleseauxinterstitielles: Technique DET
2.5.1.1 Principe
2.5.1.2 Manipulation
2.5.2 Dosagedesmétaux
2.5.2.1 Principe de l'ICP MS
2.5.2.2 Limite dequantificationetreproductibilité
2.5.2.3 Influencedutempsdepose
2.5.2.4 Comparaisonentredeuxméthodes d'échantillonnage
2.5.3 Mesurede02etN20dissous, pH,Eh
2.5.3.1 Principe
2.5.3.2 Manipulation
2.5.3.3 Test dereproductibilité
2.5.3.4 Influence duprotocole: casd'02
2.6 Récapitulatif
3 DYNAMIQUE SEDIMENTAIREALONG TERME ETCONTAMINATION DES SEDIMENTS
3.1 caracterisation physique des sediments
3.1.1 Teneuren eau
3.1.2 Distributiongranulométrique
3.2 Agedes sediments
3.2.1 Rappels
3.2.2 137Cs
3.2.3 2,0Pb
Conclusion
3.3 Contaminationdes sedimentsde laScarpe
3.3.1 Lesmétaux
3.3.1.1 Concentrations moyennes
3.3.1.2 Degré de contamination
3.3.1.3 Profils verticaux
3.3.1.4 Historique de la pollution métallique
3.3.2 Lecarboneorganique
3.3.3 L'uranium
3.3.4 Rôledusoufre
Conclusion
4. DYNAMIQUE SEDIMENTAIREA COURT TERME
4.1 Ala recherched'unoutilradioactif
4.1.1 Ledéséquilibreradioactif234Thxf38U
4.1.2 Ledéséquilibreradioactif2"'Pox/wPbss
4.1.2.1 Description de la méthode radioactive: revuebibliographique
4.1.2.2 Caractérisation des sédiments de surfaceetdes matièresensuspension
4.1.3 LeBér)>llium-7
4.1.3.1 Méthode duBéryllium-7: revuebibliographique
4.1.3.2 Pénétration verticaledu7Bedans lessédiments
Conclusion
4.2 Dynamiquesedimentairemensuelle des sediments de surface
4.2.1 Enregistrementdu7Bedanslessédiments desurface
4.2.1.1 Détermination de l'inventaire du7Bedans les sédiments
4.2.1.2 Profils verticaux de l'inventaire du7Bedans lescarottes
4.2.1.3 Inventaires de7Bedans les sédiments
4.2.2 Activitésdu7Bedans les matièresensuspension
4.2.4 Tauxdedépôtetd'érosion dessédimentsde surface
4.2.4.1 Résultatsetsuivitemporel
4.2.4.3 Hydrologie Conclusion 94 _ 96 96 96 _97 _ 97 97 97 _ 98 98 99 100 100 101 104 105 105 106 106 107 109 112 112 112 115 118 118 119 122 129 131 131 131 132 134 145 146 149 153 156 160 161 161 163 163 163 165 165 168 168 169 169 169 169 173 176 180 180 183 187
METALLIQUES A L'INTERFACEEAU-SEDIMENT 188
5.1. Transfertparticulaire-particulaire 189
5.2. Transfertparticulaire-dissous.Remobilisation 190
5.3. Transfertdissous-dissous:Paradvection 192
5.4. Transfertdissous-dissous: Pardiffusion.Mécanismes diagenetiques 194
5.4.1 Caractérisationdeseauxinterstitielles. Mécanismesdiagénétiques. 194
5.4.1.1 Eh, 02,N20, pH 195
5.4.1.2 Concentrations des métaux dans leseauxinterstitielles 200
5.4.1.3 Rôle des sulfures 203
5.4.2 Evolutiondeséchangesau coursdutemps. 205
5.4.2.1 Concentrations des métaux dans leseauxinterstitielles 205
5.4.2.2 Remobilisation des métaux dans les sédiments.Rôledu Mn. 211
5.4.2.3 Diffusionetdynamique sédimentaireà l'interface eau-sédiment. 213
Conclusion 216
CONCLUSION GENERALE ET PERSPECTIVES 219
REFERENCES BIBLIOGRAPHIQUE 223
LISTE DES FIGURES
Chapitre 1
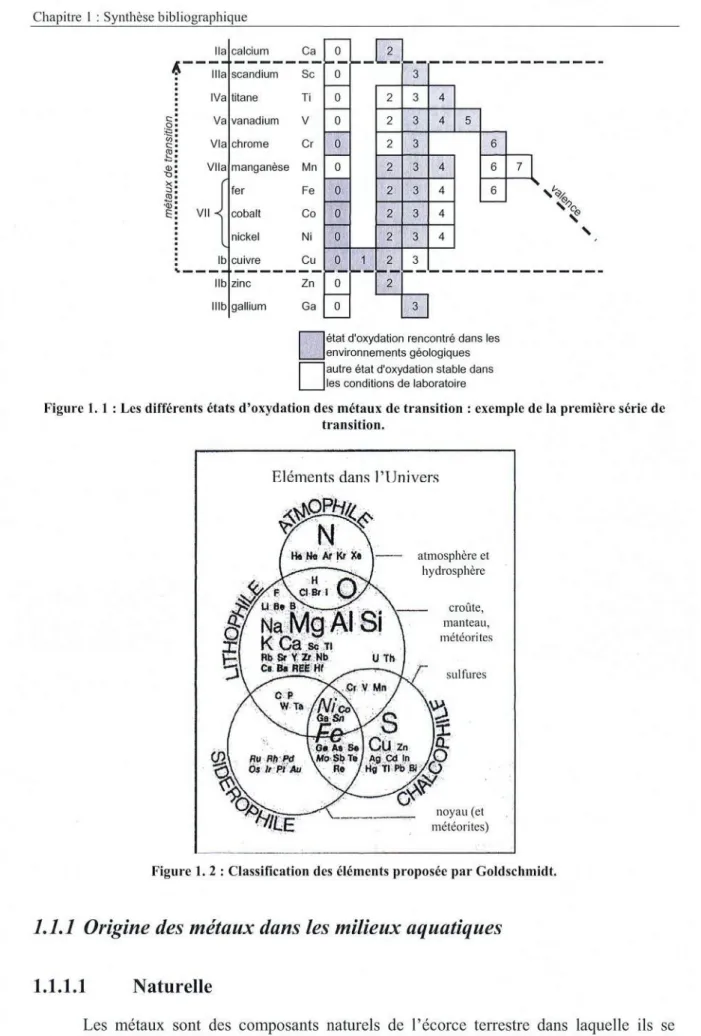
Figure 1.1: Lesdifférents étatsd'oxydationdesmétaux de transition:exemplede lapremiere
serie detransition. 24
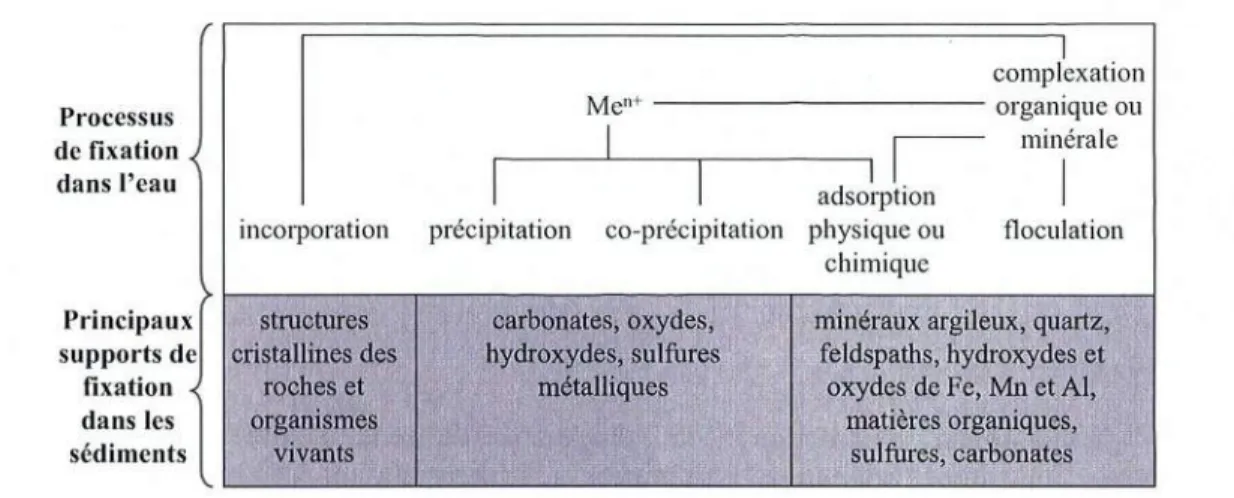
Figure 1.2: Classificationdes elements proposéeparGoldschmidt. 24
Figure 1.3: Relation typique entre la concentration en zinc adsorbe en fonction du diametre de la
particule sedimentaire.Adapte d'aprèsWestricht( 1986). 28
Figure1.4: Classification granulometrique en fonction du diametre apparent(en hm)des
particulesinorganiques.Adapted'après Calvet (2003). 30
Figure1.5: Mécanismesde transfertdes cationsmétalliques(Men+)auxsediments.Adapte d'après
Lebreton(1996). 34
Figure1.6: Influencedu potentielhydrogéné et du potentield'oxydoreductionsur la mobilité des
elements tracesmetalliques(en l'absencede matiereorganique). (a)les principaux mineraux
controlant lasolubilite desmetaux.(b)les tendances a augmenter la solubilite.D'apres
BourghetLoch(1995). 35
Figure1.7: Transportettransformation des contaminants dans les sediments.Adapte d'après
EggletonetThomas(2004). 38
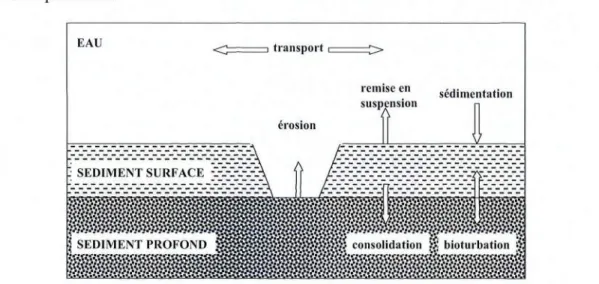
Figure1.8: Diagramme schématique des processus biogeochimiques dans le système eau-sediment.
Adapted'après Fôrstner(1995). 1 -Photosynthèse, 2-mineralisationen milieu oxyde,
3-denitrification,4-reductionduMn, 5-reductionduFe,6-reductiondes sulfates, et
7-methanisation. 39
Figure 1.9:Profildeconcentrations dans leseauxinterstitielles.Casdes sedimentsd'eaudouce
(LacMichigan). Adapted'apresNealsonetStahl(1997). 40
Figure1. 10: Sequencedesreactions redox dans les sediments de surface.Adapte d'aprèsSantschi
et al.(1990). 41
Figure1.11: Representation schématique des étapes dans la décroissance du potentiel redox en
fonctiondutemps.Cas A:système ferme sansperturbation.Cas B :système soumis a
perturbation.Adapted'après Fôrstner(1995). 42
Figure1.12:Representationschématique del'interfaceeau-sediment.Enordonnée, distance
verticale entre eau etsediment, et enabscisse, concentrationd'unsolute dans la colonne
d'eauet les eaux interstitielles.Adapted'âpres Lerman(1978). 43
Figure 1.13:Exemple d'unsystème horséquilibré. 44
Figure1.14:Diminutionde laconcentrationenmétaux dans lessediments en relation avec les
processus de depot etd'erosion. adapte d'apres fôrstner(1995). 47
FigureI. 15:RemobilisationduZndes sediments del'Elbe. Adapte d'aprèsCalmanoet al. (1993). 48
Figure 1.16Representationschématique des principauxprocessus de transport des particules.
Adapted'après LijklemaèT/IZ,.(1994). 52
Figure 1.17 :Diagramme empirique deHjulstrôm. 53
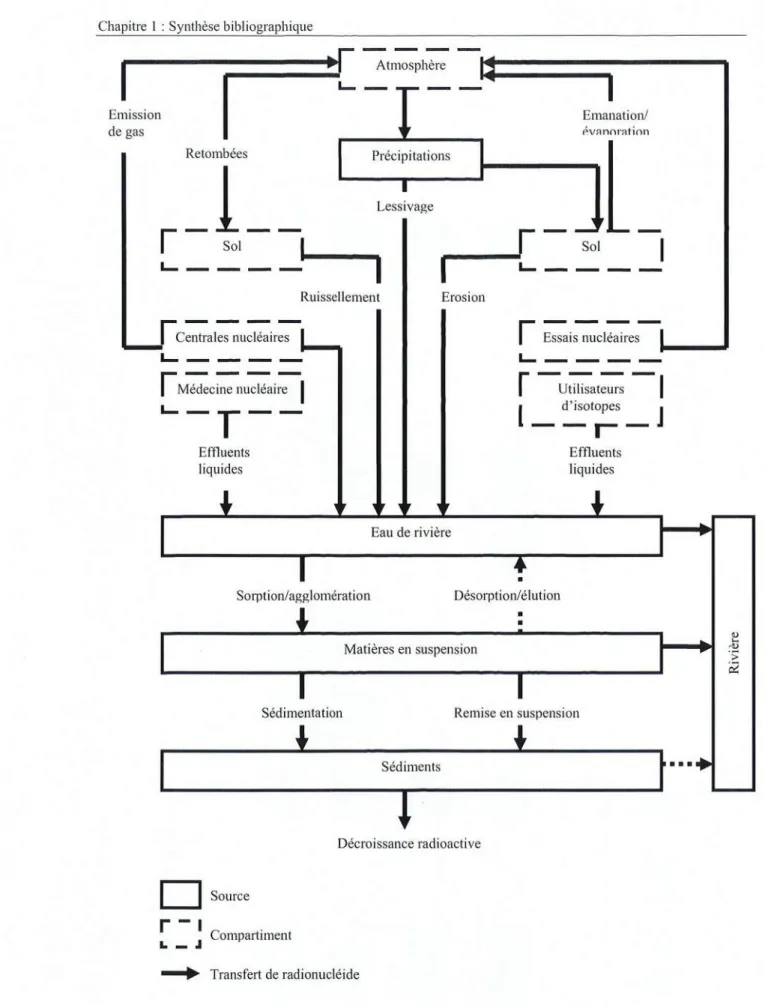
Figure 1.18:Modesdetransfertdes radionucleidesd'originenaturelleetartificielle dans une
riviere.Adapted'après Mundschenk(1995). 59
Figure 1.19:Lestrois grandes familles radioactives :238U,232Thet235U.Lesdifférentes couleurs
sontattribuees auxproprietesdes isotopes dans les conditionsenvironnementales(oxydees). 60
Figure 1.20 :Activitésdui37Csdans les sols enEuropeenMai 1986. D'après VanderPerk.et al.
(2000). 61
Chapitre 2
Figure 2.1 :Localisationdu bassinversant de laScarpe(en violet)et de lasectiondecanal
etudiee.Adapte d'après l'Agencedel'Eau Artois-Picardie. 70
Figure2.2 :Schemasimplifie des canaux. Localisationdu secteurd'etude. 71
Figure 2.3: Representation schématique de la sectiondecanal etudiee. 74
Figure 2.4 :Stationde relevage«ValleedeScarpe».Agauche:arrivée des eaux danslastation.
Adroite:rejet dans lascarpe inferieure. 76
Figure2.5 :Schema d'alimentationde la station de relevage«ValleedeScarpe».Source:
CharbonnagesdeFrance. 77
Figure2. 6 :Contaminationdes sols enPb. Localisationde laStationdeRelevage(= SR)«Vallee
Figure2.8 :Relationentre le debit mesureauniveau del'ecluse«FortdeScarpe»(Ecluse amont), de lastationd'epuration(STEP)et de la station de relevage«valleedescarpe»(SR
vallee),et lapluviometrie. 80
Figure2.9 : SectiondeScarpe Inférieure. Localisationdesrejets,affluent,pluviomètres(croix),
etsitesdeprelevement(ronds). 82
Figure2. 10:Tubespour prelevement de carottes.Degauche a droite:grand(H: 1 m)etpetit(H:
30cm)tubes,carotte a grand diametre(II :60 cm). 84
Figure 2. 11 : Agauche: accessoiresducarottier petit diametre(57/63 mm). Adroite:tetecoupante
du carottieravecmembrane. 84
Figure2.12: Systèmed'extrusionapressionhydraulique.Prelevementa laspatule eta lacuiller.
84
Figure2.13 : Representationschématique du prelevementd'unecarotte en3 exemplaires(ou
replicats)et du decoupage de chaque carotte. 85
Figure 2.14: Echantillonsde la carottek13. Degaucheadroite :tranches0-2cm a30-32 cm, par
tranche de2cmd'epaisseur. 85
Figure2.15: Echantillonsdediesal'extractionde la fractionpotentiellement disponible des
metauxdans les sediments.Agauche :echantillon de profondeur.Adroite :echantillon de surface.ladifferencedecolorationest nette ettemoigne des conditions oxydee(en surface)
etreduite(en profondeur)du milieu. 86
Figure 2.16:Piegeasediments.Dispositifpermettant larecuperationdesMES. 87
Figure 2.17:Emplacementdupiegea sedimentinstalleal'entreede lastation de relevage
«ValleedeScarpe». 87
Figure2. 18 :Schemade fonctionnement du pycnometre a helium. 88
Figure 2.19: Exemplede ladistributiongranulometrique obtenuepour un échantillon desediment
prelevee ensurface enk.36dans lascarpe. 89
Figure 2.20:Profilverticalde ladistributiongranulometriquedes sediments preleves en k13. A
gauche, le sediment a ete mis en suspension dansdudefloculant.Adroite, le sediment a subi
desUltraSons(= US)avantd'etremis en solution dans du defloculant. 90
Figure 2.21 :Spectrometregamma.CristaldeGe HPapparentet cryostat. 91
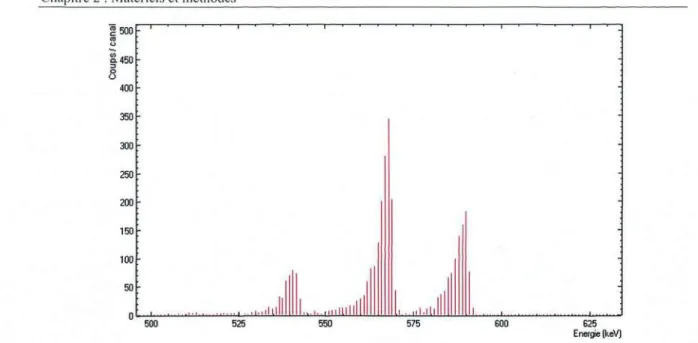
Figure2.22 :Exempled'unspectre gamma obtenupour unéchantillon de sediment preleve dansla
Scarpe. 92
Figure2.23 :Exempled'unspectrealpha obtenu pour unéchantillondesedimentprelevedansla
Scarpe. . 93
Figure 2.24: Schemadeprincipedel'ICP AES 94
Figure 2.25: Comparaison ICP AESet spectrometriegamma. 95
Figure 2.26 :Equilibrede laconcentrationen metal dissous entrel'eauinterstitielleet legel. 98
Figure2.27:Sonde DETavant(agauche)etaprès insertion(a droite)dans le sediment preleveen
k36. 99
Figure2. 28 :Schemade fonctionnement del'ICP MS. 100
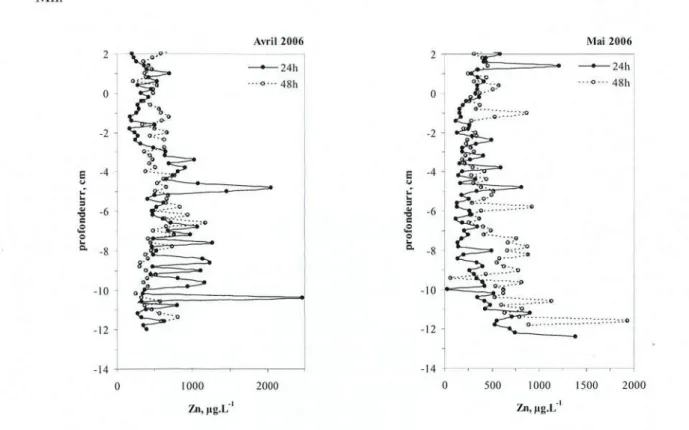
Figure 2.29:Profilsverticaux des teneurs enZndans leseauxinterstitielles des sediments
preleves enk.36enavril et mai2006. apres 24et48 h de pose dans lesediment. 102
Figure2.30:Profilsverticauxdes teneurs enMndans les eauxinterstitielles des sediments
preleves enk.36enavrilet mai2006. apres 24 et48heuresdepose dans le sediment. 103
Figure 2. 31 :Schemadu dispositifde mesure. 106
Figure2.32: Dispositifdemesureavec microelectrode dans les eaux interstitielles du sediment.
106
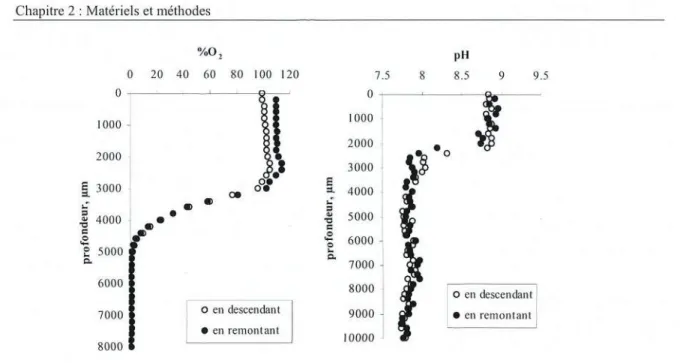
Figure2.33: Evolutiondel'oxygeneet dupHdansunecarottede sediment.Influencede la
montee/descente. 107
Figure2.34: Profilverticalde laconcentration en oxygéné dissousdansles sediments de la
Scarpeprelevesenk.36en juillet2006. Mesurerealiseeavec/sanséclairage direct de
l'interfaceeau-sediment. 107
Figure 2.35 : Profildel'oxygenedans une carottedesediment.Influencedel'arrivee d'air. 108
Figure2.36: Déroulementdescampagnes, typed'échantillonsprelevesdans laScarpe,elements
analyses, instrumentation analytique. 110
Chapitre 3
Figure 3.1 :Representationdu secteurd'etude. Localisationdel'affluent«LaCunette»,des
(=RI). Localisationdes8sites de prélèvementsk06, k09, k13, k16, k22, k.36, k.47et
k.49. 112
Figure 3.2:Teneuren eau en fonction de la profondeur dans les sediments. 113
Figure3.3: Distribution granulometrique en fonction de la profondeur dans les sediments. 116
Figure3.4: Activitésenl37Csen fonction de la profondeur dans lessediments. 120
Figure3.5 :Variationdesactivités en i37Csenfonction de lafractiondesparticulesfines. 122
Figure 3.6 :Activitésdu2I0Pbtotalet du226Raen fonction de laprofondeur dans les sediments. _ 123
Figure 3.7 :Variationdel'activitédu2I0Pbxsen fonction de laprofondeur dans lessediments._ 126
Figure3. 8 :Variationdeln[A(2I0Pbxs)]enfonction de la profondeur de carotte. 127
Figure 3.9: Representation schématique des sediments de laScarpeen fonction de leurs propriétés
physiqueset de leurage. 130
Figure 3.10: ConcentrationenZnenfonction de la profondeur dans les sediments. 135
Figure3.11: ConcentrationsenPbenfonction de laprofondeur dans les sediments. 136
Figure 3. 12:ConcentrationsenCdenfonction de la profondeur dans les sediments. 137
Figure3. 13:ConcentrationsenCuenfonction de la profondeur dans les sediments. 138
Figure 3. 14 :ConcentrationsduZn,Pb, CdetCuen fonction de la profondeur massique dansles
sedimentspeucompactesetrecents. 141
Figure3. 15 :Relationentre leZnet lePb, leCunormalises al'Aldans les sediments peu
compactes. 143
Figure3.16: Evolutionde laconcentrationenCddans les sediments peu compactes etrécents en
fonction de laprofondeur et du site echantillonne. 144
Figure3. 17 :Evolutiondel'index igeode la contaminationmétallique enfonction delà
chronostratigraphie sedimentaire(deduitedul37Cs)enk22etk.36. 145
Figure3.18 :Evolutionde la teneur enCarboneOrganique Total (= COT)en fonction de la
profondeur dans les sediments. 147
Figure3.19:Relationentreles concentrationsenZn-Cuet leCarboneOrganiqueTotal(= COT)
dans les sedimentspeucompactes. 149
Figure3.20:Relationentreles activitésdu234Th(= U)et du228Th(=Th)dans les sediments.Dans
lacroutesuperficielle,les pointss'alignentsur une droite de pente0,8. 150
Figure3.21 :Relationentre les activitésdu226Raet du234Th( U)dans lessediments.Lorsquele
226RAet son pere le238U (=234TH)sont a l equilibre seculaire, le rapportD'activitesvaut1(i.e.
pente=1). 150
Figure3.22 :Relationentre les activités du228Raetdu228Thdans les sediments. 151
Figure3. 23 :Rapport d'activités234Th/226Raen fonction de la profondeur dans les sediments. 152
Figure3. 24:Relationentrel'excesd'UetleCuet leCOTdans les sediments peu compactes. 153
Figure3.25: ConcentrationsduSen fonctionde laprofondeur dans les sediments. 154
Figure3.26: Variationde la teneur enSen fonction de la teneur enCOTdansles sediments. 155
Figure 3.27 :Variationdes teneurs enZnenfonctionde la teneur enSdansles sediments. 156
Chapitre 4
Figure 4.1 : Representation schématique desprocessus sedimentairesdansun milieuaquatique :
colonned'eau,compartiment sedimentaire, interface eau-sediment etmatieresEn suspension
(=MES). 160
Figure 4.2: LaScarpe Inférieure. Representationdu secteurd'etude. Localisationdel'affluent
«LaCunette»,des rejets de laStationd'Epuration (=STEP),desStationsdeRelevage(=SR)
etdesRejets Industriels(=RI). Localisationdes3sites de prelevementk13, k16 etk36. 161
Figure4.3 : Representationschématiquedustock de7Bedansunecarotte de sediment entre deux
collectes successives(Mois 1 & 2). Troiscas de figure:(a), (b)et(c). Source:modified'après
GiffinetReideCorbett(2003). 167
Figure4.4: Representation schématique des profils verticaux del'inventairedu7Bedans les
tranches0-3cm et3-5cm des sediments.(a) accumulationrecente de sediment.(b)
Accumulationmoindre desediment,(c)Processusdemelange,(d) Depotde sediment age sur
dusediment plus recent.(e) erosionou depot desedimentage. 17 1
Figure4.5: Evolutiondustock, nouveaude7Bedans les sedimentsen k13, k16etk.36,entre mai2005
etaoût2006. 175
Figure4.6: Activitésdu7Bedans les matières en suspension preleveesenk13,k16etk36,et pluie
cumulee entre avril2005etaout2006. 177
Figure 4.7: Evolutionde la pluie au cours dutemps :pluiequotidienne, et pluie cumulée sur la
etaout2006. 182
Figure 4.9: Evolutionduflux dedepot/erosiondans les sediments prelevesenk16entreavril2005
etaout2006. 182
Figure 4.10: Evolutionduflux dedepot/erosiondans les sediments preleves enk36entreavril
2005et aout2006. 182
Figure4.11: Debitsdel'ecluseet de lastation derelevage, etpluviométrie, entre avril2005et
aout2006(premieredonnee en mai2005). 184
Figure4.12: Variationde lapluviométrieet du debit ducanalparjourentre avril2005etaoût
2006. 185
Figure4.13: Volumedeverse par lastationderelevage et pluviométrie par jourentreavril2005
etseptembre2006. 185
Figure4. 14 :Dynamiquesedimentaireacourt-terme enk.13,Kl6etk36,et debit moyen ducanal et
de lastation(x 4),entre mai2005et aout2006. 186
Chapitre
5
Figure5.1 :Representation schématique des flux particulaire(depot, erosion)et dissous
(diffusion, advection)des polluants metalliques al'interfaceeau-sediment dans un cours
d'eau. 188
Figure 5.2 :Representationdu secteurd'etude. Localisationdel'affluent«LaCunette»,des
rejets de laStation d'Epuration(=STEP),desStationsdeRelevage (=SR)etdesRejets
Industriels(=RI). Localisationdu site de prelevementk36. 189
Figure 5.3 :Fractionreactive desmétauxcontenus dans les sedimentsdesurface(0-3 cm)preleves
enk36entre marsetjuillet2006. 191
Figure5.4 :Evolutiondela hauteur des sedimentsaffectespar les processus dedepot/erosionen
k36entre decembre2005et aout2006. 193
Figure 5.5 :EvolutiondupotentielredoxEhavec la profondeur dans lessediments prelevesen
k36,en mars et avril2006. 195
Figure5.6 :Evolutionde la concentration en oxygéné dissous avec la profondeurdans les
sediments preleves enk.36enmars, avril, mai et juillet2006. 196
Figure 5.7 :Evolutionde la concentration enN20aveclaprofondeur dans les sediments preleves
enk36en mars2006. 197
Figure 5.8 :EvolutiondupHavec la profondeur dans les sediments preleves enk36enmars,avril
et mai2006. 197
Figure5.9 :Concentrationdel'oxygeneen fonction de la profondeuraproximité del'interface
eau-sediment. 199
Figure 5.10 :Evolutiondu fluxd'oxygeneal'interfaceeau-sedimentenk36entre mars et juillet
2006. 199
Figure5.11:Profilsverticaux des concentrations duFe, Mn, Zn, PbetCddans les eaux
interstitielles des sediments preleves enk36en aout2006. 200
Figure 5.12: Surface(a gauche)etprofil(a gauche) d'unecarotte de sediment prelevee enk36.
Presencedecanaux(a gauche)et de bulles de gaz(a droite). 202
Figure5.13: Interfaceeau-sedimentd'unecarotte de sediment prelevee enk.36. Formation
d'hydroxydedeFe(III)decouleur rouille a la surface des sediments.Agauche,1 heure apres
le prelevement.Adroite,4semaines apres le prelevement, avec conservation al'airlibre.204
Figure5.14: Evolutionde la concentration duZnavec la profondeur dans les sediments preleves
enk36entre avril etaoût2006. 206
Figure5.15:Evolutiondelaconcentration duPbavec la profondeur dans lessediments preleves
enk36entre avril etaoût2006. 207
Figure 5.16: Evolutionde laconcentrationduCdaveclaprofondeurdans lessediments preleves
enk.36entre avril et août2006. 208
Figure 5.17: Evolutiondela concentration duCuaveclaprofondeurdansles sediments preleves
enk.36entre avril etaoût2006. 209
Figure5.18: Evolutiondu flux dediffusion duMnatraversl'interfaceeau-sediment entre
decembre2005et aout2006. 211
Figure 5.19:Evolutionde laconcentration duMnavec laprofondeur dans les sediments preleves
enk.36entre avril et aout2006. 212
Figure5.20 : Variationdu flux deMnal'Interface Eau-Sediment(=IES)en fonction de lahauteur
LISTE DES TABLEAUX
Chapitre 1
Tableau 1.1: Concentrationsmoyennes en métaux dans différents types de roches terrestres.
Adapted'aprèsKabata-Pendias(1992). 25
Tableau 1.2: Concentrationsmoyennesenmétaux etmétalloïdedans le fondgeochimique des
sediments de la regionartois-picardie. adapte d'apres agencedel'eau artois-picardie. 26
Tableau1.3: Concentrationsdequelques métaux dissous dans les eaux naturelles.D'après
StummetMorgan(1996). 27
Tableau 1.4: Sitesimportants de fixation descontaminantsorganiquesetinorganiquesauseindu
sediment.d'apres eggletonetthomas(2004). 34
Tableau1.5: Coefficientsde distributionKuen log pour différents métaux dansquelques fleuves
majeurs.D'aprèsZhanget al.(1994). 36
Tableau1.6: Principalesreactionsd'oxydationresponsables de la production de protons dans les
systemesaquatiques.D'apres calmanoetal.(1993). 50
Tableau1.7: Principalesreactionstampons dusediment.Source:Calmanoetal., 1993. 51
Tableau 1.8: Exemplesdf.radionuclides utilises en tantque traceurs dans les systèmes
aquatiques, pour des processus se deroulant sur quelques joursjusqu'aplusieurs siecles.
Adapte d'âpres Santschi(1986). 62
Chapitre
2
Tableau2.1 :Apportsen eaudans la section de canal etudiee. 75
Tableau2.2 :Concentrationsen métaux dans les matières en suspension desrejets. 75
Tableau2.3 :Concentrationsen métaux dans les matières en suspension des rejets de la station de
relevageet deSaprotec. 75
Tableau2.4:Données hydriquesentre mars2005et août2006(pluviométrie, debits). 79
Tableau2. 5 :Datesdescampagnes de prelevement lors du«suivide terrain»et délaiséparant
deux campagnes successives. 83
Tableau2.6:Limitededetection(=LD)pourl'ICP AES,calculéepour un échantillon solide de
0,5g. 94
Tableau2. 7 : LimitedeQuantifiationdel'ICP MSetanalyse des blancs de terrain. 101
Tableau2.8: Comparaisonentre lesconcentrations deZn,Pb, CdetCumesuréesdansl'eauselon
deux methodesd'echantillonnagedes metaux. 104
Tableau2. 9 :Microelectrodesutilisées. 105
Chapitre 3
tableau3. 1 :vitessedesedimentationdans lascarpea partir de la methode dul37cs. 121
Tableau3.2 :StockIdel37Csenfonction du site échantillonné. 121
Tableau3.3 :Vitessede sedimentation danslaScarpeapartir de laméthode du2I0Pb. 127
Tableau3.4: Concentrationsmoyennes desmétauxdanslessediments de laScarpe. 131
Tableau3.5: ConcentrationsenZn,Cd,PbetCumesures dans lessediments preleves dans
differents systemesaquatiques soumis aux activites humaines(industrielle,urbaine,miniere).
132
Tableau3.6 :Facteur d'EnrichissementGeochimique (= FEG)moyen dans lessediments. 133
Tableau3.7: Classificationde lapollution associéeal'index d'accumulation geochimiqueIgeo.
134
Tableau 3.8 :Concentrationsmoyennes en contaminantsmétalliques(Zn, Pb, Cd, Cu)dans les
sediments anciens et compactes de lascarpe. 139
Tableau3.9: ConcentrationsenCd, Pb, ZnetCudans lesmatièresen suspension prelevees dansla
Scarpeenk13, k16etk36,et al'entreede lastation de relevage, entre mai2005etaoût2006.
Chapitre 4
Tableau 4. 1 :Rapportd'activités2i0Poxs/2I0Pbxsdans les sediments de surface(0-3 cm)preleves en
k13,k16etk36enavriletmai2006. 164
Tableau4.2 :Rapport d'activité2IOPoxs/2IOPbxsdans lesmatières en suspension prelevees enk.13, k16
etk36entre mai etaoût2006. 164
Tableau4.3 :Activitésdu7Bedans les sediments preleves enk13, k16etk36en avril2005. 168
Tableau4.4 :Inventairedu7Bedans les sediments(tranches 0-3et3-5 cm)prelevesen trois
exemplaires(abc)entrois sites(k13, k16etK36)entre avril2005 (campagne n° 1 )et aout2006
(campagne n° 15). 170
Tableau4.5 :Stock total, résiduel et nouveaude7Bedans lessediments preleves enk13, k16etk36
entre avril2005et aout2006. 173
Tableau 4.6 :Activitédu7Bedans lesmatières en suspension prelevees en k13, Kl6etk36et dans la
stationderelevage, et pluviometrie, entre mai2005et aout2006. 177
Tableau 4.7 :Calculdu flux dedepot/erosiondansles sedimentsen k13,Kl6, k36,entre avril2005
et août2006. 181
Chapitre
5
Tableau 5.1 :Fluxtotalde depot et flux totald'érosionpourleZn,lePb,leCdet leCu,a la
SURFACE DESSEDIMENTSENK13, Kl6ETK36,ENTRE mai2005ET AOUT2006. 190
Tableau 5.2 :Rapportentre le flux totaldedepotet le fluxtotald'érosion. 190
Tableau5.3 :Determinationduflux advectif duPb, Cd, ZnetCulors des episodesd'érosionen
janvieretaout2006enK36. Atdesigne la periode pendantlaquelle les sediments se sont
erodes,soit entre deux campagnes de prelevement successives. 194
Tableau 5.4 :IntervallesdeconcentrationsenZn,Pb,CdetCudans les eauxinterstitielles des
sedimentsderivieres. 205
Tableau5. 5 :Fluxparticulairesdedepot/erosion,fluxdiffusif etfluxadvectif des contaminants
INTRODUCTION
Le développement industriel et urbain de nos sociétés a généré une exploitation de ressources naturelles et une production de déchets et de polluants. Depuis longtemps, les cours d'eau constituent le réceptacle d'une pollution aux formes multiples. Les polluants
proviennent des activités urbaine, agricole et industrielle. Les sources de polluants peuvent
contaminer les eaux de manière directe (rejet) ou diffuse (dépôt atmosphérique, lessivage de
sols contaminés). Lorsqu'il pleut, les eauxde surface ruissellentà traversdes surfaces plus ou
moins contaminées etcharrient avec elles leurlot de polluants. Les eaux de surface sont ainsi
capables d'intégrer les pollutionsnon traitées à l'échelle du bassin versant. L'introduction des polluants dans lecours d'eaupeutavoir des conséquences sanitaires etécologiques.
En France, les préoccupations environnementales sont devenues un enjeu social, politique et
économique. Une directive-cadre européenne d'octobre 2000 (2000/60/CE) a prévu que
chaque Etat devrait, d'ici 2009, avoir élaboré des «plans de gestion » et des « programmes
d'actions » concrets dans tousles « districtshydrographiques », afin de parveniren 2015 à un
«bon état des eaux ». Cette directive est appelée à jouer un rôle stratégique et fondateur en
matière depolitique de l'eau.
Au regard de cette directive cadre, le comportement des sédiments vis-à-vis de la colonne
d'eauestparticulièrement important à prendre en compte. Denombreuses substances peuvent
être piégées dans les sédiments et être libérées après s'être déposées. Ainsi, la question se pose : les sédiments se comportent-ils comme des pièges pour la pollution ou agissent-ils en
tantque sources de contamination vis-vis de l'eau sus-jacente ?
Les sédiments jouent le rôle de puits potentiel pour de nombreuses substances
toxiques. Les activités humainesdepuis l'ère industrielleontrejeté desmétaux lourds dans les
eaux de surface et, en raison de leurs propriétés, nombres d'entre eux se sont associés aux
sédiments. Dans les environnements où la sédimentation s'est déroulée sur de longues
périodes de temps, les sédiments constituent les archives chimiques de l'histoire d'une
pollution. Lespolluants ainsi piégés peuventsouscertaines conditionsêtre remobilisés dans la
colonne d'eau,et cetransfert vaàl'encontre des efforts menés surl'amélioration de la qualité
des eaux de surface. Les sédiments constituent ainsi « une bombe chimique à retardement»
(Stigliani, 1991). Les activités humaines (navigation, curage) et les événements naturels
(cycles hydrologiques, vents) sont susceptibles de perturber l'interface eau-sédiment et de
remettre en suspension les sédiments contaminés qui s'étaient accumulés auparavant dans le
litdes coursd'eau. Les événements de remiseen suspension/d'érosion des sédiments peuvent être à l'origine du transfert des contaminants associés aux sédiments sous forme particulaire
(érosion) (e.g. ten Hulscher et al., 1992), et/ou dissoute lorsque le confinement des eaux
porales est rompu (advection) (e.g. Krein et Symader, 2000). Les perturbations physiques (dépôt, érosion, bioturbation) provoquées à la surface des sédiments peuvent modifier les
paramètres physico-chimiques (Eh, pH typiquement) des sédiments et altérer la distribution physique etla spéciation chimique des contaminants métalliquesprésents dans les sédiments.
Enfin, à l'interface eau-sédiment, lorsque la dégradationde la matière organique estamorcée,
l'établissement de conditions particulières peut être favorable à la remobilisation des
polluants métalliques qui passent des sédiments vers la colonne d'eau (diffusion) (e.g. van
denBergetal., 1999).
La région Nord-Pas de Calais se caractérise par un réseau dense de rivières canalisées
sédimentation est favorisée par les faibles débits liés à la topographie plane. Les sédiments
marqués par le lourd passif industriel et urbain de la région présentent des concentrations
élevées en polluants métalliques et organiques. Les systèmes aquatiques sont soumis, encore
actuellement, à des rejets urbains et industriels qui continuent en partie à alimenter les
sédiments de fond en polluants métalliques et organiques. Le bassin Artois-Picardie
représente environ un tiers de sédiments pollués par rapport au volume national (Bogusz, 1999). Dans un souci croissant de la qualité des écosystèmes aquatiques, la question du
devenir des contaminantsestdoncune problématique environnementale importante dans cette
région.
La thèse s'intéresse au «devenir des polluants métalliques associés aux sédiments
contaminés dans une rivière en relation avec la dynamique sédimentaire ». Deux termes sont
importants : « devenir » et « dynamique ». Le terme « dynamique » porte sur le matériel
sédimentaire sous formeparticulate : les sédiments en place (lit de la rivière) etles sédiments
en transit dans l'eau (matières en suspension). Le « devenir» ultime des particules
sédimentaires dans un cours d'eau est de se déposer à la surface des sédiments et d'y être
enfouies. Cependant, une sédimentation à long terme n'exclut pas une alternance d'épisodes
de dépôt et d'érosion des sédiments se déroulant sur des échelles de temps plus courtes.
L'objectif du travail de thèse est de caractériser l'influence des processus sédimentaires
(dépôt/érosion) surle devenir des contaminants métalliques.
L'étude des mécanismes impliqués dans le transport des sédiments de surface passent
généralement par une approche théorique, ou des mesuresde terrain, des expérimentations, et
des simulations. La caractérisation des processus sédimentaires dans le milieu se fait souvent
sur des échelles spatiales et temporelles assez importantes. Or, dans les études d'impact
environnemental, il est nécessaire d'évaluer la mobilité des polluants sur des échelles plus
courtes.
La stratégie du travail de recherche repose sur une variation d'échelle spatio-temporelle. D'une part, la dynamique des sédiments (dépôt/érosion) a été caractérisée sur deux échelles
de temps différentes (pluri-décennale et mensuelle) à partir de l'utilisation des traceurs
• l-\~i 910 7
radioactifs environnementaux ( Cs, Pb, Be). D'autre part, le degré de contamination
métallique a été déterminé à l'échelle du compartiment sédimentaire, et le comportement
géochimique despolluants métalliques aétéétudié à proximité de l'interface eau-sédiment.
Pour aborder le sujet et mettre en place la stratégie d'étude, nous nous sommes
intéressés aux mécanismes qui régissent le transport des contaminants métalliques dans un
milieu aquatique, et à l'utilisation des traceurs radioactifs environnementaux dans le but de
caractériser les processus sédimentaires (chapitre 1). Le choix du secteur d'étude et des sites
de prélèvements est ensuite décrit, ainsi que nos méthodes de prélèvement et
d'échantillonnage, et les techniques instrumentales utilisées (chapitre 2). L'historique de la
pollutionmétalliquedans le secteurd'étudea été établi àpartir du bilan sédimentaire
(césium-137 et plomb-210) et de la contamination des sédiments (chapitre 3). Afin de caractériser la
dynamique sédimentaire sur une échelle de tempsplus courte, une méthode originaleetbasée
sur l'utilisation d'un traceur radioactif environnemental (le béryllium-7) a été mise en œuvre
(chapitre 4). Apartir de cesrésultats, l'impact des processus de dépôt/érosion sur le transfert
des métaux a pu être quantifié (chapitre 5). Les mécanismes impliqués dans les échanges
chimiques à l'interface eau-sédiment y sont également présentés. Enfin, les conclusions générales sont exposées, ainsi que les propositions de recherche complémentaire. L'ensemble
Lestravauxprésentés ontété essentiellementréalisés auCentreNational de Recherche
sur les Sites et Sols Pollués (CNRSSP) à Douai. Cette thèse a bénéficié d'une collaboration
scientifique et technique avec l'Ecole des Mines de Douai et le Laboratoire des Sciences du
Climat et de l'Environnement à Gif-sur Yvette. Le CNRSSP est un Groupement d'Intérêt
Public (GIP) crée en 1996 et entré en liquidation en 2006. Le travail de la thèse est depuis
rattachéaux activités de recherche dudépartement Génie Civil et Environnemental de l'Ecole
1
SYNTHESE
BIBLIOGRAPHIQUE
1.1 Les métaux dans le
système aquatique
Les métaux (fer, cuivre, plomb, zinc, argent et or...) sont des corps simples, dotés
d'un éclatparticulier, bons conducteurs de la chaleur etde l'électricité. Ils sont abondamment
utiliséspar l'homme depuis l'Antiquité, d'abordpour sasurvie, puis sonconfort etses loisirs.
Les métaux indispensables au métabolisme des êtres vivants constituent les oligo-éléments.
Nombreux sont cependant toxiques lorsque leur concentration dépasse un seuil, lui-même
fonction de l'état physico-chimique de l'élément considéré : c'est le cas du fer (Fe), du cuivre
(Cu), du zinc (Zn), du nickel (Ni), du cobalt (Co), du vanadium (V), du sélénium (Se) du molybdène (Mo), du manganèse (Mn), du chrome (Cr), de l'arsenic (As)etdu titane (Ti).
D'autres ne sont pas nécessaires à la vie et sont préjudiciables dans tous les cas comme le
plomb (Pb), le cadmium (Cd) etl'antimoine (Sb).
Les composés métalliques ont une toxicité variable selon leur nature et leur voie de
pénétration (ingestion, respiration, contact avec la peau). Trois de ces métaux sont à cejour
considérés comme étantcancérigènes : l'As,le Cretle Ni (Chiffoleauetal., 2001).
Les métaux de transition sont stables chimiquement. Ils sont sensibles aux processus
oxydo-réducteurs car ils présentent généralement différents degrés d'oxydation stables dans
les environnementsgéologiques (figure 1.1).
L'abondance des éléments métalliques est liée à l'affinité chimique des éléments.
Goldschmidtaproposéuneclassification des éléments enquatregroupes(figure 1.2) :
les éléments lithophiles associés à laphase silicatée ;
les éléments atmophiles enphasegazeuse ;
les éléments sidérophiles présents dans la phase métallique ;
les éléments chalcophiles présentsdans la phase sulfurée.
Par abus de langage, métaux et métalloïdes sont assimilés à l'appellation générique
métaux; néanmoins les contaminants métalliques se distinguent des métaux tels que le fer (Fe) et le manganèse (Mn) qui fournissent dans les environnements aquatiques des supports pour le transport des autres métaux (Cd, Cu, Ni, Zn, Pb...). Le fer et le manganèse que l'on
rencontre dans l'eau ou les sédiments ne sont généralement pas considérés comme des
polluants. Cependant ils sont suffisamment abondants et réactifs pour influencer le devenir
lia llla IVa Va Via Vila S VII< Ib Mb 1Mb calcium scandium titane vanadium chrome manganèse fer cobalt nickel cuivre zinc gallium Ca Se Ti V Cr Mn Fe Co Ni Cu Zn Ga 0
.S
%
étatd'oxydation rencontré dans les
environnementsgéologiques
autreétatd'oxydation stable dans
les conditions de laboratoire
Figure 1.1: Les différents états d'oxydation des métaux de transition: exemple de lapremière série de
transition.
Figure1.2: Classification des éléments proposéeparGoldsehmidt.
1.1.1
Origine des
métaux dans les milieux aquatiques
1.1.1.1 Naturelle
Les métaux sont des composants naturels de l'écorce terrestre dans laquelle ils se
présentent généralement sous forme de minerai où ils sont associés entre eux et à de
nombreux éléments (oxygène etsoufre particulier). Ils sont naturellement présents dans les
Eléments dans l'Univers
atmosphèreet hydrosphère sulfures noyau(et météorites) croûte, manteau, météorites
roches drainées par les eaux de surface (et les nappes d'eau souterraines) ainsi que dans les
poussières atmosphériques. Les volcans, de mêmeque les incendies de forêt, sont dessources
naturelles importantes de métaux pourlagéosphère et l'hydrosphère. Le tableau 1.1 donne les
teneurs moyennes en éléments métalliques à l'échelle mondiale dans différents types de
roches.
Concentrations moyennes en
mg.kg"1
Rochesmagmatiques Roches sédimentaires
Eléments Roches basiques Roches intermédiaires Roches acides Roches argileuses, sableuses Grès Carbonates Cd 0,13-0,22 0,13 0,09-0,20 0,22-0,30 0,05 0,035 Co 35-50 1,0-10 1-7 11-20 0,3-10 0,1-3,0 Cr 170-200 15-50 4-25 60-100 20-40 5-16 Cu 60-120 15-80 10-30 40 5-30 2-10 Hg 0,0x 0,0x 0,08 0,18-0,40 0,04-0,10 0,04-0,05 Mn 1500-2000 500-1200 350-600 500-850 100-500 200-1000 Mo 1,0-1,5 0,6-1,0 1-2 0,7-2,6 0,2-0,8 0,16-0,40 Ni 130-160 5-55 5-15 50-70 5-20 7-20 Pb 3-8 12-15 15-24 18-25 5-10 3-10 V 200-250 30-100 40-90 100-130 10-60 10-45 Zn 80-120 40-100 40-60 80-120 15-30 10-25
Tableau 1.1: Concentrations moyennes enmétaux dans différentstypesde rochesterrestres.Adapté
d'aprèsKabata-Pendias (1992).
Dans certainesrégions, l'abondance moyenne des éléments métalliques rencontrée est
plus élevée. Cet enrichissement observé est dû à des processus géochimiques qui peuvent
conduire à la formation de gisements naturels potentiellement exploitables. Chaque région
présente des caractéristiques géologiques et pédologiques qui lui sont propres avec pour
conséquences des concentrations variées en éléments métalliques dans les différents
réservoirs géochimiques. Ces concentrations singulières constituent le fond géochimique. Le
fond géochimique peut être déterminé selon diverses méthodes. Dans des milieux perturbés
par l'activité humaine, le référentiel local de concentrations présentes naturellementpeut être
déterminé àpartirde :
l'analyse des sédiments superficiels prélevésen zonesupposée noncontaminée (amont
descours d'eauparexemple) ;
l'analyse statistique d'un grand nombre de prélèvements à l'échelle du bassin versant
ou d'un ensemble de bassinsversants ;
l'analyse des couchesprofondes d'unecarotte de sédiment.
Dans le Nord-Pas-de-Calais, les concentrations naturelles de référence en éléments
métalliquessontéquivalentesauxvaleurs déterminées parl'Agence de l'Eau Artois-Picardieà partir des valeurs les plus basses mesurées dans les sédiments de l'Artois-Picardie (zone géographique définie par l'Agence de l'Eau). Le tableau 1.2 présente les concentrations en
métal ou métalloïde
valeurs considérées comme naturelles dans les sédiments,
en
mg.kg"1
arsenic 5 cadmium 0,5 chrome 25 cuivre 20 manganèse 250 mercure 0,1 plomb 20 fer 10000 zinc 75Tableau 1. 2: Concentrations moyennes en métauxetmétalloïde dans le fond géochimique des sédiments
de la région Artois-Picardie.Adapté d'après Agence de l'Eau Artois-Picardie.
1.1.1.2.
Anthropique
La France métropolitaine extrait relativement peu de minerai de métaux non ferreux
mais en importe de grandes quantités qu'elle raffine sur son sol. Les métaux extraits sont
ensuite transformés, utilisés, recyclés, parfois exportés. Les utilisations des métaux sont
multiples ettrès diversifiées, depuis les additifs de Pb dans les carburants, auNi ou au Cd des
batteries d'accumulateurs, au Zn des gouttières ou au Cr des aciers inoxydables, au Cu de
l'industrie électrique ou à l'As des produits phytosanitaires (Chiffoleau et al., 2001). Les
sources de contamination le sont aussi par conséquent. Durant toutes les phases d'élaboration
et/ou de recyclage de ces produits, des métaux sont rejetés, parfois en abondance, dans
l'environnement, soit directement dans les eaux continentales (rejets industriels ponctuels),
soit dans l'atmosphère où ils peuvent être transportés par les vents à des milliers de
kilomètres, associés aux poussières avant de se déposer par voie sèche ou par voie humide,
bien que la majeure partie de ces émissions atteigne le sol à proximité des sources {e.g. Sobanska, 1999). L'utilisation de produits finis contenant des métaux (l'automobile et
l'agriculture par exemple) en dissémine des quantités importantes dans l'environnement. Il
s'agit d'une contamination généralement diffuse (épandage d'engrais phosphatés
naturellement enrichisen Cdparexemple), bien que des régions à forte densité depopulation
et en particuliers les grandes métropoles soient propices à des émissions importantes. Les
fortes concentrations de métauxdans les rejets urbains ensont la résultante.
Dans la région du Nord-Pas-de-Calais, concernant la production de Pb dans l'air, la
répartition par secteur industriel en 2006 est la suivante (DRIRE Nord-Pas-de-Calais, IRE 2007):
sidérurgie/métallurgie/fonderie : 12 242kg.an-1,
verre/matériaux: 1 129
kg.an"1,
énergie : 491
kg.an"1,
traitements de déchets : 375
kg.an"1,
chimie/pétrole : 191
kg.an"1,
autres : 18 kg.an" .
La prise de conscience politique en matière d'environnement a permis de diminuer les
rejets polluants directs. L'importance qu'attribue le législateur à la protection de
l'environnement se reflète entre autres dans le nombre déjà croissant de lois et de règlements
commune a été définie dans le Traité sur l'Union Européenne en vigueur depuis le Ie' juillet 1987. L'Union Européenne a publié une directive cadre pour la protection de l'eau ; la
Directive Cadre Eau, adoptée endécembre 2000 fixe pourobjectifun « bon état écologique»
deseaux à atteindre en2015.
1.1.2 Distribution des métaux dans les milieux
aquatiques
Une fois les métaux introduits dans le milieu aquatique, ils se répartissent dans les
différents compartiments : eau et sédiment. L'interface eau-sédiment forme la limite entre
deux phases : l'eau et le sédiment (Santschi et al., 1990). L'eau comprendune fraction solide
correspondant aux matières ensuspension en transit et unefraction « dissoute ». Demême, le
compartiment sédimentaire comprend une phase solide constituée des particules solides de
sédiment etune phase liquide correspondant aux eaux interstitielles qui remplissent les pores
ausein des sédiments.
Les métaux sont présents sous différentes formes chimiques en fonction des paramètres
environnementaux.
1.1.2.1 Dans l'eau
Phase dissoute
La fraction dissoute se définit expérimentalement par la filtration de l'eau brute à
travers des pores de diamètre égal à 0,45 ja.m. Il s'agit d'une définition courante pour
distinguer les fractions dissoute et particulate. L'avènement des techniques de filtration plus précises a permis, dans les années 70-80, d'isoler des particulesplus fines (Stumm etMorgan, 1996) ; la limitedissous-particulaire apris des valeurs de plus enplus basses (entre 0,2 |imet
3 |im)et cettelimite varie selon lesauteurs.
Le tableau 1.3 présente quelques données sur les concentrations en métaux dans les milieux
lacustre, océanique et fluvial. Les concentrations en métaux dans la fraction dissoute sont
particulièrement faibles
(10~6
à10"12 mol.L"1).
Area Cu(nM) Zn(nM) Cd(nM) Pb(nM) References
U.S. East Coast rivers 17 13 0.095 0.11 Windometal. (1991)
Mississippi River 23 3 0.12 — Shiller and
Boyle(1987)
AmazonRiver 24 0.3-3.8 0.06 — Shiller and
Boyle (1987)
Lake Constance 5-20 15-60 0.05-0.1 0.2-0.5 Siggetal. (1982)
LakeMichigan 10 9 0.17 0.25 Shafer andArmstrong(1990)
LagoCristallina" 5 30 0.5 3 Sigg (1993, personal communication)
Pacific Ocean 0.5-5 0.1-10 0.01-1 0.005-0.08 Bniland and Franks(1983)
Rainwater* 10-300 80-900 0.4-7 10-200 Sigg (1993, personal communication)
Tableau1. 3 :Concentrations dequelques métaux dissousdansles eauxnaturelles.D'après Stumm et
Morgan(1996).
Dans les rivières, les concentrations en métaux observées sont liées (Stumm et Morgan, 1996) :
aux caractéristiques géochimiques des roches constitutives du bassin versant : les
métaux présents dans les eauxsontissus duprocessus chimiquedelessivage ;
à lapollution anthropique, via les rejets directset/ou les retombées atmosphériques ;
ainsi qu'aux propriétés chimiques des rivières : adsorption des ions métalliques à la
Les particules exercent un contrôle sur la solubilité des différents métaux dans les systèmes
aquatiques, carle coefficient departagesolide-liquide (KC|) estrelativement stable(e.g. Zhang
et al., 1994). L'association des contaminants métalliques avec les particules est facilitée par
l'abondance desparticules sédimentaires ensuspension.
Phaseyarticidaire
Les matières en suspension sont constituéespar le matériel particulate en transit dans
l'eau. Les concentrations des matières en suspension sont déterminées après filtration sur
membrane de porosité 0,45(impuisunepesée après dessiccation.
Lematériel particulaire présent ensuspension dans la colonne d'eaua diverses origines :
ilpeutêtre issu des produits de l'érosion des sols alentours transportéspar leseaux
de ruissellement ; leur composition est alors liée à la nature des sols érodés et
lessivés ;
les activités urbaines et industrielles sont à l'origine d'un flux de matériaux de
moindre importanceenmasseetgénéralement diffus ;
les apports atmosphériques, par retombées sèches et humides, peuvent constituer
une source supplémentairedeparticules dans le milieu aquatique,
la production biologique constitue une source de matériel particulaire importante. La part des apports particulates liée à la production biologique est tributaire des
cycles saisonniers qui se supeiposentavec les cycles hydrologiques (crue, étiage) :
elle reste faible, voire négligeable, dans le cas des apports liés aux crues
hivernales. Elle devient importante dès l'apparition des premiers blooms
phytoplanctoniques du printemps etcejusqu'enseptembre-octobre selon les cycles
climatiques annuels (Dupontetal, 2001).
l'érosion des berges etdes sédiments de fond (remise en suspension) peut enrichir
la quantitéde matériel particulaire entransit dans les coursd'eau.
Il est admis que la majorité des contaminants inorganiques (métaux) s'associe à la
matière particulaire (e.g. Briigmann, 1995 ; Horowitz, 2000). Selon Calmano et al. (1993),
plus de 90 % de la charge en métaux lourds dans les systèmes aquatiques est associée aux
particules constitutives des matières en suspension et du sédiment. Pour la plupart des
élémentsentraces (métaux),> 90 % du fluxdans les systèmes fluviaux estprésentsousforme
particulaireen associationavec le sédiment ensuspension (Walling etal., 2003).
La taille du grain est unfacteur important régissant le transport des contaminants. En
général, la concentration en métaux associés aux particules augmente quand lataille du grain
diminue et les métaux se fixent préférentiellement à la fractionargileuse (e.g. Fôrstner 2004 ;
Westricht, 1986 ;Oldetal.,2003 ;Leeetal,2003).
La figure 1.3 illustre la relation existant entre la concentration en métaux et la taille des particules. 'ûi) c'a n. "V o C/3 "O a 12 S 0.02 0,15 63 250 1000 pm
Figure1.3: Relation typiqueentrelaconcentration enzinc adsorbéenfonction du diamètre de la