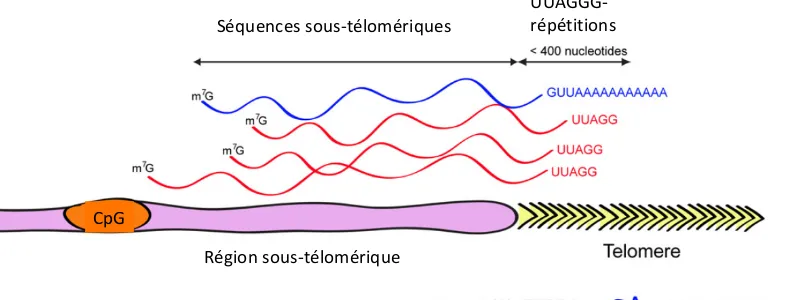
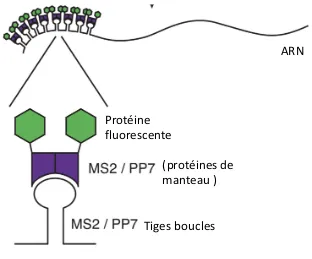
Étude de l’expression et des partenaires protéiques de l’ARN TERRA (TElomeric Repeat-containing RNA) dans les cellules de cancer humaines
Texte intégral
Figure

Outline
Documents relatifs
Bien que l’auteur s’en défende dans un entretien (El-Watan, 15-05-2005, article signé par Bouziane Benachou) « Je ne suis pas un écrivain de l’urgence », ces textes ont
Dès lors, le Manuscrit trouvé à Saragosse s’apparente en bien des points à un vaste laboratoire dans lequel des personnages cobayes subissent l’expérience
Nous avons observé un décalage entre l’intention de l’enseignant de donner du sens aux notions mathématiques avec des exemples issus de la physique et le vécu des étudiants..
Une fois cette situation sociopolitique posée, nous passerons en revue la notion de dialogue de savoirs 1 que nous avons abordée en classe à partir de l’adaptation du modèle
Vingt-quatre enfants de 10 mois sont confrontés à trois types d’événements (lancer direct, lancer avec délai et lancer sans collision) dans le cadre d’une
Cette €pid€mie ayant s€vit dans l’Oc€an Indien et notamment sur l’ƒle de La R€union a €t€ exceptionnelle „ plusieurs titres : l’apparition d’un virus
Pour parvenir à montrer le sens de lecture de l'ARNm, il faut procéder à la traduction simple d'une séquence d'A.R.N.m dans un sens donné, puis effectuer la même action sur la
En effet, non seulement l’”Essai sur les éléments de philosophie” n’est pas un ouvrage à proprement parler, puisqu’il constitue le quatrième volume