Électro-activation de l’acétate de potassium, du citrate
de potassium et du lactate de calcium et leur utilisation
dans la conservation des petits pois : impact sur les
qualités nutritionnelles et organoleptiques du produit et
évaluation de l’interaction avec l’emballage
Mémoire
Angeline Duqueyroix
Maîtrise en sciences et technologie des aliments
Maître ès sciences (M. Sc.)
Québec, Canada
© Angeline Duqueyroix, 2017
Électro-activation de l’acétate de potassium, du citrate
de potassium et du lactate de calcium et leur utilisation
dans la conservation des petits pois : impact sur les
qualités nutritionnelles et organoleptiques du produit et
évaluation de l’interaction avec l’emballage
Mémoire
Angeline Duqueyroix
Sous la direction de :
iii
Résumé
L’appertisation permet, au travers un conditionnement dans un récipient hermétique suite à un traitement thermique, d’allonger la durée de vie de nombreux produits alimentaires. Une fois le traitement thermique appliqué, la stérilisation pour les produits peu acides permet de détruire les microorganismes présents, mais dégrade fortement le produit. En plus, ce traitement est associé à un coût de production hautement significatif. De nouveaux procédés doivent donc être développés pour pallier à ces problèmes. Dans ce contexte, l’électro-activation combinée à un traitement thermique modéré pourrait contribuer à réduire les coûts de production tout en assurant une qualité adéquate du produit final. En effet, l’électro-activation combinée à un traitement thermique modéré permet de protéger le produit des microorganismes via l’action antibactérienne des solutions électro-activées. L’effet de ce procédé sur les qualités organoleptiques des petits-pois mis en conserve a été analysé ainsi que les risques toxicologiques exprimés par la migration de certains minéraux spécifiques de l’emballage métallique vers le produit. Le procédé d’appertisation a été comparé au nouveau procédé en utilisant trois solutions électro-activées et deux différents emballages. Les différentes analyses ont été menées chaque mois de stockage pendant trois mois. La couleur, la teneur en vitamine C, la fermeté ainsi que la perte en matière sèche du produit dans la saumure et la teneur en ions métalliques dans celle-ci ont été analysées. Les résultats obtenus n’ont montré aucune différence significative en ce qui concerne la couleur, la teneur en vitamine C, la perte de matière sèche du produit au bout de 3 mois de stockage entre les deux procédés. Par ailleurs, ce projet a permis de montrer que la texture du produit final était plus ferme avec le nouveau procédé utilisant l’électro-activation. En plus, il a été démontré que l’électro-activation combinée à un traitement thermique modéré a le même impact sur la qualité du produit que l’appertisation conventionnelle. Dans les solutions électro-activées, aucun ion métallique n’était présent à part le fer qui ne présente, cependant, pas de risque pour le consommateur. Finalement, comme les éléments métalliques à haut risque toxicologique comme l’étain ne migrent pas de l’emballage, l’électro-activation combinée à un traitement thermique modéré apparaît comme une alternative potentielle au procédé d’appertisation.
iv
Table des matières
Résumé ...iii
Table des matières ... iv
Liste des tableaux ... vi
Liste des figures ... vii
Liste des abréviations et sigles ... viii
Remerciements ...x
Introduction ... 1
Chapitre 1 : Revue de littérature ... 3
1.1. La conservation ... 3
1.2. Traitements thermiques appliqués lors de l’appertisation et leurs effets ... 4
1.2.1. Les traitements thermiques ... 4
1.2.2. Effets du traitement thermique sur la qualité du produit ... 5
1.3. L’effet barrière ... 8
1.4. L’électro-activation ... 9
1.4.1. Principe général ... 9
1.4.2. Utilisation de l’électro-activation dans l’industrie agroalimentaire ... 13
1.5. Effets combinés d’un traitement thermique modéré et de solution électro-activée sur la qualité microbiologique et organoleptique du produit ... 17
1.6. Transferts entre matériaux et aliment ... 18
1.6.1. Verre ... 18
1.6.2. Boîte en métal ... 19
Chapitre 2 : Hypothèse et objectifs ... 34
2.1. Hypothèse de recherche ... 34
2.2. Objectif principal ... 34
Chapitre 3 : Matériel et méthodes ... 35
3.1. Matière première ... 35
3.2. Obtention des solutions électro-activées ... 35
3.3. Préparation des échantillons ... 37
3.4. Détermination des caractéristiques organoleptiques des petits pois ... 40
3.4.1. Analyse de la couleur ... 40
v
3.4.3. Dosage de la vitamine C ... 42
3.4.4. Perte de la matière sèche dans la saumure ... 44
3.4.5. Analyse en microscopie électronique ... 44
3.5. Analyse de la migration d’éléments vers le produit (ions métalliques) ... 45
3.6. Analyse statistique ... 45
3.7. Analyse de l’influence de la température de stérilisation sur la qualité des pois ... 46
Chapitre 4 : Résultats et discussion ... 47
4.1. Obtention des solutions électro-activées ... 47
4.2. Détermination des caractéristiques organoleptiques des petits pois ... 49
4.2.1. Analyse de la couleur ... 49
4.2.2. Effet sur la texture ... 53
4.2.3. Teneur en vitamine C ... 56
4.2.4. Teneur en matière sèche de la saumure ... 58
4.2.5. Analyse en microscopie optique ... 60
4.2.6. Déductions générales ... 61
4.3. Analyse de la migration d’éléments vers le produit (ions métalliques) ... 62
4.3.1. Etude de la corrosion sans produit ... 62
4.3.2. Etude de la corrosion avec les pois ... 67
4.4. Analyse de l’influence de la température de stérilisation sur la qualité des petits pois 71 Conclusions générales et perspectives ... 72
vi
Liste des tableaux
Tableau 1 : Caractéristiques des pois blanchis ... 35
Tableau 2 : Ensemble des traitements ... 38
Tableau 3: Moyenne et écart type de la variable a* (les lettres minuscules indiquent une différence (p≤0,05) entre les traitements pour chaque durée de stockage, les lettres majuscules indiquent une différence (p≤0,05) entre les durées de stockage pour chaque traitement) ... 53
Tableau 4: Teneur en vitamines C dans les pois transférés dans les contenants en verre et la conserve (p≤0,05) ... 57
Tableau 5:Teneurs en matière sèche (p≤0,05) ... 60
Tableau 6 : Teneurs en étain au bout de trois mois de stockage (p≤0,05) ... 65
Tableau 7 : Teneurs en aluminium au bout de trois mois de stockage (p≤0,05) ... 66
Tableau 8: Teneurs en cuivre au bout de trois mois d’entreposage avec pois (p≤0,05) ... 67
Tableau 9: Teneurs en fer au bout de trois d’entreposage avec des pois (p≤0,05) ... 69
Tableau 10: Teneurs en étain au bout de trois mois d’entreposage avec des pois (p≤0,05)... 69
Tableau 11: Teneurs en aluminium au bout de trois mois de stockage (p≤0,05) ... 70
vii
Liste des figures
Figure 1: Configuration générale d’un réacteur pour l’électro-activation de solutions aqueuses .... 12
Figure 2: Composition du fer blanc adapté de FAO et Vignes et al. (1994) ... 21
Figure 3: Processus de corrosion des boîtes sans vernis adapté de Xia et al. (2012) ... 24
Figure 4: Evolution du taux de dissolution de l’étain au cours du temps (Buculei et al., 2009) ... 25
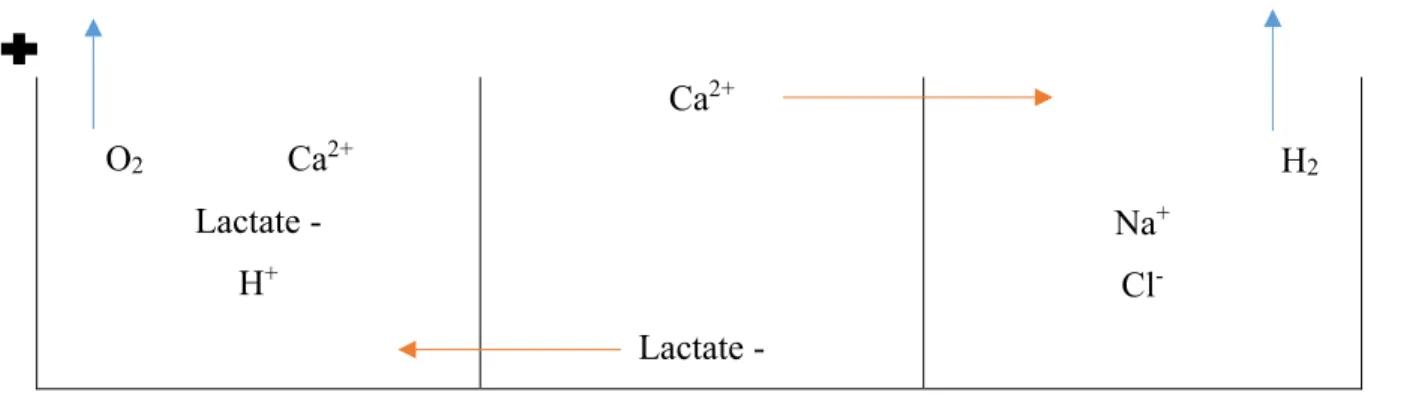
Figure 5 : Emplacement des solutions dans le réacteur et leur concentration (en mol/L) ... 36
Figure 6 : Migrations des espèces chimiques dans le réacteur d’électro-activation ... 37
Figure 7: Chaine de fabrication des pois stérilisés ... 38
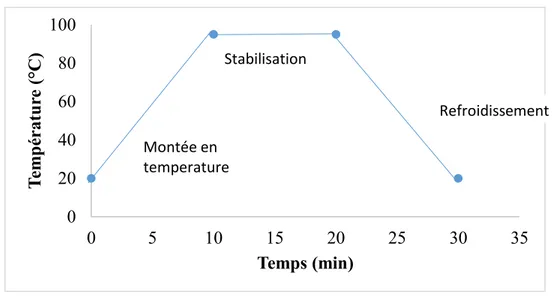
Figure 8 : Cycle du traitement thermique théorique ... 40
Figure 9: Sphère de la chromaticité absolue L*a*b* (Normaprint, 2011) ... 40
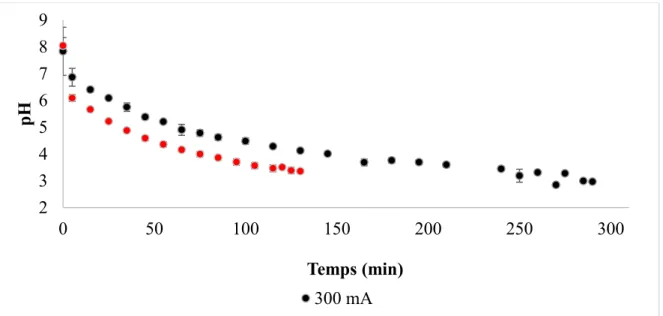
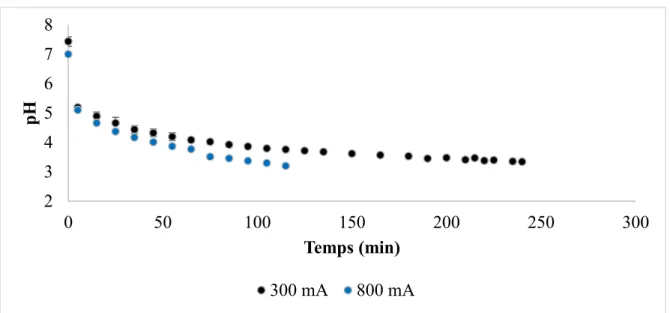
Figure 10: Evolution du pH en fonction du temps pour la solution de lactate de calcium ... 47
Figure 11: Evolution du pH au cours du temps pour la solution de citrate de potassium ... 48
Figure 12 : Evolution du pH en fonction du temps pour la solution d’acétate de potassium ... 49
Figure 13: Analyse du Chroma (les lettres minuscules indiquent une différence (p≤0,05) entre les traitements pour chaque durée de stockage, les lettres majuscules indiquent une différence (p≤0,05) entre les durées de stockage pour chaque traitement) ... 50
Figure 14: Analyse de l’angle de nuance (les lettres minuscules indiquent une différence (p≤0,05) entre les traitements pour chaque durée de stockage, les lettres majuscules indiquent une différence (p≤0,05) entre les durées de stockage pour chaque traitement) ... 51
Figure 15: Représentation de l’angle de nuance sur la sphère ... 52
Figure 16: Force de cisaillement en fonction du temps pour des pois à T0 ayant subi le traitement CV ... 54
Figure 17: Etude de la fermeté des petits pois ayant subi différents traitements au cours du stockage (les lettres minuscules indiquent une différence (p≤0,05) entre les traitements pour chaque durée de stockage, les lettres majuscules indiquent une différence (p≤0,05) entre les durées de stockage pour chaque traitement) ... 55
Figure 18: Etude de la teneur en vitamine C pour les traitements au cours des 3 mois de stockage (les lettres minuscules indiquent une différence (p≤0,05) entre les traitements pour chaque durée de stockage, les lettres majuscules indiquent une différence (p≤0,05) entre les durées de stockage pour chaque traitement) ... 57
Figure 19: Teneur en matière sèche de la saumure pour les différents traitements au cours des 3 mois de stockage (les lettres minuscules indiquent une différence (p≤0,05) entre les traitements pour chaque durée de stockage, les lettres majuscules indiquent une différence (p≤0,05) entre les durées de stockage pour chaque traitement) ... 59
Figure 20: Coupe histologique d’un grain de pois ayant subi un traitement de stérilisation dans un bocal en verre en présence d’acétate de potassium et stocké pendant 2 mois ... 61
Figure 21: Teneur en fer de la saumure pour les différents traitements au cours du temps (les lettres minuscules indiquent une différence (p≤0,05) entre les traitements pour chaque durée de stockage, les lettres majuscules indiquent une différence (p≤0,05) entre les durées de stockage pour chaque traitement) ... 63
viii
Liste des abréviations et sigles
µm : micromètre
1 ppm : partie par million, ce qui est équivalent à 1 mg/kg
a* : indice de rougissement ou de verdissement
ABTS: sel d’ammonium de l’acide 2,2’-azinobis-3-ethylbenzothiazoline-6-sulfonique
AOAC: association of analytical communities
Aw: activité de l’eau
b* : indice de jaunissement ou de bleuissement
Cl2 : chlore
Cu : cuivre
DPPH: 2, 2′-Diphenyl-1-Picrylhydrazyl
e-: electron
ECCS: electrolytic chromium/chromium oxide coated steel
ETP: electrolytic tinplate
Fe: fer
g/kg/mg : gramme/kilogramme/milligramme
H+: ion hydrogène
H2O : eau
HCl : acide chlorhydrique
HOCl : acide hypochloreux
ICP : spectrométrie à plasma à couplage inductif
ix
mA : milliampère, unité de mesure de l’intensité du courant électrique
mV : millivolt
NaCl : chlorure de sodium
NaOH : hydroxyde de sodium
O2 : dioxygène
OH- : ions hydroxydes
ORAC: Oxygen Radical Absorbance Capacity
PVC : polychlorure de vinyle
Sn : étain
TFR: tin free steel
Zn: zinc
L: low residual
MR: medium residual
M: mole/L
EDTA: Ethylenediaminetetraacetic acid
CC : citrate de potassium avec boîte en métal
AC : acétate de potassium avec boîte en métal
LC : lactate de calcium avec boîte en métal
T : témoin (NaCl avec boîte en métal)
CV : citrate de potassium avec bocal en verre
LV : lactate de calcium avec bocal en verre
x
Remerciements
Mes remerciements sont tout d’abord adressés à mon directeur de recherche, M. Mohammed Aider pour m’avoir fait confiance afin de mener à bien ce projet. Sa disponibilité, sa patience et sa bonne humeur m’ont permis de progresser sur le plan technique mais aussi personnel.
Je tiens aussi à remercier toute l’équipe et en particulier Viacheslav Liato pour ses nombreux conseils et son aide apportée tout au long de la réalisation de ma maîtrise.
Au niveau pratique, je remercie Diane Gagnon, Céline Paquin et Jocelyne Giasson sans qui le bon déroulement de ma maîtrise n’aurait pas été possible.
J'adresse mes remerciements aux personnes qui m'ont aidé de loin ou de près dans la réalisation de ce mémoire.
J’adresse aussi mes remerciements à l’Université de Laval pour son accueil bienveillant et à l’Institut Polytechnique Lasalle Beauvais pour m’avoir autorisé à poursuivre mes études à Québec.
1
Introduction
Le petit pois est un légume largement consommé au Canada. En 2008, la consommation canadienne annuelle était de 170 g par personne (Statistique Canada, 2008). Sa récolte s’étale de fin juillet à mi-octobre (Fondation Louis Bonduelle, n.d.). En dehors de cette période, le petit pois frais n’est normalement pas présent sur le marché. Cependant, la demande des consommateurs pour ce légume est présente toute l’année. Pour répondre à ce besoin, les légumes doivent être transformés après récolte, afin de pouvoir les conserver. Plusieurs techniques de conservation ont donc été développées au cours du temps. De nos jours, l’appertisation est principalement utilisée pour conserver les fruits et légumes. Cette technique fait partie des plus employées car, elle permet de conserver le produit pendant une durée de deux à cinq ans. Cette affirmation se justifie par le volume des ventes. En 2010, les ventes de produits transformés mis en conserve représentaient 3,1 milliards de dollars d’après Agriculture et Agroalimentaire Canada (2015).
L’appertisation a été découverte au XVIIIème siècle par Nicolas Appert. Cette technique est basée sur la stérilisation, dans des récipients hermétiques, de divers produits (légumes, fruits, viande, poisson). Les récipients utilisés sont principalement en métal (boîte de conserve) mais aussi en verre. La stérilisation est un traitement thermique qui a pour but de détruire tous les microorganismes, y compris les spores microbiennes, les enzymes et toxines. Cette étape est essentielle afin d’éviter toute contamination du produit ; notamment par Clostridium botulinum. En effet, Clostridium botulinum est un microorganisme que l’on peut retrouver dans le produit en cas de mauvaise stérilisation (Gouvernement du Canada, 2013). Une contamination par cette bactérie a des conséquences importantes sur la santé du consommateur pouvant aller jusqu’à l’effet létal. En effet, ce microorganisme produit une toxine appelée toxine botulique qui est une neurotoxine mortelle. Malgré une période longue de conservation, l’appertisation présente un problème majeur. Les qualités organoleptiques et nutritionnelles du produit sont dégradées pendant la stérilisation à cause de la haute température appliquée. Plus spécifiquement, les protéines sont dénaturées, les polysaccharides des parois cellulaires, les pigments et les vitamines sont également dégradés. La texture et la couleur des légumes sont modifiées ainsi que leur quantité en micronutriments (Laguerre, 2014). Des composées de Maillard peuvent également se former et altérer le produit final (Richard H, 2003). Certains constituants de l’emballage peuvent
2
également migrer vers le produit et donc le contaminer. Dans le cas des boîtes en métal, des ions métalliques comme les ions ferreux peuvent migrer dans le produit et provoquer des modifications visuelles et gustatives. Pour les bocaux en verre, aucun élément ne migre car le verre est inerte mais certains peuvent migrer du couvercle. En plus, la température de stérilisation influence le phénomène de migration.
Pour pallier aux problèmes de qualité rencontrés avec l’appertisation, de nouvelles techniques doivent être développées. De nombreuses études se sont intéressées à l’électro-activation comme barrière à intégrer dans un procédé de conservation des légumes. L’électro-activation est un procédé basé sur l’électrochimie qui permet de modifier les propriétés physico-chimiques des solutions en les soumettant à un courant électrique. Les solutions obtenues sont dites électro-activées du fait qu’elles acquièrent une réactivité élevée. Dans le cas de l’appertisation, les saumures normales sont remplacées par des saumures électro-activées possédant un pH plus acide et un pouvoir oxydant-réducteur positif. L’utilisation de cette saumure permet de réduire la température de stérilisation et donc d’avoir un gain économique très notable. Donc, l’abaissement de cette température, combinée à la saumure électro-activée, permet de protéger le produit des contaminations microbiologiques (Delagarde, 2014; Genois, 2014; Liato et al., 2015), mais pour autant cela permet-il d’améliorer la qualité organoleptique et nutritionnelle du produit ? Ainsi, l’objectif premier de cette méthode serait d’obtenir un produit ayant des caractéristiques qui soient proches de celles du produit frais. Très peu d’études se sont intéressées à ce sujet. L’étude de Genois (2014) a montré que les haricots verts étaient plus fermes avec un traitement alliant un traitement thermique et la saumure électro-activée que la stérilisation conventionnelle et aucune différence de couleur n’a été observée. Les résultats obtenus sont à approfondir, notamment en tenant compte des migrations possibles venant de l’emballage.
L’objectif principal de ce travail est de comparer l’électro-activation combinée à un traitement thermique modéré et l’appertisation conventionnelle dans le but d’obtenir des légumes de bonne qualité organoleptique et ne présentant pas de risque pour le consommateur.
3
Chapitre 1 : Revue de littérature
1.1. La conservation
La conservation est une notion de base dans le secteur de l’agroalimentaire qui vise à garder un produit comestible et ayant de bonnes qualités organoleptiques et nutritionnelles le plus longtemps possible. Pour cela, le développement de microorganismes doit être empêché. L’action des enzymes doit être inhibée afin d’éviter de nombreuses réactions (brunissement enzymatique, hydrolyse des lipides, etc.) (Laguerre, 2014). Des réactions chimiques telles que la réaction de Maillard doivent être empêchées. Plusieurs procédés de conservation ont donc été développés pour augmenter la durée de vie des produits en limitant les différentes réactions et le développement des microorganismes. Ces procédés s’appuient sur différentes techniques. Un traitement thermique peut être appliqué (stérilisation, pasteurisation, réfrigération, congélation, etc.). Le produit peut subir un abaissement de l’aw (activité de
l’eau) à travers le séchage et l’évaporation. Le pH peut être abaissé (acidification, fermentation) (Buche, 2014). Des agents de conservation peuvent être utilisés. Ces différentes techniques peuvent être utilisées séparément ou combinées.
L’appertisation est une méthode de conservation qui a été développée par Nicolas Appert vers 1810 (Biton, n.d.). Ce procédé de conservation repose sur deux techniques : le conditionnement dans un récipient hermétique aux liquides, aux gaz et aux microorganismes et un traitement thermique qui a pour but de détruire tous les microorganismes y compris les spores, les toxines ainsi que les enzymes (DGCCRF, 2014; Industrie Canada, 2015). L’appertisation permet donc de conserver de 2 à 5 ans à température ambiante de nombreux produits (DGCCRF, 2014; Uppia, n.d.).
L’appertisation est un processus qui se déroule en plusieurs étapes. Une fois les légumes réceptionnés, ils sont nettoyés et les morceaux de pierres et autres impuretés sont enlevés. Si nécessaire, les légumes sont par la suite épluchés et calibrés. Un calibrage a lieu notamment pour la mise en conserve des haricots verts (haricots verts extra fins, très fins ou fins) (Uppia, n.d.). Ils sont par la suite blanchis. Le blanchiment est un traitement thermique permettant d’inactiver les enzymes. Cette étape est essentielle lors de la mise en conserve de légumes et est caractérisée par un couple temps-température. La durée du blanchiment est très faible (de 90 secondes à 4 min et demie) et dépend notamment du type de produit et de
4
la température appliquée. La température de blanchiment est comprise entre 85 et 96°C (A
Complete Course in Canning and Related Processes, 2015).
Après le blanchiment, les légumes sont directement transférés dans un récipient qui peut être en métal, en verre ou en plastique. Une solution appelée saumure est par la suite ajoutée dans la boîte. La saumure est une solution constituée majoritairement d’eau et de sel et qui a pour but de conférer au produit une certaine saveur, de l’attendrir, de réduire la durée du traitement thermique en facilitant les transferts thermiques et de diminuer les réactions d'oxydation(CTA - ILO - WEP, 1990). La saumure représente un quart du volume total de la boîte. La boîte est fermée et subit le traitement thermique. Les boîtes sont refroidies et par la suite stockées jusqu’à leur consommation. Ce processus permet d’obtenir des produits dits appertisés, qui sont stables microbiologiquement et ne présentant pas de danger pour le consommateur (Valdez et al., 2008).
1.2. Traitements thermiques appliqués lors de l’appertisation et leurs effets
Les traitements thermiques constituent une barrière de protection du produit vis-à-vis de l’environnement. Plusieurs traitements thermiques existent mais dans le cas de l’appertisation, deux traitements thermiques peuvent être utilisés : la stérilisation ou la pasteurisation selon le type de produit mis en conserve.
1.2.1. Les traitements thermiques
1.2.1.1. La stérilisation
La stérilisation est l’étape la plus importante du processus de fabrication des conserves (en métal et en verre).La stérilisation correspond à un chauffage à une température supérieure à 100 °C pendant une durée déterminée permettant de détruire tous les microorganismes présents ainsi que les spores bactériennes (A Complete Course in Canning
and Related Processes, 2015). Lors de l’appertisation, le contenant et le contenu sont
stérilisés en même temps. La température majoritairement appliquée est de 121,1°C mais d’autres températures peuvent être employées comme 116 ou 118°C. La température utilisée aura une incidence sur la durée du traitement. La durée du traitement dépend de nombreux paramètres comme la taille de la boîte, le type de produit, les microorganismes d’intérêt et le nombre de réduction décimal considéré.
5
La stérilisation est employée pour des produits ayant un pH supérieur à 4,5 comme le foie gras, les terrines, les viandes, les plats cuisinés, les légumes et les potages (TECHNA, n.d.). Pour que la stérilisation soit efficace, le nombre de réduction décimal doit être de 12 d’après la réglementation française. Dans ces conditions, avec une température de 121,1°C, le temps de stérilisation est de 2,52 min lorsque l’on prend comme référence Clostridium
botulinum qui est le micro-organisme qu’il faut surveiller lors de la stérilisation. Avec cette
même température le temps passe à 12 min si le microorganisme est Clostridium sporogenes. Le processus de stérilisation se déroule en 3 phases. La première phase correspond à la montée en température. La deuxième phase est le chauffage à température constante. Cette phase représente le barème de stérilisation (par exemple 121°C pendant 2,52 min). La troisième phase correspond à la phase de refroidissement.
1.2.1.2. La pasteurisation
En présence d’un produit acide ou acidifié (pH inférieur à 4,5) la stérilisation est remplacée par un traitement thermique moins exigent qui se rapproche de la pasteurisation. La pasteurisation est un traitement thermique dont la température est comprise entre 65 et 100°C (UTICA, 2013). La pasteurisation est utilisée pour les jus de fruits, le lait, le cidre, le miel, la confiture, la compote, les fruits au sirop et le concentré de tomates (TECHNA, n.d.). La diminution de la température est liée au pH faible qui empêche la croissance des microorganismes. En effet la plupart des bactéries ont un pH minimal de développement de 4,5. En dessous de 4,5, seuls des bactéries lactiques (pH minimal de 3,3), des formes végétatives de bactéries pathogènes et d’altération, des moisissures, des levures, des enzymes et des toxines sont présentes. Après traitement thermique, seules des spores bactériennes subsistent mais ces spores sont inhibées par le pH acide (Laguerre, 2014; UTICA, 2013). Si la pasteurisation est appliquée sur des produits non acides, ces produits devront être conservés au réfrigérateur et la durée de conservation diminue (UTICA, 2013).
1.2.2. Effets du traitement thermique sur la qualité du produit
Le traitement thermique a des effets positifs et négatifs sur le produit. Plus la température est élevée, plus les qualités organoleptiques et nutritionnelles du produit sont affectées. Tout d’abord, les vitamines sont dégradées car ce sont des molécules très sensibles
6
à la chaleur. Les vitamines A, D, E, C (acide ascorbique), B1 (thiamine), et B2 (riboflavine) sont les plus sensibles en milieu acide (Awuah et al., 2007). Leur dégradation ne dépend pas uniquement de la chaleur mais aussi de l’oxygène, de la lumière et de leur solubilité dans l’eau. Les pigments sont aussi dégradés. La chlorophylle, les anthocyanes, les caroténoïdes et les bétanines (présents dans la viande) sont les principaux pigments dégradés (Awuah et al., 2007). La chlorophylle est convertie, sous l’action de la chaleur, en pheophytine puis en pyropheophytine ce qui entraine une diminution de l’intensité de la couleur verte. Les caroténoïdes sont quant à eux plus résistants à la chaleur que la chlorophylle. Cependant les caroténoïdes sont transformés en 5,6-epoxides et 5,8-epoxides qui ont une intensité plus faible (Awuah et al., 2007). Les anthocyanes qui sont des pigments rouges/ violets deviennent marron sous l’effet de la chaleur (Awuah et al., 2007). Les traitements thermiques modifient donc la couleur des produits (Laguerre, 2014). Cependant la disponibilité du lycopène (présent dans la tomate) et du béta carotène augmente grâce au traitement thermique (A
Complete Course in Canning and Related Processes, 2015).
La présence de sucres et de protéines associée à une haute température entraîne la formation de composés de Maillard (Awuah et al., 2007). La réaction de Maillard ou brunissement non enzymatique va avoir diverses conséquences. Des molécules volatiles apparaissent comme l’hydromethylfurfural (HMF) ou l’anhydride sulfureux. Ces molécules peuvent être toxiques à forte dose pour l’Homme donc leurs consommations doivent être limitées. L’HMF apparaît notamment lors de la cuisson de produits à base de céréales comme le pain et le pain de mie (Ramírez-Jiménez et al., 2001). Des pigments bruns sont formés ce qui est du à la formation de mélanoîdes. La formation de ces pigments modifie la couleur du produit. Dans le cas de l’appertisation, cette modification n’est pas souhaitée alors qu’elle l’est pour le pain de mie. Pour le pain de mie, la réaction de Maillard apporte du goût au produit mais entraîne une perte en acides aminés (lysine, ʟ-arginine, and ʟ -histidine) et la dénaturation des protéines (Awuah et al., 2007).
Quant aux végétaux, les parois cellulosiques sont dégradées. L’amidon peut être gélatinisé ce qui le rend plus facile à digérer. La mastication est donc plus facile (Ramesh, 2007). La texture sous l’effet d’un traitement thermique change. La texture devient moins ferme (Pedrosa et al., 2015). Cette perte de fermeté est liée à la perte d’eau et de molécules à faible poids moléculaire de la cellule. La pression de turgescence diminue. Une diminution
7
très importante de la fermeté est due à la solubilisation de substances pectiques, à la perte de la pression de turgescence et à un certain degré de séparation cellulaire (Gonçalves et al. , 2007). Les sucres et les minéraux ne sont pasaffectés par un traitement thermique mais dans le cas de l’appertisation une perte en minéraux et en sucre est observée (Pedrosa et al., 2015). Cette perte est due au passage des éléments du produit à la saumure qui est présente dans la boîte. Seuls des éléments solubles comme les sucres vont aussi passer du produit à l’eau. Ce phénomène s’appelle le lessivage (A Complete Course in Canning and Related Processes, 2015). La teneur en composés phénoliques diminue lors de la stérilisation. Cependant cela n’a pas toujours d’impact sur l’activité antioxydante. En effet d’autres composés sont formés. Ces composés peuvent avoir des propriétés anti-oxydantes. Dans ce cas, ces composés permettent d’obtenir un pouvoir antioxydant supérieur à celui du produit de départ (Nicoli et
al., 1999). L’augmentation du pouvoir antioxydant est associée à la formation de composés
de Maillard (Pedrosa et al., 2015).
Les protéines peuvent être dénaturées. Les protéines peuvent être affectées de deux manières différentes. La structure primaire peut être modifiée ce qui entraîne la diminution de la digestibilité de la protéine et sa non disponibilité. La dénaturation des structures secondaires, tertiaires ou quaternaires améliore la biodisponibilité des protéines en favorisant l’accès aux enzymes digestives (Awuah et al., 2007).
Le traitement thermique peut donc de nombreux impacts négatifs sur le produit mais il permet d’inactiver les enzymes, de détruire les micro-organismes, les spores et les toxines. Le microorganisme qui doit être absolument détruit est Clostridium botulinum. Clostridium
botulinum est une bactérie thermorésistante sporulante. Cette bactérie se développe en milieu
humide et anaérobie. Clostridium botulinum produit une neurotoxine appelée toxine botulique. La consommation de cette toxine à travers des boîtes de conserve mal stérilisées peut causer le botulisme (Gouvernement du Canada, 2013). Le botulisme est peu courant de nos jours mais le risque est toujours présent. Les inhibiteurs de trypsines présents dans les haricots verts sont des enzymes qui sont inactivées par le traitement thermique (Pedrosa et al., 2015). Son inactivation permet d’améliorer la digestion des protéines car les inhibiteurs de trypsines ont pour rôle d’empêcher leur digestion.
L’appertisation permet de conserver longtemps le produit grâce à un traitement thermique. Cependant ce traitement a un coût énergétique donc économique et a des
8
conséquences négatives sur la qualité du produit. Pour pallier à ces problèmes, de nouvelles méthodes doivent être développées. Ces méthodes devront permettre d’obtenir un produit proche de celui obtenu avec le processus d’appertisation normal (mêmes caractéristiques organoleptiques, texturales) et étant sain au niveau microbiologique. En s’appuyant sur le concept d’effet barrière (Leistner, 1994), la combinaison d’un autre traitement avec un traitement thermique moins important (température de traitement plus basse) pourrait être utilisé afin d’empêcher le développement des microorganismes. Le traitement thermique serait combiné à l’électro-activation qui permet de modifier le pH de l’aliment. La combinaison électro-activation avec un traitement thermique modéré pourrait assurer un gain économique ainsi que l’amélioration de la conservation du produit. L’économie serait liée à l’application d’un traitement thermique moins fort mais il faudrait également prendre en compte l’énergie nécessaire pour obtenir les solutions électro-activées.
1.3. L’effet barrière
De nombreux paramètres sont employés pour la conservation des aliments (Leistner, 1994). Dans certains cas, ils sont combinés entre eux afin d’assurer la sécurité microbiologique de l’aliment. La combinaison de ces paramètres est appelée l’effet barrière (en anglais, hurdles technology). Leistner est le premier scientifique à avoir utilisée cette notion. Les paramètres sont : la température (haute ou basse), le pH, l’activité de l’eau (aw),
les agents de conservation, le potentiel oxydant réducteur et la flore concurrente.
La température appliquée peut être haute ou basse. Une température haute température supérieur à 60°C) permet de détruire ou d’inhiber les enzymes, les microorganismes et leurs toxines. Les procédés utilisant des températures hautes sont la pasteurisation, la stérilisation et l’appertisation notamment. Des températures basses (température inférieure à 5°C) entraînent quant à elles le ralentissement de l'activité cellulaire, des réactions enzymatiques et du développement des microorganismes. La réfrigération et la congélation utilisent ce principe.
L’aw correspond à l’activité de l’eau. En diminuant l’aw, l’eau disponible dans le
produit diminue. Les microorganismes ont donc moins d’eau à leur disposition pour se développer. Les réactions enzymatiques sont limitées. L’aw peut être diminué par l’utilisation
9
de sel ou de sucre. Les procédés de séchage, de lyophilisation et de fumage notamment repose sur l’abaissement de l’aw (Leistner, 1992).
La diminution du pH empêche le développement de certains microorganismes. Chaque microorganisme possède un pH minimal de fonctionnement qui se situe entre 5,5 et 8. A un pH inférieur à 4,2 très peu de microorganismes survivent (Buche, 2014).
Une flore concurrente non pathogène peut être utilisée pour conserver le produit. Ce microorganisme va coloniser le milieu à la place de microorganismes pathogènes. Ce paramètre est retrouvé pour la fabrication du fromage, du yaourt. Pour le yaourt, la flore utilisée (bactéries lactiques) permet de diminuer le pH ce qui constitue une barrière supplémentaire.
Des agents de conservation comme des conservateurs, des antioxydants sont employés dans l’industrie afin de prolonger la durée de conservation du produit. Ce principe est à la base de nombreux procédés de fabrication dans l’industrie agroalimentaire et de nombreuses études s’intéressent à son application (Chauhan et al., 2014; Ena Gupta, 2013; Gabriel, 2015; Liato et al., 2015).
1.4. L’électro-activation
1.4.1. Principe général
1.4.1.1. L’électrolyse de l’eau
L’eau est un élément de base et est un des constituants majeurs des êtres humains. L’eau intervient dans de nombreuses réactions physico-chimiques et biologiques (U.S. Geological Survey, 2016). Une molécule d’eau est constituée d’un atome d’oxygène et de 2 atomes d’hydrogène. De part cette structure, l’eau est une substance possédant une structure stable ce qui limite son utilisation dans des réactions. L’électro-activation de l’eau change son état, sa structure et ses propriétés. L’eau se retrouve dans un état thermodynamiquement non stable ce qui la rend plus intéressante pour participer à des réactions chimiques. Les ions hydrogènes et hydroxydes sont séparés. Les ions hydrogènes vont pouvoir réagir avec des espèces chargées négativement tandis que les ions hydroxydes (OH-) réagiront avec des ions chargés positivement. Son activité biologique et chimique devient donc plus importante. L’eau obtenue par électro-activation est donc qualifiée d’eau « activée ».
10
Le procédé d’électro activation de l’eau repose sur le phénomène d’électrolyse (Shaposhnik et Kesore, 1997) et a été développé au Japon. Lors de l’électrolyse, l’eau est soumise à un courant électrique ce qui va provoquer diverses réactions (séparation des deux molécules de l’eau). Durant ce phénomène, deux réactions se passent simultanément : une réaction de réduction et une réaction d’oxydation.
La réaction d’oxydation a lieu du côté de l’électrode qui est chargée positivement. Cette électrode est appelée anode. La réaction de réduction a quant à elle lieu du côté de l’électrode chargée négativement appelée cathode. L’anode attire les ions chargés négativement et la cathode les ions chargés positivement lorsque le courant électrique circule dans le système.
Au niveau de la cathode: il y a captation d’électrons (e-). Les électrons réagissent avec les ions H+ (hydrogène) et forment un gaz qui est le dihydrogène (équation 1). La
réduction de l’eau donne quant à elle du dihydrogène et des ions OH- (hydroxyde) (équation
2) (Aider et al., 2012). Les équations représentent les phénomènes qui se déroulent au niveau de la cathode lors de l’hydrolyse de l’eau :
2 H+ + 2e− → H
2 (g) (Eq. 1)
2 H2O(l) + 2e− → H2 (g) + 2 OH− (aq) (Eq. 2)
Au niveau de l’anode, il y a libération d’électrons. L’eau est oxydée ce qui amène à la production de dioxygène qui est un gaz ainsi qu’à des ions H+. L’oxydation des ions OH- entraîne également la formation de dioxygène et d’eau. Les équations suivantes (3 et 4) présentent les réactions qui ont lieu du côté de l’anode :
2 H2O → O2 (g) + 4 H+ + 4e− (Eq. 3)
4 OH- (aq) → O
2 (g) + 2 H2O (l) + 4 e− (Eq. 4)
Lors de l’électrolyse de l’eau deux gaz sont formés : le dihydrogène et le dioxygène. Les électrons obtenus du côté de l’anode servent pour la réaction de réduction au niveau de la cathode.
La quantité de molécules d’hydrogène produite est deux fois supérieure à celle d’oxygène. Le volume de dihydrogène est donc supérieur à celui de dioxygène pour une
11
même pression et température (Aider et al., 2012). Ces réactions ont lieu au niveau de l’interface électrolyte/électrode. Afin de pouvoir avoir lieu, cette réaction a besoin d’une énergie importante qui est apportée par le courant électrique.
1.4.1.2. L’électrolyse d’une solution de NaCl
Le principe de l’électro-activation d’une solution de NaCl est le même que pour l’électrolyse de l’eau. Cependant les réactions qui ont lieu sont différentes et les ions présents ne sont pas les mêmes. Au niveau de l’anode, ou la réaction d’oxydation a lieu, les équations suivantes illustrent les réactions s’y produisant (Huang et al., n.d.):
2 H2O → O2 (g) + 4 H+ + 4e− (Eq. 5)
2 NaCl → Cl2 + 2 e - + 2 Na+ (Eq. 6)
Cl2 + H2O → HCl + HOCl (Eq. 7)
Du chlore est produit du côté de l’anode au court de l’électro-activation du NaCl. La solution électro-activée obtenue du côté de l’anode est une solution de HOCl (acide hypochloreux), une solution de HCl (acide chlorhydrique) diluée.
Du côté de la cathode, les réactions suivantes ont lieu (Huang et al., n.d.) :
2 H2O + 2 e- → 2 OH- + H2 (Eq. 8)
2 NaCl + 2 OH- → 2 NaOH + Cl- (Eq. 9)
Comme pour l’eau, du côté négatif, de l’hydrogène est libéré. La solution électro-activée obtenue est une solution de NaOH (hydroxyde de sodium) diluée.
1.4.1.3. Structure du réacteur
En pratique, l’électro-activation se déroule dans un réacteur électrochimique. Le réacteur est constitué de deux électrodes plongées dans un électrolyte. Pour une application agroalimentaire, l’électrode doit être inerte et insoluble dans le produit (Aider et al., 2012). De plus l’électrode doit avoir une bonne conductivité électrique et être résistante. Ces électrodes sont reliées à un générateur ce qui permet de soumettre la solution à un courant
12
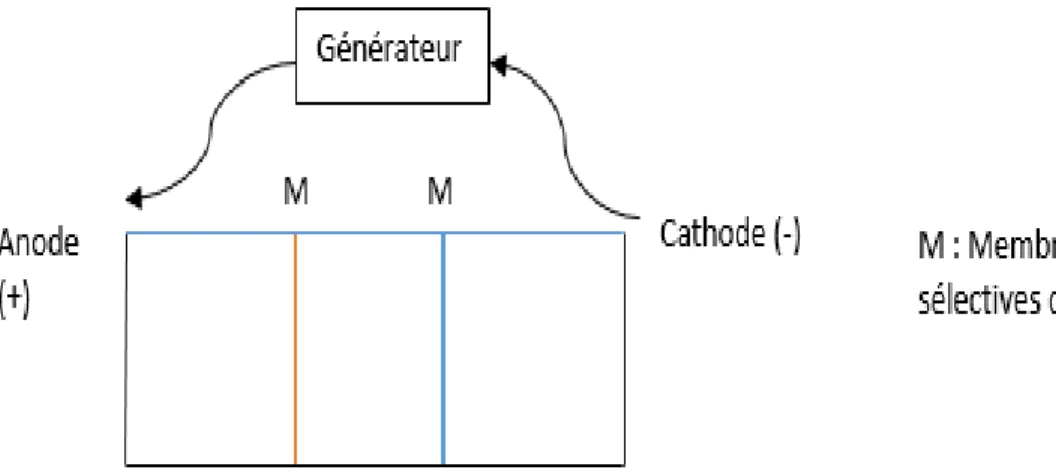
électrique. De plus, le système doit pouvoir maintenir les espèces d’intérêt du bon côté de l’électrode. Pour cela les sections anode et cathode sont séparées. La Figure 1 présente la configuration générale d’un réacteur.
Figure 1: Configuration générale d’un réacteur pour l’électro-activation de solutions
aqueuses
Le réacteur est composé de trois compartiments séparés par une membrane qui peut être sélective ou non à certains ions c’est-à-dire qu’elle peut laisser passer les ions d’un compartiment à un autre. Ces membranes permettent donc de séparer les solutions produites au niveau de l’anode en particulier les ions de celles produites au niveau de la cathode. Le type de membranes utilisées varie d’une étude à l’autre ainsi que la structure du réacteur et le type d’électrode. Cependant les membranes doivent posséder certaines caractéristiques. Les membranes doivent être chimiquement stables, avoir une faible résistance électrique, une porosité élevée et une conductivité électrique élevée (Aider et al., 2012).
1.4.1.4. Propriétés des solutions obtenues
Quel que soit l’expérience ou l’électrolyte utilisé (eau, eau distillée, NaCl ou NaHCO3), deux solutions sont générées. La solution générée au niveau de l’anode est appelée
anolyte. Elle est caractérisée par un faible pH (1,5 à 4,5), un potentiel oxydant réducteur (E) supérieur ou égal à 1150mV, un taux d’oxygène dissout élevé et la présence de chlore libre (Huang et al., n.d.). Le pH acide de la solution est lié à la libération des protons H+. Au niveau
13
hydrogène dissout et un potentiel oxydant réducteur inférieur à -950 mV. On parle de catholyte (Aider et al., 2012). Une solution ayant un fort pouvoir réducteur est obtenue du côté de la cathode et une solution avec un fort pouvoir oxydant est obtenue du côté de l’anode. L’électro-activation permet donc d’obtenir des solutions appelées électro-activées possédant des propriétés physico-chimiques et biologiques particulières. Elles deviennent plus réactives. Ces solutions sont caractérisées par leur pH, leur pouvoir oxydant réducteur et leur saturation en oxygène. Leur pouvoir oxydant-réducteur est lié à leur pH. En contact avec des matières organiques ou de l’eau normale, les solutions électro-activées perdent leurs propriétés et reviennent à leur état initial (Huang et al., n.d.). Ainsi, le pH de la solution ré-augmente. De plus leurs nouvelles caractéristiques sont plutôt stables dans le temps (Liato, 2015). L’obtention de solution électro-activée dépend de plusieurs facteurs : de la température, de la teneur en sel et du courant électrique appliqué (Aider et al., 2012; Aït-Aissa et Aïder, 2015).
1.4.2. Utilisation de l’électro-activation dans l’industrie agroalimentaire
L’électro-activation a de nombreuses applications en industries agroalimentaires. Les solutions électro-activées permettent d’inactiver des toxines, des spores, des levures, des moisissures et des bactéries. Elles sont aussi utilisées pour l’isomérisation du lactose, l’extraction de protéines ou dans la fabrication du pain. Leurs potentiels d’utilisation sont donc fortement intéressants.
1.4.2.1. Inactivation des microorganismes et des spores
L’électro-activation est un procédé permettant de détruire de nombreux microorganismes. En effet les solutions électro-activées sont des puissants désinfectants. De nombreuses études se sont intéressées à cette utilisation (Huang et al., n.d.). L’étude de Bari et al (2003) s’est intéressée à l’effet d’eau électro-activée acide (anolyte), d’une solution de chlore et d’eau distillée sur la destruction d’Escherichia coli O157:H7, Salmonella, et
Listeria monocytogenes à la surface de tomates. Le chlore est un composé qui est utilisé dans
l’industrie de l’eau en tant qu’antimicrobien. Les résultats ont montré que la solution électro-activée était plus efficace que celle de la solution de chlore de concentration 200 ppm (200 mg/L) pour la destruction des 3 microorganismes. La solution électro-activée ou anolyte possède donc des propriétés antimicrobiennes qui sont liées à la formation de chlore lors de
14
l’électro-activation. L’utilisation de solution d’acétate de sodium électro-activée a un effet antibactérien et anti-sporadique dans le cas d’une contamination par Clostridium sporogenes (Genois, 2014). Cette action n’est valable que lorsque la solution est activée. L’action antimicrobienne disparaît lorsque la solution revient à son état de départ (état stable) (Genois, 2014). En ce qui concerne les levures, les solutions électro-activées ont le même effet qu’avec les bactéries engendrant ainsi destructions. Cette caractéristique des solutions électro-activées est utilisée afin de stabiliser le vin. Une similarité d’efficacité entre la solution électro-activée et les sulfites a été observée (Godet et al., 1999). Cependant l’action des solutions électro-activées sur les microorganismes n’est pas totalement connue et reconnue. Les facteurs empêchant leur développement sont le faible pH, le potentiel oxydant réducteur positif, la présence de chlore et d’autres composés. Le pH acide empêche le développement de la plupart des bactéries car leur pH minimal est de 4,5 environ. Un potentiel oxydant réducteur supérieur à 1000 mV contribue à l’effet du pH acide. En effet pour les microorganismes aérobies le potentiel redox optimal est de 200 à 800 mV et pour les anaérobies de 200 à 400 mV (Best et al., 1985). Le bas pH peut fragiliser la membrane des bactéries ce qui entraine l’entrée d’HOCl dans la cellule. L’HOCl va oxyder des systèmes métaboliques de la cellule ce qui conduira à sa mort. Les solutions électro-activées entrainent la destruction de la membrane cellulaire et la libération du cytoplasme chez Candida albicans (Huang et al., n.d.). Le chlore, quant à lui, peut perturber la synthèse des protéines, réagir avec des acides nucléiques, etc. Un potentiel oxydant réducteur élevé peut causer des modifications métaboliques et des modifications de la production d’ATP (Huang et al., n.d.).
1.4.2.2. Isomérisation du lactose
L’électro-activation a été étudiée dans le cadre de l’isomérisation du lactose (Aider and Gimenez-Vidal, 2012; Aït Aissa and Aïder, 2013). L’isomérisation du lactose a lieu en présence d’un milieu alcalin. Le lactose s’isomérise en lactulose et en d’autres produits dérivés. Le lactulose est dégradé très rapidement après sa formation. Le lactulose est un saccharide utilisé dans l’industrie pharmaceutique et alimentaire (Aït Aissa and Aïder, 2013). Une étape de filtration est nécessaire afin de séparer le lactulose des autres composés après isomérisation. Cette étape de filtration a un coût important. Dans l’étude de Aït Aissa et Aïder (2013), la méthode d’électro-activation a été utilisée pour obtenir une haute teneur en
15
lactulose et une faible teneur en autres composés lors de l’isomérisation ; la solution de lactose était isomérisée dans le compartiment cathodique. Les résultats ont montré que l’isomérisation du lactose est toujours accompagnée par une faible quantité de galactose. En excluant le lactose, la pureté du produit final en lactulose était de 96% (Aït Aissa and Aïder, 2013). Sans exclure le lactose, la pureté du produit final en lactulose était de 31%. Les conditions optimales d’isomérisation du lactose étaient : pH de 9.84 à 11.77 avec une température de 22 à 32°C. La méthode d’électro-activation est donc une méthode relativement rapide, simple et peu coûteuse pour la synthèse du lactulose (Aït Aissa & Aïder, 2013). De plus, la synthèse de lactulose se déroule à l’intérieur d’un seul compartiment et n’est influencée que par le courant électrique et la configuration du réacteur (Aït Aissa and Aïder, 2014).
1.4.2.3. Extraction de protéines
L’électro-activation a été utilisée pour extraire les protéines du tournesol (Nabok and Plutahin, 2005) et du canola (Gerzhova et al., 2015). Dans l’étude de Nabok et Plutahin (2005), l’électro-activation a permis de créer un milieu favorable à l’extraction des protéines du tournesol (solution de pH 11) du côté de la cathode. Les protéines ont été extraites grâce à la solution catholytique. La solution obtenue à par la suite était transférée au compartiment anodique ce qui a entrainé la précipitation des protéines. Les protéines précipitent en présence d’un pH faible. Cette méthode a permis d’extraire 34% des protéines contenues dans le tourteau de tournesol. La méthode classique d’extraction des protéines est basée sur l’utilisation de solvant chimique comme NaOH. Avec cette méthode les auteurs ont démontré que le taux d’extraction était de 39%. Cependant cette méthode en plus d’extraire les protéines extrait également les fibres. Le pourcentage de protéines extraites est donc inferieur avec la méthode traditionnelle qu’avec l’électro-activation. L’électro-activation n’extrait que les protéines. Nabok et Plutahin (2005) ont aussi démontré que l’extraction par électro-activation peut être améliorée en contrôlant différents paramètres comme la taille des particules de tournesol, la surface de l’électrode et le flux. L’étude menée par Gerzhova et
al. (2015) sur le colza avait pour but de comparer deux méthodes d’extraction des protéines :
la méthode traditionnelle et la méthode utilisant l’électro-activation. Pour la méthode traditionnelle, les protéines étaient extraites grâce à une solution de NaOH. La solution
16
appelée catholyte obtenue du côté de la cathode après électro-activation servait quant à elle à l’extraction. L’extraction dans les deux cas a été réalisée sur le tourteau de canola (« soilcake »). Cette étude se rapproche beaucoup de celle menée sur le tournesol. Les résultats ont montré que l’utilisation de solution électro-activée est une bonne technique d’extraction des protéines. Les protéines étaient de meilleure qualité (moins de protéines dénaturées). L’extractabilité était supérieure avec l’électro-activation qu’avec la méthode conventionnelle. Le rendement en protéines pourrait être amélioré en augmentant le temps de traitement, la concentration en sel et l’intensité du courant.
1.4.2.4. Utilisation dans la cuisson de pain blanc
Nabok et Plutahin (2009)se sont intéressés à l’utilisation de solution électro-activée pour la fabrication du pain. Pour cela, ils ont considéré que la qualité du pain dépendait des ingrédients utilisés et notamment de l’eau. De plus, ils ont montré que la qualité de l’eau était un élément à prendre en compte dans la fabrication du pain. De nombreux paramètres de l’eau n’étaient pas pris en compte ce qui pouvait affecter ses fonctions biologiques et son potentiel. Le potentiel oxydant réducteur négatif de l’eau de table était à prendre en compte. Les solutions obtenues par électro-activation étaient caractérisées par une structure ayant une haute qualité de résonnance. Nabok et Plutahin (2009) ont étudié l’influence des solutions obtenues par électro-activation sur l’activation des levures de boulanger, sur les caractéristiques physiques et chimiques du pain après cuisson ainsi que la teneur en acides aminés. Cinq solutions électro-activées ont été utilisées. Quatre solutions (anolyte, catholyte, « drinkable » catholyte et « drinkable » anolyte) ont été obtenues à l’aide d’une méthode d’activation avec contact et une sans contact. Ces solutions étaient caractérisées par leur salinité, leur potentiel oxydant réducteur et leur pH. Les levures activées par la solution de catholyte présentaient la meilleure activité fermentaire. Pour la solution sans contact, l’activité de la levure était légèrement moins efficace qu’avec la catholyte (Nabok and Plutahin, 2009). L’anolyte n’avait pas complètement inhibé la fermentation même si du chlore était présent. Le pain obtenu à l’aide de la solution avec la méthode sans contact possédait les protéines ayant les meilleures propriétés biologiques. Le volume du pain avec solution électro-activée était supérieur à celui avec une solution d’eau normale. Le volume du pain était maximal avec la solution « drinkable » anolyte. Le volume du pain ainsi que
17
d’autres paramètres sont meilleurs lorsque la solution d’anolyte est utilisée qu’avec de l’eau normale.
1.5. Effets combinés d’un traitement thermique modéré et de solution
électro-activée sur la qualité microbiologique et organoleptique du produit
Récemment, (Genois, 2014)et Liato (2015) se sont intéressés à l’effet de solution électro-activée combinée à un traitement thermique modéré sur la qualité organoleptique des haricots verts. Dans l’étude de Genois (2014), deux méthodes ont été comparées. La méthode classique utilisait une saumure constituée d’eau distillée et de chlorure de sodium (3%) avec un traitement thermique de 121°C pendant 10 min. La nouvelle méthode consistait à utiliser une solution d’acétate de potassium électro-activée avec pour traitement thermique : 95°C pendant 12 min. Les analyses ont été réalisées à intervalle de temps régulier (tous les trois jours) pendant 12 jours. La fermeté et la croustillance ont été mesurées à l’aide d’un texturomètre. La matière sèche a été aussi mesurée sur la saumure afin de voir la perte de matière sèche du produit. La couleur a été mesurée grâce à un colorimètre basé sur l’échelle L*a*b. La vitamine C a été dosée grâce à l’adaptation de la méthode AOAC 967,21. Les résultats de Genois (2014) ont montré que les traitements avaient un impact sur la texture du haricot. La nouvelle méthode de conservation a permis de conserver la texture du légume. La texture obtenue se rapprochait de celle du produit frais. La texture ne variait pas au cours du temps. La teneur en vitamines C diminuait avec le temps mais aucune différence entre les deux traitements n’a été observée. Aucune différence de couleur n’a été observée entre les traitements. Le procédé combinant l’électro-activation avec un traitement thermique modéré a permis de préserver au maximum les nutriments dans le produit (Genois, 2014). Liato (2015) a obtenu les mêmes conclusions sur le pois et le maïs en ce qui concerne la vitamine C.
Scheichtele (2013) s’est également intéressé à l’effet de solution électro-activée combinée à un traitement thermique sur la qualité organoleptique de maïs et de petits pois congelés. De récentes études se sont également intéressées à l’effet de solution électro-activée combinée à un traitement thermique sur la destruction de microorganismes (Genois, 2014; Liato et al., 2015). Genois (2014) s’est focalisé sur le microorganisme Clostridium
18
même température optimale de croissance) que Clostridium botulinum sans être autant toxique pour l’homme. La méthode employée dans l’étude utilisait une solution d’acétate de sodium électro-activée caractérisée par un temps d’électro-activation de soixante min avec une heure de relaxation soit une heure entre la fin de l’électro-activation et l’immersion des spores. Les microorganismes ont été complétement détruits avec la combinaison solution d’acétate de potassium électro-activée et un chauffage à 95°C. Liato et al. (2015) s’est quant à lui focalisé sur Clostridium sporogenes et Geobacillus stearothermophilus. Les résultats ont montré que les solutions d’électro-activation combinées à un traitement thermique permettaient d’inhiber la croissance des spores pour les 2 types de microorganismes. Les solutions électro-activées ont donc une action anti-sporadique.L’électro-activation combinée à un traitement thermique modéré a permis d’obtenir un produit semblable voir meilleur en matière de texture à celui généré avec le procédé d’appertisation classique. De plus cette nouvelle méthode a permis de protéger le produit vis-à-vis des microorganismes. Le produit obtenu était sain microbiologiquement et ne présentait pas de danger pour l’organisme. Cependant l’aspect toxicologique reste à approfondir. En effet, il est nécessaire de valider que le nouveau procédé utilisé n’engendre pas d’altération du matériau constituant la boîte pouvant, par diffusion, contaminer le produit.
1.6. Transferts entre matériaux et aliment
L’appertisation peut être réalisée avec différents types d’emballage. Les emballages peuvent être en verre, en métal ou en plastique. Les plus employés sont le verre et le métal mais l’utilisation du plastique est de plus en plus importante.
1.6.1. Verre
Le verre est un matériau chimiquement inerte. Il protège le produit des gaz et des liquides cependant le produit n’est pas protégé de la lumière (Bonhoure, 2014). Le verre résiste moins au choc que les boîtes en métal. De plus le verre est un matériau recyclable mais lourd. Etant inerte, des problèmes de transfert de composés de l’emballage vers le produit ne sont pas présents. Le couvercle des bocaux en verre est généralement constitué de métal. Si un liquide est en contact prolongé avec le couvercle il se peut qu’il y ait passage d’éléments du couvercle à la saumure.
19 1.6.2. Boîte en métal
Le métal est utilisé en agroalimentaire en tant qu’emballage sous forme de récipients aérosols, de tubes, de plateaux, de fermetures, de couvercles et de boîtes de conserve. La boîte de conserve est l’emballage à base de métal,le plus employé aujourd’hui. La boîte sert à conserver divers produits comme la viande, le poisson, les fruits et légumes ainsi que les boissons. Les boîtes de conserve sont classées selon leur dimension, leur composition, le traitement qu’elles subissent et le vernis utilisé. Le corps de la boîte est fait principalement d’acier mais de l’aluminium peut être employé.
1.6.2.1. Composition des boîtes de conserves 1.6.2.1.1. Boîtes en aluminium
L’aluminium est utilisé pour fabriquer des boîtes dites embouties (FAO, n.d.). Les boîtes embouties sont constituées de deux pièces : le couvercle et le corps de la boîte. Pour obtenir le corps, l’aluminium est découpé en rondelles qui sont par la suite soumises à l’action d’une presse. Des coupelles sont formées (CIEMRA, 2004). Les coupelles obtenues sont étirées afin de leur donner la forme souhaitée. Le couvercle est attaché au corps de la boîte par sertissage. Les boîtes embouties à base d’aluminium servent principalement à l’emballage des boissons gazeuses et des bières. Cet emballage porte le nom de cannettes. L’aluminium peut être utilisé pur ou sous forme d’alliage. Les alliages d’aluminium contiennent du magnésium, du fer, du manganèse, du cuivre et du zinc (Oldring and Nehring, 2007). L’aluminium est résistant à la corrosion. Une couche d’oxyde d’aluminium se forme en présence d’oxygène ce qui lui sert de protection. Ces oxydes sont peu solubles à pH neutre. A pH inférieur à 4,5 et supérieur à 8,5 leur solubilité augmente (Oldring and Nehring, 2007). L’aluminium pur est attaqué par la plupart des acides dilués. L’aluminium au contact des aliments peut être dissous. Pour éviter cette dissolution, des vernis sont appliqués. Le vernis permet d’éviter la corrosion et la migration des éléments de l’emballage au produit. En pratique un vernis est toujours appliqué. En absence de vernis, le taux de dissolution de l’aluminium dépend de l’acidité du produit et de la solubilité des sels formés (Oldring and Nehring, 2007). Comparativement à l’acier, l’aluminium permet d’obtenir un emballage plus léger.
20 1.6.2.1.2. Boîtes en acier
L’acier est utilisé pour l’emballage des aliments. Différents types d’aciers sont utilisés : L (« low residual »), MC et MR (« medium residual ») (Mannheim, 1986). Ces aciers diffèrent selon leur composition. L'acier L est utilisé pour les aliments acides hautement corrosifs. L'acier MR est utilisé pour les produits qui sont peu corrosifs. Leurs propriétés sont différentes ainsi que leur résistance à la corrosion (Mannheim, 1986). L'acier est constitué principalement de fer (Fe) et de carbone (C) (Valdez et al., 2008). D'autres éléments tels que le manganèse, le phosphore, le soufre, le nickel, l’aluminium, le cuivre et le chrome peuvent être présents (DGCCRF, 2015; Total materia, n.d.). L’acier est sensible à la corrosion. L’acier n’est donc pas utilisé seul pour les emballages en métaux. L’acier est le plus souvent combiné à de l’étain (Sn). L’acier combiné à de l’étain est appelé fer blanc. Le fer blanc est utilisé dans 80% des emballages alimentaires en métal (Xia et al., 2012). Le fer blanc est obtenu en recouvrant des deux côtés la plaque d’acier par de l’étain (Bonhoure, 2014). La couche d’étain peut être appliquée par deux processus : un procédé chimique ou un procédé électrolytique (Mannheim, 1986). Le procédé électrolytique est le plus employé. Le fer blanc obtenu par le procédé électrolytique est désigné par les sigles ETP signifiant electrolitic tinplate. Le procédé utilisé a une influence sur la résistance à la corrosion de la boîte de conserve (Mannheim, 1986). Le taux d’étamage varie de 1 à 15,1g/m2. Entre la
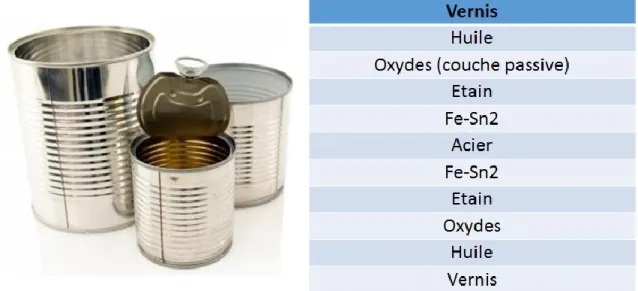
couche d’étain et l’acier, une couche d’alliage Fe-Sn est présente. La couche d’alliage Fe-Sn permet une meilleure adhésion de l’étain. Les couches d’acier, d’alliage Fe-Sn et d’étain constituent les couches de base du fer blanc. A travers d’autres traitements, une couche d’oxydes et un film d’huile sont appliqués afin d’augmenter la qualité du fer blanc(Vignes et al., 1994). L’application d’un vernis peut être réalisée par la suite pour protéger l’emballage, mais cette action n’est pas systématique (Figure 2).
21
Figure 2: Composition du fer blanc adapté de FAO et Vignes et al. (1994)
La couche d’étain permet de protéger l’acier de l’attaque du produit et de l’atmosphère. L’étain empêche la décoloration, la perte de flaveur du produit et la détérioration de l’emballage (structure) (Vignes et al., 1994). La couche d’étain permet de limiter les phénomènes de corrosion et apporte un environnement chimique réducteur. L’oxygène présent est réduit par la dissolution de l’étain. La réduction de l’oxygène minimise l’oxydation du produit. La perte de couleur et de flaveur est limitée (Mannheim, 1986). Cependant l’étain ne permet pas de protéger la boîte de toutes les attaques. Le fer blanc est donc, en fonction du produit, recouvert d’une couche de vernis. Comme pour les boîtes en aluminium, le vernis permet de protéger le métal du produit et d’empêcher la migration d’éléments de l’emballage au produit. Le fer blanc est employé pour la fabrication des couvercles et des boîtes trois pièces. Les boîtes trois pièces sont constituées d’un fond, d’un couvercle et du corps. Le corps de la boîte est formé à partir d’une plaque de fer blanc roulée. De l’étain est utilisé pour souder la plaque ce qui permet d’obtenir un cylindre. Avant l’étain, le plomb était utilisé pour réaliser la soudure. Le plomb est cependant un métal toxique et qui peut s’accumuler dans le corps (Oldring and Nehring, 2007). Son utilisation a donc été interdite. Le fond et le couvercle sont sertis au corps de la boîte (CIEMRA, 2004). Le fer chromé est utilisé en tant qu’alternative au fer blanc. Le fer chromé est désigné par les sigles ECCS (electrolytic chromium/chromium oxide coated steel) et TFR (tin free steel). Ce type d’emballage permet de limiter l’utilisation de l’étain qui est un matériau couteux. La plaque
22
d’acier est recouverte d’une couche de chrome, d’une couche d’oxyde de chrome et d’huile. La couche de chrome permet d’éviter l’oxydation atmosphérique, d’améliorer l’adhésion de vernis (Oldring and Nehring, 2007). Le TFR possède une haute résistance à la corrosion. Un vernis doit être appliqué des deux côtés du fer chromé. Le fer chromé ne peut pas être soudé (Mannheim, 1986). Il est utilisé pour la fabrication de boîtes embouties, des fonds et des couvercles des boîtes de conserve. Ce métal est inapproprié pour les produits acides (Mannheim, 1986). Trois grands types de matériaux sont donc utilisés pour la fabrication des emballages alimentaires : l’acier (fer), l’aluminium et l’étain. Ces emballages présentent de nombreux avantages mais interagissent avec l’aliment et l’environnement.
1.6.2.2. Attaque des boîtes de conserves alimentaires 1.6.2.2.1. Attaque externe
La boîte de conserve subit deux attaques en parallèle : une à l’intérieur et une à l’extérieur. Sur la face externe, une oxydation à l’air a lieu (Vignes et al., 1994). Si de l’acier est mis à nu, de la rouille se forme. La rouille n’a pas d’impact direct sur le produit mais plutôt sur l’esthétique. L’oxydation de l’acier est évitée grâce à la couche d’étain. L’application d’un vernis par-dessus l’étain contribue à pallier au risque de formation de rouille (Vignes et al., 1994).
1.6.2.2.2. Attaque interne
1.6.2.2.2.1. Processus de corrosion
A l’intérieur de la boîte, la corrosion survient. La corrosion correspond à l’altération d’un objet, d’un métal par contact avec un oxydant comme l’O2 et les ions hydroxyde (H+).
Ce phénomène s’accompagne de la production de produits de corrosion et provoque un gonflement des boîtes, l’apparition de perforations et la modification du goût des aliments. La corrosion est liée au contact de deux matériaux: l’étain et le fer. Ces matériaux forment une pile qui baigne dans une solution servant d’électrolyte. Le fer et l’étain peuvent jouer à la fois le rôle d’anode, borne positive de la pile, et de cathode, borne négative. Le rôle des métaux dépend du potentiel d’oxydo-réduction (E°) qui est de – 0,14 V pour le couple Sn2+/Sn et de – 0,44 V pour le couple Fe2+/Fe en solution aqueuse (Vignes et al., 1994). En
solution aqueuse, le fer sera donc préférentiellement oxydé et jouera le rôle d’anode car son potentiel est plus élevé. Cependant, ce potentiel dépend de plusieurs facteurs dont le pH, la