République Algérienne Démocratique et Populaire Ministère de l’Enseignement Supérieur et de la Recherche
Scientifique
Université Ahmed DRAÏA Adrar Faculté des Sciences et de la Technologie Département de Sciences de la nature et de la Vie
MEMOIRE
MASTER 02 ACADEMIQUE Domaine : Sciences de la nature et de la vie
Filière : Sciences agronomiques
Spécialité : Système de production agro-écologique Intitulé
Présenté par :
ABDOULLAHI Fatiha
KADRI Manel
Membre de juré :
o Président : Mme HADEF Khawla M.C.B Univercité d’Adrar o Examinateur : Mme HENOUDA Sarra M.A.B Univercité d’Adrar
o
Promoteur : Mr. KADRI Yasser M.A.A Univercité d’Adraro Co Promoteur: Dr. NANI Abdelhafid M.CB Univercité d’Adrar
Année Universitaire : 2018/2019
Etude ethnobotanique et antimicrobienne de
Carthamus tinctorius
et
Ammodaucus leucotrichus à
Avant tout on remercie ALLAH tout puissant de nous avoir donné le
privilège, la chance d’étudier et de nous avoir donné force, courage, et
patience pour accomplir ce travail. Sans oublier nos parents qui ont
veillé sur nous durant toute notre vie.
Nous remercions naturellement notre encadreur Mr. KADRI Yasser, pour
ces conseils et orientations éclairées,
Nous remercions Mr NANI Abdelhafid Co-promoteur soit assuré de nos
profondes gratitudes pour sa précieuse collaboration, ses critiques
constructives, son support et ses encouragements.
Nous remercions Mr . MEKNASSI Abdelkader Attaché de Recherche à
l’Unité de Recherche en Energie Renouvelables en Milieu Saharien
d’Adrar.
Nous remercions Mme. BAHIANI Malika, et Nos remerciements vont à
tousle personnel de soutien à la recherche du laboratoire de département
des Sciences Natural et de Vie et biochimie, Nous remercions aussi les
membres du jury Mme Hadef Khawla Mme Henouda Sarra de nous avoir
honorés en acceptant de juger ce travail,
Nous exprimons nos vifs remerciements à tous ceux qui nous ont aidés de
près ou de loin en complétant l’enquête que nous avons faite, et
encouragé pour la réalisation de ce mémoire, qu’ils trouvent ici
l’expression de nos remerciements les plus sincères. Nos remerciements
vont également à tous nos enseignants qui ont contribué à notre
formation,
N'oublie pas tous les amis qui nous ont aidés financièrement et
moralement le long de ce travail et particulièrement MESSAOUDI .A,
BEN SAÏD .A qui ont su créer une ambiance chaleureuse de camaraderie
et de travail qui restera un souvenir que nous conservons de cette
période.
Dédicace
Je dédie ce travail à
Ma chère Mère Mme Nadia
Mes chers enfants Lydia et Riyad
Mon cher époux Mr Mourad
Ma chère sœurs Mme Souad
Mes chers frères Brahim, Fathi et le plus gâté de la famille Amir
Tous les membres de ma famille
« Kadri » et « Ghezal »
Tous mes amis
Mes collègues de Djezzy
Toute personne contribue de loin et de près à l’élaboration de
ce travail.
Dédicace
Je dédie ce travail à
Mes chers parents
Mes chère fille Aicha
Mon cher époux Mr abdelkrim
Ma chère sœurs Mme Mebarka
Tous les membres de la famille
«ABDOULLAHI »
Tous mes amis
Toute personne contribue de loin ou de près à l’élaboration de
ce travail.
Liste des abréviations
A. Ammodaucus : Ammodaucus leucotrichus C.tinctiriusus : Carthamus tinctorius
Carthame : Carthamus tinctorius T° : Température
V : Vent H : Humidité
N : nombre d’échantillon Global P1 :Poid du creuset avec couvercle
P2 : Poid du creuset avec couvercle + échantillon
P3 : Poid de l’échantillon après séchage P1-P2 MeOH : Méthanol
H2O : Eau
MeOH / H2O : Solution eau méthanol
DMSO : Diméthylesulfoxyde
CMI : Concentration minimale inhibitrice CMF : Concentration minimale fongicide M.S : Matière sèche.
Synthese bibliographique
Chapitre I : Phytotérapie
I.1. Etude ethnobotanique. 2
I.2. Etude ethnobotanique. 2
I.2 Etudes ethnobotaniques en Algérie 2
I.2. Phytothérapie. 2
I.2.1. Avantages de la phytothérapie 3
I.2.2 Inconvénients de la phytothérapie 3
I.3. Métabolites secondaires . 3
I.3.1 Polyphénols 4
I.3.2 Alcaloïdes. 4
I.3.3 Terpènes et stéroïdes 4
Chapitre II : Généralités sur les plantes étudiées
II. Plantes étudiées 5
II.1 Carthamus tinctorius. 5
II.12. Description botanique du Carthamus tinctorius 5
II.1.3. Classification botanique du Carthamus tinctorius. 5
II.1.4. Composition chimique . 7
II.1.5. Utilisations traditionnelles du Carthame . 7
II.1.6. Utilisations et les bienfaits du Carthame 7
II. 2. Ammodaucus leucotrichus 8
6.2.1 Description botanique d’Ammodaucus leucotrichus 8
6.2.3. Effets therapeutique d’Ammodaucus leucotrichus. 9
Chapitre III : Fusarium oxysporum
III.1. Maladie vasculaire du palmier dattier ‘El Bayoud’ 10
III.2. Cycle de vie du Fusarium oxysporum 11
Chapitre VI : Matériel et méthodes
I. Enquête ethnobotanique 12
I.1. Présentation de la zone d’étude 12
I.1.1 Situation géographique de la wilaya d’Adrar 12
I.1.2 Informations géographiques générales de la daïra de Zaouiet konta. 13 I.1.3Informations géographiques générales de la daïra Tamentit 14
I.2. Climatologie 15
I.2.1 Précipitation. 15
I.2.2 Température 16
I.2.3 Vent 16
I.2.4Humidité de l’air 17
I.3. Etude ethnobotanique. 18
I.3.1Choix de zone d’étude. 17
I.3.2Identification de plante médicinale 19
II. Evaluation de l’activité antifongique
II.1. Matériels végétale 20
II.2. Taux d’humidité 21
II.3. Evaluation du pouvoir antimicrobien des extraits hydroalcooliques 22
II.3.1. Préparation de l’extrait brut. 22
II.3.2 Préparation des milieux de culture. 24
II.3.3. Préparation de l’inoculum. 24
A.Isolement et purification 24
B. Préparation des pré-cultures de souches fongiques. 24
II.3.4. Test antifongique (Bercheet al., 1991). 25
A. Préparation de la suspension sporale 25
C. Détermination de la CMF 28
Chapitre V : Résultat et discussion
I. Enquête ethnobotanique
I.1. Classes d’âge . 29
I.2. Niveau d’étude 29
I. 3. Situation familiale 30
I.4. Habitat 30
I.5. Sexe . 31
I.6. Type de plante . 31
I.7. Partie utilisée. 32
a) Carthamus tinctorius 32
a) Ammodaucusleucotrichus 32
I.8. Modes de préparations. 33
a) Carthamus tinctorius. 33
a) Ammodaucusleucotrichus 33
I.9. Dose utilisée 34
a) Carthamus tinctorius 34
a) Ammodaucusleucotrichus 34
I.10. Maladie traitées 35
I.11. Mode d’administration 36
a) Carthamus tinctorius 36
a) Ammodaucusleucotrichus 36
I.12. Résultat d’utilisation 36
a) Le 2arthamus tinctorius 36
a) Ammodaucusleucotrichus 37
II. Evaluation de l’activité fongique. 38
II.1. Taux d’humidité 38
II.2. Rendements d’extractions . 38
II.3. Résultats du pouvoir fongique 39
A. Détermination de la CMI 39
B. Détermination de la CMF 40
Discussion 41
Conclusion 43
Tableaux page
Liste des Figures
Figures Page
Figure 01 : Carthamus tinctorius à Tamentit Adrar 5
Figure 02 : Feuilles de Carthamus tinctorius à Tamentit Adrar 6
Figure 03 : Fleur de Carthamus tinctorius à Tamentit, Adrar. 6
Figure 04 : Grains de Carthamus tinctorius à Tamentit Adrar 6
Figure 05 : Ammodaucus leucotrichus 2019 à Tamentit Zaouiet Konta 8
Figure 06: Fleurs d’Ammodaucus leucotrichus à Zaouiet Konta. Adrar 9
Figure 07 :Grains d’Ammodaucus leucotrichus 2019 à Tamentit 9
Figure 8 : Forme morphologique du Fusarium oxysporum photo originale source
INRA Adrar
10
Figure 9 : Palmier infecté par « El Bayoud » 11
Figure 10:Répartition géographique de la wilaya d’Adrar 12
Figure 11 Situation géographique de Zaouit Konta 13
Figure 12 Situation géographique de Tamentit 14
Figure 13 : Distribution mensuelle des précipitations l’année 2017 15
Figure 14 : Température moyennes/mois de l’an 2017 16
Figure 15 : Vitesse du vent (m/s) à Adrar l’an 2017 17
Figure 16 : Humidité Relative De l’air à Adrar l’an 2017 18
Figure 17 : Plante Ammodaucus leucotrichus 20
Figure 18 : Grains d’Ammodaucus leucotrichus 20
Figure 19 : Plante Carthamus tinctorius 20
Figure 20 : Fleur de Carthamus tinctorius 20
Figure 21 : Echantillons sur balance 22
Figure 22 : Séchage de la matière végétale dans l’étuve 22
Figure 23 : Macération sur agitateur magnétique 22
Figure 24 : Filtration du mélange sur centrifugeuse 22
Figure 25 : Dégraissage du Carthamus tinctorius 23
Figure 26 : Dégraissage d’Ammodaucus leucotrichus 23
Figure 27 : Evaporation sur évaporateur rotatif 23
Figure 28 : Récupération de l’éxtrait 23
Figure 29 : Ébullition pendant 1h 24
Figure 30 : Filtration de la solution 24
Figure 31 : La souche de fusarium oxysporium f.sp albedinus 25
Figure 32 : comptage sur cellule de Malassez 25
Figure 33 : Ensemencement sur milieu liquide 26
Figure 37 :Pourcentage d’utilisation des plantes médicinales par classe d’âge 29
Figure 38 : Pourcentage d’utilisation des plantes médicinales selon le niveau d’étude
29
Figure 39 : Pourcentage d’utilisation des plantes médicinales selon le la situation familiale
30
Figure 40 : Pourcentage d’utilisation de la plantes médicinales par habitat 30
Figure 41 : Répartition de la fréquence d’utilisation de la plantes médicinales par le sexe Adrar
31
Figure . 42 : Pourcentage des différents types de plantes cultivées. 31
Figure 43 : Pourcentage des parties utilisées de Carthamus tinctorius 32
Figure 44 : Pourcentage des parties utilisées de l’Ammodaucus leucotrichus 32
Figure 45 : Modes de préparations Carthamus tinctorius 33 Figure 46 : Les modes de préparations d’Ammodaucus leucotrichus 33
Figure 47 : Doses utilisées du Carthamus tinctorius 34
Figure 48 : Doses utilisées de l’Ammodaucus leucotrichus 34
Figure 49 : Maladies traitées par Carthamus tinctorius et l’Ammodaucus
leucotrichus
35
Figure 50 : Mode d’administration du Carthamus tinctorius 35
Figure 51 : Mode d’administration du Ammodaucus leucotrichus 36
Figure 52 : Résultats d’utilisation du Carthamus tinctorius 36
Figure 53 : Résultat d’utilisation Ammodaucus leucotrichus 37
Figure 54 : Rendement massique du Carthamus tinctorius et Ammodaucus leucotrichus
38
Figure 55 : Détermination de la CMI de l’extrait du Carthamus tinctorius (A) et l’extrait de l’Ammodaucus leucotrichus (B).
39
Figure 56 : Résultats du CMF l’extrait de l’Ammodaucus leucotrichus. 40
INTRODUCTION
GENERALE
Durant des siècles et même des millénaires, l’homme a utilisé les plantes pour soulager ses douleurs, guérir ses maux et panser ses blessures. De génération en génération, il a transmis son savoir et ses expériences (Tabuti et al., 2003).
L’Algérie est connue par sa vaste superficie ainsi par la diversité de son climat et ses plantes qui ont des utilisations diverses dans l’ensemble des terroirs du pays. D’ailleurs, la richesse de la flore algérienne en plantes médicinales et aromatiques est incontestable.
La région de Touat de la wilaya d’Adrar est très riche en plantes médicinales qui sont plus souvent spontanées. A ce jours, malgré le progrès de la pharmacologie, l’usage thérapeutique des plantes médicinales est très présent dans certains pays du monde et surtout les pays en voie de développement (Benkhnigue et al., 2011).
Les plantes contiennent des composés phytochimiques qui appartiennent à leurs métabolismes secondaires. Les métabolites secondaires ont des activités antioxydantes, anti-inflammatoires, antimicrobiennes, anticancéreuse, antihyperglycémiantes, antihyperlipidémiantes, etc.
La présente étude a pour objectif de faire une enquête ethnobotanique de deux plantes utilisées dans la pharmacopée de la région d’Adrar à savoir : Carthamus tinctorius et Ammodaucus leucotrichus. Ces enquêtes servent à trouver des informations relatives à leurs utilisations traditionnelles. Ensuite, nous envisageons de procéder une extraction des métabolites secondaires par le méthanol puis, de déterminer l’activité antifongique des extraits de ces deux plantes sur la croissance micellaire du Fusarium oxysporum f sp albedinis.
CHAPITRE
I
I. 1. Etude ethnobotanique
I.1.1. Définition de l’étude ethnobotanique : c’est une contraction d'ethnologie et de botanique, est l'étude des relations entre l'Homme et les plantes. C’est une étude multidisciplinaire incluant les recherches archéologiques sur les civilisations anciennes jusqu'à la bio-ingénierie de nouvelles cultures comme le blé (Croza, 2001). C’est le synonyme de l’étude de plantes par des populations primitives.
I.1.2. Etude ethnobotanique en Algérie
L’Algérie reconnue par sa large superficie et la diversité de climat, ses conditions la rend riche par une vaste gamme de plantes médicinales et aromatiques, ainsi que leurs diverses utilisations populaires.
Dans le cadre d'une collaboration avec le programme d'union internationale pour la conservation de la nature (U.I.C.N) d'Afrique du nord, une enquête ethnobotanique a été réalisée dans la région de Batna. Cette étude a permis de recenser 200 plantes médicinales les plus utilisées par la population (Ghozel et Souilem, 2018). Le groupe SAIDAL (centre de recherche la développement) a réalisé plusieurs contributions à l'étude ethnobotanique, dans le cadre de valorisation de la flore médicinale Algérienne, qui ont été réalisées dans certaines régions de l’Algérie telle l’étude ethnobotanique réalisée dans la région de Bordj Bou Arreridj et dans le parc national de Chréa (Ghozel et Souilem, 2018).
De plus, plusieurs enquêtes ethnobotaniques ont été initiées à travers des mémoires de magistère et des thèses de doctorat et des articles de différentes universités sur de nombreuses espèces médicinales (Bouziani et Sidi ali,2018), (Ghozal et Souilem, 2018), (Kadri et al., 2008).
I.2. Phytothérapie
La phytothérapie, c’est l’emploi de plantes ou de médicaments à base de plantes (infusions, poudres, préparations en ampoules, etc.) pour soigner naturellement les différents maux du corps humain (Unis et Bakhtaoui, 2017). Les plantes constituent une réponse de choix pour fournir, de façon naturelle, à l’organisme les substances nécessaires pour maintenir son équilibre vital (Lahsissene et al., 2009).
Dans le code de la santé publique, il n'existe pas de définition légale d'une plante médicinale au sens juridique, mais en France « une plante » est dite médicinale lorsqu'elle est inscrite à la pharmacopée et que son usage est exclusivement médicinal. C’est-à-dire qu’elle
Chapitre I. Phytothérapie
3 est présentes pour leurs propriétés préventives ou curatives à l'égard des maladies humaines ou animales (Moreau, 2003).
Dans la médecine traditionnelle les plantes utilisées ou bien au moins une partie possède des propriétés médicamenteuses. Leur action provient de leurs composés chimiques (métabolites primaires ou secondaires) ou de la synergie entre les différents composés présents (Sanago, 2006).
I.2.1. Avantages de la phytothérapie
Les médicaments actuels classiques provoquent souvent des effets secondaires néfastes. La phytothérapie présente moins d'effets secondaires aux médicaments chimiques qui peuvent avoir des mauvaises répercussions. Il semble que le corps humain est mieux adapté à un traitement à base de plantes qu'à une thérapie chimique. (Zidane M., 2017)
Les plantes possèdent des molécules bioactives réparties dans tous les parties de la plante les feuilles, les grains, les racines, l'écorce, les sommités fleuries, les fruits, etc. Les parties utilisées de la plante varient d'une espèce à l'autre, ou pour une même plante selon l'effet désiré.
I.2.2. Inconvénients de la phytothérapie
Le manque de preuves scientifiques n'est pas en faveur de l'efficacité de la phytothérapie, la plupart des déclarations concernent les effets thérapeutiques sont faites par des praticiens eux-mêmes. Beaucoup d'entre eux n'ont pas été vérifiés scientifiquement. Le diagnostic souvent imprécis, le moyen de diagnostic connu est l'odorat, apparition des symptômes, testes d'efficacité non connus, interrogation des esprits et ancêtres chez certaines religions. Ainsi, le dosage des produits est arbitraire et imprécis. De même les méthodes de préparation sont parfois non hygiéniques (Sofowora, 2010).
I.3. Métabolites secondaires
I.3.1. PolyphénolsLes polyphénols ou composés phénoliques forment une grande classe de produits chimiques qu’on trouve dans les plantes au niveau des tissus superficielles, ils sont des composés phytochimiques polyhydroxylés et comprenant au moins un noyau aromatique à (06) six carbones (Sarni-Manchado et Cheynier, 2006).
Ces molécules constituent une famille riche en principes actifs que l'on trouve chez les plantes, ils ont un rôle principal dans la vie de la plante, dans sa défense contre les pathogènes ; principalement les moisissures et les bactéries phytopathogènes et la protection contre les rayonnements UV ; sachant que tous les composés phénoliques absorbent les rayonnements solaires (Sarni-Manchado Et Cheynier, 2006).
Les polyphénols sont classés en acides phénoliques, flavonoïdes, tanins, stilbènes.
I.3.2. Alcaloïdes
Ce sont des substances organiques azotées d'origine végétale, de caractère alcalin et des structures complexes (noyau hétérocyclique), on les trouve dans plusieurs familles des plantes,la plupart des alcaloïdes sont solubles dans l'eau et l'alcool et ont un gout amer et certains sont fortement toxiques (Wichtl et Anton, 2009).
Certains alcaloïdes sont utilisés comme moyen de défense contre les infections microbiennes (nicotine, caféine, morphine, lupinine) (Hopkins, 2003).
I.3.3. Terpènes et stéroïdes
Les terpènoïdes sont une vaste famille de composés naturels près de 15000 molécules différentes et de caractère généralement lipophiles, leurs grandes diversités due au nombre de base qui constituent la chaîne principal de formule (C5H8) n selon la variation de nombre n, dont les composés monoterpènes, sesquiterpènes, diterpènes, triterpènes, … (Wichtl et Anton, 2009). Les molécules présentent en forme des huiles essentielles ; parfums et goût des plants, pigments (carotène), hormones (acide abscissique), des stérols (cholestérol) (Hopkins, 2003).
Chez toutes les plantes on trouve ces composés liées avec un groupement alcool, nommés ‘stérols’ ; prenant une forme plane, glycosylée, analogues du cholestérol qui ne diffèrent de celui-ci que par leur chaîne latérale comme : Β-Sitostérol, Stigmastérol (Hopkins, 2003).
CHAPITRE II
GENERALITES
SUR LES
PLANTES ETUDIEES
II. Plantes étudiées
II.1 Carthamus tinctorius
II.1.2 Description botanique du Carthamus tinctorius
Le carthame est une plante médicinale chinoise, ayant des propriétés thérapeutiques purgatives, émollientes et hydratantes.Le carthame est une plante herbacée, annuelle ou bisannuelle, de 30 à 60 cm de hauteur, elle fait partie de la famille des astéracées (Ozanda, 1991).
II.1.2 Classification botanique du Carthamus tinctorius Embranchement : Angiospermes
Sous embranchement : Astéridées Ordre : Astérales
Famille : Asteraceae Sous famille :Carduoideae Genre : Carthamus
Espèce : tinctorius
Figure. 1: Carthamus tinctorius (prise par nous-même) 2019 à Tamentit, Adrar.
Chapitre II. Généralités sur les plantes étudiées
6 Les tiges du Carthamus tinctorius portent des feuilles allongées (figure 2), dentées, d’un vert foncé, et de gros capitules terminaux de fleurs tubulées d’un orange profond, entourés de bractées coriaces, qui s’épanouissent de juillet à septembre.
Noms communs : Carthame, carthame des teinturiers, Safran des teinturiers, safran bâtard, safran des près, safran mexicain, safranon, faux safran, graine de perroquet. Cette plante est connue à Adrar sous un nom local de « Zaafor ».
Floraison du carthames est du printemps à l’été (avril- juillet selon le climat) s’étalent sur une vingtaine de jours. En cime solitaire capitule tubuleux (1,5 à 3cm), fleurons comestibles enserrés dans un involucre de bractée foliacée oblongue a marge épineuse et à nerves fortement marqués.
La couleur de fleur est jaune safranée virant progressivement au jaune orange (figure3).
Les grains sont de couleur clair et anguleux, semblables à de petites graines de tournesol, qui sont consommées traditionnellement en Ethiopie et en Inde. (Messaoudi, 2005)
Figure. 3 : Fleur de Carthamus tinctorius (pris par nous-même) 2019 à
Tamentit, Adrar.
Figure. 4 : Graines de Carthamus tinctorius (pris par nous-même) 2019 à Tamentit, Adrar.
Figure. 2 : Feuilles de Carthamus tinctorius (pris par nous-même) 2019 à
Le carthame est originaire d’Asie occidentale et d’Égypte, il est cultivé aujourd’hui sur tous les continents, en particulier en Maroc, et poussent naturellement sur les terrains non cultivés et sur les endroits caillouteux et pauvres (Laffite, 1999).
II.1.3. Composition chimique
Les fleurs de carthame renferment des substances tinctoriales, dont la carthamone, vitamine C, des protides, des lipides, cellulose, glucides et d’un colorant rouge (Djender, 2003). Les graines contiennent une huile riche en acides gras polyinsaturés, dont l’acide linoléique, l’acide oléique et acide saturé (Burhan, 2007).
II.1.4. Utilisation traditionnelle du Carthame
Le carthame fait partie des plantes médicinales asiatiques, il est utilisé dans la médecine traditionnelle chinoise (Kothe., 2007).
Les fleurs de cette plante étaient préconisées en Chine pour soigner la rougeole et soulager les douleurs abdominales et les douleurs de bas ventre (Kothe., 2007).
Des études chinoises ont démontré la propriété du carthame à réduire le taux de cholestérol et de protection sur les artères coronaires (Lahmadi., 2010).
II.1.5. Utilisation et bienfaits du Carthame
Le Carthamus tinctorius protège les artères coronaires, baisse le taux de cholestérol. Il prévient aussi l'artériosclérose, et les problèmes intestinaux .dans l'industrie cosmétologique, le carthame permet d’élaborer des crèmes dermatologiques, shampooings, démaquillants, rouges à lèvres. Les fleurs de carthame sont utilisées depuis les temps anciens pour teindre les étoffes d’où son appellation de carthame des teinturiers (la rousse, 1981).
Chapitre II. Généralités sur les plantes étudiées
8
II.2. Ammodaucus leucotrichus
II.2.1. Description botanique d’Ammodaucus leucotrichus
D’après Quézel et Santa (1963) ; Guignard et Dupont (2007), la classification de Ammodaucus leucotrichus est la suivante :
Embranchement : Spermaphytes Sous-embranchement : Angiospermes Classe : Eudicots Sousclasse : Astéridées Ordre : Apiales Famille : Apiacées Genre : Ammodaucus Espèce : leucotrichus
Noms vernaculaires à Adrar : Medriga/Guerthofa/ Nessoufa/ Cumin plat.
Nom Français : Cumin velu, cumin du Sahara
Ammodaucus leucotrichus est un arbuste annuel à tige rameuse, ses fleurs blanches sont disposées selon une ombelle composée, elle a des feuilles pennatiséquées, fruits très odorant et ses côtés latéraux sont ailées (Ozenda et al., 1977).
Figure. 5 : Ammodaucus leucotrichus (pris par nous-même) 2019 à Zaouiet Konta Adrar
A mmod aucus leucot richis se trouve génér aleme nt au Sahar a Algéri
enne, Maroc, Niger, Mauritanie, et Libye qui s’étend jusqu’à l’Afrique tropicale et l’Egypt (Bramwell et Bramwell, 2001). Ammodaucus leucotrichus est une plante médicinale largement utilisée dans la région d’Adrar, cette plante a plusieurs vertus antispasmodiques, antiseptiques et carminatives, elle est utilisée également pour traiter la constipation (Ouled el hadj et al., 2003).
II.2.3. Effets thérapeutiques d’Ammodaucus leucotrichus
Ammodaucus leucotrichus est une plante à usage médicinale utilisée chez les populations du Sahara. Ses principales utilisations sont contre : les maux d’estomac, l’indigestion, les diarrhées, les vomissements, les spasmes et coliques, les vers intestinaux et la constipation (Merzoukiet al, 2000 ; Didi et al, 2003 ; Fakchich et Elachouri, 2014).
La plante est aussi utilisée pour le traitement des symptômes d’allergie (Didi et al,2003; Hammiche et Maiza, 2006). Elle est utilisée aussi contre la toux, comme emménagogue et contre l’anorexie (Hammiche et Maiza, 2006). Ammodaucus leucotrichus sont utilisés pour le traitement des palpitations cardiaques (Jouad et al ,2001). Une étude récente faite par Kabbaj et al. (2012) rapporte que quelques populationsindigènes, au Maroc, utilisent les fruits de Ammodaucus leucotrichus pour le traitement du cancer des poumons sous forme de poudre mélangée avec du miel et administrée par voie orale, ainsi une prise d’une infusion quotidienne prévient le diabète (Ouled el hadj et al, 2003).
Figure. 6 : Fleurs d’Ammodaucus leucotrichus (pris par nous-même)
2019 à Zaouiet Konta. Adrar
Figure. 7 : Grains d’Ammodaucus leucotrichus (pris par nous-même)
CHAPITRE III
FUSARIUM
III. Fusarium oxysporum
Fusarium est parmi les champignons qui provoquent les maladies vasculaires les
plus fréquentes el les plus dommageables pour les cultures (Nelson et al, 1981).
III.1. Maladie vasculaire du palmier dattier ‘El Bayoud’
Le Fusarium oxysporum comporte un ensemble de formes morphologiques identiques mais parfois trop étroite, il ya environ 80 formes spécialisées, chacun inféodés à une plantes hôte particulière (Armstrong et Armstrong, 1981), parmi ses formes la forme spéciale albedinisprovocante la fusariose vasculaire du palmier dattier connue localement par « El Bayoud ».
Selons Nelson sa position systématique est : Classe : Deuteromecetes
Ordre :Moniliales
Famille : Tuberculareaceae Genre : Fusarium
Espèce : oxysporum Forme Spéciale : albédinis
Lorsque le palmier dattier est infecté par le Fusarium oxysporum f sp albédinis ; son action parasitaire se montra catastrophiquement. Le Fusarium oxysporum f sp albédinis provoque une perte d’eau et de métabolisme nécessaire pour la survie des cellules végétale ; aussi elles détruits les constituants nécessaire des cellules végétales.La fusariose vasculaire provoque le dessèchement et le flétrissement et le jaunissement des feuilles, à la fin le palmier fane et meure complètement (Agrios,2005).
Figure. 8 : Forme morphologique du Fusarium oxysporum
Chapitre III.
Fusarium oxysporum
11
III.2. Cycle de vie du Fusarium oxysporum
Le parasite de Fusarium oxysporum a un cycle de vie représenté en deux phases : colonisation et parasitisme (Lemanceau et Alabouvette, 1993).
Le Fusarium peut survivre sur le sol sur des débris végétaux même en l’absence de sonhôte, c’est un parasite tellurique qui résiste même en hiver sous la forme de chlamydospores dans les tissus du palmier malades.
Ce champignon est très inégalement répartie dans le sol environ de 0 à 30cm du palmier malade ou mort des fois jusqu’à 1m. Les chlamydospores peuvent résister jusqu’à 8 ans même si les palmiers sont morts (Tantaoui, 1989). Le Fusarium oxysporum démarre son cycle de vie après avoir affecté le système racinaire de l’hôte avant de devenir systémique dans les tissus conducteurs de cette dernière. Les chlamydospores s’adhèrent ; germant et pénétrant les tissus vasculaires des racines, à partir de quel le mycélium atteint la tige et se ramifier dans les cellules épidermiques (Djerbi, 1983) et sa provoque la mort de la plante, qui est du probablement aux effets combinés des armes chimiques déployé par le parasite.
CHAPITREVI
Matériels et méthodes Enquête ethnobotanique
12
I
.
Enquête ethnobotanique
I.1. Présentation de la zone d’étude
I.1.1. Situation géographique de la Wilaya d’Adrar
La wilaya d’Adrar se située dans le sud-ouest Algérien avec des conditions climatiques et édaphiques très sensibles.
La wilaya d’Adrar, est composée de 11 daïras, 28 communes et 299 ksars (villages), recouvre une zone d'environ 427 000 km² et regroupe 432 193 habitants (estimation de 2011).
La wilaya d'Adrar se répartit sur quatre zones géographiques :
le Gourara, la région de Timimoun le Touat, la région d’Adrar
le Tidikelt, la région d’Aoulef
la Tanezrouft, la région de Bordj Badji Mokhtar
Figure 10: position géographique de la zone
I.1.2.DaïradeZaouïetKounta
Zouiet Kounta, est une belle oasis située à 75 km au sud du chef-lieu de la wilaya d’Adrar et à environ à 1400 km au sud-ouest d’Alger.
C’est une région hyper aride connue par sa rareté en eau de surface et des températures très élevées dépassant les 50 °c en période d’été. La commune de Zaouiet Kounta contient 12 oasis, elle est située à la périphérie ouest du plateau de Tademaït.
a) .Démographie de Zaouïet Kounta
Le nombre d'habitants de la commune de Zaouïet Kounta est à 17 116 habitants en 2014, et la densité de population Zaouïet Kounta est 1,9 habitants/km².
(https://planificateur.acontresens.net/afrique/algerie/adrar/reggane/2483761.html 03:00)
b) .Géographie de Zaouïet Kounta
La ville de Zaouïet Kounta ’étale sur une superficie de 914 000 hectares, ses coordonnées géographiques sont :
• Latitude : 27.2167, Longitude : -0.2 .27° 13′ 0″ Nord, 0° 12′ 0″ Ouest
Figure. 11
:position géographiques de Zaouiet Konta
Matériels et méthodes Enquête ethnobotanique
14
I.1.3. Commune de Tamantit
Le territoire de la commune de Tamantit se situe au centre de la wilaya d'Adrar. Son chef-lieu est situé à 13 km au sud d'Adrar.La commune de Tamantit contient les localités suivantes :
Tamantit
Ouled Sidi Ouali OuledElhadjElmamoun Noumemnass
Boufaddi Abenkour
a) Démographie de Tamantit
Le nombre d'habitants de la région de Tamantit est9 481 habitants (an 2008), la densité de population est 1,4 habitant/km².
(https://planificateur.acontresens.net/afrique/algerie/adrar/reggane/2483761.html 03:00)
b. Géographie de Tamentit
Tamantit se situe au sud du chef-lieu de la wilaya d’ADRAR entre 0°,16’de longitude Nord-est et 27° 46’ de latitude, a une altitude de 252m à 282m, et s’étend sur une superficie de 6 937 km2. (https://planificateur.acontresens.net/afrique/algerie/adrar/reggane/2483761.html 03:00) Figure12 : position géographique deTamantit Adrar Tamantit
I.2. Climatologie
Le climat de Sahara est généralement aride et plus sec sous l’influence des facteurs thermiques et des précipitations, en effet l'évaporation s'accroisse avec la température, et parallèlement, inversement proportionnelle aux précipitations.
2.1 Précipitations
Les mécanismes généraux des précipitations dans la région d’Adrar sont liés à deux secteurs de perturbations atmosphériques.
D’une parte le front inter tropical (F.I.T) ou les précipitations orageuses sont engendrées par les dépressions en prévenance des régions du sud surtout à la fin du printemps et même en période estivale.
Le tableau suivant indique les valeurs de la pluviosité moyenne annuelle et mensuelle dans la station de météo d’Adrar, de l’an 2017.
Figure13 : Distribution mensuelles des précipitations 2017 à Adrar (Source : station météo Adrar).
On distingue que les caractéristiques des pluies dans notre région sont très faibles, et irrégulières durant toute l’année.
0 2 4 6 8 10 12 14
jan. fév. mars avril mai juin jui. août sep. oct. nov. déc. mois
Matériels et méthodes Enquête ethnobotanique
16
I.2.2. Température
Le sud d’Algérie est connue par la température élevé surtout durant la saison estivale, elle constitue un des facteurs majeurs caractéristiques du climat saharien, le tableau suivant illustre les variations de la température durant l’an 2017en degrés Celsius à la station Météo d’aérodrome d’Adrar.
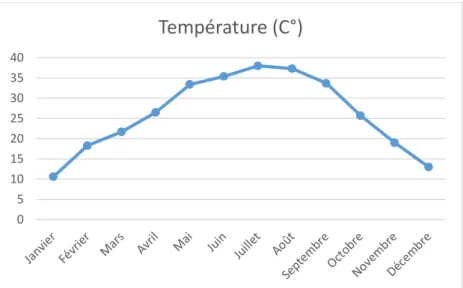
Figure 14 : Température moyennes/mois de l’an 2017 à Adrar (Source : station météo Adrar).
La température dans la région d’Adrar est élevée durant la presque toute l’année, elle attient son excès en mois de juillet.
I.2.3. Vent
La fréquence et l’intensité des vents sont également un des caractères majeurs de la climatologie saharienne. Le Touat, par sa situation au pied du plateau de Tademaït, ouvert sur l’erg chèche et la dépression au Tanezrouft est la région du Sahara Algérien ou les vents sont les plus violents en particulier le long de l’axe Beni Abbas – Adrar, et jusqu’à la dépression de Reggan qui le prolonge. Les régions du sud-Ouest sont connues par des vents assez réguliers.
0 5 10 15 20 25 30 35 40
Température (C°)
Figure. 15: Vitesse du vent (m/s) à Adrar l’an 2017(Source : station météo Adrar) .
D’après le tableau ci- dessus , nous remarquons que la vitesse du vent est supérieure à 05 m/s durant toute l’année et par conséquent notre région est très ventée.
Les caractéristiques du vent de la région est la forte fréquence de siroco, ce vent chaud et sec à un pouvoir de dessèchement élevé.
I.2.4 Humidité
L’appréciation de ce facteur est traduit par le rapporte en pourcentage (%) de la tension de la vapeur à la tension maximale correspondant à la température. Elle exprime en réalité l’état hygrométrique de l’atmosphère qui varie beaucoup au cours de la journée. Elle est maximal au levée du soleil, par contre le taux le plus faible et observé en milieu de la journée. Le tableau ci-dessous indique que l’humidité et très faible à Adrar (selon les données de la station de météo d’Aérodrome d’Adrar).
0 1 2 3 4 5 6 7 8 9 10
Jan Fev Mar Avril Mai Juin Juie Aoùt Sep Oct Nov Dec
Matériels et méthodes Enquête ethnobotanique
18
Figure. 16 : Humidité Relative De L'air l’an 2017 à Adrar (Source : station météo Adrar)
I.3. Enquêtes ethnobotaniques
3.1. Choix des zones d'étude
Dans cette étude, nous avons choisi deux zones de la région d'étude. Cela a été fait sur la base de la présence de toutes les catégories de la population qui utilisent les plantes médicinales. Les deux zones concernées par cette étude sont : la daira de Zaoiute Konta et la commune de Tamentit.
L’enquête ethnobotanique a été faite la période de mois de mars et avril 2019. Le questionnaire vise à recueillir des informations sur le citoyen et sur les plantes étudiées.
Les points de relevées, ont concerné les villages, et les ksours de façon aléatoires et simple, des échantillons de nombre restreint de 100 personnes pour chaque plante, qui constitue un ensemble d’échantillon global N (N=100×2).
Le dialogue s’est fait en langue locale (arabe) pour la majorité des fiches d’enquête.
Les informations recueillies ont concerné le profil de la personne interrogée (âge, sexe, niveau d’étude, situation familiale) et les données ethno pharmacologiques telles que le nom local commun de la plante, les usages, les parties utilisées, le mode de préparation, les voies d’administration.
0 5 10 15 20 25 30 35 40 45
Jan Fev Mar Avril Mai Juin Juie Aoùt Sep Oct Nov Dec
Nous avons utilisé l’Excel pour traiter nos donner et faire nos représentations graphiques.
Ce travail a été réalisé au niveau de laboratoires pédagogiques de science de nature et de vie et le laboratoire de chimie de l’université d’Ahmed DRAÏA d’Adrar.
L’objectif de cette partie est d'identifier l’effet thérapeutique de plantes étudiées ainsi que le pouvoir et l’activité fongique sur le champignon Fusarium oxysporum f. sp albedinus.
Matériel et méthodes Evaluation de l’activité antifongique
20
II. Evaluation de l’activité fongique
1. Matériel végétal
Les grains d’Ammodaucus leucotrichus ont été récoltés par un agriculteur à la région de zaouiet konta.
La cueillette des fleurs de Carthamus tinctorius a été faite dans un jardin à Tamentit
Le séchage des fleurs et des grains a été fait juste après la récolte et le nettoyage des déchets à une température ambiante et à l’abri de la lumière.1 mois après. Les grains
Figure .17 : Plante Ammodaucus leucotrichus (photo prise par nous même)
Figure .18 : Grains d’Ammodaucus leucotrichus (photo prise par nous même)
Figure .19 : Plante Carthamus tinctorius (photo prise par nous
même)
Figure .20 : Fleur de Carthamus tinctorius (photo prise par nous
et les fleurs ont été broyées à l’aide d’un moulin à café de marque sonny, après stockées à température ambiante et à l’abri de soleil.
2. Taux d’humidité
Détermination du taux d’humidité (Audigié et al., 1980)
a. Principe
La détermination de la teneur en eau est effectuée par une dessiccation de l’échantillon dans une étuve isotherme de 103 à 105°C jusqu’à une masse pratiquement constante. Pour éviter toute reprise d’humidité, il convient d’opérer dans des vases de tare, placées dans un dessiccateur.
b. Mode opératoire
Les creusets ont été séchés à l’étuve pendant 30 min à 103°C avec couvercles inclinés.
Après refroidissement dans un dessiccateur durant 20 à 30 min, les creusets ont été pesés avec les couvercles (P1).
Dans chaque creuset, 3 g de l’échantillon moulu ont été introduit, l’ensemble a été pesé avec les couvercles fermés (P2).
Après un étuvage de 3 h à 105°C avec couvercles inclinés puis refroidissement dans un dessiccateur pendant 15 min, les creusets sont pesés, ensuite ils sont remis à couvercles inclinés dans l’étuve durant 1 h à 105°C.
Après refroidissement comme précédemment, les creusets sont pesés (P3).
Matériel et méthodes Evaluation de l’activité antifongique
22 La différence entre deux pesées doit être inférieure à 2 mg, si non l’opération est
renouvelée jusqu’à poids constant.
3. Evaluation du pouvoir antimicrobien des extraits
hydro-alcooliques
3.1. Préparation de l’extrait brut
L’extrait brut de chaque échantillon est obtenu selon la méthode décrite par Abdallah(2017) avec des légères modifications comme suit ;
Les parties des deux plantes étudiées séchées et broyées est soumise à une macération sous agitation magnétique à température ambiante avec un mélange MeOH/H2O2 ; 80/20 pendant 2 h ensuite, le mélange a été filtré.
Figure. 23 : Macération sur
agitateur magnétique (prise par nos même).
Figure. 24: Filtration du mélange
sur centrifugeuse (prise par nos même).
Figure .22 : Séchage de la matière
végétale dans l’étuve (photo prise par nos même)
Figure. 21 : Pesé des échantillons
sur balance (photo prise par nos même).
Le filtrat a été récupéré et l'échantillon a été ré-extrait avec le même solvant hydro-alcoolique (MeOH/H2O2 ; 80/20) pendant 2 h sous agitation magnétique ; Après une 2ème
filtration les deux filtrats sont réunis;
L'extrait filtré a été dégraissé en le décantant à volume égale, avec l'hexane (Chiremba et al., 2012) dans une ampoule à décanter.
L'extrait a été évaporé à sec dans un évaporateur rotatif à 45°C sous pression réduite;
Enfin, une solution mère de 50 mg/mL est préparée en dissolvant l’extrait sec dans le DMSO.
Figure. 25 : Dégraissage du Carthamus tinctorius
Figure. 26 : Dégraissage de
l’Ammodaucus leucotrichus
Figure. 27 : Evaporation sur
évaporateur rotatif.
Figure .28 : Récupération de
Matériel et méthodes Evaluation de l’activité antifongique
24 3.2 Préparation des milieux de culture
Un extrait de pomme de terre est préparé comme suit : 200 g de pomme de terre sont lavés et épluchés puis, découpés en petits morceaux et portés à l’ébullition pendant 1 h dans 1000 mL d’eau distillée. Le filtrat est récupéré et est complété à 1000 mL avec de l’eau distillée.
3.3. Préparation de l’inoculum
La souche de champignon utilisée est Fusarium oxysporum f.sp albedinis A. Isolement et purification
La souche fongique utilisée provient de la station de l’INRAA d’Adrar. Elle nous a été fournie par Mr Boudeffeur. Elle a été isolée, identifiée et purifiée par le personnel technique de la station. Elle a été isolée à partir des rachis de palmes présentant les symptômes de Bayoud.
B. Préparation des pré-cultures de souches fongiques
A partir des cultures mères des souches fongiques filamenteuses conservées, une petite quantité est prélevée, dans des conditions aseptiques, puis ensemencée sur un milieu PDA préalablement coulé en une boîte de Pétrie. La boîte est incubée à 25°C pendant 7 jours.
Figure .29 : Ébullition pendant 1h Figure. 30 : Filtration de la
3.4. Test antifongique (Berche et al., 1991) A. Préparation de la suspension sporale
A partir d’une culture de 7 jours du Fusarium oxysporum f.sp, nous avons préparé une suspension sporale d’une concentration de 104
spores /mL comme suit : Une quantité de spores a été prélevée avec une anse de platine stérile et
dissoute dans un microtube contenant environ 1.5 mL PDB.
La numération des cellules est faite par comptage manuel au microscope en utilisant la cellule de Malassez. Pour ce faire un volume de 20 µL de l’échantillon à compter est déposé au niveau du quadrillage, et par capillarité l’échantillon est étalé entre la lame et la lamelle;
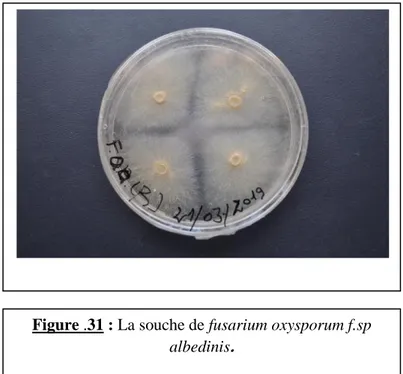
Figure .31 : La souche de fusarium oxysporum f.sp albedinis.
Matériel et méthodes Evaluation de l’activité antifongique
26 Une fois la lame chargée, elle est observée sous le microscope photonique.
Après la mise au point, on compte le nombre d’événements sur au moins 4 carrés du quadrillage. Le but est de compter environ 100 cellules selon la méthode illustrée dans la figure ci-dessous ;
Figure . 33 : Méthode de comptage des cellules fongiques sur la cellule de Malassez Après le comptage, il a suffi d’extrapoler pour déduire la concentration totale
de l’échantillon/suspension cellulaire selon la formule suivante :
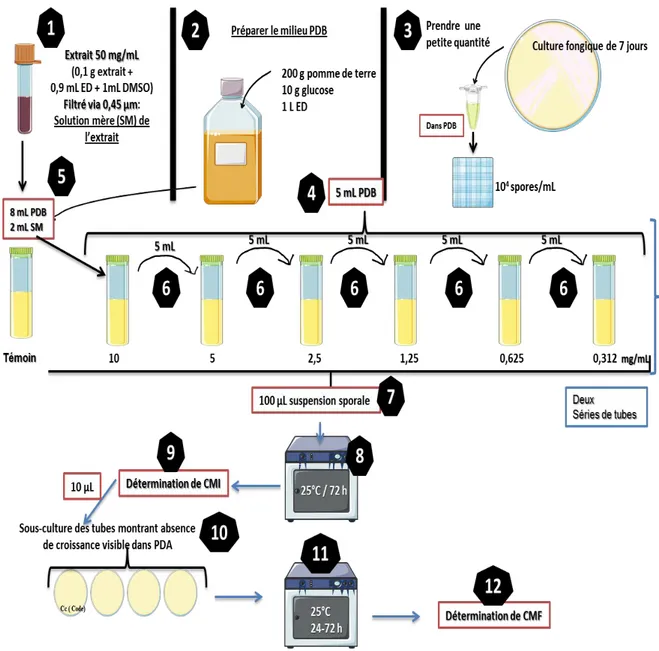
B. Préparation des dilutions de l’extrait dans un milieu liquide
Pour chaque extrait, nous avons préparé 06 concentrations dont le premier tube contenait 2 mL de la SM (50 mg/mL) et 8 mL PDB : c’est la concentration 10 mg/mL finale ;
Après homogénéisation, nous avons transféré 5 mL du contenu du premier tube à un deuxième tube contenant au préalable 5 mL PDB : c’est la concentration 5 mg/mL ;
Les concentrations 2.5, 1.25, 0.625, et 0.312 mg/mL sont préparés ensuite par la même méthode de dilution décrite ci-haut;
Un tube témoin contenant 8mL PDB + 2 mL de DMSO à 50 % a été préparé. Concentration (cellules /ml) = moyenne des cellules de 4 carrés x 100 000
Matériel et méthodes Evaluation de l’activité antifongique
28
C. Inoculation de la suspension sporale et incubation
Tous les tubes sont inoculés avec 100 µL de suspension sporale (104
spores /mL) Les tubes ont été ensuite incubés à 25 °C pendant 72 h.
D. Détermination de la CMI
CMI est définie comme étant la plus faible concentration de l’extrait qui ne montre aucune croissance fongique visible après la période d’incubation dans le milieu liquide (PDB).
E. Ensemencement sur milieu solide
Après incubation, 50 µL du contenu des tubes qui n’ont montré aucune croissance fongique visible sont repiqués sur un milieu PDA, coulé en boites de Pétrie, puis
incubés pendant 72h à 25 °C.
figure.35 : Ensemencement sur
milieu liquide
Figure. 36 : Ensemencement sur
milieu solide
C. Détermination de la CMF
La concentration minimale de fongicide (CMF) correspond à la concentration minimale, après repiquage sur milieu solide (PDA), induisant une absence de croissance fongique visible.
CHAPITREV
Résultats Enquête ethnobotanique
29
I. Enquête ethnobotanique
I.1. Classes d’âge
A Adrar l’utilisation des plantes médicinales concerne toutes les tranches d’âge. Les personnes âgées de +31 ans et [0-10] ont une fréquence d’utilisation des plantes médicinales de (34%) et (28,5 %). Les tranches d’âge [11-20], [21-30] viennent ensuite avec un pourcentage de (15%) et (22.5%) (figure37).
Figure. 37 :Pourcentage d’utilisation des plantes médicinales par classe d’âge I.2. Niveau d’étude
Concernant le niveau académique des personnes utilisateurs des plantes médicinales, les résultats obtenus montrent que (54%) sont analphabètes, alors que (20%) ont un niveau primaire et (18%) ont un niveau secondaire. Les universitaires par contre utilisent très peu les plantes médicinales (8 %). (figure38).
Figure. 38: Pourcentage d’utilisation des plantes médicinales selon le niveau d’étude. 0 -10 20-11 30-21 +31 28,5% 15% 22,5% 34% 0 -10 11 -20 Niveau académique
Néat primaire secondaire universitaire
54% 20% 18% 8% Néat primaire secondaire universitaire
I. 3. Situation familiale
Les plantes médicinales sont beaucoup plus utilisées par les personnes mariées (53 %) que par les célibataires (47 %) (figure 39).
Figure. 39 : Pourcentage d’utilisation des plantes médicinales selon le la situation familiale.
I.4. Habitat
La population étudiée est localisée dans les ksours avec un pourcentage très élève (66 %) par contre les personnes habitants le village présente une fréquence d’utilisation des plantes médicinales peu élevé (34 %) (figure40).
Figure. 40 : Pourcentage d’utilisation de plantes médicinales par habitat.
mariee celebataire
53 %
47% mariee
celebataire
Localité Kser Village
66%
34% Kser
Résultats Enquête ethnobotanique
31
I.5. Sexe
Les plantes médicinales sont beaucoup plus utilisées par les femmes (63.5%) que par les hommes (36.5%) (figure 41).
Figure . 41: Pourcentage d’utilisation des plantes médicinales par sexe.
I.6. Type de plante
Les plantes médicinales utilisées sont souvent cultivés dans la région à un pourcentage (96,5%) (figure 42).
Figure . 42 : Pourcentage des différents types de plantes cultivées.
sauvage cultivé Adventive 3,5% 96,5% 0% sauvage cultivé Adventive 36,5% 63,5% Masculin féminin
I.7. Partie utilisée
a) Le carthamus tinctorius
Les fleurs constituent la partie la plus utilisée chez toutes les personnes interrogées avec un pourcentage de (100%) (figure 43).
Figure . 43 : Pourcentage des parties utilisées de Carthamus tinctorius
b) Ammodaucus leucotrichus
Les graines constituent la partie la plus utilisée chez toutes les personnes interrogées avec un pourcentage de (100%) (figure 44).
Figure . 44 : Pourcentage des parties utilisées de l’Ammodaucus leucotrichus.
Tige fruit Graine ecorce Racine feuille Plante
entière fleurs 0% 0% 0% 0% 0% 0% 0% 100% 0% 0% 100% 0% 0% 0% 0%
Résultats Enquête ethnobotanique
33
I.8. Modes de préparations
a) Carthamus tinctorius : la poudre est le mode le plus pratiqué avec un pourcentage de (97%) et (3%) l’utilise en mode infusion (figure 45).
Figure .45 : Modes de préparations du Carthamus tinctorius .
b). Ammodaucus leucotrichus
la poudre est le mode le plus pratiqué avec un pourcentage de 69 %, suivi des graines crues à 28%, et enfin l’infusion avec un pourcentage de (3%). (Figure 46) .
Figure . 46: Modes de préparations de l Ammodaucus leucotrichus
3% 0% 0% 0% 97% 0% 0% 3% 0% 28% 0% 69% 0% 0%
I.9. Doses utilisées
a). Carthamus tinctorius
Les doses utilisées sont la pincée qui présente un taux d’utilisation de (57%) et la cuillère à 43% (figure 47).
Figure. 47 Doses utilisées du Carthamus tinctorius :
b). Doses utilisées de l’Ammodaucus leucotrichus
Les doses les plus utilisées sont la cuillère à un pourcentage de 67%, suivi de la pincée qui présente un taux de 28% et enfin la poigné à 5%. (Figure n°48).
Figure . 48 : Doses utilisées de l’Ammodaucus leucotrichus.
Dose Utilisé
Pincée Poignée Cuillère Verre 57%
0%
43%
0%
Pincée Poignée Cuillère Verre
28%
5%
67%
Résultats Enquête ethnobotanique
35
I.10.
Maladies traitéesLe Carthamus tinctorius traite les affections des troubles respiratoires à un taux de 27,51%, l’anémie à 27,51%, les maladies digestives à 24,83 % et les affections dermatologiques à 19,46%.
Tans dit que l’Ammodaucus leucotrichus est indiquée dans le traitement des affections suivantes : troubles digestifs avec un pourcentage de 48,17%, suivi du diabète à 39,2 %, et à la fin l’hypertension artérielle ayant le pourcentage de 18,29 %.
Figure . 49 :Maladie traitées par Carthamus tinctorius et l’Ammodaucus leucotrichus.
I.11. Mode d’administration
a). Mode d’administration Carthamus tinctorius
Le seul mode d’administration utilisé pour le Carthamus tinctorius c’est par voie orale à 100%. 0 5 10 15 20 25 30 35 40 45 50 48.17 18.29 39.02 19.46 27.51 24.83 27.51 % Ammodaucus leucotrichus Carthamus tinctorius
Figure. 50: Mode d’administration du Carthamus tinctorius.
b). Mode d’administration Ammodaucus leucotrichus
Le mode d’administration fréquenté pour l’Ammodaucus leucotrichus c’est par voie orale à 70%, suivi par succion à30%.
Figure. 51: Mode d’administration du« Ammodaucus leucotrichus».
I.12. Résultat d’utilisation
a). Résultat d’utilisation de Carthamus tinctorius
Le Carthamus tinctorius d’après les personnes interrogées donne un état de guérison à 50% et aussi d’amélioration de l’état de santé à un pourcentage de 50% pour tous les personnes interrogés, sans aucun effet secondaire ni toxicité ni inefficacité.
100%
0% 0% 0%
oral inhalation badigeonnage cucé
70%
0% 0%
Résultats Enquête ethnobotanique
37
Figure. 52 : Résultats d’utilisation du Carthamus tinctorius.
b). Résultat d’utilisation d’Ammodaucus leucotrichus
Ammodaucus leucotrichus montre un état de guérison à 71% et d’amélioration à un pourcentage de 39% et de 22% d’effet secondaire pour toutes les personnes interrogées.
Figure. 53 : Résultat d’utilisation de l’Ammodaucus leucotrichus.
71%
39%
22%
II. Evaluation de l’activité fongique II.1. Taux d’humidité
Apres l’expérience et les calcules on a constaté que le taux d’humidité d’Ammodaucus leucotrichus (6,97%) est plus élevé par apport au Carthamus tinctorius
(4,70%).les valeurs d’humidité nous ont permis de calculer les pourcentage de la
matière sèche (M.S) pour les deuxcultivars ; (95.30%) pour l’extrait du Carthamus tinctorius et (93.04%) l’extrait d’Ammodaucus leucotrichus.
II2. Rendements d’extractions
On a pris les pesés des pois de chaque échantillon après avoir passé l’extrait méthanolique de chaque plante sur évaporateur rotatif et on a fait les calcules selon la formules ci-dessous :
Rendement =
P1-P0/M*100On aconstaté que le rendement massique du Carthamus tinctorius (1.72%) est plus élevé que celui d l’Ammodaucus leucotrichus (1.66%)
Figure. 54: Rendement massique du Carthamus tinctorius et Ammodaucus leucotrichus. 1.62 1.64 1.66 1.68 1.7 1.72 1.74 1.76
Carthamus tinctorius Ammodaucus
leucotrichus Re n d em en t d 'e xt ra ctio n (% )
Résultats Evaluation de l’activité fongique
39
II.2. Résultats du pouvoir fongique
A. Détermination de la CMI
Après 72h de l’incubation des cellules fongiques traitées avec différentes concentrations de l’extrait brut du Carthamus tinctorius et celui de l’Ammodaucus leucotrichus nous avons pu déterminer la CMI de chaque extrait (figure 55).
Figure. 55 : Détermination de la CMI de l’extrait duCarthamus tinctorius (A) et l’extrait de l’Ammodaucus leucotrichus (B).
Il parait que l’extrait du Carthamustinctorius, avec une CMI de 2,5 mg/mL, possède un pouvoir inhibiteur plus intéressant que l’extrait de l’Ammodaucus leucotrichusqui a montré une CMI de 5 mg/mL(Tableaun°6).
Tableau N°1 : Résultats de l’évaluation de la CMI des extraits testés
Concentrations (mg/mL)
10
5
2,5
1,25
0,625 0,312
Effet antiprolifératif Carthamus tinctorius+
+
+
-
-
-
Ammodaucus leucotrichus+
+
-
-
-
-
B AB. Détermination de la CMF
Un petit volume des tubes qui n’ont pas montré de prolifération fongique (10 mg/mL et 5mg/mL des deux extraits en plus de la concentration 2,5 mg/mL du Carthamus tinctorius a été ensemencé sur un milieu solide (PDA) puis incubé pendant 72 h.
Contrairement aux résultats de la CMI, l’extrait de l’Ammodaucus leucotrichus a montré un pouvoir inhibiteur fort à celui de l’extrait du Carthamus tinctorius dont la concentration 10 mg/mL a correspondu à la CMF de l’extrait de l’Ammodaucus leucotrichus(figure 56 + figure 57).
Figure .56 : Résultats du CMF l’extrait de l’Ammodaucus leucotrichus.
Quoique nous avons observé une légère croissance fongique à la concentration de 10 mg/mL du Carthamus tinctorius, cette croissance a été plus importante à la concentration 5 mg/mL du même extrait (figure 60).
Figure. 57 : Résultats du CMF, l’extrait de Carthamus tinctorius. D’après les résultats de la CMI et de la CMF, nous avons calculé le rapport CMF/CMI. Si ce rapport est supérieur à 4, l’extrait est qualifié fongistatique, mais s’il est inférieur à 4, l’extrait est qualifié alors fongicide (Marmonier, 1990).
Témoin
C. tinctorius 10 mg/mL
Témoin C. tinctorius5mg/mL A.leucotrichus 5 mg/mL A. leucotrichus 10 mg/mL
Résultats Evaluation de l’activité fongique
41
Il résulte, à partir des rapports CMF/CMI que l’extrait de l’Ammodaucus leucotrichus exerce des effets inhibiteurs de type fongicide avec un rapport CMF/CMI estimé à 2. Par contre, il parait que extrait du Carthamus tinctorius exerce des effets inhibiteurs de type fongistatique parce que la CMF est supérieur à 10 mg/mL contre une CMI de 2,5 mg/mL.
3. Discussion
Notre étude s’est portée d’une part sur une enquête ethnobotanique de deux plantes cultivées dans la région d’Adrar, et d’autre part sur l’évaluation de leurs pouvoirs antimicrobiens. Nos résultats de l’enquête ethnobotanique ont montré que les graines d’Ammodaucus leucotrichus constituent la partie la plus utilisée de cette plante. La poudre de ces graines est consommée pour soigner certaines affections qui touchent le tube digestif. Il en est de même pour les fleurs du Carthamus tinctorius qui sont prises pour remédier certaines pathologies telles que les affections de tubes digestifs et dermatologiques. Il a été rapporté que le genre Fusarium est à l’origine de plusieurs affection dermatologiques qui peuvent être mortelles chez les personnes immunodéprimées (van Diepeningen et al., 2015 ; Rayet al., 2016). De plus de la résistance du genre Fusarium aux traitements antifongiques conventionnels tel que les azolés et les triazolés, de nombreux antifongiques de synthèse deviennent toxiques suite à une utilisation prolongée (Campoy&Adrio, 2017). Dans notre étude, l’évaluation du pouvoir antifongique a montré que l’extrait d’Ammodaucus leucotrichus a exercé des effets inhibiteurs de type fongicide contre le Fusarium oxysporum, tandis que l’extrait du Carthamus tinctorius a exercé des effets inhibiteurs de type fongistatique. Nos résultats sont en accord avec ceux trouvé par Delshad et al. (2018) qui ont rapporté une activité antimicrobienne de l’extrait méthanolique des fleurs du Carthamus tinctorius contre Cryptococcus neoformans. L’extrait méthanolique d’Ammodaucus leucotrichus a été rapporté aussi d’avoir des effets antibactériens et antifongiques contre une large gamme des bactéries et des champignons (Sebaa et al., 2018) ce qui confirme les effets fongicides observés du d’Ammodaucus leucotrichus.
Les effets antifongiques des extraits étudiés pourraient être attribués à leurs métabolites secondaires. Une étude phytochimique de l’Ammodaucus leucotrichus a montré que cette dernière contient les flavonoïdes, les tannins, les saponosides, les coumarines, les acides phénoliques, les alcaloïdes, et les glycosides (Asdjal et al., 2018). Une autre étude a montré que le Carthamus tinctorius contient les stéroïdes, les glycosides, les saponosides, et les tanins (Turgumbayeva et al., 2014). Il a été démontré que les polyphénols, les alcaloïdes, et les terpenoides ont des effets antimicrobiens (Iwasa et al., 2001; Cushnie& Lamb, 2005; Gul& Hamann, 2005; Ríos&Recio, 2005; Khan et al., 2005; Orhan et al., 2007 ; Tongnuanchan et Benjakul, 2014). L’activité
43 | P a g e antimicrobienne des huiles essentielles, terpenoides, les rend aptes d’être utilisées comme additifs alimentaires (Tongnuanchan et Benjakul, 2014). En fin, l’utilisation des polyphénols et les terpenoides comme adjuvants aux traitements antifongiques a été proposée (Zacchino et al., 2017).
Conclusion
44
Conclusion
La première approche de cette étude s’est portée sur l’élaboration d’une enquête ethnobotanique de deux plantes (l’Ammodaucus leucotrichus et Carthamus tinctorius) utilisées dans la région d’Adrar pour guérir ou moduler plusieurs affections. La deuxième approche s’est portée sur l’évaluation du pouvoir antifongique des plantes ainsi étudiées. L’enquête ethnobotanique a révélé que l’Ammodaucus leucotrichus est très souvent utilisée pour apaiser les troubles digestifs. Tandis que le Carthamus tinctorius est utilisé comme traitement des troubles digestifs et des affections dermatologique.
Les résultats de l’évaluation de l’activité antifongique ont montré que l’Ammodaucus leucotrichus exerce une activité fongicide et le Carthamus tinctorius exerce une activité fongistatique contre le Fusarium oxysporumf.sp albedinus. Ces résultats sont promettant en termes de l’utilisation des métabolites secondaires du Carthamus tinctorius et d’Ammodaucus leucotrichus comme adjuvants aux traitements antifongiques.
En perspective, il serait intéressant d’étudier la composition phytochimique des plantes étudiées ainsi, de tester leurs pouvoirs antimicrobiens sur d’autres souches microbiennes.
Les effets secondaires indésirables associés à l’utilisation des médicaments de synthèse chimique font penser à la recherche des alternatives en explorant les substances bioactives qui peuvent exister dans la nature, avec moins de toxicité sur la santé humaine.