Métrologie des actinides basée sur l’analyse des
matières fécales pour des applications dosimétriques
Mémoire
Alexandre Gagné
Maîtrise en chimie
Maître ès sciences (M. Sc.)
Québec, Canada
© Alexandre Gagné, 2014
iii
Résumé
Les techniques dosimétriques externes, telles que les dosimètres portatifs et compteurs Geiger-Müller, sont largement utilisées dans la détection et l’interprétation de dose reçue par les employés du secteur nucléaire. Toutefois, ces techniques ne permettent pas de caractériser une contamination interne, telle que celle causée par des émetteurs alpha. Actuellement au Canada, les techniques de dosimétrie biologique sont orientées sur l’analyse d’urine, de frottis nasaux et, dans de rares cas, de sang, de tissus et exceptionnellement de matières fécales. Les matières fécales, quant à elles, procurent une voie différente et complémentaire aux autres types de prélèvement, en raison de l’interaction entre le système respiratoire et le système digestif. Il n’existe aucune procédure officielle au Canada sur ce genre d’échantillon. Une nouvelle méthodologie, basée sur la fusion boratée couplée à une méthode d’extraction, a été développée dans le cours de ce mémoire, ce qui devrait permettre de résoudre ce problème.
v
Abstract
External dosimetric techniques, such as portable dosimeter and Geiger-Müller counter, are largely use in the detection and interpretation of received dose by employees of the nuclear sector. However, those techniques are inefficient for characterising internal contamination, such as alpha emitters. As for the moment, the techniques used in Canada for bioassay are oriented towards urine, nasal swabs sampling and on rare occasion; blood and tissue, exceptionally fecal samples. The fecal samples offer a different and complementary approach to other bioassays due to the interaction between the respiratory tract and the gastrointestinal tract. However, there is no official methodology for fecal analysis in Canada. For this thesis, a new methodology based on borated fusion coupled to column chromatography was developed to remedy this problem.
vii
Table des matières
Résumé ... iii
Abstract ... v
Liste des tableaux ... ix
Liste des Figures ... xi
Liste des abréviations et des sigles ... xiii
Remerciements ... xv
Chapitre 1 : Introduction ... 1
Chapitre 2 : Notions de base sur la radioactivité et radiotoxicité ... 5
La radioactivité ... 5
Les types de radiations ionisantes ... 7
Les émetteurs alpha dans le cycle nucléaire ... 9
Notions de dosimétrie ... 14
Dose et facteur de pondération ... 14
Limites d’exposition légales ... 16
Voies d’absorption des radionucléides ... 16
Distribution des actinides dans les organes ... 20
Modélisation de la dose ... 22
Effets de la radiation ionisante sur les tissus humains ... 24
Chapitre 3 : Notions de chimie radioanalytique ... 29
Composition des matières fécales ... 29
Mise en solution des cendres ... 30
Techniques de dissolution ... 30
La dissolution acide ... 30
La digestion par fusion ... 31
Techniques de séparation des actinides ... 35
Techniques de séparation ... 35
La coprécipitation ... 36
L’extraction liquide-liquide ... 36
La chromatographie d’échange ionique ... 37
La chromatographie d’extraction ... 38
viii
Techniques d’analyse des actinides d’intérêt ... 40
La spectrométrie alpha ... 40
La spectrométrie gamma ... 41
La spectrométrie de masse ... 42
Chapitre 4 : Résultats et méthode optimisée ... 45
Réactifs et instruments utilisés ... 45
Instrumentation ... 46
Préparation d’échantillons synthétiques ... 46
Calcination des échantillons synthétiques ... 48
Optimisation de la fusion ... 49
Optimisation de l’élimination de la silice ... 53
Coprécipitation des actinides par HTiO ... 56
Séparation des actinides ... 57
L’efficacité de la résine AG®MP-1M... 58
L’efficacité de la résine UTEVA® ... 60
L’efficacité de la résine DGA-N® ... 62
L’analyse des fractions ... 64
Conclusions ... 65
Chapitre 5 : Performance analytique de la méthode ... 66
Limite de détection ... 66
LDM par spectrométrie alpha ... 67
LDM par ICP-MS ... 69
Calcul de la LDM en dose ... 71
Biais relatif, précision et rendement ... 72
Calcul du biais relatif, de la précision relative et du rendement ... 73
Résultats pour le biais relatif, la précision relative et le rendement de la méthode ... 75
Conclusions ... 78
Chapitre 6 : Conclusion ... 79
Perspectives ... 80
Références ... 81
ix
Liste des tableaux
Tableau 1 : Concentration des actinides dans le combustible usé d’un réacteur CANDU, 10 ans après la fin de son irradiation dans le réacteur (puissance de 190 MWh par kg
d’uranium) ... 12
Tableau 2 : Caractéristiques nucléaires de quelques actinides d’intérêt ... 13
Tableau 3 : Facteurs de pondération des types de rayonnements ... 15
Tableau 4 : Facteur de pondération des tissus ... 16
Tableau 5 : Paramètres par défaut pour des matériaux de type F, M et S [21] ... 18
Tableau 6 : Valeur f1 pour les actinides [22] ... 19
Tableau 7 : Biodistribution des actinides [23] ... 20
Tableau 8 : Temps de demi-vie effectif des actinides pour le squelette [24] ... 21
Tableau 9 : Activité de certains isotopes d’Am, Cm, Pu et Np dans les matières fécales pour une dose de 1mSv suivant l’inhalation calculée par le logiciel GenmodPC ... 24
Tableau 10 : Symptômes probables suite à une exposition corporelle de radiation gamma [28] ... 25
Tableau 11 : Type de fondants commun par rapport à leur creuset ... 33
Tableau 12 : Teneurs en Th et en U (mg/kg) par analyse par ICP-MS de LiBO2 selon leur grade [41, 42] ... 35
Tableau 13 : Composition des matières fécales synthétiques ... 47
Tableau 14 : Récupération de l’uranium dans différentes matrices dissoutes par fusion automatisé à l’aide du Fluxer M4 ... 50
Tableau 15 : Temps nécessaire de dissolution de pastilles de cendres artificielles fusionnées par différents acides ... 52
Tableau 16 : Élimination de la silice par plusieurs PEG soumis aux mêmes conditions ... 55
Tableau 17 : Rendements (%) de récupération de 233U et de 242Pu suite à une floculation avec du PEG-6000 dans HCl 3M ... 55
Tableau 18 : Rendements (%) de récupération de 233U et de 242Pu suite à une coprécipitation par HTiO d’une solution HCl 3M ... 56
Tableau 19 : Rendements (%) des conditions d’élution pour une solution mixte contenant 0,43 Bq de 230Th et 0,28 Bq de 243Am ... 63
Tableau 20 : Valeurs de la LDM par spectrométrie alpha pour l’Am et le Cm ... 69
Tableau 21 : Valeurs de MDA par spectrométrie alpha du Pu ... 69
Tableau 22 : Valeurs de LDM par ICP-MS du Pu et du Np ... 71
Tableau 23 : Équivalent de dose pour chaque limite de détection de la méthode selon le type de particule inhalée ... 72
Tableau 24 : Activités mesurées des échantillons dopés par spectrométrie alpha de l’Am et du Cm ... 76
Tableau 25 : Activités mesurées des échantillons dopés par spectrométrie alpha du Np et du Pu ... 76
Tableau 26 : Activités mesurées d’échantillons dopés par ICP-MS du Np et du Pu ... 77 Tableau 27 : Activités mesurées d’échantillons dopés par ICP-MS du Np et du Pu (suite) 77
xi
Liste des Figures
Figure 1 : Tuyau d’alimentation dans la voute du réacteur de Bruce Power ... 2
Figure 2 : Système aspirateur utilisé pour les travaux de meulage de Bruce Power en 2009 2 Figure 3 : Diagramme de stabilité nucléaire ... 6
Figure 4 : Représentation schématique du temps de demi-vie ... 7
Figure 5 : Corrélation entre l’énergie de la particule alpha lors du réarrangement nucléaire de 340 émetteurs ayant un Z > 73 et le temps de demi-vie [17] ... 9
Figure 6 : Voies simplifiées de production des actinides dans un combustible irradié à 33 GWj t–1 selon les processus nucléaires indiqués [19] ... 11
Figure 7 : Sommaire des diverses voies d’exposition, de transferts et d’excrétion du corps humain [25] ... 23
Figure 8 : Effets directs et indirects de la radiation ionisante sur l’ADN ... 27
Figure 9 : Mécanisme d’élimination de la silice par l’acide fluorhydrique ... 31
Figure 10 : Le Fluxer M4 de Corporation scientifique Claisse ... 34
Figure 11 : Mécanisme d’extraction de l’extraction liquide-liquide pour les ions métalliques (VI) et (IV)+ à l’aide de TBP ... 37
Figure 12 : Mécanisme d’échange ionique sur une résine échangeuse d’ions (forme anionique) ... 38
Figure 13 : Mécanisme de formation de l’aqua regia ... 52
Figure 14 : Représentation statistique de l’hydroxyde de titane hydraté ... 57
Figure 15 : Schéma de séparation des actinides développer par Dai et coll. [55] ... 58
Figure 16 : Valeurs de k’ de différents actinides selon la molarité de HNO3 sur la résine AG®MP-1M ... 59
Figure 17 : Valeurs de k’ de différents actinides selon la molarité de HNO3 sur la résine UTEVA® ... 61
Figure 18 : Valeurs de k’ de différents actinides selon la molarité de HNO3 sur la résine DGA-N®... 62
xiii
Liste des abréviations et des sigles
AMAD Aerodynamic Median Activity Diameter
AMS Accelerated Mass Spectrometry
CANDU® Réacteur CANadian Deuterium Uranium
CCSN Commission Canadienne de Sûreté Nucléaire
CED Committed Effective Dose
CIPR Commission Internationale de Protection Radiologique
COG CANDU Owners Group Inc.
CRL Chalk River Laboratories / Laboratoires de Chalk River
ÉACL Énergie Atomique du Canada Limitée
HTiO Hydrous Titanium Oxide / Oxide de titane hydraté
ICP-MS Inductively Coupled Plasma Mass Spectrometry
LDM Limite de Détection de la Méthode
MDA Minimum Detectable Activity
NRU National Research Universal reactor
NRX National Research Experimental reactor
PEG PolyÉthylène Glycol
PUREX Plutonium URanium EXtraction
xv
Remerciements
L’ensemble des travaux réalisés au cours de cette maîtrise a été effectué à l’Université Laval et aux Laboratoires nucléaires de Chalk River de 2010 à 2013. Un tel travail mérite des remerciements aux collaborateurs de cette recherche.
Je désire remercier tout d’abord mon directeur de recherche, M. Dominic Larivière, pour son aide tout au long de ce projet. Je tiens également à remercier sincèrement les collaborateurs des Laboratoires nucléaires de Chalk River, en particulier M. Xiongxin Dai, M. Nicholas Priest, Mme Sheila Kramer-Tremblay et M. Joel Surette. Merci à tous les collègues de travail pour ces incroyables années passées en votre compagnie. Merci à l’aide précieuse de M. Serge Groleau et de Mme Hélène Guay pour leur support technique. Merci également au support moral de M. Mario Boucher et à son équipe du comité de gestion des produits chimiques de l’Université Laval. Finalement, j’aimerais remercier ma famille pour leur encouragement extraordinaire.
1
Chapitre 1 : Introduction
L’énergie nucléaire permet de produire 13 % de l’électricité consommée mondialement. En moyenne, 15 % de la production canadienne d’électricité provient de ce secteur et contribue pour 55 % de la production d’électricité de la province de l’Ontario. Au Canada, la production d’électricité se fait à partir de réacteurs de type CANDU® (CANada Deutérium Uranium) qui sont des réacteurs pressurisés et modérés à l’eau lourde. Des réacteurs modérés au graphite (NRX et NRU situés sur le site d’ÉACL) sont employés à des fins de recherche et à la production de radio-isotopes médicaux. On retrouve sur le territoire canadien 22 réacteurs nucléaires [1] dont 17 sont en fonction. Parmi les réacteurs à l’arrêt, un est en réfection (Point Lepreau, Nouveau-Brunswick) et un autre est en processus de déclassement (Gentilly II, Québec). Dans les cinq prochaines années, cinq réacteurs devront être réfectionnés pour pouvoir continuer leurs opérations.
L’intensification des travaux reliés à la réfection imminente ou le déclassement des réacteurs vieillissants accroît le risque de contamination des employés attitrés à ces tâches. Ces travailleurs doivent ou devront démanteler et transporter des matériaux contaminés par différents radionucléides. Bien que toutes les mesures raisonnables possibles soient prises pour éviter ou limiter l’exposition de ces travailleurs à des niveaux anormaux de radiation, des accidents peuvent survenir.
En 2009 à Bruce Power en Ontario, des employés ont inhalé des actinides, qui sont des émetteurs de particules alpha, lors de travaux sur un réacteur qui avait cessé ses activités depuis environ 10 ans. Des travaux de meulage sur la tuyauterie de la voûte du réacteur devaient être effectués à l’aide d’une meuleuse électrique. Cette dernière était connectée à un aspirateur équipé d’un filtre HEPA (Figure 1 et 2) afin de capter les particules et poussières émises. Cependant, pour une raison encore inconnue, ce dispositif de sécurité n’a pas fonctionné de façon appropriée.
2
Figure 1 : Tuyau d’alimentation dans la voute du réacteur de Bruce Power
Figure 2 : Système aspirateur utilisé pour les travaux de meulage de Bruce Power en 2009
Des tests routiniers de qualité de l’air ont d’abord montré la présence de 60Co, un émetteur gamma, dont l’activité était 7,5 fois supérieure à la limite d’exposition autorisée. Le même scénario s’est répété deux jours plus tard. Des échantillons de filtres à air ont été envoyés aux Laboratoires Kinectrics de Toronto et la présence d’émetteurs alpha dans l’air a été confirmée plusieurs semaines plus tard. L’inhalation d’éléments émetteurs de particules alpha constitue un risque très important pour la santé, ce qui a obligé Bruce Power à suspendre ses activités de meulage et à aviser la Commission canadienne de sûreté
3
nucléaire (CCSN) de la situation. À la suite de cet incident, des études dosimétriques ont été entamées sur 1506 des 2616 employés présents lors de ces travaux. Parmi ceux-ci, 945 ont dû soumettre des échantillons biologiques d’urine et de fèces pendant plusieurs mois. Il a été établi que 62 employés avaient subi, à des niveaux variables, une contamination interne à des émetteurs alpha.
La contamination par des actinides constitue un risque pour la santé, d’où l’importance de pouvoir les mesurer rapidement et efficacement lors d’opérations dosimétriques de routine. L’analyse des actinides à l’état de traces est complexe. Les actinides sont souvent sous la forme d’oxydes peu solubles lorsqu’inhalés ou ingérés. Ils vont surtout se déposer dans les poumons ou être entrainés dans le système gastro-intestinal. Par conséquent, seulement une infime fraction de ces métaux se retrouvera dans l’urine ou le sang en réponse à un incident. Pour obtenir une estimation adéquate de la dose reçue, il est nécessaire de mesurer les actinides dans les matières fécales. Cependant, les fèces constituent une matrice très complexe qui varie grandement d’un individu à l’autre et en fonction de la diète. Dû à leur faible teneur dans les matières fécales, les actinides doivent être mesurés par des méthodes spectrométriques de masse ou radiométriques très sensibles (p. ex. spectrométrie de masse couplée à un plasma induit (ICP-MS) ou spectrométrie alpha) qui sont sujettes à de nombreuses interférences. Conséquemment, une isolation et séparation en fractions distinctes des actinides est nécessaire pour les enlever. L’addition de ces nombreuses étapes rend le processus analytique long et fastidieux.
Pour mesurer les actinides dans les matières fécales, on procède généralement à une déshydratation, une pyrolyse de la matière organique à haute température [2-4], puis à une dissolution acide [2, 4, 5]. Ensuite, les actinides sont extraits et séparés généralement par chromatographie d’extraction [2, 4] ou échangeuse d’ions [4-6]. En utilisant ces procédés, les rendements sont souvent inconsistants dû à la présence d’espèces réfractaires à la dissolution acide (UO2, PuO2). L’utilisation de traceurs ne permet pas de corriger de façon
appropriée le rendement dû à la fraction minérale insoluble amenant à une sous-évaluation de la teneur réelle. De telles erreurs sont inacceptables dans le cadre de dosages biométriques où la santé des travailleurs du secteur nucléaire en dépend.
4
La fusion à haute température est un procédé qui consiste à dissoudre des échantillons à l’aide de sels fondus. Cette technique de dissolution a été utilisée avec succès pour dissoudre des échantillons très réfractaires à la dissolution acide tels que des zirconates ou silicates [7, 8]. Il a été démontré que les oxydes réfractaires d’actinides pouvaient facilement être solubilisés par fusion avec des sels de borates [9-14]. L’utilisation de la fusion pour la préparation des matières fécales pourrait avantageusement permettre leur mise en solution complète et accroître la répétabilité des résultats obtenus. Cependant, la séparation des actinides en fractions distinctes demeure nécessaire pour permettre leur mesure par les techniques analytiques usuelles (spectrométrie alpha et ICP-MS). La compatibilité entre ces deux étapes est cruciale pour permettre la détermination des actinides après fusion.
L’objectif de ce mémoire est de développer une nouvelle méthode analytique permettant de mesurer les actinides des matières fécales dans des situations d’urgence, en utilisant la fusion à haute température, par spectrométrie alpha et ICP-MS. Cette méthode devra en plus être compatible avec la séparation des actinides par chromatographie d’extraction. Elle devra être rapide, efficace, fidèle et suffisamment sensible pour respecter les critères établis par la Commission Canadienne de Sureté Nucléaire [15] ainsi que ceux édictés dans la norme internationale sur les méthodes biométriques ANSI N13.30 [16].
Dans un premier temps, les notions théoriques concernant les propriétés radioactives et le calcul des doses seront présentées. Dans les chapitres suivants, il sera fait état de la mesure des actinides et du développement de la méthode de fusion pour les matières fécales. Enfin, la technique de fusion sera couplée à la chromatographie d’extraction et la méthode analytique sera validée pour la spectrométrie alpha et l’ICP-MS.
5
Chapitre 2 : Notions de base sur la radioactivité et
radiotoxicité
Tel qu’indiqué dans l’introduction, le vieillissement des réacteurs nucléaires canadiens implique le déclassement et la réfection de plusieurs d’entre eux. Ces travaux augmentent les risques de contamination des employés du secteur nucléaire, ce qui justifie le développement de nouvelles méthodes d’analyses dosimétriques. À cette fin, dans ce chapitre, les notions fondamentales ayant trait à la radioactivité et la dosimétrie seront expliquées.
La radioactivité
La radioactivité est le résultat du réarrangement des nucléons, les constituants du noyau atomique, qui conduit à l’émission de particules et de rayonnement. Les noyaux atomiques sont composés de neutrons (n) et de protons (p) dont la cohésion est assurée par la force nucléaire. Un déséquilibre du ratio neutron/proton (N/Z) peut mener à l’instabilité du noyau atomique et à l’émission de radioactivité. Les éléments de masse atomique inférieure à 40 sont généralement stables lorsque leur ratio N/Z est unitaire. Cependant, pour les noyaux de masses supérieures, la stabilité du noyau est observée lorsque le ratio N/Z se situe autour de 1,5 (Figure 3), parce qu’il est nécessaire d’avoir davantage de neutrons pour compenser pour la répulsion électrique engendrée par la présence accrue des protons.
Un isotope est un élément pour lequel le nombre de protons est défini, mais dont le nombre de neutrons diffère. Dans le cas où un isotope est radioactif, il peut être désigné comme un radio-isotope.
6
Figure 3 : Diagramme de stabilité nucléaire
Le processus nucléaire de réarrangement du noyau n’est pas affecté par des paramètres externes tels que la pression, la température ou la nature chimique du milieu dans lequel le noyau est impliqué. Cependant, le taux de désintégration radioactive d’un radio-isotope donné obéit à l’équation logarithmique suivante :
[1]
Où
7
Dans cette équation, le terme N0 désigne le nombre d’atomes initial, alors que N représente
le nombre d’atomes au temps t, λ est la constante de désintégration et le terme t½ désigne le
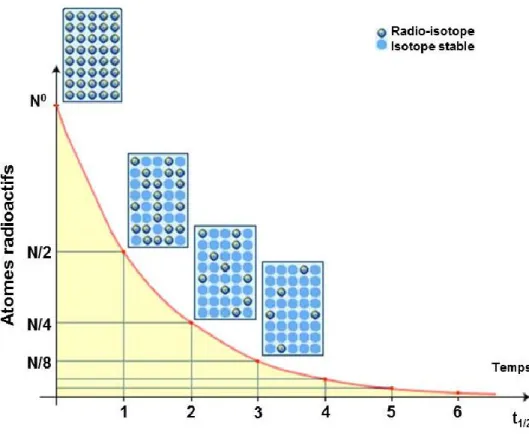
temps de demi-vie du radio-isotope. Cette équation est représentée à la Figure 4 où la fraction du nombre d’atomes est donnée en fonction du nombre de temps de demi-vie.
Figure 4 : Représentation schématique du temps de demi-vie
Les types de radiations ionisantes
Il existe plusieurs processus nucléaires permettant de stabiliser un radio-isotope. Cependant, seuls les trois plus importants du point de vue de la dosimétrie seront discutés, soit la radiation alpha, bêta et gamma.
La radiation alpha (α) est le résultat d’un réarrangement nucléaire impliquant l’émission d’un atome d’hélium doublement chargé (4He2+). Étant donné la masse et la charge élevées
8
de cette particule, la distance qu’elle peut parcourir dans la matière est faible. Elle peut être arrêtée par environ 2 cm d’air, une feuille de papier ou la couche de peau morte de l’épiderme. Les particules alpha ont normalement une énergie située entre 4 et 6 MeV. L’équation suivante illustre l’émission d’une particule alpha par la désintégration radioactive de l’uranium-238 en thorium-234 :
La radiation bêta (β) est due à l’émission d’un électron (β-) ou positron (β+) d’un noyau instable. La radiation bêta couvre un plus large spectre d’énergies que les particules alpha, soit de quelques keV à plusieurs MeV. Les particules bêta ont une distance de parcours dans la matière qui est supérieure à celle des particules alpha. Elles peuvent être arrêtées par 2 cm de Plexiglas, 1 mm d’aluminium ou 5 cm de bois. Ce type de radiation est accompagné par l’émission d’un neutrino (νe) ou antineutrino ( ̅e) la plupart du temps afin
de d’obtenir un différentiel de spin entre les produits et les réactifs unitaire. L’équation suivante représente le réarrangement nucléaire du 241Pu en 241Am par désintégration β- :
̅
La radiation gamma (γ) est une radiation ionisante résultant du réarrangement du noyau atomique suite à l’émission d’une particule alpha ou bêta. Pour que le noyau excité puisse retourner dans un état plus stable (non-excité), l’excès d’énergie peut être émis sous forme de rayonnement électromagnétique de courtes longueurs d’ondes. La radiation gamma couvre un très large spectre d’énergies et n’est généralement pas complètement bloquée par la matière, mais atténuée. Plusieurs mètres de béton ou quelques centimètres de plomb permettent généralement d’atténuer suffisamment la radiation gamma. L’équation suivante représente l’émission de radiation gamma par le 237Np métastable lors de sa conversion en
237Np.
9
Les émetteurs alpha dans le cycle nucléaire
Les réarrangements nucléaires conduisant à l’émission de particules alpha se produisent essentiellement pour des noyaux de masses élevées (nombre A>106). Les particules alpha résultant d’un réarrangement nucléaire ont généralement une énergie cinétique autour de 5 MeV et une vitesse d’environ 15 000 km·s-1, ce qui correspond à approximativement 5 % de la vitesse de la lumière. La distribution d’énergie des particules alpha pour l’ensemble des émetteurs est relativement restreinte : plus de 90% de tous les émetteurs de particules alpha émettent des particules dont l’énergie est comprise entre 4 et 9 MeV (Figure 5). Cette distribution étroite est le résultat d’une dépendance importante entre le temps de demi-vie et l’énergie de la particule, tel que défini par la loi de Geiger-Nuttall.
Figure 5 : Corrélation entre l’énergie de la particule alpha lors du réarrangement nucléaire de 340 émetteurs ayant un Z > 73 et le temps de demi-vie [17]
10
Ainsi, d’un point de vue énergétique, les émetteurs alpha ayant un court temps de demi-vie seront ceux émettant des particules alpha ayant les énergies les plus élevées et, indirectement, infligeront plus de dommages aux tissus adjacents. Cependant, comme les durées de vie sont très courtes (inférieure à une seconde), la probabilité qu’un individu soit exposé à de tels émetteurs est extrêmement faible. Suivant cette logique, il est possible d’établir que les émetteurs apha posant les risques radiologiques les plus élevés seront ceux ayant un temps de demi-vie moyen (1 an < t½ < 1 x 106 ans), une émission de particule
alpha dont l’énergie est comprise entre 4 à 6 MeV et un long temps de résidence dans le corps (ou long temps de demi-vie biologique). Basée sur ces critères, la famille des actinides est celle comprenant le plus d’éléments.
Les actinides sont les éléments ayant un numéro atomique compris entre 89 (Actinium) et 103 (Lawrencium) [18]. Quatre actinides (Actinium, Thorium, Protactinium et Uranium) existent à l’état naturel en quantités pondérables. Les 12 autres membres de la famille des actinides, appelés transuraniens, sont essentiellement des éléments artificiels produits par capture neutronique d’actinides naturels au sein d’installations nucléaires. Parmi les transuraniens, le neptunium, le plutonium, l’américium et le curium sont ceux qui sont les plus souvent formés. Les quantités produites de chaque radioélément dépendent grandement du mode de production (Figure 6.).
11
Figure 6 : Voies simplifiées de production des actinides dans un combustible irradié à 33 GWj t–1 selon les processus nucléaires indiqués [19]
Où (n, 2n), réaction 1 neutron, 2 neutrons), (n, γ), capture radiative, EC, capture électronique, β–, émission bêta moins, (n,f) fission par neutron. Les émissions alpha ne sont pas indiquées, il s’agit de 236Pu donnant 232U, 242Cm donnant 238Pu et 244Cm donnant 240Pu. La voie principale de production est doublée par des pointillés.
Dans les réacteurs nucléaires CANDU, une importante quantité de transuraniens est produite. Le Tableau 1 présente les teneurs approximatives en actinides dans le combustible usé d’un réacteur CANDU [20].
12
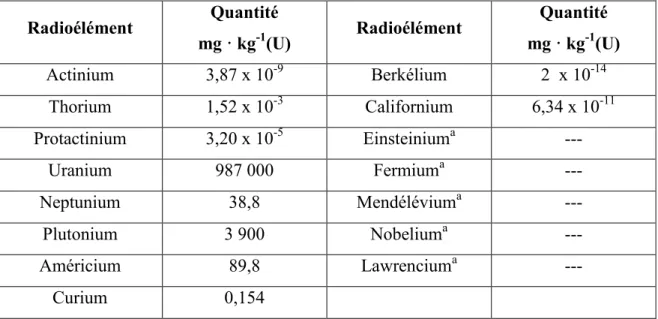
Tableau 1 : Concentration des actinides dans le combustible usé d’un réacteur CANDU, 10 ans après la fin de son irradiation dans le réacteur (puissance de 190
MWh par kg d’uranium) Radioélément Quantité mg · kg-1(U) Radioélément Quantité mg · kg-1(U) Actinium 3,87 x 10-9 Berkélium 2 x 10-14 Thorium 1,52 x 10-3 Californium 6,34 x 10-11 Protactinium 3,20 x 10-5 Einsteiniuma --- Uranium 987 000 Fermiuma --- Neptunium 38,8 Mendéléviuma --- Plutonium 3 900 Nobeliuma --- Américium 89,8 Lawrenciuma --- Curium 0,154
a: Ces radioéléments sont absents du combustible après 10 ans puisqu’aucun de leurs radio-isotopes ne possède un temps de demi-vie suffisamment long pour assurer leur présence dans le combustible usé après cette période.
Tel que mentionné précédemment seuls Np, Pu, Am et Cm seront produits en quantités significatives à l’intérieur du réacteur CANDU et par conséquent constituent les seuls transuraniens posant un risque sanitaire lors du démantèlement d’installations nucléaires. Noter que seuls les radio-isotopes de ces éléments ayant des temps de demi-vie appréciables (1 an < t½ < 1 x 106 ans) seront jugés d’intérêt d’un point de vue de la radioprotection. Le Tableau 2 présente les caractéristiques nucléaires des actinides naturels et transuraniens d’intérêt pour la dosimétrie.
13
Tableau 2 : Caractéristiques nucléaires de quelques actinides d’intérêt
Élément Degré d’oxydationa Isotope Émetteur (produit de filiation) Énergie Mev (%) t½, ans Activité spécifique, MBq/g Th (3), 4 227 α (223Ra) 5,756 (20,4) 5,977 (23,5) 6,038 (24,2) 0,051 1,14 x109 228 α (224Ra) 5,340 (26,2) 5,423 (73,2) 1,913 30,35 x 10 6 229 α (225Ra) 4,845 (56,2) 7900 7 317 230 α (226Ra) 4,620 (23,4) 4,687 (76,3) 75400 763 232 α (228Ra) 3,947 (21,7) 4012 (78,2) 1,4x10 10 0,004 U 3, 4, 5, 6 233 α (229Th) 4,824 (84,4) 1,59x105 357 234 α (230Th) 4,722 (28,4) 4,774 (71,4) 2,45x10 5 231 235 α (231Th) 4,398 (55) 7,04x108 0,080 236 α (232Th) 4,445 (25,9) 4,494 (73,8) 2,37x10 7 2,36 238 α (234Th) 4,151 (22,3) 4,198 (77,5) 4,46x10 9 0,0124 Np 3, 4, 5, 6, 7 237 α (233Pa) 4,771 (23,2) 4,788 (47,6) 2,14x10 6 26,10 Pu 3, 4, 5, 6, (7) 238 α (234U) 5,456 (28,3) 5,499 (71,0) 87,74 633,9 x10 3 239 α (235U) 5,156 (70,8) 24110 2 297 240 α (236U) 5,123 (27,2) 5,168 (72,7) 6537 8 438 241 β (241Am) 0,021 14,4 3,81 x106 242 α (238U) 4,858 (23,5) 4,902 (76,5) 3,76x10 5 145 Am (2), 3 ,4, 5, 6, 7 241 α ( 237Np) 5,485 (84,5) 432,2 127 x 103 243 α (239Np) 5,275 (86,7) 7370 7 391 Cm 3, 4, 6 242 α (238Pu) 6,113 (74,0) 0,446 1,226x108 243 α (239Pu) 5,785 (73,0) 28,5 1,91 x106 244 α (240Pu) 5,762 (23,3) 5,804 (76,7) 18,11 2,99 x 10 6
14
Notions de dosimétrie
Dans cette section, il sera fait état de la notion de dose, des voies d’ingestion des particules alpha, de la vitesse de dissolution de ces particules, de leur distribution dans les organes et des dommages qu’elles peuvent causer aux tissus.
Dose et facteur de pondération
Dans le but de quantifier le risque radiologique que représente la radiation ionisante, on utilise fréquemment le concept de dose. La dose absorbée (DT) est généralement définie
comme étant une unité d’énergie absorbée (ε) par une masse de tissus (m), et est exprimée en Gray (Gy, où 1 Gy = 1 J kg-1).
̅ ̅ [3]
L’énergie de la radiation ionisante, généralement en électron-volt, peut être convertie en joule selon la relation suivante :
[4]
Cependant, la dose absorbée ne prend en considération que l’énergie transférée à une masse de tissus et non l’effet biologique attribuable à un tel processus. Pour déterminer les effets biologiques associés à l’exposition de tissus à de la radiation ionisante, on utilise plutôt la dose équivalente (HT) qui est une dose effective pondérée selon le type de radiation. Pour
ce faire, on utilise un facteur de pondération (WR) et la dose équivalente peut être
15
∑ [5]
Le tableau suivant présente les facteurs de pondération pour les types de radiations ionisantes les plus communs.
Tableau 3 : Facteurs de pondération des types de rayonnements Type de radiation Facteur de pondération
(WR, Sv/Gy)
Gamma 1
Bêta 1
Alpha 20
La dose équivalente est exprimée en Sievert (Sv). La dose équivalente permet de mieux évaluer les dommages biologiques réels à une masse de tissus. Ainsi, pour une dose absorbée donnée, la radiation alpha sera 20 fois plus dommageable que les autres types de radiation. Par conséquent, dans le cas d’une contamination interne où le transfert de l’énergie attribuable à la radiation alpha est complet, les effets sur les tissus seront importants.
Finalement, la dose reçue peut être estimée de façon encore plus précise en tenant compte de l’organe où se produit le transfert d’énergie. Puisque chaque type de tissus a une radiosensibilité différente, un facteur de pondération spécifique (Tableau 4) a été déterminé pour chaque organe (WT). Cette façon d’exprimer la dose s’appelle la dose effective (HE) et
est calculée selon l’équation suivante :
16
Tableau 4 : Facteur de pondération des tissus
Tissus ou organe cible Facteur de pondération des tissus (WT)
Gonade 0,20 Côlon 0,12 Poumon 0,12 Estomac 0,12 Foie 0,05 Vessie 0,05 Œsophage 0,05 Peau 0,01 Surface des os 0,01
Limites d’exposition légales
Au Canada, la Commission canadienne de sûreté nucléaire (CCSN) a établi la limite d’exposition annuelle des travailleurs du secteur nucléaire associée à l’inhalation, l’ingestion ou l’injection de radionucléides à 50 millisieverts. Toute nouvelle méthode analytique dosimétrique développée devra donc satisfaire à cette obligation légale.
Voies d’absorption des radionucléides
Les radionucléides présents dans le milieu ambiant (air, eau, sol, nourriture) peuvent pénétrer dans l’organisme par diverses voies. L’absorption peut se faire par inhalation, ingestion, transfert cutané ou encore par une plaie. Les prochains paragraphes traitent sommairement des diverses voies d’absorption des radionucléides.
17
Les radionucléides sous forme d’aérosols ou de gaz peuvent être absorbés par inhalation et se retrouver dans les poumons. Certains gaz, tels que les gaz rares, seront majoritairement expulsés par les poumons et auront un effet limité sur la dose reçue. Autrement, les radionucléides déposés sur les tissus pulmonaires peuvent y demeurer s’ils sont peu solubles ou, selon leur degré de solubilité, être transférés partiellement ou totalement dans le système circulatoire sanguin. Il arrive couramment que les particules présentes dans l’air soient dirigées vers le système digestif au lieu du système pulmonaire, parce qu’elles sont captées par les muqueuses de la bouche.
Pour quantifier la vitesse d’absorption des particules dans les poumons, on utilise une échelle établie par la Commission Internationale de Protection Radiologique (CIPR, en anglais International Commission on Radiological Protection ou ICRP) où 4 niveaux d’absorption sont considérés: V, F, M et S. Les particules V (de l’anglais Very) sont absorbées par le corps de façon instantanée. Cependant, ce type d’absorption n’est pas observé pour les actinides. Les particules F (de l’anglais Fast) sont très rapidement absorbées. Des particules sont considérées F si elles sont totalement absorbées par les alvéoles des bronches ou absorbées à hauteur d’au moins 50 % dans la région nasale postérieure et du larynx, 25 % dans la région extrathoracique dans un délai de 10 minutes (ex : UF6). Les particules de type M (de l’anglais Medium) ont une solubilité moyenne où
70 % des particules sont absorbées dans la région alvéolaire ou 10 % dans la région bronchiale en 10 minutes (ex : UO3). Les particules S (de l’anglais Slow) se dissolvent le
moins rapidement. Dans ce cas, seulement ≤ 0,1 % est absorbé dans un délai de 10 minutes. Le Tableau 5 résume les paramètres d’absorption selon les catégories de l’ICRP. En fonction de la solubilité, un composé inhalé sera détecté plus facilement dans l’urine, les excréments ou encore les fluides pulmonaires, ces derniers étant beaucoup plus difficiles à obtenir.
18
Tableau 5 : Paramètres par défaut pour des matériaux de type F, M et S [21] Type d’absorption Type F (rapide) Type M (modéré) Type S (lent)
Fraction dissoute rapidement
1 0,1 0,001
Taux de dissolution :
Rapide (par jour) 100 100 100
Lent (par jour) - 0,005 0,0001
Les radionucléides peuvent être ingérés par la consommation de liquides ou d’aliments. Une fois dans le système digestif, ils peuvent être absorbés partiellement ou en totalité par l’intestin et se retrouver dans le sang pour se répartir dans les différents organes du corps selon leurs propriétés chimiques. Les éléments insolubles seront éliminés dans les fèces. La propension d’un radionucléide à traverser la barrière intestinale est mesurée par la valeur du taux de transfert gastro-intestinal (f1). Pour un radionucléide donné, plus la valeur de f1 est
élevée, plus le taux de transfert est élevé et il est total pour une valeur de 1. Le tableau 6 présente les valeurs de f1 établies par la CIPR pour les actinides.
19
Tableau 6 : Valeur f1 pour les actinides [22]
Radioélément Type F Type M Type S
Actinium 5,0 x 10-4 5,0 x 10-4 5,0 x 10-4 Thorium 5,0 x 10-4 5,0 x 10-4 5,0 x 10-4 Protactinium 5,0 x 10-4 5,0 x 10-4 5,0 x 10-4 Uranium 0,02 0,02 0,002 Neptunium 5,0 x 10-4 5,0 x 10-4 5,0 x 10-4 Plutonium 5,0 x 10-4 5,0 x 10-4 1,0 x 10-5 Américium 5,0 x 10-4 5,0 x 10-4 5,0 x 10-4 Curium 5,0 x 10-4 5,0 x 10-4 5,0 x 10-4 Berkélium 5,0 x 10-4 5,0 x 10-4 5,0 x 10-4 Californium 5,0 x 10-4 5,0 x 10-4 5,0 x 10-4 Einsteinium 5,0 x 10-4 5,0 x 10-4 5,0 x 10-4 Fermium 5,0 x 10-4 5,0 x 10-4 5,0 x 10-4 Mendélévium 5,0 x 10-4 5,0 x 10-4 5,0 x 10-4
Les actinides, à l’exception de l’uranium, possèdent une très faible solubilité dans le système digestif (f1 très faibles) et par conséquent ceux-ci se retrouveront majoritairement
dans les matières fécales suite à une ingestion.
L’absorption directe de radionucléides par une blessure ou par voie transcutanée est possible, mais généralement très peu fréquente. L’élément déposé sur une plaie ou sur la peau pourrait être entraîné dans le sang selon l’état de la peau, mais également la nature du radionucléide. La peau ne constitue pas une barrière absolue et peut laisser pénétrer certains radionucléides comme le tritium sous forme d’eau tritiée, ou encore des radionucléides liés à des molécules lipophiles.
20
Distribution des actinides dans les organes
Une fois dans le système sanguin de l’organisme, la distribution des radionucléides vers les différents systèmes et organes dépend de leurs propriétés chimiques. Les actinides ayant des propriétés chimiques semblables se distribueront de façon similaire dans le corps humain où ils y resteront un certain temps. Le tableau suivant indique le pourcentage de distribution d’actinides en réponse à une absorption dans différentes parties du corps.
Tableau 7 : Biodistribution des actinides [23] Rétention (%) Th U Np Pu Am Cm Espèce chimique Th4+ UO22+ Np4+ NpO2+ Pu4+ Am3+ Cm3+ Os 70 10-15 30-50 30-50 50 30 30 Foie 5 2-10 --- 2-10 30 50 50 Reins 3 12-25 --- 1 --- --- --- Tissus mous 4 5 5 5 10 --- --- Urine 4-6 (5 j) 65 (1 j) (1 h) 3-4 15-20 (1 h) 0,4 (1 j) < 1 (1 j) (1 j) < 1 Excréments (20 j) 7–9 70 (6 j) 15 (1 j) 20-40 (1 j) 1,4 (14 j)
Où (x j) signifie la totalité de l’espèce excrétée après x jours.
On observe au Tableau 7 que les actinides peu solubles (Th4+, Np4+, Pu4+) sont principalement excrétés par les matières fécales. Il est donc plus facile de mesurer ces éléments dans les matières fécales que dans l’urine. À l’inverse, les actinides plus solubles (UO22+, NpO2+, Am3+, Cm3+) seront davantage éliminés dans l’urine. L’élimination des
actinides peut également se faire par la transpiration ou par les organes de protection caractérisés par une kératinisation intense (dents, ongles, cheveux et poils), mais ce processus est peu favorisé. Le temps de séjour d’un radionucléide dans l’organisme dépend de 2 mécanismes indépendants : le temps de demi-vie du radionucléide et l’élimination biologique (demi-vie biologique). Cette dernière dépend du taux de renouvellement de
21
l’élément et varie en fonction de l’âge. L’équation suivante représente le temps de demi-vie effectif (t½,eff) ou temps pour lequel la quantité déterminée d’un radionucléide présent dans
un système soit diminuée de moitié par suite à la fois de la décroissance radioactive et de processus d’éliminations biologiques. La relation temps de demi-vie effectif avec le temps de demi-vie radiologique (t½) et biologique (t½,B) est donnée par l’équation suivante:
[7]
Tableau 8 : Temps de demi-vie effectif des actinides pour le squelette [24] Radionucléide t½,eff (a) Radionucléide t½,eff (a)
Thorium-228 1,89 Plutonium-238 61,9 Thorium-232 > 100 Plutonium-239 > 100 Uranium-234 0,274 Plutonium-240 > 100 Uranium-235 0,274 Plutonium-241 12,33 Uranium-238 0,274 Américium-241 > 100 Neptunium-237 > 100 Américium-243 > 100
Tel qu’observé au Tableau 8, les temps de demi-vie effectifs de certains actinides à long temps de demi-vie radiologique peuvent être supérieurs à la durée de vie moyenne d’un individu. Par conséquent, l’incorporation et l’assimilation de certains actinides par le squelette conduira à une dose continue sur une longue période de temps, augmentant ainsi le niveau de risques associés à l’absorption de ces éléments.
22
Modélisation de la dose
Le calcul de la dose reçue implique un grand nombre de paramètres et, pour pallier cette difficulté, plusieurs modèles mathématiques ont été développés. Ces modèles permettent d’évaluer la dose reçue pour l’ensemble du corps ou encore pour un organe précis, sur la base d’un scénario d’inhalation ou d’ingestion. Afin de calculer correctement la dose, la nature chimique, la valence, le type d’absorption ainsi que l’isotope inhalé doivent être pris en compte. Le CIPR a développé de nombreux modèles à cette fin. Le logiciel GenmodPC est souvent utilisé pour calculer la dose reçue par un individu et sera employé dans le cadre de ce mémoire. Le Tableau 9 montre les quantités attendues dans les matières fécales de quelques actinides en utilisant ce logiciel en fonction du nombre de jours suivant l’exposition. La Figure 7 illustre un modèle simplifié décrivant le parcours possible d’un isotope dans les divers organes et systèmes du corps selon diverses voies d’exposition. Dans cette figure, chaque flèche représente un transfert entre deux systèmes biologiques et est définie par une constante unique pour chaque forme chimique de chaque radionucléide.
23
Figure 7 : Sommaire des diverses voies d’exposition, de transferts et d’excrétion du corps humain [25]
Tel qu’illustré à la Figure 7 précédente, quatre voies d’excrétion sont possibles pour les radionucléides, soit la sueur, les muqueuses nasales, l’urine et les excréments. La mesure des radionucléides dans la sueur ou les muqueuses nasales permet de mettre en évidence une exposition récente à des radionucléides (de quelques minutes à quelques heures), tandis que la mesure des radionucléides dans l’urine et les excréments permet de mettre en évidence des expositions antérieures, puisque ces processus d’excrétion sont plus lents. Ainsi, bien que quelques études ont démontré la faisabilité d’utiliser des prélèvements sudoraux et nasaux pour effectuer des reconstitutions de doses [26, 27], dans le cadre de ce mémoire, l’accent sera mis sur l’urine et les excréments.
24
Tableau 9 : Activité de certains isotopes d’Am, Cm, Pu et Np dans les matières fécales pour une dose de 1mSv suivant l’inhalation calculée par le logiciel GenmodPC
Radionucléide
Taux d’excrétion fécale (mBqjour-1)
jour
2ième 30ième 180ième 365ième
Inhalation de type S 237Np 43 23 4,6 2,7 238Pu 32 17 3,5 2,1 239Pu 41 22 4,4 2,7 240Pu 41 22 4,4 2,7 241Am 40 21 4,3 2,6 241Pu 4100 2100 430 250 242Cm 76 35 4,3 1,2 244Cm 36 19 3,8 2,3 Inhalation de type M 237Np 19 8,5 1,0 0,28 238Pu 9,2 4,2 0,56 0,18 239Pu 8,5 3,8 0,51 0,17 240Pu 8,5 3,9 0,52 0,17 241Am 10 4,7 0,61 0,20 241Pu 470 220 28 8,8 242Cm 66 27 2.1 0,32 244Cm 16 7,2 0,93 0,31
Effets de la radiation ionisante sur les tissus humains
Les effets de la radiation ionisante sur le corps humain sont classés en deux catégories: les effets déterministes et les effets stochastiques. Les effets déterministes sont directement reliés à la dose reçue et causeront des effets physiques relativement immédiats. L’activité nécessaire pour observer ces effets dépend de l’organe touché, mais de façon générale, il faut une dose minimale d’au moins 0,25 Sv pour commencer à observer ces effets. Pour une dose égale ou supérieure à 6 Sv, la mort est inévitable. Le Tableau 10 présente la relation entre la dose et les effets déterministes possibles.
25
Tableau 10 : Symptômes probables suite à une exposition corporelle de radiation gamma [28]
Dose Symptômes
0-0,25 Gy (0-0,25 Sv)
Aucun effet clinique observable. Effets retardé mais peu probable. 0,25-1 Gy
(0,25-1 Sv)
Légère variation dans le sang. Nausée possible.
Effets graves retardés possibles mais peu probables. 1-2 Gy
(1-2 Sv)
Nausée et fatigue avec possibilité de vomissement.
Réduction du nombre de cellules sanguines avec régénération retardée. 2-3 Gy
(2-3 Sv)
Nausée et vomissement possibles dans les 24 heures.
Période latente de 2 semaines suivie de malaise généralisé, diarrhée, perte d’appétit et perte de poids modéré.
Mort possible mais peu probable dans les 2 à 4 semaines à venir. 3-6 Gy
(3-6 Sv)
Nausée, vomissement et diarrhée dans les heures suivant l’exposition. Courte période latente suivie de malaises généralisés, diarrhée, perte d’appétit, perte de poids, hémorragie, apparition de taches sur la peau et inflammation de la gorge.
Mort possible dans la première semaine. > 6 Gy
(> 6 Sv)
Nausée, vomissement et diarrhée dans les heures suivant l’exposition. Courte période latente suivie de fièvre, diarrhée, perte d’appétit, perte de poids, hémorragie, apparition de taches sur la peau et inflammation de la gorge.
Mort inévitable dans les deux premières semaines.
Les effets stochastiques sont définis comme étant des effets indirects et probabilistes en fonction de la dose reçue. Ils s’expriment en termes de probabilité d’avoir certains effets en fonction de l’exposition. Évidemment, plus la dose reçue est élevée, plus la probabilité de subir des effets physiologiques augmente (mutation, cancer).
26
Les particules alpha ont une grande énergie cinétique qui se dissipe par collision avec la matière. Ce processus entraîne l’ionisation de plusieurs molécules qui à leur tour peuvent réagir avec le milieu environnant. Ainsi, une particule ionisante de 1 MeV peut générer plus de 30 000 paires d’ions.
Le mécanisme exact d’interaction des particules ionisantes avec les tissus biologiques demeure l’objet d’un débat scientifique. D’une part, elles génèrent des scissions moléculaires (effet direct), et d’autre part, elles provoquent la radiolyse de l’eau (effet indirect) qui conduit à la formation de radicaux libres, des espèces chimiques fortement toxiques (Figure 8). L’ionisation (10-15 sec) et la production de radicaux libres (10-9 sec) sont quasi-instantanés et peuvent conduire à des bris de brins d’ADN. Ces lésions moléculaires peuvent causer des effets déterministes (cas des fortes doses) qui seront rapidement observés. Cependant, le bris de brin d’ADN peut être à l’origine d’effets tardifs pouvant survenir des années après l’exposition (cancer) ou encore affecter la descendance (mutation). On comprend alors toute l’importance des mesures mises en place pour réduire l’exposition à la radioactivité et l’implantation de programmes de dosimétrie.
27
29
Chapitre 3 : Notions de chimie radioanalytique
Les grandes notions de radioactivité et de radiotoxicité ayant été définies au chapitre précédent, ce troisième chapitre regroupe les notions nécessaires au processus d’élaboration de la méthode analytique. L’échantillonnage y est décrit ainsi que les principales étapes nécessaires à une bonne dissolution et séparation des radionucléides d’intérêt. Enfin, les différentes méthodes d’analyses sont couvertes à la fin de ce chapitre.
Composition des matières fécales
Les matières fécales sont essentiellement les résidus non assimilés et les masses de bactéries résultant du processus de digestion. Plus spécifiquement, les matières fécales sont composées en grande partie d’eau et de matière organique, tels que des résidus alimentaires non digérés, du mucus, des débris de cellules épithéliales et des bactéries (~ 40 %) [29]. La CIPR estime qu’un homme et une femme excrètent de façon journalière environ 150 et 120 g de matières fécales, respectivement [30]. Les habitudes alimentaires et la période de la journée influencent grandement leur composition. Un élément important dans la composition des matières fécales est le silicium, un nutriment essentiel pour la formation des os [31]. Des sources élevées en silicium peuvent être retrouvées dans plusieurs aliments communs, comme les végétaux (tels que les céréales, la bière, les bananes), tandis que des teneurs en silicium plus faibles sont observées dans la viande [32, 33]. Le silicium étant peu absorbé par le système digestif, la quasi-totalité du silicium ingérée se retrouve dans les excréments. De hautes teneurs en silice dans des échantillons fécaux peuvent aussi compromettre la séparation des actinides. L’urine est généralement le mode excrétoire privilégié pour les radionucléides de type F, tandis que l’excrétion par les voies gastro-intestinales est généralement celle favorisée pour les radionucléides de type M et S.
30
Contrairement aux constituants de l’urine, ceux retrouvés dans les matières fécales sont peu solubles dans l’eau.
Pour réduire au minimum le volume de l’échantillon et pour éliminer les constituants organiques peu solubles présents dans les fèces, ces dernières sont calcinées jusqu’à l’obtention de cendres minérales contenant les actinides d’intérêt.
Mise en solution des cendres
Techniques de dissolution
Afin d’isoler, de séparer et d’analyser les actinides présents dans les matières fécales, les résidus de cendres minérales suivant la calcination doivent être dissous. Pour ce faire, on utilise soit la dissolution acide soit la digestion par fusion.
La dissolution acide
La dissolution par digestion acide est la méthode la plus commune pour la mise en solution de sels inorganiques. Elle consiste à dissoudre les sels par l’usage d’acides forts (HNO3,
HCl, H2SO4, HClO4) à forte molarité à chaud. L’acide agit sur les oxydes de faibles
valences et/ou forme des sels de solubilité supérieure, ce qui permet de les mettre en solution de façon partielle ou totale selon le cas. Certaines espèces sont plus réfractaires à la dissolution acide. C’est le cas par exemple de la silice où pour la dissoudre, il faut employer de l’acide fluorhydrique (HF) qui vient former le fluorocomplexe soluble SiF62-.
31
L’utilisation d’HF est une opération dangereuse qui nécessite de la verrerie résistante à l’acide fluorhydrique (ex : Téflon, plastiques).
Figure 9 : Mécanisme d’élimination de la silice par l’acide fluorhydrique
Les digestions acides s’effectuent à reflux, peuvent prendre plusieurs heures, sont corrosives et souvent ne permettent qu’une digestion partielle de l’échantillon.
Il est possible d’augmenter l’efficacité des digestions acides par l’utilisation des micro-ondes. Dans ce cas, les échantillons sont placés dans un contenant de Téflon scellé avec un acide fort qui est chauffé par micro-ondes et est sous haute pression. Des pressions allant jusqu’à 1,4 MPa [34] peuvent être obtenues, ce qui favorise l’attaque de l’acide sur l’échantillon et sa dissolution. Toutefois, la quantité d’échantillon utilisable par une telle approche est limitée puisque la digestion par micro-ondes ne peut s’effectuer que sur quelques centaines de milligrammes [35]. De plus, la digestion acide par micro-ondes n’assure pas pour autant une dissolution totale de l’échantillon ; Motabar et coll. ont attribué dans leurs travaux des pertes de 15 à 20 % en U et Th respectivement à des fractions non-dissoutes de minerais de zircon lors d’analyse de sédiments par digestion acide [8].
La digestion par fusion
La digestion par fusion consiste à utiliser un sel inorganique, appelé fondant, pour dissoudre l’échantillon. Ainsi, l’échantillon et le fondant sont mélangés et ensuite chauffés à haute température soit au-dessus du point de fusion du mélange. Le sel fondu à haute température est alors soit directement versé dans une solution acide ou bien refroidi à
SiO2+ 6HF H2SiF6+ 2H2O
32
température de la pièce pour former une pastille qui sera par la suite dissoute en milieu acide. La fusion a l’avantage de permettre la dissolution complète de l’échantillon. Par contre, elle introduit une grande quantité d’un sel inorganique qui est souvent peu soluble et qui implique des volumes de solution importants.
Le fondant est constitué de trois éléments : l’agent fondant, l’agent mouillant et l’agent oxydant (facultatif). L’agent fondant est le solvant et le réactif, soit l’équivalent de l’acide lors de la digestion acide. Il permet de convertir les oxydes en composés solubles par métathèse des anions. Il existe plusieurs agents fondants qui sont commercialement disponibles dont l’hydroxyde de sodium (NaOH), le pyrosulfate de potassium (Na2S2O7), le
carbonate de sodium (Na2CO3), le métaborate de lithium (LiBO2), le peroxyde de sodium
(Na2O2) et le bifluorure de potassium (KHF2). Le fondant le plus utilisé est le métaborate
de lithium. Ce dernier possède un point de fusion de 845°C [36], et un caractère basique ce qui aide à la digestion des oxydes acides tels que UO2. Il est donc un fondant de choix pour
les échantillons riches en silicates et oxydes réfractaires. Plusieurs travaux ont déjà porté sur la fusion à l’aide du métaborate de lithium afin de dissoudre et mesurer les actinides [3, 11, 37, 38]. Par exemple, Rudisill et Karraker ont procédé à la dissolution de PuO2 vitrifié,
l’espèce d’actinide la plus difficile à dissoudre, par fusion avec du borax (Na2B4O7) et ont
obtenu un excellent rendement (90%) [9]. Forsberg et Beahm ont également réussit à dissoudre complètement du combustible irradié contenant du plutonium à l’aide d’oxyde de bore (B2O3) [10].
L’agent mouillant est un sel servant à rendre le mélange plus fluide dans le creuset. L’agent mouillant permet aussi d’abaisser la température de fusion du mélange, d’aider à son homogénéisation ainsi que de faciliter le versement (coulage) du mélange fondu vers une solution acide. Il agit également comme un lubrifiant qui prévient l’adhésion du fondant sur les parois du creuset. L’agent mouillant est ordinairement composé d’un halogénure d’alcalin. L’iodure de lithium est l’agent mouillant utilisé pour ce projet. Il a un point de fusion de 550°C et un point d’ébullition de 1265°C [36]. Il peut donc être facilement utilisé pour une fusion avec du métaborate de lithium à environ 1050°C.
33
L’agent oxydant est un sel que l’on peut ajouter lors de la fusion pour oxyder l’échantillon [39, 40]. Plusieurs agents oxydants peuvent être ajoutés au fondant, cependant il se peut que le creuset utilisé pour la fusion soit chimiquement attaqué par l’oxydant [7]. Dans le cadre de ce projet, un agent oxydant a été ajouté et sert à éliminer chimiquement le noir de carbone résiduel suite à la calcination, ce qui permet de réduire la taille des pastilles ainsi que de rendre la fusion plus efficace. L’agent oxydant qui a été retenu est le persulfate de sodium puisqu’il a une température de décomposition basse (180°C) et qu’il augmente peu la charge saline de la matrice car il se décompose en trioxyde de soufre gazeux [36].
Puisque le milieu réactionnel de la fusion est très corrosif, il est nécessaire d’utiliser des creusets pouvant résister au fondant utilisé. Le Tableau 11 montre, pour différents fondants, les creusets qui sont compatibles.
Tableau 11 : Type de fondants commun par rapport à leur creuset Fondant Température de fusion (°C) Creuset
LiBO2 1000-1100 Graphite, Pt
Li2B4O7 1000-1100 Graphite, Pt
Na2O2 600 Ni, Ag, Au, Zr
Na2CO3 1000-1200 Pt, Ni
NaOH 400-430 Fe, Ni, Ag, Au
KHF2 900 Pt
K2S2O7 >400 Pt
Dans le cadre de ce projet de maîtrise, seul des creusets de Pt/Au (95/5) pour le M4 Fluxer ainsi que des creusets de graphite haute pureté ont été employés.
L’entreprise Corporation scientifique Claisse a développé un appareil à fusion automatisé, le M4 Fluxer, mentionné plus tôt, qui à l’aide de brûleurs au gaz propane permet la fusion automatisée de 3 échantillons à la fois. L’appareil peut ensuite verser le mélange fondu
34
dans une solution acide. La fusion automatisée permet de rapidement dissoudre des échantillons (moins de 10 minutes) de façon sécuritaire pour le manipulateur. Toutefois, l’utilisation de grands volumes de gaz propane constitue un risque plus élevé d’incendie et plusieurs institutions n’autorisent pas son emploi.
Figure 10 : Le Fluxer M4 de Corporation scientifique Claisse
La technique de dissolution par fusion, qui permet une dissolution complète de la plupart des échantillons inorganiques, comporte cependant certains désavantages. D’abord, la fusion implique une très grande quantité de sels, souvent peu solubles, qui nécessitent de grands volumes de liquide pour les maintenir en solution. Ces sels peuvent aussi interférer lors de la séparation des actinides, lors de la préparation des échantillons par spectrométrie alpha, et peuvent réduire l’efficacité de l’ionisation par la torche à plasma de l’ICP-MS. Ensuite, les fondants contiennent à l’état de traces des actinides en quantités variables et qui peuvent nuire à l’interprétation des résultats (Tableau 12).
35
Tableau 12 : Teneurs en Th et en U (mg/kg) par analyse par ICP-MS de LiBO2 selon
leur grade [41, 42]
Grade Th U
99,9 % (Alfa Aesar) 0,2 0,02
99,997 % (Alfa Aesar) 0,00004 0,0001 Ultra pure (Claisse) (+ 1,5 % LiBr) - 0,0006
Enfin, la fusion ne permet pas l’élimination des silicates. Lors de la dissolution en milieu fortement acide, les silicates peuvent se condenser avec le temps et former un gel, ce qui peut grandement nuire à la séparation. Les solutions apportées à ce problème seront discutées plus loin dans ce mémoire.
Techniques de séparation des actinides
Techniques de séparation
Puisque les actinides sont retrouvés à l’état de traces dans les matières fécales et que leur mesure est sujette à de nombreuses interférences, il est nécessaire de procéder à une séparation des actinides. La séparation permet d’isoler les actinides et de les préconcentrer à des teneurs suffisamment élevées pour pouvoir les mesurer.
Pour ajusté les fluctuations de rendement associées à la méthode analytique utilisée, un radiotraceur est ajouté. Le traceur utilisé doit avoir un comportement similaire à l’analyte. En radiochimie, on utilise lorsque possible un isotope différent de celui étudié. Comme il s’agit du même élément chimique, il va se comporter de façon identique. Le traceur ne doit
36
pas interférer avec l’isotope à analyser et doit être facilement quantifiable. Pour ce projet de maîtrise, un traceur est toujours utilisé afin d’ajuster les résultats obtenus.
La coprécipitation
Le procédé de coprécipitation est le transfert d’un analyte à un précipité par la déposition simultanée d’un agent coprécipitant. La coprécipitation s’effectue en ajoutant un sel soluble qui précipite dans les mêmes conditions que l’analyte par l’ajout d’un anion ou d’un cation. L’agent de coprécipitation permet d’entraîner l’analyte à l’état de traces qui autrement serait resté en suspension dans la solution. Le précipité peut être ensuite filtré ou centrifugé, ce qui permet d’isoler l’espèce désirée et de réduire le volume de la solution. La coprécipitation est une technique peu sélective, mais elle permet tout de même d’éliminer un grand nombre d’interférents matriciels qui sont solubles. Dans le domaine de la chimie radioanalytique, la coprécipitation est un procédé de choix puisqu’il est rapide et économique. C’est pour ces raisons qu’il est souvent utilisé en combinaison avec d’autres procédés de séparation.
L’extraction liquide-liquide
L’extraction liquide-liquide est un procédé de séparation largement utilisé dans l’industrie nucléaire. Il sert entre autres à l’extraction de l’uranium qui entre dans la composition du combustible nucléaire. L’extraction liquide-liquide est un procédé de séparation d’une phase liquide immiscible ou partiellement immiscible dans une autre phase liquide où un composé est isolé par son affinité vers l’autre phase. Les actinides à extraire sont normalement dissous dans une phase aqueuse acide et sont extraits sélectivement par la phase organique. Des ligands présents dans la phase aqueuse forment des complexes de charge neutre qui ont une plus grande affinité pour la phase organique que la phase polaire.
37
Il existe trois façons de former une espèce neutre pouvant être extraite par le solvant soit : ajouter un anion organique, remplacer l’eau coordonnée au métal par des molécules organiques larges, ou former un complexe métal-ligand anionique qui se combine à de larges molécules organiques cationiques pour former une paire d’ions neutre. L’agent d’extraction le plus commun est le tributylphospate (TBP). Il sert à séparer l’uranium et le plutonium du combustible nucléaire irradié dans le procédé PUREX (Plutonium Uranium EXtraction).
Figure 11 : Mécanisme d’extraction de l’extraction liquide-liquide pour les ions métalliques (VI) et (IV)+ à l’aide de TBP
L’extraction liquide-liquide produit de grandes quantités de déchets inflammables, ce qui rend cette approche peu intéressante pour le développement de nouvelles méthodes analytiques.
La chromatographie d’échange ionique
La chromatographique d’échange ionique a plusieurs applications industrielles. Elle est utilisée dans le traitement et la purification de l’eau et même pour le traitement d’effluents contaminés des centrales nucléaires. C’est une technique populaire dans le domaine de la chimie nucléaire dû à son efficacité, sa rapidité et son faible coût. En chromatographie d’échange ionique, la solution contenant les ions à être séparés est circulée au travers d’une résine contenant des groupements actifs qui sont greffés sur un support solide inerte. Les ions présents dans la solution se combinent à la résine par des échanges ioniques. Une fois que l’espèce désirée est retenue sur la résine, les conditions du milieu sont modifiées pour permettre leur élution. Pour ce faire, on peut soit modifier le pH ou encore ajouter un contre-ion ou un complexe qui a une plus grande affinité pour l’analyte. Il existe deux
38
types de résines échangeuse d’ions : les résines anioniques et les résines cationiques. Les résines anioniques échangent les groupements négativement chargés tandis que les résines cationiques (à base de composé sulfonique ou carboxylique) échangent les groupements positifs.
Figure 12 : Mécanisme d’échange ionique sur une résine échangeuse d’ions (forme anionique)
La chromatographie d’extraction
La chromatographie d’extraction est une technique très populaire pour la séparation des actinides. Elle combine les avantages de la chromatographie et de l’extraction liquide-liquide. Cette technique consiste à imprégner, sur un support solide, un solvant ou ligand organique peu soluble en milieu aqueux qui a la capacité d’extraire les analytes d’intérêt. L’agent extractant sur la phase stationnaire forme des complexes avec les ions présents dans la phase mobile aqueuse. Cette technique d’extraction liquide-liquide sur support solide a l’avantage de générer moins de déchets que l’extraction liquide-liquide. Il existe plusieurs agents extractants d’intérêt pour l’isolation des actinides [43]. Le pouvoir extractant de l’agent organique pour un composé peut-être quantifié par une valeur de capacité de rétention. Ce facteur se détermine selon l’équation suivante :
( ) ( )


![Figure 5 : Corrélation entre l’énergie de la particule alpha lors du réarrangement nucléaire de 340 émetteurs ayant un Z > 73 et le temps de demi-vie [17]](https://thumb-eu.123doks.com/thumbv2/123doknet/6998086.199212/25.918.152.782.572.995/figure-corrélation-énergie-particule-alpha-réarrangement-nucléaire-émetteurs.webp)


![Tableau 5 : Paramètres par défaut pour des matériaux de type F, M et S [21]](https://thumb-eu.123doks.com/thumbv2/123doknet/6998086.199212/34.918.98.781.141.334/tableau-paramètres-défaut-matériaux-type.webp)
![Tableau 7 : Biodistribution des actinides [23]](https://thumb-eu.123doks.com/thumbv2/123doknet/6998086.199212/36.918.100.779.473.726/tableau-biodistribution-des-actinides.webp)
![Tableau 8 : Temps de demi-vie effectif des actinides pour le squelette [24]](https://thumb-eu.123doks.com/thumbv2/123doknet/6998086.199212/37.918.223.749.454.680/tableau-temps-demi-vie-effectif-actinides-squelette.webp)