de
de civil
Faculte des appliquees
Provision de la performance des argiles
Champlain comme barrieres a la migration des
contaminants dans les sites d' enfouissement.
de es
:
.bi^^v^e t &
# 94 297 014
REMERCIEMENTS
J'aimerais remercier mon superviseur. Ie Dr. Alexandre Cabral, pour ses precieux conseils, ses commentau-es critiques et ses encouragements tout au long de cette recherche.
Je suis aussi tres reconnaissante envers Jean-Guy Lemelin et Edc Drouin, tous deux du laboratoire de mecanique des sols, pour leur bonne humeur et surtout pour leur aide tres appreciee. Je remercie Serge et Irene, ainsi que tous mes collegues de travail du departement de genie civil pour leur bonne compagnie au cours de ces deux demieres ammees. Merci aussi a mon copain, Fady, pour ses encouragements et sa grande comprehension.
Ce memoire de maTtnse est dedicace a Claude et Anne, mes parents qui m'out toujours supportee et encouragee au cours de ces annees d'etudes.
RESUME
La migration des contaminants a partir d'un site d'enfouissement sanitaire est un phenomene complexe regit par trois principaux processus: 1'advection, la dispersion
hydrodynamique (dispersion mecanique et dififtision moleculaire) et la retention (attenuation). Le
projet de reglement gouvememental (MEF, 1996) propose des amenagements de barrieres de
protection bases principalement sur Ie phenomene d'advection, negligeant ainsi la contaniination
par difiusion moleculaire. Pourtant, il a ete demontre que dans les sols de faible permeabilite telles
les argiles. Ie front de contamination avance beaucoup plus rapidement par difiEusion moleculaire
que par advection seulement.Ce memoire presente done une methodologie permettant la determination, a partir d'essais
de laboratoire, des coefficients de dififtision effectifs et de distribution. Le traitement des donnees
a ete efifectue au moyen d'un modele numerique (Pollute v6). L'utilisation d'une solution a sel
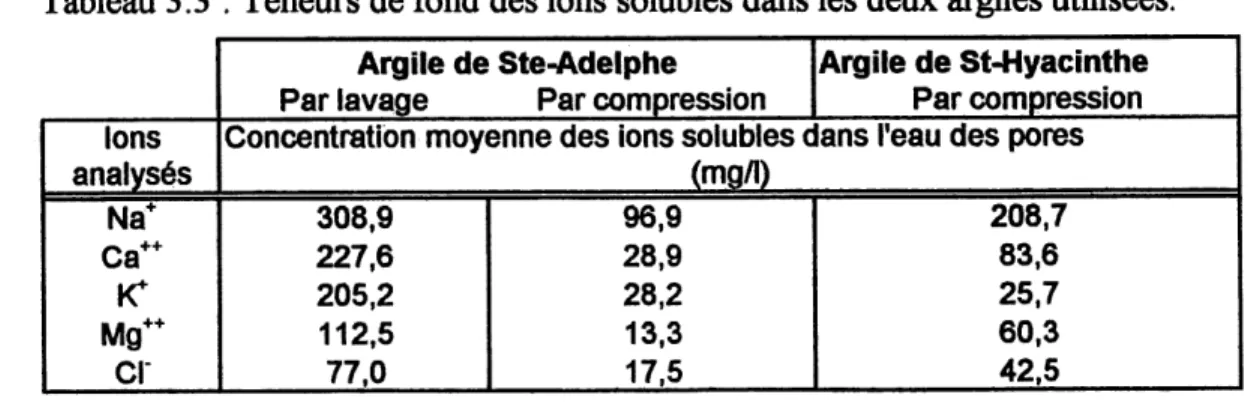
unique (NaCl) a permis la determination du Dci-, du DNB+, du Kci- et du KNa+ pour deux argilestypiques de Champlain (argile de Ste-Adelphe et de St-Hyacinthe). Le tableau suivant montre les
resultats obtenus.|||A|rgi|l||j|Jl|iam|iJaJn||
Ste-Adelphe
St-Hyacinthe
|®eii|(in2|<»»|)|
1,0 1,0il3ici|ii!ml!lllill:
0,0 0,0||||p|N|i||(|m2||QU^
1,2 0,4|||||K|^||(|Gij^|<g|)|J||
0,89
0,89La caracterisation complete de chacun de ces sols argileux est presentee dans ce memoire. La
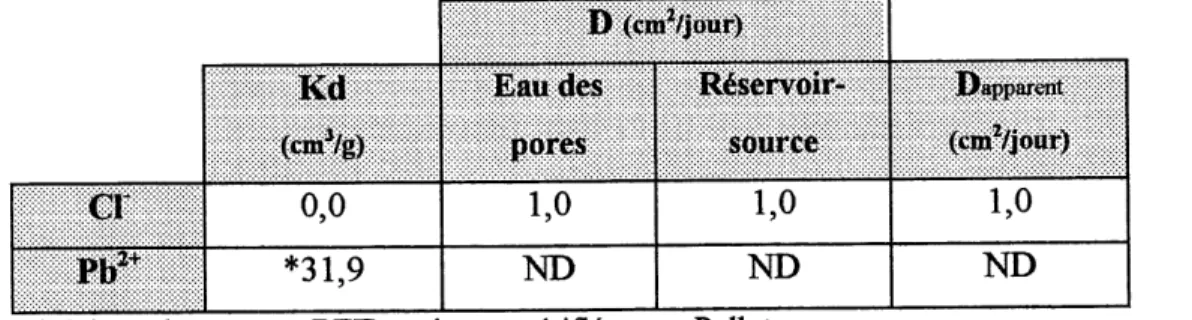
realisation de deux essais de diffusion pure avec une solution de KC1 et de PbCl2 sur Ie sol de
Ste-Adelphe indique que Ie coefficient de difiEusion du CF n'est pas aflfecte de fa90n significative par la
nature du cation auquel il est associe, ce qui corrobore les resultats d'autres chercheurs.La determination des coefficients de diffusion et de distribution permet 1'evaluation de la
performance de depots naturels d'argile Champlain dans lesquels des dechets sont enfouis ou
risquent d'^tre enfouis. Diverses simulations de la contamination au Cf et au Pb2+ ont ete efFectuees pour divers designs de sites d'enfouissement sanitaire. Une evaluation preliminaire deprotection decrits dans Ie projet de reglement gouvememental sur la mise en decharge et
Fincineration des d6chets (MEF, 1996). Les logiciels Pollute v6 et Migrate v9 ont ete utilises
pour les simulations. Les caracteristiques du sol employe sont celles de 1'argile de Ste-Adelphe.
Les coefi&cients de diffusion et de distribution utilises sont ceux obtenus pour cette argile. D'apres
les resultats, Favance du front de contamination pour les contaminants mobiles comme par exemple Ie d' depend :(1) des valeurs des coefficients de diffusion des contaminants presents;
(2) des concentrations de chaque contaminant initialement contenu dans Ie lixiviat;
(3) du taux d'efificacite du systeme de collecte du lixiviat, et
(4) de la qualite du recouvrement final.
Les trois configurations de bameres proposees s'averent efficaces contre la contamination par Ie Cl' des sols et des nappes d'eau souterraine, dans la mesure ou Ie systeme de collecte du lixiviat a un taux d'efficacite eleve et que la qualite du recouvrement final peut-etre maintenue durant toute la periode de post-fermeture du site. En outre, les barrieres construites avec une membrane composite semblent de loin les plus perfbrmantes. En ce qui a trait au Pb , lorsqu'il est en presence d'une argile Champlam, 1'avancee de son front de contamination est negligeable.
TABLE DES MATIERES
1. INTRODUCTION _1
1.1 PROBLEMATIQUE 1
1.2 OBJECTIFS DU MEMOIRE 2
1.3 LIMITATIONS DU MEMOffiE 3
1.4 ORGANISATION DE LWSEMBLE DU MEMOIRE 3
2. REVUE DE LITTERATURE _5
2.1 PMNCDPAUX PROCESSUS AFFECTANT LE TRANSPORT DES CONTAMINANTS 5
2.1.1L'ADVECTION 52.1.2 LA DISPERSION HYDRODYNAMIQUE 6
2.1.2.1 D6veloppement de F^quation gen^rale d'advection et de dispersion 9
2.1.3 RETENTION DES CONTAMINANTS 12
2.1.3.1 Adsorption des contaminants et autres processus de reaction 1 3 2.1.3.2 Capacite d'att^nuation des sols argileux 18 2.1.3.3 L'importance de la double couche difiEuse 19
2.2 IMPORTANCE DE I/AVANCEE DU FRONT DE CONTAMINATION PAR
DIFFUSION MOLECULAIRE 22
2.3 CAS HISTOMQUES (LOVE CANAL, KEELE VALLEY, CONFEDERATION ROAD) 23
3. METHODOLOGIE DES ESSAIS _29
3.1 CARACTEMSATION DES ARGILES UTILISEES 30
3.1.1 ESSAI OEDOMETRIQUE 32 3.1.2 DETERMINATION DES UMTFES D'ATTERBERG 32 3.1.3 DETERMINATION DUPHDU SOL 33 3.1.4 ESSAI DE SEDIMENTOMETRIE 333.1.5 COMPOSITION MINERALOGIQUE 34
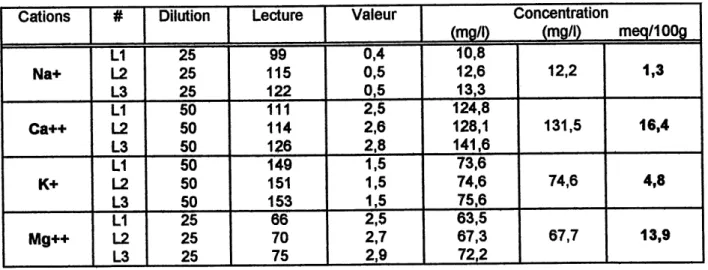
3.1.6 DETERMINATION DES CONCENTRATIONS DES IONS SOLUBLES (TENEURS DE FOND) 35
3.1.6.1 Par m^thode de lavage 37 3.1.6.2 Par compression ^ Faide d'une presse triaxiale 37
3.1.7 DETERMINATION DES CONCENTRATIONS DES CATtONS ADSORBES CTENEURS
3.1.7.1 Cations adsorb6s suite ^ une extraction des ions solubles par lavage 39 3.1.7.2 Cations adsoib^s suite a une extraction des ions solubles par compression 39
3.1.8 INFLUENCE DE LA METHODE D'EXTRACTION DE L'EAU DES PORES 40 3.1.9 DETERMINATION DE LA CEC 40 3.1.10 DETERMINATION DE LA SSA 40 3.1.11 COEFNCIENTDEDISTRffiUTIONDUNa+, KdNa+(ARGILE DE STE-ADELPHE) 41 3.1.11.1 Facteur de retardement du Na (argile de Ste-Adelphe) 42 3.1.12 COEFFICIENT DE DISTRIBUTION DU Na+, KdN^ (ARGDLE DE ST-HYACINTHE) 42
3.1.12.1 Facteur de retardement du Na+ (argile de St-Hyacinthe) 43
3.2 ESSAIS DE DIFFUSION PURE (ESSAIS EN LABORATOIRE) 43
3.2.1 PREPARATION DE LA SOLUTION DU RESERVOIR-SOURCE 46 3.2.2 MONTAGE D'UNE CELLULE DE DIFFUSION 46
3.2.3 PRfiLEVEMENTS DE LA SOLUTION DU RESERVOIR-SOURCE 46
3.3 ESSAIS DE LESSIVAGE (ESSAIS EN LABORATOIRE) 47
3.3.1 PREPARATION DE LA SOLUTION DE LESSIVAGE 50
3.3.2 MONTAGE D'UNE CELLULE DE LESSF^AGE 50 3.3.3 PRELEVEMENTS DE L'EFFLUENT 523.4 METHODE ^EXTRACTION DES IONS SOLUBLES (EAU DES PORES) 52
3.5 METHODE D'EXTRACTION DES CATIONS ADSORBES 53
3.6 ANALYSE CHIMIQUE DES CATIONS ADSORBES 53
3.7 ANALYSE CHIMIQUE DU CHLORURE (CI) 53
3.8 DETERMINATION DES COEFFICIENTS DE DIFFUSION EFFECTIFS 54
4. PRESENTATION ET DISCUSSION DES RESULTATS DES ESSAIS _55
4.1 ESSAIS DE DIFFUSION AVEC L'ARGILE DE STE-ADELPHE 55
4.1.1ESSAIN°2(NaCl) 56 4.1.2ESSAIN°4(NaCl) 59 4.1.3ESSAIN°6(NaCl) 63
4.1.4ESSAl?3(KCl) 65
4.2 ESSAI DE DIFFUSION AVEC I/ARGILE DE ST-HYACINTHE 68
4.2.1ESSAIN°9(NaCl) 71
4.3 ESSAIS DE LESSIVAGE AVEC L*ARGILE DE STE-ADELPHE 75
4.3.1 ESSAIS ? 8 ETN° 10 75
5. MODELISATION NUMERIOUE _83
5.1 CHOIX DES CONTAMINANTS 83
5.2 TYPE DE SOL CHOISI POUR LES SIMULATIONS 84
5.3 TYPES DE SIMULATIONS EFFECTUEES 84
5.4 HYPOTHESES DE BASE QUANT A LA MODELISATION DE LA CONTAMINATION
85
5.5 RESULTATS 87
5.5.1 SDMULATIONS EFFECTUEES SELON LES CONDITIONS DECMTES A L'ARTICLE 15 87
5.5.1.1 Comparaison de la contamination par advecdon seulement et par dijffusion mol^culaire
dans la barriere argileuse 93
5.5.2 SIMULATIONS EFFECTUEES SELON LES CONDITIONS DE L'ARTICLE 16 94
5.5.2.1 Premiere possibility d'am^nagement: barriere d'argile compactee. 95 5.5.2.2 Deuxi^me possibility d'am^nagement: membrane composite. 98
5.6 CONCLUSIONS DE CE CHAPITRE 101
CONCLUSIONS
RECOMMANDATIONS
BIBLIOGRAPHIE
ANNEXES
104
106
108
112
Annexe A: Caracterisation des argiles utilisees:
Annexe B: Description de certaines des manipulations des essais. Annexe C: Resultats de Fessai de diffusion n° 2 (argile de Ste-Adelphe). Amiexe D: Resultats de 1'essai de difEusion n0 4 (argile de Ste-Adelphe). Annexe E: Resultats de 1'essai de diffusion n° 6 (argile de Ste-Adelphe). Annexe F: Resultats de 1'essai de diffiision n° 3 (argile de Ste-Adelphe). Annexe G: Resultats de 1'essai de diffusion n° 7 (argile de Ste-Adelphe). Annexe H: Resultats de Fessai de difi&ision n° 9 (argile de St-Hyacinthe). Annexe I: Resultats des essais de lessivage n° 8 etn° 10 (argile de Ste-Adelphe). Annexe J: Resultats des simulations du chapitre 5.
LISTE DES TABLEAUX
TABLEAU 2.1 : PROCESSUS DE RETENTION (BEST ET COLL., 1993; YONG, 1985). 12
TABLEAU 2.2 : PROPRIETES PHYSICO-CfflMIQUES DE L'ARGILE SDLTEUSE ; SITE DE SARNIA
(BARONE ET COLL., 1988; CROOKS ET QUIGLEY, 1984). 25
TABLEAU 2.3 : COMPOSITION MINERALOGIQUE ET UMITES D'ATTERBERG DES SOLS
D'AVONDALE CONSTfTUANT LA COUCHE DE SOL COMPACTE AU SrTE DE KEELE
VALLEY (KING ET COLL., 1992). 27 TABLEAU 3.1: PROPRffiTES PHYSICO-CfflMIQUES DES ARGILES DE STE-ADELPHE ET DEST-HYACINTHE 31
TABLEAU 3.2 : CARACTERISTIQUES DU SOL OBTENUES AVEC L'ESSAI OEDOM^TRIQUE. 32
TABLEAU 3.3 : TENEURS DE FOND DES IONS SOLUBLES DANS LES DEUX ARGILES UTILIS^ES. 37
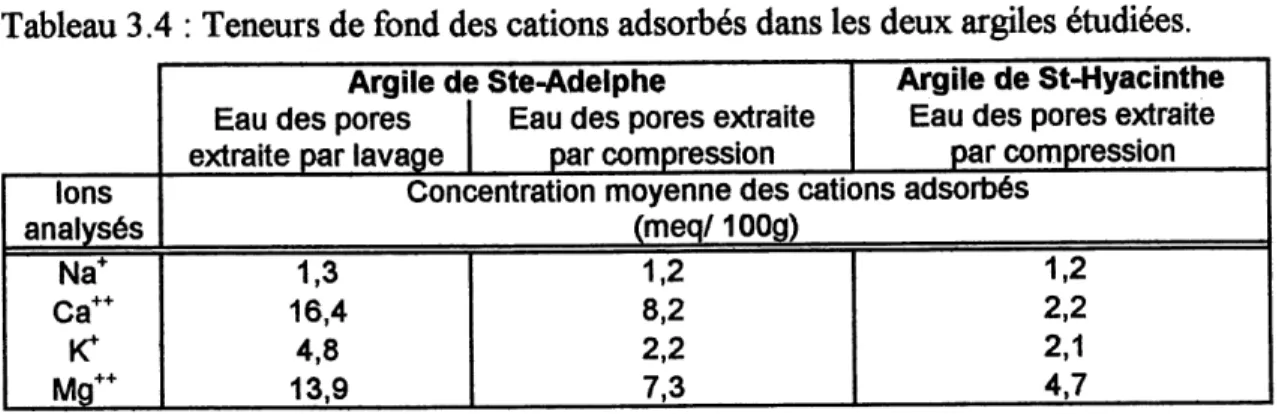
TABLEAU 3.4 : TENEURS DE FOND DES CATIONS ADSORBfiES DANS LES DEUX ARGILES
ETUDIEES. 39
TABLEAU 4.1: COEFFICIENTS DE DIFFUSION EFFECTIFS ET DE DISTRIBUTION (ESSAI ? 2,
NaCl). 59
TABLEAU 4.2 : COEFFICIENTS DE DIFFUSION EFFECTIFS, APPARENTS ET DE DISTRIBUTION
(ESSAIN°4,NaCl). 62
TABLEAU 4.3 : COEFFICIENTS DE DIFFUSION EFFECTIFS, APPARENTS ET DE DISTRIBUTION
(ESSAIN°6,NaCl). 65
TABLEAU 4.4 : COEFFICIENTS DE DIFFUSION EFFECTIFS, APPARENTS ET DE DISTRTOUnON
CESSAl?3,KCl). 68
TABLEAU 4.5 : COEFFICIENTS DE DIFFUSION EFFECTFS, APPARENTS ET DE DISTRTOUTION
(ESSAIN07,PbCl2). 71
TABLEAU 4.6 : COEFFICIENTS DE DIFFUSION EFFECTIFS, APPARENTS ET DE DISTRIBUTION
(ESSAIN°9,NaCl). 74
TABLEAU 4.7 : COEFFICIENTS DE DISTRIBUTION, DE DIFFUSION EFFECTIFS ET APPARENTS
(ESSAIS?8ETN°10). 79
TABLEAU 4.8 : RfiCAPITULATION DES COEFFICIENTS DE DIFFUSION EFFECTIFS, APPARENTS ET
DE DISTRIBUTION DU Cl- ET DU Na+ OBTENUS DES TROIS ESSAIS DE DIFFUSION
AUNaCl 80
TABLEAU 5.1: PARAMETRES D'ENTREE POUR LES SIMULATIONS D'UN SITE T^PE SUIVANT
L'ARTICLE 15. 88
TABLEAU 5.2 : CONCENTRATIONS DE Cl- ET DE PB2+ (MG/L) AU POINT D'ANALYSE A DE LA
FIGURE 5.3, SELON LE TAUX D'EFFICACFTE DU SYSTEME DE COLLECTE (T=100
ANS APRES LA FERMETURE DU SITE). 90
TABLEAU 5.3 : [Cl- ] AU POINT D'ANALYSE B (T =75 ANS). 90
TABLEAU 5.4 : CONCENTRATIONS DE Cl- ET DE Pb2+ (MG/L) EN FONCTION DU TAUX
D'lNFILTRATION (T =60 ANS). 91
TABLEAU 5.5 : CONCENTRATIONS DE Cl- ET DE Pb2+ (MG/L) EN FONCTION DE LA VALEUR DU
Dci. ET DU Dpb2+ AU POINT D'ANALYSE A DE LA FIGURE 5.3 92
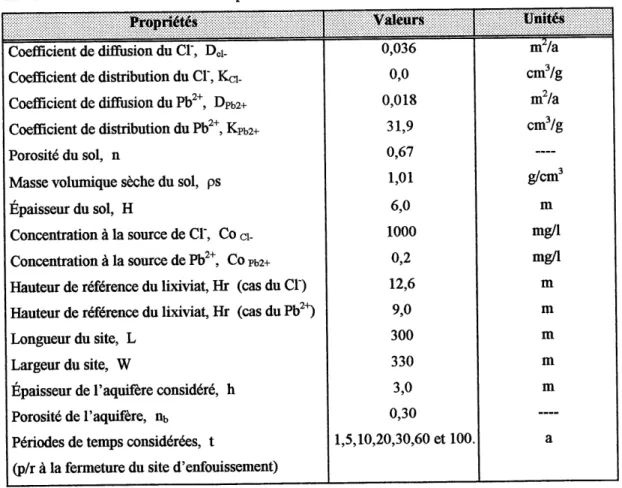
TABLEAU 5.6 : PARAMETRES D'ENTR^E GENERAUX POUR LES SIMULATIONS SUWANT LES
CONDITIONS DECRTTES A L'ARTICLE 16 (1) 96
TABLEAU 5.7 : PARAMETRES D'ENTREE SPECIFIQUES AUX SIMULATIONS SUIVANT L'ARTICLE
16 (1) 96
TABLEAU 5.8 : CONCENTRATIONS DE Cl- AU POINT D'ANALYSE C DE LA FIGURE 5.5 (T =30,60
ET130ANS) 98
TABLEAU 5.9 : PARAMETRES D'ENTREE SPECINQUES AUX SIMULATIONS SUIVANT L'ARTICLE
16 (2) 99
TABLEAU 5.10 : CONCENTRATIONS DE Cl- EN FONCTION DE LA FREQUENCE DES TROUS AU
POINT D'ANALYSE A (FIGURE 5.6), SOFT A 3,6 M DE PROFONDEUR (T = 100 ANS)
LISTE DES FIGURES
FIGURE 2.1 : REPRESENTATION DE L'ADVECTION 5
FIGURE 2.2 : CONDITIONS D'ECOULEMENT OU LA DIFFUSION MOLECULAIRE JOUE UN R6LE
IMPORTANT DANS LA MIGRATION DES CONTAMDMANTS A PARTffi. PAR EXEMPLE,
D'UN LES: a) DIFFUSION SANS ADVECTION (PAS DE GRADmNT HYDRAULIQUE) ; b)
DIFFUSION AVEC UNE ADVECTION POSniVE (ECOULEMENT VERS L'EXTERIEUR DU
LES); c) DIFFUSION AVEC UNE ADVECTION NEGATIVE (CAS D'UN PIECE
HYDRAULIQUE) (FIGURE ADAPTEE DE SHAKELFORD, 1989,1991-b) 7
FIGURE 2.3 : DISPERSION LONGFTUDINALE : a) CONCENTRATION CONSTANTE DU TRACEUR A
L'AFFLUENT ; b) CONCENTRATION RELATIVE C/CO DI TRACEUR A T == 0,; c) COURBE
D'lNFLEXION DU TRACEUR EN FONCTION DU TEMPS DE LESSIVAGE; d)
CONCENTRATIONS DU TRACEUR SELON LA DISTANCE POUR DIFFERENTS TEMPS
(FIGURE ADAPTER DE FREEZE ET CHERRY, 1979) 8
FIGURE 2.4 : DISPERSION LONGITUDDSTALE ET TRANSVERSALE 9
FIGURE 2.5 : FLUX DE MASSE D'UN VOLUME DANS L'ESPACE (FIGURE ADAFTEE DE FREEZE ET
CHERRY, 1979) 10
FIGURE 2.6 : SOLUBIUTE D'UN HYDROXYDE D'UN METAL EN FONCTION DE LA VALEUR DU PH
(FIGURE ADAPTEE DE GALVEZ, 1989) 18
FIGURE 2.7 : INTERACTIONS ENTRE LES IONS DE L'EAU DES PORES DU SOL ET UNE PARTICULE
D'ARGILE (FIGURE ADAFTEE DE YONG ET COLL., 1992) 20
FIGURE 2.8 : MODELE THEORIQUE DE STERN-GOUY : a) DISTRIBUTION DES IONS SELON LA
DISTANCE ; b) DISTRIBUTION DU POTENTIEL ELECTRIQUE SELON LA DISTANCE
(FIGURE ADAPTER DE SHANG ET COLL., 1994) 21
FIGURE 2.9 : PROFILS T^PIQUES DE CONTAMINATION PAR ADVECTON ET DIFFUSION
MOLECULAffiE 23
FIGURE 2.10 : CONCENTRATION DE L'EAU DES PORES EN Na+ ET Cl- DANS LE DEP6T D'ARGILE
SOUS LES DECHETS CT = 6 ET 12 ANS) (NGURE TIREE DE QUIGLEY ET ROWE, 1986) 26
FIGURE 2.11 : PRONL DE CONCENTRATIONS DU CHLORURE DANS LE SOL SOUS-JACENT LES
DECHETS ENFOUIS AU SITE DE KEELE VALLEY (T = 4,25 ANS) (NGUKE TIREE DE IONG
ET COLL., 1992) 28 FIGURE 2.12 : PROFD. DE CONCENTRATIONS DES CATIONS Na+, K+, Ca2+ ET Mg2+ (MG/L) DANS LACOUCHE D'ARGILE SOUS LES DECHETS ENFOUIS CT = 4,25 ANS) (FIGURE TIREE DE
KING ET COLL., 1992) 28FIGURE 3.1 : SCHEMA DU PROGRAMME EXPERIMENTAL DE CETTE RECHERCHE 30
FIGURE 3.2 : COURBE GRANTJLOMETRIQUE DU SOL DE STE-ADELPHE 34
FIGURE 3.3 : SPECTROGRAMMES DES ANALYSES ATG ET ATD SUR UN ECHANTD.LON D'ARGD^E
NATURELLE DE STE-ADELPHE 36
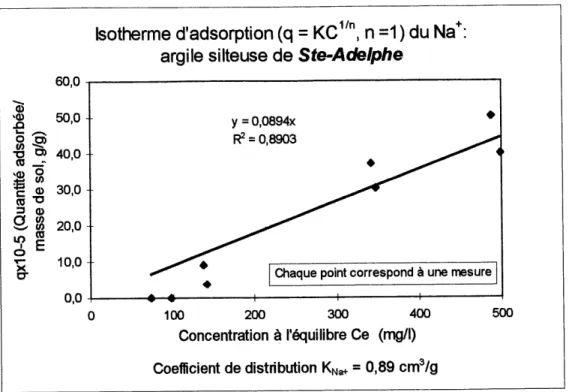
FIGURE 3.4 : ISOTHERME D'ADSORFTION DU Na+, ARGILE SD.TEUSE DE STE-ADELPHE 42 FIGURE 3.5 : ISOTHERME D'ADSORFTION DU Na+, ARGD.E DE ST-HYACINTHE 43FIGURE 3.6 : CELLULE DE DIFFUSION (FIGURE ADAFTEE DE BARONE ET COLL., 1988) 44
FIGURE 3.7 : PRINCIPALES ETAPES D'UN ESSAI DE DIFFUSION PURE 45
FIGURE 3.8 : CELLULE DE LESSIVAGE (PHOTO PMSE PARE. DROUIN) 48
FIGURE 3.9 : MONTAGE DE DEUX CELLULES EN COURS D'ESSAI (PHOTO PRISE PAR E. DROUIN) 49
FIGURE 3.10 : PROCEDURES D'UNE SERffi D'ESSAIS DE LESSIVAGE (ADAPTEE ET MODIFIEE DE
WAMTH, 1987) 51 FIGURE 5.1 : PROFIL TYPE 84
FIGURE 5.2 : CONFIGURATION DU SHE TO>E 85
FIGURE 5.3 : SCHEMA D'UN SITE D'ENFOUISSEMENT TO»E CONCU SELON L'ARTICLE 15 87
FIGURE 5.4 : COMPARAISON DES FRONTS DE CONTAMINATION DU Cl- PAR ADVECTION VERSUS
PAR DIFFUSION MOL^CULAIRE, DANS UNE BARRIERE ARGD.EUSE AMENAGEE SELON
L'ARTICLE 15, POUR DIFFERENTS TEMPS 94FIGURE 5.5 : SCHEMA D'UN SITE D'ENFOUISSEMENT TYPE CONCU SELON L'ARTICLE 16 (1) 95
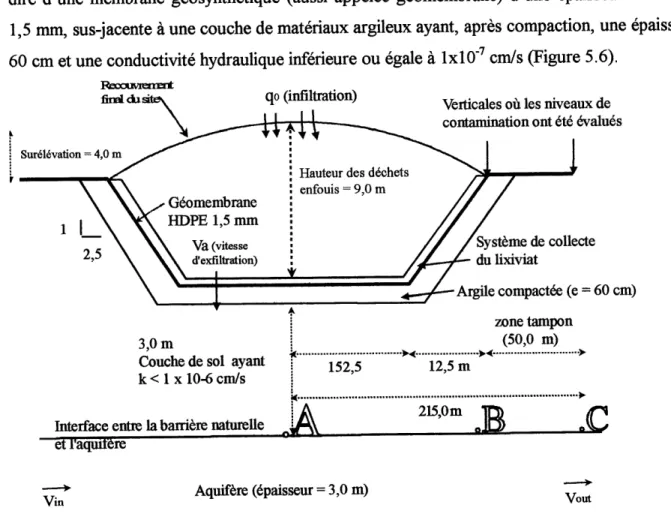
FIGURE 5.6 : SCHEMA D'UN SITE D'ENFOUISSEMENT T?E CONCU SELON L'ARTICLE 16 (2) 98
1. INTRODUCTION
Le Quebec produit annuellement plus de 7 millions de tonnes de residus. Actuellement, plus de 70% de ces residus ne sont toujours pas recycles et 81% de ceux-ci sont elimines par
enfouissement (PAERLES, 1994). Les lieux d'enfouissement sanitaires (LES) que 1'on retrouve
au Quebec ont ete construits suivant d'anciennes reglementations gouvemementales. Une desprincipales caracteristiques du reglement sur les dechets solides de 1978, est par exemple
Facceptation du principe d'attenuation naturelle du lixiviat par Ie sol comme principal moyen de
protection des eaux souterraines et des sols. Bien que plusieurs modifications aient ete apportees a ce reglement, la penode de consultation publique necessaire a 1'elaboration d'une nouvelle reglementation n'est pas encore tout a fait terminee. Selon la revision actueUe du projet dereglement sur I'incineration et la mise en decharge (MEF, 1996), Ie concept de confinement,
d'etancheisation des LES est preconise comme Ie moyen efficace de protection de
1'environnement. Les resultats de 1'etude presentee dans ce m^moire examineront quelques aspects de cette question.1.1 Probl6matique
Aujourd'hui, il est bien connu que la migration des contammants a partu- d'un LES est un phenom^ne complexe regit par differents processus. n existe au moms trois principaux processus gouvemant la progression de la contamination dans les sites d'enfouissement sanitaires. D'abord
Fadvection, soit Ie processus par lequel les contaminants sont transportes dans Ie Ibdviat au
travers de la barri^re suite b une accumulation de Ibdviat au fond de la cellule (Tenfouissement,
creant ainsi un gradient hydraulique. Puis, il y a Ie processus de la dispersion hydrodynamique
qui regroupe la dispersion mecanique et la diffusion moleculaire. La diffusion moleculaire est un
phenomene par lequel un contaminant migre dans Ie sol de la bamere a cause (Tune difference entre la concentration du contaminant dans Ie lixiviat et dans 1'eau des pores du sol sous-jacent.Enfin, il y a Ie phenomene de retention (aussi appele attenuation) des contaminants par les
particules de sol de la barriere, causant ainsi un retardement de leur migration.Dans la derniere version du projet de reglement sur 1'incineration et la mise en decharge
des dechet solides (MEF, 1996), Ie ministere de 1'Environnement et de la Faune du Quebec
propose divers scenarios de barrieres hydrogeologiques exigeant des materiaux relativement impermeables. Les exigences du nouveau reglement visent surtout 1'atteinte d'un faible gradient hydraulique au fond de la cellule d'enfouissement. Cependant, la difference de concentration des contaminants dans Ie lixiviat et dans 1'eau des pores du sol sain sous-jacent est telle qu'un gradient de concentration s'etablira. Ce gradient de concentration va entrainer la migration des contaminants au travers de la barriere de faible lpermeabilite par diffiision moleculaire. Dans les sols de faible permeabilite, telles les argiles. Ie front de contamination avance beaucoup plusrapidement par diffusion moleculaire que par advection seulement (Quigley, 1995; Shackelford,
1991; Barone et coll., 1988; Best et coll., 1993; Crooks et Quigley, 1984; Quigley et Rowe, 1986;
Desaulniers et coll., 1981; Goodall et Quigley, 1977). L'importance de la diffusion moleculaire est
telle, que tot ou tard des tests de difiusion devront etre realises en laboratoire afin d'estimer les parametres de contamination (coefficients de diffusion et de distribution, etc.) associes auphenomene de diffusion (Shackelford, 1991). Au Quebec, relativement peu de donnees sont
disponibles pour les depots naturels ou les LES sont ou pourraient etre installes.1.2 Objectifs du memoire
L'objectif principal de ce memoire est de determiner les coefScients de diffiision de deux
composes morganiques (Ie Na et Ie Cl" ) et d'evaluer la performance de deux dep6ts naturels du
Quebec comme barrieres a la migration de ces composes dans les LES. Des essais de diffusion etde lessivage (faisant intervenir a la fois Fadvection et la difiEusion) ont ete realises avec des
echantillons de sols argileux typiques de la mer de Champlain. Les sols utilises proviennent de
Ste-Adelphe (rive nord du Saint-Laurent) et de St-Hyacinthe (rive sud du Saint-Laurent). Avant
de proceder a tout essai, une caracterisation complete de ces sols a ete faite.1.3 Limitations du memoire
Les coefficients de diffusion ont ete determines a partir d'une solution a sel unique (NaCl,
KC1) ou de PbClz. Cependant, il est reconnu que les valeurs de coefficients de difiusion du CF et
du Na^ pourraient etre respectivement plus fortes et plus faibles dans Ie cas ou un vrai lixiviat domestique aurait ete utilise comme solution. Get ecart s'expliquerait par la competitivite entre les divers contaminants presents dans Ie lixiviat, pour les sites d'adsorption disponibles a la surface du sol argileux (Barone et coll., 1988).1.4 Organisation de Peusemble du memoire
Ce memoire comporte 5 chapitres et 10 annexes. Le contenu de chacun de ces chapitres se decrit comme suit:
Chapitre 1: La problematique est exposee, les objectifs sont definis, et les principales limitations du
memoire sont precisees.Chapitre 2: Une revue de litterature met en evidence Fimportance du phenomene de diffijsion
moleculaire dans les sols de faibles permeabilite. Quelques cas historiques y sont
presentes.
Chapitre 3: Les methodologies d'essais de diffusion, de lessivage et d'analyses chimiques sont
presentees, de meme que les caracteristiques physico-chimiques des sols argileux utilises.Chapitre 4: Les resultats des essais de laboratoire ainsi que la determination des coefiScients de
diffusion effectifs et de distribution des composes etudies a 1'aide du logiciel Pollute v6
sont presentes et discutes.Chapitre 5: Diverges simulations cTune contamination par Ie chlorure ou Ie plomb selon trois designs de sites d'enfouissement sanitaires, sont presentees et discutees.
Le contenu de chacun des annexes se decrit comme suit; Annexe A: Caracterisation des argiles utilisees.
Annexe B: Description de certaines des manipulations des essais.
Annexe C: Resultats de 1'essai de diffusion n 2 (argile de Ste-Adelphe).
Annexe D: Resultats de Fessai de diffusion n° 4 (argile de Ste-Adelphe).
Annexe E: Resultats de Fessai de diffusion n 6 (argile de Ste-Adelphe).
Annexe F: Resultats de 1'essai de diffusion n° 3 (argile de Ste-Adelphe).
Annexe G: Resultats de 1'essai de diffusion n 7 (argile de Ste-Adelphe).
Annexe H: Resultats de Fessai de dififtision n° 9 (argile de St-Hyacinthe).
Annexe I: Resultats des essais de lessivage n° 8 etn° 10 (argile de Ste-Adelphe).
Annexe J: Resultats des simulations du chapitre 5.2. REVUE DE LITTERATURE
Ce chapitre explique quels sont les principaux processus regissant la migration des
contaminants et presente quelques cas histonques appuyant Fimportance du phenomene de diffusion moleculaire dans Favancee du fi-ont de contamination.2.1 Principaux processus affectant Ie transport des contaminants
Plusieurs phenomenes interviennent dans la migration des contaminants qu'ils soient issus cTun site d'enfouissement sanitaire, d'effluents nuniers ou de catastrophes ecologiques. Ces phenomenes peuvent etre de nature physique, chimique, biologique et meme radioactive.
L'advection, la dispersion hydrodynamique (incluant la dififtision moleculaire) et la retention font
part! des principaux processus afifectant Ie transport des contaminants (Best et coll., 1993; Freeze
et Cherry, 1979).
2.1.1 L'advection
L'advection est la composante du mouvement d'un solute, d'un corps dissous comme par exemple un contaminant vehicule par ecoulement des eaux souterraines (Freeze et Cherry, 1979). Done, c'est Ie processus par lequel les contaminants sont transportes a travers les pores cTun sol sous FefFet d'un gradient hydraulique. Dans Ie cas de Fenfouissement sanitaire, les contaminants sont transports dans Ie lixiviat au travers de la barriere de protection, suite a une accumulation de
lixiviat au fond du site d'enfouissement induisant ainsi un gradient hydraulique. La Figure 2.1
ci-apres illustre Ie phenomene.v
Hauteur du lixiviat
IBalmere
i^^ Legende: q = taux d'mfiltration; K = conductivite hydraulique |du sol de la barriere;Selon Ie type de sol, Ie transport par advection peut ^tre Ie principal mecanisme
responsable du transport des contaminants. C'est Ie cas notamment des sols grossierement ou moyennement grenus, tels les sables et graviers qui constituent des aquiftres (unites geologiques permeables satures d'eau). Le taux d'infiltration par advection au travers d'une couche de sol estfonction de la conductivite hydraulique du sol "K" appelee couramment Ie coefificient de
permeabilite du sol (se referer a la Figure 2.1). La conductivite hydraulique peut etre definie
comme une mesure de la facilite qu'a un liquide (tel 1'eau) a s'ecouler librement dans Ie sol. A toutes fins utiles, la vitesse d'ecoulement dans Ie sol est directement proportionnelle au gradienthydraulique, tel que decrit par la loi de Darcy :
va K*i K^Bh _ . .. .
v = — = — —-— = ~ —"' —1- Equation 1: Loi
n n n
ou, v = vitesse d'ecoulement (average linear velocity) n = porosite du sol
va = vitesse de Darcy (specific discharge)
K = conductivite hydraulique
i = gradient hydraulique
h = charge hydraulique
x = distance dans la dkection de 1'ecoulement
2.1.2 La dispersion hydrodynamique
Au fur et a mesure que les contaminants sont transportes, ils ont tendance a se disperser. C'est ce qu'on appelle la dispersion hydrodynamique. Ce processus entraine une dilution des contaminants dans leur milieu, en partie a cause du brassage cause par la turbulence associee au
mouvement de Feau (dispersion mecanique) et en partie a cause du phenomene de la diffusion
moleculaire (Freeze et Cherry, 1979).
La dispersion mecanique est un processus microscopique qui est fonction du diametre et de la mgosite des pores du milieu, des diverses vitesses d'ecoulement des molecules voyageant dans
les pores du sol et de la tortuosite du milieu. La diffusion moleculaire se definit comme Ie
mouvement des contaminants dans les pores du sol suivant un gradient de concentration. C'est un processus irreversible. Dans les L.E.S. la difference entre la concentration du contaminant dans Ielixiviat et dans Peau des pores du sol sous-jacent a la barriere, produit un gradient de concentration. Ainsi, les contaminants migrent de la zone a forte concentration a la zone de faible
concentration (Quigley, 1995; Shackelford, 1991). La Figure 2.2 presente les trois conditions
d'ecoulement ou Ie phenomene de difiRision joue un role important dans Ie transport des
contaminants. Direction of Advectlva Flow I None Dlfctlon of DIHualon Leachate (c > 0) l^fi'a:MLfiJ [Natural Soil (c=0)l (a) Leachate (c > 0) lilU'MiLUjtlrU IRatural Soil (c=0)l (b) Leachate (c > 0) |»N'iB:J:U3LU I Natural Soil (c=0)t (c)Figure 2.2: Conditions d'ecoulement ou la difi&ision moleculaire joue un role important dans la
migration des contaminants a partir, par exemple d'un LES : a) DiflEusion sans advection (pas de
gradient hydraulique) ; b) Dififtision avec une advection positive (^coulement vers 1'exterieur du
LES) ; c) Diffusion avec une advection negative (cas cTun piege hydraulique) (figure adaptee de
Shackelford, 1989, 1991 b).
La dispersion des contaminants s'effectuant dans la direction de Fecoulement souterrain
est dite longitudinale. Celle qui s'effectue peq)endiculairement a cet ecoulement principal est
appelee dispersion transversale (Freeze et Cherry, 1979). Chacun des types de dispersion sont
presentes ci-apres.Representation du phenomene de dispersion
Le processus de dispersion longitudinale (c'est-a-dire dans une dimension) est communement illustre par une colonne de sol, sature d'eau a travers laquelle un traceur (par exemple: Ie chlorure) de concentration connue Co, est introduit (voir Figure 2.3-a). La concentration du traceur a 1'efiEluent (Ce) est mesuree a differents moments. Le profil de la
concentration relative (Ce/Co) versus Ie temps de lessivage du sol par Ie traceur definit la courbe
d'inflexion (breakthrough curve) telle que presentee a la Figure 2.3c).
Continuous supply of tracer at concentration Co after time to
v breakthrough, tg
Outflow with tracer at concentration C after time t
(a) (d)
Figure 2.3: Dispersion longitudinale : a) Concentration constante du traceur a 1'affluent; b)
Concentration relative C/Co du traceur a t= 0; c) Courbe d'inflexion du traceur en fonction du
temps de lessivage; d) Concentrations du traceur selon la distance pour differents temps (Figure
adaptee de Freeze et Cherry, 1979).
Si on admettait que Ie traceur puisse migrer au travers de la colonne sans se disperser, Ie
profil Ce/Co selon Ie temps de lessivage se resumerait a une verticale illustree en pointilles a la
Figure 2.3-c; ce qui reviendrait a af5rmer que la concentration du traceur dans Ie sol demeure nulle jusqu'a un certain moment ou, soudainement, sa concentration Ce a 1'effluent atteindrait la valeur Co mitialement introduite. En realite, on remarque un etalement de cette verticale de partet d'autre du point d'inflexion correspondant a la concentration relative de 50% (Ce/Co = 0.5).
Get etalement est du au phenomene de dispersion hydrodynamique. La courbe d'inflexion met en
evidence 1'apparition du traceur a Feffluent de la colonne a un temps inferieur a celui de la vitesse lineaire moyenne d'ecoulement de la solution aqueuse.
La Figure 2.3-d montre differentes courbes d'inflexion du traceur au fur et a mesure qu'il est transporte dans la colonne de sol. L'avancee du front du traceur devient de plus en plus etendue avec la distance parcoume (Freeze and Cherry, 1979).
Une dispersion a la fois longitudinale et transversale (en 2-D) implique que Ie traceur
(appelons-le: contaminant) une fois libere de sa source, se deplace suivant deux directions. La Figure 2.4 montre une dispersion en 2-D. L'avancee du front de contammation du traceur s'allonge dans Ie sens ou la migration est dominante, soit dans Ie sens de 1'ecoulement regional(Freeze et Cherry, 1979; Tchobanoglous et Shroeder, 1987; Best et coll., 1993).
Source du contaminant
Figure 2.4: Dispersion longitudinale et transversale.
2.1.2.1 Developpement de I'equation generale d'advection et de dispersion
Le developpement d'equations difFerentielles permettant de decrire Ie transport des
contaminants dans un milieu sature repose sur Ie prindpe de conservation de la masse. Lespiomiiers du developpement de 1) equation generale d'advection et de la dispersion sont Ogata
^1
F.+irdz ^^y
t-^""
•Fx+^dx<)x
->• x
Figure 2.5: Flux de masse d'un volume dans Fespace (Figure adaptee de Freeze et Cherry, 1979).
La concentration du contaminant C est definie comme la masse de contaminant par unite de volume de solution. La masse du contaminant par unite de volume de sol est done nC (n etant
la porosite du sol). De fa^on generale, on definit Ie transport par advection par la formule:
v n CdA Equation 2 : Transport par advection.
Pour Ie transport par dispersion, la fonnule est:
nD^dA
0X
Equation 3 : Transport par dispersion.Dans cette demiere, D est Ie coefBcient de dispersion selon F axe des x et dA, est un element de surface traversee par Ie contaminant.
L'equation 3 represente Ie cas ou la migration d'un contaminant est regit uniquement par un gradient de concentration. A partir de cette equation, on peut determiner Ie flux de masse F,
correspondant a la premiere lot de Pick:
F = nD
0C
ax
I fire
Equation 4; lere Loi de Pick.
ou D = Dm + De. Dans ce cas. Dm est Ie coef&cient de dispersion mecanique et De est Ie
coefficient de diffusion effectif. Le coefiEicient de dispersion mecanique est fonction de la
1979; Rowe, 1987). Le coefi&cient de dif&sion effectif , represente par De est Ie produit du
coefficient de diffusion d'un ion dans une solution a dilution mfinie, Do, et de la tortuosite du
milieu poreux, T, de telle sorte que De = Do T (Shackelford, 1991; Rowe, 1988). fl ressort de
cette demiere equation que la dififtision moleculaire sera ralentie entre autres, par une augmentation de la tortuosite .Le flux de masse dans la direction de 1'axe des x, Fx, egale la masse totale de contaminants transportes par unite de surface transversale et par unite de temps:
oc
F^ = v^ nC -n2)^ -^— Equation 5.
ffx
Le signe negatif place a Favant du terme de dispersion indique que les contaminants se deplacent
de la zone fortement concentr^e a celle faiblement concentree. De fa9on similaire, les flux de masse dans les directions des y et des z s'expriment ainsi:ffC _
F^=v^nC-nD^ — Equation 6.
ffy
0C ^
F^ = v.nC -nD^ — Equation 7.z 'z"~ -z 0Z
Le flux de masse des contaminants entrant dans 1'element cubique (voir Figure 2.5) est:
F^ dzdy + F' dxdz + F^ dxdy Equation 8.
Le flux de masse des contaminants sortant de 1'element cubique est:\F^^X-dx\dzdy^\F^^-\dxdz^\F^^Z-\dxdy Equation9.
x ' ffx ")"~ ~v \^~y ffy ) " "- ^- z ffz La difference entre Ie flux de masse entrant et sortant du volume cubique est alors:2 II est ^ noter que la nomenclaturc du coefi&dent de difi&ision efiGsctif vade souvent d'un auteur ^ I'autre.
Shackelford (1991-a), Gilham (1987) d6finissent Ie coeffident effectif comme 6tant D*. Dans ce m6moire, Ie coefi&cient de diffusion effectifest toujours pr6seat6 par D pour €tre confomie avec la nomenclature employee dans les logiciels utilises pour 1'analyse des r6sultats (Pollute v6 et Migrate v9)
' SFx , SFy . <9Fz) _,. _,. ,_ ^___^
-+— ^-—\dxdydz Equation 10.
ffx 6y ffz
En assumant que Ie type de contaminants en presence ne r6agit pas avec Ie milieu, alors la difference entre Ie flux entrant et Ie flux sortant egale la quantite de contaminants accumules dans Ie milieu. Suivant Ie principe de conservation de la masse, on a:
0Fx BFy SFz BC _,___,_„_, ^C OF „_ „
.+—4-——= -n—, qui se resume a ~^—= - — Equation 11. ffx ' By ' ffz -^.-z"-"-——- ^ ^
En reprenant la premiere loi de Pick et en y ajoutant 1'equation de conservation de la
masse, il devient alors possible de deriver une equation differentielle qui tienne compte de la
variation dans Ie temps et dans 1'espace de la concentration du contaminant difiusant dans Ie
milieu. I/ equation unidimensionnelle obtenue est appelee seconde loi de Pick:
0C ^02C „ , 12. at ^ axl
L'equation generale d'advection et de dispersion suivant une dimension peut ainsi etre deduite:
alc ac ac ^ ,
nD^ —— - nv—— = n— Equation 13.
x0Xi ^X 01
Dans les sols de faible conductivite hydraulique, la vitesse d'ecoulement 6tant faible, la
migration des contaminants est controlee principalement par la diffusion moleculaire (Barone et
al., 1988, Rowe et al, 1987, Desaulniers, 1981, Freeze and Cherry, 1979). Lorsqu'on etudie lamigration des contaminants dans les sols argileux, il est plus juste d'associer D au coefficient de
diffusion efifectifCRowe et aL, 1987).
2.1.3 Retention des contaminants
A cause des interactions entre les particules constituant les sols argileux des bameres et les contaminants du Ibdviat, les contaminants qui migrent peuvent etre retenus, ou capt6s, par les particules du sol. Dans un premier temps, Fadsorption des contaminants ainsi que d'autres processus de reaction sont presentes. Puis, la capacite d'attenuation sp6cifique aux sols argileux
est decrite. Enfin, 1'importance de la double couche diffiise vis-a-vis de 1'ecoulement des
2.1.3.1 Adsorption des con tam inan is et autres vrocessus de reaction
Les mineraux des argiles out la capacite de "filtrer Ie lixiviat" en Ie debarrassant de ces
contaminants (Yong, 1985). En efifet, les sols argileux ne sont pas inertes, ils influencent
1' accumulation et la mobilite des contaminants dits "non-conservateurs". Un contaminant (un ion et/ou un compose chimique) "non-conservateur" peut reagir avec Ie milieu dans lequel il se trouve selon divers processus de reaction. Sa migration au travers d'une couche de sol argileux est alors retardee. Les sulfates, les nitrates, les metaux lourds et plusieurs composes organiques font parti des especes reactives.Les divers processus de reaction a mtervenir entre Ie sol argileux et les contaminants sont
fonctions de deux aspects: les proprietes physico-chimiques du sol et les caracteristiques des
contaminants en contact avec Ie sol. Le type de mineraux argileux, les groupes fonctionnels (parexemple: les oxydes hyddques, la matiere organique). Ie pH du sol, les ions echangeables, Ie type
et la concentration de chaque contaminant, la composition et la quantity de mineraux amorphessont autant de facteurs influen^ant les processus de reaction (Yong, 1985). Les principaux
processus de retention des contammants se regroupent en six grandes classes: 1'adsorption, laprecipitation, 1'oxydoreduction, la formation de complexes, la biodegradation et la desint^gration
radioactive (Best et al, 1993, Yong, 1985). Le Tableau 2.1 resume les principaux processus de
retention.Tableau 2.1. Processus de retention (Best et coll., 1993, Yong, 1985) Processus:
(Adsorption/ desorption)
Pr6cipitation
Oxydoreduction
Formation de complexesBiodegradation
Desintegration radioactive
Breve description:Echanges d'ions entre la phase liquide du milieu
et la surface charg6e d'une particule du sol.
Accumulation (Tune substance sur les particulesargileuses donnant lieu a un nouveau solide soluble. Transfert d'electrons d*un ion a 1'autre.
Reaction d'un ion metallique avec un ligand:
OH-, C1-, S042",
CN-Destruction d'une substance par Faction bactenologique. Transformation spontanee d'une substance avec
Les processus cToxydoreduction et de formation de complexes sont presentes de fayon succincte. Une plus grande importance est accordee aux processus d'adsoq)tion/ desorption et de
precipitation puisque ce sont principalement ces processus qui prennent place lors des essais
exp6rimentaux de cette presente recherche.Breve explication des processus d'oxydoreduction et de formation de complexes
Les reactions d'oxydoreduction impliquent que les constituants reduits du lixiviat (de la
solution polluee) agissent comme donneurs d'electrons en se fixant aux constituants du sol (par exemple 1'oxygene, les nitrates, les oxydes de Fe3 et Mn4) qui les re^oivent (Heron et coll., 1991). Ainsi les contaminants sont fixes a la surface des particules du sol.D'autre part, la reaction entre un ion metallique, (par exemple, Ie Pb2+) et un ligand (molecule ou ion uni a 1'atome central d'un complexe par une liaison de coordination) tels OH~, Cl", S04 et CN~, engendre la formation de complexes. La reaction entre un ion metallique et au mains deux ligands, donne lieu a une chelation. La formation de complexes et la chelation stabilisent la solution Uxiviatee la rendant mains nocive pour 1'environnement.
Description du processus d'adsorption et de desorption
Parmi les processus de retention, Ie phenomene d'adsorption/ desorption en est un des plus unportants. L'adsorption peut etre definie comme etant Ie partage d'une substance (par exemple
un contaminant) entre la phase liquide et la phase solide du sol (Yong et aL, 1992). La
distribution du contaminant entre chacune des phases liquides et solides du sol s'exprime par un
coefficient de distribution Kd, caracteristique d'une substance ionique pour un milieu donne.
Exp6rimentalement, Ie coefficient de distribution est couramment determine a partir de tests
appeles "Batch Equilibrum Tests (BET)" (Shackelford, 1991a). Altemativement, U peut ^tre
determine par des tests de lessivage ou de diffusion (Barone, 1993 ; Yong et coll., 1992).
Toutefois, cette demi^re technique sera exposee au chapitre de la determination des coefificients
de diffusion efifectifs (chapitre 6). Pour les BET, Ie sol sec et la solution contenant un solute
donne (par exemple: une solution de NaCl pour determiner Ie Kd Na+ ) sont melanges dans unrapport de 1/10, puis centrifuges. Apres analyse du sumageant, les quantites du salute adsorbee
par unite de masse de sol sec (S) et dans la solution en 6quilibre (C) sont determinees.
L'isotherme d'adsoqrtion obtenu est regit par la relation S == Ka C (n egale une constante) (Yong
et coll., 1992). Si on considere les reactions d'adsoq)tion rapides par rapport a la vitesse
d'ecoulement de la solution contaminee (par exemple Ie lixiviat), une variation de la quantite de
salutes adsorb6s par unit6 de sol sec dans Ie temps est egale a:
0S _[0S\^ffC ^_^
* — Equation 14.0t \0C) 01
ou, I —— I = Kd (n etant egale a 1; 1'isothemie d'adsorption est represente par une droite passant .^c
par 1'origine). Bien que les BET soient simples et rapides a faire. Ie fait qu'ils impliquent la
dilution d'un sol en suspension fait en sorte de ne pas toujours refleter la realite (Yong and Cabral,
1992). En multipliant Ie produit '- a chacun des temies de 1'equation precedente, on definit Ien
terme de retention:p ,SS _ p ,0S ,ffC
* "L" — /L1 * Equation 15 : Terme de retention.n St n 0C St
L? equation generale d'advection-dispersion devient 1'equation d'advection -dispersion -retention pour certains composes chimiques reactifs :
^C _0C ,{0p0S\ 0C ^_^
D^— - v— +| —r— | = — Equation 16.
'x ^ T ffx \ n 0t) ~ fft
Un rearrangement de cette equation permet d'isoler Ie facteur de retardement:
a'lc ffc ac[^p 8s\ ^_^
£)x^i- - v^ = ^ 11+5 -i^ I Equation 17.
ffx^ ffx St \^ n
Le facteur de retardement Rd (sans dimension) 6gale done : (1 + pK<i / n). Ce facteur traduit Ie taux
d'avancement d'une substance chimique non reactive (non adsorbee) tel Ie d', par rapport a une substance chimique reactive sujette a un processus de retention. Les substances non retard6es ontun facteur de retardement. Rd, egale a 1 (Shackelford, 1991).
Les pnncipaux facteurs qui influencent la capacite d'adsorption d'un sol pour un
contaminant donn6 sont: la composition du sol. Ie type de liaisons ioniques des constituants du
sol, les groupes fonctionnels , Ie pH du sol, la capacite d'echange cationique (C.E.C.), la surface specifique (S.S.A.), Ie potentiel zeta, la valence et la concentration du contaminant et finalement, la temperature (Yong, 1985, Best et coll., 1993).
La capacite d'echange cationique, generalement exprimee en milliequivalent par lOOg de
sol, correspond a la quantite d'ions presents dans la zone adjacente k la surface de la particule de
sol (dans la double couche) et pouvant etre echanges a d'autres cations (Freeze and Cherry,
1979). Autrement dit, la C.E.C. est la quantite de cations echangeables necessaire pour balancerIe manque de charges d'une particule argileuse (chargee negativement). La surface specifique
(m2/g), caracteristique propre a chaque sol, renseigne sur la taille des particules d'un sol. En effet,elle est inversement proportionnelle a la taille des particules minerales du sol. Sachant que les
contaminants (cations) en solution sont toujours hydrates, il y aura consecutivement plus de
surfaces chargees negativement dans Ie sol qui engendreront des mteractions entre Ie sol et les contaminants plus nombreuses. Par consequent, il y aura done plus de molecules d'eau retenues par Ie sol. Ainsi, plus la surface specifique d'un sol est elevee, plus la quantite de contaminants retenus a Finterieur du sol sera grande.A partir des valeurs de la C.E.C et de la S.S.A, propres a chaque sol argileux, la densite de charges disponibles, a, peut etre determinee. Le rapport de la capacite d'echange cationique sur la surface specifique (o == - C.E.C/ S.S.A) correspond a la density de charges. Selon Yong et
Warkentin (1987), la connaissance de la densite de charges constitue une bonne approximation de
la capacite d'adsorption d'un sol argileux.L'adsorption d'un ion en solution peut se faire & differeates intensites selon la nature des
forces d'interactions entre 1'ion en solution et la particule chargee. L*adsorption est de nature physique lorsque les forces d'interactions sont electrostatiques. Dans ce cas, la reaction cTadsorption est rapide et reversible, c'est-a-dire que Ie solute adsorbe, retenu par la particuleLes groupes fonctioimels sont les parties chimiquement actives b la surface du sol et du contaminant (Cabral, 1995). Selon Sposito (1984), les groupes hydroxyles (de type OH) sont les groupes fonctionnels dominants pour les
chargee du sol argileux peut etre desorbe, relache au profit d'un autre ion de valence plus importante (Yong et al., 1992). Par exemple un ion Na+, adsorbe peut etre libere dans Feau des
pores du sol au profit de 1'adsorption d'un autre ion par exemple. Ie Pb . L'adsorption est dite
specifique lorsque les forces d'interactions sont electromagnetiques en plus d'etre electrostatiques.L'adsorption specifique est un type d'adsorption d'une affinite relativement plus forte que
Fadsorption physique. L'adsorption est de type chimique lorsque les forces d'interactions sont
associees a des energies d'activation plus importantes. L'adsorption chimique est un type(Tadsorption de tres haute afifinite (Yong et coll., 1992; Cabral, 1995).
Selon Ie modele de Stem-Gouy qui decrit la distribution des ions dans la zone adjacente a
la surface de Fargile (concept explique au chapitre 2.1.3.3), les adsorptions de type physique ont
lieu dans la couche de Gouy. Les adsorptions de type specifique se retrouvent a la fronti^re des
couches de Stem et de Gouy. Quant aux adsorptions de type chimique, de tres haute affinite, on
les retrouve seulement dans la partie inteneure de la couche de Stem, plus ou moins "imbdquees"par les groupes hydroxyles de la particule d'argile (Shang et coll., 1994). Autrement dit, plus la
distance entre 1'ion et la surface de la particule cTargile duninue, plus les forces d'interactions sont
fortes.Description du processus de precipitation
Le processus de precipitation (I'inverse de la dissolution) implique 1'accumulation d'un
solut6 sur les particules argileuses donnant lieu a un nouveau solide soluble. Le processus se passe en deux etapes: d'abord la nucleation, puis la croissance de la particule. Le pH du sol et de 1'eaudes pores du sol et la concentration du solute sont les principaux facteurs du controle de la
precipitation (Galvez, 1989; Yong et coll., 1992). La Figure 2.6 illustre la solubilite d'un compose
hydroxyde de metal (tel Ie PbOI^) selon la valeur du pH. Des concentrations elevees de solutes
sont necessaires pour qu'il y ait pr6cipitation dans Feau des pores parce que Ie processus exigeque soit depasse Ie produit de solubilite. II est a noter que la precipitation est I'un des principaux
processus de retention des metaux lourds.I
<n u8
•3 id pfdpltafdPb(OH)s ^
pHo PH p^>Figure 2.6. Solubilite (Tun hydroxyde d'un metal en fonction de la valeur du pH (Figure tiree de
Galvez, 1989).
2.1.3.2 Cavacite d'attenuation des sols arsileux
Les sols a grains fins ont, contrairement aux sols granuleux, la capacite de capter et de retenir les contaminants inorganiques et certains organiques, les empechant ainsi de se propager. Les processus d'interactions entre les contaminants et les constituants du sol peuvent donner une accumulation de contaminants dans Ie sol (Yong et al., 1992). Cependant, il faut savoir que ces sols ne peuvent pas retenir completement et indefiniment les contaminants en solution car il y a epuisement de la capacite d'attenuation du sol.
La capacite d'att6nuation ou "buffering capacity" des contaminants par les sols argileux
est directement liee a la capacity des materiaux contenus dans ces sols, a tamponner les contaminants (Yong et Cabral, 1992). Comme il a ete vu au paragraphe 2.1.3.1, plus la surfacespecifique cTun sol est grande, plus la capacity de retention du sol est importante.
Les mecanismes impliques lors du tamponnement des contaminants ne dependent pas uniquement du type des argilo-mmeraux, de la presence de carbonates et de matiere organique, mais dependent aussi des caract6ristiques physico-chimiques des contaminants en presence. L'action de I* ensemble des mecanismes suscites (adsorption, precipitation, complexation etc.) lors
du passage des contaminants dans les sols argileux sont tres complexes et r^sultent toujours par
des changements de la capacity d'attenuation des sols (Yong et Warkentin, 1987). Selon 1'avis de
ces auteurs, la capacite (Tattenuation devrait ^tre un des aspects prepond6rants a considerer dans 1'evaluation des barrieres de protection dans les sites d'enfouissement. Leur point de vue s'appuiesur Ie fait que la capacite d'attenuation ou "buffering capacity" refere au changement de
concentration des contaminants en solution apres interaction avec Ie sol, alors que la capacite d'adsorption (au sens large) w carrying capacity" refere exclusivement aux processus d'adsorption et de retention par Ie sol. La performance (Tune barriere de protection est evaluee par les niveaux de concentrations des substances dans Ie Uxiviat recueilli a la sortie du site d'enfouissement.II importe done de se demander a quel moment la capacite tampon des sols sera 6puisee. En (Tautres termes, quand est-ce que les contaminants ne pourront plus etre retenus par les sols ? La valeur de la densite de charges, a, donne une bonne approximation de la capacite d'attenuation du systeme en autant qu'on admette que les charges variables des surfaces du mineral peuvent etre
influencees par Ie pH du systeme (Yong et Warkentin, 1987).
Un sol sera tres attenuateur s'il montre une forte resistance aux changements de pH, lors du passage de solutions contamin^es fortement addes ou basiques. Ces sols ont un contenu eleve
en matiere organique et selon Yong (1985), les sols organiques constituent d'excellents agents de
chelation en presence d'ions m^talliques.
Un autre facteur a considerer dans revaluation des depots naturels comme barrieres
hydrog6ologiques a la contamination dans les sites d'enfouissement, est Finfluence de la double
couche diffuse propre aux min6raux des argiles. Ce sujet sera discute par la suite.
2.1.3.3 L'importance de la double couche diffuse
La particule cTargile de surface negative interagit avec les electrolytes (cations et anions)
contenus dans 1'eau des pores pour g^nerer une double couche dififtise. La Figure 2.7 illustreschematiquement les interactions entre une particule d'argile charg6e n^gativement et 1'eau des
pores du sol. La surface chargee negativement de la particule d'argile attire une premiere rangee
de charges positives (cations hydrates) (Yong et coll., 1992).
Negatively charged clay pantote
Gallon
Electric double layer (EDL)
SkJevtewof parttete
^•+
+t++
^+
+,+
.«T+-+-+++
u<-_t Diffuse ton-layer (DL)Figure 2.7 : Interactions entre les ions de 1'eau des pores du sol et une particule d'argile (Figure tiree de Yong et coll., 1992).
Selon Mitchell (1976), la double couche diffiise d'une particule argileuse est la region qui
englobe la surface chargee negative de 1'argile et la distribution des ions adjacents a celle-ci.
Plusieurs modeles (Hehnoltz-Perrin, Gouy-Chapman, Stem-Gouy, etc.) ont ete proposes pourdecrire la distribution des ions adjacents aux surfaces charges de collol'des (particules argileuses).
Parmi ces modeles, celui de Stem-Gouy s'est avere d'une importance fondamentale dans 1'etudede la conductivite hydraulique des sols argileux naturels lorsque lessives par des contammants
(Quigley et coll., 1987).
Dans Ie modele de Stem-Gouy, la double couche consiste en une couche inteme (couche
de Stem) et une couche exteme (couche de Gouy). La couche de Stem est compos6e de dipfiles
orientes vers la surface de la particule argileuse. La couche de Gouy est constitute
principalement de cations hydrat^s (retenus par des forces 61ectrostatiques) en equilibre avec la
presence cTune diffusion mol^culaire vers 1'exterieur de la double couche. La Figure 2.8repr6sente Ie modele de la double couche diffuse selon Stem-Gouy (non a l^chelle). L'epaisseur
de la couche de Stem 6tant tres mince, on considere l'6paisseur de la double couche 6gale ^
F6paisseur de la couche de Gouy (Shang et coll., 1994).
(a
^
T3
Q
/.
) Couche de Stem (o.6nm)
Surface cxtonc dc la couchc de Stem
• ^;—.—-;
T !+ + + + +t f-'. '
I \- + + . *i^ +
Couche de Gouytt\+
tttN
Ugne de partage (poteatiel Zet*)
Distance p/r ^ la surface de Fargile
Potentiel Zeta Potentiel de Stem
Potentiel de surface
Figure 2.8 : Modele theorique de Stem-Gouy : a) Distribution des ions selon la distance.
^Distribution du potentiel electrique selon la distance (Figure adaptee de Shang et coll., 1994).
La Figure 2.8 b) montre que Ie potentiel electnque de la particule argileuse diminue avec la
distance, lineairement dans la couche de Stem et exponentiellement dans la couche de Gouy. Ladistribution du potentiel electrique et 1'epaisseur de la double couche sont directement influences
par la densite de charges de surface du type d'argiles, par la concentration des electrolytes, par la
valence des electrolytes, par Ie pH du milieu et par la constante dielectrique du solvant dans Ie sol
argileux. Chacun de ces facteurs a une influence sur la conductivite hydraulique (Quigley, 1993,
Shang, 1994).
Une augmentation de la concentration des electrolytes entraine une diminution du potentiel
electrique qui entraine a son tour une diminution de 1'epaisseur de la double couche. Lorsque la double couche diffuse s'ecrase, la structure des particules d'argile devient floculee. U s'ensuit uneaugmentation de la conductivit^ hydraulique du sol et de la dispersion mecanique.
Consequemment, les fluides tels les lixiviats des L.E.S. peuvent percoler au travers Ie sol.Les electrolytes (cations) ayant une valence plus forte s'approchent plus pres de la surface
de 1'argile (Shang, 1994). L'epaisseur de la double couche ainsi affectee, est r^duite. Le lessivage
d'un sol argileux par un fluide de faible constante dielectrique entrainera aussi un retrecissement
de la double couche diffiise. De la meme fa?on, une variation a la baisse du pH affecte Ie
comportement des sols argileux en engendrant une tendance a la floculation des particules d'argile.La double couche diffuse a done une influence notable sur Ie comportement des sols argileux et
incidemment sur Ie transport des contaminants (Quigley, 1993; Shang, 1994; Cabral, 1995).
2.2 Importance de Pavancee du front de contamination par
diffusion moleculaire
Dans la pratique courante des annees 70, les sites d'enfouissement en Ontario etaient amenag^s dans des depots naturels de sols argileux. On croyait amsi contraindre la migration des
contammants en raison du caractere " impermeable " des sols argileux (Goodall et Quigley, 1977).
Les donnees rapportees de quelques sites etudies, comme celui de "Confederation Road" de la region de Samia (Ontario) ont permis d'evaluer 1'etat de la contamination. L'analyse des contaminants a demontre que la contamination s'est effectuee sur une plus grande distance quecelle initialement calculee avec la valeur de la conducdvite hydraulique du sol argileux utilise a
cause de la diffusion moleculaire (Quigley et Rowe, 1986; Crooks et Quigley, 1984; Goodall et
Quigley, 1977).
Afin de montrer 1'importance de l'avanc6e du front de contamination par diffusion
mol^culaire, ki Figure 2.9 illustre les profils de la contamination respecdvement par advecdon et
par difi&ision moleculaire.
Concentration du contaminant
Profondeur
dans la
barriere
tl
t2
t3
Front de contamination par advection; Front de contaminationpar diffusion.
tl t2 t3
Figure 2.9. Profits typiques de contamination par advection et dijffusion moleculaire.
Pour une meme penode de temps, par exemple au temps tl, Ie front de contamination par difiEusion moleculaire a parcoum une plus grande distance en profondeur comparativement au front de contamination par advection. Au fur et a mesure que Ie temps passe, prenons par exemple a t3, la dififusion de la contamination dans Ie sol sous-jacent atteint des niveaux de concentrations de plus en plus importants. A un moment donne, la migration des contaminants dans Ie sol par difiEusion moleculaire pourrait attemdre, voir depasser les normes permises. Dans les sols de faible conductivite hydraulique, 1'avancee du fi-ont de contamination avance beaucoup plus rapidement par difRision moleculaire que par advection seulement. II est done necessaire de se pr^occuper du
transport des contaminants par diffusion moleculaire dans les calculs de Fepaisseur de la couche
protectnce amenagee au fond et Ie long des parois d'un LES. (Crooks et Quigley, 1984;
Shackelford, 1989; Barone et coll., 1988; Barone, 1993).
2.3 Gas historiques (Love Canal, Keele Valley, Confederation Road)
La preoccupation des legislateurs et autres intervenants ayant trait a la migration des
contaminants dans les sols est relativement recente. Certains cas problematiques, comme celui deLove Canal (Ontario) ont ete tres mediatis6s et ont contribue a 1'avancement des connaissances du
comportement des sols lors de la migration des contaminants. Apres une breve description du casde Love Canal, 1'impact de la contamination des sites cTenfouissement de Confederation Road
(Samia, On.) et de Keele Valley (Toronto, On.) est presente.
Parmi les cas d'intoxication associes a 1'enfouissement de dechets chimiques, celui de Love
Canal est Ie plus connu du public. Love Canal devait etre a 1'origine (vers 1890) un canal d'une
longueur de 10 Km devant servir au developpement hydroelectrique des chutes Niagara. Alors
que 900 m etait excave, Ie projet a du etre abandonne. Entre 1942 et 1953, plus de 22 000 tonnes
de substances chimiques ont 6te enfouies dans ce canal. Ce n'est qu'au debut des annees 1976 queles residents de la region ont commence a respirer des odeurs chimiques et i souffrir de divers
malaises. Mais Ie pire etait a venir puisque trois autres au'es d'enfouissement situees non loin deLove Canal avaient re^u a la meme epoque plus de 343 000 tonnes de dechets chimiques. Le tolle
qui s'en suivit a non seulement suscite Pinteret du public sur les dangers de la contammation des sols, mais a aussi fait avancer les recherches afin de determiner les facteurs-cles du controle de lamigration des contaminants (Rowe, 1993).
Le site de Confederation Road pres de Samia en Ontario, construit en 1971, a fait 1'objet
de plusieurs etudes pour evaluer les parametres de contr61e de la migration des contaminants et enmodeliser leur transport dans Ie temps. Confederation Road, c'est 7,0 m de d^chets solides (dont
5,5 m enfouis) recouverts d'une couche d'argile de 0,5 m d'epaisseur. Le sol sous-jacent estconstitu^ d'un d^pot d'argile silteuse grise massive et homogene, ayant une conductivit6
hydraulique inf6rieure a 1x10 cm/s (Quigley et coll., 1977). Les principales proprietes
physico-chimiques sont resumees au Tableau 2.2. L'616vation de la nappe d'eau se situe a environ 1,0 mde profondeur a partir du niveau naturel du terrain (Quigley et Rowe, 1986).
U extraction et Fanalyse de Feau des pores de quelques 6chantillons preleves a l'int6rieur
du site ont permis d'obtenir les profils de la migration des contaminants. La Figure 2.10 montre
les profils du Na et du d' en fonction de la profondeur pour une p^riode de temps de 6 et 12 ans
de meme que les fronts d'^coulement (d'advection) estimes pour 12 et 100 ans.
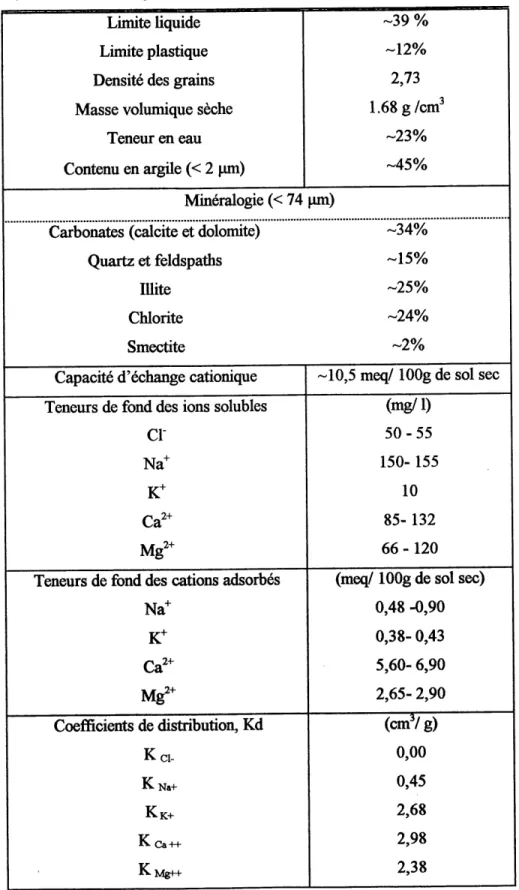
Tableau 2.2 : Propnetes physico-chimiques de 1'argile silteuse ; site de Samia (d'apres et Barone
et coll., 1988 ; Crooks and Quigley, 1984).
Limite liquide
Limite plastique
Densite des grains Masse volumique secheTeneur en eau Contenu en argile (< 2 pm) -39 % -12% 2,73 1.68 g/cm3 -23% -45%
Mineralogie (< 74 ^un)
Carbonates (calcite et dolomite) -34% Quartz et feldspaths ~ 15%
lUite -25%
Chlorite -24%
Smectite -2% Capacite d'echange cationiqueTeneurs de fond des ions solubles
a
Na+
K+
Ca2+
Mg2+
Teneurs de fond des cations adsorbes Na+ K+ Ca2+
Mg"
Coefficients de distribution, Kd
KCI-K.Na+ K.K+ KCS++ Mg^-10,5 meq/ lOOg de sol sec
(mg/1)
50-55 150-15510
85- 132 66 - 120(meq/ lOOg de sol sec)
0,48 -0,90 0,38- 0,43 5,60- 6,90 2,65- 2,90
(cm3/g)
0,00 0,45 2,68 2,98 2,38CONCENTRATION (mg /L)
0 200 400 600 800 1000 1200 1400
Ldj°
CL LUi i
I.
UJm
?3
a.@
a
I 1Tk SOLID
? WASTE
TI I~ II I I I2888^]
Na+ RANGE at t« 6a —rrr,:^
Na+at t« 12a ^////^//y/^////^/^/y^y^/y' / ^ ^ / / y^-^
' ^ / ^ ^ ^ ^7 / / / / / ^LEGEND
/QS1
t « 12a t • 100 aESTIMATED SEEPAGE
FRONT
Na+. t • 6a Na+«, t » 12am cr. T «i2a
Figure 2.10 : Concentration de 1'eau des pores enNa et CF dans Ie depot cTargile sous les dechets
(t = 6 et 12 ans) (Figure tiree de Quigley et Rowe, 1986).
Apres 12 ans d'exposition a la percolation du Uxiviat sur Ie site du depotoir, la migration
de ces contaminants s'est faite sur une distance de 1,5 m a2,0 men 12 ans comparativement a unedistance initialement estim6e b 3 a 4 cm pour Ie front cTecoulement par advection. Ceci vient
confirmer Ie r61e significatifde la diflEusion moleculaire dans la migration des substances chimiques
(Quigley, 1992 ; Quigley et Rowe, 1986 ; GoodaU et Quigley, 1977).
Le site d'enfouissement de Keele Valley, situe a Maple (10 Km au nord de Toronto,
Ontario), a aussi et6 invesdgu6. Ce site est am6nage sur une couche de sable de 30 cm sus-jacentea une couche de sol argileux compacte (till glaciaire) de 1,2 m d'epais. La conductivite
hydraulique du till est consider^e inf6rieure k 1x10 cm/s (Reades and Thompson, 1984). Le sol
argileux utilise pour 'am6nagement du site de Keele Valley provient des formations d'Avondale
ou Fon distingue deux horizons ; un alt6re et I'autre, intact. Le Tableau 2.3 presente quelques unedes propnetes physico- chimiques disponibles sur les sol argUeux d'Avondale.
Tableau 2.3 : Composition min6ralogique et limites cTAtterberg des sols d'Avondale constituant
la couche de sol compacte au site de Keele Valley (d'apres King et coll., 1992).
Limite Uquide
Limite plastiquehidice de plasticite
Contenu en argile (< 2 pm)Mineralogie (< 74 pm)
Carbonates QuartzFeldspaAs
Ulite
Vermiculite - SmectiteChlorite
25%
15%
10%
25%
Horizon altere29%
25%
23%
14%
7%
2%
Horizon intacte39%
16%
22%
13%
2%
8%
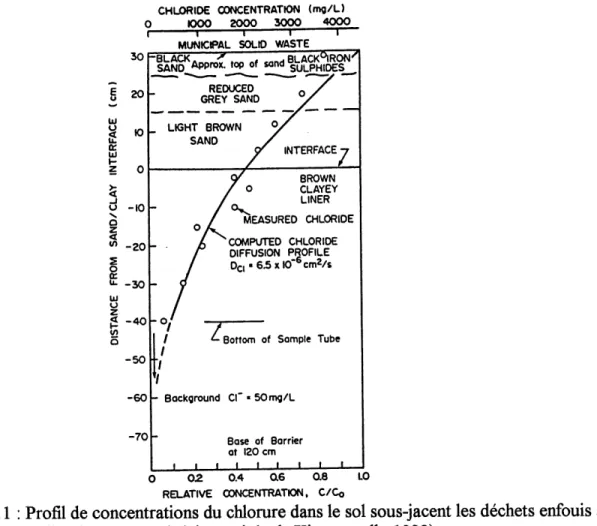
Les profits de diffusion du chlomre et de certains cations sont illustres a la Figure 2.11 et a la Figure 2.12. Pour une periode de 4,25 annees, la diffusion du chlomre s'est faite sur une
distance de plus de 70 cm a partir du sommet de la couche de sable.
A la Figure 2.12, on peut voir que Ie Na+ a migre sur une distance de 65 cm partant du sommet de la couche de sable. Le Na est legerement retard^ par 1'adsorption dans la couche
cTargile. Le K a ete fortement retarde par adsoq)tion dans Ie sol argileux car sa distance de
migration dans cette couche n'a ete que de 5 cm . Le profil de diffiision du Ca2+ est cambre sur
toute la profondeur 6tudiee. Cette cambrure, appelee "halo de durete" (hcsrdness halo) est
produite par la d^sorption du Ca2+ qui accompagne 1'adsorption des cations Na+ et K+ et
possiblement de Wb+ et de Mg2+ (Quigley, 1992 ; King et coll., 1992).
30 20 10
CHLDRIOE CONCENTRATION (mg/L) 0 1000 2000 SOOO 4000
MUNICIPAL SOLID WASTE
'5 0 0 -K) "s a tn -20 -30 -40 -50 -60 -70 I^App^topofsond^i?^^^ REDUCED GREY SAND LKSHT BROWN SAND INTERFACE BROWN CLAYEY °^__ __. UNER_ MEASURED CHLORIDE COMPUTED CHLORIOE OIFRJSION P80FILE Oci-65xl0'6cm2/s -0
7
Bottom of Sample Tube - Background Cl~ * 50mg/LBase of Barrier at 120cm
1111
0 02. 0.4 06 08 LO RELATIVE OONCENTRATK3N, C/Co
Figure 2.11: Profil de concentrations du chlomre dans Ie sol sous-jacent les dechets enfouis au
site de Keele Valley (t = 4,25 ans) (Figure tiree de King et coll., 1992).
CATIOW CtWCENTRATIOH (•a/L) 500 1000 1500
>
•+/
f IHUNICIPAL SOLID WASTE
Approx. top of **nd ^ Ih'Shelby tube 12-1 -Hgw. [~a /A. / •^ ^ SAND /'>^((.+ a* A| /•
~w
/ • INTERFACE.i!_/_
~Y~7~
^<-N.+ H8++./A .. "'
! \ ^- c*++ I yf LE6EKO / • K*+^
+ C.++ f ..._^ 0 N«++ Bottom of •Shelby tube f2-ZJ_I_L
500 1000 1500 2000 CATION COKCOmUTION (•g/L)3. METHODOLOGIE DES ESSAIS
Les essais de difiEusion pure et de lessivage ont ete realises avec des echantillons de deux
sols argileux typiques de la mer de Champlain, soit 1'argile silteuse de Ste-Adelphe et Fargile de
St-Hyacinthe. Comme il en a ete discute prec^demment, la migration des contaminants (composeschimiques) depend a la fois du type de contaminants et des propriety physico-chimiques du sol.
Ainsi, dans un premier temps, la caractensation de ces deux argiles est presence.Dans un second temps, les pdncipales ^tapes des essais de dififiision pure et des essais de
lessivage sont exposees. Les methodes d'extracdon des ions solubles et des cations adsorbes desechantillons des cellules de difi&ision et de lessivage sont bnevement d^cntes. Les analyses
chimiques des cations et de 1'ion chlomre sont par la suite presentees. Finalement, ladetermination des coefi&cients de difEusion effectifs du CF et du Na (principaux composes
etudies), a partir de leurs profils des concentrations dans Ie reservoir source et dans Feau des pores est exposee. La Figure 3.1 resume sommairement les principales etapes de la phaseexperimentale de cette recherche. Des schemas plus detailles de 1'execution des essais de diffasion
pure et de lessivage sont presentes ulterieurement dans ce chapitre.lll(3ixi^itiiaioiiidesii|8<(^
|||||^SLt|g||l|e|de|Ste|^detp^
l||||g^|(^|SfiK|5^^
y
FPropri6t6s physico-chimiques : - Density relative des grains ;
- Masse volumique du sol sec; - Teneur en eau naturelle ;
- Pression de pr^consolidation;
- Degr6 de saturation; - Porosit6 du sol; - pH du sol;
- Limites d'Atterberg;
- Composition min6ralogique qualitative;
- Teneurs de fond des ions solubles; - Teneurs de fond des cadns adsorb^s;
- Surface sp^cifique (SSA);
- Capacity d'6changes cationiques (CEC) ; - Coeffident de distribution du Na ; - Coefficient de distribution du Pb2+;
lilslsalsli^ldlliltQ^a^ix^i
-L
||||Es!^||d&|di|ffiigi|oa||^
^rr Argile de Stc-AdeIphc:- Essai avec Ie NaCl (n°2,no4etn°6); - Essai avec KC1 (essai n° 3); - Essai avec PbClz (essai n° 7). Argile de St-Hyacinthe:
- Essai avec NaCl (essai n° 9).
J-||||]iSigajis||(ie||l^si|vage|||||
ITr Argile de Ste-Adelphe: - Lessivage de Ix, 2x, 3x et 5x Ie volume des pores (essai n° 8); - Reprise du lessivage de Ix et 2x Ie volume des pores (essai n° 10).Figure 3.1 : Schema du programme experimental de cette recherche.