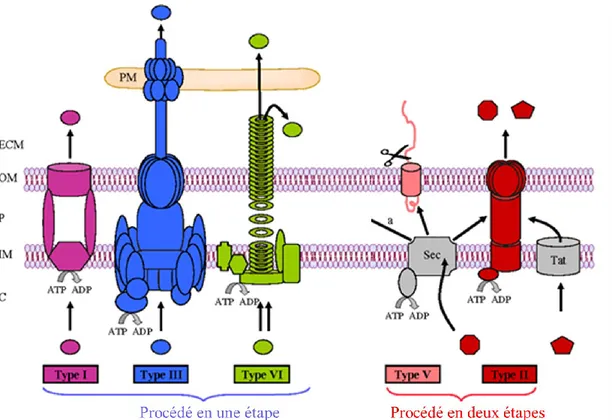
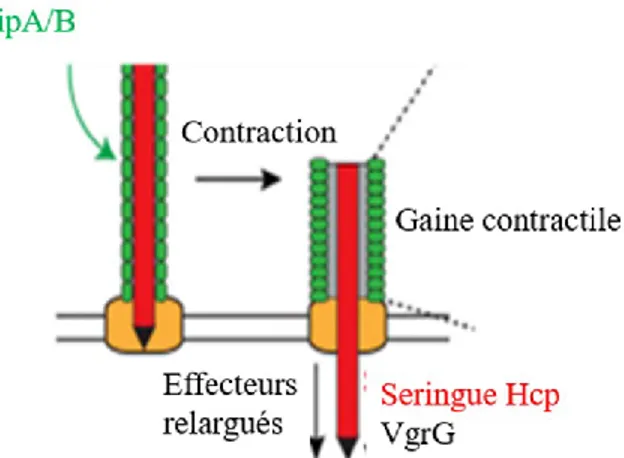
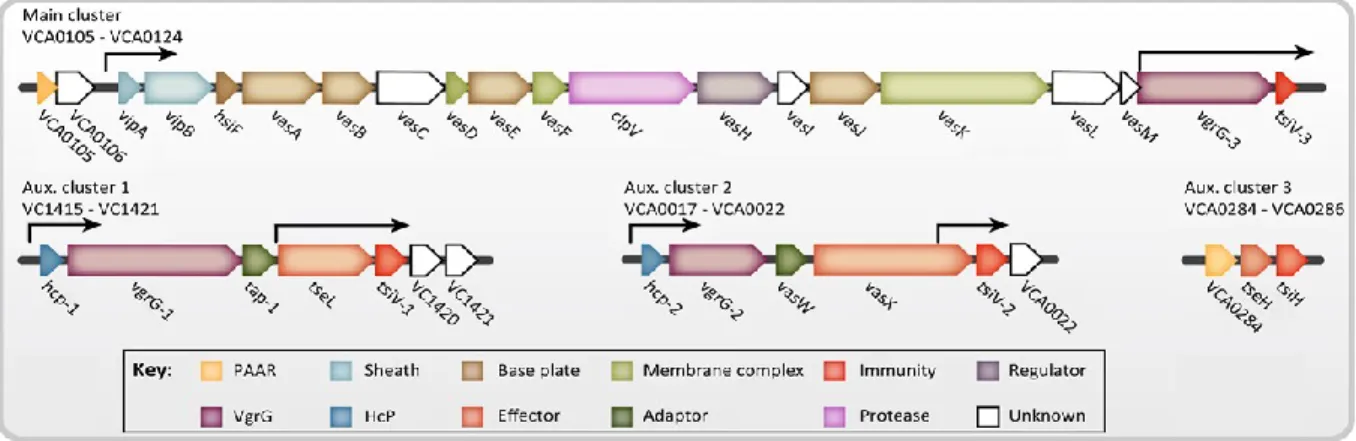
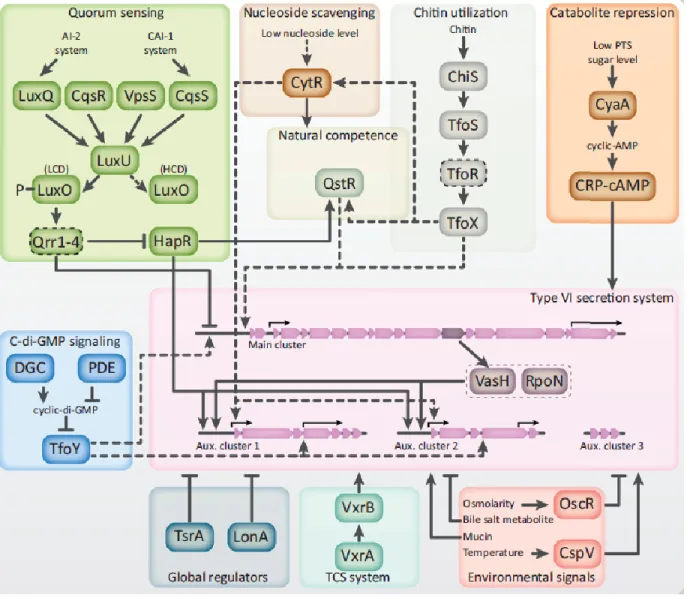
L'étude des antimicrobiens comme modulateurs du système de sécrétion de type VI de vibrio cholerae
Texte intégral
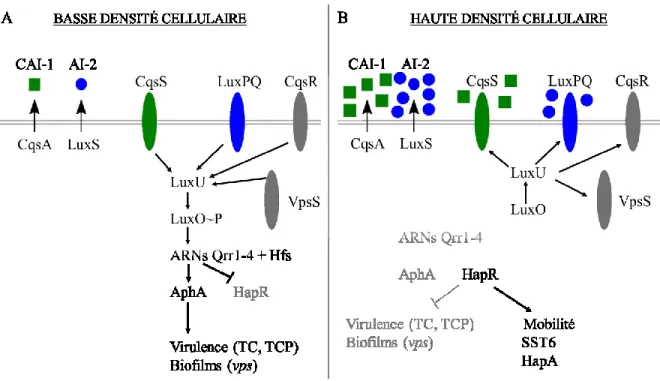
Figure



Documents relatifs
Et l’on verra effectivement, chemin faisant, que des deux réponses classi- quement avancées pour justifier l’étude de l’histoire médiévale en arguant de son
the complicated expressions of the cost functionals it is difficult to use an analytical approach for the development of an optimized algorithm for the whole roundabout. For
Anarchie et cohésion sociale chez les Toubou : les Daza Kécherda (Niger), Cambridge University Press/ Editions de la Maison des sciences de l’Homme, pp.11-79, 1985,
L’archive ouverte pluridisciplinaire HAL, est destinée au dépôt et à la diffusion de documents scientifiques de niveau recherche, publiés ou non, émanant des
It will be shown that the scale factor errors depends on the knowledge of the lever arm from the CG of the shuttle to the location of the accelerometers in
04 ZOUAIMIA Rachid, Les Autorité administratives indépendantes et la régulation économique en Algérie, Editions @ et distribution @ , Houma,
The transport properties are similar in the Weyl and gapped cases at high values of Fermi energy. For energies lower than the band gap, only the Weyl phase has a finite
51 On pourrait même supposer que l'auteur aurait pu avoir un projet d'introduire l'enseignement du russe pour les élèves des écoles centrales, parce que l’enseignement de la