HAL Id: dumas-01817673
https://dumas.ccsd.cnrs.fr/dumas-01817673
Submitted on 18 Jun 2018HAL is a multi-disciplinary open access archive for the deposit and dissemination of sci-entific research documents, whether they are pub-lished or not. The documents may come from teaching and research institutions in France or abroad, or from public or private research centers.
L’archive ouverte pluridisciplinaire HAL, est destinée au dépôt et à la diffusion de documents scientifiques de niveau recherche, publiés ou non, émanant des établissements d’enseignement et de recherche français ou étrangers, des laboratoires publics ou privés.
transfusionnel : expérience du CHU de Grenoble
Laurence Mège
To cite this version:
Laurence Mège. Application des concepts qualité au processus transfusionnel : expérience du CHU de Grenoble. Sciences pharmaceutiques. 1995. �dumas-01817673�
AVERTISSEMENT
Ce document est le fruit d'un long travail approuvé par le
jury de soutenance et mis à disposition de l'ensemble de la
communauté universitaire élargie.
Il n’a pas été réévalué depuis la date de soutenance.
Il est soumis à la propriété intellectuelle de l'auteur. Ceci
implique une obligation de citation et de référencement
lors de l’utilisation de ce document.
D’autre part, toute contrefaçon, plagiat, reproduction illicite
encourt une poursuite pénale.
Contact au SID de Grenoble :
bump-theses@univ-grenoble-alpes.fr
LIENS
LIENS
Code de la Propriété Intellectuelle. articles L 122. 4
Code de la Propriété Intellectuelle. articles L 335.2- L 335.10
http://www.cfcopies.com/juridique/droit-auteurUNIVERSITE Joseph FOURIER - GRENOBLE I
U.F.R. de PHARMACIE
Domaine de, la Merci - LA TRONCHE
ANNEE: 1995
N° 'd'ORDRE:
f
os-i.,
APPLICATION DES CONCEPTS QUALITE
AU PROCESSUS TRANSFUSIONNEL
Expérience' du C.H.U. de GRENOBLE
THESE
Présentée à l'Umversité Joseph Fourier - GRENOBLE 1
pour obtenir le grade de : DOCTEUR EN PHARMACIE
Par
Mademoiselle MEGE Laurenc.e
Cette thèse sera soutenue publiquement le 13 Décembre 1995
Devant:
Monsieur le Professeur J. CALOP
Mademoiselle .le Professeur J. ALARY
Monsieur le Docteur N. DROUET
Monsieur le Docteur B. SCHWEIZER
I
Président du Jury
A Yannick,
Pour son amour
Ta bonne humeur, ta patience et ton soutien m'ont permis de mener
à
bien ce
travail.
A mes parents,
Pour m'avoir laissé choisir librement les études que je voulais mener
Et pour leur confiance tout au long de mon cursus universitaire
Je vous en serai éternellement reconnaissante.
A ma soeur,
à
Thierry, à Bastien et
à
Arnaud
Pour leur soutien, leurs conseils, et leur accueil toujours chaleureux.
A ma grand mère,
Ton souvenir est un profond réconfort.
Je tiens
àadresser mes plus sincères remerciements :
à
Monsieur le Professeur
J.
CALOP,
pour avoir accepté de présider ce Jury, pour ses précieux conseils et pour l'intérêt portéà
ce travail.Grâce à vous, l 'Assurance Qualité rentre progressivement dans les pratiques du C.H.U.de Grenoble et les étudiants peuvent participer
à
ce projet majeur et inévitable.à
Monsieur le Docteur N. DROUET,
pour m'avoir accordé sa confiance et confié ce travail et pour le temps précieux qu'ily
a consacré.Le chemin à parcourir est encore long et semé d'embûches mais c'est là, tout l'intérêt d'être pionnier.
à Mademoiselle J. ALARY,
pour m'avoir fait découvrir l' Assurance Qualité à travers ses cours.Vous avez guidé mon choix dans la voie industrielle, et plus particulièrement dans la Qualité et je vous en suis reconnaissante.
à
Monsieur le Docteur B. SCHWEIZER,
pour avoir accepté de juger ce travail et pour ses conseils.Votre enthousiasme et votre engagement constituent un atout majeur pour la réussite de la démarche Qualité appliquée à la transfusion sanguine.
SOMMAIRE
INTRODUCTION
9
PARTIE A: REVUE BIBLIOGRAPHIQUE
1. ADAPTATION DES CONCEPTS QUALITE A LA TRANSFUSION SANGUINE 10
1.1 EVOLUTION DE LA TRANSFUSION SANGUINE 10
1.1.1 Evolution de l'organisation de la transfusion sanguine en France 10
1. 1.2 Le nouveau visage de la transfusion sanguine en France 11
I.1.2.1 L'organisation de la transfusion sanguine 12
1.1.2.2 Le statut des produits sanguins stables 21
1.1.2.3 Conclusion 22
1.2 NOUVELLE ORGANISATION DE LA TRANSFUSION SANGUINE : LA
QUALITE, UNE OBLIGATION LEGALE POUR LES E.T.S. 23 I.3 LES ETABLISSEMENTS DE SOINS FACE A LA NOUVELLE
ORGANISATION DE LA TRANSFUSION SANGUINE 26
1.3.1 les obligations légales des Etablissements de Soins, en matière de transfusion
sanguine 26
1.3 .2 Réactions et adaptation des établissements de soins à la nouvelle organisation de la
transfusion sanguine 28
1.3.2.1 Réforme et exercice professionnel dans les E.S. 28
1.3.2.2 Réforme et nouvelles structures dans les E.S. 29
1.3.3 Commentaires 31
L4 CONCLUSION 33
Il. LE PROCESSUS TRANSFUSIONNEL 34
ILl LE PROCESSUS TRANSFUSIONNEL : VUE D'ENSEMBLE 34 Il.2 DESCRIPTION ET ANALYSE DU PROCESSUS TRANSFUSIONNEL 37
II.2.1 Le processus d'approvisionnement · 38
II.2.1.1 Fonction 38
II.2.1.2 Référentiel 39
II.2.1.3 Analyse 39
11.2.2 Le processus d'analyses biol9giques 44
II.2.2.1 Fonction 44
II.2.2.2 Référentiel 44
II.2.2.3 Analyse du processus d'analyses biologiques 45
II.2.3 Le Processus de préparation 47
II.2.3.1 Fonction 47
Il.2.3.2 Référentiel et analyse 48
II.2.3 .4 Les produits sanguins stables 55
II.2.4 Le processus de distribution 55
II.2.4.1 Fonction 55
II.2.4.2 Référentiel 56
II.2.4.3 Les étapes du processus de distribution 56
II.2.4.4 La prescription médicale 57
II.2.4.5 Transmission de l'information du prescripteur à l'établissement de transfusion
sanguine 60
II.2.4.6 Réception de l'information par l'établissement de transfusion sanguine 61
II.2.4. 7 L'attribution 62
II.2.4.8 Stockage intermédiaire éventuel, en l'attente de la distribution proprement dite64
II.2.4.9 Distribution 66
II.2.4.10 Réception des produits sanguins au sein du service demandeur 69 II.2.4.11 Stockage intermédiaire éventuel en l'attente de l'utilisation 69
II.2. 5 Le processus d'administration 71
II.2.5.1 Fonction 71
II.2.6 Le processus de suivi transfusionnel 73
II.2.6. l Fonction 73
II.2.6.2 Traçabilité 73
II.2.6.3 Hémovigilance 74
II.2. 7 Le risque transfusionnel 76
II.2. 7.1 Le risque infectieux 76
II.2.7.2 Le risque immunologique 78
II.2. 8 Conclusion 80
Ill. LA MAITRISE DU PROCESSUS TRANSFUSIONNEL 81
fill LES CONCEPTS QUALITE ET LE PROCESSUS TRANSFUSIONNEL 81 III.1.1 Organisation de la structure Qualité 81 ID.1.1.1 Organisation du système Qualité dans l'établissement de transfusion sanguine 83 ID.1.1.2 Organisation du système Qualité au sein d'un établissement de soins 84
ID.1.2 Référentiel Qualité 86
ID.1.2.1 Différences entre B.P.F. et Normes I.S.O. 86 III.1.2.2 Les Bonnes Pratiques Transfusionnelles 87 III.1.2.3 Les Normes l.S.O. appliquées à la Transfusion Sanguine 88
ID.1.3 Evaluation du processus 93
III.1. 3 .1 Description du processus 93
ID.1.3.2 Formalisation du processus 94
III.1.4 Maîtrise de la main d'oeuvre 95
III.1.4.1 La responsabilisation 95
III.1.4.2 La Qualification 96
ID.1.4.3 La formation 96
ID.1.4.4 L'information 99
III. 1. 5 MaI"trise des matières 101
ID.1. 5 .1 Les matières autres que les produits sanguins 101
III.1.5.2 Le produit sanguin 102
III.1.6 Maîtrise du milieu 103
III.1.6.1 Les locaux 103
IlI.1.6.2 L'envimîmement et les cûnditions de travail 104
ID.1. 7 Maîtrise du matériel 105
ID.1. 7.1 Les spécifications 105
ID.1.7.2 Qualification 105
ID.1. 7 .3 La maintenance 107
III. 1. 7.4 L'utilisation 107
ID.1. 7 .5 L'étalonnage 107
III.1. 8 Maîtrise des méthodes et des procédés 107 ID.1.8.1 La maîtrise des procédés liés au produit sanguin 107 III.1.8.2 La maîtrise des protocoles de soins infirmiers 109
III.1. 9 Le système documentaire 110
III. 1. 9 .1 Rôle de la documentation 110
ID.1.9.2 Quels documents 111
III.1.9.3 Rédaction d'une procédure 116
ID.1.9.4 Mise en place et mat"trise des procédures 118
III.1.10 Mesurer pour améliorer 120
Ill.1.10 .1 La mesure de la Qualité au niveau de l'utilisateur 120 III.1.10.2 La mesure de la Qualité par l'entreprise 122
ID.1.11 L'audit Qualité 125
III.1.11.1 Définition 125
ID.1.11.2 L'audit interne 125
III.1.12 Méthodes de maîtrise et d'amélioration de la Qualité 126 ID.1.12.1 Principe d'une analyse prévisionnelle de sûreté de fonctionnement 127
ID.1.12.2 Méthode 128
ID.1.12.3 Déroulement del' A.M.D.E.C. de processus 128 III.1.12.4 Application et exemples d' A.M.D.E.C. 129 ID.2 LES OUTILS QUALITE ET LA THERAPEUTIQUE TRANSFUSIONNELLE132
III.2.1 Situation française 132
III.2.2 Etats-Unis: exigences de la Joint Commission on Accreditation ofHealth Care
Organisation 13 3
ID.2.3 J.C.A.H.O. et transfusion sanguine 133
ID.2.3.1 Les standards 133
ID.2.3.2 Audit clinique 134
III.2.4 Efficacité des guides et des audits cliniques 136
III.2.5 Conclusion 138
IV. CONCLUSION
PARTIE B: EXPERIENCE DU C.H.U. DE GRENOBLE
l. LE CONTEXTELlLESPARTENAIRES I.1.1 Le C.D.T.S. de Grenoble I.1.2 Le C.H.U. de Grenoble I.1.3 C.D.T.S. et C.H.U.
L2 LA STRUCTURE QUALITE I.2.1 Rôles
I.2.1.1 L'Assemblée Générale et le Conseil de Fédération
139 141 141 141 142 143 143 144 144
1.2.1.2 La Cellule Qualité Transfusionnelle 144
Il. LES ACTIONS MENEES PAR LA C.Q.T. 146
11.1 ETAT DES LIEUX DU PROCESSUS TRANSFUSIONNEL AU C.H.U. DE
GRENOBLE 146
II.1.1 La prescription des produits sanguins au C.H.U. 146 II.1.2 La distribution des produits sanguins 146 II.1.3 L'administration des produits sanguins 147
II. l. 4 Le suivi post-transfusionnel 14 7
11.2 QUELQUES ACTIONS DE LA C.Q. T. 148
II.2.1 Actions portant sur le personnel impliqué dans la transfusion 148
II.2.1.1 L'information du personnel 148
II.2.1.2 La responsabilisation du personnel 148
II.2.1.3 La formation continue 150
II.2.2 La normalisation des pratiques transfusionnelles 150
II.2.3 La maîtrise des documents 151
II.2.4 Propositions de réforme des circuits transfusionnels du C.H.U. 153 Il.2.4.1 Le transport des produits sanguins entre C.D.T.S. et C.H.U. 153 II.2.4.2 La traçabilité des produits sanguins 154
Il.2.5 L'hémovigilance 155
11.3 LA CERTIFICATION LS.O. 9002 DE LA C.Q. T. 155
II.3.1 Le périmètre de certification 155
II.3.2 Les principaux écarts entre la situation qualité présente de la F.Q.T. et l'esprit de la
norme I.S.O. 9002 156
11.3.2.1 Responsabilité de la Direction 156
Il.3.2.2 Système Qualité 156
11.3 .2.3 Maîtrise des documents et des données 156
11.3.2.4 Achats 156
11.3.2.5 Identification et traçabilité du produit 157
II.3.2.6 La maitrise des processus 157
11.3.2.7 La maîtrise du produit non-conforme 157 11.3.2.8 Actions correctives et préventives 157 Ill. AMELIORATION DES CIRCUITS TRANSFUSIONNELS HOSPITALIERS 158 IILl POURQUOI AVOIR CHOISI UN TEL SUJET DE TRA V AIL? 158
ID.2 LE CONTEXTE 158
III.2.1 Elaboration de Procédures 160
ID.3 PROCEDURE CIRCULUS: CQT OlV P5 161
III.3 .1 Etat des lieux 161
III. 3 .1.1 Aspect quantitatif 161
III.3 .1.2 Aspect qualitatif 166
III.3.2 Analyse de l'existant 169
III.3.3 Elaboration de procédure 170
III. 3. 3 .1 Pourquoi ? 170
III.3.3.3 CIRCULUS CQT OlV P5 III.3 .4 Mise en place et évaluation
III.3.4.1 Essai de qualification des boites isothermes
III.3.4.2 Vérification du fonctionnement de l'armoire réfrigérante III.3.4.3 Un choix d'indicateurs de petformance
fil4 PROCEDURE SIRIUS : CQT 02E P2
III.4.1 Etat des lieux
III.4.1.1 aspect quantitatif III.4.1.2 Aspect qualitatif III.4.2 Analyse de l'existant IIl.4.3 Elaboration de procédure
III. 4. 3 .1 Pourquoi ? IIl.4.3.2 Comment?
III.4.3.3 SIRIUS: CQT 02E P2 III.4.4 Mise en place et évaluation
ms
DISCUSSION 171 173 174 175 175 178 178 178 189 192 194 194 194 194 195 196 fil6 CONCLUSION : IMPRESSIONS APRES NOTRE TRA V AIL AU SEIN DE LAC.Q.T-C.H.U. DE GRENOBLE 199
PARTIE C: DISCUSSION
200
CONCLUSION
207
BIBLIOGRAPHIE
208
LISTE DES ABREVIATIONS ET DES SIGLES UTILISES
215
LISTE DES TABLEAUX
217
LISTE DES SCHEMAS
218
INTRODUCTION
La transfusion sanguine, en France et dans le monde, est en pleine mutation, suite aux évènements dramatiques du sang contaminé.
Cette évolution ne consiste pas à renier cette thérapeutique qui a sauvé et sauve encore de nombreuses vies, mais vise à améliorer la sécurité transfusionnelle.
Depuis la loi de 4 Janvier 1993 relative à la sécurité en matière de transfusion sanguine et de médicaments, le système transfusionnel français a un nouveau visage qui introduit entre autres, l 'Agence Française du Sang, comme tutelle de la transfusion sangwne.
L 'Agence Française du Sang inscrit la sécurité transfusionnelle dans un objectif de santé publique.
Pour atteindre un niveau de sécurité transfusionnelle maximum, l' Agence Française du sang a choisi un moyen provenant du monde industriel : les concepts Qualité.
Ainsi, la mise en oeuvre d'une démarche Qualité dans les établissements de transfusion sanguine s'est vue imposer règlementairement par la loi du 4 Janvier 1993.
Mais la sécurité transfusionnelle ne se limite pas à la Qualité du produit sanguin, elle repose aussi sur les circuits de distribution et les pratiques transfusionelles des établissements de soins.
Donc, pour s'inscrire dans une dimension de Qualité du soin transfusionnel, la démarche Qualité doit être étendue aux établissements de soins, c'est-à-dire doit concerner l'ensemble du processus transfusionnel du don de sang à l'acte transfusionnel en passant par la qualification du don, la préparation et la distribution des produits.
A travers une description d'un processus transfusionnel global puis des éléments Qualité et grâce à des exemples concrets, nous allons nous appliquer à répondre à plusieurs questions, à savoir :
• les concepts Qualité sont-ils adaptables au processus transfusionnel ?
• les concepts Qualité sont-ils adoptés par les acteurs de la transfusion sanguine? • les concepts Qualité sont-ils efficaces en terme de sécurité transfusionnelle? Dans le contexte actuel où se trouve la transfusion sanguine, la démarche Qualité sera réussie si elle atteind :
• son objectif, qui est d'optimiser le fonctionnement du processus transfusionnel, • son but, qui est de réduire les risques inhérents à toute transfusion,
1. ADAPTATION DES CONCEPTS QUALITE A LA
TRANSFUSION SANGUINE
1.1 EVOLUTION DE LA TRANSFUSION SANGUINE
La transfusion sanguine est avant tout une thérapeutique qui a sauvé et sauve encore de nombreuses vies mais, comme toute thérapeutique, elle n'est pas dénuée de tout risque. Si après la seconde guerre mondiale, la transfusion sanguine a connu un rapide développement et a suscité un engouement important conduisant à une certaine banalisation de l'acte, les années 80 ont marqué un tournant radical, dans son évolution.
En effet, les évènements dramatiques du sang contaminé ont considérablement terni l'image de la transfusion sanguine en France et à travers le Monde.
Pour tenter de restaurer la confiance des patients et des donneurs, et pour remotiver les équipes médicales et scientifiques, une nouvelle organisation de la transfusion sanguine est élaborée et mise en place par les autorités.
Cette réforme se base notamment, sur l'application des concepts Qualité, qui paraissent être des outils adaptés pour identifier les défaillances du système transfusionnel et pour y remédier.
Après un rapide rappel de quelques évènements marquants de l'histoire de la transfusion sanguine, nous décrirons son nouveau visage, puis nous situerons plus précisement les concepts Qualité, dans cette organisation naissante.
1.1.1 Evolution de l'organisation de la transfusion sanguine en
France
Au début des années 80, la tragédie du sang contaminé a clairement mis en évidence les faiblesses du système alors en place, tant sur le plan national que local.
A cette époque, la transfusion sanguine est toujours sous le régime de la loi de Juillet 1952 qui a introduit en droit français, les principes d'utilisation du sang humain et de ses dérivés.
Pour mieux situer le contexte de cette loi, remontons 50 ans en arrière.
La seconde guerre mondiale a marqué une étape importante pour la transfusion sanguine en France en créant, par un élan de solidarité important, l'idée du bénévolat. A la fin de cette guerre, deux courants se distinguaient, les partisans du don non-rémunéré et les défenseurs du don non-rémunéré.
La loi de Juillet 1952 favorisait le bénévolat mais ne l'imposait pas, car cela aurait risqué d'entraîner des ruptures de stocks de sang et de ses dérivés. Il régnait alors, une certaine euphorie
et
on cherchait à organiser et à stimuler la thérapeutique transfusionnelle.Ce développement important permet à la France, à la fin des années 1970, de parvenir à l'autosuffisance à partir de sang bénévole. Seuls deux autres pays européens ont également atteint ce niveau, la Belgique et la Hollande. (63)
Pendant toutes ces années, les connaissances scientifiques et les techniques transfusionnelles ont évolué, permettant ainsi de mieux cerner les risques transfusionnels et de les limiter.
Mais, en 1981, les premiers cas de transmission du virus H.I.V. par voie transfusionnelle ont remis brutalement en cause l'engouement pour la transfusion sangmne.
Donneurs, malades, praticiens, chercheurs et autorités se sont alors, retrouvés dépourvus face
à
une situation qu'ils ne maîtrisaient plus.Les premières mesures prises par les autorités pour répondre au risque Sida, touchent trois étapes dans le processus transfusionnel.
La première est l'étape de sélection du donneur qui vise à exclure du don les personnes ayant un comportement à risque. Elle a été mise en place en 1983.
Appliquée avec rigueur, elle a révélé une efficacité non négligeable.
La seconde technique repose sur les tests de dépistage des anticorps anti-H.I.V. et se situe au niveau du don lui-même. Le premier test efficace date de 1985.
Et la dernière, consiste en l'inactivation physicochimique de la partie plasmatique du sang. Elle est du ressort des laboratoires de fractionnement.
Ainsi, à partir de 1985, les contaminations par le virus H.I.V. par voie transfusionnelle sont devenues rarissimes, sans pour autant devenir nulles.
Mais il était trop tard, l'image de la transfusion sanguine était ternie et tout particulièrement en France, où la prévalence nationale du Sida était estimée en 1989 entre 1 OO 000 et 150 000 cas, chiffres relativement élevés comparés aux 30 000 à 50 000 cas dénombrés en Angleterre, pour des populations équivalentes. (63)
Après avoir élaboré et mis en oeuvre les décisions se rapportant à la lutte contre l'épidémie, les autorités, face à un système transfusionnel globalement sinistré, praticiens démobilisés, patients et donneurs inquiets, scientifiques démunis, ont à partir de 1992, posé les bases d'une profonde réorganisation de la transfusion sanguine en France.
1.1.2 Le nouveau visage de la transfusion sanguine en France
Le nouveau visage de la transfusion sanguine, en France, est officialisé par la promulgation de la loi du 4 Janvier 1993.
Cette loi fait reposer la réforme de cette thérapeutique substitutive sur 3 fondements essentiels :
• les principes éthiques de gratuité, consentement, anonymat et garantie de non-profit, qui sont pour la première fois inscrits dans un texte législatif.
• une nouvelle organisation de la transfusion sanguine, et
• l'application d'un régime spécifique aux produits stables dérivés du sang.
Nous ne revenons pas sur les principes éthiques de la transfusion sanguine, nous tenons, seulement, à souligner que le principe du bénévolat du don a attendu une vingtaine d'années pour être traduit législativement.
Nous allons à présent détailler chaque élément de la nouvelle organisation, en précisant les liens et objectifs de chaque élément, et nous spécifierons les particularités du régime des produits sanguins stables.
1.1.2.1 L'organisation de la transfusion sanguine
La loi du 4 Janvier 1993 crée une véritable pyramide institutionnelle comprenant au sommet, le Ministère de la Santé, disposant d'un Comité de Sécurité Transfusionnelle puis, l' Agence Française du Sang, tutelle d'une structure comprenant à la base les établissements de transfusion sanguine (E.T.S.), organisés par secteurs territoriaux par les commissions régionales d'organisation de la transfusion.(24)
L'hémovigilance est centralisée au niveau d'un Centre National d'Hémovigilance. Schéma 1 : Le nouveau visage de la transfusion sanguine en France
Agence du médicament
Ministère de la santé Comité de sécurité transfusionnelle
- - - Agence Française du Sang
Centre national d'hémovigilance
Commission d'organisation de la transfusion sanguine
.,.41---... E.T.S. et L.F.F.B.
Le Comité de Sécurité Transfusionnelle
Il est indépendant, composé de trois personnes, et est en relation directe avec le Ministre.
Il est chargé :
• d'évaluer la situation en matière de sécurité transfusionnelle
• de proposer toute mesure visant à améliorer la sécurité transfusionnelle
• d'alerter le Ministère de la Santé sur toutes les questions d'ordre médical ou
scientifique qui peuvent avoir une incidence sur
l'activitétransfusionnelle.
Le Comité de sécurité transfusionnelle peut se saisir de toute question relative à la sécurité transfusionnelle et adresser des recommandations au Ministère de la Santé. ( 5) (24)
L 'As;ence Erançaise du Sans: : A.ES.
L 'Agence Française du Sang est mise en place le 1er Juillet 1992 et son statut définitif lui est donné par
la
loi du 4 Janvier 1993.C'est un établissement public administratif, qui constitue la clef de voute du nouveau système et devient l'unique interlocuteur des établissements de transfusion sanguine.
=>Fonctionnement
Le fonctionnement de l' Agence Française du Sang repose sur : un Conseil d 'Administration
Il comprend pour moitié, des représentants de l'Etat et pour l'autre moitié, des représentants des principaux acteurs de la transfusion sanguine, caisse nationale d'assurance maladie, fédération :française des donneurs de sang bénévoles, associations d'hémophiles ...
un Conseil Scientifique
Il éclaire par ses avis, l' Agence Française du Sang sur toute question de nature médicale, scientifique et technique ayant une incidence sur une de ses missions.
une Direction Médicale et Scientifique
Elle est chargée du développement (nonnes, formation, recherche ... ) et du suivi du réseau sur le plan médico-technique.
une Direction de l'organisation et de la gestion des B.T.S.
Elle est chargée de concevoir les outils d'une gestion harmonisée des B.T.S., d'assurer le suivi de cette gestion ainsi que l'instruction des décisions d'agrément, d'autorisation ou de subvention incombant au Président de l'agence.
un service juridique
un service de presse et de communication (3) ::>Missions
L 'Agence Française du Sang doit remplir trois types de missions : • définir et appliquer la politique de la transfusion sanguine, • contrôler et coordonner l'activité et la gestion des E.T.S.,
• exercer l'ensemble des missions d'intérêt national à l'activité transfusionnelle. Missions d'intérêt national
A titre d'exemple, nous pouvons citer la tenue d'un fichier national de donneurs de groupes rares et la participation à l'organisation et à l'acheminement des secours, en cas de catastrophes. De plus, en période estivale, pendant laquelle de nombreux E.T.S. sont confrontés à une relative pénurie, l'A.F.S. met en contact le maximum d'E.T.S. pour qu'ils puissent s'aider mutuellement. Enfin, elle peut lancer un appel public pour mobiliser les donneurs de sang au niveau national. (58)
Politique transfusionnelle
La politique transfusionnelle de l 'Agence Française du Sang comprend :
• l'organisation nationale de la transfusion sanguine par l'établissement de schémas territoriaux d'organisation de
la
transfusion sanguine,• la mise en place de l 'hémovigilance coordonnée par le centre national d 'hémovigilance
• l'application des principes de Qualité aux établissements de transfusion sanguine par l'édition de Bonnes Pratiques Transfusionnelles servant de référentiels pour les agréments.
La coordination et le contrôle des E.T.S.
La coordination et le contrôle des activités des E.T.S. a commencé dès l'automne 1992, par la signature d'une convention type entre !'Agence Française du Sang et chaque établissement de transfusion sanguine.
Par cette signature, les E.T.S. s'engagent à satisfaire, dans un délai limité, aux exigences de qualité et de sécurité énoncées dans la dite convention.
Sur le plan de la coordination, nous pouvons citer la gestion du fond d'orientation de la transfusion sanguine. Une partie de ce fond a servi, en 1993, à équiper les E.T.S. d'appareils nécessaires à l'arrêt de l'utilisation des plaquettes de pool préparées à
partir de plusieurs donneurs, en faveur de l'utilisation des plaquettes de donneurs uniques. (2)
Concernant l'étape de contrôle des B.T.S., il est clair que cette activité est
à
la base des décisions d'agrément ou de suspension des B.T.S. prises par le Président del' Agence Française du Sang après avis du Conseil d' Administration.Ce système repose sur des inspections régulières des établissements de transfusion sanguine, par des inspecteurs issus de
la
Direction médicale.Sur ce point, il faut insister sur le rôle de ces inspecteurs qui« n'est pas de terroriser les responsables des E. T.S. en brandissant la menace de retirer un agrément à la moindre incartade ou insuffisance technique mais, de contrôler et d'orienter dans une action positive, les E. T.S. dans le cadre des Bonnes Pratiques Trans.fusionnelles
»
comme le souligne P. HERVE dans sa lettre ouverte aux responsables d'établissement de transfusion sanguine. ( 4 7)L' Agence Française du Sang fait désormais partie du paysage transfusionnel français et son action est capitale pour la coordination du réseau transfusionnel.
Pour reprendre les propos de P. HERVE « l'A.FS., par sa fonction cohésive représente l'outil capable de fédérer les E.T.S., de soutenir leur action et la spécificité de leur mission, de leur rappeler leurs devoirs et leurs responsabilités, de les préparer
à ces modifications structurelles médico-techniques et économiques avec des projets d'entreprises mobilisateurs tout en assurant des contrôles réguliers du respect des Bonnes Pratiques Transfusionnelles et de la fiabilité des hommes et des structures
»
(47)
Les schémas territoriaux d'organisation de la tram,fusion sanguine
La loi du 4 janvier 1993, dans le cadre de la réorganisation de la transfusion sanguine prévoit la mise en place de schémas territoriaux d'organisation de la transfusion sangwne.
Les schémas territoriaux d'organisation de la transfusion sanguine déterminent: • la zone de collecte de chaque établissement de transfusion sanguine • la répartition des activités entre les B.T.S.
• les installations et équipements nécessaires à la satisfaction des besoins sanitaires
• les modalités de coopération entre les B.T.S.
Le cadre régional est donc apparti plus adapté
à
l'activité transfusionnelle que1'
échelon départemental, hier, compétent.Au niveau national, les projets ont
étécoordonnés par 1' Agence Française du Sang, en
Dans chaque région, la loi a prévu l'institution d'une commission d'organisation de la transfusion sanguine composée essentiellement de la Direction Régionale des Affaires Sanitaires et Sociales, des établissements de transfusion sanguine et des établissements de soins, des associations de donneurs de sang bénévoles et des associations de patients. (59)
Ces commissions d'organisation de la transfusion sanguine peuvent être consultées par l'Agence Française du Sang, sur toute question concernant l'activité de transfusion sanguine, dans le ressort du schéma territorial. ( 5)
26 schémas territoriaux d'organisation de la transfusion sangwne ont été alllSl,
élaborés, correspondant aux régions administratives.
Il est toutefois prévu le regroupement de certaines activités sur un plan inter-régional ou la création de passerelles entre établissements de différentes régions.
Sur la base de ces schémas territoriaux, de nouvelles structures juridiques vont être constituées sous la forme de groupements d'intérêt public, unissant les associations loi
1901 et les hôpitaux qui gèrent actuellement, la transfusion sanguine. (59)
Deux points essentiels caractérisent ces schémas territoriaux d'organisation de la transfusion sanguine :
• le maintien du réseau très décentralisé des sites de collecte et de distribution des produits sanguins labiles, afin de préserver la notion de proximité de la transfusion sanguine vis à vis des malades et des donneurs,
• le regroupement sous forme de plateau technique, des activités de contrôle du don et de préparation du produit sanguin, au niveau de centres répondant aux exigences de sécurité plus élevées.
Nous pouvons dégager deux buts principaux à cette démarche.
Sur le plan sanitaire, ces schémas territoriaux doivent garantir durablement une homogénéité de sécurité, sur l'ensemble du territoire et permettre de mieux couvrir les besoins du malade. (59)
Sur un plan scientifique et technique, ils vont permettre de mieux appréhender l'évolution inéluctable de la transfusion sanguine vers la biotechnologie.
Equipés, organisés, entourés de collaborateurs rompus à la biologie moléculaire, à la thérapeutique immunomoléculaire, à la microbiologie, à la médecine transfusionnelle, les plateaux techniques prétendront à un niveau scientifique de réference. (47)
Ces schémas territoriaux d'organisation de la transfusion sanguine constituent un bouleversement sans précédent, mais, sont une urgence absolue.
Les établissements de tram.fusion sanguine : E.
T.
S
Ils exercent une mission de santé publique dans le cadre de la transfusion sanguine. Ils doivent être agréés par l 'Agence Française du Sang, cet agrément étant subordonné à des conditions techniques, sanitaires et médicales, définies par décret, et administratives, car seules les associations à but non lucratif et les groupes d'intérêt public peuvent être agréés.
Outre la collecte du sang, la préparation des produits sanguins labiles et leur distribution, les établissements de transfusion sanguine ont vocation à développer toute activité liée à la transfusion sanguine, au conseil et au suivi des actes transfusionnels. Ils peuvent aussi exercer des activités de soins et de laboratoires, d'enseignement et de recherche. (24)(5)
L 'hémovigilance
On entend par hémovigilance,
«
/'ensemble des procédures de surveillance, organisées depuis la collecte du sang et de ses composants jusqu'au suivi des receveurs, en vue de recueillir et d'évaluer les informations sur les effets inattendus ou indésirables, résultant de /'utilisation thérapeutique des produits sanguins labiles et d'en prévenir /'apparition.»
(2)Le décret du 24 Janvier 1994 fixe les conditions de mise en oeuvre des règles d'hémovigilance d'une part, et les obligations d'autre part.
Les règles comportent, pour toute unité préparée de produit sanguin labile,
• le signalement de tout effet inattendu ou indésirable lié ou susceptible d'être lié à l'usage thérapeutique de ce produit,
• le recueil, la conservation et l'accessibilité des informations relatives à son prélèvement, à son utilisation ainsi qu'aux effets mentionnés ci-dessus,
• l'évaluation et l'exploitation de ces informations en vue de prévenir la survenue de tout effet inattendu ou indésirable résultant de l'utilisation thérapeutique des produits sanguins labiles.
Les obligations sont les suivantes :
• obligation d'informer le patient, de tout acte transfusionnel,
• obligation de conserver dans le dossier médical, trace de tout acte transfusionnel,
• obligation de déclarer tout accident ou incident chez le patient,
• obligation, pour les établissements de transfusion sanguine, de tenir un registre incluant l'identification du receveur du produit sanguin qu'ils ont délivré,
• obligation, pour les établissements de soins, de tenir un registre des patients receveurs de produits sanguins labiles et de leurs conséquences immédiates, à moyen et long terme. (2)
Le décret d'hémovigilance définit également, les éléments nécessaires à un recueil et à une circulation des données d'hémovigilance à l'échelle nationale.
Au niveau national, le Centre National d'Hémovigilance crée le 09 Octobre 1992 est installé à Bordeaux.
Il est placé sous la responsabilité del' Agence Française du Sang. (24)
L'exploitation nationale des observations faites lors d'incidents transfusionnels est assurée par l' Agence Française du Sang avec le concours du Centre National d'Hémovigilance.
Au niveau régional, chaque région a depuis le début du mois de Mars 1995, son coordinateur d'hémovigilance, placé auprès de la Direction Régionale des Affaires Sanitaires et Sociales, chargé d'animer un réseau régional d'hémovigilance.
Au niveau local, établissements de transfusion sanguine et établissements de soins doivent désigner chacun, un correspondant d'hémovigilance. (24) (2) (59)
A noter également, l'existence d'un Comité de Sécurité Transfusionnelle et
d'Hémovigilance d'Etablissement, au sein de chaque établissement de soins public et privé. Ce dernier regroupe le Directeur de l'établissement de soins, le Directeur de l'établissement de transfusion sanguine, les 2 correspondants d'hémovigilance et des représentants des personnels médicaux, soignants, médico-techniques et administratifs de l'établissement de soins.
Il a pour mission de contribuer, par ses études et ses propositions, à l'amélioration de la sécurité des patients transfusés, et de coordonner les actions d 'hémovigilance entreprises au sein de l'établissement de soins.(6)
Schéma 2 : Organisation de l 'hémovigilance sur le plan national
B.T.S. Correspondant d 'hémovigilance
Agence Française du sang Centre National d 'Hémovigilance
(Bordeaux) Coordinateur d'hémovigilance / régional (D.R.A.S.S.) Préfet de région E.S. Correspondant d 'hémovigilance
~
---
~
• --• · - Comité de s_écurité transfusionnelle et --• • ••
. .
--.
d'hémovigilance d'établissement de soins _ •• ·---
--
-
--~---·----·
--·
Dans la pratique, tout incident ou accident lié à une transfusion sanguine doit être signalé au correspondant d 'hémovigilance de l'établissement de soins, dans lequel a été administré le produit.
Ce dernier procède à une enquête au sein du service concerné et informe le correspondant d'hémovigilance de l'établissement de transfusion sanguine distributeur. Ensemble, ils rédigent une fiche d'incident transfusionnel.
Cette fiche est transmise au coordinateur régional mais aussi, au Préfet et à l 'Agence Française du Sang. Une quatrième copie est versée au dossier du malade. ( 6)
Schéma 3 : Déclaration d'incident transfusionnel médecin
pharmacien
Tout chirurgien-dentiste
qui a connaissance de l'administration d'un produit
sanguin labile
sage-femme infirmier( e)
et
INFORMATION
qui constate un effet inattendu ou indésirable dû à son administration Correspondant d'hémovigilance de l'E.S. INFORMATION examens copte copte copie Correspondant d 'hémovigilance de l'E.T.S. Rédaction de la fiche d'incident transfusionnel A.F.S. Coordonnateur régional Préfet Dossier médical
Le coordinateur régional veille à ce que soient prises les mesures qu'appelle la situation constatée :retrait de produits, recherche et traitement éventuel des receveurs et du donneur.
L 'hémovigilancerepose sur lanotion de traçabilité, car elle suppose de pouvoir suivre
«à
latrace» le sang du donneur, depuis le don jusqu'àladistribution, en passant par lapréparation du produit et laconservation.Elle va permettre, suite à un incident ou accident, de remonter du transfusé vers le donneur, dans le respect de l'anonymat et de redescendre du donneur vers d'autres personnes, éventuellement traitéspar des produits de même origine.
Pour être efficace, cela implique le respect de procédures rigoureuses, dont les principales sont :
• l'attributiond'un numéro unique à chaque unité:
à ce sujet, une codification nationale a été mise en place par l'Agence Française du Sang pour harmoniser lanumérotation des produits et faciliterleuridentification. En Mars 1996, chaque prélèvement se verra affecter un numéro unique en France. (59)
• l'élaboration de documents types, assurant le recueil des informations exigées par l'hémovigilance, comme le dossier transfusionnel, les fiches d'incident transfusionnelet lesdossiers d'enquête. (24)
• l'aménagementde liaisonsinformatiséesentre B.T.S. et E.S ..
L'hémovigilance devrait permettre de répondre de façon ponctuelle à un incident ou accident transfusionnel et à moyen et long terme d'organiser des études épidémiologiques visant notamment, à améliorer nos connaissances des risques transfusionnelsrésiduels, ~ mais aussi immunologiques.
1.1.2.2 Le statutdes produits sanguins stables
Dans un but d'harmonisation européenne, laloidu 4 Janvier 1993 intègredans le droit français, les dispositions de laDirective européenne n° 89/381/CEE du 14 Juin 1989, ayant pour objet de soumettre lesproduits sanguins stables issusdu fractionnement du sang, albumine, immunoglobulines et facteurs de coagulation au droit commun-du médicament contenu dans lelivreV du Code de laSanté Publique.(22)
Les produits sanguins stables sont donc, soumis à une autorisation de mise sur le marché, octroyée par l'Agencedu Médicament, pour être distribués.
D'autre part, depuis le 1er Janvier 1995, ils appartiennent au circuit de distribution pharmaceutique.
A ce titre, ilsne sont plus délivrés par lesB.T.S. mais, par lespharmacies hospitalières et cela toujourssur prescription médicale.
Enfin, l'activité de fractionnement du sang est complètement réorganisée. Elle est régie par un organisme public unique, ayant le statut de laboratoire phannaceutique, le Laboratoire Français de Fractionnement et des Biotechnologies. Il regroupe deux des six établissements de fractionnement existant actuellement en France (Lille et Les Ullis), au sein d'un groupement d'intérêt public et détient le monopole de préparation des produits sanguins stables à partir de l'ensemble du plasma collecté en France. Les quatre autres établissements sont appelés à disparaitre. (22) (24)
Mais la structure juridique de cet établissement souple et ouverte, lui permet d'associer, le cas échéant, d'autres partenaires, notamment industriels, français ou étrangers, qui respectent les principes éthiques posés par la loi.
Ce dispositif n'exclut donc pas que des industriels du fractionnement à statut privé puissent exercer leur activité en France, à la condition toutefois, d'entrer dans le Laboratoire Français du Fractionnement et des Biotechnologies. Bien plus, la loi n'interdit pas l'activité en France d'une firme pharmaceutique qui importerait du plasma issu de donneurs rémunérés et réexpédirait ensuite l'intégralité de sa production hors de nos frontières. (22)
Mais, concernant les principes d'éthique caractérisant la transfusion sanguine en France,
la
transposition de la Directive ne fait pas obstacle à leur application. En effet, l'autorisation de mise sur le marché ne pourra être accordée qu'à des produits issus de dons non rémunérés, sauf si des produits ne satisfaisant pas à ces conditions présentaient un intérêt thérapeutique justifiant de les mettre à disposition des patients. (5)Pour en terminer avec le statut des produits sanguins stables, nous tenons à préciser qu'en matière d'hémovigilance, ils font l'objet d'enquêtes de pharmacovigilance. Tout incident ou accident est déclaré à l 'Agence Française du Médicament qui entretient des relations étroites avec l' Agence Française du Sang.
1.1.2.3 Conclusion
Si en 1952, l'objectif principal de la transfusion sanguine était d'atteindre l'autosuffisance nationale, actuellement, le législateur cherche
à
rationaliser cette pratique.La réforme radicale du système transfusionnel en France, se place dans la perspective de faire de la transfusion sanguine, service public, un véritable réseau plus homogène dans ses pratiques médico-techniques et de gestion, plus coordonné par un pilotage régulier de l' Agence Française du Sang, plus efficient grâce au regroupement de certaines activités et plus contrôlé grâce aux interventions des services d'inspection de l'agence. (3)
Sur le plan strictement médical, les deux grandes notions à retenir sont : e
une sécurité transfusionnelle maximale,
• une traçabilité donneur<=> receveur.
Débordant de ce cadre, soulignons que cette réforme a le mérite d'insister aussi sur l'importance de la transparence passant par une définition claire et précise des responsabilités.
Nous venons de décrire en détail le nouveau visage de la transfusion sanguine en France. Mais où se situent les principes Qualité choisis par les autorités pour regagner la confiance des malades, des donneurs et de toute une profession, et en quoi consistent-ils?
1.2 NOUVELLE ORGANISATION DE LA TRANSFUSION SANGUINE : LA QUALITE, UNE OBLIGATION LEGALE POUR LES E.T.S.
Si nous considérons les propos tenus au cours du 1er congrés de la Société Française de Transfusion Sanguine qui s'est déroulé du 6 au 10 Juin 1994 à Angers, la Qualité apparait comme un enjeu majeur, mobilisateur de toute une profession. (1)
Cette mobilisation a toute sa raison d'être, compte tenu du fait que les nouveaux textes règlementaires font de l 'Assurance Qualité, une obligation légale pour les établissements de transfusion sanguine.
Chronologiquement, l'arrêté du 29 Juillet 1992 qui fixe «les conditions auxquelles doivent satisfaire les E. T.S. pour conserver le bénéfice de l'agrément prévu à l'article L 667 du Code de la Santé Publique» est le premier texte, dans lequel apparait clairement la notion, d' Assurance Qualité. Ce texte instaure un modèle de convention-type qui précise «les règles de fonctionnement des E.T.S. et les modalités de leur relation avec l'Agence Française du Sang».
Il est stipulé au chapitre
Ier«
qu'en vue d'assurer la qualité des produits et la sécurité transfusionne/le, l'établissement de transfusion sanguine met en oeuvre un dispositif d 'Assurance Qualité concernant les activités de collecte, de préparation, d'identification, de conservation et de contrôle des produits sanguins».Chacune de ces opérations doit faire l'objet d'une procédure écrite établie en fonction de normes en vigueur, des recommandations de }'Agence Française du Sang et de l'état des pro grés de la science et de l'évolution des techniques.
Doivent être également établies par écrit les modalités d' autoinspection et les modalités de rappel de produit.
Enfin, une attention particulière doit être portée à l'adéquation de la qualification des personnels aux tâches qui leur incombent. (52)
Nous retrouvons dans cette convention, quelques grands principes Qualité: • la documentation,
• l' autoinspection,
La loi du 4 Janvier 1993 relative à la sécurité en matière de transfusion sanguine et de médicaments, qui confinne ainsi l'arrêté du 29 Juillet 1992, dispose que les B.T.S. doivent être agréés par l' Agence Française du Sang. Ceux-ci doivent appliquer des Bonnes Pratiques dont les principes sont définis par un règlement établi par l 'Agence Française du Sang.
La démarche de l 'Agence consiste à adapter les principes d' Assurance Qualité issus des Bonnes Pratiques de Fabrication de l'industrie pharmaceutique, à la transfusion sangmne.
La tradition d' Assurance Qualité pour les établissements de transfusion sanguine étant très faible, l 'Agence Française du Sang a décidé de préciser et de détailler le plus possible, ces principes.
Des groupes d'experts ont été constitués dès l'été 1993. Ils ont entrepris un travail considérable afin d'aboutir à des documents qui reflètent l'état de l'art transfusionnel et qui définissent rigoureusement des pratiques médico-techniques, afin d'atteindre un niveau de qualité et de sécurité homogène.
Les Bonnes Pratiques Transfusionnelles comptent 5 thèmes :
• Bonnes Pratiques de Prélèvement : arrêté du 22 Septembre 1993
• Bonnes Pratiques de Préparation des produits sanguins labiles arrêté du 7 Février 1994
• Bonnes Pratiques de Distribution des produits sanguins labiles arrêté du 4 Août 1994
• Bonnes Pratiques de Qualification Biologique du Don: arrêté du 4 Janvier 1995 • Bonnes Pratiques d'Autotransfusion, (en cours d'écriture)
Il est préciser que chaque texte est soumis à enquête publique, afin que chacun puisse expnmer son oprmon.
Les Bonnes Pratiques Transfusionnelles constituent des référentiels opposables aux établissements de transfusion sanguine, qui doivent les appliquer conformément, pour être agréés par l 'Agence Française du Sang.
Mais, elles ne sont en rien figées, au contraire, elles doivent être évolutives et donner lieu à des modifications, compte tenu de l'état de l'art et des observations transmises à l' Agence Française du Sang par les acteurs de terrain. (47)
Par le biais des Bonnes Pratiques Transfusionnelles et des dispositifs d' Assurance Qualité, la Qualité entre en force dans le secteur de la transfusion sanguine, mais plus particulièrement dans les établissements de transfusion sanguine.
En effet, nous pouvons souligner d'ores et déjà que rien n'est très précis dans ces textes, en ce qui concerne la démarche à adopter par les établissements de soins.
En élargissant notre champs de vision, nous discernons une volonté de démarche Qualité dans la mise en place des schémas territoriaux d'organisation de la transfusion sangmne.
La concentration de moyens et de compétences, au sein de différents plateaux techniques va dans le sens d'une maîtrise de la qualité des appareils, des processus et des personnels.
Ces plateaux techniques ont pour tâche entre autres, le contrôle des dons, en mettant en jeu des tests de dépistage dont la qualité est essentielle pour la sécurité du ou des receveur(s). La fiabilisation des tests est une étape importante dans le cadre de la prévention d'une transmission virale par transfusion sanguine. A ce sujet, des procédures d'évaluation de la qualité des tests s'organisent en France.
Cela se traduit par un examen des dossiers de réactifs centralisé au niveau de
1'
Agence du Médicament. (36)Cette approche est à mettre en parallèle avec ce qui se passe en Angleterre et aux Etats Unis.
En Angleterre, un système de contrôle de la qualité des tests se met en place sur le plan national et au sein même des établissements de transfusion sanguine.
Sur le plan national, les laboratoires de diagnostic, soumettent leur test au Central Public Health Laboratory qui les évalue, à partir d'un panel de différents témoins de contrôle positif.
Ces témoins et d'autres fournis par le National Institute of Biological Sam.pies Control, sont également à la disposition des établissements de transfusion sanguine qui les utilisent en routine.
La National Blood Authority,
1'
Agence britannique du sang, nouvellement créée, se charge d'une analyse centralisée des résultats. (17)Aux Etats-Unis, l'organisation du système transfusionnel de la Croix Rouge Américaine, qui recueille 6 millions de dons de sang par an, soit la moitié des prélèvements réalisés dans ce pays, est entrain d'évoluer vers une centralisation sur 10 sites de
1'
activité de dépistage pour l'ensemble du pays. Cela se traduit par exemple, par une centrale d'achats qui assure notamment, l'homogénéité des réactifs pour tous les établissements. ( 17)Ainsi la France, comme d'autres pays, harmonise et centralise les opérations de qualification du don au sein de plateaux techniques, afin de maîtriser tous les paramètres impliqués et cherche à mettre en oeuvre des procédures permettant de justifier de la qualité du dépistage et de son homogénéité.
Enfin, nous retrouvons les concepts Qualité dans un élément de base de la nouvelle organisation de la transfusion sanguine en France, l'hémovigilance.
L'hémovigilance a pour objectif principal d'analyser des incidents et des accidents liés
à
une transfusion sanguine, et surtout, d'entreprendre toutes mesuresafin
qu'ils ne se reproduisent pas.Recueillir et analyser des données, et corriger des défaillances, sont des principes importants de la Qualité. Cela fait de l 'hémovigilance un outil de sécurité transfusionnelle unique.
Nous venons de voir que la transfusion sanguine est en pleine mutation. Cette réorganisation envisage l'intégration des concepts Qualité afin d'atteindre une sécurité transfusionnelle maximale.
La Qualité est à présent, un enjeu majeur pour les partenaires de la transfusion sanguine. En effet, elle est devenue une obligation légale pour les établissements de transfusion sanguine et nous évoluons vers une maîtrise des opérations de collecte du don, de préparation, de conservation, de distribution des produits sanguins.
Mais la transfusion sanguine ne se résume pas à cette étape de production des produits sanguins, elle a aussi une dimension médicale dans laquelle les établissements de transfusion sanguine sont partie prenante, sous la forme de conseils médicaux, d'enseignement, d'élaboration de protocoles, mais qui implique surtout les établissements de soins.
Qu'en est-il des obligations légales en matière de transfusion sangmne des établissements de soins ?
Comment réagissent-ils face à la nouvelle organisation de la transfusion sanguine? Comment abordent-ils les concepts Qualité
?
C'est à ces 3 questions que nous allons tenter de répondre maintenant. I.3 LES ETABLISSEMENTS DE SOINS FACE A LA NOUVELLE ORGANISATION DE LA TRANSFUSION SANGUINE
1.3.1 les obligations légales des Etablissements de Soins, en matière de transfusion sanguine
L'Etablissement de soins est impliqué
à
différents niveaux dans le processus transfusionnel à savoir, dans la prescription médicale, dans la réception des produits sanguins distribués par l'E.T.S., dans la transfusion elle-même et enfin dans le suivi du receveur.La circulaire du 15 Janvier 1992, relative au suivi de la sécurité transfusionnelle entre les E.T.S. et les E.S. précise les rôles et les compétences de chacun, afin de favoriser leur collaboration et de faciliter les enquètes transfusionnelles en permettant la filiation donneur <=> receveur. ( 11)
Concernant les établissements de soins, nous retrouvons d'abord dans ce texte, des règles claires de prescription et d'utilisation des produits sanguins et un chapitre
réservé à la vigilance dans l'acte transfusionnel. A ces niveaux, les responsabilités des médecins prescripteurs sont précises.
Sur le plan de la distribution des produits sanguins, les E.S. sont tenus de «fixer explicitement des règles internes de circulation avec des lieux de conservation peu nombreux et prédéterminés et avec des équipements de conservation qualitativement et quantitativement satisfaisants. » (11)
Cependant, la maîtrise des circuits intrahospitaliers implique largement les B.T.S. qui « doivent prendre les dispositions nécessaires pour que la distribution de leurs produits sanguins, à l'intérieur et à l'extérieur de l'établissement s'établisse sur des circuits élaborés et bien définis. » «Ils doivent pouvoir intervenir à tout moment, tout au long de la chaine qu 'ils contrôlent, pour qu 'un produit suspect puisse être retiré de l 'utilisation thérapeutique. »( 11)
Cette notion se retrouve également dans l'arrêté du 29 Juillet 1992 fixant les conditions auxquelles doivent satisfaire les B.T.S. pour conserver le bénéfice de l'agrément. L'article 6 prévoit que
«
lorsque du sang ou des produits sanguins sont conservés dans un établissement de soins, l' E. T.S. s'assure que les conditions de conservation garantissent la sécurité notamment, en ce qui concerne les locaux et les matériels. »Donc, d'après ces textes, dès qu'un produit sanguin sort d'un B.T.S., il rentre dans un circuit transfusionnel hospitalier, bien défini par les E.S. qui veillent à assurer la qualité des lieux et des équipements de stockage. Cependant, la conservation de ce produit sanguin reste sous le contrôle del' B.T.S. distributeur qui peut intervenir à tout moment, pour vérifier les conditions de sécurité mises en place par l'E.S ..
Les Bonnes Pratiques de Distribution établies par l' Agence Française du Sang, doivent aboutir à la maîtrise des circuits de distribution des produits sanguins labiles, tant dans les B.T.S. que dans les E.S ..
Elles constituent un outil essentiel pour l'amélioration des circuits des produits sanguins labiles, en reprenant de façon précise et poussée les outils de la Qualité. Cependant, nous pouvons déjà repréciser qu'elles ne sont d'application obligatoire que pour les B.T.S. et qu'elles n'impliquent que très vaguement, à titre de collaboration, les E.S. dans la démarche Qualité.
Enfin, en matière de suivi des receveurs, les obligations des E.S. sont clairement écrites dans la circulaire du 15 Janvier 1992 qui insiste sur le fait« qu 'E. T.S. et E.S. doivent posséder des systèmes d'enregistrement des informations qui permettent de suivre un produit ou une procédure, depuis la première étape jusqu'à la dernière, du donneur au receveur et de participer à l 'hémovigilance.
» (
11)Ces obligations des E.S. en matière d'hémovigilance se retrouvent dans le décret d'hémovigilance de 24 Janvier 1994.
1.3.2 Réactions et adaptation des établissements de soins
à
la nouvelle organisation de la transfusion sanguineLa réforme de la transfusion sanguine voit les responsabilités et les missions des équipes médicales renforcées notamment, dans le domaine de la prescription et du suivi du malade.
Elle aboutit à des changements plus ou moins bien perçus, tant sur le plan de l'exercice des professions concernées que sur le plan organisationnel.
1.3.2.1 Réforme et exercice professionnel dans les E.S.
Nous nous limitons à deux grandes catégories de personnels impliqués dans l'aspect médical de la transfusion sanguine, le médecin prescripteur et plus particulièrement l'anesthésiste réanimateur, et d'un autre côté, le personnel soignant.
Sur le plan de la prescription médicale, de nombreuses instructions se retrouvent dans les textes règlementaires. La prescription de produits sanguins doit être écrite par un médecin et en aucun cas par un( e) infirmier( e ).
De plus, la circulaire du 15 Janvier 1992 précise que« les médecins doivent prescrire
aux malades, les produits les plus adaptés, en évitant toutes les indications qui ne sont pas strictement justifiées et en ne retenant que les produits et les techniques les plus
sûres. »
Cette notion est capitale, pour les prescripteurs de produits sanguins, qui doivent redoubler de prudence et de vigilance dans leur prescription de produits sanguins. En effet, l'affaire du sang contaminé a entraîné une évolution des mentalités concernant la responsabilité médicale en matière de transfusion sanguine. Le patient aujourd'hui, ne veut pas seulement être soigné, en accord avec les progrés de la science, c'est à dire avec obligation de moyens, il veut être guéri et surtout il refuse d'assurer les conséquences du risque thérapeutique. On s'aligne donc sur l'obligation de résultats tant à l'échelon national qu'à l'échelon européen. (60)
Ainsi, à présent, la responsabilité du médecin peut être recherchée en cas d'indications transfusionnelles inadaptées, de même si la transfusion est elle-même rendue nécessaire en raison d'une faute médicale. (48)
Une fois le produit sanguin prescrit, médecins et personnel soignant sont partie prenante dans la mise en place de la traçabilité.
Afin que les E.T.S. distributeurs soient capables d'identifier le receveur effectif d'un produit sanguin, il faut que le personnel des E.S. assure la saisie d'informations au lit du malade, après la transfusion.
Beaucoup affirment que cela est déjà pratiqué. Mais il faut modérer ces propos car, noter à postériori dans le dossier du patient qu'il a reçu tel produit sanguin est une information inerte. Il faut transmettre ces données de façon à ce qu'elles soient intégrées à un système informatique exploitable par les E.T.S ..
A ce titre, l 'Agence Française du Sang a publié la directive technique du 08 décembre 1994 relative à l'informatisation de la traçabilité.
Il semble que le message de la traçabilité ait eu du mal à passer auprès des médecins anesthésistes qui invoquent le manque de temps et vivent cette démarche comme une contrainte administrative supplémentaire. (36)
Toujours dans le cadre de l'hémovigilance, les deux professions doivent s'impliquer dans le suivi du receveur et dans le recueil de tout incident ou accident lié ou succeptible d'être lié à une transfusion sanguine. Ils doivent s'organiser autour de ces activités et apprendre à transmettre, en toute confiance, toute déclaration d'incident à un nouvel interlocuteur, le correspondant d'hémovigilance de l'établissement de soins. Enfin, l 'hémovigilance demande l'élaboration et la gestion de nouveaux documents comme les fiches d'incidents transfusionnels, le dossier transfusionnel et le dossier d'enquête, dont les premiers utilisateurs sont les personnels soignant et médical.
Nous venons de voir les nouvelles bases de la pratique de la transfusion sanguine dans les établissements de soins. Certaines existaient déjà, mais font l'objet de précisions complémentaires.
Ces notions apparemment sensées et indispensables à une sécurité transfusionnelle maximale, placées dans le contexte quotidien ne sont pas toujours faciles à appliquer, pour des raisons de manque de temps, de moyens et d'effectif.
Mais il est évident que les établissements de soins et leurs personnels doivent rapidement si conformer pour deux raisons, d'une part regagner la confiance des patients et d'autre part, pour faire face aux nouvelles données en matière de responsabilité médicale.
1.3.2.2 Réforme et nouvelles structures dans les E.S.
Au début de la mise en place du nouveau paysage règlementaire de la transfusion sanguine en France, la circulaire du 15 Janvier 1992 pose la première véritable brique d'une collaboration étroite entre les B.T.S. et les E.S., afin d'assurer une sécurité transfusionnelle maximale et la traçabilité donneur
<=>
receveur.En effet, il est demandé à chaque E.S. de «mettre en place une coordination centralisée de l'activité transfusionnelle ... » A cette fin, il est suggéré de « créer une
instance appropriée composée de représentants du corps médical, de représentants du personnel soignant, médicotechnique et administratif et du Directeur de l 'E. T.S..
»
(11)
Les objectifs de cette coordination sont de :
• «mettre en évidence un consensus sur des standards de pratiques
transfusionnelles
»
• «
améliorer dans sa globalité, le fonctionnement de l'ensemble de l'activité transfusionnelle au sein de chaque E.S.»
(11)Si le regroupement de telles compétences était formulé sous forme de souhait dans cette circulaire, nous le retrouvons clairement défini dans le décret du 24 Janvier 1994 relatif aux règles d'hémovigilance qui dispose que dans chaque E.S., un Comité de Sécurité Transfusionnelle d'établissement, que nous avons déjà cité, doit être constitué.
Suite à la publication de ces textes, un grand nombre de comités transfusionnels hospitaliers a vu le jour, chacun ayant un nom, une organisation et des missions propres et adaptées à chaque situation.
A ce propos, un état des lieux du fonctionnement de ces comités hospitaliers transfusionnels a été réalisé sous forme d'enquête, un an après la publication de la circulaire du 15 Janvier 1992. Elle n'est pas le reflet exact de la situation car seuls les E.T.S. ont été interrogés; or ils ne participent pas tous à des comités. Cependant, cette enquête permet de mesurer le degré de motivation des E.S .. (52)
Sur le plan des structures, sont distingués :
• Comité unique d'un établissement de soins public ou privé (le plus courant) • Comité regroupant des représentants d'autres établissements de soins (Lille) • Comités centraux coordonnant plusieurs comités dans des établissements de
soins d'un département
• Structure universitaire regroupant tous les établissements de soins publics et privés du département
En conséquence, le nombre de membres vane de 6 à 84 avec une composition moyenne:
60 % de personnel médical 22 % de personnel paramédical 11 % d'administratifs
Les principales missions de tels comités sont :
• l'amélioration de la prescription, la rédaction de guide d'utilisation des produits sangmns
• le dossier transfusionnel, le lien receveur
<=>
donneur et la traçabilité des produits sanguins• l'information et le suivi du patient.
• une forte demande de protocoles rigoureux concernant le circuit, les règles de prescription et les Bonnes Pratiques Transfusionnelles, de la part du personnel soignant,
e une bonne représentation du personnel paramédical, élément dynamique indispensable pour le fonctionnement des comités hospitaliers de transfusion.
Par contre, un point faible est souligné, à savoir qu'un comité sur deux révèle avoir des problèmes liés à la présence et à la motivation des médecins.
L'explication de cette faible implication des médecins repose sur trois raisons principales :
• fragilisation de l' Administration de la Santé qm la pnve d'une légitimité nécessaire à toute action d'envergure,
• méfiance traditionnelle de la profession médicale pour tout ce qui ressemble de prés ou de loin à une organisation administrative,
• «
rebellion »de la profession médicale vis-à-vis de tout ce qui peut sembler être une atteinte à la liberté d'exercice (69)1.3.3 Commentaires
Les établissements de soins comme les établissements de transfusion sanguine compte tenu de leur très large implication dans la transfusion sanguine, doivent faire face à un bouleversement dans leurs pratiques transfusionnelles.
Certains hospitaliers ne sont pas encore convaincus de l'intérêt de tels changements qu'ils ressentent comme de nouvelles contraintes et comme une entrave à leur liberté d'exercice.
Certes, sous ces nouveaux textes règlementaires, regroupés dans le tableau suivant transparaît la volonté d'uniformiser des pratiques et d'homogénéiser le système transfusionnel sur le plan national.
Mais, si ces objectifs sont fixés, les moyens pour les atteindre ne sont pas formellement imposés. Ce qui laisse libre cours aux différents acteurs de la transfusion sanguine pour se conformer à ces nouvelles dispositions, pour ainsi, restaurer rapidement l'image de la transfusion sanguine.
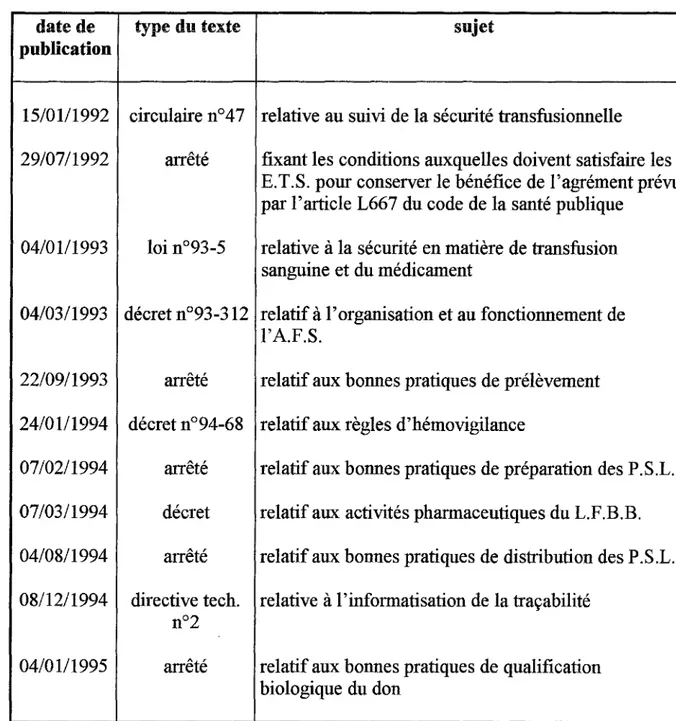
Tableau A : liste non-exshautive des textes règlementaires consécutifs à la réforme de la transfusion sanguine
date de type du texte sujet
publication
15/01/1992 circulaire n ° 4 7 relative au suivi de la sécurité transfusionnelle 29/07/1992 arrêté fixant les conditions auxquelles doivent satisfaire les
B.T.S. pour conserver le bénéfice de l'agrément prévu par l'article L667 du code de la santé publique
04/01/1993 loi n°93-5 relative à la sécurité en matière de transfusion sanguine et du médicament
04/03/1993 décret n°93-312 relatif à l'organisation et au fonctionnement de l'A.F.S.
22/09/1993 arrêté relatif aux bonnes pratiques de prélèvement 24/01/1994 décret n°94-68 relatif aux règles d'hémovigilance
07/02/1994 arrêté relatif aux bonnes pratiques de préparation des P.S.L. 07/03/1994 décret relatif aux activités pharmaceutiques du L.F.B.B. 04/08/1994 arrêté relatif aux bonnes pratiques de distribution des P.S.L. 08/12/1994 directive tech. relative à l'informatisation de la traçabilité
n°2
04/01/1995 arrêté relatif aux bonnes pratiques de qualification biologique du don
1.4 CONCLUSION
A travers ce chapitre, nous venons d'exprimer l'entrée des concepts Qualité en médecine transfusionnelle, suite à la réforme du système transfusionnel français.
L'étude des textes règlementaires fait apparaître une différence d'exigences pour les B.T.S. et pour les E.S ..
En effet, les B.T.S. ont à satisfaire des exigences Qualité alors que les E.S. doivent répondre à des exigences de sécurité uniquement.
Cette incohérence dans les exigences des deux partenaires principaux de la transfusion sanguine risque d'entraîner un décalage dans leurs objectifs et donc, dans les moyens entrepris pour les atteindre.
De plus, cela ne facilitera pas la mise en oeuvre du changement de mentalité nécessaire pour opérer en profondeur cette mutation.
Cependant, il apparait que, compte tenu de leur implication dans le processus transfusionnel, les E.S. prennent largement conscience que le circuit transfusionnel hospitalier ne peut pas fonctionner efficacement sans connaître les principes de Qualité.
En effet, il serait aberrant qu'un produit sanguin rigoureusement qualifié, préparé conservé et distribué par un E. T .S. selon des procédures écrites, se retrouve dans un milieu hospitalier n'intégrant pas les mêmes concepts.