T
T
H
H
È
È
S
S
E
E
En vue de l'obtention du
D
D
O
O
C
C
T
T
O
O
R
R
A
A
T
T
D
D
E
E
L
L
’
’
U
U
N
N
I
I
V
V
E
E
R
R
S
S
I
I
T
T
É
É
D
D
E
E
T
T
O
O
U
U
L
L
O
O
U
U
S
S
E
E
Délivré par l'Université Toulouse III - Paul Sabatier Discipline ou spécialité : Physique et ingénierie des plasmas
JURY
Olivier Eichwald (Président, PR UPS) Thierry Belmonte (Rapporteur, DR CNRS)
Vincent Puech (Rapporteur, DR CNRS) André Ricard (Directeur de thèse, DR CNRS) Jean Philippe Sarrette (Directeur de thèse, CR CNRS)
Franck Clément (MCF UPPA) Maria David (PR INP) Pierre Vervisch (DR CNRS)
Ecole doctorale : GEET Unité de recherche : LAPLACE
Présentée et soutenue par Benoît Rouffet Le 30 juin 2008
Titre : Etude d'un réacteur de post-décharge d'azote en flux dédié à la décontamination de l'instrumentation médicale.
Application à la détermination des probabilités de recombinaison hétérogène de l'azote atomique
Table des matières
Avant propos ...7
Chapitre 1 : Généralités, concepts de base et résultats antérieurs
...11
I. Rappels et définitions : ... 12
I.1. Etat plasma – Rappels sur la structure des atomes et des molécules :... 12
I.2. Azote atomique et azote moléculaire :... 21
II. Décharge et post-décharge micro-ondes d’azote : ... 24
II.1. Décharge :... 24
II.2. Post-décharge spatiale : ... 25
II.2.1. Proche post décharge :... 26
II.2.2. Lointaine post décharge :... 27
III. Stérilisation du matériel médical : ... 28
III.1. Définitions :... 29
Table des matières
Rouffet Benoît 2
III.2.1. Stérilisation par chaleur sèche :... 30
III.2.2. Stérilisation par rayonnements ionisants (radio-stérilisation) : ... 31
III.2.3. Stérilisation par vapeur d’eau (autoclave) :... 31
III.2.4. Stérilisation par oxyde d’éthylène C2H4O :... 32
III.3. Travaux antérieurs du groupe en décontamination bactérienne :... 34
III.4. Température des substrats : ... 37
IV. Recombinaison des atomes d’azote sur les surfaces : ... 39
IV.1. Généralités sur l’adsorption : ... 39
IV.2. Physisorption et chimisorption : ... 40
IV.3. Recombinaison atomique de surface : ... 41
IV.3.1. Mécanismes :... 41
IV.3.2. Probabilité de recombinaison γ : ... 43
IV.3.3. Taux de recombinaison à la paroi : ... 46
IV.3.4. Etat de l’art sur la probabilité de recombinaison de surface des atomes d’azote :... 47
V. Conclusion :... 48
Chapitre 2 : Etude expérimentale ...51
I. Dispositif expérimental : ... 51
I.1. Alimentation des gaz : ... 53
I.2. Surfatron (source plasma) :... 53
I.3. Injecteur : ... 55
I.4. Enceinte de travail : ... 56
I.5. Acquisition optique :... 57
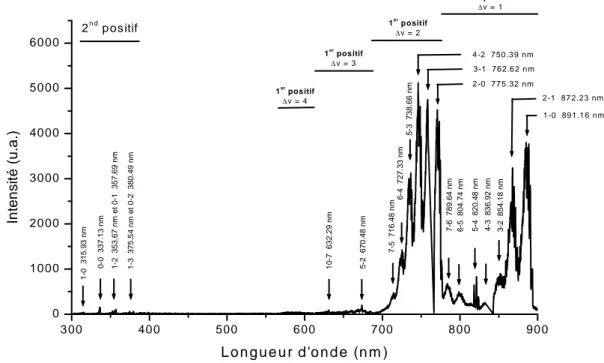
II. Spectroscopie d’Emission Optique de la post décharge d’azote : ... 57
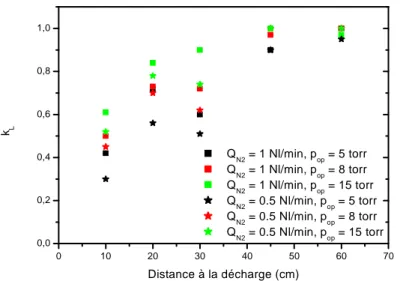
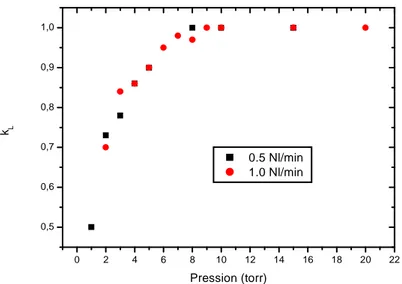
II.1. Critère d’évaluation des zones de proche et lointaine post-décharges : ... 65
II.2. Mesure de la concentration en atomes d’azote par spectroscopie d’émission optique :... 69
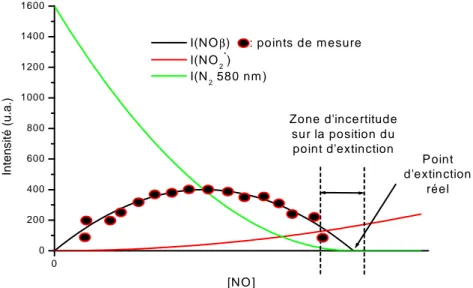
II.2.1. Titrage chimiluminescent au monoxyde d’azote NO : ... 69
II.2.2. Suivi de l’intensité de la tête de bande 11-7 du 1er système positif de l’azote à 580,43nm :... 72
II.2.3. Discussion :... 74
II.2.4. Résultats : ... 76
III. Fluorescence induite par laser : ... 80
III.1. Principe : ... 80
III.2. Théorie : ... 82
III.3. Calibration :... 84
IV. Système d’excitation et de récolte des photons de fluorescence : ... 88
IV.1. Laser Nd-YAG :... 88
IV.2. Laser à colorant :... 89
IV.3.1. Système de détection :... 92
IV.3.2. Intégrateur-moyenneur BoxCar et acquisition : ... 95
IV.3.3. Choix du colorant :... 97
IV.4. Mesures TALIF à l’entrée du réacteur :... 98
IV.5. Comparaison des mesures de la densité d’atomes N obtenues par titrage au NO et par TALIF en entrée de réacteur : ... 99
IV.6. Comparaison des mesures de la densité d’atomes N obtenues par TALIF et à partir de l’émission à 580 nm : ... 100
V. Température du gaz de post décharge :... 101
V.1. Mesure de la température de surface de matériaux par thermocouple : ... 101
V.2. Modélisation du spectre d’émission du 1er système positif de l’azote : ... 103
VI. Conclusion : ... 114
Chapitre 3 : Modélisation du réacteur de post-décharge ...117
I. Equations utilisées : ... 118
II. Méthode de résolution, maillages et conditions aux limites :... 122
III. Etude préliminaire de la zone d’injection :... 124
IV. Modélisation du réacteur vide :... 129
IV.1. Intensité des vitesses : ... 129
IV.2. Densité en atomes [N] :... 131
IV.3. Ratios Rci :... 132
IV.4. Etude paramétrique : ... 133
IV.5. Profils de densité axiaux : ... 136
IV.6. Conclusions partielles : ... 137
V. Détermination des
γγγγ
Nà partir de mesures d’échauffements de
matériaux :... 139
VI. Détermination des probabilités
γγγγ
Nà partir des profils de densité au
voisinage des matériaux : ... 145
VII. Conclusion : ... 155
Chapitre 4 : Décontamination de substrats tubulaires par
post-décharge d’azote en flux ...157
Table des matières
Rouffet Benoît 4
II. Décontamination de substrats tubulaires dans le réacteur : ... 160
III. Décontamination de substrats tubulaires en amont du réacteur : . 161
IV. Conclusion : ... 165
Conclusion et perspectives ...167
Références ...173
Remerciements
Au départ rien ne m’emmener vers les plasmas mais le chemin de ma vie devait passer par là. Et quelle chance, merci à toi Jean Baptiste de m’avoir aiguiller sur cette voie.
Je remercie dans un premier temps les membres du jury qui m’ont fait l’honneur de regarder mes travaux de thèse.
Je suis arrivé dans un laboratoire très sympathique en pleine mutation. Je remercie donc tout le personnel de m’avoir fait un tel accueil qui m’a permis de finir ma formation et de m’épanouir : l’accueil de la direction (Alain, Georges, Christian) pour leurs disponibilités, l’accueil administratif (Myriam, Soraya, Agnès, …) qui m’ont aider dans mes démarches et l’accueil technique (Julien, Jean-luc, Alain, Roland, Franck, Jacques, Sounil, ...).
Je remercie l’ensemble de l’équipe PRHE tant au niveau de la recherche et de l’administratif (Mohammed, Marie Claude, Nofel, Michel, Gérald, …) qu’au niveau des enseignements (Olivier, Vassante, Frédéric, …). Je remercie aussi l’équipe MMP pour le partage de la manipulation laser.
Avant propos
Rouffet Benoît 6
Ensuite , je remercie mes encadrants, tuteurs et amis : André, pour avoir accepter d’être mon directeur de thèse et pour ces conseils ; Freddy et Jean Philippe l’un pour la partie expérimentale, l’autre pour la partie modélisation pour leurs disponibilités, leurs échanges, leurs conseils, …
Après je pense à mes amis dont la liste est longue : ceux du laboratoire (François, Jasmine, Aude, Et-touhami, Ionut, Sarah, Youssef, Mathieu, Nicolas, …) et ceux d’ailleurs (Yacine, Georges, Olivier, les Nicos, Mélanie, Sandrine, Violaine, …).
Tout cela n’aurait pas été possible sans ma famille, qui m’a soutenu, encouragé, supporté, aimé, …
Avant propos
Aujourd’hui, la stérilisation des dispositifs médicaux dans les établissements de santé occupe une place primordiale dans la lutte contre les infections. Le code de déontologie, la loi hospitalière et ses textes d'application rappellent l’obligation, pour les professionnels et les structures de soins, d'assurer la sécurité des patients vis à vis du risque infectieux.
L'obtention de l’état stérile et son maintien jusqu'au moment de l'utilisation correspondent dorénavant à une obligation de résultat, les établissements de santé devant mettre en place un système qualité basé sur des référentiels normatifs relatifs aux exigences des dispositifs stérilisants utilisés. Cependant, les matériels médicaux de haute technologie (et de coût élevé) sont de plus en plus incompatibles avec les techniques de stérilisation éprouvées. Certaines classes d’instruments (endoscopes, fibroscopes) dont on sait pertinemment qu’ils constituent des vecteurs privilégies de transmission des infections nosocomiales, ne sont pas stérilisés entre chaque utilisation, faute de moyen approprié.
Avant propos
Rouffet Benoît 8
Les décharges et post-décharges dans les gaz ont démontré depuis longtemps leur intérêt, notamment pour le traitement des matériaux mais ce n’est qu’au cours de la dernière décennie que l’on a vu exploser le nombre de travaux liant la physique des décharges aux sciences du vivant et traitant en particulier des potentialités des procédés plasmas appliqués à la stérilisation de l’instrumentation médicale. Cette voie, encouragée par les forts enjeux économiques et sociétaux qui s’y rattachent, semble très prometteuse bien que l’interaction avec le monde du vivant soit un sujet difficile d’approche de par la pluridisciplinarité qu’elle impose et de par la complexité des phénomènes physico-bio-chimiques mis en jeu.
Depuis 2001, les travaux réalisés dans l’équipe Plasmas Réactif Hors Equilibre (PRHE) du LAboratoire PLAsma et Conversion d’Energie (LAPLACE) ont permis de démontrer l’efficacité antibactérienne d’une post-décharge en flux basse pression dans le mélange azote-oxygène (thèse de Sandrine Villeger, 2004), puis dans l’azote pur (thèse de Sarah Cousty, 2007). L’optimisation du procédé de stérilisation basé sur cette post décharge implique une bonne compréhension de l’hydrodynamique et de la cinétique chimique de l’écoulement réactif entre la zone de production des espèces actives (décharge) et la zone de traitement (réacteur). Ceci a constitué l’objectif principal de cette thèse, centré sur la mise en place d’un moyen de diagnostic de la concentration locale en atomes d’azote (la fluorescence induite par laser à deux photons), identifiés précédemment comme le vecteur essentiel de la décontamination pour le procédé.
Dans le premier chapitre, nous rappellerons succinctement quelques éléments sur la structure de la matière et décrirons les zones de décharge (plasma) et de post décharge proche et lointaine. Les définitions de base et les moyens actuels de la stérilisation seront ensuite évoqués. Une fois les principaux résultats obtenus précédemment par notre groupe présentés
brièvement, ce chapitre se terminera par une présentation des notions essentielles de la recombinaison atomique sur les surfaces et par une revue des probabilités de recombinaison hétérogène de l’azote atomique, disponibles dans la littérature.
Le second chapitre sera dédié à la description du dispositif expérimental et aux différents moyens de diagnostic utilisés (spectroscopie optique d’émission, fluorescence induite par laser, mesures de température); un rappel théorique sera fait sur chacun d’eux.
Le troisième chapitre décrira le modèle fluide tridimensionnel de la post-décharge que nous avons réalisé à l’aide du code commercial Fluent. Les cartographies mesurées et calculées de la concentration en atomes d’azote seront comparées, permettant d’obtenir les variations avec la pression de la probabilité de recombinaison de l’azote sur différents matériaux.
Enfin, un court quatrième chapitre présentera les premiers résultats encourageants concernant l’utilisation du procédé de post décharge d’azote en flux pour la désinfection de tubulures de faible diamètre.
Chapitre
1 : Généralités, concepts de base et
résultats antérieurs
L’objectif de ce chapitre est de placer notre travail dans son contexte et d’introduire différentes notions utiles pour la suite de l’étude. Une présentation rapide sera faite sur la matière, les décharges dans les gaz, les post-décharges et leurs applications actuelles. Le point sera ensuite fait sur les travaux antérieurs relatifs à la décontamination de matériel médical par procédé post décharge en flux sous basse pression à base d’azote. Le lien sera rappelé entre l’efficacité du procédé et la montée en température des substrats. Enfin, le thème de l’interaction gaz - surface sera abordé avec une présentation du processus de recombinaison des atomes sur les surfaces et une revue bibliographique des probabilités de recombinaison de l’azote atomique disponibles dans la littérature.
Chapitre 1 : Généralités, concepts de base et résultats antérieurs
Rouffet Benoît 12
I.
Rappels et définitions :
I.1.
Etat plasma – Rappels sur la structure des atomes et des
molécules :
[V.N. Kondratiev, 1964] et [G. Hertzberg, 1950].
La matière est composée d’un ensemble de particules : atomes, molécules... On peut représenter les atomes par un noyau chargé positivement autour duquel gravitent les électrons chargés négativement et les molécules comme un groupe d’atomes énergétiquement liés les uns aux autres.
La matière est classiquement ordonnée en trois états (solide, liquide, gazeux) selon l’intensité des énergies de liaison des particules qui la composent. L’état plasma (souvent appelé quatrième état de la matière) est obtenu soit lorsque l’énergie cinétique moyenne des particules Ec est supérieure à l’énergie d’ionisation du gaz Ei, soit par collision avec des
particules d’énergie supérieure à l’énergie d’ionisation.
Le plasma est donc un milieu ionisé composé d’un mélange de particules neutres n0,
de particules chargées positivement (anions) n+ et de particules chargées négativement
(électrons et cations) n-. Il possède les mêmes propriétés mécaniques (écoulements, ondes
acoustiques, etc.) que le gaz neutre mais, bien qu’électriquement neutre à l’échelle macroscopique (n+ = n-), ses propriétés électromagnétiques (conductivité électrique, indice de
réfraction) en diffèrent par suite de la présence d'électrons libres en son sein.
Dans le cas d’un plasma formé de particules neutres (n0), d’ions positifs (ni) et
d’électrons (ne), il est possible de classer les plasmas en fonction de leur degré d’ionisation
α
= ne / (ni + n0) dont la valeur varie en pratique depuis des valeurs très faibles, de l'ordrede 10-10, jusqu'à 1. Les plasmas dits « chauds » correspondent à des degrés d’ionisation importants (
α
> 0.1). Notre étude concerne les plasmas dits « froids ou faiblement ionisés », pour lesquelsα
est typiquement compris entre 10-4 et 10-7.Une autre grandeur fondamentale des plasmas est la température T, mesure de l’énergie cinétique moyenne des particules (Ec = 3/2 kB.T, où kB = 1,380662.10-23 J.K-1 est la
constante de Boltzmann), qui peut devenir du même ordre que leur énergie d'ionisation Ei.
Dans ces conditions, lorsque deux particules entrent en collision, il peut y avoir ionisation de l'une d'entre elles. Si le gaz est en équilibre thermodynamique (ET), ce processus est contrebalancé (principe de micro-réversibilité) par un processus de recombinaison entre un ion et un électron. L’ionisation est déterminée par les conditions de pression et de température, il en résulte que les grandeurs
α
, n (densité totale, n = n0 + ne + ni) et T ne sontpas indépendantes,.
Dans de nombreux cas, et dans la suite de cette étude, l’ionisation est due à un champ électrique extérieur, et le gaz n'est pas en équilibre thermodynamique. Il atteindra souvent un état stationnaire que l'on pourra caractériser par les paramètres Te (température des électrons),
Ti (température des ions) et Tn (température des neutres). Les transferts de quantité de
mouvement et d’énergie cinétique entre les électrons, facilement accélérés par le champ électrique et les particules lourdes du gaz (ions et neutres) sont en général faibles et l’on considère le plus souvent que Ti = Tn = Tg(température du gaz).
Chaque particule (atome, molécule) possède différents états d’énergie interne. Pour les atomes, la distribution de ces états est discrète (discontinue) et correspond aux différentes orbitales atomiques dont l’évolution dans l’espace est régie par une équation aux dérivées
Chapitre 1 : Généralités, concepts de base et résultats antérieurs
Rouffet Benoît 14
partielles, l’équation de Schrödinger. Toute variation d’énergie de l’atome est la conséquence du passage d’un électron d’une orbite à une autre.
Pour les atomes hydrogénoïdes pour lesquels un électron unique gravite autour du noyau, les fonctions d’onde (orbitales) solutions exactes de l’équation de Schrödinger font intervenir quatre nombres appelés "nombres quantiques" : n, l, m et s :
• n : nombre quantique principal (n = 1,2,3,…∞) qui définit la couche quantique (énergie de l'électron). On appelle couche l'ensemble des orbitales qui possèdent la même valeur de n.
• l est le nombre quantique orbital ou azimutal, il peut prendre toutes les valeurs comprises entre 0 et n-1. l définit la notion de sous-couche et détermine la géométrie des orbitales atomiques. Il y a 2l+1 orbitales.
• m est le nombre quantique magnétique, il définit la case quantique. m peut prendre toutes les valeurs comprises entre -l et +l.
Chaque orbitale atomique est donc caractérisée par une combinaison des trois nombres quantiques n, l et m. Pour une même valeur de l’énergie (fixée par n), plusieurs fonctions d’onde peuvent-être représentatives de l’électron, la valeur de l’énergie correspondante est dégénérée.
Dans la notation spectroscopique, à chaque valeur de l correspond une fonction d'onde désignée par une lettre : s pour l = 0, p pour l = 1, d pour l = 2, f pour l = 3, etc…
Pour décrire totalement l'état de l’électron, il faut lui attribuer un quatrième nombre quantique s, lié à la rotation de l’électron sur lui-même. Ce nombre ne peut prendre que deux valeurs s = ±1/2.
On utilise aussi le nombre quantique j lié au moment cinétique total couplant moment orbital et moment de spin. Les valeurs possibles de j sont fixées par la relation :
│l-s│< j < l+s.
Pour les atomes à plusieurs électrons, l’équation de Schrödinger n'admet que des solutions approchées, calculées en minimisant les répulsions inter-électroniques. Il y a couplage entre les moments individuels orbitaux, magnétiques et de spin, définissant les nombres quantiques L (associés aux orbitales S, P, D, … selon que L = 0, 1, 2, …), M et S. La multiplicité totale du niveau est alors égale à 2S+1.
Pour les atomes de faible numéro atomique, le couplage est maximal entre les moments résultants L = Σli et S = Σsi, définissant le nombre quantique résultant J. La notation du niveau est alors : 2S+1LJ.
Pour les atomes de numéro atomique important, il y a d’abord couplage entre le moment orbital et le moment de spin de chaque électron, faisant apparaître le nombre quantique interne ji, puis interaction entre les différents moments internes.
Un atome est dans son état fondamental lorsque ses différents électrons remplissent l’ensemble des couches possibles de plus basses énergies. Cet atome passe dans un état excité lorsque l’un des électrons du cortège passe sur une couche d’énergie supérieure.
Toutes les transitions entre les états ne sont pas permises. Pour le couplage L-S, dans l’approximation dipolaire électrique, les transitions permises doivent obéir aux règles de sélections suivantes :
∆L = 0, ±1 mais L = 0 → L = 0 est interdite, ∆J = 0, ±1 mais J = 0 → J = 0 est interdite,
Chapitre 1 : Généralités, concepts de base et résultats antérieurs
Rouffet Benoît 16
∆S = 0, aucune transition ne peut avoir lieu entre niveaux de multiplicités différentes.
L’assemblage de deux ou plusieurs atomes est appelé molécule, néanmoins nous ne considérerons ici que le cas des molécules diatomiques. Comme pour les atomes, chaque électron de la molécule est décrit par une fonction d’onde Φ appelée orbitale moléculaire. Pour que la molécule puisse exister de façon stable, elle doit posséder au moins une orbitale liante ayant une énergie plus faible que celle des orbitales atomiques indépendantes. Dans la méthode LCAO (Linear Combination of Atomic Orbitals), l’orbitale moléculaire Φ est définie à partir d’une combinaison linéaire des orbitales atomiques Ψ. Dans le cas d’une molécule AB, on aura :
Φ = c1ΨA + c2ΨB, où c1 et c2 sont des coefficients réels. (I.1)
Tout comme pour les atomes, chaque état électronique moléculaire est défini par :
• le moment angulaire électronique Lr et sa projection Λr sur l’axe internucléaire, caractérisé par le nombre quantique Λ (Λ = 0, 1, 2, …) définissant le type d’orbitale (Σ, Π, ∆, …) ;
• la résultante Sr du spin des électrons et sa projection Σr sur l’axe internucléaire, pouvant prendre les 2S+1 valeurs (multiplicité de l’état) Σ = -S, …, +S.
Chaque valeur de Λ correspond à un état moléculaire désigné par une lettre : X pour l’état fondamental, A, B, C, … (resp. a, b, c, …) pour les états d’énergie croissante de même multiplicité que l’état fondamental (resp. de multiplicité différente).
Par ailleurs, une fonction d’onde Φ symétrique (resp. antisymétrique) par rapport à un plan contenant l'axe internucléaire sera indicée + (resp. -). Pour les molécules diatomiques
possédant un centre de symétrie, ce qui est le cas des molécules homonucléaires, les probabilités de présence des états sont les mêmes de part et d'autre de ce centre de symétrie. En conséquence, les fonctions d'onde peuvent être ou symétriques, ou antisymétriques par rapport à ce centre. On note respectivement les états symétriques g (pour gerade = pair) et les états antisymétriques u (pour ungerade = impair).
Suite aux possibles mouvements de vibration des atomes le long de l’axe internucléaire et de rotation autour de ce même axe, les états électroniques moléculaires sont dégénérés en niveaux vibrationnels (caractérisés par le nombre quantique v) et en sous niveaux rotationnels (caractérisés par le nombre quantique J). L’énergie Ee,v,J d’un état
ro-vibrationnel d’un état électronique peut se décomposer comme la somme des énergies rotationnelles Fv(J) (≈ 10-3 eV), vibrationnelle G(v) (≈ 0,1 eV) et électronique Te (quelques
eV) :
Ee,v,j = Te + G(v) + Fv(J), (I.2)
Les termes énergétiques G(v) et Fv(J) peuvent être calculés à partir des coefficients de
Klein-Dunham Yij (constantes spectroscopiques) par :
... ) 2 1 v ( y w ) 2 1 v ( x w ) 2 1 v ( w ) 2 1 v ( Y ) v ( G 3 e e 2 e e e i ,... 1 i i0 + + + + − + = + =
∑
= (I.3) 2 2 v v v(J) B J(J 1) D J (J 1) F = + + + (I.4) ... ) 2 1 v ( ) 2 1 v ( B ) 2 1 v ( Y B 2 e e e i ,... 0 i i1 v =∑
+ = −α + +γ + + = (I.5) ... ) 2 1 v ( D ) 2 1 v ( Y D i e e ,... 0 i i2 v =−∑
+ = +β + + = . (I.6)Ces expressions permettent de tenir compte des interactions mutuelles entre les différents mouvements : le couplage entre les mouvements de vibration et des électrons est
Chapitre 1 : Généralités, concepts de base et résultats antérieurs
Rouffet Benoît 18
introduit grâce à l’anharmonicité de l’expression (I.3) et le couplage vibration – rotation à travers les expressions (I.4) à (I.6) du rotateur vibrant.
Les différents cas de Hund correspondent aux différents modes de couplage possibles entre les mouvements de rotation des électrons, sachant que chacun d’eux est « idéal » et que des transitions entre ces cas ont lieu lorsque la rotation de la molécule augmente. Nous n’évoquerons ici que les deux cas les plus courants :
Dans le cas « a » de Hund, l’interaction entre le mouvement de rotation des noyaux (Nr ) et le mouvement des électrons (
L
r
+Sr) est très faible, ce dernier étant très fortement lié à l’axe internucléaire. Dans ce cas, le spin Sr se couple d’abord avec le moment orbital Lr (figure 1.1.a), conduisant à l’existence d’un moment angulaire électronique total Ωr le long del’axe, associé au nombre quantique Ω = Λ+Σ et pouvant prendre les 2S+1 valeurs
Ω = Λ−Σ , …, Λ+Σ. Ωr est ensuite couplé au moment angulaire Nr de rotation des noyaux pour former le moment résultant Jr = Ωr +Nr , associé au nombre quantique J = Ω, Ω+1, ….
Dans le cas « b » de Hund, le champ magnétique associé à Λr est si faible que l’interaction entre Λr et Sr est faible comparée à l’effet de la rotation de la molécule sur le spin. Sr n’est alors plus couplé avec l’axe internucléaire, Σ n’existe pas et Ωr n’est pas défini.
Λr et Nr forment le moment angulaire Kr = Λr+Nr (figure 1.1.b), associé au nombre quantique K = Λ, Λ+1, Λ+2, …. Kr est ensuite couplé à la résultante de spin Sr pour former le moment angulaire total Jr = Kr +Sr. Ainsi, chaque niveau K est composé de 2S+1 sous niveaux J tels que J = K+S, …, K −S .
Figure 1.1 : Couplage des différents moments angulaires dans les cas « a » et « b » de Hund.
Tout comme pour les transitions entre états atomiques, toutes les transitions entre états moléculaires ne sont pas permises.
Les transitions rotationnelles et vibrationnelles pures (sans changement d’état électronique) correspondent respectivement aux émissions dans les zones micro-ondes et infrarouge du spectre. Elles ne sont possibles que si la molécule possède un moment dipolaire électrique permanent, ce qui n’est pas le cas des molécules diatomiques homonucléaires qui vont nous intéresser dans la suite de cette étude.
Pour ce type de molécules, les seules transitions possibles correspondent à des changements d’états ro-vibrationnels d’états électroniques différents. Lorsqu’ils sont peuplés, la désexcitation radiative des différents états excités va donner lieu à l’émission d’un spectre de raies discontinu dans la zone visible – UV du spectre. La longueur d’onde λ de chaque raie dans le vide (généralement exprimée en nm) étant reliée à la différence d’énergie des deux niveaux par l’expression :
λ
hc = E
e’,v’,J’ – Ee’’,v’’,J’’ (I.7)
L
r
Λ
r
S
r
Σ
r
Ω
N
r
J
r
L
r
Λ
r
N
r
J
r
K
r
S
Cas « a » Cas « b » A BChapitre 1 : Généralités, concepts de base et résultats antérieurs
Rouffet Benoît 20
où les notations (’) et (”) désignent respectivement les niveaux supérieur et inférieur de la transition, h étant la constante de Planck (h = 6,626176.10-34 J.s) et c la vitesse de la lumière dans le vide (c = 2,99792458.108 m.s-1).
Dans la littérature, les transitions sont indifféremment répertoriées en longueur d’onde
λ, nombre d’onde σ ou fréquence ν , tels que :
ν = c . σ = c / λ (I.8)
Les règles de transition entre états électroniques concernent les propriétés de symétrie :
+ ↔ – + ↔/ + – ↔/ – et g ↔ u g ↔/ g u ↔/ u, auxquelles il faut rajouter :
1 , 0 ± =
∆Λ et ∆S = 0.
Les autres règles dépendent du cas de couplage de chacun des deux états électroniques concernés par la transition. Néanmoins, quels que soient les cas de couplage des deux états, la règle :
1 , 0 J= ±
∆ avec J’ = 0 →/ J’’ = 0 est impérative.
Lorsque les deux états électroniques obéissent au cas « a » ou au cas « b » de Hund, il faut rajouter les règles :
1 , 0 ± =
∆Λ et ∆S=0.
Ces règles permettent de distinguer les états radiatifs des états métastables pour lesquels aucune transition vers un état électronique de plus basse énergie n’est possible.
Les collisions entre les électrons et les particules lourdes sont très efficaces pour modifier l’état d’énergie interne de ces dernières (collisions inélastiques). Les transferts entre l’énergie cinétique des électrons et l’énergie interne des espèces lourdes vont conduire aux processus :
• d’excitation ou de désexcitation correspondant soit à un changement d’orbitale électronique (atomes et molécules), soit à un changement de la fréquence de vibration et/ou de rotation des molécules autour de leurs axes interatomiques ;
• de création (ionisation) ou de disparition (recombinaison) de paires électron – ion à partir des atomes et des molécules ;
• de dissociation des molécules en atomes élémentaires et de reformation des molécules à partir des atomes (on emploiera ici aussi souvent le terme recombinaison).
Les collisions entre espèces lourdes sont également susceptibles d’induire les mêmes processus inélastiques ainsi que de nombreux autres, plus spécifiques parmi lesquels les transferts d’excitation, également appelés quenching et les transferts de charge.
I.2.
Azote atomique et azote moléculaire :
L’azote atomique est un atome à 7 électrons dont l’état fondamental correspond à la structure électronique 1s2 2s2 2p3 (4S3/2). Les deux premiers états excités sont les états métastables 2p3 (2D5/2,3/2) et 2p3 (2P1/2,3/2) situés respectivement à 2,38 et 3,58 eV, le premier état radiatif est l’état 2p2 (3P) 3s (4P1/2,3/2,5/2) à 10,32 eV. Son énergie d’ionisation est de 14,53 eV. La figure 1.2 représente la répartition énergétique des niveaux électroniques tels
Chapitre 1 : Généralités, concepts de base et résultats antérieurs
Rouffet Benoît 22
que n ≤ 5 et l ≤ 3 (diagramme de Grotrian) ainsi que les principales transitions radiatives qui les relient.
Figure1. 2 : Diagramme de Grotrian partiel de l’azote atomique. [C. Park, 1990]
La figure 1.3 représente les courbes de potentiel des principaux états électroniques des molécules N et 2 N . Le premier état excité électronique de +2 N est l’état triplet 2
métastable Σ+
u 3
A , situé à 6,1 eV de l’état fondamental singulet X1Σ+g, et dont la durée de vie
radiative est de l’ordre de la seconde. Dans les conditions de notre étude, les états radiatifs impliqués dans les principaux systèmes émissifs sont les états B3Πg et C3Πu de N , situés 2
respectivement à 7,3 et 10,9 eV de l’état fondamental. Le niveau fondamental de l’ion +
2
N ,
+
Σg
2
X , est à 15,5 eV et le premier état radiatif, Σ+
u 2
B , à 18,6 eV. L’émission de l’azote moléculaire est essentiellement concentrée dans les systèmes :
• premier positif de N2 :
B3Πg → A3Σu+ + hν (470-2530 nm) (R1)
• second système positif de N2 :
C3Πu→ B3Πg + hν (260-550 nm) (R2)
• premier système négatif de N2+ :
B2Σu+→ X2Σg+ + hν (300-590 nm). (R3)
Chapitre 1 : Généralités, concepts de base et résultats antérieurs
Rouffet Benoît 24
II.
Décharge et post-décharge micro-ondes d’azote :
II.1.
Décharge :
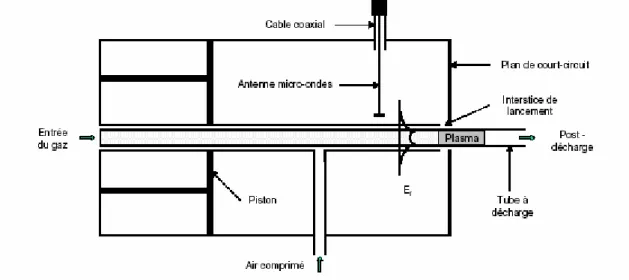
Notre étude a été réalisée dans une post-décharge en flux obtenue à partir d’un plasma d’azote à basse pression (1 – 30 Torr, avec 1 Torr = 1 mm Hg = 1 / 760 atm = 133,322 Pa) lequel est généré par une décharge micro-onde fonctionnant à 2450 MHz.
Ce type de plasma appartient à la catégorie des plasmas hautes fréquences, c’est-à-dire entretenus par un champ électrique alternatif rapide. Le domaine des hautes fréquences comprend les fréquences radio (de 1 à 300 MHz) et les fréquences micro-ondes (de 0,3 à 300 GHz). Le champ électrique haute fréquence E transmet l’énergie aux particules chargées par l’intermédiaire de la force F = qE où q est la charge de la particule. Au cours du temps, la particule acquiert dans ce champ une vitesse v inversement proportionnelle à sa masse m:
v = (qE).t / m (I.9)
La masse des ions étant élevée et le champ électrique à haute fréquence, la force électrique n’a pas le temps de mettre en mouvement les ions avant que le champ ne change de direction. Elle agit donc essentiellement sur les électrons légers et le plasma est créé par la redistribution de l’énergie cinétique des électrons vers les autres particules du gaz au cours des collisions. La basse pression induisant un faible nombre de collisions, la thermalisation avec les particules lourdes ne s’effectue pas et on obtient un plasma hors ET.
Les processus se produisant dans la zone de décharge sont extrêmement nombreux et variés [V. Guerra, 2004]. Si on se limite à la production des espèces atomiques, on observe
deux mécanismes majeurs [E. Tatarova, 1999] faisant intervenir les 46 niveaux vibrationnels stables (v = 0 – 45) de l’état fondamental X1Σ+g :
• la dissociation par impact électronique :
e + N2(X,v) → e + N + N, (R4)
• et le transfert d’énergie vibrationnelle :
N2(X,v) + N2(X,v = 45) → N2(X,v-1) + N + N, (R5)
et des processus plus minoritaires :
2 N2(X, 10 < v < 25) → N2(X) + N + N, (R6) N2(A) + N2(X, 14 < v < 19) → N2(X) + N + N, (R7) 2 N2(A) → N2(X) + N + N et (R8) e + + 2 N (X) → N + N (R9)
Les pertes en atomes d’azote sont consécutives aux réactions de recombinaison :
• en volume :
N + N + N2→ N2(B) + N2, (R10)
• et sur les parois du tube à décharge :
N + wall → ½ N2 + wall. (R11)
II.2.
Post-décharge spatiale :
Dans un montage en post-décharge spatiale, un flux de gaz continu entraîne l’ensemble des espèces produites par la décharge dans une zone aval où elles ne subissent plus l’influence du champ électrique. Dans cette zone aval, la température de la post décharge
Chapitre 1 : Généralités, concepts de base et résultats antérieurs
Rouffet Benoît 26
diminue et la composition du gaz évolue en fonction des durées de vie collisionnelles et radiatives des différentes espèces. On distingue typiquement deux régions (figure 1.4) :
• une première région extrêmement lumineuse nommée « early afterglow » ou « pink afterglow » et correspondant à la zone de proche post décharge,
• puis une région jaune orangée nommée « Lewis Rayleigh afterglow » ou lointaine post décharge.
Figure 1.4 : Les systèmes émissifs observés dans les différentes régions de post-décharge [Cousty, 2007]
II.2.1.Proche post décharge :
Dans cette zone, malgré l’absence de champ électrique extérieur, il reste suffisamment d’énergie transportée par les états métastables à longue durée de vie pour permettre une ré-ionisation du gaz [C. Normand-Chave, 1991].
Très lumineuse, cette zone se caractérise par l’émission dominante du 1er système négatif de N2+ et par la présence des 1er et 2nd systèmes positifs de N2.
Décharge Post-décharge Proche Lointaine « Pink » 1er système négatif N2+ 1er système positif N2 2nd système positif N2 « Lewis Rayleigh » Intensité maximale des
transitions
N2(B, v’ = 11) → N2(A, v’’) + hv du 1er système positif N2
Injection de N2
L’état excité +
2
N (B) est produit par un jeu de 3 réactions entre les niveaux vibrationnels excités de l’état fondamental N2(X,v) et l’état métastableN2(a’) : [J. Levaton,
2002]. N2(X, v > 15) + N2(X, v > 15) → N2(a’) + N2(X,v). (R12) N2(a’) + N2(a’) → e + N (X) + N2 +2 (R13) + 2 N (X) + N2(X, v > 11) → N (B) + N+2 2(X) (R14)
L’état N2(C) est généré par les collisions (réactions de pooling) entre les états
métastables N2(A) :
N2(A) + N2(A) → N2(C, v) + N2(X,v = 0), (R15)
Alors que l’état N2(B) est produit par les réactions :
N2(X, 4 ≤ v < 14) + N2(A, v = 0,1) → N2(B, 0 ≤ v < 12) + N2(X,v) et (R16)
N2(X,v) + N2(X,v) → N2(B, v) + N2(X). (R17)
II.2.2.Lointaine post décharge :
La zone de lointaine post-décharge se situe en aval de la pink afterglow et correspond à une zone dans laquelle les concentrations d’états métastables ne sont plus suffisamment importantes pour permettre la ré-ionisation du gaz. Les seules espèces présentes sont les atomes N(4S) et les molécules N2(X,v). C’est encore une zone luminescente puisqu’on y
observe l’émission du 1er système positif, liée à la recombinaison des états fondamentaux N(4S) de l’azote atomique via l’état faiblement attractif N2(5Σg+) dont la courbe de potentiel
croise celle de l’état B pour v = 11 (figure 1.3) :
Chapitre 1 : Généralités, concepts de base et résultats antérieurs
Rouffet Benoît 28
Contrairement à la zone de proche post-décharge, la post-décharge lointaine est donc caractérisée par un intense rayonnement provenant des niveaux vibrationnels proches de v’ = 11. En vertu du principe de Franck-Condon (lors d’une transition entre états, les modifications de l’orbitale électronique s’établissent quasi instantanément et les positions des noyaux restent identiques à celles de l’état initial), l’émission est maximale pour la transition : N2(B, v’ = 11) → N2(A, v’’ = 7) + hv centrée à 580 nm. (R19)
III.
Stérilisation du matériel médical :
L’utilisation d’une post-décharge spatiale dans un procédé permet de découpler la zone de production des espèces actives (décharge) de la zone de traitement (réacteur). La recombinaison rapide des espèces chargées dès la sortie de la décharge supprime l’agressivité liée au bombardement ionique des substrats, inévitable dans le plasma, et autorise des traitements beaucoup plus « doux ». L’innocuité des traitements post-décharge est également renforcée par le fait que la température du gaz est proche ou égale à la température ambiante. De plus, l’utilisation d’un vide primaire permet une bonne diffusion des espèces actives et un traitement relativement homogène dans des volumes importants sans être trop contraignant d’un point de vue industriel.
Les applications de post-décharges en flux à base d’azote sont nombreuses : nitruration de l’acier [A. Ricard, 1990], dépôt de films minces assisté par laser [C. Jama, 1999] ou pas [W. Kulisch, 1993], nettoyage de surfaces métalliques [M. Gaillard, 1999] et plus récemment la décontamination bactériologique ([S. Moreau, 2000], [S. Villeger, 2005] et [S. Cousty, 2006]).
Le réacteur étudié dans cette thèse est spécifiquement dédié à cette dernière application pour laquelle nous allons rappeler quelques concepts et définitions de base et faire le bilan des résultats importants précédemment obtenus par notre équipe.
III.1.
Définitions :
L’état stérile est défini comme étant un état exempt de tout micro-organisme viable [Pharmacopée européenne, 1997, 3ème édition, pp 295-296]. Les cinétiques d’inactivation des populations microbiennes suivent le plus souvent des lois exponentielles :
N(t) = N0 . exp (-kt) (I.10)
où N0 est le nombre initial de bactéries, ce qui implique que l’on ne puisse jamais garantir
qu’un dispositif stérilisé, pris de façon aléatoire dans une population de tels dispositifs, soit effectivement stérile, quelle que soit l’efficacité du procédé de stérilisation utilisé.
On définit alors la stérilité d’une population de dispositifs comme la probabilité d’existence d’un dispositif non stérile dans cette population. La Commission de la Pharmacopée européenne estime qu’un objet peut être considéré comme stérile lorsqu’un niveau d’assurance sanitaire (N.A.S.) égal à 10-6 est atteint [Norme européenne EN/NF 556: 1194-A1:1998 – Stérilisation des dispositifs médicaux – Exigences pour les dispositifs médicaux ayant subi une stérilisation terminale étiquetée « Stérile », in Stérilisation des dispositifs médicaux, Recueil Normes & réglementation, AFNOR, 2000, 2ème édition, pp 193-200], ce qui signifie que parmi une population d’un million de dispositifs stérilisés, il peut se trouver au maximum un dispositif non stérile.
Chapitre 1 : Généralités, concepts de base et résultats antérieurs
Rouffet Benoît 30
III.2.
Moyens de stérilisation actuels :
Ces dernières années l’instrumentation médicale moderne à fait des progrès considérables : la médecine moderne utilise des endoscopes et des fibroscopes pour explorer l’intérieur du corps tandis que la pose d’implants, pacemakers et prothèses articulaires se développe rapidement. La prévention des infections nosocomiales (maladies d’origine bactérienne, fongique, parasitaire, virale, ou à prion, cliniquement ou microbiologiquement identifiable, contractées dans une unité de soin) impose la stérilisation des instruments médicaux après chaque utilisation.
Il existe schématiquement aujourd’hui quatre types de stérilisateurs dont les moyens d’action et les caractéristiques d’application sont bien définis :
III.2.1.Stérilisation par chaleur sèche :
Elle est produite par l'action conjuguée de l'oxygène de l’air et de la chaleur dans une étuve appelée Poupinel. Les protéines bactériennes y sont oxydées à une température de l’ordre de 180 °C pendant plusieurs heures. Compte tenu de la haute température atteinte, les matériaux pouvant être traités sont limités au métal et au verre. De plus, ce procédé est considéré comme peu fiable en raison d'une difficulté habituelle à assurer la bonne répartition de la chaleur. Le ministère de la santé en déconseille formellement l'usage, à défaut de l'interdire.
III.2.2.Stérilisation par rayonnements ionisants (radio-stérilisation) :
Les rayonnements ionisants utilisés sont soit des électrons accélérés, soit des rayons gamma correctement dosés afin de leur donner la capacité de modifier la structure atomique ou d’induire des lésions définitives de l’ADN. Ils agissent aussi indirectement par radiolyse de l’eau dont sont majoritairement formés les micro-organismes. L'énergie des rayonnements gamma émis par les sources radioactives, ainsi que l'énergie des faisceaux d'électrons dont le niveau est inférieur à 10 MeV, ne permettent en aucune manière de provoquer une radioactivité induite dans un corps quelconque. La radio-stérilisation est donc un procédé de stérilisation très fiable et très intéressant pour plusieurs raisons : il n'utilise pas de gaz toxique ou corrosif, pas de vapeur ni de chaleur et il permet de traiter des quantités importantes d'objets. On notera ici que les énergies mises en jeu sont très nettement supérieures à celles des espèces de la post-décharge (quelques eV).
Néanmoins, étant donné la lourdeur des installations nécessaires et les opinions réticentes face à l'utilisation des rayonnements ionisants, ce mode de stérilisation demeure un procédé qui se développe lentement et qui est plutôt réservé à la stérilisation du matériel à usage unique.
III.2.3.Stérilisation par vapeur d’eau (autoclave) :
Son principe est basé sur la libération d'une grande quantité de chaleur lorsque la vapeur se condense au contact des instruments dont la température est plus basse. Au contact des micro-organismes, cette chaleur provoque la dénaturation des protéines bactériennes par hydrolyse de liaisons et conduit, à l'intérieur des cellules, à des modifications cytoplasmiques irréversibles. Afin de bénéficier de ces propriétés et pour les mettre en œuvre efficacement, il
Chapitre 1 : Généralités, concepts de base et résultats antérieurs
Rouffet Benoît 32
est nécessaire d'utiliser une vapeur d'eau saturée en l'absence d'air résiduel. Les stérilisateurs à vapeur d'eau saturée sont donc munis d'un dispositif faisant préalablement le vide dans la chambre de stérilisation et éliminant les poches d'air résiduel. Le cycle de stérilisation le plus performant prévoit une température de 134 °C pendant au moins 18 minutes, à une pression de 3 bars.
Ces stérilisateurs conviennent aux métaux et aux alliages compatibles avec la vapeur d'eau saturée, au verre, au caoutchouc, à certaines matières plastiques modernes ; ils permettent de stériliser les instruments et le matériel massifs, le matériel de forme creuse à une ou deux ouvertures et les objets poreux (textiles, non-tissés). Les matériels à stériliser peuvent être conditionnés dans un emballage perméable à l'air et à la vapeur d'eau mais étanche aux micro-organismes. Les instruments et objets stérilisés par cette méthode resteront stériles jusqu'à l'ouverture de l'emballage, à l'unique condition qu’ils sortent parfaitement secs de l’autoclave.
Une circulaire de la Direction Générale de la Santé (DGS) [Circulaire DGS/VS2 – DH/EM./EO n°97-672 du 20 Octobre 1997 relative à la stérilisation des dispositifs médicaux dans les établissements de santé] indique que « dans l'état actuel des connaissances la stérilisation par la vapeur d'eau saturée sous pression doit être la méthode appliquée lorsque le dispositif le supporte », c'est-à-dire pour tous les matériels non thermosensibles. C’est donc aujourd’hui le mode de stérilisation de référence.
III.2.4.Stérilisation par oxyde d’éthylène C2H4O :
L’oxyde d’éthylène possède une activité bactéricide reconnue, il agit par alkylation (substitution d’une fonction chimique par une autre), très efficace sur les acides nucléiques. C’est un procédé basse température (55 °C) dont l’action présente l’avantage de ne pas
endommager les matériels délicats qui ne peuvent pas supporter les conditions de température, d’humidité et de pression utilisées pour la stérilisation à la vapeur par autoclave.
Ses inconvénients sont multiples. C’est un gaz inflammable, explosif et toxique qui nécessite de nombreuses et contraignantes précautions pour son stockage (il doit être dilué dans du CO2), sa manipulation (l’enceinte doit être en surpression) et son utilisation par les
personnels. La durée du traitement varie de 1 à 6 heures mais il est ensuite nécessaire de laisser les matériels désorber pendant plusieurs jours avant de pouvoir les utiliser. De plus, les prions semblent résistants à ce mode de stérilisation. Compte tenu de ces éléments, une circulaire du Ministère de la Santé Publique spécifie que la stérilisation par l'oxyde d'éthylène ne doit être utilisée que si aucun autre moyen de stérilisation approprié n'existe et doit être exclusivement réservée aux instruments thermosensibles.
Compte tenu des inconvénients inhérents à chacun des moyens de stérilisation évoqués ci-avant, il existe un important enjeu sanitaire et économique lié au développement d’un procédé de stérilisation basé sur de nouveaux concepts, fonctionnant à froid, facilement maniable et contrôlable et utilisant un agent stérilisant stable, non toxique, compatible avec les matériaux utilisés en milieu médical et dont on connaisse le mode d’action.
Le plasma est capable de générer simultanément à partir de gaz non toxiques un échauffement, l’émission de rayonnement ainsi que de nombreuses espèces chimiques actives sur les composés organiques. L’utilisation du plasma apparaît donc comme un moyen a priori idéal pour la stérilisation, à condition de combiner judicieusement les différents effets.
Chapitre 1 : Généralités, concepts de base et résultats antérieurs
Rouffet Benoît 34
III.3.
Travaux antérieurs du groupe en décontamination
bactérienne :
Les décharges électriques dans les gaz ont été utilisées dès le 19ème siècle par Siemens [W. Siemens, 1857] pour la production d’ozone à des fins de désinfection de l’eau. Plus récemment Menashi [W.P. Menashi, 1968] a été le premier à déposer un brevet pour l’inactivation de micro-organismes à l’aide d’une décharge Corona pulsée et depuis le début des années 80, de nombreux travaux ont été publiés sur le sujet (voir par exemple les papiers de revue de Moisan [M. Moisan, 2001] et de Laroussi [M. Laroussi, 2002]).
En 2002, [V. Monna, 2002], le potentiel décontaminant de post-décharges en flux basse pression générée par une source micro-ondes dans les mélanges N2-O2 a été exploré
dans notre groupe.
0 2 4 6 8 10 0 1x1015 2x1015 3x1015 4x1015 5x1015 0 100 200 300 400 500 600 700 800 D en si té (O) (N) INOβ (a.u) x % O2-(100-x) %N2 UV
Figure 1.5 : Densité des atomes d’azote, d’oxygène et intensité du rayonnement UV
(transition NO B,v’=0 →→→→ NO X, v’’=8 à 320 nm) mesurés dans une post décharge lointaine N2-O2 en fonction
du pourcentage d’oxygène moléculaire pour pop = 5 Torr, PMW = 100 W et Qtot = 1 Nl/min. [S. Villeger , 2004]. La première étape a consisté à optimiser la production d’espèces actives (rayonnement UV, atomes N et O) en fonction des paramètres de décharge et de post-décharge (figure 1.5) : puissance micro-ondes PMW, pression de travail dans le réacteur pop, débit Qtot et composition
du mélange de gaz et à tester leur effet germicide sur différents types de micro-organismes (bactéries, levures, spores, …). [S. Villeger, 2004] On notera ici que l’ADN des micro-organismes est particulièrement sensible à l’émission du rayonnement UVc, dans une gamme de longueur d’onde assez étroite, comprise essentiellement entre 240 et 290 nm. Les lampes UV de longueur d'onde 253,7 nm sont couramment utilisées pour la décontamination de l’eau mais ne peuvent être employées qu’en complément d’autres techniques pour la stérilisation des matériels du fait de possibles problèmes d’ombrage.
Dans les post-décharges N2-O2, le rayonnement UV est lié à la présence des états
excités NO A2Σ+ et NO B2Π, responsables de l’émission des systèmes γ (transition
A2Σ+→ X2Π) et β (transition B2Π→ X2Π), et produits par les réactions :
N2(A) + NO → N2 + NO(A) et (R20)
N + O + M(=N2,O2)→ NO(B) + M(=N2,O2). (R21)
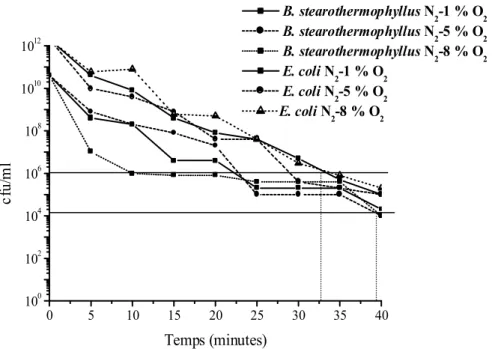
Figure 1.6 : Evolution du nombre de bactéries E. coli et B. stear. survivantes en fonction de la durée
d’exposition aux effluents de post décharges lointaines N2-x%O2 (pop = 5 Torr, PMW = 100 W et
Qtot = 1 Nl/min). [S. Villeger, thèse, 2004].
0 5 10 15 20 25 30 35 40 100 102 104 106 108 1010 1012 cf u/ m l Temps (minutes) B. stearothermophyllus N2-1 % O 2 B. stearothermophyllus N2-5 % O 2 B. stearothermophyllus N2-8 % O 2 E. coli N2-1 % O 2 E. coli N2-5 % O 2 E. coli N 2-8 % O2
Chapitre 1 : Généralités, concepts de base et résultats antérieurs Rouffet Benoît 36 0 10 20 30 40 100 102 104 106 108 1010 1012 E . c o li ( cf u /m l) Temps (min) N2-5 % O2 N2-5 % O2 60°C N2-5 % O2 80°C N2-5 % O2 120°C
Figure 1.7 : Evolution du nombre de bactéries E. coli survivantes en fonction de la durée d’exposition aux effluents d’une post décharge lointaine N2-5%O2 (pop = 5 Torr, PMW = 100 W et Qtot = 1 Nl/min ) sur un porte
bactéries en acier thermostaté à 20, 60, 80 et 120 °C. [S. Villeger, thèse, 2004].
L’effet de durées croissantes d’exposition d’une population de bactéries Escherichia coli (E. coli) et de spores Bacillus stearothermophyllus (B. stear.) aux effluents de cette post-décharge est visible sur les figures 1.6 et 1.7. On remarque :
• Une décroissance de 6 ordres de grandeurs (6 log) de la population de bactéries initiale au bout de quelques dizaines de minutes de traitement. Cette décroissance est suffisante pour pouvoir qualifier le procédé post-décharge de « stérilisateur », à condition que la même efficacité soit reproductible sur l’ensemble des différents types de micro-organismes.
• Une efficacité quasi indépendante de la composition du mélange N2-O2.
• Un effet synergique de la température de traitement sur sa durée. La même décroissance de 6 log est atteinte en moins de 3 minutes à 120 °C et une décroissance de 12 log est obtenue en 5 minutes à cette température. Le même effet a également été démontré sur la spore Bacillus stearothermophilus où une décroissance de 12 log a été obtenue en 20 minutes
Cependant, l’utilisation de l’oxygène dans le procédé est susceptible d’induire une oxydation de l’instrumentation traitée ce qui est néfaste au maintien à long terme de ses propriétés, sachant qu’un même matériel est appelé à être stérilisé plus d’une centaine de fois pendant sa durée de vie. Pour cette raison, l’étude s’est ensuite orientée vers l’analyse des propriétés germicides des post-décharges d’azote pur [S. Cousty, 2007].
Cette étude a mis en évidence l’action antibactérienne spécifique (figure 1.8) de l’azote atomique, les post-décharges d’azote pur ne permettant évidemment pas la production d’oxygène atomique ni celle du rayonnement UV par les réactions R20 et R21. A la température ambiante, cette activité est toutefois plus faible (2 log de décroissance au bout de 40 minutes d’exposition) que celle obtenue avec les post décharges N2-O2 mais un apport
modéré de température (60 °C) permet la même décroissance de 6 log au bout de 40 minutes de traitement.
Figure 1.8 : Comparaison entre les cinétiques de décontamination obtenues par un chauffage de l’enceinte de traitement à 60 °C (sans décharge) et avec l’exposition à la post-décharge d’azote pur avec et sans chauffage
de l’enceinte à 60 °C. [S. Villeger, 2008]
III.4.
Température des substrats :
On voit à travers les résultats précédents que la température des substrats est un élément important de la maîtrise du procédé de décontamination par post-décharge qui doit
Chapitre 1 : Généralités, concepts de base et résultats antérieurs
Rouffet Benoît 38
être contrôlé. Le chauffage peut être obtenu par un dispositif externe (circulation d’eau, manchon chauffant, …) mais il est également du à l’apport enthalpique lié aux processus de recombinaison hétérogène R11 des atomes sur les parois du réacteur et des substrats, dans lequel les atomes sont susceptible de céder à la paroi tout ou une partie de une enthalpie de recombinaison (égal à 9,76 eV, [C.Park,1990]).
Comme le montre la figure 1.9, la température atteinte par la paroi dépend du matériau sur lequel les atomes recombinent et est une fonction du flux Js d’atomes reçu par la surface,
qui dépend de la densité nat en atomes de la phase gazeuse :
at at th at S m kT 8 4 n v 4 n J π = = (en m-2.s-1). (I10)
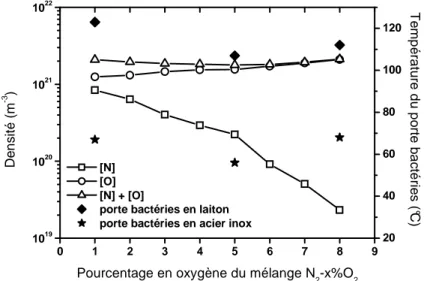
Le minimum de température obtenu pour des portes bactéries en laiton et en acier inox coïncide ainsi avec le minimum de la densité atomique totale (N + O) mesuré en post-décharge lointaine. 0 1 2 3 4 5 6 7 8 9 1019 1020 1021 1022 [N] [O] [N] + [O]
porte bactéries en laiton porte bactéries en acier inox
Pourcentage en oxygène du mélange N2-x%O2
D e n s it é ( m -3 ) 20 40 60 80 100 120 T e m p é ra tu re d u p o rte b a c té rie s ( °C )
Figure 1.9 : Corrélation entre la densité atomique totale (N + O) obtenue dans des post décharges lointaines N2-x%O2 (pop = 5 Torr, PMW = 100 W et Qtot = 1 Nl/min ) et la température de surface de portes bactéries en
laiton et en acier inox mesurée après 40 minutes d’exposition pour différentes teneurs en oxygène du gaz plasmagène. [Villeger, 2005]
IV.
Recombinaison des atomes d’azote sur les surfaces :
IV.1.
Généralités sur l’adsorption :
[P.W. Atkins, 2004]
Les surfaces réelles étant généralement des systèmes très complexes : plans cristallins différents, joints et défauts divers, marches monoatomiques ou polyatomiques, crans le long de ces marches, inclusion d’atomes étrangers, etc.…, les propriétés de cette surface varieront selon la position de la particule interagissant avec elle. Sans ignorer l'importance de ces défauts, la représentation (simpliste) qui suit se limitera au cas des surfaces homogènes (faces monocristallines) ou à imperfections contrôlées.
L'adsorption est un phénomène de surface universel. En effet, toute surface est constituée d'atomes n'ayant pas toutes leurs liaisons chimiques satisfaites. Cette surface a donc tendance à combler ce manque en captant les particules passant à proximité. Quand une particule gazeuse s'approche de la surface, elle est soumise à des forces d'interactions attractives et/ou répulsives qui, selon leur nature, vont conduire à l'adsorption ou non de cette particule sur la surface. On parle d’adsorption lorsque la durée de l’interaction entre la particule et la surface devient non négligeable (> 10-7 s). Dans ce cas, la particule aura perdu toute mémoire de son état initial (énergie cinétique, angle d’incidence) lorsqu’elle quittera la surface (désorption).
L'énergie potentielle d'interaction Epi(r) entre le solide et la particule adsorbée est
représentée sur la figure 1.10 en fonction de la distance r à la surface. Cette figure met en évidence le minimum d'énergie Eads
Chapitre 1 : Généralités, concepts de base et résultats antérieurs
Rouffet Benoît 40
intermédiaires (états précurseurs) d'énergie Ep et les énergies d'activation (barrières) de
désorption Edes
– Eads, de diffusion à la surface du solide Edis – Eads et d'adsorption Edes – Egaz (souvent négligeable).
On définit classiquement le degré d’adsorption par le taux de recouvrement θ : adsorption ' d sites de total nombre occupés adsorption ' d sites de nombre = θ (I11)
La vitesse d’adsorption correspond à la variation du taux de recouvrement en fonction du temps dθ/dt.
Figure 1.10 – Représentation énergétique des phénomènes d’adsorption.
IV.2.
Physisorption et chimisorption :
Les particules peuvent s’adsorber sur les surfaces de deux façons :
• Dans la physisorption (ou adsorption physique), l’attraction est assurée par les forces d’interaction entre les nuages électroniques de la particule et des atomes de la surface. Ces forces à longue distance, de type van der Walls, sont très peu énergétiques (< 0,3 eV) et vont conduire à une faible liaison de la particule. Le processus est aisément réversible et la désorption facilitée par l’agitation
thermique liée à une température de gaz élevée. La barrière de diffusion (Edis – Eads) étant faible, la particule peut également migrer sur la surface du solide en passant d’un puits de potentiel de physisorption à un puits de potentiel adjacent.
• Dans la chimisorption (ou adsorption chimique), les particules sont liées à la surface par une liaison chimique (généralement covalente, dans laquelle les orbitales électroniques de la particules et des atomes de la surface sont partagées par certains électrons). L’énergie mise en jeu est beaucoup plus grande (typiquement 10 fois supérieure à l’énergie de physisorption), conférant à la chimisorption un caractère irréversible. La chimisorption étant généralement liée à des défauts locaux de la structure atomique du solide, le nombre de sites de chimisorption est beaucoup plus faible que le nombre de sites de physisorption.
IV.3.
Recombinaison atomique de surface :
IV.3.1.Mécanismes
:
Dans le procédé de décontamination par post décharge en flux d’azote, la prise en compte de la recombinaison atomique de surface (appelée aussi recombinaison catalytique ou recombinaison hétérogène) est importante pour deux raisons :
• elle est l’une des causes principales de disparition des atomes d’azote, supposés être le vecteur essentiel de l’interaction avec les micro-organismes ;
Chapitre 1 : Généralités, concepts de base et résultats antérieurs
Rouffet Benoît 42
Au cours de la recombinaison de surface, deux atomes N de la phase gazeuse vont réagir sur la surface pour former une molécule N2. La surface constitue alors le catalyseur de
la réaction et on peut distinguer pour la recombinaison atomique trois types de surfaces :
• les surfaces idéalement non catalytiques pour lesquelles tout atome adsorbé subira la désorption sous la forme atomique ;
• les surfaces idéalement catalytiques pour lesquelles tout atome adsorbé subira la désorption sous la forme moléculaire ;
• les surfaces réelles qui sont des surfaces partiellement catalytiques.
La recombinaison peut faire appel à deux types de mécanismes :
• dans le mécanisme de Langmuir-Hinshelwood (LH), elle s’effectue par rencontre entre atomes adsorbés ;
• dans le mécanisme d’Eley-Rideal (ER), la recombinaison a lieu entre un atome adsorbé et un atome de la phase gazeuse.
Il existe dans la littérature différents modèles stationnaires ([Y.C. Kim, 1991], [B. Gordiets, 1996]) et transitoires [G. Cartry, 2000], décrivant la recombinaison hétérogène à partir d’une suite de processus élémentaires (figure 1.11) :
• physisorption : Ng + Sp→ Np (R22)
• physidésorption : Np→ Ng + Sp (R23)
• diffusion sur la surface : Np→ Np (R24)
• chimisorption ER : Ng + Sc→ Nc (R25)
• chimisorption LH : Np + Sc→ Nc+ Sp (R26)
• recombinaison ER : Ng + Nc→ N2g+ Sc (R27)
Figure 1.11 : Représentation schématique des processus de recombinaison atomique de type ER et LH Les carrés blancs et gris représentent respectivement les sites de physisorption et de chimisorption. Les espèces de
la phase gazeuse sont en blanc et les espèces adsorbées en gris. [G. Cartry , 2000].
Dans ces réactions, Ng et N2g représentent les atomes et les molécules de la phase
gazeuse, Np et Nc les atomes physi et chimisorbés et Sp et Sc les sites de physi et de
chimisorption vides.
IV.3.2.Probabilité de recombinaison
γγγγ
:
La probabilité de recombinaison d’un atome sur la surface (généralement notée γ dans la littérature) s’exprime comme le produit de la probabilité q pour qu’un atome de la phase gazeuse frappant la surface atteigne un site de chimisorption multipliée par la probabilité de recombinaison des atomes chimisorbés : [Y.C. Kim, 1991]
γ = q . exp (-Er / kT), (I12)
où Er est l’énergie d’activation de la recombinaison, égale à l’énergie nécessaire pour briser la liaison covalente établie entre le site de chimisorption et l’atome adsorbé.
Chapitre 1 : Généralités, concepts de base et résultats antérieurs
Rouffet Benoît 44
La probabilité q est une fonction complexe de a : rayon moyen d’un site de physisorption (2a = distance moyenne entre deux sites de physisorption), 2b : distance moyenne entre deux sites de chimisorption et Xd : rayon de collecte moyen d’un site de
chimisorption. Ce rayon définit une aire de collecte dans laquelle les atomes frappant la surface vont pouvoir diffuser sans désorption jusqu’au site de chimisorption (figure 1.12). Sa valeur peut être obtenue à partir du coefficient de diffusion de l’atome adsorbé Ds :
Ds = νD (a2/4) exp(-ED/kT), (I13)
où νD et ED sont respectivement la fréquence et l’énergie d’activation de la diffusion de
surface, et du temps moyen τr de résidence des atomes sur la surface :
τr = νd-1 exp(Ed/kT), (I14)
où νd et Ed sont cette fois ci la fréquence et l’énergie de désorption :
Xd = (Ds.τr)1/2 = (νD/ νd)1/2 (a/2) exp[(Ed- ED )/2kT] (I15)
Selon Kim, la probabilité q vaut :
ϕ + + − = ) X / a ( K ) X / b ( I ) X / b ( K ) X / a ( I ) X / b ( K ) X / a ( I ) X / a ( K ) X / b ( I b aX 2 q d 0 d 1 d 1 d 0 d 1 d 1 d 1 d 1 2 d , (I16)
où Ii et Ki sont les fonctions de Bessel d’ordre i.
Le premier terme de cette expression représente la probabilité de chimisorption LH (par diffusion des atomes physisorbés) et ϕ est la probabilité de chimisorption ER, égale à la fraction de la surface couverte par les sites de chimisorption (a/b)2.
2a 2b Aire de collecte du site Site de chimi-sorption Xd
Figure 1.12 – Schéma du modèle de surface de Kim.
A basse température ou basse pression, la diffusion des atomes sur la surface n’est que peu gênée par les collisions avec les particules de la phase gazeuse et tous les atomes physisorbés pourront atteindre le site de chimisorption (Xd >> b), entraînant :
q = 1 et γ = exp (-Er / kT).
A haute température ou haute pression, la recombinaison se fera uniquement par les processus de recombinaison ER (Xd = a) et l’on aura :
q = ϕ et γ = (a/b)2 . exp (-Er / kT).
En l’état actuel des connaissances et des moyens d’investigation expérimentaux, l’accès aux différentes grandeurs (fréquences et énergies d’activation des processus élémentaires, dimensions des sites) impliquées dans ces modèles reste problématique. La plupart d’entre elles sont généralement estimées, conduisant à une approche qualitative des probabilités de recombinaison γ et de leurs évolutions avec les paramètres macroscopiques de contrôle des procédés (température de gaz, température de paroi, pression, …).
![Figure 1.4 : Les systèmes émissifs observés dans les différentes régions de post-décharge [Cousty, 2007]](https://thumb-eu.123doks.com/thumbv2/123doknet/2121417.8300/28.892.128.770.370.655/figure-systemes-emissifs-observes-regions-post-decharge-cousty.webp)
![Figure 2.11 : Distributions théoriques normalisées RB,v’ des concentrations des niveaux vibrationnels [N2(B,v’)] en fonction de v’ pour différentes conditions de post-décharge.](https://thumb-eu.123doks.com/thumbv2/123doknet/2121417.8300/68.892.195.671.462.737/distributions-theoriques-normalisees-concentrations-vibrationnels-fonction-conditions-decharge.webp)