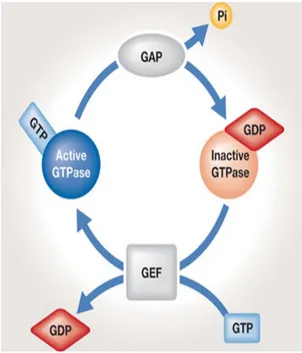
Etude des mécanismes dépendants de GBF1 et impliqués dans la réplication du virus de l'hépatite C
220
0
0
Texte intégral
Figure



+7
Documents relatifs