Développement d’un outil d’aide à la
communication
Parler aux enfants mineurs du résultat d’un test BRCA1/2
Mémoire
Ariane Santerre-Theil
Maîtrise en sciences pharmaceutiques
Maître ès sciences (M.Sc.)
Québec, Canada
ii
Développement d’un outil d’aide à la
communication
Parler aux enfants mineurs du résultat d’un test BRCA1/2
Mémoire
Ariane Santerre-Theil
Sous la direction de :
iii
Résumé
Les individus porteurs d’une mutation des gènes BRCA1/2 s’inquiètent généralement du risque de leurs enfants d’avoir hérité de la mutation génétique familiale. Malgré l’absence d’avantages médicaux pour les enfants mineurs et l’impossibilité pour eux d’être testés avant d’être adultes, une majorité des parents leur communiquent néanmoins le résultat du test génétique BRCA1/2. Les parents confrontés à cette situation disent avoir besoin d’être accompagnés dans cette décision. L’objectif de ce projet, à devis qualitatif, était de développer un outil d’aide à la décision à l’intention des individus porteurs quant à la communication du résultat de test BRCA1/2 à leurs enfants mineurs. Développé conformément aux critères de l’International Patient Decision Aids Standards, le prototype a été évalué lors de groupes de discussion et d’entrevues individuelles menés auprès de mères porteuses d’une mutation des gènes BRCA1/2 (n=9). Des professionnels de la santé l’ont également commenté (n=3). Une analyse thématique a été effectuée à partir des transcriptions des entrevues. Globalement, les résultats de cette étude suggèrent que les mères ne présentent pas de besoin quant à la décision de communiquer ou non le résultat BRCA1/2 à leurs enfants mineurs, puisqu’elles semblent déjà avoir choisi d’en parler. Elles désirent un outil pour les préparer et les aider à communiquer l’information à leurs enfants. La visée de l’outil a donc été modifiée afin de répondre aux besoins des mères. L’outil d’aide à la communication est présenté sous la forme d’un livret. Il comprend les avantages et les inconvénients de communiquer, des étapes afin de s’y préparer, des conseils et des témoignages de parents. D’autres études seront nécessaires afin d’évaluer l’effet de cet outil pour les parents porteurs dans leur processus de communication.
iv
Table des matières
Résumé ... iii
Table des matières ... iv
Liste des tableaux ... vi
Liste des figures ... vii
Remerciements ... ix
Avant-propos ... x
Introduction ... 1
CHAPITRE 1 : État des connaissances ... 2
1.1 Épidémiologie du cancer du sein ... 2
1.2 Test de prédisposition génétique ... 4
1.2.1 Indications pour le test génétique ... 4
1.2.2 Prise en charge des individus porteurs d’une mutation des gènes BRCA1/2 ... 5
1.3 Test de prédisposition génétique BRCA1/2 chez les enfants ... 6
1.4 Communication du résultat de test BRCA1/2 aux enfants ... 7
1.5 Motivations et obstacles à communiquer le résultat aux enfants ... 8
1.6 Impacts de la communication et réactions chez les enfants ... 9
1.7 Besoins des parents en matière de communication aux enfants ... 12
1.8 Matériel d’information disponible sur la communication familiale du résultat de test BRCA1/2 ... 13
1.9 Outils d’aide à la décision ... 14
1.9.1 Définition ... 14
1.9.2 Apport des outils d’aide à la décision ... 14
1.9.3 Développement d’un outil d’aide à la décision ... 15
1.10 Objectif ... 16
1.10.1 Pertinence de cette étude ... 16
CHAPITRE 2 : Méthodologie ... 17
2.1 Contexte du projet de recherche ... 17
2.2 Développement du prototype de l’outil d’aide à la décision ... 17
2.2.1 Cadre, objectif et population visée ... 17
v
2.2.3 Comité consultatif ... 18
2.2.4 Première version du prototype ... 18
2.2.5 Discussions et modifications par le comité consultatif : processus itératif ... 18
2.2.6 Évaluation du contenu auprès des patients et des professionnels de la santé ... 19
2.3 Évaluation du contenu ... 19
2.3.1 Participants ... 19
2.3.2 Mesures ... 20
2.3.3 Collecte des données ... 20
2.3.4 Analyse ... 21
2.3.5 Considérations éthiques ... 22
CHAPITRE 3: Article de recherche ... 23
Résumé ... 23
Development of a Tool to Guide Parents Carrying a BRCA1/2 Mutation Share Genetic Results With Underage Children ... 24
Abstract ... 25
Introduction ... 26
Materials and methods ... 26
Results ... 28
Discussion ... 31
Tables and figures ... 35
Conclusion ... 40
Bibliographie ... 46
Annexe 1: International Patient Decision Aids Standards Collaboration’s Model Development Process for Decisions Aids ... 56
Annexe 2 : Processus de développement de l’outil d’aide à la décision (adapté du modèle de l’International Patient Decision Aids Standards Collaboration) ... 57
Annexe 3: Grille de lecture ... 58
Annexe 4 : Questionnaire socio-démographique... 59
Annexe 5 : Guide d’entrevue semi-structuré – Groupes de discussion ... 60
vi
Liste des tableaux
Table 1. Selected quotes from the 1st draft assessment ... 38 Table 2. Selected quotes from the 2nd draft assessment ... 39
vii
Liste des figures
Figure 1: Development Process of the Tool (adapted from the International Patient
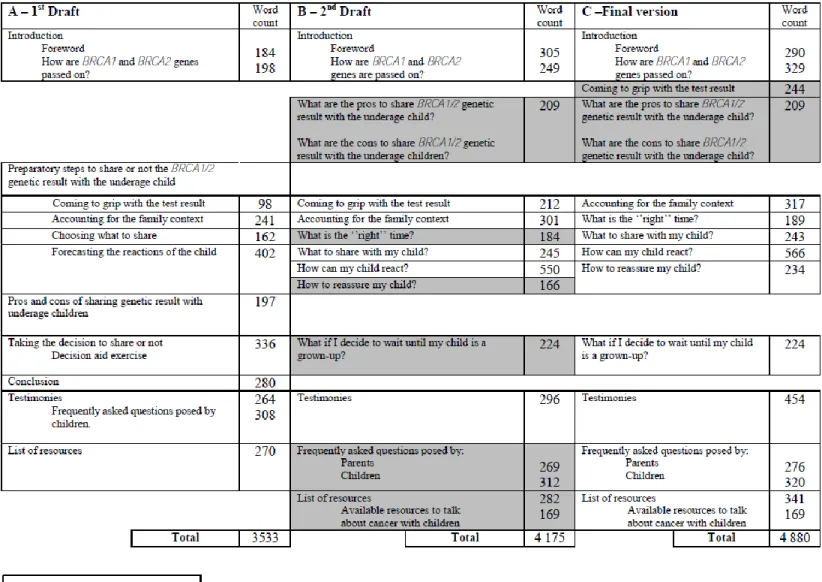
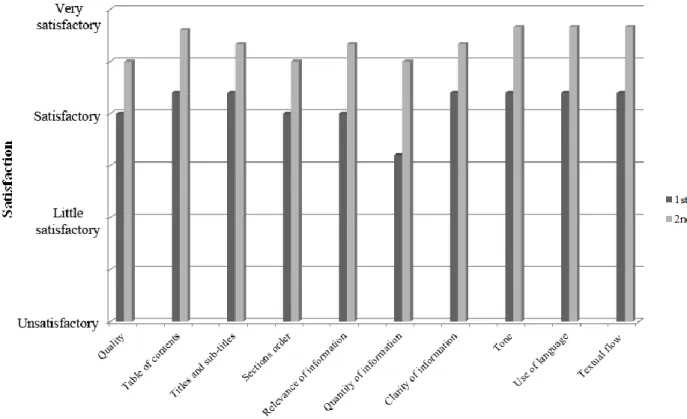
Decision Aids Standards Collaboration) ... 35 Figure 2: Content and word count for each section of the different versions of the tool ... 36 Figure 3: Mean satisfaction scores according to version of the tool (n=9) ... 37
viii
Ce que tu donnes est à toi pour toujours, ce que tu gardes est perdu à jamais.
ix
Remerciements
Au cours des trois dernières années, j’ai eu la chance de travailler sur un projet de recherche exceptionnel, qui m’a non seulement captivée, mais qui aura des retombées à très court terme et qui répondra à un besoin des femmes à haut risque de cancer du sein.
J’aimerais tout d’abord remercier mon directeur de recherche, le docteur Michel Dorval, pour sa disponibilité, son soutien et ses conseils qui ont permis la réalisation de ce mémoire. J’aimerais aussi remercier madame Karine Bouchard, coordonnatrice de recherche, pour son aide précieuse et sa présence inébranlable. Je remercie également la Faculté de Pharmacie de l’Université Laval pour la bourse d’étude qu’elle m’a octroyée. Finalement, je veux remercier la Fondation du cancer du sein du Québec pour son soutien financier tout au long du développement de l’outil faisant l’objet de ce mémoire.
Je ne serais pas arrivée à cette étape sans l’aide précieuse de mes collègues de travail Dominique St-Pierre, Claudia Côté, Geneviève Larouche, Catherine Gonthier et Sylvie Pelletier. Pour cela, et plus encore, je les remercie. Je tiens à remercier du fond du cœur Joanie Leclerc et Véronique Dorval, collègues et maintenant amies, pour leur oreille attentive, leur présence, leurs conseils et pour nos échanges qui ont enrichi ces trois dernières années. Finalement, je désire exprimer toute ma gratitude à mon copain pour son aide et ses encouragements et à mes parents qui m’ont donné tout ce dont j’avais besoin pour réussir.
x
Avant-propos
Contribution personnelle à la rédaction de l’article scientifique
Le projet présenté dans ce mémoire a été réalisé dans le cadre des activités du Centre ROSE (Centre de Ressources en Oncogénétique pour le Soutien et l'Éducation des familles à risque de cancer du sein) financé par la Fondation du cancer du sein du Québec (FCSQ). Le Centre ROSE a pour mission d’informer et soutenir les familles à risque de cancer du sein du Québec et de sensibiliser le grand public et les professionnels de la santé aux enjeux des cancers du sein familiaux. Mon directeur de recherche, le docteur Michel Dorval, est le directeur scientifique du Centre ROSE.
En tant que premier auteur du manuscrit de l’article présenté dans ce mémoire, j’ai participé à toutes les étapes de l’étude, depuis les recherches documentaires jusqu’à la soumission du manuscrit dans une revue internationale. J’ai rédigé la première version de l’outil, dont le développement est présenté dans ce mémoire, assuré la planification et la gestion des rencontres des membres du comité consultatif et apporté les modifications suggérées par ces derniers. Par la suite, j’ai organisé le recrutement des participants et assuré le suivi des dossiers tout au long du projet. Conjointement avec la coordonnatrice de recherche du Centre ROSE, j’ai animé les groupes de discussion. J’en ai fait la retranscription, j’ai saisi les questionnaires et réalisé l’analyse thématique. Forte de l’expérience acquise, j’ai réalisé seule les entrevues individuelles et l’analyse thématique des données résultant de ces rencontres. J’ai rédigé la première version en langue anglaise de l’article et apporté les modifications suggérées par mon directeur, les co-auteurs et les réviseurs. Cet article fut par la suite corrigé et vérifié par un traducteur professionnel. La version présentée dans ce mémoire a été approuvée par l’ensemble des coauteurs et, au moment du dépôt initial, elle était sous-évaluation dans une revue internationale.
1
Introduction
Depuis l’identification des gènes BRCA1 et BRCA2 (BRCA1/2) comme étant liés au développement des cancers du sein et de l’ovaire, il est possible pour les individus ayant des antécédents familiaux d’avoir recours à un test génétique pour savoir s’ils ont un risque accru de cancer. En plus de permettre aux femmes à haut risque de cancer du sein d’avoir un suivi personnalisé en termes de dépistage et de prévention, l’identification d’une mutation génétique des gènes BRCA1/2 comporte des implications pour les autres membres de la famille du premier et du second degré, y compris les jeunes enfants. Toutefois, puisque les cancers du sein et de l’ovaire ne se développent qu’à l’âge adulte et qu’aucun suivi médical pour ces cancers n’est recommandé avant l’âge de 25 ans, le test de prédisposition génétique n’est pas accessible aux enfants mineurs. Une majorité de parents testés communiquent néanmoins leur résultat de test BRCA1/2 à leurs enfants même s’ils sont mineurs. La décision de communiquer le résultat de test BRCA1/2 peut être une source de stress et d’inquiétude pour les parents, si bien que ceux-ci expriment le désir d’obtenir davantage d’accompagnement et de soutien dans ce processus. L’objectif de ce projet de recherche vise à développer un outil d’aide à la décision pour aider les parents porteurs d’une mutation des gènes BRCA1 ou BRCA2 à communiquer le résultat de test à leurs enfants mineurs.
L’avènement de la médecine personnalisée et le souci d’optimiser l’information présentée en consultation génétique rendent impératif de développer du matériel afin d’outiller les individus et de les appuyer dans une des décisions importantes qu’ils devront prendre suite au test. L’information obtenue dans ce projet de recherche peut contribuer à offrir du soutien aux parents porteurs ayant de jeunes enfants et leur permettre, s’il y a lieu, d’engager une discussion sur le sujet avec leur professionnel de la santé.
2
CHAPITRE 1 : État des connaissances
1.1 Épidémiologie du cancer du sein
Au Canada, le cancer du sein est le cancer le plus fréquemment diagnostiqué et la deuxième cause de décès chez les femmes (1). La Société canadienne du cancer estimait qu’en 2015, 25 000 femmes avaient reçu un diagnostic de cancer du sein (1).
Le cancer du sein est une maladie multifactorielle. Ainsi, un indice de masse corporelle élevé, une alimentation riche en gras, une consommation élevée d’alcool, le tabagisme, la sédentarité, l’exposition aux hormones exogènes (hormonothérapie de substitution, contraceptifs oraux) et aux rayonnements ionisants (radiothérapie du thorax) sont connus comme étant des facteurs augmentant le risque de développer un cancer du sein (2-4). Pour chacun de ces facteurs, le risque de développer un cancer du sein varie de faible à modéré (RR < 2) (3). Des caractéristiques ou des événements de la vie reproductive comptent également parmi les facteurs de risque. Ainsi, avoir son premier enfant après l’âge de 35 ans, le fait de ne pas allaiter et la nulliparité sont connus comme des facteurs augmentant le risque de cancer du sein à cause d’une exposition plus longue aux œstrogènes endogènes (2). L’apparition précoce de la ménarche et celle tardive de la ménopause augmentent aussi le risque de cancer du sein en raison de l’exposition prolongée aux hormones endogènes (2, 4).
Le sexe et l’âge jouent également un rôle important. Le risque est, en effet, beaucoup plus important pour une femme que pour un homme (3, 4). Au Canada, on estime que 220 cas de cancer du sein chez l’homme ont été diagnostiqués en 2015 (1). Le risque de développer un cancer du sein augmente aussi avec l’âge. Chez les femmes ménopausées, le risque de développer un cancer du sein double à chaque décennie jusqu’à l’âge de 80 ans (4). La densité mammaire et certaines affections bénignes du sein, comme l’hyperplasie atypique, constituent aussi des facteurs de risque (4, 5). Les femmes ayant une histoire familiale de cancer du sein, autant du côté maternel que paternel, ont un risque deux fois plus élevé de développer un cancer que les femmes sans antécédents familiaux (4). Ce
3
risque varie cependant selon le nombre de parents atteints, de leur âge au diagnostic, du lien familial et de la présence d’une prédisposition génétique (6).
Environ 5% à 10% des cancers du sein sont dus à la présence d’une mutation dans un gène de prédisposition de forte pénétrance (6-8). Ces cancers, dits héréditaires, sont le plus souvent attribuables à des mutations des gènes BRCA1 ou BRCA2 (BRCA1/2) respectivement identifiées dans les chromosomes 17 et 13 (7, 9). Cependant, des mutations dans d’autres gènes de prédisposition tels que MSH6, TP53, PTEN, CHEK2 et PALB2 augmentent aussi le risque de cancer du sein (8). Dans ce mémoire, il sera principalement question des mutations BRCA1/2. Environ 65% des cancers héréditaires du sein et 95% des cancers héréditaires de l’ovaire sont causés par la présence de mutations dans les gènes BRCA1 ou BRCA2 (10, 11). Les mutations des gènes BRCA1/2 se transmettent selon le mode autosomique dominant, ce qui signifie qu’elles peuvent être transmises aussi bien par la mère que par le père (6, 7, 9, 12). Chaque enfant d’un individu porteur a donc un risque de 50% d’avoir hérité de la mutation. De plus, une seule copie mutée suffit à augmenter le risque d’un individu (7, 9). Ces gènes sont de pénétrance incomplète, c’est-à-dire qu’un individu peut être porteur d’une mutation des gènes BRCA1/2 sans nécessairement développer un cancer du sein au cours de sa vie (5). Ainsi, le risque pour une femme porteuse d’une mutation des gènes BRCA1 ou BRCA2 de développer un cancer du sein peut atteindre 87 % (7, 13, 14) et jusqu’à 68% de développer un cancer de l’ovaire (7, 13, 15). Les femmes porteuses d’une mutation des gènes BRCA1/2 qui ont déjà été atteintes d’un cancer du sein sont aussi plus à risque de développer un cancer au sein controlatéral (16). Le risque de cancer du sein des hommes porteurs d’une mutation BRCA1/2 peut atteindre 8%, comparativement à un homme de la population générale dont le risque se situe autour de 0,1% (17, 18). Le risque de développer un cancer de la prostate pour un homme porteur d’une mutation BRCA1 peut atteindre 14% et jusqu’à 20% pour un homme porteur d’une mutation BRCA2 (1, 12, 14). Ces mutations augmentent également le risque de développer d’autres types de cancer, tel qu’un cancer du pancréas, du mélanome, du côlon et du larynx, bien que le niveau d’évidences, pour ces cancers, soit encore faible (1, 12, 14).
4 1.2 Test de prédisposition génétique
Les individus ayant une histoire familiale ou personnelle de cancer du sein et/ou de l’ovaire peuvent avoir recours à un test de prédisposition génétique, afin de savoir s’ils sont porteurs d’une mutation les prédisposant à ces cancers (8).
1.2.1 Indications pour le test génétique
Un nombre élevé d’apparentés ayant développé un cancer du sein ou de l’ovaire, un jeune âge au diagnostic, un cancer du sein triple négatif, un cancer du sein controlatéral, un homme atteint d’un cancer du sein et une ascendance d’origine juive Ashkénaze sont des caractéristiques qui augmentent la probabilité d’avoir hérité d’une mutation génétique BRCA1/2 (12). En général, le test est indiqué lorsque que la probabilité d’être porteur d’une prédisposition au cancer du sein est supérieure à 10% (19).
Le test consiste en la recherche de mutations dans les gènes BRCA1 et BRCA2 à partir d’un prélèvement sanguin. Chez les individus provenant d’une famille au sein de laquelle une mutation a déjà été identifiée, seule cette mutation est généralement cherchée chez les individus testés. Si le résultat est positif pour la mutation recherchée, on dira que l’individu est porteur de la mutation et non-porteur si, au contraire, cette mutation n’est pas identifiée (20, 21). Dans les familles au sein desquelles aucune mutation n’a été préalablement identifiée, les mutations les plus fréquentes dans la population donnée sont cherchées chez les individus atteints d’un cancer du sein ou de l’ovaire. Si aucune mutation n’a été identifiée, mais que l’histoire familiale suggère la présence d’une mutation génétique, on dira que le résultat est non concluant. Dans ce cas, l’excès de cancers peut être dû à des mutations de gènes encore inconnues ou non testées, à une combinaison de polymorphismes ou à des facteurs environnementaux (20, 21).
Il est recommandé que le test génétique soit précédé d’une rencontre en conseil génétique (19-21). Le conseil génétique vise d’abord à déterminer l’admissibilité de l’individu au test génétique en examinant l’histoire familiale de cancer, autant du côté paternel que maternel, à fournir de l’information sur la procédure du test et à expliquer la signification des différents résultats possibles. En outre, cette rencontre permet de préparer
5
l’individu aux éventuelles conséquences médicales, psychologiques et familiales que pourrait avoir le résultat du test génétique (22). De cette façon, l’individu sera en mesure de prendre une décision éclairée en ce qui concerne le test de prédisposition génétique qui lui est offert (20, 21).
1.2.2 Prise en charge des individus porteurs d’une mutation des gènes BRCA1/2
L’identification d’une mutation génétique permet d’offrir aux femmes porteuses des mesures de dépistage adaptées à leur niveau de risque et des mesures de réduction de risque.
Comme les femmes porteuses présentent un risque plus élevé de développer un cancer du sein ou de l’ovaire au cours de leur vie, il est recommandé que leur dépistage soit plus fréquent et qu’il commence à un plus jeune âge que celui offert aux femmes de la population générale. Il peut débuter dès l’âge de 25 ans ou, selon le cas, 5 ans avant les cancers diagnostiqués dans la famille (23). Les méthodes de dépistage du cancer du sein chez les femmes porteuses incluent l’examen clinique des seins et l’imagerie (mammographie, résonance magnétique (IRM) et l’échographie), et peuvent être pratiquées annuellement (23). Cependant, les recommandations peuvent varier selon l’état de santé, l’histoire médicale personnelle et familiale de la femme (12, 20, 23, 24). Les méthodes actuelles de dépistage du cancer de l’ovaire incluent un examen et une échographie de la région pelvienne et le dosage de l’antigène CA-125 (12, 20, 24). Cependant, il n’existe présentement aucune preuve soutenant l’efficacité de ces méthodes de dépistage pour détecter le cancer de l’ovaire chez les femmes à haut risque (23). Les faibles sensibilité et spécificité de ces tests peuvent faussement rassurer ou inquiéter les femmes, et mener à des interventions inutiles (23).
Les hommes porteurs sont invités à demeurer vigilants aux changements de leurs seins et à passer un examen clinique annuellement, 10 ans avant le premier diagnostic de cancer du sein dans la famille (20, 23). De plus, compte tenu de leur risque plus élevé de développer un cancer de la prostate, ils sont invités à passer un examen clinique de la
6
prostate annuellement et à effectuer une mesure de l’antigène PSA, généralement à partir de 40 ans (20, 23, 24).
Parmi les mesures de réduction de risque disponibles, on compte la pharmaco-prévention, la mastectomie préventive et la salpingo-ovariectomie bilatérale préventive. La pharmaco-prévention consiste en la prise de tamoxifène ou de raloxifène, des modulateurs du récepteur d’œstrogène qui diminuent le risque de cancer du sein chez la femme jusqu’à 53% (25, 26). Par contre, contrairement aux États-Unis, le tamoxifène et le raloxifène ne sont pas approuvés au Canada en prévention primaire du cancer du sein. La mastectomie préventive consiste en l’ablation du tissu mammaire avant le développement d’un cancer du sein et elle réduit jusqu’à 95% le risque de développer un cancer du sein (27, 28). Suite à la mastectomie préventive, il est possible pour les femmes d’avoir une reconstruction mammaire, une chirurgie qui consiste à rétablir la forme et le volume des seins. Deux méthodes sont disponibles pour reconstruire les seins : la reconstruction par prothèses mammaires et la reconstruction par tissus autologues (23, 24). La salpingo-ovariectomie préventive consiste en l’ablation des ovaires et des trompes de Fallope. Cette chirurgie peut réduire jusqu’à 68% le risque de développer un cancer du sein (29-31). Elle est offerte aux femmes porteuses après que ces dernières aient eu les enfants qu’elles désiraient (24). Puisque la mastectomie et la salpingo-ovariectomie préventives sont permanentes et irréversibles, des rencontres avec des professionnels de la santé sont nécessaires avant l’intervention, afin de favoriser une prise de décision éclairée.
1.3 Test de prédisposition génétique BRCA1/2 chez les enfants
En plus de leur permettre de connaître leur risque personnel, une des principales motivations des femmes à consulter en oncogénétique est de savoir s’il existe un risque pour leurs enfants d’avoir hérité de la mutation génétique (32-35). Dans l’éventualité d’un résultat positif chez la femme, ses enfants pourront avoir accès au test et/ou bénéficier d’un suivi médical adapté à leur niveau de risque. Cette motivation est également partagée par les hommes qui disent vouloir connaître leur résultat pour permettre à leurs enfants de prendre des décisions éclairées pour leur santé et pour leur avenir (33). Toutefois, bien que le test BRCA1/2 soit maintenant couramment offert aux individus lorsque la présence d’une
7
mutation héréditaire est soupçonnée au sein de la famille, il n’est pas accessible avant l’âge adulte.
En 2003, une déclaration encadrant les tests de prédisposition génétique au cancer chez les enfants mineurs et asymptomatiques est publiée par l’American Society of Clinical Oncology (ASCO) (36). L’ASCO est catégorique : si le risque de développer le cancer en question pendant l’enfance est faible et s’il n’existe pas de mesures de prévention ou de réduction de risque pour l’enfant, le test de prédisposition génétique ne doit pas lui être offert avant qu’il n’ait atteint l’âge adulte (36). Tel est le cas pour les principales mutations des gènes prédisposant aux cancers du sein et de l’ovaire, à l’exception des mutations du gène TP53 associées au syndrome de Li-Fraumeni (37-39). Le syndrome de Li-Fraumeni augmente le risque de cancers pouvant survenir en bas âge (tissus mous, os, peau, côlon, cerveau, sang (leucémie)) (39).
1.4 Communication du résultat de test BRCA1/2 aux enfants
Malgré l’absence d’avantages médicaux pour les enfants et l’impossibilité pour eux d’être testés avant d’être adultes, les études portant sur la communication familiale indiquent qu’une majorité des parents communiquent le résultat du test génétique BRCA1/2 à leurs enfants mineurs (40-44) et ce, peu de temps après que le parent l’ait, lui-même, reçu (41-46). Récemment, une étude menée auprès de 253 parents de 505 enfants âgés de 3 à 35 ans, dont 262 avaient entre 3 et 17 ans, révélait que 66% des enfants avaient été informés du résultat de test BRCA1/2 de leurs parents (45). Parmi les parents ayant informé leurs enfants, 84% affirmaient l’avoir fait moins d’un mois après avoir reçu leur résultat (45).
Plusieurs facteurs sont associés à la décision de communiquer le résultat du test BRCA1/2 (40-42, 44, 45, 47). En 2001, Tercyak et ses collaborateurs ont observé que les personnes utilisant davantage de mécanismes d’adaptation, et présentant de la détresse générale avant et après le test génétique, étaient plus susceptibles de communiquer leur résultat aux enfants (47). Cette étude, menée auprès de 133 parents d’enfants âgés de 18 ans et moins, a utilisé l’Inventaire COPE afin de mesurer le recours à des mécanismes d’adaptation (i.e. planifier, chercher du soutien social, exprimer ses émotions, interpréter la
8
situation de manière positive) et l’échelle CES-D (Center for Epidemiologic Studies Depression) afin de mesurer les symptômes dépressifs (47-49). Cependant, aucune association n’a été observée entre la communication du résultat aux enfants mineurs et la détresse liée spécifiquement au cancer, évaluée à l’aide de l’échelle IES (Impact of Events Scale) (47, 50).
Les résultats d’une étude menée auprès de 42 parents porteurs ont révélé que l’âge de l’enfant, le sexe du parent et le recours à une chirurgie préventive étaient associés à la décision de communiquer le résultat du test (42). Les enfants âgés (14-18 ans) étaient plus susceptibles d’être informés que les enfants plus jeunes (13 ans et moins) (42). De plus, les résultats d’une autre étude révèlent qu’il n’y a pas de différence significative entre les proportions d’enfants ayant été informés entre l’âge de 14 et 17 ans (85%), ceux âgés de 18 à 30 ans (92%) et ceux de plus de 30 ans (93%), suggérant que les enfants âgés de plus de 14 ans étaient aussi souvent informés du résultat de leur parent qu’un enfant-adulte (51). Les mères communiquent davantage leur résultat que les pères et elles sont plus susceptibles de le faire si elles ont eu une chirurgie préventive (42, 47). En revanche, les antécédents personnels de cancer et le sexe de l’enfant ne sont pas des facteurs associés à la décision de communiquer le résultat du test (42). Enfin, alors que certaines études rapportent n’avoir observé aucune différence significative entre la décision de communiquer et le résultat de test génétique (44, 47), les résultats d’études récentes ont révélé que les enfants étaient plus susceptibles d’être informés si les parents ont eu un résultat négatif (42). Depuis la publication de cette étude, d’autres équipes de recherche ont obtenu des résultats similaires (40, 41).
1.5 Motivations et obstacles à communiquer le résultat aux enfants
Seulement quelques études ont identifié les motivations et les obstacles influençant la décision de communiquer le résultat aux enfants mineurs (41, 42, 44). Les motivations les plus souvent rapportées incluent le sentiment de responsabilité du parent, le droit de l’enfant d’être informé, la promotion d’une communication ouverte et honnête, l’accès au test génétique à l’âge adulte et la sensibilisation (44). Plusieurs parents mentionnent
9
également percevoir la communication du résultat comme une opportunité d’expliquer l’histoire familiale de cancer ou une chirurgie préventive (41, 42).
Parmi les obstacles, les parents mentionnent l’absence d’avantages médicaux, la crainte d’inquiéter inutilement, le risque d’incompréhension dû au jeune âge et le désintérêt de leur enfant pour ce sujet (41, 42). Une majorité des parents estiment avoir besoin de temps pour s’adapter au résultat avant d’être capables d’en parler (41, 42). Finalement, d’autres parents veulent éviter que leur enfant prenne conscience du nombre important de personnes atteintes dans la famille et soulignent que le contexte familial ne se prête pas toujours à ce genre de discussion (ex. : deuil, séparation, maladie) (41, 42). La décision de communiquer ou non le résultat du test BRCA1/2 peut donc varier selon plusieurs facteurs reposant principalement sur les valeurs des parents et le contexte familial.
1.6 Impacts de la communication et réactions chez les enfants
L’impact que peut avoir la communication du résultat de test BRCA1/2 sur les apparentés a largement été étudié (51-60). Cependant, seules quelques études qualitatives ont tenté de mieux comprendre les impacts de la communication sur les enfants mineurs (41-43, 45, 61, 62).
Une première étude, menée auprès de 42 individus, parents d’au moins un enfant âgé de 24 ans et moins au moment du test, s’appuie sur les perceptions des parents pour étudier la compréhension, la réaction des enfants et l’effet sur la relation parent-enfant lors du partage du résultat de test BRCA1/2 (42). Parmi les 86 enfants, 59 étaient âgés de 17 ans et moins. Parmi les 23 parents ayant communiqué leur résultat, près de la moitié ont rapporté que leur enfant ne semblait pas avoir compris l’information partagée. Quant aux réactions des enfants, près de la moitié des parents disent avoir observé des réactions négatives, entre autres de l’inquiétude, de la peur et des pleurs. Cependant, la communication du résultat de test BRCA1/2 ne semble pas avoir eu d’impact sur la relation parent-enfant puisque la majorité des parents indiquent ne pas avoir perçu de changement à cet égard. Quant aux autres parents, près du quart ont dit se sentir plus près de leurs enfants après en avoir discuté.
10
Publiée en 2009, une étude rétrospective a été menée auprès de 22 enfants adultes ayant été informés du résultat de leur parent alors qu’ils étaient âgés de moins de 25 ans (43). La majorité des enfants adultes se rappellent avoir bien compris ce que leurs parents avaient dit la première fois qu’ils ont abordé le sujet, alors qu’ils étaient encore enfants. Par ailleurs, plusieurs signalent que les discussions subséquentes leur ont permis de mieux comprendre ce qui leur avait été expliqué. Une majorité dit avoir cherché de l’information supplémentaire, entre autres en consultant Internet. Lorsque questionnés sur leur réaction initiale, la majorité des participants rapportent s’être bien adaptés à l’information. Quelques participants ont mentionné avoir été surpris, s’être inquiétés à propos de leur propre risque ou de celui de leur parent, avoir nié l’information ou avoir eu des pensées irréalistes. Lorsque questionnés sur l’impact de la communication, 18% rapportent avoir vécu du stress ou de la colère associés au risque de cancer, alors que 77% disent n’avoir perçu aucun impact négatif sur leur santé émotionnelle. Plus important encore, les résultats de cette étude suggèrent qu’informer les enfants mineurs du risque héréditaire pourrait avoir un effet bénéfique sur la santé de ceux-ci. En effet, plusieurs participants ont rapporté qu’avoir été informés du risque héréditaire lorsqu’ils étaient mineurs les avait poussés à adopter des habitudes de vie plus saines, par exemple cesser de fumer. Selon les chercheurs, il existerait donc un avantage à communiquer le résultat aux enfants mineurs.
Une deuxième étude, menée auprès de 253 parents de 505 enfants, portait sur le partage de l’information avec l’enfant, le moment choisi et la perception du parent de la réaction initiale de l’enfant (45). Parmi les 505 enfants, 262 étaient âgés de 3 à 17 ans. Les parents, ayant communiqué leur résultat, ont été questionnés sur leur perception de la réaction initiale de leur enfant. Parmi les 182 parents d’enfants mineurs, 41% ont dit ne pas avoir observé de réactions particulières et 28% mentionnent avoir observé de la joie ou du soulagement, mais seulement chez ceux qui avaient reçu un résultat négatif. Certains parents rapportent que leurs enfants semblaient inquiets (13%) pour eux-mêmes, pour leur parent et pour d’autres membres de la famille. Onze pour cent des parents ont observé de la colère, 7% de l’incompréhension, 4% de la reconnaissance d’avoir été informés et 5% se sont fait poser des questions. Les parents ayant reçu un résultat positif au test de
11
prédisposition génétique ont rapporté plus souvent avoir observé de la détresse chez leurs enfants que les autres parents. Les perceptions des parents varient également selon l’âge de l’enfant. Les parents d’enfants plus jeunes (< 10 ans) ont plus souvent rapporté des réactions de détresse, des difficultés de compréhension de l’information et des questionnements. Quant aux parents d’enfants plus âgés (14 à 24 ans), ils ont davantage observé de l’inquiétude. Une différence dans les réactions est également notable entre les garçons et les filles. Les parents ont observé que les garçons réagissaient de façon plus neutre et posaient plus de questions que les filles, qui semblaient plus inquiètes. En revanche, elles trouvent l’information plus utile que les garçons.
Les études portant sur la communication du résultat de test BRCA1/2 aux enfants mineurs sont sujettes à des limites méthodologiques et éthiques que présentent les études dont les sujets de recherche sont des enfants. Par conséquent, afin d’étudier l’impact de la communication et les réactions chez les enfants mineurs, plusieurs de ces études ont été menées de manière indirecte, en questionnant les parents, ou de manière rétrospective. Une autre limite de ces études est la composition des échantillons qui ne se limite pas aux enfants de moins de 18 ans. Le critère d’inclusion principal étant d’avoir une mère ou un père ayant été testé pour la prédisposition génétique BRCA1/2, alors qu’eux-mêmes n’avaient pas encore accès au test. De ce fait, plusieurs échantillons de ces études sont aussi composés de ce qu’on pourrait qualifier de jeunes adultes (18-25 ans), ne permettant donc pas d’obtenir un portrait précis de l’impact de la communication et des réactions chez les enfants mineurs.
Afin de pallier ces limites, le programme LEGACY Girls Study, implanté à New-York, Philadelphia, Salt Lake City, San Francisco et en Ontario, a été mis sur pied dans le but de mieux comprendre les jeunes filles grandissant dans des familles ayant une histoire familiale ou une prédisposition génétique au cancer du sein. À partir de cette cohorte, une nouvelle étude a été publiée portant sur l’impact de l’histoire familiale de cancer du sein, sur l’ajustement psychologique et sur les comportements de santé des jeunes filles (61). Cette étude a été menée auprès de 869 jeunes filles (6 à 13 ans) et leur mère provenant de familles à risque et de familles dont le risque était comparable à celui de la population
12
générale. Les résultats révèlent que les jeunes filles provenant de familles à plus haut risque (n=441) ne semblent pas avoir davantage de problèmes d’ajustement psychologique et ne présentent pas de comportements de santé différents des jeunes filles du groupe contrôle (n=428). Cependant, les jeunes filles provenant de familles à risque sont plus susceptibles de vivre de la détresse en lien avec le risque de développer un cancer du sein que celles de la population générale. Selon les chercheurs, les mères pourraient bénéficier d’un soutien afin de favoriser une adaptation psychosociale chez les jeunes filles.
1.7 Besoins des parents en matière de communication aux enfants
La littérature suggère que la communication du résultat de test BRCA1/2 aux enfants mineurs se produit relativement fréquemment malgré l’absence d’avantages médicaux pour ces derniers. Toutefois, les parents confrontés à cette situation disent avoir besoin d’être accompagnés dans ce processus (41, 42, 46, 63-65).
Une étude menée auprès de 187 mères confrontées à la décision de communiquer ou non leur résultat de test génétique révèle que 93% d’entre elles auraient souhaité avoir du matériel d’information présentant les avantages et les inconvénients de communiquer le résultat de test génétique et les réactions que de telles discussions peuvent entraîner chez l’enfant (63). Elles suggèrent également que d’échanger avec des parents ayant déjà vécu cette situation aurait pu leur être utile (79%). Certaines d’entre elles auraient aussi aimé rencontrer un professionnel de la santé à sujet, et plus particulièrement, pouvoir en parler avec une conseillère en génétique (63).
Dans une étude similaire, les parents questionnés ont affirmé percevoir l’impartialité des conseillères en génétique comme un avantage dans ce contexte. Ils auraient aimé que ces dernières fournissent des informations sur le nombre de parents qui communiquent et qui ne communiquent pas leur résultat à leurs enfants et les préparent aux réactions et impacts qui pourraient s’ensuivre (41). Cependant, ce ne serait pas tous les parents qui souhaiteraient rencontrer un professionnel de la santé pour les aider dans leur décision. Certains préfèreraient plutôt prendre cette décision seuls ou en consultant l’autre parent (42).
13
1.8 Matériel d’information disponible sur la communication familiale du résultat de test BRCA1/2
Afin d’améliorer la compréhension et la rétention des informations complexes qui sont communiquées lors du conseil génétique, et ainsi optimiser une prise de décision éclairée, du matériel d’information peut être remis aux individus lors de cette rencontre (66, 67).
En 2014, Dorval et al. ont publié une revue systématique décrivant les caractéristiques des outils utilisés sur le plan international dans le contexte des tests BRCA1/2 (68). Les résultats révèlent que bien qu’un nombre important d’outils soient utilisés lors de la phase de conseil génétique, très peu abordent les enjeux liés à la communication du résultat aux membres de la famille. D’après les auteurs, l’élaboration d’outils d’information donnerait l’opportunité aux individus testés de réfléchir aux enjeux liés à la communication du résultat aux enfants et d’en discuter avec les conseillères en génétique.
En 2010, un article a été publié présentant le développement et l’évaluation préliminaire d’un outil d’aide à la décision destiné aux mères ayant eu recours au test BRCA1/2 afin de les aider dans la décision de communiquer ou non leur résultat à leurs enfants mineurs (69). Le contenu de l’outil d’aide à la décision est basé sur des thèmes récurrents identifiés à partir d’une entrevue semi-structurée menée auprès de 17 mères ayant reçu des résultats différents au test BRCA1/2 et ayant au moins une fille âgée de 13 à 17 ans. Une première version de l’outil a ensuite été évaluée par 23 mères, lors d’entrevues téléphoniques et d’un groupe de discussion. Les résultats indiquent que les connaissances des participantes sur la communication parent-enfant se sont améliorées et qu’elles semblent être plus confiantes et satisfaites de leur décision. Les mères ont particulièrement apprécié les récits de parents, les exercices de réflexion et les citations dans l’outil. Elles ont cependant moins aimé le contenu répétitif. Bien qu’à notre connaissance l’outil ne soit pas encore disponible, les résultats présentés dans cet article suggèrent qu’un outil d’aide à la décision pourrait être utile et aider les personnes testées à décider s’ils souhaitent communiquer leur résultat à leurs enfants mineurs, et si oui, comment s’y prendre.
14 1.9 Outils d’aide à la décision
1.9.1 Définition
La prise de décision partagée fait de plus en plus partie de la prestation des soins de santé (70). La prise de décision partagée est un processus nécessitant la participation conjointe du professionnel de la santé et du patient lors d’une décision médicale en présentant les options disponibles et en considérant les préférences et les valeurs du patient (70-72). Découlant de cette pratique, les outils d’aide à la décision ont fait leur apparition (73). Ces outils visent à aider les patients et les professionnels de la santé dans leur décision en rendant explicite la décision à prendre, en fournissant de l’information au sujet des options disponibles et des résultats sur la santé et en clarifiant les valeurs personnelles (74). Bien que le matériel d’information standard puisse aider à comprendre un diagnostic, un traitement ou les recommandations résultantes, il ne permet pas nécessairement aux individus de participer aux décisions concernant leur santé (75). Ils peuvent prendre une variété de formes, que ce soit un format papier (brochure, dépliant, livret) ou électronique (CD, DVD, site Internet) (73, 76). En général, un outil d’aide à la décision doit 1) présenter la décision à prendre, 2) fournir de l’information sur les options disponibles sur un problème de santé en particulier, 3) présenter les avantages et les inconvénients de chaque option et 4) clarifier les valeurs personnelles de l’individu (77). Les outils d’aide à la décision ont été conçus afin d’accompagner, et non de remplacer, les conseils donnés par un professionnel de la santé (73, 76, 77). Les outils d’aide à la décision sont utilisés lorsque plusieurs options sont disponibles pour diagnostiquer ou traiter un problème médical et qu’il n’existe pas d’évidences qu’une option est définitivement meilleure qu’une autre (77, 78). La décision, résultant de cette réflexion, sera alors considérée comme le « meilleur choix » pour l’individu.
1.9.2 Apport des outils d’aide à la décision
Chaque année, la librairie Cochrane publie une revue systématique d’études randomisées sur les outils d’aide à la décision (77). L’objectif principal de cette revue est d’évaluer l’efficacité des outils d’aide à la décision développés pour les individus devant choisir entre plusieurs interventions ou traitements utilisés dans différents contextes
15
médicaux (77). Les résultats de la revue de 2014 sont basés sur l’analyse de 115 études, impliquant 34 444 participants de neuf pays (Australie, Canada, Chine, Finlande, Allemagne, Pays-Bas, Suède, Royaume-Uni et États-Unis) (77). Les effets les plus importants des outils d’aide à la décision par rapport aux outils standards d’information sont l’amélioration des connaissances en lien avec la décision à prendre, une perception plus réaliste des risques et une congruence entre la décision et les valeurs de la personne (77). L’utilisation d’outils d’aide à la décision permet également de diminuer les conflits liés au sentiment d’incertitude devant la décision à la prendre et semble avoir un effet positif sur la communication entre le patient et le professionnel de la santé (77). Par contre, l’effet des outils d’aide à la décision sur l’anxiété ne diffère pas de celui des outils standards d’information (77).
1.9.3 Développement d’un outil d’aide à la décision
Le modèle d’aide à la décision d’Ottawa (ODSF) a été développé afin de guider l’élaboration d’interventions permettant de préparer les patients et les professionnels de la santé à la prise de décision partagée (79). Ce modèle définit les fondements théoriques, méthodologiques et empiriques nécessaires à l’opérationnalisation de concepts pertinents à la prise de décision basée sur des concepts liés à la psychologie, à l’analyse de décision, au conflit décisionnel, au soutien social ainsi qu’aux concepts économiques ayant trait aux valeurs et aux attentes (79). L’objectif d’un outil d’aide à la décision est « de rectifier les déterminants pouvant nuire à la décision telles que des connaissances insuffisantes, des attentes irréalistes, des conflits et du soutien insuffisant » (73). L’ODSF développe également un cadre conceptuel articulé autour de trois pôles 1) identifier les déterminants et les besoins des patients et des professionnels de la santé 2) fournir un soutien à la décision et à sa mise en action et 3) évaluer la qualité du processus et du produit (79).
En 2003, l’International Patient Decision Aids Standards Collaboration (IPDAS), une équipe internationale, composée de médecins, de patients et de décideurs publics de plus de 14 pays, est mis sur pied afin d’améliorer la qualité, l’uniformité et l’efficacité des aides à la décision. Inspiré du modèle de l’ODSF, ils publient un processus de développement systématique s’articulant autour de huit étapes (Annexe 1) : 1) définir le cadre, l’objectif et
16
la population visée, 2) réaliser une revue de la littérature, 3) créer un comité consultatif composé d’experts, 4) rédiger un prototype, 5) évaluer le prototype auprès des patients et de professionnels de la santé, 6) réviser le prototype avec le comité consultatif, 7) tester l’outil auprès de patients et de professionnels de la santé, 8) analyser les résultats et produire un outil final (traduction libre) (73, 78).
1.10 Objectif
Ce projet vise à développer un outil d’aide à la décision pour aider les parents porteurs d’une mutation des gènes BRCA1 ou BRCA2 à dans la décision de communiquer ou non le résultat de test à leurs enfants mineurs.
1.10.1 Pertinence de cette étude
Les individus porteurs d’une mutation des gènes BRCA1/2 s’inquiètent généralement du risque de leurs enfants d’avoir hérité de la mutation génétique familiale. Malgré l’absence d’avantages médicaux pour les enfants mineurs et l’impossibilité pour eux d’être testés avant d’être adultes, une majorité des parents leur communiquent néanmoins le résultat de leur test BRCA1/2. Les parents confrontés à cette situation disent avoir besoin d’être accompagnés dans cette décision. Le peu d’études portant sur les perceptions et réactions des enfants informés du résultat de leur parent alors qu’ils étaient mineurs suggèrent que l’information n’aurait pas d’impact négatif important sur le développement des enfants. Certaines études avanceraient même que la communication du résultat pourrait inciter les enfants à adopter de saines habitudes de vie. À notre connaissance, il n’existe pas d’outils disponibles actuellement, portant sur la communication du résultat BRCA1/2 d’un parent à son enfant (68). Le développement d’un tel outil répondrait aux besoins de soutien et d’accompagnement formulés par les parents et par les professionnels de la santé. De plus, un outil d’aide à la décision est indiqué dans ce contexte où plus d’une option est possible sans pour autant qu’il n’existe d’évidences qu’une de ces options est définitivement meilleure. La décision de communiquer ou non le résultat génétique BRCA1/2 revient donc aux parents.
17
CHAPITRE 2 : Méthodologie
2.1 Contexte du projet de recherche
Ce projet, de nature qualitative, s’inscrit dans le cadre du programme de recherche du Centre ROSE (Ressources en Oncogénétique pour le Soutien et l’Éducation des familles à risque de cancer du sein). Ce programme a pour mission d’informer et soutenir les familles à haut risque de cancer du sein du Québec et de sensibiliser le grand public et les professionnels de la santé aux enjeux des cancers du sein familiaux. Le programme de recherche du Centre ROSE est composé de trois volets : soutien, information et formation, regroupant différentes activités. Le présent projet s’inscrit dans le volet information qui vise, entre autres, à développer du matériel d’information afin d’améliorer la qualité des services offerts et de maximiser la compréhension et la rétention des informations tout au long du processus. Ces outils contribuent à améliorer la qualité des décisions, souvent difficiles, qui doivent être prises par les personnes à haut risque de cancer du sein.
2.2 Développement du prototype de l’outil d’aide à la décision
Le développement de l’outil d’aide à la décision se base sur une adaptation du modèle reconnu de l’IPDAS (73, 78, 80, 81) (Annexe 2). Ce modèle comporte huit étapes.
2.2.1 Cadre, objectif et population visée
La première étape, qui consiste à définir le cadre, l’objectif et la population visée, a été réalisée à partir d’analyse de résultats d’études antérieures de l’équipe de recherche (56, 57).
2.2.2 Revue de la littérature
Les besoins des parents porteurs en matière de soutien et d’information quant à la communication de leur résultat de test BRCA1/2 à leur enfant ont été identifiés à partir d’une revue de la littérature. Celle-ci a été réalisée entre juin et septembre 2013 et mise à jour périodiquement par la suite. Les articles ont été identifiés à partir de la base de données
18
PUBMED en utilisant les mots-clés suivants : « BRCA1/2 », « genetic testing », « family communication », « risk communication », « hereditary breast/ovarian cancer », « disclosure », « children », « offsprings ». Une première sélection des articles a été effectuée à partir des titres et des résumés, puis une deuxième selon le critère d’inclusion. Pour être inclus, les articles devaient porter sur la communication du résultat de test génétique BRCA1/2 aux enfants mineurs. Cette revue de la littérature a permis d’identifier 21 articles traitant de ce sujet (40-47, 51, 61, 63-65, 82-89). Une liste de thèmes a été développée à partir des sujets récurrents afin d’organiser l’information présentée dans chaque étude : l’information communiquée, les avantages/inconvénients, le moment choisi, les conséquences possibles et les recommandations.
2.2.3 Comité consultatif
Un comité consultatif est impliqué dans toutes les étapes de développement du prototype, et ce, jusqu’à la version définitive. Ce comité est composé d’individus travaillant en oncogénétique dont une omnipraticienne-sénologue, une travailleuse sociale, deux infirmières en génétique, un chercheur, une coordonnatrice de recherche et une agente de liaison.
2.2.4 Première version du prototype
Une première version du prototype de l’outil d’aide à la décision a été rédigée basée sur la revue de la littérature et conformément aux critères internationaux préconisés par l’IPDAS. Pour des raisons de pratiques, le prototype a été développé en format papier.
2.2.5 Discussions et modifications par le comité consultatif : processus itératif
Le comité consultatif a révisé et commenté le prototype. Trois rencontres du comité consultatif ont été nécessaires afin d’obtenir un consensus sur les modifications à effectuer dans l’outil. Après avoir incorporé les modifications, le prototype était prêt à être évalué. Le processus de développement inclut un processus itératif permettant de répéter autant de fois que nécessaire les étapes 5, 6 et 7 afin d’atteindre la saturation des données (Figure 1).
19
2.2.6 Évaluation du contenu auprès des patients et des professionnels de la santé
L’évaluation du contenu auprès de la clientèle et des professionnels de la santé a été réalisée selon trois méthodes de collecte différentes : groupe de discussion, entrevue individuelle et questionnaire. L’utilisation de groupe de discussion permet d’obtenir une compréhension approfondie de l’expérience d’une population donnée (90). Les groupes de discussion offrent également un environnement favorisant les échanges entre les participants (90). L’utilisation d’entrevue individuelle a permis d’évaluer si les changements apportés à l’outil, découlant de l’analyse des groupes de discussion, répondaient aux besoins de la clientèle cible. Ces deux premières méthodes ont été utilisées dans le cadre de l’évaluation du contenu auprès des patients (clientèle). Finalement, l’utilisation d’une grille de lecture a permis d’obtenir les commentaires des professionnels de la santé, et de les accommoder, étant donné leurs nombreuses obligations. Le détail des procédures pour ces trois méthodes est présenté dans la prochaine section.
2.3 Évaluation du contenu 2.3.1 Participants
Pour être admissible à cette étude, les participants devaient être porteurs d’une mutation des gènes BRCA1/2. Les participants devaient aussi être parent d’au moins un enfant mineur, au moment où ils ont appris leur résultat et s’exprimer en français. Les participants ayant déjà eu un cancer du sein ou de l’ovaire pouvaient participer à l’étude si leur traitement était terminé depuis au moins un an, afin de ne pas ajouter à l’épreuve qu’ils traversaient déjà. Le fait d’avoir communiqué leur résultat à leur enfant n’était pas une condition requise pour participer à l’étude.
En mai 2014, l’invitation à participer à l’étude a été envoyée en format courriel depuis la liste de diffusion utilisée pour faire la promotion des activités du Centre ROSE. Comme l’inscription à cette liste se fait de façon volontaire, il est difficile d’estimer, sur les 1 500 inscriptions, combien de personnes remplissaient les critères d’admissibilité et par conséquent, de calculer un taux de participation. Au total, dix personnes ont répondu au courriel en acceptant d’être contactées par le groupe de recherche. Les individus ont été
20
contactés par téléphone afin de leur présenter l’étude de façon plus exhaustive et de vérifier leur admissibilité. De ce nombre, neuf répondaient aux critères d’admissibilité. Une personne ne remplissait pas les critères d’inclusion en raison d’un diagnostic récent de cancer et n’a donc pas pris part à l’étude.
Les professionnels de la santé ont également été invités à donner leurs commentaires. Une invitation à participer a été envoyée par courriel aux professionnels de la santé collaborant avec le Centre ROSE.
2.3.2 Mesures
Une grille de lecture a été utilisée afin d’accompagner les participants dans leur première lecture de l’outil (Annexe 3). La grille de lecture comporte des questions sur l’organisation de l’information, le contenu, la compréhension, le niveau de langage et le ton. Cet instrument est composé de 12 items dont le choix de réponses se présente sous la forme d’une échelle de Likert en quatre points et d’un espace pour inscrire des commentaires. Six variables sociodémographiques ont également été utilisées afin de dresser un portrait des caractéristiques des participants. Les variables sociodémographiques sont l’âge, le niveau de scolarité, le statut d’emploi, le statut marital et le statut parental (Annexe 4). Les mesures ont été acheminées par la poste à chacun des participants avec le formulaire d’information et de consentement, une version papier du prototype de l’outil d’aide à la décision, ainsi que les instructions pour les groupes de discussion. La grille de lecture et une version électronique de l’outil ont été envoyées par courriel aux professionnels de la santé ayant accepté de participer à l’étude.
2.3.3 Collecte des données
Groupes de discussion – Deux groupes de discussion de 2 et 4 personnes chacun ont été constitués. La disponibilité des participants a orienté la composition des groupes. Les groupes de discussion ont duré approximativement trois heures et se sont déroulés à l’Hôpital du St-Sacrement du CHU de Québec – Université Laval dans une salle munie d’un système d’enregistrement. Avec l’aide d’un membre de l’équipe de recherche,
21
l’auteure a animé les groupes de discussion à partir d’un guide d’entrevue semi-structuré (Annexe 5). Celui-ci se divise en deux parties. La première a permis d’obtenir les commentaires des participants sur l’organisation de l’information, le contenu, la compréhension, le niveau de langage et le ton. La deuxième partie avait comme but de recueillir les commentaires des participants sur l’aspect général du document : le graphisme, les images, le format. Les participants ont été invités à donner leurs commentaires sur chaque page de l’outil en suivant cet ordre. Finalement, les participants avaient à se prononcer sur ce qu’ils avaient le plus et le moins aimé. Les entretiens ont été enregistrés et retranscrits. Le questionnaire socio-démographique, la grille de lecture, la version papier du prototype de l’outil d’aide à la décision ont été recueillis lors des groupes de discussion.
Entrevues individuelles – Trois entrevues individuelles ont été réalisées entre mars et juillet 2015 avec de nouvelles participantes. Les entrevues individuelles ont duré environ 1 heure. Deux des entrevues ont eu lieu au téléphone et une en personne, et elles ont toutes été enregistrées et retranscrites. L’auteure a dirigé l’entrevue à partir du guide adapté de celui précédemment utilisé lors des groupes discussion. Dans le contexte des groupes de discussion et des entrevues individuelles, le questionnaire socio-démographique, la grille de lecture, la version papier du prototype de l’outil d’aide à la décision ont été recueillis à la fin des rencontres.
Questionnaire –Trois professionnels de la santé (une omnipraticienne, une généticienne et une psychothérapeute) ont fait parvenir leurs commentaires par courriel.
2.3.4 Analyse
À partir des transcriptions, deux membres de l’équipe de recherche, dont l’auteure de ce mémoire, ont effectué une synthèse des différents commentaires selon les thèmes abordés lors des discussions (contenu, compréhension, niveau de langage et support matériel utilisé). La synthèse des commentaires a ensuite été présentée et discutée avec les membres du comité consultatif afin d’atteindre un consensus sur les changements à apporter à l’outil d’aide à la décision pour en arriver à une version finale.
22 2.3.5 Considérations éthiques
Cette étude a été approuvée par le Comité d’éthique de la recherche du CHU de Québec –Université Laval (DR-022-1310). Le consentement écrit a été obtenu de tous les participants. Afin de préserver l’anonymat des participants, aucune information nominative n’était inscrite sur les questionnaires qui n’étaient identifiés que par des numéros de code. Les données nominatives et celles provenant des questionnaires ont été saisies dans deux bases de données différentes, protégées par des codes de sécurité et les enregistrements ont été encryptés. La participation à cette étude n’a entraîné aucun inconvénient à l’exception du temps consacré à remplir les questionnaires, à la première lecture du livret à la maison et à la participation au groupe de discussion ou à l’entrevue individuelle. Les participants ont également dû se déplacer à l’Hôpital du Saint-Sacrement du CHU de Québec – Université Laval. Les participants ont reçu un montant forfaitaire de 50$ afin de couvrir les frais de déplacement, de repas, de garde ou de stationnement occasionnés par leur participation.
23
CHAPITRE 3: Article de recherche
Résumé
Les parents porteurs d’une mutation des gènes BRCA1/2 s’inquiètent généralement du risque de leurs enfants d’avoir hérité de la mutation génétique. Cette étude vise à développer un outil d’aide à la décision à l’intention des parents porteurs quant à la communication du résultat de leur test BRCA1/2 à leurs enfants mineurs. Développé conformément aux critères de l’IPDAS, le prototype a été évalué auprès de mères porteuses d’une mutation des gènes BRCA1/2 (n=9) et de professionnels de la santé (n=3). Les résultats indiquent que les mères désiraient plus qu’un outil les aidant dans leur décision. Elles désiraient un outil pour les préparer à communiquer l’information à leurs enfants. La visée de l’outil a donc été modifiée. L’outil d’aide à la communication comprend les avantages et les inconvénients de communiquer le résultat, des étapes afin de s’y préparer, des conseils et des témoignages de parents. D’autres études seront nécessaires afin d’évaluer l’effet de l’outil sur le processus de communication en tant que tel.
24
Development of a Tool to Guide Parents Carrying a BRCA1/2 Mutation Share
Genetic Results With Underage Children
Authors: Ariane Santerre-Theil (1,2,3), Karine Bouchard (2,3), Dominique St-Pierre (1,2,3), Anne-Marie Drolet (2,3), Jocelyne Chiquette (2,3), Michel Dorval (1,2,3), on behalf of Centre ROSE (1,3)
Affiliations: (1) Faculté de pharmacie, Université Laval, Quebec City, Canada; (2) Centre des maladies du sein Deschênes-Fabia, Quebec City, Canada; (3) Centre de Recherche du CHU de Québec – Université Laval, Hôpital du Saint-Sacrement, Québec, Canada.
Corresponding Author: Michel Dorval, Ph.D., Axe oncologie, Centre de Recherche du CHU de Québec – Université Laval, Hôpital du Saint-Sacrement, 1050 chemin Ste-Foy, QC, Québec, G1S 4L8. Telephone: (418) 682-8047; Fax: (418) 682-7949; email: mdorval@crchudequebec.ulaval.ca
25 Abstract
Aims: To develop a tool to help parents carrying a BRCA1/2 genetic mutation decide if and how to communicate genetic test result to their children. This study sets out the development process of the tool.
Methods: This is a qualitative study. A prototype was developed based on the IPDAS framework. Content was assessed based on feedback from focus groups, individual interviews and healthcare professionals. Participants were BRCA1/2 mutation carriers with underage children. Thematic analysis was conducted using the interview transcripts.
Results: Participants: nine mothers who tested positive for a BRCA1/2 mutation and three healthcare professionals. Instead of a decision aid (to communicate or not), mothers wanted a tool to help them communicate genetic test result to children. To meet the parents’ needs, a communication guidance booklet was developed, setting out the pros and cons of communication, steps to prepare sharing the test result, communication tips and parents’ testimonies.
Conclusions: Globally, the results suggest the mothers want a more comprehensive tool than a decision aid on whether or not to communicate the information to underage children. Further studies are needed to assess the impact of the communication process on parents who are BRCA1/2 mutation carriers and their children.
26 Introduction
BRCA1/2 mutations increase an individual’s lifetime risk of developing breast cancer by up to 87% and ovarian cancer by up to 68% (7, 13-15). Given these risks, it is recommended that women who test positive undergo more frequent monitoring for breast and ovarian cancer starting at age 25. Because this genetic predisposition is inherited as an autosomal dominant trait, each child of a mutation carrier has a 50% risk of inheriting the mutation (7, 9). It is up to parents to decide whether or not to share their BRCA1/2 test result with children. Since breast and ovarian cancers do not develop until adulthood, genetic predisposition testing is not available to underage children (91, 92).
Previous studies indicate that most parents with a BRCA1/2 genetic mutation share their genetic test result shortly after disclosure, even with underage children (40-45). Parents have mixed feelings about their moral duty to share such important information versus the need to protect children from the impact of the information (41, 42, 63, 64). Some parents report feeling duty-bound to promote open honest communication, share the result and raise their child’s awareness (41, 42, 44). They want to discuss their family history of cancer and risk-reduction surgery. Others consider their children too young to understand and want to avoid causing them unnecessary anxiety (41, 42, 44). To make the best decision, parents seek help and support (41, 42, 63, 64). Specifically, they need support to decide if, when and how to share risk information about cancer genetic testing and what reaction to expect from children. They also want healthcare professionals, such as genetic counsellors, to be more involved in the communication process (63). Although a significant number of tools are used in genetic counselling for hereditary breast and ovarian cancer, only one addresses the key issues of communicating results to underage children (68). The tool was written for mothers with a positive genetic test result who have underage daughters. However, despite having been the subject of an article setting out its development and preliminary assessment results, the tool is not yet available for the public use. This article sets out the development process of a decision aid to guide parents in communicating a genetic test result to underage children.
Materials and methods
27
The tool was developed based on the International Patient Decision Aids Standards Collaboration (IPDAS) framework for decision aids (73, 78). Our adapted process includes the eight steps shown in Figure 1. First, the tool’s scope, purpose and target audience were defined using secondary analyses from our previous studies on family communication of BRCA1/2 test results (56-59). Second, a literature review of genetic test result communication by BRCA1/2 mutation carriers to underage children was conducted between June and September 2013 and updated regularly. Twenty-one articles were identified (40-47, 51, 61, 63-65, 82-89). The relevant information from each study was organized according to the following themes: type of information shared with children, the pros and cons of sharing the information, timing and possible consequences of sharing information with children. Third, an advisory committee of healthcare professionals and researchers involved in genetic testing for breast cancer predisposition was involved in all steps of tool development. Fourth, based on the literature review, and in accordance with IPDAS, a first draft prototype was developed (Figure 2a). Fifth, the advisory committee met three times to review and comment on the prototype, until consensus was reached. Sixth, the tool content was evaluated by BRCA1/2 mutation carriers and healthcare professionals. Seventh, the results were analyzed to produce the final version. The tool was developed using an iterative process to repeat steps 5, 6 and 7 as often as necessary until saturation of data.
Evaluation by potential users and healthcare professionals
Participants: Eligible study participants were French-speaking carriers of a deleterious BRCA1/2 germline mutation who were parents of at least one underage child (˂ 18 years old) when tested. Individuals with cancer were eligible if they had been in remission for at least one year. Recruitment was conducted via email using addresses from the Centre ROSE database, which at the time of the study included over 1500 individuals concerned by hereditary breast and ovarian cancer (e.g. patients, family members, healthcare professionals). Other participants were recruited during educational activities. Individuals expressing an interest in participating were then contacted by telephone to explain the study and verify eligibility. Cancer genetics health professionals were also invited to participate. Ethics approval was obtained from the CHU of Quebec Research Center – Laval University Ethics Committee.