HAL Id: hal-01791653
https://hal.archives-ouvertes.fr/hal-01791653
Submitted on 15 Apr 2019
HAL is a multi-disciplinary open access
archive for the deposit and dissemination of
sci-entific research documents, whether they are
pub-lished or not. The documents may come from
teaching and research institutions in France or
abroad, or from public or private research centers.
L’archive ouverte pluridisciplinaire HAL, est
destinée au dépôt et à la diffusion de documents
scientifiques de niveau recherche, publiés ou non,
émanant des établissements d’enseignement et de
recherche français ou étrangers, des laboratoires
publics ou privés.
Peamacléine Pru p 7 : épidémiologie, implications
cliniques et place dans le diagnostic moléculaire de
l’allergie à la pêche en région méditerranéenne
C. Klingebiel, A. Poisson, J. Lidholm, A. Ehrenberg, J. Ostling, V. Liabeuf,
C. Agabriel, J. Birnbaum, F. Porri, R. Arif-Lusson, et al.
To cite this version:
C. Klingebiel, A. Poisson, J. Lidholm, A. Ehrenberg, J. Ostling, et al..
Peamacléine Pru p
7 : épidémiologie, implications cliniques et place dans le diagnostic moléculaire de l’allergie à la
pêche en région méditerranéenne. Revue francaise d’allergologie, Elsevier, 2018, 58 (1), pp.16-22.
�10.1016/j.reval.2017.07.005�. �hal-01791653�
Disponibleenlignesur
ScienceDirect
www.sciencedirect.comRevuefrançaised’allergologie58(2018)16–22
Article
original
Peamacléine
Pru
p
7
:
épidémiologie,
implications
cliniques
et
place
dans
le
diagnostic
moléculaire
de
l’allergie
à
la
pêche
en
région
méditerranéenne
Peamaclein
Pru
p
7:
Epidemiology,
clinical
implications
and
place
in
the
molecular
diagnosis
of
peach
allergy
in
the
Mediterranean
region
of
France
C.
Klingebiel
a,∗,
A.
Poisson
b,
J.
Lidholm
c,
A.
Ehrenberg
c,
J.
Östling
c,
V.
Liabeuf
d,
C.
Agabriel
e,
J.
Birnbaum
d,
F.
Porri
b,
R.
Arif-Lusson
f,
M.
Gouitaa
g,
A.
Aferiat-Derome
h,
D.
Charpin
g,
T.
Sofalvi
g,
I.
Cabon-Boudard
i,
Y.-P.
Massabie-Bouchat
i,
C.
Soler
a,
I.
Cleach
j,
J.-L.
Mège
j,k,
J.
Vitte
f,j,
le
réseau
ANAFORCAL
Provence
aLaboratoireMontgrand,LBMmultisiteSELDAIX,BIOPLUS,13006Marseille,France
bServicedepneumo-allergologie,hôpitalSaint-Joseph,13008Marseille,France
cThermoFisherScientific,Uppsala,Suède
dServicededermatologie-vénéréologie,hôpitalTimone,Aix-Marseilleuniversité,AP–HM,13005Marseille,France
eServicedepédiatriemultidisciplinaire,hôpitalTimone,Aix-Marseilleuniversité,AP–HM,13005Marseille,France
fInsermUMR1067CNRS7333,Aix-Marseilleuniversité,13009Marseille,France
gServicedepneumologie,hôpitalnord,Aix-Marseilleuniversité,AP–HM,13016Marseille,France
hCabinetmédical,lesjardinsdeCastellane,45,avenueJules-Cantini,13006Marseille,France
iCabinetmédical,138,rueduDr-Cauvin,13012Marseille,France
jLaboratoired’immunologie,hôpitaldelaconception,Aix-Marseilleuniversité,AP–HM,13005Marseille,France
kURMITE,UMRCNRS6236,13005Marseille,France
Rec¸ule7juin2017;acceptéle11juillet2017 DisponiblesurInternetle1erseptembre2017
Résumé
Certainesallergiesimmédiatesàlapêchenesontpasélucidéessurleplanmoléculaireparl’explorationdesIgEspécifiquesutiliséesenroutine: extraitdepêche,Prup1(PR-10),Prup3(protéinedetransfertlipidique),Prup4(profiline)etgroupementsglucidiquesàréactivitécroisée, etcemalgrédestestscutanésfortementpositifsetunehistoirecliniqueconvaincante.L’explorationdecespatientsparuntestd’activationdes basophilesenprésenced’extraitdepêcheestfortementpositive,suggérantl’implicationd’unallergènemoléculairedelapêche,absentdesoutils diagnostiquesinvitroactuels.Nousrapportonsicilaforteprévalencedelasensibilisationvis-à-visdelapeamacléine(Prup7)chezlespatients méditerranéensallergiquesàlapêche(régiondeMarseille),ainsiquelescaractèresépidémiologiques,cliniquesetbiologiquesassociésàcenouvel allergène.
©2017Publi´eparElsevierMassonSAS.
Motsclés :Peamacléine;Prup7;Allergieàlapêche;Allergènemoléculaire;IgE;Anaphylaxieàlapêche;Anaphylaxieidiopathique;Profilmoléculairedela pêche;Allergènemajeurdelapêche
Abstract
Molecular-basedallergydiagnostickitsusingstandardIgEreagentssuchaspeachextract,Prup1(PR-10),Prup3(non-specificlipidtransfer protein),Prup4(profilin),andcross-reactivecarbohydratedeterminants,areunabletoidentifytheoffendingallergenincertainpatientswithpeach
∗Auteurcorrespondant.
Adressee-mail:caro.klingebiel@orange.fr(C.Klingebiel).
https://doi.org/10.1016/j.reval.2017.07.005
C.Klingebieletal./Revuefrançaised’allergologie58(2018)16–22 17
allergyinSouthernFrance,despitepositiveskintestsandaconvincingclinicalhistory.Theconstantandhighpositivityofthebasophilactivation testwithpeachextractinsuchpatientssuggeststheinvolvementofamolecularpeachallergennotincludedinexistinginvitrodiagnostickits. Hereinwereportthatpeamaclein(Prup7)isamajorallergeninpeach-allergicpatientsintheMediterranean(Marseille)regionandwedescribe theepidemiological,clinicalandlaboratorycharacteristicsassociatedwiththisnovelallergen.
©2017PublishedbyElsevierMassonSAS.
Keywords: Peamaclein;Prup7;Peachallergy;Molecularallergen;IgE;Peachanaphylaxis;Idiopathicanaphylaxis;Molecularprofileofpeach;Majorallergenof
peach
1. Introduction
Enfonctiondelavoiedesensibilisation, l’hypersensibilité immédiate alimentaire peut résulter d’une réactivité vis-à-vis de deux types d’allergènes. Les allergènes de classe I sontdes allergènesalimentaires responsables d’une sensibili-sation primaire au niveau du tractus digestif. Les allergènes declasseIIsontresponsablesd’unesensibilisationsecondaire parréactivitécroiséed’unesensibilisationprimaireviale trac-tusrespiratoirevis-à-visd’allergènespolliniqueshomologues. Àlafinde lapetiteenfanceetjusqu’àl’âgeadulte, l’allergie alimentaire par réactivité croisée est prédominante (60 %)
[1–3].
EnEuropecentraleetduNord,l’allergènedeclasseIIleplus fréquentappartientàlafamille desPR-10(Betv 1 et homo-logues,dontPrup1),moinsfréquemmentauxprofilines (Bet v 2 ethomologues, dontPrup 4). Danslesrégions méditer-ranéennes,ilexisteuneplusfortesensibilisationvis-à-visdes allergènesdelafamilledesprofilinesetdesprotéinesdetransfert lipidique(LTP).L’allergènePrup3estlechefdefiledugroupe desLTP«alimentairesetpolliniquesàréactivitécroisée»,qui comprendentreautresMald3(pomme),Plaa3(platane),Ole e7(olivier)etArtv3 (armoise).Lesprévalencesdeces sen-sibilisationssontcorréléesauxprévalencesdessensibilisations primairesvis-à-visdespollens[3,4].
L’allergiealimentaireauxfruitsestunecausefréquentede consultationd’allergologie.Lesfruitslesplussouventencause appartiennentàlafamilledesRosacées[4].Cetteallergie ali-mentaireestleplussouventdueàunsyndromepollen-fruit: pollinose primaire avec sensibilisation secondaire aux fruits. Dans ce cadre, l’allergie alimentaire à la pêche est souvent décriteparunsyndromeoral(Prup1,plusrarementPrup4) etdans de plusrares casuneanaphylaxie sévère (impliquant classiquementPrup3).
Dans les régions méditerranéennes, de nombreux cas d’allergie avéréeà la pêche ne sont pas élucidés sur le plan moléculaireparlarecherched’IgEspécifiquesdelapêchePru p 1,Prup 3, Prup 4 etgroupements glucidiquesvégétaux à réactivitécroisée(CCD)[5].Ilexisteunediscordanceentredes testscutanés(TC)fortementpositifsetdesvaleursd’IgEcontre la pêchetrès basses, voire indétectables. Le test d’activation desbasophiles(TAB)avecl’extraitdepêcheetPrup3s’avère positifchez ces patients, suggérantl’implication d’un nouvel allergène[6–8].Eneffet,leréactifutilisépourleTABétantun allergènemoléculairenaturelnPrup3,uneéventuelle copuri-ficationdecelui-ciaveclapeamacléine(Prup7) estpossible
[9,10].Nousavonsdonceffectuéunerecherched’IgEvis-à-vis dePrup7pourcespatients[8].
Prup7 oupeamacléineestunpeptideantimicrobiendela familledesgibberellinregulatedprotein[9–12].Cesprotéines interviennentdansladéfensedesvégétauxetplus particulière-mentdesfruitsavecunefonctionantimicrobienne.Onlestrouve aussibiendanslapeauquedanslapulpedufruit.Des homo-loguessontdécritsdansdiversalimentsd’originevégétale:la pêche,l’orange(Cits7)[13],lagrenade(Pung7:pommaclein)
[11],l’abricotduJapon(Prum7),ainsiquedansletubercule depommedeterre[9].
Lapeamacléineestunepetitemoléculede7kDa(par compa-raison, la LTP Pru p 3 a une masse moléculaire de 9kDa) comprenant63acidesaminés.Elleestricheencystéinesavec 19%derésiduscystéineet6pontsdisulfureluiconférantune structuremixte:␣-hélicoïdaleetfeuillet-plissé.
Lapeamacléineestuneprotéinebasiqueavecunpoint iso-électriquesituéà8,97,prochedeceluidePrup3à9,25.Elle estthermorésistanteetrésistanteàladigestionacide,parcontre, ellen’estpasdigéréeparlatrypsine,contrairementàPrup3qui l’estpartiellement.
Demassemoléculaireetpointisoélectriqueproches,Prup 3etPrup 7sontdifficilementséparables.Ilestdoncpossible d’avoirunecontaminationdenPrup3parPrup7.
Afind’évaluerlafréquencedesensibilisationvis-à-visdece nouvelallergènedanslarégiondeMarseille,nousavons sélec-tionnédessérumsdepatientspourlesquelsunehistoireclinique d’allergieàlapêcheavait étéévoquée, ainsiquedespatients avec une histoired’anaphylaxie sans cause retrouvée malgré une anamnèse minutieuseet des testscutanés et biologiques exhaustifs.
2. Patientsetméthodes 2.1. Patients
Étuderétrospectivemonocentriqueensoincourantdes dos-siersetdesrésultatsbiologiquesde121patientsexploréspour unesuspiciond’allergieàlapêchedansleréseauANAFORCAL Provence etau laboratoired’immunologie de l’hôpitalde La Conceptionoudansunlaboratoireprivéduréseau SELDAIX-BIOPLUS,entrefévrier2012etjuin2016.
Recueil des arguments diagnostiques : histoire clinique, résultats des tests cutanés avec l’extrait commercial et/ou l’alimentnatif,sensibilisationbiologiquevis-à-visdesextraits
etdesallergènesmoléculairesdisponiblespourlediagnosticin vitro.
2.2. Corrélationentrelesdonnéescliniquesetbiologiques
Les données cliniques relatives aux symptômes d’allergie alimentaire et lerésultat des TC àlectureimmédiate ont été comparésauxdonnéesbiologiques.
Lagravité de laréaction immédiate clinique aété classée selonles3gradesdesévéritéd’anaphylaxiedécritsparMuraro, adaptédeSampson[14,15].
Ces auteursretiennent lediagnostic d’anaphylaxiecomme hautementprobablesi1des3critèressuivantsestrempli: • réaction aiguë (minutes à quelques heures) à type de
signescutanéo-muqueux(urticairegénéralisée,prurit, bouf-féesvaso-motrices,œdèmedelalangueetluette)associésàau moins1desélémentssuivants:signesrespiratoires(dyspnée, bronchospasme,stridor,hypoxie)ousignescardiovasculaires àtyped’hypotension;
• aumoins2ouplusdescritèressuivantsapparaissantdansles minutes à quelquesheures aprèsexposition àun allergène probable pour ce patient : signes cutanéo-muqueux (urti-cairegénéralisée,prurit,boufféesvaso-motrices,œdèmedela langueetluette),respiratoires(dyspnée,bronchospasme, stri-dor, hypoxie),cardiovasculaires (hypotension) et/ousignes digestifspersistants(douleursabdominales,vomissements); • étatdechoc:hypotensiondeplusde30%parrapportàla tensionartériellebasale,collapsus,aprèsexpositionàun aller-gèneconnudupatient,survenantdanslesminutesàquelques heures.
Notonsquela définitiondesauteurs « minutesàquelques heures » peut être rapprochée de l’intervalle généralement acceptéde4heuresmaximum.
2.3. Prélèvements
Les prélèvements veineux ont été réalisés sur tube sans anticoagulant,sansconditionspré-analytiquesparticulières(le résultatdudosaged’IgEspécifiquesestconnupourêtre indé-pendantd’uneprisemédicamenteuseoualimentaire).Lestubes ontété centrifugés etlesérumconservé à+4◦Cpendant une semaine,−20◦Cau-delàjusqu’à réalisationdu dosage d’IgE spécifiques.
LesTAB ontété effectuéssursang totaldans les2heures suivantleprélèvementveineuxsurtubeEDTA.
2.4. Méthodes,appareilsetréactifs 2.4.1. IgEspécifiquesunitaires
LarechercheetledosagedesIgEspécifiquesontétéréalisés chezles121patientsparlaméthodefluoro-immunoenzymatique FEIA ImmunoCAP® de Thermo Fisher (ImmunoCAP 250, ThermoFisher,Uppsala,Suède).Cetteméthodenécessiteune prised’essaide40Ldesérum(volumemort+20L).C’est
uneméthodequantitativeavecunrenduderésultatslinéaireentre 0,10kUA/L et100kUA/L. Leseuil de positivité a été fixé à 0,10kUA/L[16–19].
Lesdosagesd’IgEspécifiquesvis-à-visdel’extraitdepêche, desallergènes moléculairesPrup 1,Prup3,Prup4 etCCD (groupements MUXF3, o214) et du pollen de Cupressacées (extrait depollen de cyprèst23, degenévrier t6ou allergène majeuretspécifiquenCupa1t226)ontétéréalisésavecles réac-tifscommercialiséspourdiagnosticinvitro,selondesméthodes accréditéesCOFRAC.
Larechercheetledosaged’IgEspécifiquesvis-à-visdePru p7ontétéeffectuésparledépartementR&DdeThermoFisher ImmunoDiagnostics(Uppsala,Suède),enutilisantPrup7natif etrecombinantencouplageexpérimentalpourFEIA Immuno-CAP.
Chez 6 patients, la recherche d’IgE spécifiques vis-à-vis des allergènes moléculaires Prup 1, Prup 3 etPrup 4 sous formepurifiéeaétécontrôléeparméthodeImmulite(Siemens, Munich,Italie).
2.4.2. MultitestFABER®
UneexplorationparmultitestFABER(CAAM,Rome, Ita-lie) a été réalisée chez 6 patients. La méthode FABER offre unpanelmixtede122extraitsallergéniqueset122allergènes moléculaires,incluantdeuxextraitsdepêche(pulpeetpeau),les allergènesPrup1,Prup3etPrup7,ainsiquel’homologuePun g7(grenade).FABERestuneméthodesemi-quantitative,avec unrenduderésultatenunitésquiluisontpropres(fluorescence
intensityunits[FIU]).
2.4.3. Testsd’activationdesbasophiles(TAB)
Un TAB (trousse et réactifs de Bühlmann Laboratories, Suisse)enprésenced’extraitdepêcheetdesallergènes molé-culaires nPru p 3 (LTP), Mal d 1 (réactif PR-10), Tri a 12 (réactif profiline) a été réalisé pour 10 patients suivant une procédure standard avec 4 concentrations par allergène (concentrationsfinales62,5ng/mL,31,3ng/mL,12,5ng/mLet 1,25ng/mL). L’extrait de lait de vache a servi ici comme témoindebonnetoléranceclinique(touslespatients consom-maient du lait et des produits laitiers régulièrement et sans problème).
Dans un deuxième temps, un TAB en présence de Pru p 7 et de Pru p 3 purifiés et recombinants (fournis gracieuse-mentparThermoFisher)aétéréalisépour7patients.Pourcette seconde sériedeTAB, 11concentrationsdechaque allergène ont ététestéesavecdeux méthodes:lekitcommercial Bühl-mannLaboratoriesetuneméthodeBeckman-Coulter.LeTABa étéconsidérépositifquandlepourcentagedebasophiles expo-sés àl’allergèneetexprimant CD63étaitaumoinsdeux fois supérieurautémoinnégatif.Nousavonstesté7 patients,dont 6allergiquessévèresàlapêcheetprésentantdesIgEPrup7 iso-lées(sansIgEPrup1,Prup4,Prup3ouCCD)etunpatient présentant des épisodes anaphylactiques répétésavec des ali-mentsvégétaux,sansIgEPrup1,Prup3,Prup4,Prup7ou CCD.
C.Klingebieletal./Revuefrançaised’allergologie58(2018)16–22 19
2.5. Expressiondesrésultatsetanalysestatistique
Les données sont exprimées en médiane et extrêmes. L’analyse statistique a été effectuée avec le test de Mann-WhitneyetcoefficientdedéterminationR2.Lesrésultatssont considéréscommestatistiquementsignificatifspourp≤0,05.
3. Résultats
3.1. Démographieetdiagnosticretenu
Parmi les 121 patients, on trouve 51 hommes (sex-ratio hommefemme:0,73).L’âgemédianestde19,8ans(4–74).
L’analysedesdonnéescliniques(histoirecliniqueetrésultats destestscutanés)apermisdedistinguer3groupesdepatients: allergiquesconfirmésàlapêche(n=74),nonallergiques (tolé-rants)àlapêche (n=35) etimpossiblesàconclure. Eneffet, pour12patients,lediagnosticd’allergiealimentaireàlapêche n’a pas pu être établi (renseignements cliniques insuffisants, testscutanés ininterprétables ou manquants, histoire clinique peuconvaincante).
3.2. Caractérisationdelasensibilisationvis-à-visdePrup 7
Surles121sérumsanalysés,112(93%)sesontrévélés posi-tifsvis-à-visdel’extraitdepêcheet77(64%)ontmontréune réactivitéIgEvis-à-visderPrup7.Parmiles74patients aller-giquesconfirmésàlapêche,58(78%)avaientdesIgEanti-Pru p7positives(Tableau1).
Dans49/77(64%)descas,laréactivitéIgEàPrup7était isolée(pasdedétectiond’IgEvis-à-visderPrup1,rPrup3ou rPrup4).
Tableau1
Profilmoléculairedelapêchedansles3groupesdepatients:allergiquesàla pêche(n=74),tolérantsàlapêche(n=35)etpatientsnongroupables(n=12). Prévalence Prup1 Prup3 Prup4 Prup7 Allergiquesàlapêche, 74patients 15(20%) 21(28%) 12(16%) 58(78%) Tolérantsàlapêche, 35patients 7(20%) 14(40%) 12(34%) 11(31%) Renseignementscliniques insuffisantsounon obtenus,12patients 5(42%) 2(17%) 3(25%) 8(67%)
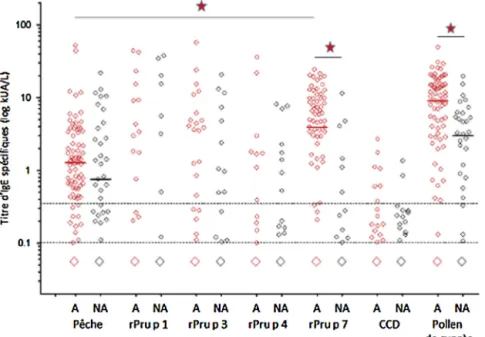
Lestauxd’IgEspécifiquesvis-à-visdePrup7étaientplus élevés que ceux vis-à-vis de l’extrait de pêche (médiane : 4,9contre1,3kUA/L;respectivementintervalles:0,10à30,72; 0,10à52,4;p=0,003;coefficientdecorrélation−0,15)(Fig.1). Parmiles7sérumsnégatifsenIgEcontrelapêche,deuxont ététrouvéspositifsvis-à-visderPrup7(0,81et1,24kUA/L).De même,parmiles19sérumspourlesquelslesvaleursd’IgEcontre lapêcheétaientcomprisesentre0,10et0,35kUA/L,14ontété trouvéspositifsàrPrup7(0,10à6,44kUA/L)avecdesvaleurs d’IgEsupérieuresàcellesobtenuesavecl’extrait.
TouslespatientssensibilisésàPrup7étaientsensibilisésaux pollensdeCupressacées,maisl’inversen’étaitpasvrai.
3.3. Profilmoléculairedesensibilisationetparticularités cliniques
Parmi les74 patients allergiques confirmésàla pêche,41 (55 %)décrivent uneréactionclinique sévèregrade IIIaprès ingestion de pêche. Au total, 24 patients (32 %) décrivent l’existenced’uncofacteur,leplussouventl’effort(17patients sur24),parfoislaprised’alcool.Uneparticularitécliniqueàtype
Fig.1.Analysequantitativedelasensibilisationvis-à-visdel’extraitetdesallergènesmoléculairesdepêcheetdespollensdeCupressacées.Lesvaleursminimales, médianes(si>0,10kUA/L)etmaximalesdestitresd’IgEspécifiquessontreprésentéesenéchellelogarithmiquekUA/L.Chezlespatientsallergiquesàlapêche, letitred’IgEPrup7estplusélevéqueletitred’IgEcontrel’extrait(p=0,003).Lestitresd’IgEPrup7etd’IgECupressacéessontplusélevéschezlespatients allergiquesàlapêche(p<0,01).Iln’yapasdedifférencesignificativepourlesIgEPrup1,Prup3etPrup4.
Tableau2
PrévalencedelasensibilisationbiologiqueàPrup7etdonnéescliniquesdansles2populationsdepatients:allergiquesàlapêche(n=74)ettolérantsàlapêche (n=35). Prévalencedela sensibilisationà Prup7(effectifet %) Anaphylaxie gradeI: MURARO Anaphylaxie gradeII: MURARO Anaphylaxie gradeIII: MURARO Gravitédela réactionnon précisée Cofacteur identifié Œdèmede laface Allergiquesàla pêche,74patients 58(78%) 17(23%) 10(14%) 41(55%) 6(8%) 24(32%) 39(53%) Tolérantsàlapêche, 35patients 11(31%) 14(40%) 3(9%) 7(20%) 11(31%) 1(3%) 5(14%)
Pour6patientsdanslegroupeallergiques,et11patientsdanslegroupetolérants,l’analysedesrenseignementscliniquesn’apaspermisdeclasserlagravitédela réactionallergique.
d’œdèmedelafaceestretrouvéechez39(53%)despatients allergiquesconfirmésàlapêche(Tableau2).
Chez les patients allergiques à la pêche, des différences cliniquessontobservéesselonleprofilmoléculairede sensibi-lisation(Tableau3).Lesréactionscliniquessévères,l’existence d’unœdèmedelafaceetlaprésencedecofacteurssontplus fré-quentschezlespatientsavecsensibilisationbiologiquevis-à-vis dePrup7.
Enfonctiondel’allergènemoléculairedétecté,d’autres par-ticularités cliniques ont été notées. Les 3 grades de sévérité cliniquesontpossibleslorsquedesIgEcontrelaLTPPrup3sont encause.LesseulesréactionscliniquesgradeIIIassociéesàun profilPR-10Prup1ouprofilinePrup4sontsurvenueschez despatientsco-sensibilisésavecPrup7.
3.4. MultitestFABER
LaprésencedePrup7etdesonhomologuedelagrenadePun g7ajustifiélaréalisationd’uneexplorationFABER,confirmant lapositivitéPrup7chez5patients(5/6).
SurlemultitestFABER,troispatientsétaientégalement posi-tifspourl’extraitdepêche:2vis-à-visdelapeauuniquement, 1vis-à-visdelapeauetlapulpe.Lanégativitévis-à-visdePru p3aétéconfirméeenFABERpourles6patients.
Pourun patient,lesIgEspécifiques unitairesetleTAB se sontrévélés positifs pour Prup 7 malgré unrésultat FABER négatif.
3.5. ExplorationdelacapacitéactivatricedePrup7en testfonctionnel:testd’activationdesbasophiles 3.5.1. TABavecextraitdepêcheetnPrup3Bühlmann Laboratories
LesTABréalisésenprésenced’extraitdepêcheetdenPru p 3purà95% (BühlmannLaboratories)étaientpositifschez 10/10patientspourl’extraitdepêcheetpournPrup3.Ilsétaient négatifs pour Mald1 (réactif représentantlafamillePR-10), pour Tria12(réactifreprésentantlafamilledesprofilines)et pour l’extraitdelait devacheservanticide témoinde bonne toléranceclinique.
3.5.2. TABavecnPrup7,rPrup7,nPrup3etrPrup 3ThermoFisher
LesTABréalisésenprésencedenPrup7etderPrup7étaient positifschezles6patientsavecdesIgEunitairescontrePrup 7détectables(6/6)etnégatifchezlepatientsansIgEdétectées contrePrup7,prouvantl’activitéallergéniquedePrup7etla spécificitédelaréaction.L’ensembledesTABétaitnégatifavec lesallergènesrPrup3etnPrup3depuretévérifiéepar spectro-métriedemassepourl’ensembledelagammedeconcentrations finalestestées,allantde0,25pg/mLà2,5g/mL.
LaconcordanceTAB–multitestFABERpourlapositivitéPru p 7 étaitde 5/6,le patient sans IgE Prup 7 détectables par méthodeFABERréagissantfortementànPrup7etrPrup7lors duTAB(maisavecdesIgEunitairespositivescontrePrup7).
LesallergènesnPrup7etrPrup7ontdémontréaucoursdes TABlacapacitéàactiverlesbasophilesdèslaconcentrationde
Tableau3
Particularitéscliniquesenfonctionduprofildesensibilisationmoléculairechezlespatientsallergiquesconfirmésvis-à-visdelapêche(n=74). Particularitéscliniqueset
cofacteurs(nombrede patients)
Prup1 Prup3 Prup4 Prup7
MURAROI 3(dont1co-sensibiliséPrup7) 7(dont4co-sensibilisésPrup7) 3(dont1co-sensibiliséPrup7) 10
MURAROII 2 3(dont2co-sensibilisésPrup7) 0 7
MURAROIII 1(co-sensibiliséPrup7) 3 1(co-sensibiliséPrup7) 37
Œdèmedelaface 6(dont4co-sensibilisésPrup7) 6(dont2co-sensibilisésPrup7) 1 31
Cofacteurs 3(dont2co-sensibilisésPrup7) 1 0 21
Pour4patientssensibilisésàPrup7,l’analysedurecueildesrenseignementscliniquesn’apaspermisdeclasserlagravitédelaréaction.Pourunpatientavec cofacteuretœdèmedelaface,aucunsubstratmoléculairedelapêchen’aétémisenévidence.
C.Klingebieletal./Revuefrançaised’allergologie58(2018)16–22 21
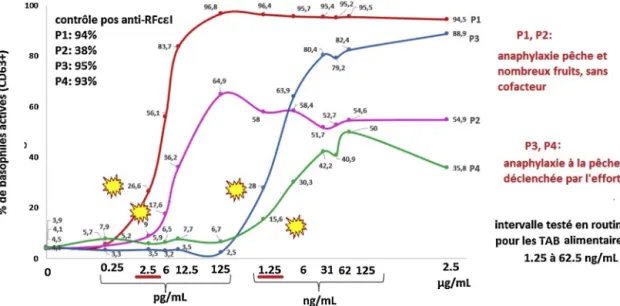
Fig.2.Courbesdose-réponsedel’activationdesbasophilesavecPrup7chez4patientsreprésentatifs.Laconcentrationminimaleactivatriceestindiquéepourchaque patientparuneétoile.L’intensitémaximaled’activationenprésencedePrup7peutêtrecomparéeàl’intensitéobservéeaveclecontrôlepositifanti-RFcepsilonI pourchaquepatient.Onobservedeuxprofilsderéponse:doseactivatricede2,5pg/mLdePrup7pourlesbasophilesdespatientsréagissantsanscofacteuretde 1,25ng/mLpourlesbasophilesdespatientsréagissantavecuncofacteur.L’intensitémaximaled’activationavecPrup7estcomparableavecl’intensitéd’activation aveclecontrôlepositif,saufpourunpatient(P4)chezquielleresteinférieured’environ50%.
2,5pg/mL(5/6patients),500×inférieureàladernière concen-trationdelagammequenousutilisonsenroutine(1,25ng/mL) et10000×inférieureàlaconcentrationhabituellement recom-mandéepourunaliment,àsavoir25à100ng/mL(Fig.2).
4. Discussion
L’analysede121patientsdelarégiondeMarseilleapermis demontreretdécrirel’implicationdelapeamacléine(Prup7) chez78%despatientsallergiquesconfirmésàlapêcheversus 28% pourPrup3,20%pourPrup1et16%pourPrup4. Prup7 estdans notresérie leseulallergènemajeur chezces patients.LapertinencefonctionnelledePrup7estconfirmée parlapositivité destestsd’activationdesbasophileschez les patients présentant des IgEvis-à-vis de Prup 7. Un élément remarquableestl’activationdesbasophilesdèslazonedestrès faiblesdosesdePrup7(2,5pg/mL).Lasensibilisationvis-à-vis dePrup7estprésentedèsl’enfance,avecunâgeminimumde 4ansetunemédianeautourde20ans.
Parmilesraisonspouvantexpliquerl’absencededescription decettesensibilisationàforteprévalenceilnoussemble impor-tant de soulignerles mauvaises performances des extraitsde pêche,souventutiliséspourlediagnosticdepremièreintention. Dansnotrepopulation,detrèsfaiblesvaleursd’IgEunitaires vis-à-visdel’extraitdepêche(indétectablesou0,10–0,35kUA/L) étaient associées à des IgE contre Pru p 7 allant jusqu’à 6,44kUA/L.Letitred’IgEvis-à-visdePrup7était systémati-quementsupérieurautitred’IgEcontrel’extraitdepêchechez les77patientssensibilisésàPrup7.Demanièresimilaire,des IgEcontre les extraits de pêche(peau et pulpe) présents sur lemultitestFABERétaientdétectéesseulementchez2patients parmiles5présentantdesIgEPrup7aveccettemêmeméthode. Prisensemble,cesrésultatssuggèrentquePrup 7est insuffi-sammentreprésenté dans lesextraitsutilisés pourlesréactifs
dediagnosticIgEinvitro.Uneévaluationdesextraits commer-ciauxpourtestscutanéspourraitêtreutile,bienquel’utilisation desalimentsnatifsrestelaréférencedanscedomaine.
Surleplanclinique,uneétude d’Inomata etal.de2014a montréquelapeamacléineétaitunmarqueurdesévéritéclinique dansl’allergiealimentaireàlapêcheauJapon[20].Demanière similaire,dansnotrepopulationd’étude,Prup 7estassociéà desréactionscliniquessévères:lesIgEvis-à-visdePrup7sont présenteschez37des41patientsallergiquesàlapêcheetclassés gradeIIIdeMuraro[14].
Dans notre étude, l’intervention d’un cofacteur, généra-lement l’effort physique, est très fréquente en association avec lasensibilisationàPru p 7 (21 patients/24). Cerésultat pourrait expliquer l’échec fréquent dans l’identification d’un substrat moléculaire dans les anaphylaxies alimentaires aux fruitsinduitesparl’effort.Danslalittérature,onretrouvedescas d’anaphylaxieliéeauxfruitsdesRosacéesetinduiteparl’effort, parfois attribuéeau substrat LTP dans les régions méditerra-néennes [21].Dansd’autres cas,lesubstrat moléculairereste inconnu,notammentpourlesréactionsàlapêche.L’implication d’IgEvis-à-visd’uneisoformedePrup3différentedecelle uti-liséepourlarecherched’IgEspécifiquesenroutineetdoncnon détectablesparlesméthodesactuellesaétéproposée[22–24]. Comptetenudelaparentéphysico-chimiquedePrup 3etde Prup7etdelacapacitéactivatricedePrup7àdesdosestrès inférieuresàcelleshabituellementobservéesaveclesallergènes alimentaires,dumoinsinvitro,laprésencedePrup7dansles préparationsutiliséespourcertainesétudesantérieuresnepeut êtreexclue.
Uneautreparticularitécliniquedespatientsallergiquesàla pêcheetsensibilisésàPrup7 estlasurvenuefréquented’un œdème de la face, rapportée chez les patients japonais [25]
et confirmée dans notre étude avecune prévalence de 31/58 (53%).
Enfin,nous avons égalementdocumentéla présence cons-tante d’IgE anti-Cupressacéeschez les patients sensibilisés à Prup7.Chezchaquepatient,letitred’IgEvis-à-visdupollen deCupressacéesestsystématiquementsupérieurautitred’IgE vis-à-visdePrup7.Cetteétudeayantétéréaliséeuniquement chez des patients de la région de Marseille, il serait intéres-santdelacompléterparuneétudesurlasensibilisationàPru p 7horsdelazone depollinisationdesCupressacéesafinde mieuxcomprendrelesliensentrePrup7etlespollinoses.
5. Conclusion
Prup7complèteleprofilmoléculairedelapêcheets’avère nécessairepourrésoudrelediagnosticd’allergieàlapêchechez lespatientsméditerranéens.Dansl’allergieàlapêche,lamise en évidenced’un substrat moléculairePrup 7 est unfacteur pronostiquede sévérité clinique,d’anaphylaxie alimentaire à la pêcheinduitepar l’exercice et d’une présentationclinique incluantfréquemmentunœdèmedelaface.
La cosensibilisation constante au pollen de Cupressacées placePrup7enpositiondecandidatpourlechaînonmanquant dusyndromecyprès-pêchedesrégionsméditerranéennes.
Déclarationdeliensd’intérêts
Jonas Lidholm, Angelica Ehrenberg et Jonas Östling sont employésparThermoFisher.RihaneArif-Lussonestdoctorante en thèseCIFRE encollaboration avecBeckman Coulter.Les autresauteursdéclarentnepasavoirdeliensd’intérêts.
Remerciements
Mme Colette Mavier et Mme Catherine Tissot (Thermo Fisher),DrFabriceGuerber(LaboratoiresOriade-Noviale, Gre-noble).
Références
[1]Werfel T, Asero R, Ballmer-Weber BK,Beyer K, Enrique E, Knulst AC, et al.Position paperof the EAACI: food allergydue to immu-nological cross-reactions with common inhalant allergens. Allergy 2015;70:1079–90.
[2]PopescuFD.Cross-reactivitybetweenaeroallergensandfoodallergens. WorldJMethodol2015;5:31–50.
[3]MastrorilliC,TripodiS,CaffarelliC,PernaS,DiRienza-BusincoA,SfikaI, etal.Endotypesofpollen-foodsyndromeinchildrenwithseasonalallergic rhinoconjunctivitis:amolecularclassification.Allergy2016:1181–91.
[4]AndersenMB,HallS,DragstedLO.Identificationofeuropeanallergy patternstotheallergenfamiliesPR-10,LTP,andprofilinfromRosaceae fruits.ClinRevAllergyImmunol2011;41:4–19.
[5]TenenbaumJ,LeoniMC,DemolyMP,BourrainJL,DemolyP,Chiriac AM.Allergieàlapêcheavectauxd’IgEspécifiquespêcheetallergènes majeursnégatifsoufaiblementpositifs.RevFrAllergol2016;56:441–5.
[6]Klingebiel C, PoissonA,Rousseau M,GuieuC, CleachI, Mège JL, etal.SensibilisationPrup3chezl’allergiqueàlapêche:apportdutest
d’activationdesbasophileschezlespatientsavecIgEPrup3indétectables. RevFrAllergol2016;56:282.
[7]KlingebielC,PoissonA,RousseauM,GuieuC,CleachI,MègeJ-L,etal. ThebasophilactivationtestconfirmsPrup3sensitizationinpeach-allergic patientswithnegativesIgEtoPrup3.Allergy2016;71(S102):154.
[8]KlingebielC,LidholmJ,EhrenbergA,ÖstlingJ,CleachI,MègeJL,etal. Prup7isamajorpeachallergeninpatientsfromSouthernFrance.Clin TranslAllergy2017;7(S1):OP18.
[9]TuppoL,AlessandriC,PomponiD,PiconeD,TamburriniM,Ferrara R,etal.Peamaclein–anewpeachallergenicprotein:similarities, dif-ferencesandmisleadingfeaturescomparedtoPrup3.ClinExpAllergy 2013;43:128–40.
[10]TuppoL,SpadacciniR,AlessandriC,WienkH,BoelensR,GiangriecoI, etal.Structure,stability,andIgEbindingofthepeachallergenpeamaclein (Prup7).Biopolymers(PeptideScience)2014;102:416–25.
[11]TuppoL,etal.Pomegranatecultivars:identificationofthenewIgE-binding proteinpommacleinandanalysisofanti-oxidantvariability.JAgricFood Chem2017;65(13):2702–10.
[12]PortoWF,FrancoOL.Theoreticalstructuralinsightsintothesnakin/GASA family.Peptides2013;44:163–7.
[13]InomataN,MiyagawaM,AiharaM.Identificationoforangepeamaclein asanewallergeninorangeallergy.Allergy2015;70(S102):107.
[14]MuraroA,RobertsG,ClarkA,EigenmannPA,HalkenS,LackG,etal.The managementofanaphylaxisinchildhood:positionpaperoftheEuropean academyofallergologyandclinicalimmunology.Allergy2007;62:857–71.
[15]SampsonHA,Munoz-FurlongA,CampbellRL,AdkinsonJrNF,BockSA, BranumA,etal.Secondsymposiumonthedefinitionandmanagement ofanaphylaxis: summaryreport—secondnationalinstituteofallergy andinfectiousdisease/foodallergyandanaphylaxisnetworksymposium. JAllergyClinImmunol2006;117:391–7.
[16]Kleine-TebbeJ,PoulsenLK,HamiltonRG.Qualitymanagementin IgE-basedallergydiagnostics.JLabMed2016;40:81–96.
[17]LambertC,SarratA,BienvenuF,BrabantS,Nicaise-RolandP,Alyanakian MA,etal.TheimportanceofENISO15189accreditationof allergen-specificIgEdeterminationforreliableinvitroallergydiagnosis.Allergy 2015;70:180–6.
[18]HamiltonRG.ClinicallaboratoriesworldwideneedtoreportIgEantibody resultsonclinicalspecimensasanalyticalresultsandnotusedifferential positivethresholds.JAllergyClinImmunol2015;136:811–2.
[19]HamiltonRG.Allergicsensitizationisakeyriskfactorforbutnot syno-nymouswithallergicdisease.JAllergyClinImmunol2014;134:360–1.
[20]InomataN, OkazakiF,Moriyama T, Nomura Y,Yamaguchi Y, Hon-johT, etal.Identificationof peamaclein asa markerallergen related tosystemicreactions inpeach allergy.AnnAllergy AsthmaImmunol 2014;112:175–83.
[21]RomanoA, Scala E, Rumi G,Gaeta F, Caruso C, AlonziC, etal. Lipidtransferproteins: themost frequentsensitizerin Italiansubjects with food-dependent exercise-induced anaphylaxis. Clin Exp Allergy 2012;42:1643–53.
[22]BianchiA,DiRienzoBusincoA,BondaniniF,MistrelloG,CarlucciA, TripodiS.Rosaceae-associatedexercise-inducedanaphylaxiswithpositive SPTandnegativeIgEreactivitytoPrup3.EurAnnAllergyClinImmunol 2011;43:122–4.
[23]MiceliSopoS,MonacoS,GiorgioV,CalvaniM,MistrelloG,Onesimo R.Food-dependentexercise-inducedanaphylaxis(FDEIA)bynectarine inapaediatricpatientwithweaklypositivenectarineprick-by-prickand negativespecificIgEtoPrup3.AllergolImmunopathol2013;41:201–3.
[24]HottaA,InomataN,TanegasimaT,OdaK,InoueY,AiharaM.Case offood-dependentexercise-inducedanaphylaxisduetopeachwithPru p7sensitization.JDermatol2016;43:222–3.
[25]InomataN,MiyakawaM,AiharaM.Eyelidedemaasapredictivefactor forsensitizationtoPrup7inpeachallergy.JDermatology2016;43:900–5.