UNIVERSITE MOHAMMED V
FACULTE DE MEDECINE ET DE PHARMACIE -RABAT-
ANNEE: 2008 THESE N°: 24
A
A
l
l
l
l
e
e
r
r
g
g
i
i
e
e
a
a
u
u
x
x
a
a
c
c
a
a
r
r
i
i
e
e
n
n
s
s
d
d
e
e
l
l
a
a
p
p
o
o
u
u
s
s
s
s
i
i
e
e
r
r
e
e
D
D
o
o
m
m
e
e
s
s
t
t
i
i
q
q
u
u
e
e
THESE
Présentée et soutenue publiquement le :………..
PAR
Mlle. Fatima WAKIT
Née le 24 Octobre 1982 à Casablanca
Pour l'Obtention du Doctorat en
Pharmacie
MOTS CLES Allergie – Acariens – House dust mite – Prévention de l'allergie –
Les anti-allergiques.
JURY
Mr. M. ZOUHDI PRESIDENT Professeur de Microbiologie Mr. Y. CHERRAH RAPPORTEUR Professeur de Pharmacologie Mr. A. GAOUZI Professeur de Pédiatrie Mme. K. ALAOUI Professeur de PharmacologieA Mes très chers parents
Aucune dédicace ne saurait traduire mon amour, mon respect
et mon affection
Sans vos précieux conseils, vos prières, votre générosité
et dévouement, je n’aurais pu surmonter le stress
de ces longues années d’études.
Veuillez trouvez dans ce travail, ma gratitude et ma
sincère reconnaissance pour vos sacrifices sans limites
que vous avez consenti pour mon éducation,
votre compréhension, votre affection débordante
dont vous m’avez toujours entouré.
Puisse Dieu vous procurer bonheur, santé, longue vie
et vous garder à mes cotés le plus longtemps
A mes sœurs :
Fatna et Aziza
L’entente qui nous unit m’a toujours rendu fière de vous
que ce travail soit le témoignage de la profonde
affection que j’ai pour vous et dieu vous procure tout le
bonheur et la réussite dans votre vie familiale et
professionnelle.
A mes frères :
Fouad et El Mehdi
Vous êtes des frères dont je suis fière à vous deux,
je dédie cette thèse en témoignage de mon
amour profond.
A mes oncles et tantes
A mes cousins et cousines
Je ne trouve pas les lettres pour vous exprimer tout ce
que je ressens envers vous. Vous avez toujours
été à mes cotés, votre amour et votre confiance en moi
m’ont poussé vers l’avant et j’espère être
à la hauteur de vos espérances.
Que dieu le tout puissant vous protège et
vous procure longue vie.
A toutes mes amies et amis
En souvenir d’agréables moments passées ensemble, et
en témoignage de notre amitié.Je vous exprime par ce travail
toute mon affection et j’espère que notre amitié
restera intacte et durera pour toujours.
A toute ma famille.
A tous ceux qui me sont trop chers et que j'ai
omis de citer.
A tous ceux qui ont contribué, de près ou de
loin à l'élaboration de ce travail.
A NOTRE MAITRE ET RAPPORTEUR
DE THESE Monsieur le Professeur Y. CHERRAH
Professeur de pharmacologie
Je vous remercie de m’avoir si bien aidé à mener à bien
ce travail, vous n’avez jamais lésiné ni
sur votre temps ni sur votre savoir tout le long de ce
travail.
Qu’il me soit permis, Monsieur, de vous témoigner ma
Plus haute considération et mes sentiments
les plus distingués.
Puissiez-vous trouver dans ce travail l’expression
de ma sincère gratitude et mon plus
A NOTRE MAITRE ET JUGE DE THESE
Monsieur Le Professeur A. GAOUZI
Professeur de pédiatrie
Nous mesurons l’honneur que vous nos faites en acceptant
de siéger parmi notre jury de thèse.
Qu’il me soit permis, Monsieur, de vous exprimer ma
profonde gratitude et mes sincères
remerciements.
Merci pour votre sympathie, votre gentillesse
et votre disponibilité.
A NOTRE MAITRE ET PRESIDENT DE THESE
Monsieur Le Professeur M. ZOUHDI
Professeur de microbiologie
Je vous remercie, Monsieur, de m’avoir fait l’honneur
d’accepter de présider le jury de ma de thèse.
Qu’il me soit permis, Monsieur, de vous exprimer
toute ma reconnaissance, mon respect
et mon estime.
Veuillez croire, Monsieur, à l’expression de mes
sentiments les plus distingués.
A NOTRE MAITRE ET JUGE DE THESE
Madame Le Professeur K.ALAOUI
Professeur de pharmacologie
Je vous remercie, Madame, de m’avoir fait l’honneur
d’accepter de faire partie de mon jury
de thèse.
Qu’il me soit permis, Madame, de vous exprimer toute
ma reconnaissance, mon respect
et mon estime.
Veuillez croire, Madame, à l’expression de mes
sentiments les plus distingués.
Liste des abréviations
AD : Acariens domestiques
AMPc : Adénosine Monophosphate Cyclique APD : Acariens de la poussière domestique APM : Acariens de la poussière de maison ATP : Adénosine Triphosphate
Bt : Blomia tropicalis
CMH : Complexe majeur d’histocompatibilité CPA : Cellules présentatrices d’antigène Cys : Cystéinyl-leucotriène DA : La dermatite atopique Dpt : Dermatophagoïdes pteronyssinus Df : Dermatophagoïdes farinae HRB : Hyperréactivité bronchique Ig : Immunoglobuline IL : Interleukine
ITSC : Immunothérapie par voie sous-cutanée ITSL : Immunothérapie par voie sublinguale LT : Leucotriène
PM : Poussière de maison PPM : Parties par million
RAST : Radio allergo sorbent test
Th2 : Lymphocytes T auxiliaires de type 2 VEMS : Volume expiratoire maximum par seconde
Liste des tableaux
Tableau 1 : nouvelle classification OMS de la rhinite allergique Tableau 2 : quelques acaricides commercialisés aux Maroc
Tableau3: Antihistaminiques H1 non anticholinergiques et sans effet sédatif Tableau 4 : Les Antihistaminiques H1 anticholinergiques à effets sédatifs non prolongés
Tableau 5: Les Antihistaminiques H1 anticholinergiques sans effets sédatifs Tableau 6: quelques stabilisateurs de mastocytes commercialisés au Maroc Tableau 7: formes orales des corticoïdes
Tableau 8 : corticoïdes injectables d’action rapide et brève Tableau 9: corticoïdes injectables à action prolongée
Tableau 10 : les principaux Dermocorticoїdes disponibles au Maroc Tableau 11: corticoïdes non associés en rhinologie
Tableau 12 : corticothérapie par inhalation
Tableau13 : quelques spécialités pharmaceutiques alpha-sympathomimétiques utilisées au Maroc
Tableau 14: les formes inhalées des β2mimétiques de courte durée d’action Tableau15 : Les formes injectables des β2mimétiques de courte durée d’action Tableau16 : les formes inhalées des β2mimétiques de longue durée d’action Tableau 17: quelques spécialités de la Théophylline commercialisées au Maroc Tableau 18 : Quelques spécialités pharmaceutiques de vaccin pour ITSC Tableau 19 : Quelques spécialités pharmaceutiques de vaccin pour ITSL
Liste des figures
Figure n°1: Photo de Dermatophagoïdes pteronyssinus
Figure n° 2 : Dessin de Dermatophagoïdes pteronyssinus
Figure n°3 : Les déjections des acariens
Figure n°4 : Aspect, en microscope électronique à balayage, d’un acarien de la poussière de maison, Dermatophagoïdes
pteronyssinus et ses déjections.
Figure n° 5 : Schéma général de la réaction d’hypersensibilité de type I
Figure n°6 : Prick-test donnant une réaction intense et isolée à
Dermatophagoïdes pteronyssinus, encadrée de tests
Négatifs.
Figure n°7 : Eczéma induit par un test cutané, Réaction cutanée érythémateuse et eczémateuse 48 heures après l’application de 5 µg de d’antigène purifié d’acariens de PM. Der p 1 sur la peau d’un patient avec dermatite atopique.
Table de matière
Introduction générale
……….1Partie I : allergie et hypersensibilité
……….
4I-Définitions
………...
51. Allergie ………...5
2. Les allergènes………..7
II-Les réactions d’hypersensibilité
………
81. Hypersensibilité type I ………...8
2. Hypersensibilité type II………...9
3. Hypersensibilité type III………..9
4. Hypersensibilité type IV……….9
Partie II : allergie aux acariens de la poussière domestique……..
10I-Les acariens
………...
111. Historique……….11
2. Classification et caractères généraux ……….12
3. Morphologie………...15 3.1.Leprosoma……….15 3.2.L’opisthoma………...16 4. Biologie………..17 4.1. La nutrition………...17 4.2. La reproduction……….17 5. Ecologie de Dermatophagoïdes………...18 5.1. Température et humidité………...18
5.2. Altitude………... 19
6. Le pouvoir pathogène ………..20
6.1.Sources des allergènes d’acariens………..20
6.2. Les différents types d’allergènes………20
6.2.1.Les allergènes du groupe 1 ……….……….21
6.2.2. Les allergènes du groupe 2 ……….22
6.2.3 Les autres groupes d’allergènes………..23
7. Localisation des acariens et leurs allergènes………...24
8. Aérobiologie………...24
II-Allergie aux acariens………..25
1. Etiologie……….25
2. Physiopathologie de la réaction d’hypersensibilité IgE- Dépendante………...26
2.1. Présentation des allergènes………26
2.2. Interaction lymphocytes Th2-lymphocytes B………...27
2.3. Les immunoglobulines E ou IgE………..28
2.4. Phase de sensibilisation……….28
2.5. Phase effectrice de la réaction allergique………..28
3. Facteurs de risque contribuant au développement de l’allergie aux acariens………32
3.1. La prédisposition génétique……….32
3.2.Exposition aux allergènes d’acariens………...34
3.2.1. Relation entre l’exposition aux allergènes et la sensibilisatio…...34
3.2.2.Relation entre exposition allergénique et apparition de la maladie Allergique………..35
3.3. Rôle de la pollution atmosphérique………..38
3.4. Tabagisme passif ………..40
3.5. Rôle des infections dans le développement de l’allergie………...40
3.6. Hypothèse hygiéniste……….41
4. Allergie croisée et réactivité croisée………42
4.1. Définition………...42
4.2. Allergie croisée à l’intérieur de la famille pyroglyphidae……...43
4.3. Allergie croisée entre les Pyroglyphidae et les acariens de stockage ………...44
4.4. Allergie croisée entre les acariens et les autres invertébrés ………….45
Partie III : symptomes cliniques et diagnostic
……….
47I-La Dermatite atopique
………..
491. Définition………....49 2. Épidémiologie……….49 3. Aspects cliniques………50 II-Rhinite allergique………...52 1. Définition………....52 2. Classification………..52 3. Épidémiologie………53 4. Aspects cliniques………....54 III-L’asthme……….55 1. Définition………...55 2. Épidémiologie………55
3. Les facteurs de risque……….56
IV-Diagnostic de l’allergie……….60
1. Interrogatoire……….60
2. Tests cutanés……….61
3. Tests biologiques………....65
3.1. Dosage des IgE sériques totales………65
3.2. Dosage des IgE sériques spécifiques……….65
4. Tests de provocation spécifiques………66
Partie IV : mesures préventives et traitement de l’allergie aux
acariens………...
68I-Prévention de l’allergie aux acariens………...69
1. La prévention primaire………...69
2. Prévention secondaire……….70
3. Prévention tertiaire………70
4. Mesures d’évictions des acariens………...71
4.1. Influence de l’environnement intérieur et de caractéristiques de l’habitat sur la charge allergénique………71
4.1.1. Influence de la ventilation, humidité, et la climatisation………..72
4.1.2. Influence de l’ameublement………73
4.1.3. Autres éléments………...73
4.2.éviction des acariens………74
4.2.1. Mesures physiques………..74
4.2.2. Mesures chimiques : les acaricides……….79
4.4. Faisabilité………82
II-Traitement médicamenteux anti-allergique
………
831. Les antihistaminiques H1………...83
1.2. Mécanisme d’action des antihistaminiques H1 ………..83
1.3. Effets………...84
1.4. Indications thérapeutiques………..85
1.5. Effets indésirables, précautions d’emploi, contre indications...86
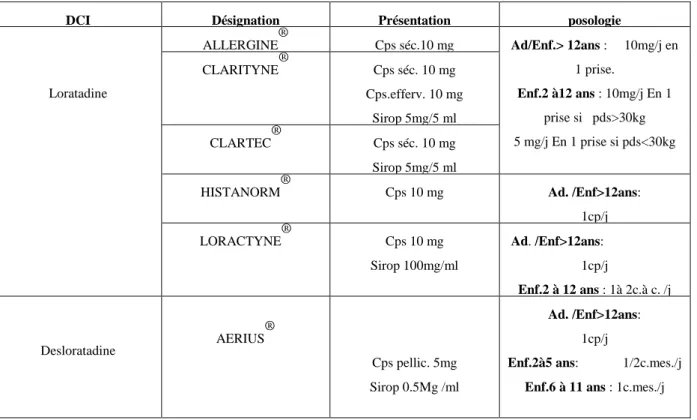
1.6. Les principaux antihistaminiques utilisées au Maroc pour leur effet anti-allergique……….87
2. Stabilisateurs de membranes : les antidégranulants Mastocytaires……….89
2.1. Cromoglycate……….89
2.2. Nédocromil……….90
2.3. Kétotifène………...90
3. Les corticostéroïdes………...92
3.1. Mécanisme d’action des corticostéroïdes ………..92
3.2. Propriétés et effets………..93
3.3. Effets secondaires de la corticothérapie……….93
3.4. Contre-indications de la corticothérapie ………94
3.5. Les Corticoïdes inhalés, dermocorticoïdes, Corticothérapie Intra-nasal ………...95
3.6. Les principales spécialités pharmaceutiques………..97
4. Les autres traitements médicamenteux anti-allergiques………..100
4.1. Les alpha-sympathomimétiques………100
4.2. Les bronchodilatateurs………...101
4.2.2. Les anticholinergiques……….102 4.2.3. La théophylline………103 4.2.4. Les antileucotriènes………...105
III-Traitement de l’allergie : immunothérapie spécifique
……...
107 1. Mécanisme de la désensibilisation………..108 2. Indications………110 3. Les Contre indications………..111 4. Mise en œuvre………..111 5. Sécurité de l’immunothérapie spécifique……….113 6. Quelques spécialités pharmaceutiques de vaccin pour ITS……….114IV-Intérêt des cures climatiques
………..
115Conclusion
………..
116Résumé
………..119L’allergie constitue actuellement un problème de santé publique, en effet sa prévalence a considérablement augmenté, elle occupe désormais le quatrième rang par ordre de fréquence des maladies répertoriées par l’OMS.
Toutes les tranches d’âge sont concernées avec des conséquences socio professionnelles par fois importantes en particulier pour l’enfant et l’adulte jeune.
L’apparition d’une maladie allergique exige une sensibilisation préalable de l’organisme.
Le confinement des habitations et l’augmentation du temps passé à l’intérieur de celles-ci ont fait que les allergènes de l’habitat sont ceux le plus souvent associés au développement des allergies.
Les acariens sont des arachnides, dont trois familles sont impliquées dans les phénomènes d’allergies, dans la famille des pyroglyphidae on trouve les acariens de la poussière domestique, dont les plus répandus sont
Dermatophagoïdes pteronyssinus et Dermatophagoïdes farinae.
Les débris d’acariens morts et leurs déjections sont responsables de la majorité des rhinites et des asthmes pérennes. Ils jouent aussi un rôle important au cours de l’eczéma atopique, comme le prouvent la positivité des tests cutanés, celles des dosages d’IgE sériques spécifiques et l’amélioration des lésions cutanées après éviction des acariens, dans ce cas, elle précède généralement l’apparition de l’asthme ou de la rhinite.
Un enfant atteint de la dermatite atopique a trois à quatre fois plus de possibilités de développer un asthme dans les années à venir. [1]
Il est donc important de diagnostiquer l’origine allergique de ces pathologies suffisamment tôt afin de mettre en place un traitement adapté et de réaliser une éviction des allergènes.
Objectif du travail
Dans ce travail nous proposons de faire une revue de la littérature sur ce type d’allergie :
Les principales caractéristiques des acariens, et de leurs allergènes ;
Les facteurs de risque de déclenchement et d’aggravation de l’allergie aux acariens ;
Les allergies qui peuvent être associées à celle-ci ;
Les éléments du diagnostic et surtout ceux de l’interrogatoire permettant de confirmer l’atteinte par ce type d’allergie ;
les mesures de prévention comprenant aussi bien l’éviction des acariens et de leurs allergènes ;
Ces mesures ont fait l’objet d’études récentes dont les conclusions méritent d’être soulignées ;
Traitement médicamenteux des symptômes ;
La désensibilisation spécifique comme traitement étiologique.
Les affection appelées « allergiques » ont été connues depuis les temps les plus éloignés tandis que la pathogénie n’a pu être dégagée qu’au début du XXème siècle, lorsque l’expérimentation a défini le concept d’hypersensibilité.
Ainsi, la signification et l’implication de la notion d’allergie se sont considérablement élargies sur le plan biologique et clinique.
Ce qui n’était qu’une notion, constitue maintenant une véritable discipline, dont l’importance se traduit par d’innombrables publications.
Dans le domaine clinique, l’allergologie est devenue une discipline autonome dont l’activité croissante contribue chaque jour à élargir et compléter nos connaissances. Elle intéresse essentiellement le spécialiste, mais aussi le praticien, toujours confronté à des problèmes complexes et, par le fait que les maladies allergiques sont très répandues, ce qui implique une grande nécessité d’information actualisée. [2]
I-Définitions
3. Allergie :
le terme allergie a été utilisé pour la première fois en 1906 par le médecin Autrichien Clémens von pirquet, afin de distinguer les réactions utiles des réactions nocives au sein des différentes réponses immunes. Aujourd’hui, le terme d’allergie est utilisé pour désigner une réaction immunitaire spécifique mais exagérée et nocive contre les substances exogènes (allergènes).
Les maladies auto-immunes se démarquent des allergies par le faite que la réponse immune nocive est dirigée contre des antigènes du corps propre. La réaction spécifique et acquise du système immunitaire, est d’une importance capitale pour la réaction allergique : lors d’un contact avec un allergène
potentiel, l’organisme se sensibilise, mais il n’y a pas encore de symptômes cliniques. Il y a formation de lymphocytes et d’anticorps spécifiques contre l’allergène en question. C’est seulement lors d’une ré-exposition à cet allergène que survient une réaction allergique. [3]
Il y a souvent confusion entre allergie, pseudo allergie, intolérance et toxicité.
Pseudo-allergie : les pseudo-allergies ont souvent un tableau clinique identique à celui des allergies. Cependant le mécanisme pathogénique, qui souvent n’est pas connu, est différent.
Les pseudo-allergies jouent surtout un rôle important dans les réactions après la prise de médicaments et d’aliments. Il s’agit d’une réaction d’intolérance ressemblant à des allergies, cependant, sans pouvoir prouver une sensibilisation spécifique. L’importance de la réaction est dose-dépendante et il est possible qu’elle se déclare déjà lors d’un premier contact avec une substance exogène.
Idiosyncrasie, intolérance : l’idiosyncrasie est une réaction d’hypersensibilité innée et non immunologique dirigée contre une substance exogène. Un déficit enzymatique en est souvent la cause. Les symptômes sont dose-dépendants et surviennent lors du premier contact avec la substance en question.
Toxicité : le terme toxicité est utilisé pour décrire les effets nocifs d’une substance chimique ou d’un facteur physique pour un organisme. Elle est dose dépendante.
Un exemple de réaction cutanée ressemblant à une allergie est la dermatite aux graminées. La dermatite non allergique est provoquée dans ce cas, sous l’influence de la lumière, par une substance contenue dans la plante. [3]
4. Les allergènes
Selon les réactions immunitaires induites, on dénomme, antigènes ou allergènes les substances capables de provoquer une réponse, traduite par l’apparition d’éléments spécifiques appelés anticorps.
La propriété antigénique est liée à la nature physico-chimique de la molécule et de certains de ses groupements fonctionnels. Elle appartient à toute espèce moléculaire, d’origine biologique ou synthétique, qui, après avoir pénétré dans le milieu intérieur de l’organisme, ou même appartenant à cet organisme (auto-antigène), est reconnue par le système immunitaire. Dans ce cas, l’antigène peut réagir spécifiquement avec les structures de reconnaissance du système immunitaire : molécules d’anticorps et récepteurs des lymphocytes T.
L’antigène est définit de façon fonctionnelle comme immunogène s’il induit chez l’hôte une réaction immunitaire et comme tolérogène si, au contraire, il donne lieu à un phénomène de tolérance immunitaire.
Les études immunologiques ont montré que la spécificité antigénique est souvent liée à une petite fraction de la molécule. [2]
II-Les réactions d’hypersensibilité
[4]
Les réponses immunitaires excessives aux antigènes étrangers peuvent porter atteintes aux tissus. Ces réactions sont appelées réactions d’hypersensibilité.
C’est en 1964 que Gell et Coombs proposèrent une classification des phénomènes allergiques. Cette classification a été établie en fonction de la chronologie des réactions et de leurs mécanismes physiologiques.
On distingue quatre grands types, les types I à III sont liés aux anticorps alors que la réaction de type IV est cellulaire.
8. Hypersensibilité type I
C’est le type le plus fréquent et le plus important du point de vue clinique. Il correspond à l’hypersensibilité immédiate ou hypersensibilité anaphylactique ou atopique avec anticorps circulants. Ces anticorps ou réagines sont également appelés anticorps homocytotropiques. Ce sont des immunoglobulines de type IgE capables de se fixer sur les mastocytes tissulaires et sur les basophiles du sang circulant. Les mastocytes sont riches en granules contenant l’histamine et les autres médiateurs chimiques de l’allergie.
La caractéristique des réactions de l’allergie de type I est que les symptômes apparaissent très rapidement après l’exposition à un allergène, en règle générale en 10 à 20 mn, mais parfois moins, d’où le nom d’hypersensibilité immédiate. Cependant quelques manifestations de l’allergie de type I se prolongent parfois bien au-delà de ce délai. L’asthme allergique extrinsèque, les rhinites et les conjonctivites, allergiques, l’œdème de Quincke, le choc anaphylactique… se sont des exemples d’allergie de type I.
9. Hypersensibilité type II
Dans ces réactions immunes, les anticorps sont libres dans le sérum alors que l’antigène est fixé à la surface de certaines cellules ou c’est un composant de la membrane cellulaire elle-même. Quand les anticorps réagissent avec l’antigène, il se produit une activation du complément qui aboutit à la détérioration de la cellule et même sa lyse. Les maladies relevant de ce mécanisme sont essentiellement les accidents de transfusion incompatible et les cytopénies médicamenteuses.
10.
Hypersensibilité type III
Ces réactions sont dues à des anticorps circulants, les précipitines qui appartiennent à la classe des IgG. Le système complémentaire est activé quand ces anticorps réagissent avec des antigènes pour produire un complexe antigène-anticorps. Cette activation du complément entraîne une accumulation de polynucléaires et une libération d’histamine et aboutit à des lésions tissulaires analogues à celles du phénomène d’Arthus.
11.
Hypersensibilité type IV
Elle se différencie des trois autres en ce sens qu’elle n’est pas produite par des anticorps mais par des cellules imumuno-compétentes, les lymphocytes.
Elle se caractérise aussi par le délai de 24 à 72 heures nécessaire à l’apparition des manifestations après la réintroduction de l’antigène : d’où le nom d’hypersensibilité retardée à médiation cellulaire.
I-Les acariens
L’allergène poussière de maison n’est plus un allergène en tant que tel et l’allergie à la poussière de maison correspond en fait à l’allergie à l’un de ses constituants : parmi ceux-ci, les acariens jouent un rôle prépondérant.
Les acariens, principaux allergènes de la PM, sont également retrouvés dans beaucoup d’autres lieux. [5]
1. Historique
Dès 1921 KERN, COOKE en 1922 et STORM VAN LEEWEN en 1924 attribuaient un rôle allergénique important à la poussière de maison qui était bientôt reconnue comme l’une des causes principales de l’asthme bronchique et de la rhinite apériodique.
Pendant de nombreuses années les chercheurs ont étudié la composition de la PM : celle-ci est très complexe et comprend des substances très diverses : d’origine minérale (sels divers, particules calcaires, siliceuses, argileuses, charbon, boue desséchée, matériaux de construction divers…), d’origine végétale (fragments de plantes, fibres de coton, pollens, moisissures…), d’origine animale (poils ou squames, plumes, débris d’insectes, acariens, bactéries…).
Antérieurement à ces travaux DEKKER, en étudiant, en 1928 la composition chimique de la poussière de maison, avait remarqué en Allemagne l’importance des acariens inhalés par les asthmatiques. Cependant, il n’identifie que certaines espèces : Glyciphagus domesticus, Tyroglyphus siro, Aleurobius
En 1962 le problème connaît un regain d’intérêt grâce aux travaux de VOORHORST qui suspecte comme responsable de l’allergénicité de la poussière domestique, un organisme vivant, variant quantitativement selon le lieu et la saison des prélèvements. Les recensements méthodiques effectués par SPIEKSMA et SPIEKSMA-BOOZEMAN mettent en évidence de façon quasi constante la présence d’acariens du genre Dermatophagoïdes, dans les poussières des maisons de Hollande.
En 1966, à la demande des auteurs Hollandais, FAIN identifie le
Dermatophagoïdes responsable, comme étant Dermatophagoïdes pteronyssinus.
Ces acariens, improprement dénommés « mites » par les auteurs anglo-saxons, sont retrouvés ultérieurement aussi bien en Belgique, en Angleterre, en France, qu’au Japon, aux Etats-Unis et en Australie. [6]
2. Classification et caractères généraux
Les acariens font partie de l’embranchement des Arthropodes, et du sous embranchement des chélicérates. Un des plus allergisants du règne animal qui comporte quatre classes : les Arachnides, les Crustacés, les Hexapodes et les Insectes.
L’ordre des Acariens, figure dans la classe des Arachnides. [6]
Les Arthropodes sont munis d’une paire d’appendices prébuccaux, le corps est divisé en deux régions ou tagmes :
Le céphalothorax ou prosoma qui résulte de la fusion de l’acron et de six premiers segments du corps ;
Les Arachnides sont des chélicérates terrestres à respiration aérienne qui comportent, outre une paire de chélicères, quatre paires de pattes et une paire de pédipalpes, organes servant à la mastication.
L’ordre des Acariens se caractérise par un abdomen non segmenté. De plus, le céphalothorax et l’abdomen sont fusionnés ce qui donne au corps un aspect globuleux. [7]
Cet ordre se divise en diverses familles, à la famille des Pyroglyphides appartient le genre Dermatophagoïdes. Huit espèces issues de cette famille sont habituellement rencontrées dans la poussière d’habitation : Dermatophagoïdes
pteronyssinus, Dermatophagoïdes farinae, Euroglyphus maynei, Dermatophagoïdes evansi, Euroglyphus longior, Sturnophagoides brasiliensis et Malayoglyphus intermedius. [6]
Les trois espèces les plus répandues dans la PM sont Dermatophagoïdes
pteronyssinus, Dermatophagoïdes farinae et Euroglyphus maynei.
Certaines espèces d’acariens dites acariens de stockage (Glyciphagus
domesticus, tyrophagus putrecentia, acarus siro) sont présentes au sein des
céréales stockées et de la farine. Ces espèces ne sont pas retrouvées dans la literie, mais elles ont une importance allergénique certaine dans la poussière des maisons très humides, dans l’habitat rural et agricole, ainsi qu’en milieu tropical où la croissance des moisissures favorise leur développement. [5]
3. Morphologie
Les acariens du genre Dermatophagoïdes ont une taille comprise entre 170 et 500μm. Les femelles ont, en général, une taille plus importante que les mâles :
-la femelle mesure 420 microns en longueur sur 320 microns en largeur, -le mâle mesure 420 microns en longueur sur 245 microns en largeur.
Leur corps est blanc et globuleux avec un prosoma et un opisthosoma fusionnés, le terme acarien vient d’ailleurs du grec akari qui signifie « qui n’est pas divisé ». Toute segmentation apparente a disparu chez les acariens et la distinction prosoma-opisthosoma n’est plus possible dorsalement. Seule l’observation ventrale permet de différencier les deux tagmes.
L’aspect de la cuticule varie selon les espèces : elle peut être lisse, striée ou couverte de très fines spicules. Le tégument présente une ornementation variée : ponctuation, striation, réticulation.
Le corps et les appendices sont recouverts de poils dont la disposition permet de différencier les genres et les espèces, leur nombre et leur nature permettant de connaître le degré de développement de l’acarien. [9] [10]
3.1. Le prosoma [7] [9]
Le prosoma est divisé en deux régions : le gnathosoma et le podosoma. Le gnathosoma : il constitue la région antérieure et comporte le rostre,
prolongement de la carapace dorsale. Ce rostre mobile, porte les chélicères transformées en lames masticatrices, biarticulées et dorsales par rapport à la bouche ainsi que les pédipalpes, ventraux.
Le podosoma : il représente la partie postérieure du prosoma et porte les quatre paires de pattes articulées en six articles : coxa, trochanter, fémur, patella, tibia et tarse. Le coxa peut être mobile ou fixe et la forme du trochanter détermine l’orientation de la patte. Le fémur est un article fort commandant l’amplitude du mouvement de la patte. La patella, le tibia et le tarse assurent la souplesse de l’organe locomoteur et portent de nombreux poils et organes sensoriels.
3.2. L’opisthoma
Il est apode mais il porte l’anus au niveau du dernier segment. L’orifice génital situé sur la plaque génitale, au niveau du deuxième segment. Les stigmates respiratoires sont absents chez Dermatophagoïdes qui fait partie des astigmates. Il respire à travers le tégument de sa carapace ou éventuellement grâce à son canal intestinal. [7] [9]
4. Biologie
La nutrition
Les Dermatophagoïdes sont phanérophages, c’est-à-dire qu’ils se nourrissent des squames humaines, animales et également d’autres débris kératinisés (ongles, poils, plumes). Dermatophagoïdes est d’ailleurs un nom latin signifiant « mangeur de peau ».
Leurs besoins qualitatifs et quantitatifs en nourriture sont modestes. Deux cent cinquante milligrammes de squames humaines suffisent à nourrir plusieurs milliers d’acariens pendent un trimestre, or chez l’Homme la perte quotidienne de squames est de 70 à 140 mg. [3] [12]
Les chélicères et les pédipalpes dilacèrent les aliments. Les acariens ne peuvent absorber que de la nourriture liquide. Ainsi, des régurgitations du tube digestif et des sécrétions de glandes spéciales provoquent une liquéfaction et une prédigestion de l’aliment.
Les chélicères permettent la préhension des aliments et, grâce à leur articulation, les introduisent dans la cavité buccale d’où ils gagnent le pharynx, principal organe d’aspiration des aliments. [9]
La reproduction
Les acariens vivent à l’état adulte huit à treize semaines, ils s’accouplent une à deux fois dans leur vie. La femelle pond vingt à cinquante œufs, l’œuf se transforme en larve puis en protonymphe et en nymphe.
Cette transformation complète nécessite 25 jours. Lorsque les conditions de vie sont défavorables, le stade de protonymphe peut être une phase quiescente.
A l’éclosion, la larve ne possède que trois paires de pattes ambulatoires, elle est dite « hexapode » et son organisation rappelle celle de l’adulte. Elle mène une vie active, différente de celle de l’adulte puis s’immobilise et passe par une phase pulpaire où elle subit des changements importants, elle revient à l’état d’une masse embryonnaire complètement dédifférenciée. Les organes de la larve hexapode se reforment et la quatrième paire de pattes thoraciques, disparue pendant l’embryogenèse initiale, apparaît. [9]
5. Ecologie de Dermatophagoïdes
Le nombre d’acariens dans une maison dépend de la température, du degré d’humidité intérieure et du renouvellement de l’air. Ces conditions vont influencer la reproduction et le développement.
Présents essentiellement dans la literie, ils vivent aussi au niveau des tentures murales, des coussins, des tapis, des moquettes…
5.1. Température et humidité
Un développement optimal au laboratoire est obtenu lorsque la température est comprise entre 26,6 et 32,2°C et l’humidité relative ambiante est de 70 à 80 %.
Une température de 20 à 25 °C dans une habitation représente les conditions idéales de vie pour ces animaux.
Par contre, les taux de reproduction et de développement peuvent différer d’une partie à l’autre de l’habitat, en fonction des variations de température. En effet, il semble que les populations d’acariens se développent plus lentement dans les tapis sur les sols froids que les matelas et les sofas. [13]
L’humidité est un facteur crucial dans le développement des Pyroglyphides. En effet, ils sont composés de 70 à 75% d’eau et ne peuvent qu’absorber l’eau extraite de l’humidité ambiante puisqu’ils sont dépourvus de tout autre moyen d’ingestion hydrique. Cette absorption se fait grâce à la glande supra-coxale située à la base des premières paires de pattes. Celle-ci sécrète une substance hyperosmotique de chlorure de sodium et de potassium qui permet l’extraction de l’eau. [14]
5.2. Altitude
Dermatophagoïdes pteronyssinus et Dermatophagoïdes farinae sont
absents au dessus de 1600 à 1800 mètres d’altitude où les conditions d’hygrométrie et de température sont défavorables à leur croissance.
Une étude menée par Vervloet et coll. en 1982 sur une période de 1 an où un comptage des acariens au niveau du matelas a été effectué dans des habitations de la région de Briançon à différentes altitudes et à différentes saisons et dont les résultats sont sans équivoque : 80% des échantillons contenaient des acariens en plaine contre 40% entre 900 et 1100mètres, 14% entre 1200 et 1350mètres, 6% entre 1400 et 1600 et 0% au delà. La quantité d’acariens diminuait également dans les échantillons positifs au fur et à mesure que l’on s’élevait en altitude. Autre élément intéressant de cette étude : les acariens de la plaine ne sont pas les mêmes que ceux de la montagne :
Dermatophagoïdes pteronyssinus et Dermatophagoïdes farinae prédominent en
plaine et Euroglyphus maynei en altitude. [15]
La raréfaction des acariens en altitude est liée à une diminution de l’humidité relative et de la température car dans les régions d’altitude où
l’humidité est forte, comme au Guatemala ou en Colombie, on trouve une quantité importante d’acariens. [13]
6. Le pouvoir pathogène
Les sources principales de nombreux allergènes ont été clairement identifiées : il s’agit du corps des acariens et leurs déjections.
6.1. Sources des allergènes d’acariens
Dpt et Df produisent une cinquantaine d’antigènes, mais seule une dizaine d’entre eux sont allergisants.
Les allergènes des déjections sont des enzymes provenant du tractus digestif. D’autres allergènes pourraient provenir de la salive ou des sécrétions de la glande supra-coxale.
Les particules fécales s’accumulent dans la poussière domestique, leur taille est comprise entre 10 et 35 μm et elles sont entourées d’une membrane chitineuse perméable à l’eau ce qui permet une élution rapide des allergènes. [14] 6.2. Les différents types d’allergènes
Les allergènes respiratoires dont les allergènes des acariens, dans la nomenclature actuelle, sont désignés par les trois premières lettres du genre, la première lettre de l’espèce et un nombre arabe représentant l’ordre de la découverte. Les allergènes homologues d’espèces voisines ont, en général, un chiffre identique. Le chiffre 1 sera toutefois toujours attribué à l’allergène majeur. Ainsi, les allergènes majeurs sont Der p 1 et Der p 2 pour
Dermatophagoïdes pteronyssinus et Der f 1 et Der f 2 pour dermatophagoïdes farinae.
Der p1 a d’ailleurs été le premier allergène purifié. Les allergènes du groupe 1 et du groupe 2 sont dits majeurs car ils ont une prévalence de sensibilisation comprise entre 70 et 90%. Ceci signifie que ces allergènes sont reconnus par plus de 80% des sujets allergiques aux acariens. [16]
6.2.1. Les allergènes du groupe 1
Les allergènes du groupe 1, Der p 1 et Der f 1, sont des glycoprotéines acides, thermolabiles, d’un poids moléculaire d’environ 25 kDa. Ils ont une activité cystéine protéase et présentent 80% d’homologie entre eux. D’autres allergènes du groupe 1, par exemple Eur m 1 issu d’Euroglyphus maynei, ont également 80% d’homologie avec les deux allergènes précédents.
Le Der p 1 est l’un des premiers allergènes clonés et séquencés, l’activité protéolytique de cet allergène a été mise en évidence dans les extraits de poussière et jouerait un rôle non négligeable dans l’inflammation des voies aériennes et l’hyperréactivité bronchique présentes dans l’asthme.
Der p 1 est retrouvé dans la pelote de défécation qui a presque la même taille qu’un grain de pollen et se disperse dans l’air ambiant pendant les activités domestiques mettant la poussière en suspension. Il y est présent à une concentration de 0,1 nanogramme par particule et 15% de la quantité de Der p 1 retrouvée dans l’environnement est produite en un jour. Après 15 minutes de la mise en suspension de la poussière, 10 à 20% de particules, les plus petites porteuses d’allergènes, sont toujours en suspension. [16] [17]
6.2.2. Les allergènes du groupe 2 [17]
Les allergènes du groupe 2, Der p 2 et Der f 2, sont des glycoprotéines basiques thermorésistantes de 14 kDa environ, leur fonction n’est toujours pas identifiée.
Actuellement, on sait seulement qu’ils sont similaires par leur séquence, leur taille et la distribution des résidus cystéine, à une famille de protéines épididymères. On retrouve 88% d’homologie entre ces deux allergènes.
Der p 2 a pu être mis en évidence au niveau des fèces mais également au niveau de l’œsophage et du tube digestif.
Ces allergènes ont un comportement aérien identique à celui du groupe 1.
Figure n° 4: l’aspect en microscope électronique à balayage, d’un acarien de la poussière de maison, Dermatophagoïdes pteronyssinus. [18]
les déjections fécales (en bas à droite), des grains de pollen biconcaves (en haut à droite) donnent l’échelle et montrent que ce sont les déjections fécales et non l’acarien lui-même qui peuvent être transportées par voie aérienne et atteindre les poumons. [18]
6.2.3. Les autres groupes d’allergènes
Les allergènes du groupe 3, Der p 3 et Der f 3, ont une activité sérine protéase et possèdent les mêmes sites catalytiques et de liaison que la trypsine. Ils présentent une homologie avec les trypsines des mammifères et des invertébrés ainsi qu’avec d’autres sérine protéases. Ces allergènes sont à rapprocher de ceux du groupe 6, Der p 6 et Der f 6, qui présentent une activité sérine protéase et ont une certaine homologie entre eux. De même, ils sont similaires aux chymotrypsines des mammifères et des invertébrés, Le groupe 4 représenté par Der p 4 a une activité amylase. Les allergènes tels que Der p 1, Der p 3, Der p 4 et Der p 6, sont des enzymes digestives qui peuvent améliorer l’accès des allergènes aux cellules présentatrices d’antigènes, en favorisant la pénétration trans-épithéliale bronchique. Cette même activité enzymatique pourrait faciliter la synthèse des IgE par les cellules B. [16] [17]
7. Localisation des acariens et leurs allergènes
[5] [13]La poussière du matelas est le principal réservoir d’acariens et de leurs allergènes. Il a été démontré que les concentrations d’allergènes du groupe 1 dans les sommiers capitonnés étaient en moyenne deux fois et demie plus élevées que dans les matelas. Les tapis et les moquettes constituent un réservoir important. La présence d’allergènes d’acariens est notée également dans la poussière de canapés, de chaises capitonnées, de fauteuils et de vêtements.
Les acariens ont été retrouvés dans le cuir chevelu d’enfants à une concentration de 800/g de poussière.
Dans l’air, les allergènes des acariens (groupe 1 et 2) sont portés par des particules de plus de 10μm et ne sont mesurables que lors d’activités ménagères mettant de la poussière en suspension. Une exposition aux allergènes des acariens a été mesurée dans les classes de maternelle, et les crèches en Suède, mais également dans certains transports publics (trains, avions), et dans des lieux comme les cinémas en Angleterre.
8. Aérobiologie
Le nombre des acariens dans divers écosystèmes (dont la poussière de maison) peut être déterminé au microscope, mais il est plus simple et plus précis de doser par méthode immunochimique la quantité d’allergènes présents. Les poussières contenant des acariens du genre Dermatophagoïdes, par exemple, sont riches en guanine (qui est le catabolite final du métabolisme azoté des acariens), présente dans les fèces des acariens, ces derniers contenant la plus grande part des allergènes, cette guanine peut être dosée simplement par méthode colorimétrique, dont les résultats sont donnés en quatre classes. [19]
II-Allergie aux acariens
L’allergie aux acariens représente l’une des allergies les plus courantes et les plus préoccupantes en raison de sa prévalence qui est très élevée, et sa symptomatologie, les acariens sont responsables de la majorité des rhinites, des conjonctivites et d’asthme celui-ci représente la manifestation la plus fréquente. La prévalence de la sensibilisation aux acariens dans la population générale est d’environ 30% pour quelques régions, la sensibilisation peut s’élever jusqu'à 43%, elle est plus rare dans les pays nordiques où la diminution de la température s’oppose au développement des acariens. [12]
Cette augmentation nette de la prévalence de sensibilisation aux acariens correspond à une augmentation du temps passé à l’intérieur des habitats. Le confinement des maisons et les systèmes de chauffage sont plus performants, donc l’intérieur des habitats est plus chaud et humide. Ce sont les conditions idéales pour la croissance des acariens. [20]
1. Etiologie
L’allergie dirigée contre les acariens fait partie des réactions excessives ou inappropriées de la réponse immunitaire. Ces réactions comme nous avons vue ont été appelées hypersensibilité et classées en quatre types, l’hypersensibilité responsable des phénomènes allergiques dus aux acariens appartient au type I.
Cette réalité a été démontré in vivo et in vitro, les tests cutanés aussi bien que les tests ventilatoires ont permis de mette en évidence des réactions de type immédiat. [6]
2. Physiopathologie de la réaction d’hypersensibilité IgE-
Dépendante
[21] [22] [23]Les réactions d’hypersensibilité immédiate ont deux caractéristiques essentielles : elles sont très rapides (hypersensibilité immédiate) et très sensibles, pouvant être déclenchées par de très petites quantités d’allergènes.
2.1. Présentation des allergènes
2.1.1. Cellules présentatrices
On range sous ce terme des cellules qui participent à la réponse immunitaire à côté des lymphocytes en leur présentant l’antigène. Ce sont essentiellement les cellules dendritiques et les lymphocytes B. la lignée monocytes-macrophages Présente également des antigènes aux lymphocytes T.
2.1.2. Lymphocytes Th2
Lorsqu’un allergène pénètre dans l’organisme d’un sujet allergique, les lymphocytes T spécifiques deviennent d’un type particulier, défini par le profil de cytokines produites. Les lymphocytes T spécifiques de l’allergène chez l’allergique sont appelés Th2, ils produisent schématiquement de l’interleukine (IL-4), de l’IL-13 et de l’IL-5, mais pas ou peu d’IL-2 et (IFN)γ.
Les cytokines sont des protéines qui ont pour fonction de permettre la communication entre cellules voisines, mais non confluentes. Elles sont sécrétées, et vont agir en se fixant sur leur récepteur à la surface de la cellule cible. L’IL-4 est, avec l’IL-13, la cytokine essentielle à la production d’IgE par les plasmocytes, et IL-5 est un facteur majeur d’activation des polynucléaires éosinophiles. L’IFNγ est spécialisé dans l’activation de la phagocytose et des
mécanismes de cytotoxicité. Ainsi les lymphocytes Th2 sont les initiateurs des cellules et des molécules effectrices de l’allergie.
L’activation des lymphocytes Th2 se fait alors en réponse à l’allergène, chez l’allergique. En effet, chez le non allergique, il existe également une réaction spécifique en réponse à un allergène ayant pénétré dans l’organisme, mais celle-ci est de type Th-1.
2.2. Interaction lymphocytes Th2-lymphocytes B
En produisant de l’IL-4, les lymphocytes Th-2 vont induire la production d’IgE en favorisant la commutation isotypique vers la biosynthèse des IgE. En effet, de façon spontanée, les lymphocytes B alors différenciés en plasmocytes produisent des IgM ou éventuellement des IgD. Sous l’action de certains facteurs, les gènes codant pour les chaînes d’immunoglobulines vont se ré-arranger pour pouvoir produire les autres isotypes d’immunoglobulines IgA, IgG et IgM. Ce phénomène est appelé commutation isotypique.
Pour qu’il se produise, il faut qu’une interaction entre les cellules T et les plasmocytes aient lieu, mettant en jeu à nouveau des co-récepteurs. En particulier, il est nécessaire que CD80 ou CD86, exprimés à la surface du plasmocyte, interagissent avec CD28 sur le lymphocyte T. parallèlement, un autre couple de co-récepteurs doit interagir : il s’agit du CD40, exprimé par le plasmocyte, et de son ligand CD40 sur la cellule T. si l’interaction entre ces deux couples des co-récepteurs est réalisée, la commutation est possible, et, si ces interactions se font en présence d’IL-4, cette commutation aboutit à la synthèse des IgE.
2.3. Les immunoglobulines E ou IgE
Les IgE, sont des glycoprotéines de 190 kDa de masse moléculaire, sont principalement produites au niveau des muqueuses ; chez le sujet normal, leur concentration sérique est de l’ordre de 100 ng/ml. Ces anticorps ne sont biologiquement actifs qu’après s’être fixés sur des cellules exprimant des récepteurs spécifiques de leur région Fc. Il existe deux principaux types de récepteurs pour l’IgE, appelés FcεRI et FcεRII, qui diffèrent par leur affinité, leur structure moléculaire, leur distribution cellulaire et leur fonction. Leur demi-vie plasmatique est de 2 ou 3 jours alors qu’elles persistent pendant plusieurs semaines après s’être fixées aux cellules porteuses de son récepteur.
2.4. Phase de sensibilisation
Passant cliniquement inaperçu, la phase de sensibilisation est mal connue. La sensibilisation IgE-dependante expérimentale chez l’animal est, en revanche, très codifiée. On sait qu’elle dépend de nombreux facteurs, dont les plus importants sont la nature de l’antigène, sa dose, sa voie et son rythme d’administration. Ces facteurs créent de la différenciation de clones de lymphocytes Th2 spécifiques de l’antigène, la production d’IgE et la différenciation de lymphocytes T mémoire qui réagissent rapidement lors d’une exposition ultérieure.
2.5. Phase effectrice de la réaction allergique
C’est la phase clinique de la réaction immuno-allergique de type I. C’est une réaction, qui comprend néanmoins une phase précoce et une phase retardée.
2.5.1. Phase précoce de l’hypersensibilité immédiate
La phase précoce correspond à la dégranulation des cellules exprimant FcεRI en grande quantité à leur surface. L’antigène en pénétrant dans un organisme sensibilisé va aller se fixer à la surface des mastocytes qui sont porteurs des IgE spécifiques fixées via le FcεRI. Les IgE étant, comme toutes les immunoglobulines, porteuses chacune deux sites de reconnaissance de l’antigène, les différentes molécules d’antigènes vont co-agréger les FcεRI entre eux. C’est cette agrégation qui va entraîner une cascade d’événements intracellelaires qui vont mener à la coalescence des granules et de la membrane plasmique et libération des médiateurs qu’ils contiennent.
Ces granules contiennent les médiateurs à l’origine des symptômes immédiats de la réaction allergique, et des cytokines.
L’histamine
Le chef de file de ces médiateurs essentiels de la phase effectrice. En se fixant sur ses récepteurs H1, l’histamine entraîne une vasodilatation, un oedème,
une augmentation des sécrétions muqueuses. Lors d’un test de provocation nasal, l’histamine reproduit tous les signes de l’allergie immédiate : prurit nasal, rhinorrhée, éternuements, puis obstruction nasale.
Avec l’histamine sont libérés d’autres médiateurs dont les actions sont proches : sérotonines, bradykinine…
Par ailleurs, les granules contiennent des médiateurs lipidiques issus du métabolisme de l’acide arachidonique, qui sont les prostaglandines et les leucotriènes. Initialement désignés comme la « slow reactive substance of anaphilaxis».
Les leucotriènes agissent de façon retardée par rapport à l’histamine, mais avec des effets plus puissants, ils favorisent à leur tour l’oedème, les sécrétions, et ainsi l’obstruction et la rhinorrhée.
Enfin, les granules des mastocytes libèrent des cytokines, permettant une accélération des phénomènes inflammatoires de la phase tardive. Il s’agit notamment de l’IL-4 et du TNF-α, mais aussi de l’IL-5 et de cytokines chimiotactiques (chimiokines), notamment pour les éosinophiles et les lymphocytes.
a. Phase tardive de l’hypersensibilité immédiate
Chez la plupart des patients, la stimulation allergénique spécifique entraîne quelques heures après la réaction précoce, une réaction tardive. Celle-ci correspond à l’afflux dans la muqueuse nasale de polynucléaires éosinophiles.
Cet afflux de polynucléaires éosinophiles est dépendant de chimiokines produites au lieu de l’inflammation par les cellules endothéliales et épithéliales, et par les cellules inflammatoires au premier rang desquelles se trouvent les mastocytes. Les cellules répondent aux chimiokines en se déplaçant le long d’un gradient de concentration croissante de ces molécules jusqu’à rejoindre le lieu de la réaction inflammatoire.
Les éosinophiles sont des cellules toxiques, notamment pour les épithéliums. Cette toxicité est médiée par la production par les éosinophiles de protéines basiques. La plus importante est appelée « major basic protein », suivie de l’ « éosinophil cationic protein » de la peroxydase de l’éosinophile. Cette toxicité des éosinophiles favorise à son tour l’oedème et l’obstruction nasale.
Il faut bien prendre en compte que la distinction entre phase précoce et phase tardive ne vaut réellement que pour les conditions expérimentales de la stimulation allergique spécifique. En réalité, quand le sujet allergique est exposé en permanence à un pneumallergène à plus ou moins forte concentration, on assiste en permanence à une conjonction des événements précoces et tardifs, qui constituent la maladie chronique.
3. Facteurs de risque contribuant au développement de
l’allergie aux acariens
3.1. La prédisposition génétique
Le facteur de risque le plus prédisposant au développement des allergies, est de loin l’existence de cas identique dans la famille.
Le terme «atopie» proposé en 1923 par Coca et Cook pour expliquer une prédisposition génétique à présenter certaines maladies dites :
« Maladies atopiques » (dermatite atopiques, rhinite Allergique, asthme allergique, allergie alimentaire).
Dans les années 1970, Pepys définit l’atopie comme étant « l’anormale facilité à synthétiser des anticorps immunoglobuline E (IgE) spécifiques vis-à-vis d’allergènes naturels pénétrés dans l’organisme par des voies naturelles ».
Au total, l’atopie est une maladie génétique en rapport avec un déséquilibre immunitaire au profit des lymphocytes Th2 se traduisant par une production excessive d’IgE spécifiques dirigées contre des allergènes naturels de l’environnement. [24]
Les antécédents familiaux [3]
Ils constituent le meilleur marqueur du risque allergique d’un enfant :
-Si aucun des membres de la famille n’est allergique, le risque est autour de 5 à 15%.
-Si l’un des deux parents est atopique, cette fréquence augmente à 20-40%.
La comparaison des séquençages des gènes a permis de montrer que plusieurs gènes sont responsables de l’atopie. Une localisation en est le chromosome 11q et une autre se situe près du gène de l’IL-4 du chromosome 5q. Les gènes présents dans ces régions pourraient affecter les réponses IgE. En effet, ceux présents sur le chromosome 11 codent pour la sous-unité β du récepteur de haute affinité aux IgE, ceux du chromosome 5 codent pour des cytokines (IL-3, 4, 5, 9, 12, 13 et GM-CSF) importante dans la commutation isotypique vers l’IgE, le suivie des éosinophiles et la prolifération des mastocytes.
Le CMH de classe II
Un second type de variations héréditaires dans les réponses IgE-dépendantes est lié à la région du CMH et affecte la réponse aux allergènes. De nombreuses études ont montré que la production d’IgE en réponse à un allergène particulier était associée à certains allèles du CMH de classe II. Ceci implique que certaines combinaisons peptide-CMH peuvent favoriser une réponse TH2. [3]
Le rôle des facteurs génétiques dans la transmission de l'atopie est bien admis. L'étude de la transmission de l'allergène en cause a révélé que chez 89 % des pères sensibilisés aux acariens, l'enfant l'était et que dans 72 % des cas où la mère était sensibilisée à cet allergène, l'enfant avait la même allergie.
Ceci suppose l'intervention des facteurs environnementaux qui sont communs à tous les membres de la même famille. [25]
3.2. Exposition aux allergènes d’acariens
3.2.1. Relation entre l’exposition aux allergènes et la sensibilisation A côté des facteurs génétiques l’importance de l’exposition aux allergènes constitue un facteur de risque de sensibilisation.
De nombreux travaux ont mis en évidence la présence d’une relation positive entre l’exposition aux allergènes d’acariens et l’acquisition d’une sensibilisation vis-à-vis de ces allergènes. Chez les enfants de la naissance à l'âge de trois ans, de cinq à douze ans et chez les adolescents de douze à quatorze ans. [26] [27] [28]
Concernant le seuil de sensibilisation, l’acquisition d’une sensibilisation aux acariens est corrélée à un taux de Der p1 au moins égal à 2 microgrammes de Der p1 par gramme de poussière ce qui correspond à 100 Dpt [29].
Cependant ce seuil n’est pas toujours vérifié, En effet, dans son étude prospective, Wahn et coll. [30] montrent que 3 % des enfants de familles d'atopiques développent une sensibilisation vis-à-vis des acariens pour des taux d'allergènes du groupe 1 inférieurs à 2 µg/g de poussière.
Dans une étude prospective réalisée à Marrakech entre décembre 2002 et décembre 2005, chez 160 enfants atopiques, la sensibilisation aux acariens a été observée chez 56% malgré le climat chaud et sec qui caractérise cette ville. [31]
Dans l’étude de Hallas sur la sensibilisation aux acariens à Reykjavik où les habitants sont exposés à des taux extrêmement bas d’acariens au domicile, 9% des adultes jeunes ont des IgE sériques spécifiques dirigées contre
Il semble que les enfants nés au mois d’octobre ont un risque maximum de devenir allergiques aux acariens, dans une étude menée par Montis et coll qui avait comme objectif de rechercher une relation entre la date de naissance et la sensibilisation aux acariens, afin d’améliorer la prévention. Le résultat du « radio allergo sorbent test » d1, qui apprécie la présence dans le sérum d'IgE spécifiques de l'acarien Dermatophagoïdes pteronyssinus, a été étudié en fonction de la date de naissance de 5 747 enfants et adolescents présumés allergiques. Les moyens éventuels qu'auraient pu introduire des différences de distribution, d'un mois à l'autre, de certains paramètres (sexe, antécédents personnels et familiaux) ont été corrigés mathématiquement. Une corrélation entre le mois de naissance et le risque d'avoir des IgE sériques spécifiques du
Dermatophagoïdes pteronyssinus a ensuite été recherchée.
Il existe un rythme circannuel du risque de sensibilisation aux acariens, selon la date de naissance, qui évolue selon une courbe sinusoïde dont le maximum, à 104 %, est en octobre et le minimum, à 96 %, en avril.
En effet, ces enfants passent les premiers mois de leur vie dans une atmosphère surchauffée, peu aérée, car les parents craignent que le bébé n’attrape froid. Ils vivent ainsi sur des matelas envahis d’acariens et s’y sensibilisent plus facilement. [33]
3.2.2. Relation entre exposition allergénique et apparition de la maladie Allergique
La grande majorité des études s'intéressant au lien entre exposition aux pneumallergènes et symptômes a trait à l'asthme et, par conséquent, à l'effet des allergènes sur l'hyperréactivité bronchique, les symptômes d'asthme et la sévérité de la maladie. Concernant la rhinite, un nombre très limité d'études a été
publié. En effet, les études transversales et prospectives ont souligné la nécessité d'une sensibilisation préalable associée à une exposition pour l'apparition de symptômes. [27]
Pour les acariens de la poussière domestique, les premières études qui ont suggéré le rôle de l’exposition allergénique sur les symptômes ont montré
une amélioration de la symptomatologie d’asthme après éviction des allergènes lors de séjours dans des lieux appauvris en acariens.
L’une des premières publications est celle de Platts- Mills et coll. [34]
qui a montré, chez neuf sujets allergiques aux acariens, une amélioration des signes cliniques et une diminution de l’hyperréactivité bronchique, après un séjour de 2 mois dans un milieu hospitalier sans acariens. Ces constatations ont été confortées par les études de Boner et coll. [35] et de Peroni et coll. [36] réalisées auprès d’enfants asthmatiques séjournant à 1756mètres d’altitude. Un aspect intéressant de ces dernières études est l’existence d’une récidive des symptômes et de l’aggravation de l’HRB non spécifique lorsque les enfants séjournaient de nouveau à leur domicile originel, riche en allergènes d’acariens, traduisant le rôle probable de ceux-ci dans la responsabilité de la symptomatologie d’asthme.
Si la survenue de symptômes lors d'une exposition allergénique chez des sujets sensibilisés semble claire, la définition du seuil de déclenchement des manifestations cliniques est controversée. Cette valeur dépendra des méthodes de mesure de l'exposition allergénique qui variera en fonction de l'allergène considéré. En effet, les concentrations d'allergènes d’acariens retrouvés dans la poussière ne correspondent pas à celles pénétrant réellement dans les voies aériennes. Ainsi, la quantité d'allergène nécessaire pour induire une réaction clinique avec les acariens serait différente de celle nécessaire avec les autres
![Figure 1. Photo de Dermatophagoïdes pteronyssinus [8]](https://thumb-eu.123doks.com/thumbv2/123doknet/15037300.690594/36.892.158.840.179.701/figure-photo-de-dermatophagoïdes-pteronyssinus.webp)
![Figure n° 2 : dessin de Dermatophagoïdes pteronyssinus [11]](https://thumb-eu.123doks.com/thumbv2/123doknet/15037300.690594/38.892.331.553.648.952/figure-n-dessin-de-dermatophagoïdes-pteronyssinus.webp)
![Figure n° 3 : les déjections des acariens [18]](https://thumb-eu.123doks.com/thumbv2/123doknet/15037300.690594/44.892.234.660.520.821/figure-déjections-acariens.webp)

![Figure n° 5 : Schéma général de la réaction d’hypersensibilité de type I [23]](https://thumb-eu.123doks.com/thumbv2/123doknet/15037300.690594/53.892.147.720.413.797/figure-schéma-général-réaction-hypersensibilité-type.webp)
![Tableau 1 : nouvelle classification OMS de la rhinite allergique. [63]](https://thumb-eu.123doks.com/thumbv2/123doknet/15037300.690594/75.892.121.787.162.640/tableau-nouvelle-classification-oms-rhinite-allergique.webp)

![Figure n° 8 : schéma d’une housse anti-acariens [85]](https://thumb-eu.123doks.com/thumbv2/123doknet/15037300.690594/98.892.204.736.123.362/figure-schéma-housse-anti-acariens.webp)