HAL Id: tel-00910947
https://tel.archives-ouvertes.fr/tel-00910947
Submitted on 28 Nov 2013
HAL is a multi-disciplinary open access
archive for the deposit and dissemination of
sci-entific research documents, whether they are
pub-lished or not. The documents may come from
teaching and research institutions in France or
abroad, or from public or private research centers.
L’archive ouverte pluridisciplinaire HAL, est
destinée au dépôt et à la diffusion de documents
scientifiques de niveau recherche, publiés ou non,
émanant des établissements d’enseignement et de
recherche français ou étrangers, des laboratoires
publics ou privés.
Millot Romain
To cite this version:
Millot Romain. Les isotopes du lithium: exemples d’applications en géochimie. Sciences de la Terre.
Université d’Orléans, 2013. �tel-00910947�
M
oi e p se t e vue de l’o te tio de
l’Ha ilitation à Diriger des Recherches
Dr. Romain MILLOT
BRGM
– Direction des Laboratoires
I stitut des S ie es de la Te e d’O l a s
UMR 7327 BRGM-ISTO
Les isotopes du lithium:
exemp
les d’applicatio s e géochi ie
Soutenue le 27 novembre 2013
devant le jury composé de :
Pr. Francis ALBAREDE (École Normale Supérieure, Lyon) - rapporteur
Dr. Marc CHAUSSIDON (CRPG, Nancy) - rapporteur
Pr.
E i MA‘COUX U i e sit d’O l a s) - examinateur
Dr. Philippe NEGREL (BRGM, Orléans) - examinateur
Dr. Bruno SCAILLET (ISTO, Orléans) - di e teu du la o atoi e d’a ueil
Pr. Avner VENGOSH (Duke University, USA) - rapporteur
Ce mémoire constitue la synthèse des travaux de Recherches menés au BRGM au cours de ces
10 dernières années.
Après une introduction qui précise le contexte et les objectifs de ce travail, ce manuscrit
p se te tout d a o d les g a ds p i ipes de la g o hi ie isotopi ue du lithiu .
Puis, dans un second temps, nous décrivons en détails le protocole de mesure des isotopes du
lithium dans des matrices liquides et solides.
E suite, et ette pa tie o stitue le œu de e a us it, ous illust o s au t ave s de
différents exemples ciblés
l appli atio de et outil isotopique à la compréhension des
systèmes et des milieux comme les eaux de pluies et les fleuves ainsi que dans les interactions
eau/roche à basse et haute température, au travers des eaux thermo-minérales et des eaux
géothermales et enfin des systèmes expérimentaux. Les eaux thermales ou thermominérales
du Massif Central ont été séparées des eaux géothermales (Antilles et N
elleZélande qui se
trouvent en contexte volcanique insulaire).
La dernière partie de ce manuscrit est consacrée à la synthèse des activités de recherches en
terme de publications (articles, congrès, rapports)
et d e ad e e t s ie tifi ue d tudia ts.
Nous présentons aussi une synthèse des activités de recherches dans le cadre de projets de
R&D. Enfin, en annexe, une sélection
d articles scientifiques illustre ces travaux par
thématique. Ces exemples ont été sélectionnés dans le but de garder un fil conducteur dans
ce manuscrit. Il a donc fallu faire des choix pour illustrer au mieux les différentes applications.
Le lecteur est averti ici que les illustrations sont en anglais, ces figures sont directement
reproduites de publications scientifiques internationales rassemblées en annexe.
Sommaire
1.
Introduction ... 9
2.
Géochimie isotopique du lithium ... 13
2.1. Variations isotopiques du lithium dans les matériaux géologiques ... 13
2.2. Fractionnement isotopique du lithium et paramètres de contrôle ... 15
3.
Mesure des rapports isotopiques du lithium ... 19
3.1. Spectrométrie de masse ... 19
3.2. Protocole de purification du lithium ... 21
3.3. Acquisition de données et corrections ... 26
4.
Exemples d’applications : synthèse des principaux résultats ... 31
4.1. Eaux météoriques (Millot et al., 2010) ... 31
4.2. Eaux de rivières (Millot et al., 2010 ; Lemarchand et al., 2010) ... 37
4.2.1. Le bassin du fleuve Mackenzie ... 37
4.2.2. Le bassin du Strengbach ... 41
4.3. Eaux thermominérales (Millot et al., 2007 ; Millot et Négrel, 2007) ... 43
4.3.1. Caractérisation multi-isotopique Li-B-Sr-
Nd d’eau the o i
ales du
Massif Central ... 43
4.3.2. Approche couplée isotopique et géothermométrie ... 44
4.4. Eaux géothermales (Millot et al., 2012 ; 2010) ... 48
4.4.1. Eaux géothermales de N
elleZélande ... 48
4.4.2. Eaux géothermales des Antilles : Guadeloupe et Martinique ... 49
4.5. Approche expérimentale (Millot et al., 2010) ... 52
5.
Conclusions et perspectives ... 59
6.
Références bibliographiques ... 63
7.
Curriculum Vitae ... 69
EXPÉRIENCE ET FORMATION ... 69
COMPÉTENCES TECHNIQUES ... 70
LABORATOIRES DE RECHERCHE ... 70
COLLABORATIONS SCIENTIFIQUES EXTERNES (PAR ORDRE ALPHABÉTIQUE) ... 70
ACTIVITÉ“ D’ENCAD‘EMENT ... 70
BILAN SYNTHÉTIQUE DES ACTIVITÉS DE RECHERCHE ... 71
8.
Liste détaillée des publications et de l’activité de recherche ... 75
ARTICLES SCIENTIFIQUES EN 1
ERAUTEUR (12) ... 75
AUTRES ARTICLES SCIENTIFIQUES (24 EN CO-AUTEUR) ... 76
RAPPORTS SCIENTIFIQUES (19 DONT 3 EN PREMIER AUTEUR) ... 77
CONFÉRENCES INVITÉS (5) ... 79
CONFÉRENCES EN 1
ERAUTEUR (34) ... 79
AUTRES CONFÉRENCES (44) ... 82
ACTIVITÉS ET PROGRAMMES DE RECHERCHES (DEPUIS 2003) ... 85
9.
Remerciements ... 89
10.
Annexes : Sélection de publications ... 91
Liste des illustrations
Figure 1 - Classification des éléments chimiques dans le tableau de Mendeleïev. Les couleurs
identifient les différentes systématiques isotopiques appliquées, en développement et en
projet au BRGM à la date de ce document. ... 10
Figure 2 - Représentation schématique des isotopes de masse 6 et 7 du lithium avec
respectivement 3 et 4 neutrons. ... 10
Figure 3 - Analogie entre une étude démographique et une étude géochimique. ... 11
Figure 4 - Abondances en % des deux isotopes du lithium. ... 13
Figure 5 -
G aphi ue ep se ta t l’ a t de asse elati
atomique Z (Johnson et al., 2004). ... 14
Figure 6 - Variations des compositions isotopiques du Li dans les matériaux terrestres.
Modifi d’ap s To as ak
). ... 15
Figure 7 - Spectromètre de masse à source solide (TIMS) modèle MAT 262 du brgm. La partie
en premier plan correspond à la sourc
e, e suite ous pou o s ape e oi l’ai a t au se o d
plan à gauche et enfin le tube et la partie « collection/détection
» à l’a i e pla à d oite. ... 19
Figure 8 - Neptune MC-ICP-MS en service au brgm. ... 20
Figure 9 - Nombre de publications scientifiques par année dans la thématique des isotopes
du lithium dans les Sciences de la Terre (étude bibiographique réalisée en 2010). ... 21
Figure 10 - Colonnes en Téflon contenant de la résine cationique, ces colonnes se trouvent
dans une hotte à flux laminaire, elle-même située dans une salle blanche. ... 22
Figure 11 - Schéma de principe de séparation de deux éléments par chromatographie
ionique. ... 23
Figure 12 -
Cou es d’ lutio du lithiu et du sodiu e ilieu a ide HCl . N pou u e
matrice eau de mer. Seule la fraction comprise entre 10 et 35 mL est collectée (flèche rouge)
et o tie t u i ue e t le lithiu . A ote la diff e e d’ helle sig ifi ati e e t e le
lithium et le sodium. ... 23
Figure 13 - Evolution de
la o positio isotopi ue du lithiu au ou s de l’ lutio su si e
ha geuse d’io s d’ap s To as ak,
). ... 24
Figure 14 - Compilation des mesures de la com
positio isotopi ue de l’eau de e pa TIM“
(en bleu) et MC-ICP-MS (en rouge). Nos valeurs sont reportées à droite de la figure (Millot et
al., 2004). ... 25
Figure 15 - Comparaison entre les valeurs obtenues à Nancy (axe des Y) et au BRGM (axe des
X) lors de la mesure de 3 solutions standards Li6-N, LiCl-N et Li7-N (Carignan et al., 2007). A
noter les erreurs différentes reportées en haut à gauche pour deux MC-ICP-MS différents... 25
Figure 16 - Schéma et photographie de la source ICP du Neptune. Successivement de gauche
à droite : le lithiu est tout d’a o d io is da s le plas a, les io s so t e suite e t aits pa
une différence de potentiels de 2000 V, puis ce faisceau est accélerré (5000 V) et focalisé à la
fois da s les di e sio s de l’espa e X-Y-Z) mais aussi en énergie par un filtre
électrostatique. ... 26
Figure 17 - Principe du standard-bracketing et de la correction des blancs. Le schéma du bas
o t e l’ olutio au ou s du te ps du appo t isotopi ue pou le sta da d et l’ ha tillo
ai si ue le p i ipe d’i te polatio pour le calcul du delta. ... 27
Figure 18 - “ st
e “I“ d’i t odu tio de l’ ha tillo li uide da s le plas a. ... 27
Figure 19 - Schéma de fonctionnement du MC-ICP-MS Neptune. ... 28
Figure 20 - Configuration pour la mesure des isotopes du lithium sur les cages L4 et H4. Les
spe t es de asse pou les asses et so t do
s pou la esu e d’u e solutio
standard de 30 ng/mL de lithium. ... 29
Figure 21 - Carte de localisation des sites de suivi des eaux de pluies sur fond de carte
géologique (Millot et al., 2010c). ... 31
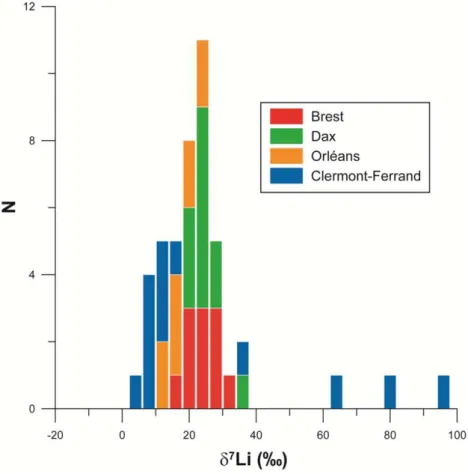
Figure 22 - Histogramme des compositions isotopiques du lithium des eaux de pluies pour les
sites d’ tude Millot et al.,
). ... 32
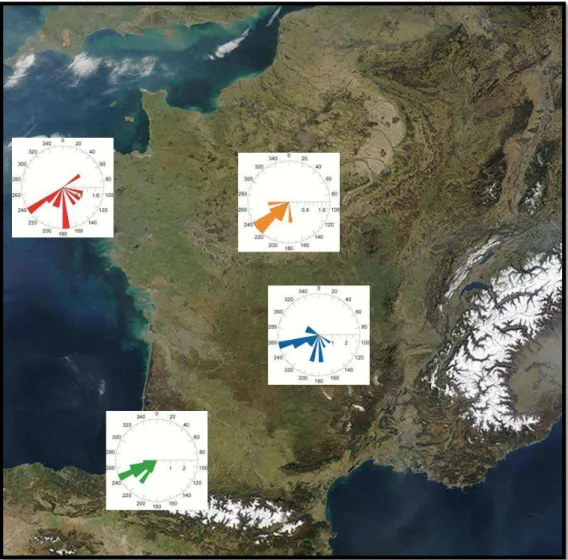
Figure 23 -
‘oses des e ts pou les sites d’ tude Millot et al.,
). ... 33
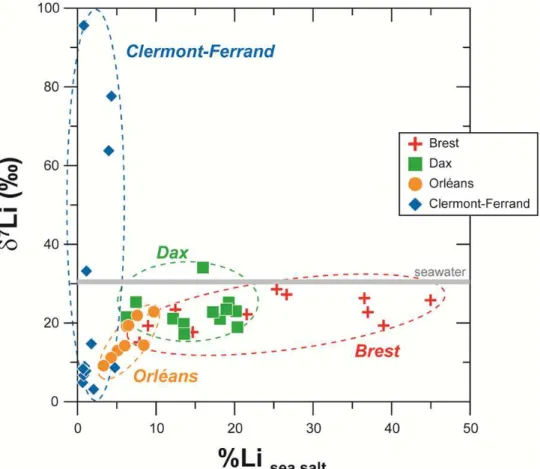
Figure 24 - Composition isotopique du lithium en fonction de la contribution marine du
lithium (Millot et al., 2010c). ... 34
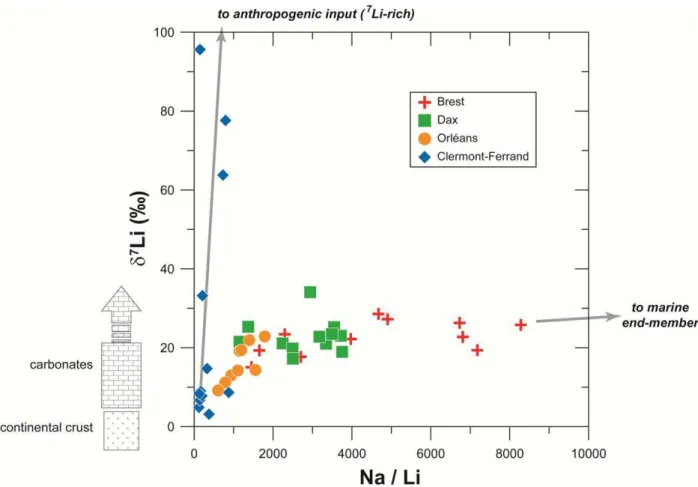
Figure 25 - Composition isotopique du lithium en fonction du rapport molaire Na/Li (Millot et
al., 2010c). ... 35
Figure 26 - Ca te du assi du fleu e Ma ke zie a e les poi ts d’ ha tillo age et les zo es
morphotectoniques (Millot et al., 2010a). ... 38
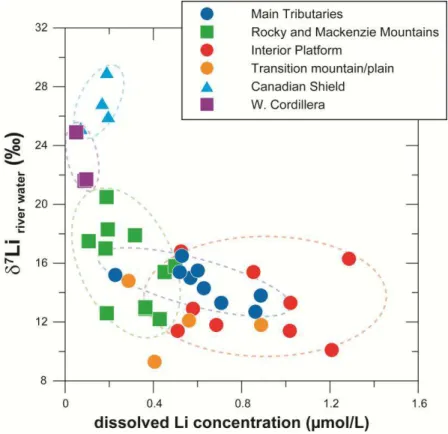
Figure 27 - Compositions isotopiques du lithium en fonction de la teneur en lithium dans les
eaux du bassin du fleuve Mackenzie (Millot et al., 2010a). ... 39
Figure 28 - Compositions isotopiques du lithium des eaux (rouge), des matières en
suspension (bleu) et des roches (vert) dans le bassin du fleuve Mackenzie (Millot et al.,
2010a). ... 39
Figure 29 - Compositions isotopiques du lithium des eaux en fonction de la charge dissoute
p o e a t de l’alt atio des o hes sili at es Millot et al.,
a). ... 40
Figure 30 - Schéma conceptuel de contôle des compositions isotopiques du lithim dans le
bassin du fleuve Mackenzie entre les différentes zones morphotectoniques et les régimes
d’alt atio Millot et al., 2010a). ... 41
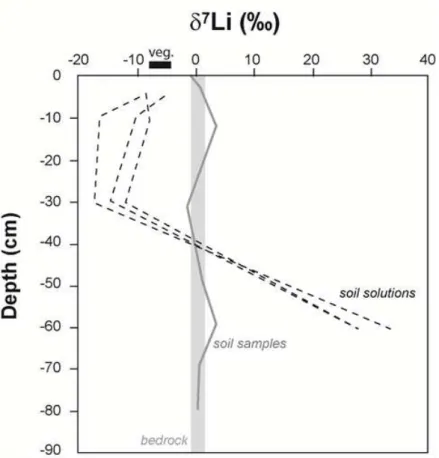
Figure 31 - Compositions isotopiques du Li mesurées dans le bassin versant du Strengbach.
L’ ha tillo de o he
e ed o k) o espo d à la o he affleu a t da s le ilieu du
bassin versant du Strengbach (Lemarchand et al., 2010). ... 42
Figure 32 - (a) carte de localisation du Massif Central, (b) carte du bassin de la Limagne avec
la localisation des dix sites de prélèvement, (c) coupe géologique synthétique et séquence
lithostratigraphique (Millot et al., 2007). ... 43
Figure 33 - Compositions isotopiques du Sr et du Nd reportées en fonction de celle du Li pour
les eau et les o hes de la zo e de la faille d’Aiguepe se. Les u
os o espo de t au
eaux suivantes : [1] Joze, [2] Montpensier, [3] Royat - Eugénie, [4] St Myon, [5] Chatel Guyon
- Carnot, [6] Chatel Guyon - Louise, [7] Gimeaux, [8] Vichy - Dôme, [9] Vichy - forage Antoine
and [10] Bourbon Lancy - Marquise. (Millot et al., 2007). ... 44
Figure 34 - Carte de localisation des eaux thermales étudiées avec à droite un zoom sur les
eaux thermominérales du Massif Central (Millot et Négrel, 2007). ... 45
Figure 35 - Composition isotopique du lithium représentée en fonction de la température du
réservoir calculée par géothermométrie (Millot et Négrel, 2007)... 46
Figure 36 - Carte des champs géothermaux étudiés en N
elleZélande (Millot et al., 2012). ... 48
Figure 37 - Compositions isotopiques du lithium en fonction de la teneur en lithium dans les
eaux géothermales de la Taupo Volcanic Zone en N
elleZélande (Millot et al., 2012). ... 49
Figure 38 - Carte de localisation des champs géothermaux étudiés en Guadeloupe et en
Martinique (Millot et al., 2010b). ... 50
Figure 39 - Composition isotopique du lithium en fonction du rapport Li/Cl pour les eaux du
Lamentin et de Bouillante (Millot et al., 2010b). ... 51
Figure 40 - Dispositif expérimental pour les interactions à 25°, 75° et 200°C (BRGM). ... 53
Figure 41 - Dispositif expérimental pour les interactions à 200° et 250°C (ISTO). ... 53
Figure 42 - Evolution temporelle de la composition isotopique et de la concentration en
lithium dans la solution à différentes températures (Millot et al., 2010b)... 54
Figure 43 -
“ h
a i te p tatif de l’ olutio te po elle de la o positio isotopi ue et de
la concentration en lithium (Millot et al., 2010b). ... 55
Figure 44 -
F a tio e e t isotopi ue du lithiu e t e l’eau et la o he e fo tio de
l i e se de la te p atu e Millot et al.,
). ... 56
Figure 45 - Schéma qui rappelle les objectifs de ce travail. ... 59
1. Introduction
La ati e est o stitu e d’ l
e ts hi i ues tous âtis su le
e od le : l'atome est
constitué d'un noyau composé de protons (chargés positivement) et de neutrons
(électriquement neutres). Autour de ce noyau gravitent des électrons, particules chargées
négativement.
Chaque atome se distingue donc par son nombre de protons (ou d'électrons), également
appelé numéro atomique Z, le nombre de neutrons N et le nombre de nucléons (protons +
neutrons) A.
E : élément chimique
A : masse atomique (protons + neutrons)
Z : numéro atomique (nombre de protons)
Le o
e de p oto s est gal au o
e d' le t o s, e ui assu e la eut alit de l’ato e.
L'ensemble des atomes dont le noyau possède le même couple (Z, A) est appelé un nucléide;
un élément chimique correspond à l'ensemble des atomes de même numéro atomique Z.
Le mot isotope, composé du grec isos "égal, le même" et topos "lieu, place", proprement
"qui occupe la même place", fait référence à la classification de Mendeleïev (Figure 1) car
pour un même élément chimique, il peut exister différents noyaux. En effet, si le nombre de
protons est toujours égal à Z, le nombre de neutrons peut varier et on parle alors d'isotopes
de l'élément chimique. Les isotopes sont caractérisés par le nombre de nucléons (protons +
neutrons) A. On différencie les isotopes d'un élément E par la notation
AE avec par exemple,
le noyau de l'atome d'hydrogène qui est constitué d'un proton pouvant à l'état naturel être
accompagné de zéro, un ou deux neutron(s). L'hydrogène existe donc sous trois formes
isotopiques
1H,
2H (appelé deutérium, noté D) et
3H (appelé tritium, noté T). Les propriétés
chimiques des isotopes d'un même élément sont identiques car ces isotopes ont le même
nombre d'électrons.
La géochimie isotopique a connu ces dernières années un développement sans précédent
en ce qui concerne les applications concernant le traçage des éléments dans
l’e i o e e t. Cet esso est le sultat des d eloppe e ts i st u e tau da s le
do ai e de l’a al se isotopi ue. E effet, l’outil de spectrométrie de masse à source plasma
et multi-collection (MC-ICP-MS : Multi Collector Inductively Coupled Plasma Mass
Spectrometer) a permis la mesure juste et précise à de très faibles teneurs de systèmes
isotopiques non traditionnels, notamment certains métaux, métalloïdes et non-métaux.
Figure 1 - Classification des éléments chimiques dans le tableau de Mendeleïev. Les couleurs
identifient les différentes systématiques isotopiques appliquées, en développement et en
projet au BRGM à la date de ce document.
L
’ l
e t hi i ue lithium (Z=3) est constitué de deux isotopes de masse 6 et 7, voir la
figure 2, ci-dessous. Le lithium 7 (
7Li) est l’u des a es u lides a a t t fo
lo s de la
nucléosynthèse primordiale (Big Bang), alors que très peu de
6Li a été généré durant cet
évènement. De nos jours, les atomes de Li sont principalement produits lors de réactions de
spallations, c'e
st‐à‐di e lo s de la dest u tio d’ato es plus lou ds de a o e et d’o g e
sous l’effet de a o e e ts os i ues. La os o hi ie du lithiu e t u e i po ta e
particulière car les rapports isotopiques
7Li/
6Li permettent à la fois d'aborder des problèmes
cosmologiques, c'est-à-dire touchant au Big-Bang et à l'origine de l'Univers, et d'étudier
l'évolution de la composition chimique et isotopique de la galaxie (Chaussidon et Robert,
1998 ; Beck et al., 2004).
Figure 2 - Représentation schématique des isotopes de masse 6 et 7 du lithium avec
respectivement 3 et 4 neutrons.
1 2H
B Analyses en routine au BRGMHe
1.008 4.00 3 4 5 6 7 8 9 10Li
Be
Mo En cours de développementB
C
N
O
F
Ne
6.94 9.01 10.81 12.01 14.01 16.00 19.00 20.18 11 12 13 14 15 16 17 18Na
Mg
Sn En projetAl
Si
P
S
Cl
Ar
23.00 24.31 26.98 28.09 30.97 32.06 35.45 39.95 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36K
Ca
Sc
Ti
V
Cr
Mn
Fe
Co
Ni
Cu Zn
Ga Ge As
Se
Br
Kr
39.10 40.08 44.96 47.90 50.94 52.00 54.94 55.85 58.93 58.71 63.55 65.38 69.72 72.59 74.92 78.96 79.90 83.80 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54Rb
Sr
Y
Zr
Nb
Mo
Tc Ru Rh Pd Ag
Cd
In
Sn Sb Te
I
Xe
85.47 87.62 88.91 91.22 92.91 95.94 98.91 101.07 102.90 106.40 107.90112.40 114.80 118.70 121.80 127.60 126.90 131.30 55 56 57 72 73 74 75 76 77 78 79 80 81 82 83 84 85 86Cs Ba La* Hf
Ta
W
Re Os
Ir
Pt
Au Hg
Tl
Pb
Bi
Po
At
Rn
132.90 137.30 138.90 178.50 181.00 183.90186.20 190.20192.20 195.10 197.00 200.60 204.40207.20209.00 (210) (210) (222) 87 88 89 104 105Fr
Ra Ac** Ku Ha
(223) (226) (227) (258) (260) 58 59 60 61 62 63 64 65 66 67 68 69 70 71*Lanthanides
Ce
Pr
Nd
Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu
140.10 140.90144.20 (145) 150.40 152.00 157.30 158.90 162.50 164.90 167.30 168.90 173.00 175.00 90 91 92 93 94 95 96 97 98 99 100 101 102 103**Actinides
Th
Pa
U
Np Pu Am Cm Bk
Cf
Es Fm Md No
Lr
232.00231.00 238.00237.00 239.10 (243) (247) (247) (251) (254) (257) (256) (254) (258)Le développement technologique instrumental des cers dernières années a généré de
nombreux programmes de recherches appliquée
s o e a t l’ tude de l’origine, du
transfert et du devenir de ces éléments dans les systèmes géologiques de surface et de
sub-surface.
La mise en évidence de variations des signatures isotopiques pour ces éléments dans les
différents réservoirs géochimiques permet non seulement
d’ tudie les p o essus ou
mécanismes de transfert de ces éléments entre ces réservoirs, mais aussi de quantifier les
flux et de caractériser les réactions physico-
hi i ues à l’o igi e de es f a tio e e ts
isotopiques (Faure, 1986 ; 1998 ; Allègre 2005).
Ai si, la g o hi ie isotopi ue utilise les o t astes h it s de l’histoi e de la Te e
(différenciation des réservoirs géochimiques terrestres) pour étudier les transferts
géochimiques actuels des éléments entre les différents réservoirs terrestres superficiels et
profonds (Allègre, 1987 ; Wasserburg, 1987).
L
’a alogie i t essa te ui peut t e faite i i pou e pli ue le i eau d’i fo atio
suppl
e tai e o te u pa l’a al se isotopi ue pa appo t à l’a al se l
e tai e est
décrite ci-après (Figure 3). En faisant le parallèle entre une étude géochimique et une étude
d
og aphi ue, l’a al se l
e tai e
esu e de la o e t atio d’u l
e t)
s’appa e te à o pte le o
e d’i di idus da s u e populatio . Alo s ue la esu e
isotopique consiste à faire le rapport des individus selon leur sexe (rapport isotopique) ou
selon leur âge (datation en géochronologie).
D’u e a i e g
ale, les o positions isotopiques mesurées dans les éléments
hi i ues peu e t selo les as, soit a a t ise les sou es o igi e de l’ l
e t) ou soit
être des marqueurs des processus physico-chimiques conduisant à un fractionnement entre
isotopes et par là-même à une modification de la composition isotopique. Il est évident que
les deux phénomènes peuvent très bien se surimposer.
En ce qui concerne le traçage des sources
o igi e et ua tifi atio des flu ), l’e e ple le
plus connu est probablement celui des isotopes du
plo
. E effet, l’utilisatio des
différents rapports isotopiques du plomb (
206Pb/
204Pb,
207Pb/
204Pb et
208Pb/
204Pb) permet
g
ale e t de ett e e ide e la p se e d’u e ou plusieu s sou es de plo
da s
l’e i o e e t ito s i i les t a au pionniers dans le domaine de Clair Patterson et son
équipe dès les années 1960 : Tatsumoto et Patterson 1963 ; Murozimi et al., 1969).
La gamme de variation de la composition isotopique en Pb dans les matériaux terrestres est
telle e t i po ta te ue l’e p ei te isotopi ue laiss e pa l’histoi e g ologi ue du P
(différenciation des réservoirs et évolution dans le temps) est intégrée à la source de
pollution. Ainsi, la composition isotopique du plomb varie en fonction du rapport chimique
initial U/Pb (rappo
t dit p e/fils) et de l’âge de so gise e t d’e t a tio . De e fait, le
plo
a th opi ue pa e e ple dispe s da s l’at osph e pa diff e ts p o essus
i i
atio , o
ustio ...) o se e la sig atu e isotopi ue de so i e ai d’o igi e,
lequel diffère très généralement du plomb endogène local. Et donc, on utilise la composition
isotopi ue du plo
à la a i e d’u e e p ei te digitale pou dis i i e diff e tes
sources naturelles ou anthropiques.
En ce qui concerne les processus, les principaux mécanismes de fractionnements
isotopiques résultent principalement des réactions physico-chimiques comme les
t a sfo atio s d’o do du tio , de la dissolutio ou de la p
ipitatio de i
au et/ou
de phases néoformées (oxy-
h d o des) lo s de l’alt ation, mais aussi des mécanismes
d’adso ptio et de d so ptio su des su fa es. A ela peu e t s’ajoute les effets li s au
micro-organismes (bactéries) qui pour leur développement peuvent intégrer certains
tau da s leu
ta olis e et t e à l’o igi e de fractionnements isotopiques dans leurs
milieux de croissance.
2. Géochimie isotopique du lithium
2.1. Variations isotopiques du lithium dans les matériaux
géologiques
Le lithium est un métal alcalin et comme les autres éléments de son groupe, le Li possède un
seul électron de valence qui est facilement perdu pour former le cation Li
+, ce qui explique sa
faible électronégativité. Le Li est le 3
èmeélément de la classification périodique de
Mendeleïev, il se place en colonne 1A juste au-dessus du sodium, un élément aux propriétés
chimiques très proches. Comme souvent dans le tableau périodique, le Li peut être relié à
l’ l
e t oisi selo u e diago ale: le ag siu . E effet, le rayon ionique du Li est 0.163
nm
’est à di e très proche de celui du Mg 0.168 nm et permet donc une substitution de ces
deux éléments. Toutefois le lithium, contrairement au Mg, reste un élément incompatible
lo s des p o essus de fusio et de la istallisatio . D’ap s la lassifi atio de Golds h idt,
le Li est dit lithophile, modérément incompatible et se trouve donc en abondance dans les
roches silicatées de notre planète (lithium vient de « lithos » : la roche).
Le lithium est un élément chimique qui possède deux isotopes de masse 6 et 7, dont les
abondances naturelles sont respectivement de 7.5% et 92.5% (Figure 4).
Figure 4 - Abondances en % des deux isotopes du lithium.
Le lithium présente donc un caractère lithophile et très fortement soluble. La différence de
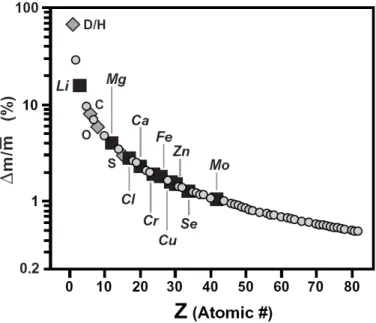
masse relative entre les deux isotopes est considérable (17%, Figure 5) et engendre des
fractionnements de masse importants lors des processus géochimiques. Coplen et al., (2002)
ont montré que la gamme de variation des compositions isotopiques du lithium est de plus
de ‰ da s les at iau g ologi ues.
Figure 5 -
G aphi ue ep se ta t l a t de asse elatif
m/m) en fonction du numéro
atomique Z (Johnson et al., 2004).
La o positio isotopi ue du lithiu d’u ha tillo (« sample ») se note en déviation
elati e e ‰) pa appo t à la aleu d’u sta da d:
Le standard de référence est un carbonate de lithium (L-SVEC, NIST RM8545) dont la valeur
du
7Li est de 0
‰ pa d fi itio
7Li/
6Li = 12.02 ± 0.03, Flesch et al., 1973).
Da s so a ti le de s th se, To as ak
) a o pil l’a plitude des a iatio s
isotopiques des différents réservoirs terrestres. De plus, Teng et al., (2004) ont également
reporté les compositions isotopiques de différents types de roches (shales, loess et granites)
da s le ut d’esti e la o positio isotopi ue du lithiu de la oûte o ti e tale
supérieure.
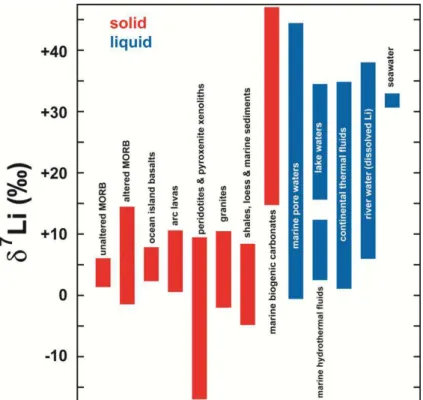
Ainsi, les granites présentent des compositions isotopiques en lithium comprises
généralement entre -
et + ‰, ua t au asaltes de t pe MO‘B, OIB et asaltes d’a )
leurs
7Li
a ie t de + à + ‰.
L’eau de e actuelle possède une composition isotopique en lithium très homogène
d’e i o + ‰, les eau de i i es o t des o positio s i te
diai es e t e + et + ‰
et les eaux thermo-minérales ont des compositions isotopiques qui varient entre -20 et
+ ‰ Figu e ).
3 6 7 6 7 710
1
‰
SVEC L sampleLi
Li
Li
Li
Li
Figure 6 - Variations des compositions isotopiques du Li dans les matériaux terrestres.
Modifi d ap s To as ak
.
D’u e a i e g
ale, les concentrations en lithium des eaux ne sont contrôlées que par
les p o essus d’i te a tio s eu -
es i te sit d’interaction, température et assemblage
minéralogique),
pa la fo atio de i
au se o dai e d’alt atio ainsi que par les
p o essus d’adso ptio /d so ptio lo s d’ ha ge e t e le lithiu e solutio et les surfaces
i
ales. D’aut e pa t, il a été mont ue les
a tio s d’o do-réduction, de
o ple atio o ga i ue ou de sp iatio ’o t au u effet de o t ôle is-à-vis des
concentrations de lithium dans les eaux.
2.2. Fractionnement isotopique du lithium et paramètres
de contrôle
Deux grands types de fractionnement des isot
opes sta les so t aujou d’hui connus :
1- l
e f a tio e e t d’ uili e se produit lors des réactions chimiques ou physiques
faisant intervenir une
a tio d’équili e. L’i po ta e de e t pe de
fractionnement est directement proportionnelle à la différence de masse entre les
deux isotopes et
l’a plitude du f a tio e e t est inversement proportionnelle à la
température. En effet, lorsque la température de la réaction augmente, le
fracti
o e e t isotopi ue d’ uili e tend à devenir nul.
2-
lo s d’u fractionnement cinétique, les isotopes les plus légers sont
systématiquement avantagés par leur vitesse lors des réactions chimiques ou lors des
processus de transport. Ce mode de fractionnement est théoriquement insensible à
E e ui o e e l’a plitude des f a tio e e ts isotopi ues du Li lors des interactions
eau/roche et les facteurs qui les contrôlent, des études menées dans des contextes
d’alt atio de asse/ o e e te p atu e o t o t ue le f a tio e e t isotopique
asso i au i te a tio s eau/ o he fa o ise l’e i hisse e t de la solutio e isotope lou d
(
7Li). Ce résultat vient du fait que l
’isotope l ge
6Li) est préférentiellement retenu dans les
phases solides en particulier dans les minéraux secondaires
d’alt atio .f. To as ak,
2004).
Lo s de l’alt atio des o hes par les eaux à la surface de la Terre, les isotopes du lithium
so t fo te e t f a tio
s α
1peut varier de 0.970 à 0.990 entre les phases dissoutes et
particulaires transportées par les rivières ; Huh et al., 1998 ; 2001).
A l’ helle d’u assi
versant, l
a sig atu e isotopi ue du lithiu des eau ’est pas un traceur des lithologies, mais
il a été montré que
l’a plitude du fractionnement isotopique () est à mettre en relation
a e l’i te sit de l’alt atio Huh et al., 2001 ; Millot et al., 2010a).
En ce qui concerne le fractionnement isotopique à plus haute température, notamment lors
des p o essus d’alt atio sous-marine de la croûte océanique, Chan et al., (1992) ont
o t u’il existait un fractionnement de
= 0.981 pour une température de 150°C
(
minéral-fluide), alo s u’il est de .
à .
à
°C e i o Cha et al., 1993). Enfin,
l’a al se isotopi ue du lithiu de diff e tes la es d’u e s ie de diff e tiatio
magmatique a clairement
o t l’a se e de f a tio e e t isotopi ue à pa ti de
°C
(Tomascak et al., 1999a). De plus, une loi expérimentale qui relie le fractionnement
isotopique (entre une solution et la phase solide) et la température a été établie par Millot
et al.,
) et s’e p i e de la faço sui a te a e la te p atu e e Kel i :
solution – solide
= 7847 / T
– 8.093
La plupart des fractionnements isotopiques du lithium se produisent à la surface de la Terre.
La faible charge ionique, le rayon relativement petit et le fort degré de covalence dans ses
liaiso s do e t au lithiu des p op i t s ui o t fai e u’il se a p se t da s de
nombreux environnements géochimiques (eaux, roches, sols, sédiments...). Le lithium
poss de e solutio u e oo di atio t t a d i ue h d at e pa des ol ules d’eau. Da s
les solides, le lithium occupe des sites de coordination soit tétraédrique, soit octaédrique.
Le fractionnement isotopique associé à la cristallisation/recristallisation, dans laquelle le gain
e e gie se p oduit pa l’i o po atio p f e tielle d’u isotope pa appo t à l’aut e
dans un site cristallographique, est un mécanisme important à la surface de la Terre. Les
calculs thermodynamiques (Yamaji et al.,
) o t e t ue l’ ha ge de lithiu e s des
sites istallog aphi ues o ta d i ues à pa ti d’u e solutio fa o ise l’i o po atio
p f e tielle de l’isotope
6Li dans le solide. Ce fractionnement isotopique a été mis en
ide e da s de o
eu e i o e e ts atu els, et l’effet de f a tio e e t se
le
être dépendant à la fois de la température de réaction et du rapport eau/roche dans une
moindre mesure (Wunder et al., 2006 ; Millot et al., 2010b).
Les lois thermodynamiques de fractionnement isotopique du lithium lors de la dissolution de
i
au p i ai es f a tio e e t d’ uili e) tie e t o pte des fai les diff e es
1
est le facteur de fractionnement entre les phases A et B, tel que : 10
3x ln
d’ e gies de liaiso e t e les io s des diff e tes asses O’Neil, 1986). Ainsi la rupture de
la liaison du
6Li (haute énergie) est favorable du point de vu énergétique, de telle sorte que
le f a tio e e t isotopi ue d’ uili e a fa o ise l’e i hisse e t elatif de la solutio
en isotope
6Li.
D’aut e pa t, lo s d’e p ie es de dissolutio de e es asalti ues, Ve e
-Carron et al. (2010) ont montré que des lessivages partiels peuvent également produire des
solutions enrichies en
6Li du fait de l’e i hisse e t pa diffusio de et isotope léger dans
les couches externes des verres basaltiques. Toutefois, il a été aussi montré (Pistiner et
Henderson, 2003) par des expériences de dissolution de roches en laboratoire que la
dissolution minérale
o g ue te e se
le pas t e à l’o igi e d’u fractionnement
isotopi ue sig ifi atif ’est à di e esu a le da s la li ite des pe fo a es a al tiques
actuelles, au mieux ± 0.5
‰).
Quoi u’il e soit, la dissolution en tant que mécanisme de f a tio e e t isotopi ue ’est
pas forcément le processus dominant dans les environnements de basse température, où
ses effets sont généralement masqués par des processus postérieurs, comme lors
l’alt atio o ti e tale et la néoformation de i
au d’alt atio Huh et al., 01 ;
Millot et al., 2010a ; Lemarchand et al, 2010).
L’adso ptio su les su fa es i
ales est u des
a is es ajeu s du f a tio e e t
isotopi ue du lithiu da s l’h d osph e. A la te p atu e de la su fa e de la Te e,
l’adso ptio du lithiu su des phases i
ales à pa ti d’u e solution a été mise en
évidence (Taylor et Urey, 1938 ; Anderson et al.,
), ie ue les lois d’adso ptio
prédisent que le lithium doit être adsorbé en faible proportion en comparaison des autres
éléments de la famille des alcalins. La sorption et la rétention des ions en solution dépend
fortement de la chimie des surfaces minérales et de la composition de la solution.
D’aut e pa t, il a t o t e p i e tale e t ue l’a plitude du f a tio e e t de
masse à la désorption est équivalente à celle liée
à l’adso ptio Ta lo et U e , 1938), alors
ue des a al ses d’ ha tillo s atu els o t o t ue e f a tio e e t ’ tait pas
réversible (James et Palmer, 2000
). L’i
e si ilit de e p o essus peut t e att i u e au
fait que du lithium soit incorporé dans des sites cristallographiques structuraux plutôt que
da s des sites ha gea les à la su fa e, sugg a t ue l’a plitude de e f a tio e e t
peut être très différente selon les surfaces minérales considérées.
Le comportement du lithium dissous lo
s de la so ptio d’u e eau de e su des i
au
argileux et des sédiments a été étudié par Zhang et al., (1998). Ces auteurs ont observé un
fractionnement isotopique similaire pour la vermiculite, la kaolinite et des sédiments du
fleuve Mississippi (
~0.978). Pistiner et Henderson (2003) ont également réalisé des
e p ie es su l’effet isotopi ue lo s de la so ptio du lithiu su diff e ts i
au .
Leu s sultats o t e t ue les a tio s de so ptio da s les uelles le lithiu ’est pas
incorporé de manière structurale ne produit pas de fractionnement isotopique. Alors que
leurs expériences montrent que lorsque le lithium est incorporé par des liaisons plus fortes,
un fractionnement isotopique est observé et dépend de la structure chimique des minéraux,
en accord avec les données acquises par Anghel et al. (2002). Le fractionnement le plus
important est mesuré pour la gibbsite avec
~0.986, ce résultat est en accord avec ceux de
3. Mesure des rapports isotopiques du lithium
3.1. Spectrométrie de masse
Les
appo ts isotopi ues d’u l
e t sont mesurés par un spectromètre de masse, où un
fais eau d’ions est produit dans une source sous vide à partir d'un échantillon. Les différents
ions sont séparés selon leur rapport masse/charge par une combinaison de champs
électromagnétiques incluant une accélération/focalisation par un champ électrique et une
séparation en masse par un champ magnétique. Ils sont enfin détectés et exprimés en
fonction de leur abondance relative.
Dans la spectrométrie de masse appliquée aux isotopes du lithium deux grands types sont
utilisés :
1- les spectromètres de masse à source « solide » (TIMS pour Thermo-Ionisation Mass
Spectrometer)
2- les spectromètres de masse à source plasma à couplage inductif et multi-collection
MC-ICP-MS.
Figure 7 - Spectromètre de masse à source solide (TIMS) modèle MAT 262 du brgm. La partie
en premier plan correspond à la source, ensuite nous pouvons ap
e evoi l ai a t au se o d
plan à gauche et enfin le tube et la partie « collection/détection
» à l a i e pla à d oite.
La technique TIMS (Thermo-ionisation Mass Spectrometry, Figure 7), met en jeu la
thermo-io isatthermo-io d’u l
e t da s u e sou e dite « solide » sous ide à des te p atu es
sup ieu es à
°C. L’ ha tillo est d pos sous fo e de t s fi es gouttes su des
laisse un sel sur le filament. Ce filament est chauffé jusqu'à une température suffisante pour
que le sel soit évaporé et que
l’ l
e t soit ionisé.
Figure 8 - Neptune MC-ICP-MS en service au brgm.
Les MC-ICP-MS (Figure 8) utilisent la méthode dite à source plasma des ICP-MS pour la
apo isatio et l’io isatio des ha tillo s oupl e a e la te h i ue de spe t o
t ie de
asse pou la s pa atio des isotopes et la esu e des appo ts isotopi ues. L’ ha tillo
liquide est introduit dans la source du spectromètre sous la forme
d’u a osol où il est
vaporisé et ionisé par un plasma, gaz partiellement ionisé sous l'influence d'une forte
différence de potentiel. Cette méthode, par rapport à la technique TIMS, présente
l'avantage de créer un très bon taux d'ionisation pour un grand nombre d'éléments.
Au préalable à cette mesure isotopique par TIMS ou MC-ICP-MS,
l’ ha tillo su it u e
étape de préparation
: l’ l
e t do t o souhaite esu e la o position isotopique doit
être purifié
, ’est à di e s pa du este de la at i e. Cette tape de p pa atio des
ha tillo s,
essai e pou isole l’ l
e t do t o eut a al se les isotopes, se d oule
dans des salles blanches en surpression, avec des réactifs purifiés permettant une
contamination négligeable.
Les premières mesures isotopiques du lithium ont été réalisées par spectrométrie de masse
à thermo-ionisation (TIMS) dans l
es a
es , à des i eau de p
isio p o he de à ‰
et pour une quantité de lithium de 100 ng à 1000 ng (Chan, 1987 ; Xiao et Beary, 1989). Mais
e ’est ue t s
e
e t, a e le d eloppe e t te h ologi ue des de i es
générations de spectromètres de masse à source plasma et multi-collection (MC-ICP-MS),
que la mesure isotopique a été rendue possible pour des quantités beaucoup plus faibles (20
à g) a e u e p isio eilleu e . à ‰ ; Tomascak et al., 1999b ; Nishio et Nakai,
2002 ; Bryant et al., 2003 ; Millot et al., 2004
). A l’heu e a tuelle, la esu e pa MC-ICP-MS
combine de très nombreux avantages, notamment en ce qui concerne la sensibilité, la
reproductibi
lit ais gale e t la apidit d’a al se.
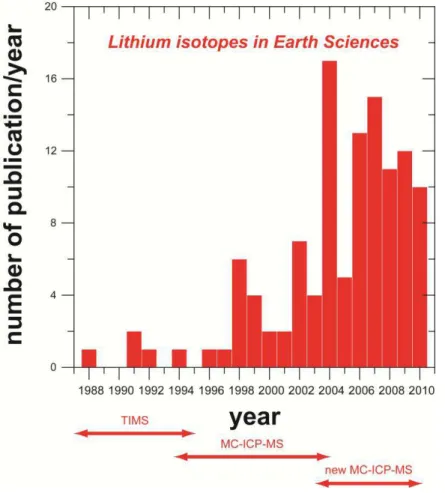
Le lien qui existe entre les développements des méthodes instrumentales et le nombre de
publications dans la thématique du lithium dans les Sciences de la Terre est représenté
graphiquement dans la Figure 9, où sont reportées les publications par année avec en bas les
différentes évolutions dans les techniques de mesures. Cette compilation bibliographique,
bien que datant de 2010, illustre
l’aug e tatio sig ifi ati e des pu li atio s da s le
domaine en relation avec les dernières évolutions de MC-ICP-MS au début des années 2000.
Figure 9 - Nombre de publications scientifiques par année dans la thématique des isotopes du
lithium dans les Sciences de la Terre (étude bibiographique réalisée en 2010).
3.2. Protocole de purification du lithium
Comme déjà dit précédemment, avant la mesure isotopique, nous procédons à une
p pa atio hi i ue de l’ ha tillo de faço à obtenir une quantité purifiée de lithium de
60 ng. Pour les échantillons solides (roches, sédiments, minéraux) une autre étape préalable
à la pu ifi atio est
essai e et o siste e la ise e solutio de l’ ha tillo pa atta ue
acide à chaud (HF, HNO
3HClO
4, HCl).
Un fois en solution, le lithium est donc séparé de sa matrice par chromatographie ionique
sur
si e ha geuse d’io s da s u e salle la he sous hotte à flu la i ai e Figu e ).
Figure 10 - Colonnes en Téflon contenant de la résine cationique, ces colonnes se trouvent
dans une hotte à flux laminaire, elle-même située dans une salle blanche.
L’ tape de pu ifi atio pa h o atog aphie ionique consiste à séparer les éléments
chimiques contenus dans une matrice. Le principe repose sur les équilibres successifs lors de
l’ lutio d’u e solutio da s u e olo e contenant de la résine, ces équilibres sont régis
par les coefficients de partage des différents éléments
e t e la si e et la phase d’ lutio .
La figure 11 illustre le principe de séparation des deux éléments. Les résultats de la
calibration en ce qui concerne les éléments Li et Na sont reportés dans la figure 12 pour une
at i e d’eau de mer. L’e e ple de la pu ifi atio du lithiu de l’eau de e a t hoisi
d’u e pa t pa e ue le appo t Na/Li de l’eau de e est t s i po ta t et d’aut e pa t
parce que les éléments Li et Na possèdent des coefficients de partage relativement proches
pour ce type de résines (les autres cations majeurs Mg
2+, K
+, Ca
2+sont retenus en milieu
acide HCl 0.2
N da s la si e). La s pa atio ua titati e du Li et du Na de l’eau de mer
constitue donc un vrai challenge analytique.
Figure 11 - Schéma de principe de séparation de deux éléments par chromatographie
ionique.
Figure 12 -
Cou es d lutio du lithiu et du sodium en milieu acide HCl 0.2N pour une
matrice eau de mer. Seule la fraction comprise entre 10 et 35 mL est collectée (flèche rouge)
et contient uniquement le lithium.
A ote la diff e e d helle significative entre le lithium
et le sodium.
100%. Dans la figure 13, le rapport isotopique
7Li/
6Li est reporté en fonction du pourcentage
de Li élué. Ce graphique illustre bien la différence qui existe
au ou s de l’ lutio : le
6Li et le
7
Li présentent un comportement légèrement différent (le
6Li est fixé de manière plus
efficace du fait de la différence de masse).
Figure 13 - Evolution de la composition isotopique du lithium au ou s de l lutio su si e
ha geuse d io s d ap s Tomascak, 2004).
Au cours des développements analytiques que nous avons réalisés, nous avons testé
l
’a se e de f a tio e e t lo s de l’a al se répétée de solutions de référence de Li (après
purification). De plus, nous avons également évalué notre reproductibilité totale externe par
la mesure répétée du stand
a d d’eau de e I‘MM BC‘-403 après purification chimique
(
7Li = + . ± . ‰,
, n = 31, Millot et al., 2004). La figure 14 montre les données
o pil es da s la litt atu e pou l’eau de e a tuelle, sa ha t ue la o positio
isotopi ue du lithiu de l’o a est ho og e Huh et al.,
). La reproductibilité que
ous o te o s est de ± . ‰
).
Le standard de roche JB-2 a également été analysé après la mise en solution de ce basalte
par attaque acide et la purification du lithium de sa matrice. Nous obtenons la valeur
moyenne de
7Li = + . ‰ ± .
n = 17), qui est en très bon accord avec les données
publiées dans la littérature (voir une compilation des données dans Tomascak 2004).
D’aut e pa t, da s le ad e d’u e collaboration avec le Centre de Recherches
Pétrographiques et Géochimiques de Nancy (CRPG) qui a synthétisé 3 solutions standards
(Li6-N, LiCl-N et Li7-N) qui couvre une très large gamme de variations isotopiques du lithium
(de -
à + ‰), nous avons pu tester la justesse de notre mesure (Carignan et al., 2007 ;
Figure 15) sur deux instruments différents
: espe ti e e t l’I“OP‘OBE à Na
et le
NEPTUNE à Orléans.
Figure 14 -
Co pilatio des esu es de la o positio isotopi ue de l eau de e pa TIMS
(en bleu) et MC-ICP-MS (en rouge). Nos valeurs sont reportées à droite de la figure (Millot et
al., 2004).
Figure 15 - Comparaison entre les valeurs obtenues à Nancy (axe des Y) et au BRGM (axe des
X) lors de la mesure de 3 solutions standards Li6-N, LiCl-N et Li7-N (Carignan et al., 2007). A
3.3. Acquisition de données et corrections
Le iais de asse i st u e tal ui se p oduit da s la sou e plas a de l’i st u e t sulte
de l’e t a tio et de la transmission préférentielle des ions les plus lourds dans la source ICP
(Figure 16).
Figure 16 - Schéma et photographie de la source ICP du Neptune. Successivement de gauche
à droite : le lithium est
tout d a o d ionisé dans le plasma, les ions sont ensuite extraits par
une différence de potentiels de 2000 V, puis ce faisceau est accélerré (5000 V) et focalisé à la
fois da s les di e sio s de l espa e X-Y-Z) mais aussi en énergie par un filtre
électrostatique.
Afin de corriger de ce biais de masse instrumental et de sa dérive au cours du temps, la
mesure de la composition isotopique se fait selon la méthode dite de «
standard-bracketing » en normalisant au standard L-SVEC (NIST, RM8545). Chaque mesure isotopique
(échantillon et standard L-SVEC) est également corrigée du « blanc » qui correspond au
ilieu d’i t odu tio o te a t l’ ha tillo HNO
33%) et au bruit de fond instrumental. Le
principe est décrit dans la figure 17
, où l’o alterne successivement un standard, un
échantillon, un standard etc.
La mesure des isotopes du lithium se fait en mode « plasma chaud » (1200W) et le système
d’i t odu tio utilis est le “I“ “ta le I t odu tio “ st
e) ui est o stitu d’u e dou le
chambre de nébulisation (cyclonique + type Scott) associée à un micro-nébuliseur en Téflon
PFA (Figure 18).
U e fois l’ ha tillo li uide i t oduit da s la sou e sous la fo e d’u a osol, le lithiu
est ionisé dans le plasma (partie ICP : Inductively Coupled Plasma, Figure 19). Le faisceau
d’io s ai si
est a
l
puis fo alis pa u s st
e o pos de le tilles et de pla ues
de focalisation.
Figure 17 - Principe du standard-bracketing et de la correction des blancs. Le schéma du bas
o t e l volutio au cours du temps du rapport isotopique pou le sta da d et l ha tillo
ai si ue le p i ipe d interpolation pour le calcul du delta.
La partie princip
ale du spe t o
t e de asse est l’ai a t pa tie MS : Mass Spectrometry,
Figu e ). E effet, ’est da s ette pa tie ue les t aje toi es des pa ti ules ha g es o t
être séparées en fonction de leur masse.
Figure 19 - Schéma de fonctionnement du MC-ICP-MS Neptune.
Enfin, dans la partie MC (Multi Collection) les faisceaux
d’io s pou les isotopes et du
lithium sont mesurés en multi-collection statique sur les cages de Faraday les plus éloignées
(L4 et H4, Figue 20) après amplification du signal.
La esu e se fait lo s de l’a uisitio des sig au su les asses et pendant 15 scans de
se o des de te ps d’i t g atio . La esu e au total du e do i utes, au uels il
faut ajouter 1 minute 30 «
d’uptake » pou pe ett e à la solutio d’a i e et au sig al de
se stabiliser. Avec la configuration telle que décrite précédemment, nous obtenons des
signaux proches de 2V et 0.1V respectivement pour les masses 7 et 6 du lithium (Figure 20).
La statisti ue de esu e ous do e u e e eu i te e de l’o d e de . à . ‰
m). Lors
de la esu e, e i o
µL d’u e solution à 30 ng/mL sont consommés, ce qui correspond
à une quantité totale de 15 ng du lithium.
E fi , le la ilieu d’i t odu tio de l’ ha tillo ) est faible, de l’o d e de uel ues V
sur la masse 7 du lithium, ce qui correspond à moins de 0.2% du sign
al de l’ ha tillo . U
rinçage en milieu HNO
33% pendant 5 minutes entre chaque mesure est suffisant pour un
Figure 20 - Configuration pour la mesure des isotopes du lithium sur les cages L4 et H4. Les
spectres de masse pour les masses 6 et 7 sont donné
s pou la esu e d u e solutio sta da d
de 30 ng/mL de lithium.
Pour conclure en ce qui concerne la mesure des isotopes du lithium par MC-ICP-MS, nous
retiendrons que :
La méthode de mesure des isotopes du lithium sur Neptune MC-ICP-MS est
relativement rapide et très sensible : 15 ng de lithium suffisent pour la mesure de la
composition isotopique.
Cette esu e e uie t des glages fi s de l’i strument et
u e o e validatio de l’e se
le de la hai e a al ti ue.
Au préalable à la mesure, une étape de purification du lithium est nécessaire. Lors
de ette tape, il faut s’assu e du e de e t de
%, de l’absence de
f a tio e e t et de l’absence de contamination soit par les réactifs soit par
l’op ateu . Au ou s de la p pa atio de l’ ha tillo , l’appo t e lithiu li au
réactifs utilisés et à la manipulation est totalement négligeable. Aucune correction
de la de hi ie ’est donc apportée. Toutefois des mesures de blancs de chimie
et des réactifs sont réalisées périodiquement pour contrôler leurs niveaux et leurs
reproductibilités.
Le protocole a été validé par la mesure répétée sur le long terme de différentes
d’ ha tillo s atu els après pu ifi atio est de ± .5‰
, 2 standard déviation)
(Millot et al., 2004).
D s lo s, l’i e titude a al ti ue att i uée à chaque
détermination de
7Li est do de ± .5‰
), elle correspond à la reproductibilité
totale externe du protocole.
4.
E e ples d’applications : synthèse des
principaux résultats
4.1. Eaux météoriques (Millot et al., 2010
2
)
Dans cette étude, nous reportons pour la première fois la composition isotopiq
ue d’eau de
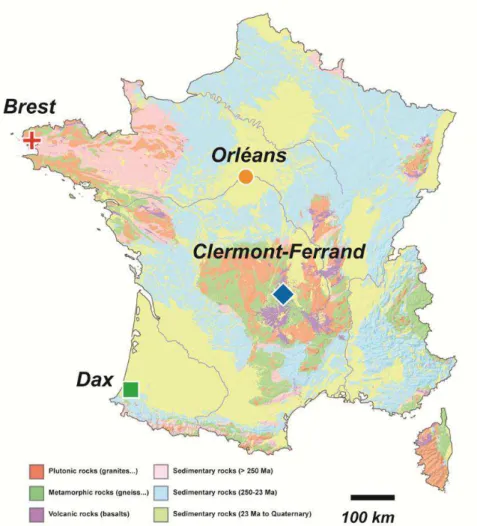
pluies. Nous avons réalisé le suivi mensuel de 4 sites en France
tout au lo g d’une année à la
fois pour
des statio s p o hes de l’océan (Brest, Dax) et des stations plus continentales
(Orléans, Clermont-Ferrand ; Figure 21).
Figure 21 - Carte de localisation des sites de suivi des eaux de pluies sur fond de carte
géologique (Millot et al., 2010c).
L’o je tif de e t a ail tait de o t ai d e l’o igi e du lithiu da s les eau de pluie pa u e
approche isotopique en étudiant les variations spatio-temporelles des eaux météoriques à
l’échelle de la France au ou s d’un suivi annuel. Un autre objectif de ce travail visait
gale e t à o t ai d e l’appo t des eau
t o i ues au eau de su fa e e te e de
2