Adaptation de l’activité nerveuse sympathique dirigée vers la peau à la suite d’une période d’acclimatation à la chaleur chez de jeunes adultes sains
Texte intégral
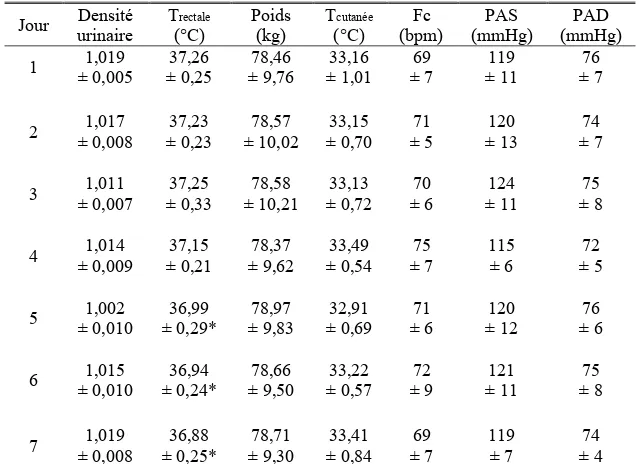
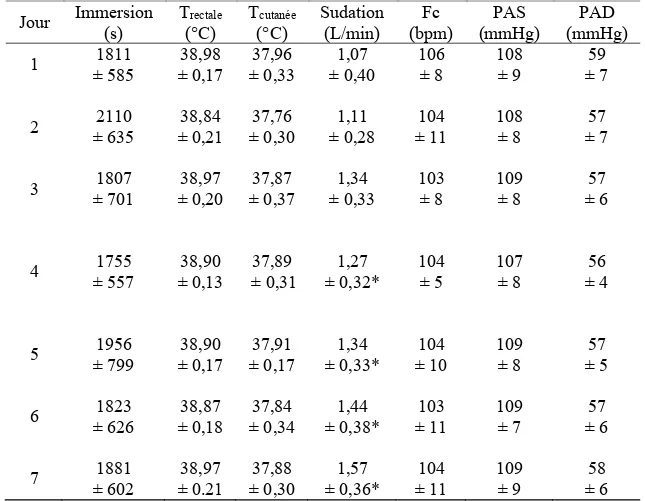
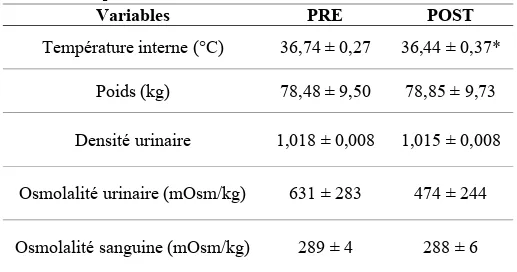
Figure

Documents relatifs
• Les nutriments sont utilisés dans les réactions du métabolisme pour produire de l’énergie, en particulier grâce à la respiration cellulaire, mais aussi par la
En pratique, l’évolution spontanée de l‘angiostrongylose nerveuse est habituellement bénigne chez l’adulte avec une résolution en 4 à 6 semaines; elle peut être grave
[r]
(a) Donner les coordonnées de quatre points de cette droite, qu’ont-elles de particulier.. (b) D’autres points de cette droite ont-ils la
Si il est nécessaire dʼy répondre par un mouvement, un autre ensemble de neurones va fabriquer un nouveau message nerveux, à rôle moteur, qui va être envoyé dans la
Parmi les paramètres influençant la valeur de la conductance, certains dépendant de la solution ionique et d’autres de la cellule de mesure ; classer les
une tache brun-clair aux frontières tourmentées sur sa peau un duvet se redresse soyeux quand de l’auriculaire j’en trace les contours La surface effl eurée de la pulpe
Le fond d’œil retrouve un œdème papillaire important, une hyalite cotée à 1+ et des taches jaunâtres péripapillaires (nodules de Dalen-Fuchs) [figure 2].. L’angiographie à
