République Algérienne Démocratique et Populaire
Ministère de l’Enseignement Supérieur et de la Recherche Scientifique Université Mohammed Seddik BenYahia
Filière : Science et génie de l’Environnement Département du génie des procédés
Mémoire de
En vue de l’obtention du diplôme :
Option :
Membres de Jury
Président : Djamaa Noureddine Nafa Samira
Examinateur : Chabou Nadjet
Encadrant : Boussetoua
Année Universitaire 201
Caractérisation des eaux d’irrigation
destinées à l’agriculture dans le périmètre de
République Algérienne Démocratique et Populaire
Ministère de l’Enseignement Supérieur et de la Recherche Scientifique Université Mohammed Seddik BenYahia-Jijel
Filière : Science et génie de l’Environnement Département du génie des procédés
Mémoire de fin d’études
En vue de l’obtention du diplôme : Master : Génie des procèdes de l’Environnement
Thème
Présenté par :
: Djamaa Noureddine Nafa Samira
: Chabou Nadjet Hamrouche Ahlam
: Boussetoua Hocine
Année Universitaire 2018-2019
Caractérisation des eaux d’irrigation
destinées à l’agriculture dans le périmètre de
Jijel-Taher
Ministère de l’Enseignement Supérieur et de la Recherche Scientifique
Présenté par :
: Djamaa Noureddine Nafa Samira
amrouche Ahlam
Caractérisation des eaux d’irrigation
destinées à l’agriculture dans le périmètre de
ﻢﺴﺑ
ﻢﺴﺑ
ﻢﺴﺑ
ﻢﺴﺑ
ﻢﻴﺣﺮﻟا ﻦﻤﺣﺮﻟا ﷲا
ﻢﻴﺣﺮﻟا ﻦﻤﺣﺮﻟا ﷲا
ﻢﻴﺣﺮﻟا ﻦﻤﺣﺮﻟا ﷲا
ﻢﻴﺣﺮﻟا ﻦﻤﺣﺮﻟا ﷲا
ﻰﻟﺎﻌﺗ ﷲا لﺎـﻗ
"
ٍءْﻲَﺷ ﻞُﻛ ِءﺎَﻤْﻟا َﻦِﻣ ﺎَـﻨْﻠَﻌَﺟَو
َنﻮُﻨِﻣْﺆُﻳ َﻼَـﻓَأ ﻲَﺣ
"
)
ﺔﻳﻵا ءﺎﻴﺒﻧﻷا ةرﻮﺳ
30
(
ﷲا لﺎـﻗ
ﻰﻟﺎﻌﺗ
"
َﻦِﻣ َلَﺰْﻧَأ يِﺬﻟا َﻮُﻫ
ِﻪﻴِﻓ ٌﺮَﺠَﺷ ُﻪْﻨِﻣَو ٌباَﺮَﺷ ُﻪْﻨِﻣ ْﻢُﻜَﻟ ًءﺎَﻣ ِءﺎَﻤﺴﻟا
َنﻮُﻤﻴِﺴُﺗ
"
))))
ﺔﻳﻵا ﻞﺤﻨﻟا ةرﻮﺳ
ﺔﻳﻵا ﻞﺤﻨﻟا ةرﻮﺳ
ﺔﻳﻵا ﻞﺤﻨﻟا ةرﻮﺳ
ﺔﻳﻵا ﻞﺤﻨﻟا ةرﻮﺳ
10
10
10
10
((((
ﷲا لﺎـﻗ
ﻰﻟﺎﻌﺗ
"
َلَﺰْﻧَأَو
َﻦِﻣ
ِءﺎَﻤﺴﻟا
ًءﺎَﻣ
َجَﺮْﺧَﺄَـﻓ
َﻦِﻣ ِﻪِﺑ
ِتاَﺮَﻤﺜﻟا
ﺎًـﻗْزِر
ﻢُﻜَﻟ
"
))))
ةرﻮﺳ
ةرﻮﺳ
ةرﻮﺳ
ةرﻮﺳ
ةﺮﻘﺒﻟا
ةﺮﻘﺒﻟا
ةﺮﻘﺒﻟا
ةﺮﻘﺒﻟا
ﺔﻳﻵا
ﺔﻳﻵا
ﺔﻳﻵا
ﺔﻳﻵا
22
22
22
22
((((
Remerciements
Louange à Allah, le miséricordieux, sans lui rien de tout cela
n’aurait pu être, je remercie le bon Dieu qui nous a orienté au chemin de
savoir et les portes de la science.
Nous tenons à adresse nos plus vifs Remerciements à : Monsieur
Boussetoua Hocine. Pour nous avoir encadré, guidé et prodigué tout
l’aide nécessaire pour la réalisation de notre travail.
Nous Remerciements vont aussi aux membres de jury de nous avoir
fait lhonneur de bien vouloir participer au jury de ce mémoire et pour
toute lattention qu’ils vont prété à l’valuation de notre travail.
Nous tenons remercier aussi tout les enseignants du département du
génie des procédés de l’université de Mohamed Seddik Benyahia - Jijel.
Et enfin, Nous tenons à remercier toute personne qui nous a aidé ou
encouragé de prés ou de loin à la réalisation de ce mémoire.
Dédicace
Au nom d’Allah, le Tout Miséricordieux, le Très Miséricordieux
Tout d’abord je tiens à remercier le tout puissant de m’avoir donné
l e courage et la patience pour arriver à ce stade afin de réaliser ce
travail que je dédie :
A ma très chère mère Malika, qui n’a jamais cessé de prier
pour moi A mon très cher père Abdelhamid, pour ses
encouragements son soutien, surtout pour son amour et son
sacrifice afin que rien n’entrave le déroulement de mes études.
À mes chers frères Abdel-Ali et Abdel-Haq:
Mes chers frères, présents à chaque instant, je teste avec leur
soutien moral et leurs surprises agréables. Je vous souhaite un
avenir plein de joie, de bonheur, de réussite et de sérénité.
Mes soeurs: nabila , amel et karima , et leurs maris.
Et à tous les membres de ma famille, jeunes et vieux.
A tous ceux que j’ai connus, et qui reconnaitrons. A tous ceux
que j’aime et ceux qui m’aiment.
Dédicace
Je dédie ce moodete travail à :
mon très chére pére Youcef : lui qui a instauré
l’intérêt pour moi d’aller a la recherche de la connaiance.
La lumiere de me yeux :
Ma très chére mére , Hamama , ma premier
Enseignant , qui m’a soutenu toujours par son
amour sa
compréhension et son encouragement , qu’elle
trouve ici l’expression de ma vive reconnaissance
mes très chéres sœurs : Hasina,Houda,Karima ,Affaf
mes très chéres fréres :Abd elhakim ,Ali Khaled Imad
et Houssem eddine
a mon fiancé : Salah
tous les membres de la famille petits et grands
a mes meilleurs amis
l’ensemble des étudiants de la promotion M2 de l’année
2018/2019
tous ceux que j’aime et que m’aiment
Résume :
La région Taher –Jijel constitue un périmétre ou l’activité agricole se considére l’activité principale de la population . Certes d éveloppement de cette activité est limité par la sévérité du climat , la dégradation de la qualité des eaux d’irrigation . les agriculteurs de
Cette région utilisent n’importe quelle eau se trouvant à coté de ses terres pour
irriguer leur culture : les eaux des pluits , les eaux des oueds et les eaux des barrages , sans savoir est ce que ces eaux sont dans les normes ou non .
C’est dans ce contexte que nous avons choisi de travailler . l’objectif principal de ce travail est de caractériser cinq types des eaux , trois oueds à savoir : oued Djendjen , oued Nil et oued Saayoud , eau d’un puit situé à el Mzair et l’eau du barrage d’El agram , en terme de ses propriétes physique (pH,temperature) et chimiques (cations et ions …) . les résultats montrent que les eaux du barrage d’El agram respectent les normes internationales pour l’irrigation , tandis que les eaux des Oueds sont inadmissibles , parceque les pourcentage trouvées surtout pour le calcium dépassent les limites pour les périodes sans pluie .pour la période d’hier , on peut recommander d’utiliser les eaux des Oueds pour l’irrigation ou la turbidité est faible .
Table des matiére
Remerciement Dédicaces Résumé Sommaire Liste de tableaux Liste de figures Liste deabréviations Introduction généraleChapitre 1 : Recherche bibliographique
1.1. Introduction………... .. ……...1 1.2. Définition... …….. …….….1 1.3. Le cycle de l’eau... ………….….. 1 1.3.1. Compositions du cycle... ……….2 1.3.1.1. Les précipitations... …….. 2 1.3.1.2. Les ruissellements... …….. 2 1.3.1.3. L’infiltration... …..….. 3 1.3.1.4. L’évapotranspiration... …..….. 3
1.4. Les ressources en eau…... ... ……...3
1.4.1. Les différents types d’eau... …….. ……….3
a. Les eaux de pluie... ……….. 3
b. L’eau de mer... ……….3
c. Les eaux de surface... …….. 3
d. Les eaux souterraines... …….. 3
1.5. L’usage de l’eau ………... .. ….…...4
1.5.1. L’usage domestique... …….. ……….4
1.5.2. Les besoins agricoles... ……….. 4
1.5.4. Usage pour l’urbanisation... …….. 4
1.5.5. Cause de rareté de l’eau... ……..…….. 4
1.5.5.1. La surexploitation... …..….. 5
1.5.5.2. La pollution... …..….. 5
1.5.5.3. Les mauvaises techniques d’irrigation... ..…..….. 5
1.6. Analyse physico-chimique………...……...5 1.6.1. Paramètre physique... …….. ……….5 La température...……….. 5 pH... ……….5 1.6.2. Paramètres chimiques... …….. 6 La conductivité... …….. 6 Carbonates et bicarbonates...…..….. 6 Chlorure (Cl-)... ...….. 6 La dureté…... ………..……...6
La dureté calcique (THCa)... ...….. 6
La dureté magnésienne (TH Mg)………...……....6
Les sulfates...…….. ……….7
nitrates... ………...……….. 7
Ammonium... 7
ortho phosphates...…….. 7
1.7 Qualité de l'eau d'irrigation...…….. 8
1.8 Les normes de qualité des eaux destinées à l’irrigation...…..….. 8
Chapitre 2: présentation de la région d’étude 2.1. Introduction………... .. ……...10
2.2. Présentation de la région... …….. …….….10
2.3. Site et situation géographique de la commune Taher... ...….….. 10
La population... ………….…….. 11
2.5. Economie... …….. 11
2.6. La géologie... …..….. 11
2.7. Le Climat... 12
2.7.1 Etude des paramètres climatiques…... ... ……...12
Les précipitations... …….. ……….12 La température de l’air... 12 2.8. Hydrologie... ……….12 Oued Nil... …….. 13 Oued Djendjen... …….. 14 Oued Sayoud………... .. ….…...14
Barrage d’El Agrem... …….. ……….16
Puit El Mezaïr... ……….. 16
Chapitre 3 Matériels et Méthodes
3.1. Introduction………... .. ……...173.2. Technique d’échantillonnage des eaux... …….. …….….17
3.3. Mode de prélèvement des échantillons... ………….….. 17
3.4. Nettoyage de la verrerie... ……….18
3.5. Mesures des paramètres physico-chimiques... 19
3.5.1. Les paramètres physiques (mesure in situ)... 19
3.5.2. Les éléments chimiques (analyses au laboratoire)...…..….. 19
Résultats et discussion
4.1. Résultats... …..….. 294.1.1 Paramètre physique globaux mesurés « in situ » …... ……...29
PH... …….. 29
Température... 30
Conductivité électrique... ….. 31 Elément chimique... …….. 33 Calcium (Ca2+)………... .. ….…...34 Magnésium (Mg2+)...….. …….…….34 Chlorures (Cl-)... ……….. 36 Ammonium (NH4+)... 36 Carbonates (CO3-2)... ………...…….. 37 Bicarbonates (HCO3-) :... ………...…..…….. 38 Sulfates (SO4-2)………... ... ….…...38 Nitrates (NO3-)... ……….39 phosphates (PO4-3)... ………...……….. 40 Conclusion générale Référence bibliographique Annexes
Liste de figures
Figure 1.1. Le cycle d’eau 2
Figure 2.1. Carte de situation géographique de la région de Taher 10
Figure 2.2. Situation hydrologique 13
Figure 2.3. Photo prised’un point sur l’oued Nil 13
Figure 2.4. Photo prised’un point sur l’oued Djendjen 14
Figure 2.5. Photo prised’un point sur l’oued Sayoud 15
Figure 2.6. Situation d’oued Sayoud par rapport aux autres oueds 15
Figure 3.1. Carte présentative des sites de prélèvement 18
Figure 3.2.: Multi paramètre manuel (Hanna 98129) 19
Figure 3.3. La titrimétrie pour les mesures au laboratoire 20
Figure 3.4. Mesure de la conductivité de l’eau 21
Figure 3.5: Différentes étapes pour le titrage de la dureté total(TH) 22
Figure 3.6: Différentes étapes pour le titrage du Chlorure 24
Figure 3.7. Le spectrophotomètre (UV 1600 PC) 25
Figure 4-1:Evolution de PH en fonction du temps 30
Figure 4-2: Variations des températures en fonction du temps 30
Figure 4-3:évolution de la conductivité électrique en fonction du temps 32
Figure 4.4 : la concentration de calcium en fonction du temps en mg/l 34
figure 4.5:concentration de magnésium en fonction du temps 35
Figure 4.6: concentration des chlorures en fonction du temps 36
Figure 4.7: évolution de l'ammonium en fonction du temps 37
Figure 4.8: concentration des carbonates en fonction du temps 37
Figure 4.10 : concentration des sulfates en fonction du temps 39
Figure 4.11:concentration des nitrates en fonction du temps 40
Liste de tableaux
Tableau 1.1. Les normes de qualités de l'eau d'irrigation (Directive de l’OMS 2002) 9 Tableau 1.2. Barème de qualité pour les eaux d'irrigation proposée par la FAO 9 Tableau. 2.1. Répartition de la population et la densité 2008 de la zone d’étude 11 Tableau 4 1- Résultats physiques des paramètres globaux mesurés ‘’in situ’’ 29 Tableau 4-2 : Conductivité électrique des eaux de la région de Taher 31
Tableau 4-3 : Risque de salinité des eaux d’irrigation en fonctions de la conductivité électrique 32 Tableau 4.4- Résultats chimiques exprimés en mg/l 33
ABREVIATIONS
% Pourcentage.
Ag Cl Chlorure d’Argent AgNO3 Nitrates d’argents.
ANIREF Agence national d’intermédiation et de régulation fonciére BA barrage de l'Agram
°C Degré Celsius.
CE Conductivité électrique Cm3 Centimètre cube
DHW Direction d’Hydraulique de la Wilaya.
E Est
E.D.T. A Acide Ethylène Diamine Tétraacétique FAO Food and Agriculture Organisation
g gramme
hab. Habitants
hab./km2 Habitants par kilomètre carré HCl Acide chlorhydrique
H2SO4 Acide sulfurique
km2 Kilomètre carré
K2CrO4 Chromate de potassium
m mètre
m3 mètre cube
mg milligramme
ml millilitre
mg/l milligramme par litre. Mm3/an Million mètre cube par an. ms/cm milicimens par centimètre MNT Modèle Numérique du Terrain.
N Nr
N Nord
Na Cl Chlore de sodium. NaOH Hydroxyde de sodium NET Noir ériochrome T
O Ouest
OMS Organisation mondiale de la santé
O D Oued Djendjen
O N Oued Nil
O S oued Saayoud
pH potentiel d’hydrogène P M Puits de l'Mzair
RPGH Recensement général de la population et de l’Habitat
S Sud T Température TH Dureté THt Dureté total THca Dureté calcique THMg Dureté magnésienne THp Dureté permanente UV Ultraviolet
µs/cm micro-siémens par centimètre.
Abréviation des éléments chimiques
Ca+2 : Calcium, Mg+2 : magnésium, Cl-: Chlorure, HCO3-: Bicarbonates, NH4+ : Ammonium,
Introduction général
Introduction général
L’agriculture, de façon générale, est l’un des secteurs les plus consommateurs d’eau, qui dans les conditions arides et semi arides, vient souvent à manquer. Pour pallier à cet inconvénient, le meilleur moyen que les hommes aient trouvé jusqu’ici a été un appoint d’eau, à l’aide de procédés divers. C’est ce complément d’eau que l’on appelle irrigation[1].
Mais, il arrive que la qualité de l’eau exigée ne soit pas toujours disponible. Dans le but de sauver voire d’améliorer leurs rendements, les exploitants agricoles se trouvent contraints à recourir à différentes sources d’eaux pour l’arrosage de leurs cultures. Il se trouve que sur certains sites, ils sont contraints d’utiliser des eaux usées non traitées, pouvant provenir via les oueds aussi bien des ménages que des industries[1].
Ces eaux d’oued, qui constituent une ressource importante, engendrent cependant des nuisances dans les milieux récepteurs et des risques sanitaires pour les populations qui sont en contact permanent ou consommant les produits agricoles irrigués avec ces eaux. Pour se prémunir de ces risques, le législateur a, selon le principe de précaution, décrété des normes de qualité pour toute sorte d’eau destinée à l’irrigation [1].
Les ressources hydriques de l'Algérie sont limitées, et dépendent essentiellement de l'apport du ciel. Cette situation s'explique d'une part, par une pluviométrie précaire, irrégulière et mal répartie, et d'autre part, par la croissance démographique et ses aléas sur l'accroissement des besoins et la pollution de la ressource. Dans ce cadre interviennent les études hydrologiques des bassins versants pour appréhender le fonctionnement du processus de création de ruissèlement en fonction de la pluviométrie et d’identifier quantitativement et qualitativement la ressource pour l’exploiter à bon escient [2].
La wilaya de Jijel est caractérisée par une abondance en eau souterraines où la capacité ésotérique est de 73.8 Mm3/an (DHW). Ces eaux sont utilisées pour l’alimentation en eau potable de plusieurs communes de la wilaya et pour l’irrigation [3]. Mais plusieurs agriculteurs n’ont pas les moyens pour faire des puits et l’utiliser comme source de l’eau pour irriguer leur terre, surtout en été où l’évaporation augmente. Certains d’entre eux sont contraints d’utiliser des eaux non traitées
Introduction général
provenant des oueds. Les autorités locales de la willaya de Jijel ont fait recours pour résoudre ce problème à installer un réseau d’eau pour l’irrigation provenant directement du barrage d’El Agram situé à Chadia commune de Kaouas. Donc d’après notre enquête sur terrain trois types d’eau sont utilisées pour l’irrigation dans le périmètre Taher- Jijel : eau des puits, eau des oueds et eau du barrage.
Notre objectif principal dans ce travail est de donner des informations sur la qualité de ces eaux utilisées pour l’irrigation en leur faisant une caractérisation physico-chimique. Parmi les sous objectifs de ce travail on trouve la comparaison entre ces eaux et est-ce que ces eaux répondent aux normes internationales.
Dans ce manuscrit, le chapitre 1 est une recherche bibliographique. Après avoir présenté une définition de l’eau et l’état de l’eau trouvant dans la nature, nous décrivons les différentes ressources d’eau et leur usage dans la vie quotidienne de l’être humain. Le dernier paragraphe de ce chapitre est consacré à l’eau destinée à l’irrigation en donnant différentes normes existants de la qualité de cette eau.
Dans le chapitre 2 nous présentons la zone d’étude de point de vue : géographique, hydrologie, géologie, géomorphologie et socio-économie.
Le chapitre 3 décrit la technique utilisée pour la préparation des échantillons, il présente également le mode opératoire et le protocole des essais.
L’ensemble des résultats obtenus des analyses effectués et les propriétés physico chiques des eaux d’irrigation étudiées sont présentées dans le chapitre 4. La
discussion et l’interprétation de ces résultats sont données également à la fin de ce chapitre. Nous terminerons ce mémoire par une conclusion générale et des
Chapitre 1 : Recherche bibliographique
1
1.1.
Introduction :L’eau est un élément constitutif fondamental de la vie [4]. C’est pourquoi elle mérite une attention toute particulière, dans la mesure où elle est très menacée par les activités humaines, quotidiennes notamment domestique, industrielles et agricoles ce qui la rend un élément récepteur exposé à tous les genres de pollution [5].
1.2.
Définition:L’eau est une matière très importante pour la survie des êtres vivants. C’est un composé incolore, inodore, insipide et liquide à température ordinaire C’est un corps composé résultant de la combinaison de deux atomes d’hydrogène et un atome d’oxygène de formule H2O. Elle bout à
la température de 100°C. 1 cm3 à 4°C pèse sensiblement 1g [6].
1.3.
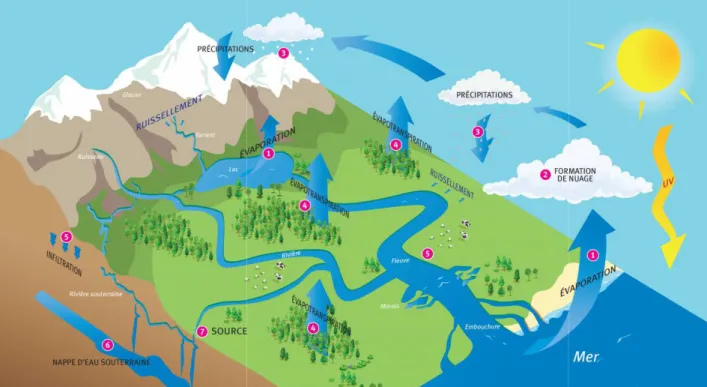
Le cycle de l’eau :On appelle la circulation naturelle d'eau sur la planète le cycle hydrologique [7]. L'eau est évaporée par le soleil, incorporée aux nuages comme vapeur d'eau, tombe sur la terre et sur les étendues d’eaux sous forme de pluie, à partir de la terre elle retourne de nouveau aux ressources d'eaux dans le cycle hydrologique [7]. Tout d’abord, cette notion de cycle est une notion dynamique, elle implique un mouvement et des échanges entre différents réservoirs, de plus son essence cyclique nous ne permet pas de définir son commencement ni sa fin [8]. Six composants principaux du cycle hydrologique : les précipitations, l’infiltration, l’évaporation, les eaux de surface, la transpiration et écoulement des eaux souterraines [7].
Chapitre 1 : Recherche bibliographique
L'évaporation à la surface et la transpiration des végétaux ont un rôle majeur dans le de l'eau ; ces deux phénomènes sont pris en compte dans le seul terme
L'eau qui arrive à la surface d'un sol se trouve à la pression atmosphérique, cette eau à s'infiltrer sous l'effet de la gravitation dans le cas d'un sol saturé ou par
potentiel matriciel pour un sol non saturé [
présente. Il se forme alors un front d'infiltration qui progresse au limité par la filtrabilité du milieu qui dépend de la
état hydrique [9].
1.3.1. Compositions du cycle : 1.3.1.1. Les précipitations
Les précipitations constituent presque toutes nos réserves en eau douce elles sont d’une région à l’autre suivant le climat et le relief [
1.3.1.2. Les ruissellements
Parvenue sur le sol, une partie des précipitations s’écoulent à sa surface vers le hydrographique et les étendues d’eau libre [
Chapitre 1 : Recherche bibliographique
2
Figure 1.1. Le cycle d’eau
L'évaporation à la surface et la transpiration des végétaux ont un rôle majeur dans le de l'eau ; ces deux phénomènes sont pris en compte dans le seul terme d’évapotranspiration [
qui arrive à la surface d'un sol se trouve à la pression atmosphérique, cette eau
à s'infiltrer sous l'effet de la gravitation dans le cas d'un sol saturé ou par effet du gradient de potentiel matriciel pour un sol non saturé [10]. L'eau pénètre dans le sol et
Il se forme alors un front d'infiltration qui progresse au fil du temps. Le flux infiltré est limité par la filtrabilité du milieu qui dépend de la conductivité hydraulique du milieu et de son
:
Les précipitations constituent presque toutes nos réserves en eau douce elles sont d’une région à l’autre suivant le climat et le relief [11].
partie des précipitations s’écoulent à sa surface vers le hydrographique et les étendues d’eau libre [11].
Chapitre 1 : Recherche bibliographique
L'évaporation à la surface et la transpiration des végétaux ont un rôle majeur dans le cycle d’évapotranspiration [9]. qui arrive à la surface d'un sol se trouve à la pression atmosphérique, cette eau tend toujours
effet du gradient de sol et pousse l'eau déjà fil du temps. Le flux infiltré est conductivité hydraulique du milieu et de son
Les précipitations constituent presque toutes nos réserves en eau douce elles sont variables
Chapitre 1 : Recherche bibliographique
3
1.3.1.3. L’infiltration
Une partie des précipitations pénètre dans le sol et dans le sous-sol, aliments les réseaux souterrains constituant le stock d’eau du sol et les réserves des nappes aquifères [11].
1.3.1.4. L’évapotranspiration
C’est la somme des pertes par transformation de l’eau en vapeur. On distingue deux composantes :
L’une constituée par le retour direct de l’eau dans l’atmosphère. L’autre constituée par la transpiration des plantes [11].
1.4.
Les ressources en eau :L’eau sur toutes les formes est abondante sur terre, en effet : elle représente 1380 millions de kilomètre cubes. La majorité est constituée d’eau de mer 92.7%, la glace qui représente 2.15% est inutilisable directement, et enfin l’eau douce dont la disponibilité est sous forme de : lacs, fleuves, eau souterraine, elle se représente que 0.7% de la ressource totale. L’origine des eaux servant à l’alimentation humaine provient des eaux souterraines, les eaux douces de surface c'est-à-dire celle des ruisseaux, des rivières, des fleuves, des barrages, ou dans certains cas, par adoucissement des eaux de mer [12].
1.4.1. Les différents types d’eau a. Les eaux de pluie
Les eaux de pluie peuvent être considérées comme les eaux naturelles les plus pures. Elles Renferment des particules, des poussières et des gaz dissous. Les eaux de pluie peuvent être Contaminées par des poussières atmosphériques [13].
b. L’eau de mer
Elle constitue la majeure partie des réserves d’eau du globe. Cependant à cause de son forte salinité, on l’utilise rarement pour produire de l’eau potable. La mer aussi n’échappe pas à la Pollution [13].
c. Les eaux de surface
Les eaux continentales de surface, des lacs et des cours d’eau sont alimentées par des eaux de pluie, de ruissellement et par les eaux souterraines resurgissant. Trop souvent, elles reçoivent des eaux usées ou fortement polluées [13].
d. Les eaux souterraines
Les eaux souterraines sont souvent plus stable et de meilleure qualité que les eaux de surface. Certaines de ces eaux sont très riches en sels minéraux et renferment fréquemment du fer.
Chapitre 1 : Recherche bibliographique
4
Les eaux souterraines modèlent les terrains calcaires d'une façon bien particulière: les eaux de pluies, dont sont issues les eaux souterraines, sont naturellement acides et dissolvent le calcaire en circulant dans les fractures de la roche, créant tout un réseau de cavernes. Ces terrains calcaires sont appelés des terrains karstiques (du mot karst, terrains calcaires de Yougoslavie) [13].
1.5.
L’usage de l’eau : 1.5.1. L’usage domestique :Les eaux de consommation publique sont utilisées à différentes fins. Un habitant consomme aux environ de 230 l /j, n’en utilise que seulement 1 % pour la boisson et 6 % pour la préparation de la nourriture, les 93 % restant sont consacrés aux bains-douches (39 %), aux sanitaires (20 %), au lavage de la linge (12 %), de la vaisselle (10 %), à des usages domestiques divers (6 %) et au lavage des voitures et arrosage du jardin (6 %) [14].
1.5.2. Les besoins agricoles :
L’agriculture est une grande consommatrice de l’eau pour l’irrigation et l’élevage.
L’irrigation nécessite des volumes considérables. Un hectare de maïs par exemple consomme 20000 m3 d’eau pendant sa période végétative, et un hectare de riz 40000 m3 en moyenne [15].
1.5.3. Les besoins industriels :
L’industrie est consommatrice de l’eau. Elle a de multiples fonctions, par exemple celle de fluides de refroidissement et de substance primaire (dans le domaine de la production) ou de solvant et de milieu réactionnel (dans l’industrie chimique par exemple) [16].
1.5.4. Usage pour l’urbanisation :
Avec la croissance de la population, l'urbanisation et le développement économique, la demande en eau douce augmente dans toutes les zones urbaines du monde. Parallèlement, le changement climatique et la pollution influent également sur la quantité d’eau disponible pour les résidents des villes [17].
1.5.5. Cause de rareté de l’eau :
L’eau est menacée dans sa qualité et dans sa quantité. La rareté grandissante des ressources en eau qui résulte de la diminution des quantités disponibles par habitant, la dégradation de la quantité et les objectifs de développement économique et social imposent donc l’élaboration et la définition d’une stratégie de gestion de l’eau à moyen et à long terme [18]. Dans notre pays, l’eau s’est raréfiée en raison du climat, mais d’autres facteurs y ont contribué :
Chapitre 1 : Recherche bibliographique
5
1.5.5.1. La surexploitation
Pendant longtemps l’exploitation de cette ressource s’est faite sans aucune planification ce qui a poussé à un usage excessif. Le gaspillage : par définition cela implique tout écoulement d’eau non justifié tel que les robinets ouverts, les fuites dans les foyers, les industries et dans les réseaux urbains [19].
1.5.5.2. La pollution
A cause de la pollution, certaine ressources deviennent inutilisables [19].
1.5.5.3. Les mauvaises techniques d’irrigation :
L’irrigation avec excès apporte aussi du sel en excès qui s’accumule dans le sol et qui contribue à la perte de l’eau. Le sel attire l’eau de la nappe par capillarité qui s’évapore. Ainsi, le niveau de la nappe descend [19].
1.6. Analyse physico-chimique :
1.6.1. Paramètre physique :
La température
Les eaux souterraines sont à température relativement constantes toute l’année, 12°c à 15°C environ lorsque leur environnement n’est pas modifié (mise à nu de la nappe, etc.) La température des eaux superficielles (rivières, lacs et retenues) est très variable selon les saisons et peut passer de 2°C en hiver à 30°C en été. Les causes principales de l’augmentation de la température d’origine anthropique, pour les eaux de surface sont constituées par les centrales thermiques et nucléaires (70 à 80%), par la diminution des débits d’étiages due à une trop importante mobilisation de la ressource en été [20].
pH
Le terme pH est la concentration d’ions hydrogène dans une solution. Dans l’eau, ce facteur est d’une importance exceptionnelle, en particulier dans les procédés de traitement. Dans les laboratoires de routine des usines de traitement, il est mesuré et ajusté si nécessaire pour améliorer la coagulation/floculation ainsi que pour contrôler la désinfection de l’eau. La valeur du pH allant de 0 à 14. En dessous de 7, l’eau est considérée comme acide et au-dessus de 7 comme alcaline. L’eau au pH de 7 est neutre [21].
Chapitre 1 : Recherche bibliographique
6
1.6.2. Paramètres chimiques :
La conductivité
Par définition, c’est la conductance d’une colonne d’eau comprise entre deux électrodes métalliques de 1 cm2 de surface, séparées l’une de l’autre de 1 cm. Donc ce paramètre traduit une aptitude de l’eau à laisser passer le courant électrique [21].
Carbonates et bicarbonates
La détermination des carbonates et bicarbonates se fait suivant une méthode titré métrique très répandue : un aliquote de l’eau est titré avec un acide (H2SO4 ou HCl) à faible concentration
(0.1N) en présence successivement de phénolphtaléine (indicateurs des carbonates) et du méthyle orange (indicateur des bicarbonates) [21].
Chlorure (Cl-)
Ils sont rencontrés en grandes quantités dans les eaux souterraines. Elles peuvent provenir de la contamination par les eaux usées d’origines domestique et industrielle, et de la dissolution des sels naturels par le lessivage des terrains salés. Le Cl- est aussi un bon traceur des activités anthropiques. Les concentrations en chlorures montrent des valeurs variables, qui dépassent parfois les normes fixées par l’OMS à 250 mg/l, pour atteindre une valeur maximale qui tourne autour de 300mg/l près des cours d’eau, le premier lieu des rejets domestiques et industriels [21].
La dureté
Le titre hydrotimétrique ou dureté de l'eau, est l’indicateur de la minéralisation de l’eau. Elle est surtout due aux ions calcium et magnésium. La dureté s’exprime en mg/L de CaCO3
.Généralement, l’eau est souvent simplement classifiée comme l’eau «douce » ou « dure » [20].
La dureté calcique (THCa)
Le calcium est le plus abondant dans les eaux, cet élément traduisant la dureté totale des eaux naturelles. Il provient essentiellement de la dissolution des formations carbonatées (calcite et dolomite), qui caractérisent les faciès de plusieurs niveaux stratigraphiques au niveau de la région d’étude (ex : calcaires lacustres) [21].
La dureté magnésienne (TH Mg)
C’est le deuxième élément de la dureté totale, qui présente une origine semblable à celle du calcium. Il provient généralement des formations dolomitiques par l’attaque des eaux en
Chapitre 1 : Recherche bibliographique
7
présence du gaz carbonique, et de la dissolution de magnésium MgSO4 dans les terrains gypsifères [21].
Les sulfates
Les sulfates naturels de l'eau proviennent de la dissolution du gypse (CaSO4.2H2O) ou du
Lessivage des terrains contenant des pyrites dont les sulfures entraînés s'oxydent en sulfates à l'air. Les concentrations inférieures à 200 mg/l ne posent pas de problèmes. Des concentrations supérieures provoquent la précipitation du sulfate de calcium dans les eaux calcaires. Des concentrations supérieures à 100 mg/l favorisent la corrosion des métaux.
La concentration admissible en sulfates pour l'homme est de 250 mg/l. Au-delà de celle-ci, ils ont un effet laxatif excessif. Ces ions proviennent essentiellement des engrais agricoles et de la minéralisation de l’azote organique abandonné par les êtres vivant [15].
nitrates
Les nitrites sont oxydés en NO par Cl, ClO et O. Les traitements biologiques peuvent transformer NH en NO. Si la quantité d’oxygène de l’eau n’est pas suffisante pour poursuivre l’oxydation jusqu’au stade de nitrate. Ce phénomène peut se produire la nuit sur des filtres lents à débit forcé en raison de la diminution de la photosynthèse [21].
Ammonium
Les eaux souterraines peuvent contenir de faibles quantités d’ions ammonium,
généralement inférieures à 1 mg/l. Dans des eaux d'égout, ces ions sont libérés par la dégradation des protéines et de l'urée. La présence de concentrations élevées dans un cours d'eau indique une zone de pollution organique ou d’eutrophisation. En générale l’ammoniaque se transforme assez rapidement en nitrites et nitrates par oxydation ; la mise en évidence, dans l’eau, de teneurs importantes en azote ammoniacal implique généralement une contamination récente par les matières organiques en décomposition [15] .
ortho phosphates
En milieu acide et en présence de molybdate d'ammonium les ortho phosphates donnent un complexe phosphomolybdique qui, réduit par l’acide ascorbique, développe une coloration bleue susceptible d’un dosage spectrophotométrie. Certaine s formes organiques pouvant être hydrolysées au cours de l’établissement de la coloration et donner des ortho phosphates, le
Chapitre 1 : Recherche bibliographique
8
développement de la coloration est accélérée par l’utilisation d’un catalyseur, le tartrate double d’antimoine et de potassium [20] .
1.7 Qualité de l'eau d'irrigation :
La qualité de l'eau utilisée pour l'irrigation est un paramètre essentiel pour le rendement des cultures, le maintien de la productivité du sol et la protection de l’environnement. Ainsi, les propriétés physiques et chimiques du sol, telle que sa structure (stabilité des agrégats) et sa perméabilité, sont très sensibles au type d'ions potentiellement échangeables présents dans les eaux d’irrigation [22].
La qualité de l'eau d'irrigation peut être mieux déterminée par une analyse chimique en laboratoire. Les facteurs les plus importants pour déterminer la qualité requise de l'eau dans l'agriculture sont les suivants [22] :
pH ;
risque de salinité ;
risque de sodium (degré d'adsorption de sodium ou SAR) ;
carbonate et bicarbonates en relation avec les teneurs en Ca et Mg ; Autre traces d'éléments ;
Anions toxiques ; Aliments ;
Chlore libre.
1.8 Les normes de qualité des eaux destinées à l’irrigation :
L’agriculture représente le plus gros consommateur des ressources en eau. Ces ressources, suivant les régions dont elles proviennent, et leur contact éventuel avec des sources de pollution ont des caractéristiques très diversifiées [23]. De plus, vu la diminution des apports en eau constatée depuis plusieurs décennies, les agriculteurs, notamment dans les régions continentales, s’intéressent à l’utilisation des eaux usées. C’est ainsi que des normes de qualité des eaux destinées à l’irrigation ont été établies.
Une eau est conforme à l’irrigation est une eau dont les caractéristiques respectent les valeurs limites imposées par des textes de lois et inscrites dans des tableaux de normes. L’exemple du, tableau 1 donne les normes de qualité des eaux destinées à l’irrigation
Les normes varient selon les pays, mais dans la majorité des pays on fait référence, à quelques exceptions près, aux cinq critères de qualité sus cités [23].
Chapitre 1 : Recherche bibliographique
9 Les normes ont pour objectif de :
protéger le public et les ouvriers agricoles ;
protéger les consommateurs des produits agricoles ;
protéger les ressources en eau superficielle et souterraine et les sols ; protéger le matériel d’irrigation ;
maintenir des rendements acceptables [23].
Tableau 1.1. Les normes de qualités de l'eau d'irrigation (Directive de l’OMS 2002).
Paramètre de l'eau Symbole Unité Valeurs indicatives
Conductivité électrique CE dS/m 3 Calcium Ca⁺⁺ mg/l 400 Magnésium Mg⁺⁺ mg/l 60-75 Carbonates CO₃⁻ mg/l 3 Bicarbonates HCO3- mg/l 610 Chlore Cl⁻ mg/l 1065 Sulfate SO₄⁻⁻ mg/l 960 Nitrate NO₃⁻ mg/l 10 Ammonium NH₄⁺ mg/l 5 Phosphate PO₄⁻ mg/l 2 Potentiel hydrogène pH 6-8,5 Température T °C 35
Tableau 1.2. Barème de qualité pour les eaux d'irrigation proposée par la FAO.
Type de problème Guide pour la qualité de l’eau
Pas de Problèmes. problèmes croissants Problèmes graves
Conductivité (ms/cm) ˂0 ,75 0,75-3.0 ˃3 Alcalinité ou dureté 80-120 / ˃120 pH (risque de colmatage) ˂7 7-8 ˃8 Chlore Cl Irrigation de surface Irrigation par aspiration
˂4 ˂3 4-10 ˃3 ˃10 Azote ˂5 5-30 ˃30 Bicarbonate Hco3- ˂1,5 1,5-8,5 ˃8,5
Chapitre 2: présentation de la région d’étude
10
2.1. Introduction
Nous commençons notre étude par la présentation générale de région de Taher la wilaya de Jijel. Ce chapitre concerne la mise en exergue des caractéristiques naturelles de la région, des ressources en eau, des activités agricoles et de l’irrigation.
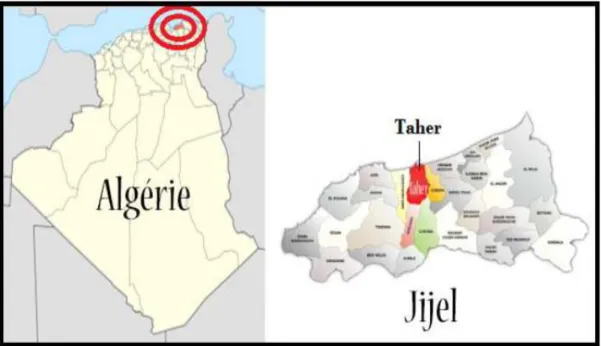
2.2. Présentation de la région
La commune de Taher (Figure.2.1) fait partie de wilaya de Jijel. Elle occupe une superficie de 56.86 km². Dont la population est estimée à 134839 habitants en 2000. La wilaya de Jijel se situe au Nord Est du pays, elle est limitée : au Nord par la mer méditerranée ; à l’Est par la wilaya de Skikda ; à L’Ouest par la wilaya de Bejaia ; au Sud par les Wilaya de Mila et Sétif [20].
2.3. Site et situation géographique de la commune Taher
La commune de Taher est située à 15 km à l’est de la ville de Jijel , dont sapopulation est de 77367 habitants depuis le dernier recensement (RPGH) de l’année 2008 . Elle est limitée : Au Nord par la mer Méditerranée ; au Sud Chahna Oudjana ; à l’Est par la commune de Chekfa et Chahna ; à l’Ouest par la commune Émir Abdel Kadar [20].
Chapitre 2: présentation de la région d’étude
11
2.4. Cadre socio-économique
L’étude socio-économique a pour objet de déterminer les différents éléments démographiques, et les activités économiques et leurs impacts sur la dynamique de l’occupation des sols dans la zone étudiée [23].
• La population
En 2008 : 77367 d'habitants (dont 38059femmes et 39307 hommes) avec un taux d'accroissement de 1,5%. Le recensement de 2008 compte 77367 habitants de la commune, dont 59250 personnes agglomérées dans le chef -lieu, 16706 habitants des agglomérations secondaires et 1411 habitants des zones éparses [23].
Tableau. 2.1. Répartition de la population et la densité 2008 de la zone d’étude
Commune Habitants 2008 Superficie km2 Densité hab. /km2
Taher 77367 56,86 1361
2.5. Economie
La commune de Taher posse d’une double vocation : l'industrie et l'agriculture. Ces principales infra structures économiques sont :
• la zone industrielle d'Ouled Salah comportant notamment l'usine du verre Africaver ;
• le central électrique d'Achouat ;
• l'usine de briques d'Achouat ;
• la gare ferroviaire de Bazoul ;
• l'aéroport international Ferhat Abbas ;
• le port de Djendjen avec une capacité de 4,5millions de tonnes par an et d'une superficie de 104 ha.
Elle renferme également de vastes terraines agricoles sur les rives des oueds de Nil et de Djendjen consacrés principalement à la serriculture [24].
2.6. La géologie
Les traits de la géologie locale sont très simples, La région de Taher appartient au bassin néogène marin de Jijel qui est limité au Sud par l’arête montagneuse du massif de Béni Khettab, à l’Est par l’arête montagneuse de Seddat, à l’Ouest par le massif volcanique
Chapitre 2: présentation de la région d’étude
12
Il est constitué de dépôts datant du mi pliocène (tertiaire) et constitués par des marnes, des argiles, des calcaires et de dépôts actuels (quaternaire) qui correspondent aux sables dunaires, aux dépôts de terrasses alluviales et à des dépôts sur les versants (éboulis de blocs et conglomérats …) [25] .
2.7. Le Climat
La région de Taher fait partie de la zone littorale. Son climat est sous influence maritime. Les étés secs et tempérés, et des hivers doux et humides. La température est très douce en hiver (11° en moyenne au mois de janvier) et la chaleur est tempérée par la brise de mer en été (26°en moyenne au mois d’Août). Cette petite région est soumise à des précipitations fréquentes particulièrement en saison hivernale puisqu’elle reçoit une tranche d’eau supérieure à 1 000 mm. Celle-ci atteint les 1 200 mm au niveau des sommets des contre forts montagneux [24].
2.7.1 Etude des paramètres climatiques
• Les précipitations
Les précipitations constituent un facteur climatique principal de l’alimentation du réseau hydrographique d'une région ainsi que son système aquifère. Elles sont caractérisées par une répartition inégale d’un point à un autre et d’une saison à une autre. Pour déterminer cette inégalité, une étude sur l’évolution spatiale et temporelle des précipitations a été abordée [24].
• La température de l’air
Température de l’air est un facteur qui a une grande influence sur le bilan hydrologique du fait de son impact sur le déficit d’écoulement (évapotranspiration). Elle varie en fonction de l’altitude, de la distance de la mer et de la position topographique [24].
2.8. Hydrologie
Les plaines sont les débouchés des cours d’eau. Les plus importants d’ouest en est sont : L’oued Mencha, l’oued Djendjen, l’oued Nil, l’oued Boukraa, l'oued El Agram, et oued Saayoud. Ces oueds qui proviennent de l’encadrement montagneux disposent de bassin versants relativement petits. Leur régime est irrégulier puisqu’ils sont presque à sec en été et ils se remplissent rapidement en hiver pouvant provoquer des inondations. Ces oueds et leurs affluents se déversent dans lamer méditerranée car il n'existe qu’un seul barrage réservoir situé au sud de la commune d’Emir Abdelkader [25].
Chapitre 2:
• Oued Nil
Figure 2.
La nappe alluviale d’oued Nil fait partie des nappes côtières de la wilaya de Jijel, elle se trouve dans les territoires des communes de Taher, Chekfa, et El
superficie de 27 km², sa capacité est estimée à 20 Mm essentiellement par un remplissage des alluvions grossiers, avec des passages de quartz, sables, et
présentation de la
13
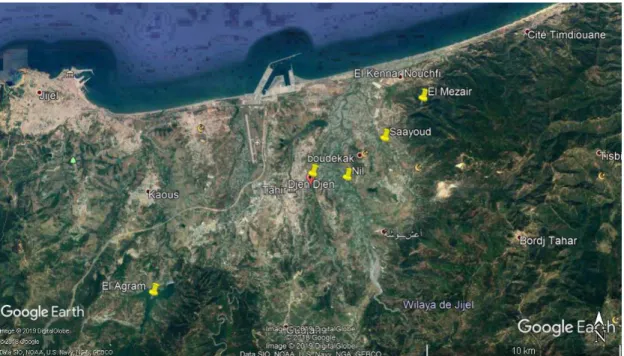
Figure 2.2. Situation hydrologique
Figure 2.3. Photo prise d’un point sur l’oued Nil.
La nappe alluviale d’oued Nil fait partie des nappes côtières de la wilaya de Jijel, elle se trouve dans les territoires des communes de Taher, Chekfa, et El
superficie de 27 km², sa capacité est estimée à 20 Mm3/an. La couche aquifère est constituée essentiellement par un remplissage des alluvions quaternaire (galets, graviers fins, moyens, et grossiers, avec des passages de quartz, sables, et schistes). Son substratum est composé par de la région d’étude
La nappe alluviale d’oued Nil fait partie des nappes côtières de la wilaya de Jijel, elle se trouve dans les territoires des communes de Taher, Chekfa, et El Kennar, avec une La couche aquifère est constituée quaternaire (galets, graviers fins, moyens, et schistes). Son substratum est composé par
Chapitre 2:
des marnes plastiques. L’hydrodynamique de la nappe est présentée par un écoulement des eaux souterraines du sud vers le nord (ANRH, 2011
• Oued Djendjen
Elle fait partie des plaines côtières de la région de
territoires des Communes de Texanna, Taher, et El Amir Abdelkader, elle referme une nappe libre contenue dans un alluvial quaternaire (galets, graviers moyens à grossiers, et des comportant quelque fois des intercal
alluvionnaires est constitué essentiellement par des La capacité de la nappe est évaluée de10 Mm
25 l/s/Km². L’écoulement des eaux souterraines converge vers l’axe central de la p parcouru par l’oued Djendjen
Figure 2.4. Photo prise d
• Oued Sayoud
Oued Sayoud, se situe au
wilaya de Jijel. Il et l’un des principaux affluents de oued Nil
présentation de la
14
L’hydrodynamique de la nappe est présentée par un écoulement des du sud vers le nord (ANRH, 2011) [26].
Elle fait partie des plaines côtières de la région de Jijel, Elle est située dans les territoires des Communes de Texanna, Taher, et El Amir Abdelkader, elle referme une nappe libre contenue dans un alluvial quaternaire (galets, graviers moyens à grossiers, et des
fois des intercalations argileuses). Le substratum de ces formations alluvionnaires est constitué essentiellement par des marnes grises d’âge miocène inférieur). La capacité de la nappe est évaluée de10 Mm3/an avec un débit spécifique de
des eaux souterraines converge vers l’axe central de la p parcouru par l’oued Djendjen [26].
. Photo prise d’un point sur l’oued Djendjen.
se situe au Nord-est algérien, à une distance de 15 Km du
wilaya de Jijel. Il et l’un des principaux affluents de oued Nil avec l’oued Boulkraa et oued Tassift de la région d’étude
L’hydrodynamique de la nappe est présentée par un écoulement des
Jijel, Elle est située dans les territoires des Communes de Texanna, Taher, et El Amir Abdelkader, elle referme une nappe libre contenue dans un alluvial quaternaire (galets, graviers moyens à grossiers, et des sables, Le substratum de ces formations marnes grises d’âge miocène inférieur). /an avec un débit spécifique de
des eaux souterraines converge vers l’axe central de la plaine
’un point sur l’oued Djendjen.
algérien, à une distance de 15 Km du chef-lieu de la avec l’oued Boulkraa et oued Tassift
Chapitre 2:
Figure 2.5
Figure 2.6. Situation d’oued
présentation de la
15
5. Photo prise d’un point sur l’oued Sayoud.
Situation d’oued Sayoud par rapport aux autres oueds
de la région d’étude
Chapitre 2: présentation de la région d’étude
16
• Barrage d’El Agrem
Le barrage d’EL Agrem est situé sur l’oued El Agram à environ 15 km au sud-est de la ville de Jijel (Wilaya de Jijel). Il est destiné à :
• L’alimentation en eau potable et industrielle de la ville de Jijel (Wilaya de Jijel) ;
• L’irrigation d’environ 6 500 Ha des périmètres agricoles situés à l’aval [26].
• Puit El Mezaïr
C’est un puit ordinaire réalisé traditionnellement, il est situé à côté de la raille ferroviaire à une centaine de mètre de la mer. Les agricultures locales l’utilisent régulièrement pour irrigation de leur terre [24].
Chapitre 3 Matériels et Méthodes
17
3.1. Introduction :
A Jijel le secteur de l’agriculture est le plus occupé par la population avec un pourcentage de 23% d’après ANIREF 2013. Avec l’augmentation de l’évaporation de l’eau pendant l’été et l’utilisation de la technique des serres en hiver dans le domaine de l’agriculture, la quantité d’eau destinées à l’irrigation est très importante, pour cette raison les agriculteurs font courir à utiliser n’importe quelle eau trouvé à proximité de ses terres. En faisant une enquête sur place, nous avons remarqué qu’une partie des agriculteurs utilisent l’eau des oueds, d’autres les eaux des puits, et une partie utilisent les eaux du réseau installé par les autorités locales, provenant du barrage d’El Agram situé à Kaouas.
Dans le but de déterminer la qualité de ces eaux destinées à l’irrigation, nous avons réalisé, durant le mois d’avril, Mai, et juin une compagne d’échantillonnage : nous étions dans l’obligation de répartir nos points de prélèvement dans le périmètre choisi Jijel -Taher.
Au total, 15 échantillons des eaux ont été prélevés, trois fois (trois dates différentes) pour cinq types des eaux, trois oueds à savoir : oued Djendjen, oued Nil et oued Saayoud, eau d’un puits situé à el Mzair et l’eau du barrage d’El Agram.
3.2. Technique d’échantillonnage des eaux :
L’échantillonnage est une étape primordiale, car il conditionne la pertinence de l'analyse des eaux. La technique d’échantillonnage détermine la fiabilité des résultats. La répartition des échantillons était en fonction de la disponibilité d’un point d’eau d’irrigation. Pour les oueds, nous avons choisi les points faciles à accéder (sous les ponts), concernant l’eau du barrage, nous l’avons prélevé grâce à une vanne située en aval du réseau, enfin l’eau souterraine est prélevée depuis un puit avec un seau[27].
3.3. Mode de prélèvement des échantillons :
Les prélèvements d’eaux brutes ont été effectués entre Avril 2019 et Juin 2019 aux dates suivantes :
Campagne 1 07/04/2019 Campagne 2 12/05/2019 Campagne3 17/06/2019
Chapitre 3 Matériels et Méthodes
18
Les prélèvements sont effectués dans des bouteilles de 1.5 L en polyéthylène lavées à l’acide chlorhydrique (5%) , puis rincées à l’eau distillée. Au moment de l’échantillonnage les bouteilles sont rincées trois fois avec l’eau à échantillonner. L’eau est prise à une profondeur de 15 à 30 cm de la surface de l’eau, en évitant la pénétration de l’air. A chaque bouteille nous rajoutons deux goutes de la solution de chlorure de mercure pour assurer une conservation jusqu'à l’analyse [28].
Figure 3.1. Carte présentative des sites de prélèvement
Le transport des échantillons depuis le point de prélèvement jusqu’au laboratoire se fait dans une glacière à 4 °C. Lorsque les échantillons sont conservés, ils sont mis au réfrigérateur. Avant de procéder aux opérations analytiques, il est essentiel que toutes les dispositions soient prises, telles que l’homogénéisation au moment du dosage.
3.4. Nettoyage de la verrerie
Les flacons destinés au dosage des sels nutritifs (ammonium, phosphates, nitrates, nitrite) et des autres dosages, ont été nettoyés et rincés à l’aide de HCL (10%) puis rincé à l’eau robinet et en fin rincés à l’eau distillés, séchés et fermés. Trois méthodes analytiques sont utilisées pour la détermination des paramètres chimique [29].
Chapitre 3 Matériels et Méthodes
19
3.5. Mesures des paramètres physico-chimiques
3.5.1.
Les paramètres physiques (mesure in situ)La température, pH, sont des paramètres très sensibles aux conditions du milieu et susceptibles de varier dans des proportions importantes s’ils ne sont pas mesure in situ. Pour cela nous avons utilisé des multi-paramètres manuels de marque
Hanna 9812. Pris du département des sciences de la terre et de l’univers de
l’université MSB de Jijel. Les paramètres physiques mesurés sont : la température c(T°C), le potentiel d’hydrogène (pH, l’eau à analyser est versée dans un récipient ou l’électrode est prolongée, lorsque l’écran d’affichage se stabilise sur une valeur, on peut noter les résultats pour procédé à analyser de l’échantillon suivant il faut rincer l’électrode par de l’eau distillée [30].
Figure 3.2.: Multi paramètre manuel (Hanna 98129)
3.5.2. Les éléments chimiques (analyses au laboratoire)
Une analyse complète des éléments chimiques a été effectuée : éléments majeurs (Ca2+, Mg2+, Cl-, SO42- et HCO3-) et le cycle de l’azote (NO3-, NO2- et NH4+).
Deux méthodes d’analyses ont été utilisées :
3.5.2. 1. Méthode volumétrie (Titrimétrie) :
Une technique de dosage dont le but est de déterminer la quantité de matière contenu dans un échantillon. La méthode de titrage que nous avons utilisé pour le dosage du calcium et de chlorures ainsi pour la détermination de la dureté et de l’alcalinité de l’eau par la
Chapitre 3 Matériels et Méthodes
20
mesure de (TAC et TH) est la volumétrie ou la concentration d’une solution inconnue est déduite de la mesure d’un certain volume d’une autre solution de concentration connue.
Le matériel utilisé dans cette technique est la burette avec des réactifs spécifiques pour chaque élément à doser [31].
Figure 3.3. La titrimétrie pour les mesures au laboratoire
• La conductivité électrique (au laboratoire)
Donne une idée sur la dureté de l'eau, cette mesure permet de déterminer la quantité totale de sels minéraux dissous dans l'eau, elle est mesurée à l’aide d’un conductimètre exprimée en µS/cm. le protocole adopté est le suivant :
On place dans un bécher de 100 ml une quantité suffisante de l’échantillon. On place ensuite l’électrode du conductimètre dans le bécher, et on lit La valeur donnée par l’appareil.
Chapitre 3 Matériels et Méthodes
21
Figure 3.4. Mesure de la conductivité de l’eau.
La dureté totale (TH) :
Principe :
Le titre hydrotimétrique, ou dureté de l'eau, est l’indicateur de la minéralisation de l’eau. Elle est surtout due aux ions calcium et magnésium. La dureté s’exprime en mg/L de CaCO3.
Réactifs utilisés :
Solution tampon ammoniacal de pH=10 ; Noir erriochrome en poudre (NET), indicateur ; EDTA (0,01N);
Mode opératoire :
A l’aide d’une pipette, introduire 25ml de l’échantillon dans une fiole conique, puis en ajoute 2ml de la solution tampon et une pincée de NET, qui donne une couleur violet.
Ensuite on titre avec l’EDTA en continuant d’agiter jusqu’à avoir un virage du rouge violet au bleu, on note le volume de l’EDTA versé. Le titrage est refait 3 fois, puis la moyenne est calculée pour les trois résultats [33].
Chapitre 3 Matériels et Méthodes
22
Figure 3.5: Différentes étapes pour le titrage de la dureté total(TH).
La dureté calcique (THCa) :
Principe :
Titrage des ions calcium avec une solution aqueuse de l’EDTA à un pH compris entre 12 et 13. L’indicateur utilisé est le murexide, qui forme un complexe rose foncé avec le calcium.
Réactifs utilisés :
Solution hydroxyde de sodium NaOH (1N) ; EDTA (0,02N);
Murexide 1% comme un indicateur coloré;
Mode opératoire :
A l’aide d’une pipette, introduire 25ml de l’échantillon dans une fiole conique, puis en ajoute1ml de la solution NaOH (1N) et une pincée de murexide avec une spatule (quelques grains), on agite quelques instants jusqu’à développement d’une coloration rose foncée. Ensuite on titre avec l’EDTA en continuant d’agiter jusqu’à
Chapitre 3 Matériels et Méthodes
23
avoir un virage du rose au bleu violet, on note le volume de l’EDTA versé. Le titrage est refait 3 fois, puis la moyenne es t calculée pour les trois résultats [33].
La dureté magnésienne (TH Mg) :
Principe :
Connaissant la dureté totale d'une part et la dureté calcique d'autre part, il est facile par différence de calculer la dureté magnésienne .
TH = TCa2+ + TMg2+
TMg2+ = TH – TCa2+ (en mg/L)
TH: Dureté totale
TCa2+: Dureté calcique
TMg2+:Dureté magnésienne [34].
Bicarbonates et Carbonates
Réactif :
Acide chlorhydrique (HCL) concentré à 37% ; Phénolphtaléine (indicateur) ;
Méthyle orange (indicateur).
MODE OPÉRATOIRE
Carbonates
Prélever 25 ml d’eau a analysé.
Ajouter 1 goutte de solution de phénolphtaléine (indicateur) ;
Si aucune coloration n’apparait et le pH est inférieur a 8 donc les carbonates =0 dans ce cas on détermine seulement le (Bicarbonate) [33].
Bicarbonates
Prélever 25 ml d’eau a analysé.
Ajouter 1 goutte de méthyle orange (indicateur) Titrage avec HCL jusqu'à coloration jaune orangé Note le volume titré et faire le calcule[33].
Chapitre 3 Matériels et Méthodes
24
Dosage des chlorures :
Méthode de Mohr :
Principe :
Réaction des ions chlorure avec des ions argent pour former du chlorure d'argent insoluble qui est précipité quantitativement. Addition d'un petit excès d'ions argent et formation du chromate d'argent brun-rouge avec des ions chromates qui ont été ajoutés comme indicateur. Cette réaction est utilisée pour l'indication du virage. Durant le titrage, le pH est maintenu entre 5 et 9.5 afin de permettre la précipitation [33].
Mode opératoire :
Placer 100 ml d’échantillon dans le flacon Erlenmeyer ;
Ajouter le pH entre 7 et 10 ?, en cas de besoin avec NaOH ou H 2SO4 ;
Ajouter 1 ml de la solution indicatrice K2CrO4 ;
Titrer la solution avec AgNO3 à 0,01 N jusqu’à ce que la solution vire au jaune rougeâtre qui est le pont de fin de titrage.
Chapitre 3 Matériels et Méthodes
25
3.5. 2.2. Méthode spectrophotométrie d’absorbation moléculaire :
La technique de spectrophotométrie est basée sur la propriété de la matière et plus particulièrement de certaines molécules, il consiste à absorber certaines
longueurs d’ondes du spectre UV-visible. Elle permet de réaliser des dosages grâce à la relation de proportionnalité entre l’absorbance et la concentration.
Nous avons utilisé cette technique pour le dosage du fer, d’ammonium, des phosphates, des nitrites, des nitrates, des sulfates et d’azote ammoniacal.
Le matériel utilisé est un spectrophotomètre UV. Visible, avec un trajet optique de 1 cm (cuve en quartz)[35].
Figure 3.7. Le spectrophotomètre (UV 1600 PC)
Nitrate (NO3-) :
Méthode par spectrophotométrie d’adsorption moléculaire :
Principe :
En présence de salicylate de sodium, les nitrates donnent du paranitrosalicylate de sodium, coloré en jaune et susceptible d'un dosage spectrophotométrique[36].
Mode opératoire :
Introduire 10mL d’eau naturelle dans une capsule de 60 mL (pour des teneurs en azote nitrique supérieures à 10mg/L , opérer une dilution).
Chapitre 3 Matériels et Méthodes
26
Alcaliniser faiblement avec 1ml de la solution d’hydroxyde de sodium. Poursuivre de dosage comme pour la courbe d’étalonnage , en suivant les memes étapes que précédemment :
Ajouter 0 .5 ml d’une solution d’azoture de sodium. Ensuite ajouter 0.2ml d’Acide acétique pur à 100% .
Agiter en tournant légèrement la capsule avec la main, afin d’homogénéiser le mélange .attendre 5minutes puis évaporer modérément à sec au bain-marie ou sur une plaque chauffante réglée à 80°C (ne pas surchauffer trop longtemps).
Ajouter 1mL de solution de salicylate de sodium ,mélanger puis évaporer à sec sans calcination (à sels humides ) sur la plaque chauffante .laisser refroidir .
Reprendre le résidu par 1ml d’acide sulfurique concentré ayant soin de l’humecter complètement.
Attendre 10 minutes, puis ajouter 15ml d’eau distillée et 10ml de solution d’hydroxyde de sodium qui développe la couleur jaune .Agiter la solution à la main avant d’effectuer la lecture au spectromètre à la longueur d’onde de 415nm .
Expression des résultats :
Les résultat est donné directement en mg/L à la longueur d’onde de 415nm . Sulfates (SO42- ) :
Principe :
Les sulfates sont précipités et passés à l'état de sulfate de baryum en présence de Ba Cl2 [37].
Ba Cl2 + SO2-4 → BaSO4 + 2Cl-
Mode opératoire :
Prendre 20 ml d'eau à analyser puis compléter à 100 ml d'eau distillée ; Ajouter 5 ml de la solution stabilisante ;
Ajouter 2 ml de chlorure de baryum ; Agiter énergiquement pendant 1 mn ; Passer au spectrophotomètre λ = 420 nm.
Expression des résultats :
Chapitre 3 Matériels et Méthodes
27 Ortho phosphates :
Méthode par spectrophotométrie d’adsorption moléculaire :
Principe :
En milieu acide et en présence de molybdate d'ammonium les ortho phosphates donnent un complexe phosphomolybdique qui, réduit par l’acide ascorbique, développe une coloration bleue susceptible d’un dosage spectrophotométrie. Certaine s formes organiques pouvant être hydrolysées au cours de l’établissement de la coloration et donner des ortho phosphates, le développement de la coloration est accélérée par l’utilisation d’un catalyseur, le tartrate double d’antimoine et de potassium [27].
Mode opératoire :
Vérifier le pH de l’échantillon qui doit être compris entre 2 à 7, l’ajuster si nécessaire .introduire 20 ml d’eau dans une fiole jaugée de 25 ml, ajouter 1ml de solution d’acide ascorbique puis poursuivre comme pour l’établissement de la courbe d’étalonnage. Tenir compte de la valeur lue pour le témoine. Se reporter à la courbe d’étalonnage.
Expression des résultats :
La courbe donne la teneur en phosphore, exprimée en milligrammes pour la prise d’essai.
Ammonium (NH4+) :
Méthode au bleu d’indophénol :
Principe :
En milieu alcalin et en présence de nitroprussiate qui agit comme un catalyseur, les ions ammoniums traités par une solution de chlore et de phénol donnent du bleu d’indophénol susceptible d’un dosage par spectrophotométrie d’absorption moléculaire [27].
Chapitre 3 Matériels et Méthodes
28
Mode opératoire :
Introduire dans une fiole conique de 100 ml, 20ml d’eau à analyser puis poursuivre le dosage comme pour la courbe d’étalonnage. Préparer de la même façon un témoin avec 20 ml d’eau permutée. Effectuer les lectures au spectrophotomètre à la longueur d’onde de 630 nm et tenir compte de la valeur lue pour le témoin. Se reporter à la courbe d’étalonnage.
Expression des résultats :
Pour une prise d’essai de 20 ml, la courbe donne directement la teneur en ions ammonium, exprimée en milligrammes par litre.