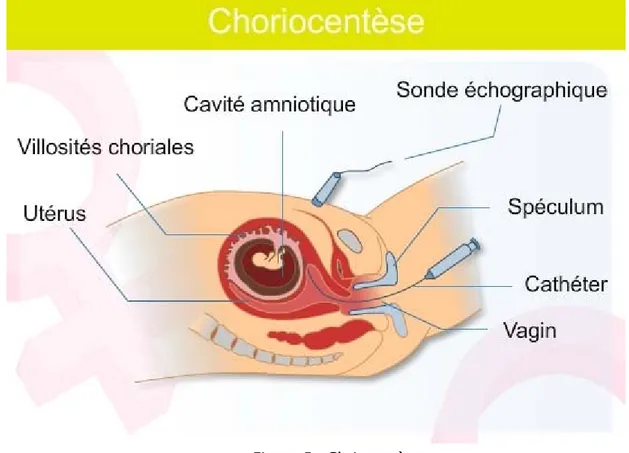
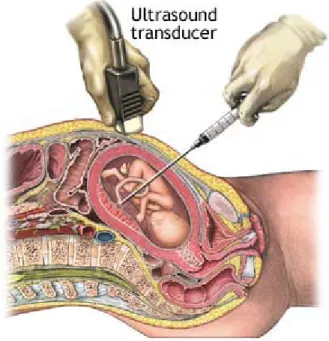
Prélèvements fotaux dans le diagnostic prénatal
Texte intégral
Figure
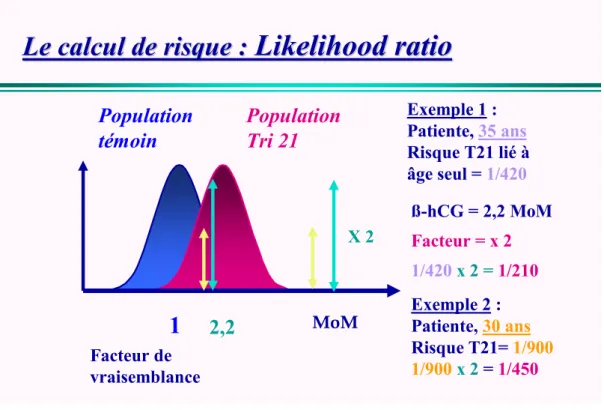
![Tableau 2 : Performances de différentes combinaisons de marqueurs sériques pour un taux de dépistages positifs constant fixé à 5% [41] :](https://thumb-eu.123doks.com/thumbv2/123doknet/1962452.170/30.892.99.792.208.598/tableau-performances-combinaisons-marqueurs-seriques-depistages-positifs-constant.webp)
Documents relatifs
Obéissant aux ordres qui leur venaient d'ailleurs Par des gens bien placés se disant les meilleurs Mais les raisons obscures qui motivent les guerres Sont issues très souvent du
Qui relie les deux pôles qu’on appelle cosmiques Sont au nombre de trois pour atteindre la cible Qui est la position du grand lotus mythique L’adepte recherchant les
7 Recopie les phrases en complétant les verbes avec la bonne terminaison du futur, -ras ou -ra :..
Reduction of the latter by PEEP or continuous positive airway pressure (CPAP), therefore may cause cardiac output to increase (point 8) [ 55 , 56 ], or at least to be better preserved
We calculated the G values of hydroxyl and hydrogen radicals that react with cyto- chrome c as well as the G values of CO 3 •– formed in the presence of various concentrations
Die Frage stellt sich also in solchen Ringen in einer etwas anderen Form, n¨amlich ob derartige Faktorzerlegungen in unzerlegbare Elemente (bis auf Einheiten) eindeutig
Dans la routine clinique, le clinicien ne dispose d’aucune information préopératoire durant la pose de cette sonde VG, et la seule visualisation dont il dispose pour naviguer dans
Explicitly, we are concerned with the fundamental questions: (i) how accurately can we predict the active pressure in the presence of interparticle interactions, (ii) to what degree