LES LIXIVIATS ET LA RESISTANCE DU POMMIER A LA. T.A. VELURE
par
LA NATURE CHIMIQUE DES LIXIVIATS DE FEUILLES ET LEUR ROLE DANS LA RESISTANCE DU FOMMIER A LA. TAVELURE
(VEN'l'URIA I~UALIS ( CKE.) WINT. )
. par
Léon M. Tartier
Thêse soumise A la. Faculté des Etudes et des Recherches des Gradués, en accomplissemnt partiel des exigences requises pour l'obtention du Grade de Maitre es Sciences.
Département de ~pathologie
Université McGill Montréal, Canada.
R. L. Pelletier qui a
augV6 ·
oe projet de reehei'Ohe et a proci1ca6 tou lea ooœeila Moeaaai.Jtea ~. 1. la rûl5 utiea dea exp6rieaaea qu •A la r6dact.ion de ca trawil.Je déaire 6p~ re.rc~r
toua
les protea•111'8et
lea 6tudianta du D6partei8Dt de ~pathelogie qui l u. aome:nt
ou ua autn ••at aiü
da leura coœeila.lntia, je r.trcie le Conseil dea Recherches .lgr:lcol.ea
4u Q'dbeo .qui a pDmuaaent fo111"Di aon npport
n....cter
PAGE
I.
INTRODUCTION ••••••••••·•••••••·••••••••••••••••••••••
1II.
•••••••••••••••••••••••••••••••• 3 .1. INTRODUCTION ••••••••••••••••••••••••••••••••• •-• •• 3 B. StJBSTAN~ ORGAJII.Q'UE •••••••••••••••••••••••••• ·••1.
•
•••••••••••••••••••••••••••••••2. SUCRES •••••••••••••••••••••••••••••••••••••••
3.
FACTIURS IHB'LtJDCllrl' Ll LIXIVIATION DISSUBSTANCES OIGliiQUES ••••••••••••····••••••••
O. 'BIBMBI'TS IBORC!A.NIQUD .- ••••••••••••••••••••••••••. • 7
D. DFLUENOB D&S SUBST.llrol!:S BmDUES PAR LBS FEtJII,.'LE
SOR LES OBGARISM:&S HII!OP.A.mOGEIES ••••••••••••••• 9
m.
• ••••••••••••••••••••••••••••••18
A. LBS POMMIIRS ••••••••••••••••••••••••••••••••••••• 18 B. L •ORGANISME;. PARASIT.liD • • • .• • • • • • • • • • • • • • • • • • • • • • • 18
O. LA. PREPARATION DE L'IliiOCUilJ)I • • • • • • • • • • • • • • • • • • • • •
19
D. TECHNIQUE D 'lNOCULlTION DES POMMIEBB • • • • • • • • • • • • • 20 E. LA. CULTURE SUR PILLIC'OI,;E DE CELLOPHANE • • • • • • • • ••• 20
F.
LA. TEOBNIQUEum.nDm
AU COURS DES ESSAISDE GBRMIIATION .••••••••••••••••••••••••••••••••••
21
1. IB NETTOYAGE DES LAMBS DE VERRE • • • • • • • • • • • • • • 21 2. Ll PREPJ.RlTION DE LA. SUS:EUSION DES SPORÉi3· ·• • .. 22
3.
LE MELANGE DES LIIIVIATS ET DE IA SUSmNSIONDl SPORES ••••••••••••••••••••••••••••••••••••
22
la..
LES !BSA.IS DE GIRHIIA.TION •••••••••••••••••••• 22 G. LA. . 'l'ECHBIQUE DE REOO:LD DES LIIIVIATS • • • • • • • • • • • • 23H'.
I.
J.
PAGE L 1 ANALYSE DES LIXIVIATS
. .
"... .
25
1. SEPARATION SUR COLONNE D 'ECHANGEURS D'IONS • •
25
2. TECHNIQUES .DE CHROMATOGRAPHIE •••••••••••••••• 27 a. Chromatographie des acides aminés • • • • • • • • 27 b. Chromatographie des sucres ••••••••••••••• 29 3. IDENTIFICATION DES ACIDES AMINES ET DES SUCRES 29 a. Identification des acides aminés ••••••••• 29( i) Réaction des acides aminés avec la
ninhydri.e •••••••••••••••••••••••••• 29
(ii) Comparaison des chromatogrammes
obte-:nu.s avec des chromatogrammes témoiœ 30 b. Identification des sucres •••••••••••••••• 31
(i) Révélation des sucres avec la
p-anisidine-phosphate ••••••••••••••• 31 {ii) Comparaison des chromatogrammes
obte-nus avec des chromatogrammes témoins 32 TECHNIQUE UTILISEE LORS DE LA PHOTOSYNTHESE DANS
UNE ATMOSPHERE ENRICHIE DE
cf40
2 •••••••.••..•••••
RECOLTE DES LIXIVIATS RADIOACTIFS ••••••••••••••••
33
35
K. Cû-CHROMATOGRA.HIIE ET AUTORADIOGRA.HIIE DES
LIXIVIATS RADIOACTIFS ·••••••···••••••···
35
L. UTILISATION DU SPECTROMETRE A SCINTILLATEURLlQUIDE ••••••••••••••••••••••••••••••••••••••••• 38
IV. RESULTATS EXPERIMENTAUX • • • • • • • • • • • • • • • • • • • • • • • • • • • • • •
.40
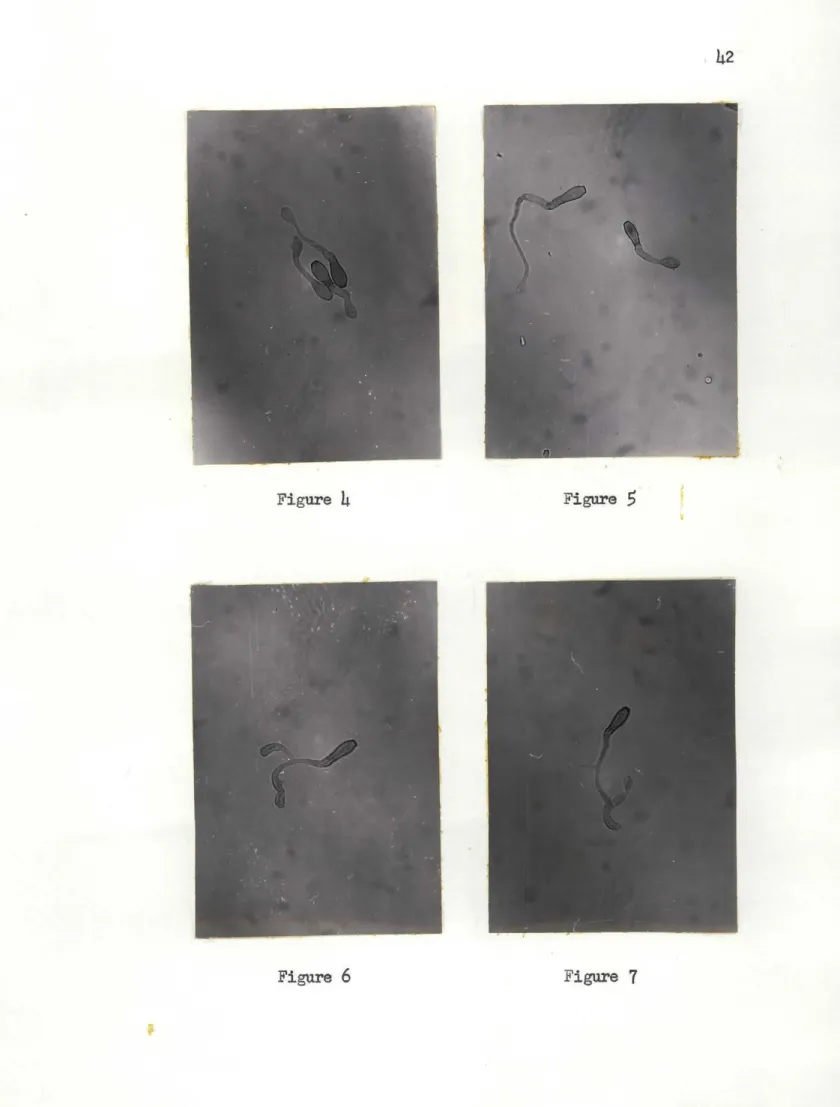
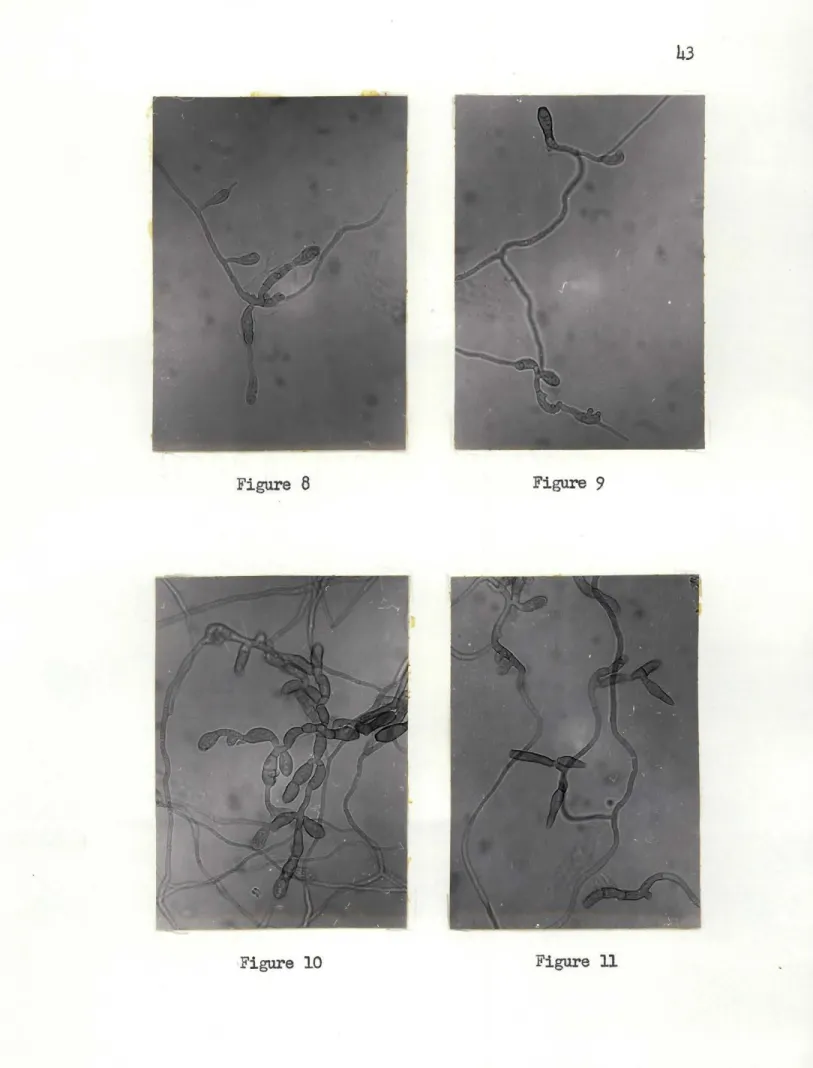
A. ETUDE SUR LA CROISSANCE DE V. INAEQUALIS SURPEL-LICULE DE CELLOHiANE •••••• -:...
40
1. INTRODUCTION ·•••••••••••••••••••••••••••••••.40
2. OBSERVATIONS ···•••••••••••••••••••••••••41
B. ESSAIS DE GERMINATION DES CONIDIES DANSiii
PAGE
1. INTRODUCTION ···•••••••••••••••••
44
2'. ESSAIS DE GERMINATION DANS LES LrnviATS
PEU CONCENTRES •···•••••••••••••••••••••
45
3. ESSAIS DE GERMINATION DANS LES LinVIATS
TRES CONCENTRES ···••••••••••••••• $~
4.
LA. GERMINATION DES CONIDIES DANS LES EXTRAITSETHERES DE LIXIVIATS ···•••••••••••••••••••••
53
a.
Introduction ••••••••••••••••••••••••••••53
b. Observatioœ . • • • • • • • • • • • • • • • • • • • • • • • • • • •54
C. ACIDES AMINES ET SUCRES PRESENTS DANS LESLin-VIATS RECUEILLIS DE FEUILLES SAINES DE POMMIER • •
56
l. INTRODUCTION • • . • • • • • . • • • • • • • • • . • • • . • • • • • • • • •
S6
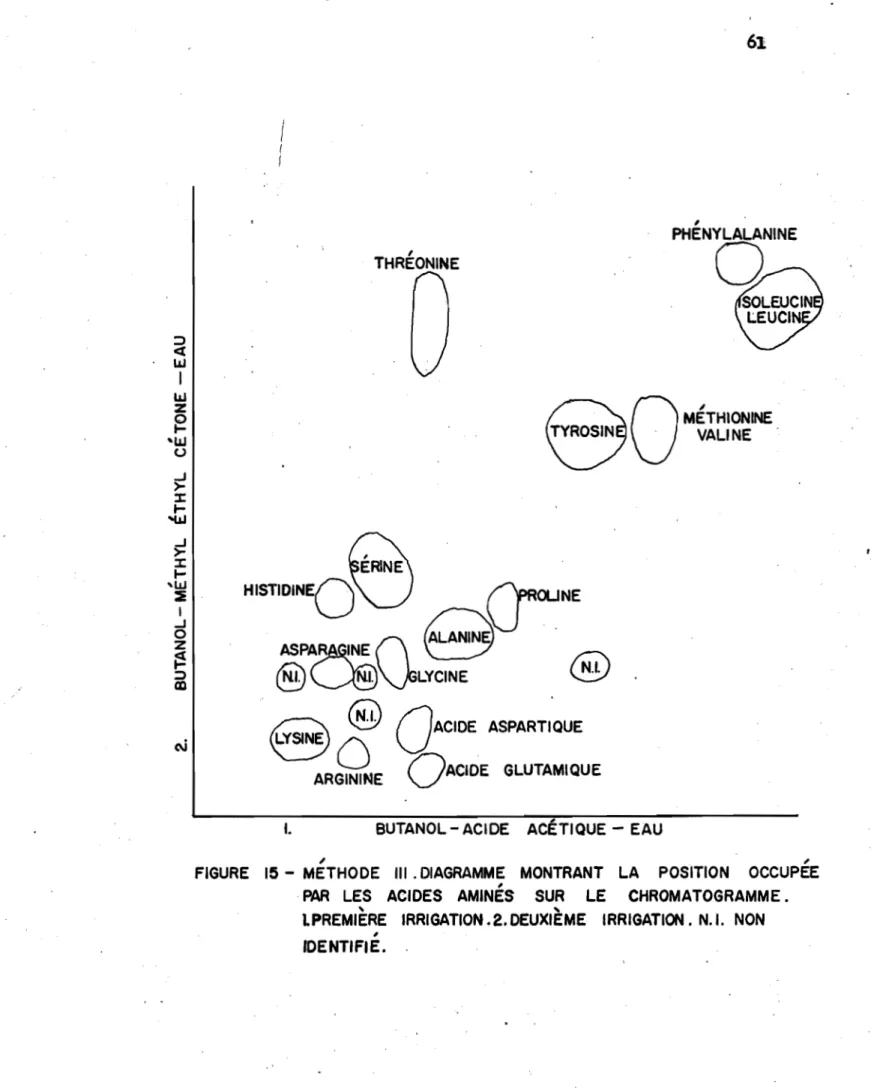
2. ACIDES AMI'NE::I ••••• •.. • • • • • • • • • • • • • • • • • • • • • • •58
3 . SlTCRES • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • • 62 D. lBS ACIDES AMDmS DANS LES LinVIATS OBTENUS DEFEUII.LiS SAINES ET DE~ MALADES • •• • • • • • ••
65
l. INfRODUCTION ••••••••••••••••••••••••••••••••65
2. QUANTITES TOTALE"S DEol4
PERDUESsœs
FORMED 1 ACIDF.S AMINES • • • • • • • • • • • • • • • • • • • • • • • • • • • • •
6 7
3.
AUTORADIOGRA.HUE DES CHROMATOGR.AMMES • • • • • • • •68
E. LES SUCRES DANS LES LIXIVIATS OBTENUS DE FEUILLES
SAINES ET DE FEUILLES MALADES • • • • • • • • • • • • • • • • • • • 70
1. INTRODUCTION...
70
2. Q.UANTI'l'ES TOTAlES DE
cl4
P.l'!:RDUES SOUS FORMEDE SUCRES ET AUTRES SUBSTANCES NEUTRES • • • • • • 71
3 •
CHROMA.TOGR.A.FHIE DES SUCRES •••••••••• • • • • • • • • 72. 4.
AUTORADIOGRAPHIE DES CHROMATOGRAMMES • • • • • • • •74
5.
ANALYSE QUANTITATIVE A L'AIDE DU SPECTBOMETREv.
VI.
m.
DISCUSSION ET CONCLUSION
••••••••••••••••••••••••••••• SOMMliRE •••••••••••••••••••••••••••••••••••••••••••••BIBLIOGRAPHIE ••••••••••••••••••••••••••••••••••••••••
PAOE
79
89
91
I. D1'1'iODUC!IOW
ta tavalve elu pol8ier, eauée par Ve:Guria 1Daepal1! (CD.) lfJ.Dt. 1 est p.robablueDt · la •lacl1e la plus illportu:te dea wrpra
des r6,P.oœ teapér6ea, 7 cempria le Qa6bec. Le chapipoa reapoua-ble de cette ul.adie est u repriaelltaDt d •ua gro'Clpe de cbulp:f.po• Jil71;opathopœa ea:ractAriaéa par un type particulier de parui tia•.
En ettet 1 ap:Ns la péllétratiea de la cuticule, la croissance elu o:bam.-p:lpoa est lild.t6e entre la cuticule et lea cellules épidend.quea
1
aoua-jaoeatea dont il déri:ve sa aevriture et cela jusqu
•t
un atap aftDCé de la-ladie.
Peur les raiao• ûcœahs préo6d.,..st, il aou a aellblé im-portut dt étudier quelles étaient les réactio• du o)!uœpi pea
lers-q1l •:tl 'ftl:aait ea coâact avec laa substances •turelle•a prûentes A la surface des feuilles, quelle .était la u.ture de ces substuces et leur rtle daD8 l•établiaa...t de la •ladie et auai COllllllent
uœ
fois la aladieêtablie,
le cbaapig:non pouvait attecter la u.ture etla ...,œ1t6 de ces Slil.bs1iances qui aout perdl1es par l.es feuilles seu l'action de la pluie.
Deux te~• sont empJ.oTû coœt . . .
nt
daœ ce tra:va.il et 1J.D1It déti:nitioa de obacu d•nx a
•impose pour par.mttre une •il.JAIUJ."e coaprihell8ion da. sujet, ce aoat: Lix:l'riatia.- Le tel'D8 lixl:'f'ia-ti.on tel qv.'aaplAJ;yé rétèe 1 l'action e.roée par des aelutioœ aqueuses au.r des plantes ou parties d8 plaates ea '111.8 d •eatra!:œr laperte de sùstucea orgaDiqus ,
ou
inorguiquea par ces .._. plaJites. AiDai, la perte de sùataDces peutetre
eDrdaée par l'action de laphd.e, par la rosée, par pttation, par 'ftporiaation d ' • • nr l.es
pl.&Dtes ou eacere par treapap des dittmnta or.-s de la plante
dana dea selutioœ
aqueuses.
I4:d:riats.- P&r lixbiata on eRteDd le liquide recueilli par lixi:datioa des feuilles.Le préses tra'ftU relate l.ea résultats d •e:çérieœes
eure-prises au D'parteiBDt cie ftvtopathologie du Coll.t\ge Hacdomalt! de 11thlliftrsité Hc0111, Montréal, P. Q.
1 àl'ant la p6riod.e allant
II. REVUE BIBLIOORA.PHIQUB
A. - IN'J.'IODUO'l'IOI
De:puis de nombreuses années on soupçonne que la pluie ou la rosée enlAve aux plantès des substances mtritives. Bien que l'on œ eonnaisse pas encore toute l'importance des pertes ainsi slibies par les plantes, tout partieuli.rement les feuilles 1 plusieurs ,lilytopatholog:Lstea ont pensé que ees substances pourraient avoir
3
un r6le A jouer dans les relations plante h8te-pathogêne. Cette revue bibliographique r6sume les observations faites par de nombreux
ehereheurs sur la nature et les quantités des substances perdues par les feuilles, ainsi que sur les faeteurs qui in.tlueneent ces pertes. Nous reverrons également le r6le et 1 'inf'luenœ que peuvent avoir ees substances sur la germination et la croissance des organimœs phyto-pathogênes et sur le développement général des maladies des plantes. les substances organiques ayant fait l'objet de nos reeberehes
seront surtout considérées. Cependant, les substances inorganiques seront mentionnées briAvemant pour compléter la vue d •ensemble sur le problême de la lixiviation.
CJa:iJ.'Mrt., Xead et Jaobn (1931) ..
a
probù~t laatm
preld.era l rearquer • • las :teuillaa perdent 'lM pariie de lev
colltea •• pn~s MD l'ef't'et de la li:l:i"f'iatioa; 11.8 ~nt. auai que cea pertes ftl'iea.t d.'ae eeplce Tépkle l l'autre, cea
pertes 'l1ll'iaDt de
1%
peur 1 •anime l1.6%
peur la luera~ et l 18% pour le bro•. Il t'aut cepellldaat aoter CJ.'U ces r6eultats hnut obtenu par 1•aaqse de lix1.Tiata proftDU.t de plantes ceupêea wrtes et a6chéee, ou natareJ.J.e.llt .trie a et aéehéea, ••• ceacU.-tioae • :re~ pu laa cead:l.tiua •tveU.. de lixt:ri.a-tiea lenque les plantes sent n.r piada. LiDaJœ• (1955) ( cit6 parBiner,
1960)a
éple•JJ.toeutaté
lapréaeœe
depluieurs
aeides Md aéa daD8 les 11x1T.l.ats abteJIU par tre~~p~.&e de feuilles
--de
te•te
c1aœ de 1•eau pealaat 30 ld.autea. :LcDBC, S.et et'l'ulœ7
(1956&) co•tateut ausi la pr6eeœe cl1acid8a
•""*
daDa les lizl-Tiata réaelt6a de plaat.a de Jtarieeta •urr18 ea Jd.l:la'a. liquide. ee-peada:Dt 1 les ét\ldea les plua o-.pJAtea • • la •ture dea s11DR&noes eraardcl•• prieeatea daœ laa 11x1.T.l.ata da te11illea ta:rent et't'eotuéea par1'a.b7,
Jr. , et Boberge:r ( 1959) 1'1'ù:87,
Jr. (]962), fa.kq, Jr. et'.l'a1œ7
(1.962). Ba et'tet, dea êtlldss dftaillées e:at pend.a t ces cber-cheura de trouwr de ao.brea aeidea ,,.., ... laa liziTiata :re-cueillis de plu.ta de haricots et cl.e ptcbera (VeiDlleld, 1961).2. SUCRIS
o•est égalel8s GailDert et a~. (1931) qui DOU deœ.llt laa
prell:ljres bdicatioœ sur la préseœe de a11erea clana laa lixl.viata ..---de plaat.es. En effet, 1la :raarq•llt qae la •türe ergud.que • •
-azotée extraite par lixi:riatioa '9U'ie de
6%
du·peida He pour le bre• (Brcllla Mrdeaceu L.) lJS%
pnr la l.uerDe (Meclioap ld.!pidaOaertn.) J cea chercheurs eataat que ces pertes repriaent.eat lar-~·t las ncres. Ohol.odJV' (1932) (cité par Dalbre, 19S7) 'botn8
égals•nt des neres daœ l u 1ixi 'riats de plaats de 'blé obt.ellll8
par UM pluie a.rtiticiella. CholodD;r ceuidtlre que la perte de ces sw:res peut
•t:re
la cause de la d1w1Jmi;ion de la récolte de gra1Dsaprês l1D8 pluie prolemgée. De plu, 11 coœicYre la sa"Veur dea fraises et autres traits dét6rierée par urae p6r:l.Gde de auftia tapa coaae le riaultat clirect de la perte de S\101"8s eauée par la pluie. Engel (1939) oouic:klre qU8 les substances ~mtritifts perdues par laa feuillas soat sunoü de D&t111"8 ozogaud.qU8, les oeDdres couti "t1la.lâ seulement 10 l
2S%
du résidu obte• apris ~rsion de feuilles daJul J.•eau peDdant 24 beures. Dal.bro (19)7) est~ que la quaatit' de•tiêre organique perdue par les feuillas de po.W.r
a
cause de la pluie est sup6rieure l une totœe par hectare par armée, le gros da ces pertes étant prc)bùJe.IS des sucres. tu~œ7, Jr.,i'uke7
et Wittwr (19S6), Tuke;r, Jr. et Romberger (19S9), Tulce;r, Jr. (1962) et Tu.lœy Jr. et Tuke;r (1962) c:oaatateut; éplement la préaeœe de plusieurs ncreadaD8 les lixiv:l.ats, ils 1cleM~rent laa b;ydrates da carboae sui'V&Ilts:
3.
:r
.&C!IOS III'I.IBICll'.ru.
LIXIVI.l!mx
DIS SUB8'1UCI8 OIOAIIQUDDiftmats facteuw ,....,.. affecter la perie de su'bstaœes orpalqu.es par les pl.a.utes s . . l'effet de la lizirlation, ces taote'll'll
••t
ta) Esplce Tégétala t tel que Mté par Qa.ilber1;
et
al. (1931)-'·-les pertes ea éU.ldis orp.Diques "fU::.eat
cl,.._
eaploe Téaé-tale l l•aâN, a1Mi cea ehenlwva t1"011'ftat ,,. les J8NS subies par le b:rae tureat aupér:l.eurea . aux pertes aubie• parla~ et l'aftt..
b) Age dea feuilles: Dal.Dro (1957) note qua les pertes •• éU.nta erptd.quea aupeBteRt awe l'approche. de la •tv.-r:J.té et de la aémsceDCe dea fellil.laa.
c) Iuiire:
.fûe7,
Jr., Wittwr et 'l1lkey (U.S7) eti'II.Jœ7,
lt.l:ttver et ~~ Jr. (19$8) oo•tateut ·CJ.W' lea pert. en hydrates de car'boM par liz1T.t.at1on •at
111n'••
lorsque la plaDte reste a&DS l'UJI:5Jre, laa pertes av.g~~~~nta.Dtgra-dueU..at awc 1 ~aupentation d.e l'iateaaité 1111111Muae.
Bien que DtD
u.co:re
étudiée, i l est tov.t probable qœ de nOJibreu: av.treat•ctnr•
iBt1.11eace»:fi la perie d •éléœeDta erprd.-qœa par lixl:ri.ation par eDÇle, 11 étatete
santé et de :autritioades plaatea, les caractêrea morphologiques de la cuticule ( 6paia-sev de la cuticule}, i:ate.nai té de la pl.ui8, etc •••
1
b
rûuû,
l 10D • oaiiMti . - JeU de cho• sur la•tv.re
etlAta qa:a.titû de subatucea
oraaaf4:a.ea
perdues par les pl.u:tea aoua l 1ettet ela la lixl:rlatioa.n ....
ldan bident qœ d •au.tru ét'Gd.essenat
D6eeaad.rea pourea
..._~r toute l'illportaDOe.Si 1 •6tude des substuoas erpaiquea perdues par les pl.aates
est tort riceate, ila1eD est J,aS cle .._ pour las é1é.ats
iDorp-Jtiquea et il faut
remonter
l deSaun.re
(180k) (eiU par Tab;y,Jr.,
Talœ;r at Wittwar, 19S8) qui reaaJ."tlU8 que de 11eaa 'ftl1&Ilt ea coataot
awc les feuilles contiellt des sels &leal :1 DB. Par la suite 1 Bucheaau
(1883}
at
TOD Ho-.YW (1883) (oit6a par!ulca7
1Jr.
,!!.,!!.
1 19$8)publient dea rapports qui
i.Dd.i4uaat
que cles nbatances peuwatetre
perdaes par les feuilles seua l'action da la pluie. Depuis ce tapa, dittmJIIies coEIDJI1catioœ appa.rai.ssaBt par iD.termitta:n.ca daDS du re"f'Ua soientitiquea, (Iaclarc at BN&seala • 1908; IWm
et
Yallaae, 192lu V&llaoe, 1930J Ou.illlert1 Hlad at Jaolaloa,llllJ
ChelAdaT,
1932; Areaa, l934J Lauaberg, 193SJ ~~ l931JED&e1,
1939; :IIlgbaa, l9SO;'laa,
19SlJ Sohooh, l95SJ Will, l9S5J Fuji118:N.:.-lt.da,
19S6t l'inplq et&1.,
l9S71 Voigt, 1960). Tou ces rapport8 d6oriwllt la parte--
d •éu.ats lllaéraux aeua 1•ettet de la lixl:viation, les éJJ.nts étudiés
sos
~][,
P, 1, la, Mg, Cl,aa, s.
quaUtatiw.· du :petes •• 61'-el&a ~ n.biea par l u plaa:Ma1
panicalJAlraeldi laa
te'lillea,
ce • •eat eepeDdaat qu 1&'980
1 11ltil:laa-tioa dea U.tepaa raci1Mct1ta ..- l•ea peut •• fain . . id6e eaete de 116te:ad.ue dea pertes nb:laa par laa
plut.ea.
Mea (19Sia)et
:tolll,
S.et
et
'.rll1œ7
(19S6a, 19S6b)tuut
laa prea:le:ra l 11t11:1Mr lea 1setopaa radieaetitaet
11.8· 4'-l.utreat d.éfiaiti.,._ù que laaél6-ments :a1Dél'"aux absorbés par lee aebee pe....,.U eDinlite ttre perdu par laa feuilleaJ par la n1te1 c!•ald;rea ü11.dea 'l'iDreat ooDtirMr eea r6nl.tata (!u.Jaq, Jr., 111ttwr et ~,
19.57
JT'ù:e7
et A•li~~g,1958,
T\tlœ7,
Jr.,
Ta.lot7
etlfJ.ttwr,
usa,
!'ake;r, lilttwr et!alce7,
Jr., 1958; Bbu., Yallaee et Imrt,,
1959;
!ulœ7'
1 Jr.et
Bom'beraer,19.59;
!ulœ71 Jr. etfalœT,
1959;
Tulœ7"
1 Jr. et!'a.lœ7
1 ]962).De Delibreu
.taoteva attene:at
laperte
d•éU..ta
Jd.Jaézoauzpar les plaatea, oe aoü :pl"i:aoipalaas t
a) L'qe 4• teuillaat la auceptib111té l la 11xbiatiea
..,..m;a
awo la -.turité des feuillu. (Leclerc et Breaseale,1908; 'h1laQ' 1
Jr.
at
!!• ,
19.58).b) lsploe
riPW.Ie
et la var:l.ét6t Wallace (19.30), OU1lbert et al. (19.31), Hu {19~), ! ù q et al. (1958) 1 laaaat.eva
-~
~'-trouwnt que laa pertes par 11x1rlatioa "''8ri.el1t d1uœ ea-plce
rigétale
l l'autre et d •uœ variüé l 1 •autre. o) liatU1"8 et épaiaaeur de la cu.Ucula t Lau.aberg (193.5)rearque qu les plantes l cutinle épaiaae aont; 1101Bs
sujettes l la 1ix1 Tiation par la pluie que les plantes t
9 cl) Etat de aaat6 de la pl.alltet les feuilles blessées soat;
plu njettes
A
la lixiv.l.ation que les feuilles sa:l.œs (1'11kq, Jr. et Morgan, 196)}.e) fiat de œtrition de la plante: Lona
!!
.!!•
(19S6a)d.ao:u-tr.lreat; que des plants de haricots an milieu liqdde l haute co:ace:n:tration saline sont plu susceptibles l la lixiviation que des plants en Jdlieu liquide l basse co:acentration aaliœ. t) Rature de 1 •élément perdu: le sodi.a et le •CJiêsium.
semblent être des élélllents facilemeut lessi'ftbles (!'uby, Jr.
!l
al. 1 (1958). D •autres auteurs trouwnt que le potassium.est 11élél&nt le pl:a.s facilement leuivé (Arens, 1934), ou.
e:acore le chlore ( Gailbert
.!i
.!!•,
1931).g) Pluie forte ou fine:
uœ
pluie fine emporte plu d •él6-1811tsm:Lnérawt
qu'uœ
pluie forte, {Laus berg, l9 35) •D •autres facteurs peuvent probablement faire' varier 1 'effet
da la lixi:viation par eDmple, la position dea .feuilles sur la tige, 1 'intensité l.1:aRd œuse, etc •••
D •. DFLtJEHCE Dm SUB$'l'A.NCF8 PBRDUFS lU. LIS FEUILLES SUR W ORGA.NISMIS Hm'OPJ1'H()(.EHIS
Il 7 a lollgl;empe que de nombreux chercheurs s'interrogent sur l'inf'luence des substances nutritives présentes dans les lixiv.lats de feuilles et d •autres organes de la plante sur la germination et la
croissancè des organismes phytopathopœs , 1 ainsi que sur le dévelop-pemallt pnéral des aladies des plantes.
Bzw (.lP22) r Jle
etre
là pl"811ier & :rearquer qœ de 1 •eau dinillêe restée ea contact • ...., l8s p6\alas ,.a.
. tleva.
de certa:.I.DIsporea trait6es est beaucoup .. plu
l.G11a
ca.-
celui dea speres taoial genaées cJaœ de l'eaudistill61
~ ~ reJII.'l"<I.Wl · ausai que plu 1'eau reste
loDg1;apa • OOJitac't·awe
l u p6tal.ea • plu la . .Dduo-tirlt6 6laotriqua de cel~•-' ·~; . grests: oetk a-c-atatioa . paral-:Yle ct. la pl'ld..atiea ..rait âa d•aprls Brom, 1. l'eDBlll08e des éU.IIts faoi:U..râ diffuiblas tels q• l8s Hla.. Lea a11Ves cons-tituszms tels que las lqdrates de carboœ, mo:lDS faeilaant diftu-aibles, contribueraient pell & aeerolt:re la co:nduct1T.i"'~et auraie:rll; ua 1101a:lre effet sur la germ..tion .. · .les r6au.ltat8 obteDUS awc les p6talea de Cereua :turent conft.rMa awc les p6tales d •autres eapleea de plantes, (Rr.Tl.locactu, !Rlipa,
CJ'd.dia,
Lat!qrus .odoratus, Petud.&, Geranium, Rosa, Violf,, Lil:iUJD.~ Begoâ'la, Glo:d.Jd.a) 1 1.1 oi leslixi-v.tats aua-ntaient la gend.natioa, 11 7 a'nd.t une aupentatioa
paral-JjJa de la coDd.uct1'Vité. Par co~re, Brcnm. œte que les lixi.'Viats obteJIU.II· de feuilles de Vieia faba, Blalleolu wlgaria et Tradescentia discol,or aontrent u:ne tl'f!s baute oculd.u.cti'Vité Mis n•out. peu. ou pas d •ef'fet sur la ge:rmiDation dea apores de
.!!.
ciœrea 1 dana certainacas on obtieadrait
me.
ua effet répressif.Y8.1'WOOd. {19S2)
ooutate
que lwaque dea · jem.a feuilles deHlaaeolua '!!l.p:ri! flottaieDt aur de l'eau dana des ebl.bree aaariea d'haidité, 11 se forait
gêaérale•ilt
de l'eau de gu:t.tatioa sur la11 face de la te~lle expoe6e A l'air. Loraqv.e ces feuilles de. haricots tarent illoculéea avec des spores 84lebaa de UZ'O!l!!a pba!eoli ou de Oolletotriehua l:JDdeDltldaD\1111 et dea feuilles de
r•.,.
geurgam(Vicia taDa.) iDoculéea avec B •
.u.rea.,
l'iatection résultante tut positiWMnt reliée 1. la quantité de ga.ttatioa.Au cours d •une
6tu.de
nr la tache cercosporée~me de labette-r&'V\t 1. sucre,
Kcmte.
(19SS) :rtmarq\18 que les coftidiea de Cercospora betieola gemeJIIt plus lente.llt sur les feuilles de w.riêtés réais-tantes, que sur les feuilles de vari6t6a ausoeptiblès. PotlrSUiftD'tson étude, Koftce conatate que la :rosée, la plld.e ou l'eau
d1Bt11-Ue (
d •abord w.poris-'e, eDSuite recullie) a,.ant séjeurnê sur dea feuilles de· w.riêtéa réaiata.tea earcent une plus forte action inhibitrice sur la gend..Dation .dea conidies dec.
beticola ou, daDa certaiœ cas' sur le taux de croiaaame du tube gel'lliMtit' qœ le liquide recueilli dea feuilles de w.ri'téa auoeptibles 1. la tache cercospor6ezme. Des coDidiea d'lltermria tenuis 110lltrlrent le. _ coaport;ement que les conidies de .!:!:_ betieola. les e:mrétioœ cutiaula:ires et leur iapertanoe m poiBt de vue ph;Jtopa.\hologique
furent de DOU.'9UU étudiées par Kaftca et Sulke (19S6). Plusieurs
eaptcea vég6talea (blé, trille rouge,. lilas, peuplier, ]liant, toate, bettera.,. 1. sucre) et
dittmnta
chaapipoDS (~-cilllrea, Aacoplvt&1!:!!
1 PtlcciDia .triticia) furent étudiés. Ces chercheurs reaarqut-rent que 11acti 'Vi té des emrétio• cu.tieulairea ditfareat 4 •ueeeptce A l'autre et d'ua chaapip.on A l'autre. .AiDai, les spores de B. ciœrea aollt
-
plu seœiblea et laa spores de P. triticiœ leaout moi.JIIII. Uœ action 1Jibib1Vice ou ncore ni•lante h t dé.oa-trée pour les e:mrétioM cutioulairea· cle ehaqu esptee T6ptale, cela dépeDdaD.t de la col'lCOBra.tion des e:IIINtiou aiD&i que de la
IIU8oep-tibilité du chulpipon traité. Ces etteta hreld; attribués l dea n.bstaacea apéeitiques tda actifta,
ditf'mntes
dea IIUbstaœes iDor-ganiques facile•nt o~blel qui a•aura:Lent rien l voir dau la rigal.ar::laation de la gel'lliation dea spores. Lea aubstaacea actiws aeraient lente.nt perdues par laa feuilles et dana des colM!itio• aturelles, el.l.es pourraient etre prieentea daD8 la reaée ou la pluie en coœentration nttiaante pev 1Dbiber la gel"'liutioa dea conidies de !!._. eiœrea.'l'eppe et Wàin
(19.$7)
oat éple•nt ét1141é 11iDflueD.ee deslix:i:riats obteJmS par la'VB.p r6p6té c:le teuil.lea sur la prJRiutioa et la creisaance du t'llbe pmba'td.f clea sp.-. · da ~ ot.aa. Ils
uaqàrent les lixiv.Lats obteaul de o:ue eapicea d'arbres et du lierre griç&Dt (Hedera tplix). Les lixl:riata obteDU par trois la-'f&ges successifs de œmbreua.. feuilles l aix heures d 1iDtenalla :ae mo~reat aucune activité sur la gel'lliu.t1on dea spores de
B~ Q:l•rea, cela étant pnD&bJ.e.nt dd l la trop grande dil.utioa dea lix:l:viata. Les autelll"B precWJreut alors l UDe extraction l l •éther des lix:l.nata. t•extrd.t aiui obte• Matra une aotiT.I:t6 hDg:l.ata-tiqu aip:l.ticatiw aur la gend.Dation das aperes. FA effet, les lix1 viata obteJmS de la plupart des espAces Tégt\tales étudi6es re-tarcYrellli la croissa.DCe du. 'hbe pnd.Batit des spores et daDa cer-taiJUI cu, (lixl:riats de coudrier et de chltaipier), \Dl épais-aias._.t du tube pnd.atit ffD remarqaé. Les extraits obtenus des
13 · feuilles de sureau et de troêne furent les plus fungistatiques. Ces résultats portêrent Topps et Wain (1957) l croire que dans la nature ces substances tungistatiques peuvent être présentes en concentration suffisante pour inhiber la germination des spores et qu 1elles pourraient
représenter pour la plAnte un moyen de défense naturel contre les at-taques des champignons.
Dans le m8me ord.r• d'idée, To:xopeus (1958) publie une note sur la variation dans l'expression de 11hypersensivité de plants de pommes
de terre du Phytophtora inf'estans.
n
remarque que dans certains cas, ilm
1est pas possible d'observer de cellules mortes et il pense quedans certains cas, les cellules réagissent si. rapidement que 1 'hyphe du champignon est arrêtée dans sa croissance immédiatement aJ>Ns ~tre
venue en contact avec le protoplaSJRe. Cependant, Toxopeus (1958) remarque que l'on ne sait pas si le champignon 12rce réelle:rœnt le mur cellulaire et il admet qu1il est mante possible que le tube germi-.
natif des sporanges ou des zoospores soit ar~é par quelque exsudat de la plante.
Weintraub, Miller et Schantz (1958) ont trouvé des substances stimulant la germination des conidies de Piricularia oryzae (agent causatif du "rice blast") dans la rosée présente sur la surface des feuilles de plants de riz. La rosée recueillie fut mélangée avec de l'agar et des essais de germination effectués. Dans tous les cas observés, la rosée recueillie aprês
5
l1.6
heures de séjour des plantsdans une chambre spéciale stimu.la grandement la germination des coni-dies. Cette stimulation ne fut cependant pas spécifique pour les
triciti furent aussi stimulées. Iss auteurs cependant, n•identifiêrent pas le ou les .t'acteurs acti.f's dans la rosée.
n
est intéressant de constater que tandis que certains chercheurs trouvent que des substances présentes dans les l.i.xi viats peuvent aug-menter ou diminuer la germination, d •autres chercheurs ne constatent aucun ef.f'et. Ainsi, Weinhold (1961) a trouvé que les li.xi.viats recueil-lis de feuilles de pêcher, et· cela quelle que soit leur concentration, n •ont aucun effet sur la germination des conidies de SPf!:!rotheca1!!!!-~ (agent causatif' du blanc da pêcher).
Endo et Amacher (1962) rapportent que le liquide de guttation recueilli de pousses d 1 orge augmente la germination des spores de
Helminthosporium soriakum, ainsi. que la .f'ormation de structures res-semblant aux: appressoriums et a~ hyphes d •infection. la germination dans le liquide de guttation (dilué ou non) tut de
15
à75%
plus élevée que dans de l'eau distillée utilisée conme témoin. Lewis (1962) note que le liquide de guttation provenant de pousses de blé susceptibles à Claviceps purpurea favorise le plus la croissance du tube germina-tif des conidies de.2•
purpu.rea. Le liquide de pousses de suscepti-bilité intermédiaire, moins de croissance taDti.s que celui provenantde pousses rési$tant~s favorise à peu près la même croissance que de l'eau servant de témoin.
Il existe aussi d 1autres rapports oll les lixiviats provenant de
lS
succls de l'attaque par des champignons phJ'toJ8thogêœs. Ainsi, Orella:na et Thoas (1962) reurquent que la haute ou la œn-auscept;i-bilité des follicules de ricin (lieillu coaud.s) A Botrytis sp. est associée A leur haute ou basse teœur en b7dr&tes de carboœ f'acile-•nt lessivables. Un autre eDllple noua est donn6 par Kosuge, Dutra et Hewitt (1962) et losuge et Hewitt (1964) qui rearquent que les conidies de Aaperg:l.llua .tl.avus,
!•
niger et!•
ciœrea (agents causa-tite du 0bunch rot• des raisins)prment
tris peu dans de l'eau, ilsconstatent cependant que le taux et le pourcentage de ger.mination sont grandement accrus lorsqu 'ils ajoutent des substances contenues dans
les l.ixiviats obtenus par lavage de raisins avec de l'éthanol A 6S~.
De: DOllbreux travaux ont été égale1118nt publiés concernant la
relation entre les exaudats de racines et les organi81118s parasitaires. (e.g. Scbroth et SJJ7der 1961, 1962).
En
Nsum.é,
on peut dire que les travaux publiés jusqu•l
dateont d6montré plus ou moiœ concluaivement que les substances contenues dans l.es l:u::l:rl.ats de .:teu:il.l.es ou d •autres orsa-s de la pl..ante ont un rOle l jouer dans la détermination de la résistance ou de la suscep-tibilité dea plantes l la maladie. D
•une
f'açon gén6rale, on penseca.ue
cea substances peuvent etre présentes en concentration suffisante, lla surface des feuilles ou d'autres organes de la plante, pour inhiber ou stimuler la germination des spores dea champipoDS parasitaires, 1
•etf'et
"VU"iant cepe:rrlant avec les espèces végétales et les variétés ainsi que les parasites concernés.subata.,.a nutriti Yes par les pl.a:atea sous 1 'action de la pluie 1 de
la rose J par guttation ou autre ll8l'8 artiticiel (irrigation folaire)
peut avoir d'importantes . répercuaaiODB sur la plante elle-ll.ême. 'l'11lœ)" et 'hlœ7, Jr. ( 1959) et TulaJy', Jr. et 1'uk.ey ( 19 59, 1962) énoncent quelques coœéqueœes possibles de la lix:lviation; ainsi, les plantes qui poussent en serre oontieDDeat mJe quaatité plus élevée d•él.élleats
nutritif's lessivables que les plantes qui poussent en plein air, ceci peut expliquar la difficulté re:aeont.r6e lorsqu 'on essaie de coaparer les résultats d'expériences obtenus avec des plantes de
serre
et dea plantes de plein air. les pesticides employée dans la lutte contre les parasites des plantes peuvent aussi augmeDter la quaDtité d •élé-ments rmtritif's perdus en altérant les propriétés }Vdropb.obiques na-turelles des feuilles. Comme ces applications de pesticides se font généralement au printemps et au début de l'été, les pertes d'éléments rmtritits encourues par les feuilles l ce JIIOD.ent-lA peuvent êtN cru-ciales pour les plantes qui en ont le plus besoin. L'irrigation fo-liaire des plantes peut entra1œr une perte coœi.d.6rable d •éléMnts nutritif's; il en est de.e.
dams les ohaabret
baute teneur d 'humi-dité od 1 ton propage des bou'\ ures ('1'ult:e7,
Jr. , 1962). La perte d 1é-1'-nts mtritits par les plantes eDtratne également une dilli.nution dea récoltes et une qualité médiocre dea prodnits. Les élé'Mnts perdus par les plantes retournent au sol et peuwnt. entratœr une IIOditication de la texture et de la balance des éU.nts d.lœ le sol et par voie de conséquence, affecter l'écologie et la distribution des plantes.
17
Ces quelques consid6ratioœ devraient suttire pour saisir toute la aigrd.tication et l'içortance de la lix.l'ri.ation, tout spéciale.nt au point de ~ pbytopatholog1.qœ. c•est, pour clarifier quelque peu le rtle joû par les substances prûentea dans lss li:x:S:ri.ats da
feuilles dana le complexe (pommier-!.inaeg,aalis)que les études ci-a.~s ont
6t6
entreprises.III. MATERIEL ET TECHNIQUES
A - LES POMMIERS
Au cours des différentes expériences nous avons utilisé des pommiers Mcintosh agés de deux â trois ans achetés au mois d'octobre 1960 â une pépiniêre locale. Les pommiers furent gardés â une tempé-rature de 4°C; â partir de février 1961, des groupes de quatre â six pommiers furent retirés de la chambre froide â intervalles réguliers et plantés dans des pots de gr~s (22 cm de di~tre, 24 cm de hauteur) et le sol arrosé avec une solution nutritive. Une pulvérisation de bouillie soufrée (solution 1:20) sur les arbres â l'état dormant et leur transfert subséquent dans une serre préalablement désinfectée . â la bouillie soufrée s •avéra très efficace pour le contrOle du blanc
(Pbdospgaera leucotricha) qui sans cela devenait épiphytique et nuisait considérablement â la poursui te des travaux. Les pommiers furent gardés en serre A une température de 18 â 21°C. jusqutâ leur utilisation pour les expériences.
B - L'ORGANISME PARASITAIRE
Les lignées 365.4 et 1096 de Venturia inaequalis furent utilisées pour nos travaux. La première de ces lignées produit des lésions typi-ques sur les feuilles de Mc!ntosh, tandis que la seconde ne produit que des mou<rhetures et n'est point considérée comme pathogène dans la nature. Une culture de chacune . de ces lignées fut obtenue du Dr. D. M. Boone du Département de Phytopathologie de 1 'Université du Wisconsin. Ces cul-tures furent repiquées et conservées sur un milieu composé de gilose
19 (l5g/l) l l 1eau de pommes de terre (40g de tubercule/1), contenant du
glucose (5g/l). Le repiquage de ces cultures tut effectué par isole-ment et transfert d •une seule conidie de la culture mare dans un tube l essai contenant de la gélose l l'eau de pommes de terre. Cela rut effectué de la façon sui vante : une partie marginale d •une culture mare sporulante rut transférée dans un tube l essai et macérée dans
quelques millilitres d 1eau distillée stérilisée. Le contenu du tube l essai fut alors versé dans une botte de Pétri contenant de la gélose. L1e:xcês de solution fut drainé et la boite de Pétri incubée pour une
période de 12 l 15 heures â l6.5°c. Au bout de cette période, les spores gar.mées furent isolées une par une l l 1aide d'un microscope
stéréoscopique et transférées dans un tube l essai contenant de la gélose glucosée l l'eau de pommes de terre et incubées l 16.5°C. pour 3 l
4
semaines.C - LA PREPARATION DE L t INOCULUM
La. préparation de l'inoculum se fit suivant la méthode décrite ci-dessous. Cette méthode a été utilisée par Phillips (1959). Des cultures de
!•
inaequalis 4gées d'un mois furent macérées dans5
mld'eau distillée stérilisée, la. suspension ainsi obtenue fut versée dans des bouteilles à flancs droits de 200 ml contenant 20 ml d •eau de ponmes de terre glucosée (40g tubercule, 5g glucose par litre d •eau.) Les bouteilles furent placées sur leur cOté plat dans un incubateur à 16.5oa. pour une durée de 10 à 12 jours. Une suspension de spores fut obtenue par filtration des cultures à travers huit couches de coton à fromage et centrifugation du filtrat l 7000 rpm pendant 25 minutes.
la llilieu de culture tut jeté, les spores furent resuspendues da:ns de l'eau distillée pour enlever le milieu de culture adhérent et centri-fugées une :nouvelle fois. Les spores aiDai obtenues .turent alors re-suspendues dans de l'eau distill6e pour obtenir la concentration d •ino-cul.mn désirée.
D - TECHNIQUES D 1DOCULA.TION DES R>MMIERS
Une auspeœion de spores proftnant de cultures de
!•
inaequalia .36.5.4 tgées d'une dizaine de jours .tut préparée de la f'açon cUcrite précédeDœent. ViDgt-quatre ':heures avant l'Înocu.l.ation, les pe.:iers f'urent placés dans une chambre de · croissaœe (éclairement de 16ooo lux,14
beures par jour) A une teçérature de 16 l 18°0. et dans une atmosph4re saturée· d'humidité. La suspension de spores .tut ensuite pulvéris~ sur les feuilles l 1 'aide d •un po.lvériaateur De Vilbiss no. 1.5. Un pœmnier ne f'ut pas inoculé et servit de t'-oin. A.pris 11 inoculation, les pollliers turent gardés dana l•atmosph4re saturée d1lnulddité pour une durée de48
heures. Par la suite, l'humidité tutllllintenue entre .50 et
60%
(H.R.). Au bout de 10 l 12 jours, les pre-miers a,m.pt6mea de l'infection .tirent leur apparition. La tavelure apparaissait surtout sur les plus jeunes feuilles.E • LA. CUZTURE SUR PELLICUlE DE OELWPH1RB
Lors des études de croissance, le champi gœn tut cultivé sur pelliCUle de Cellophane M.S.T • .300 (DuPont of' Canada, Limited). Selon les u.nu.tacturisrs 1 cette pellicule end:Oit~ d •une substance visant l la rendre im:perm.éable a uœ épaisseur de 0.001 pouce. Pour les·
21 exp6rie:aces le recouvraent iapel"'lléable fut enlari par ialersion de la
Cellophane dal'la de l'eau bouillante. La Cellopbaœ perm.6able ail!uli obtenue, tut coup6e en morceaux qui turent fiDs sur Ul'l anaeau da verre
(17 mm da diallatre) du type utilisé pour lea cellul•s de Vm Tiegbem, l 11aide d •uœ baDde élastique. L'anneau lllUli da la pellicule tut en-suite déposé daDa u.œ botte de Pétri contenant Ul'l milieu de culture
liquide (eau de pommes 1 de terre glucosée: 40g de tubercul.es/1,
Sg
glu'-cose/1), la Oellopha:œ 6tant en contact avec le IB:i.lieu. La surface su-p6rieure de la pellicule tut eœemencée avec uœ suspension de spores préparée de la taqon décrite préc6daaaent. Les bottes de Pétri turent alors plac6es dans Ul'l incubateur l 16.
SOc.
La germination et lacrois-sance du champignon turent observées l intervalles réguliers pendant
1ÙI8 seJE:Jœ.
F - IA 'l'ICIŒIQUE tr.l'ILISD J.U COURS DES ESSAIS DE GERMINATION
Au cours des études sur l 1intluence des lixlv:iats sur la
gend-nation des conidies de
!•
inaegualis, nous avona suivi de trt\s pris les techr:d.ques rec0l11118lldées par l'American J:lbTtopathologicalSociet,-(1943) pour les essais sur 1 1intluence des fongicides sur la germi-nation des spores des champignons.
1. LI NET'!OYAΠDES UMES DE VERRE
Les lames de verre utilisées ( 75 x
25
mm.) turent :œtto,'ées avec uœ solution d •acide sulfurique et de bichroEte de potassiml.. Ellesoonte•nt du bioar'boœte de aodi11111 et fiœ.lemant r11106ea p1uaieun .tois daDa de l 1eau diatill6e et a6ch6e entre deux oouobes de papier
filtre.
2. Ll PREPARA.TIOH DE LA. SUSPBBSION DE SPORES
Dea auspeœions p:rowœnt de cultures tg6ea de 10 & 12 joUl"S ·
.turent prépariea de la .taçon d6cr1te pr6o6de.aent. La ooDCentration des spores dans la auspeœion fut déterm:1D6e l l'aide d'an haemocyto-llltre.
La
suspension .tut par la suite d1.J.uAe de façon 4 obtenir uœ concentration d •env.t.l'onSSO,ooo
spores/:ml..3.
U: MEUR GE DIS LIXIVIATS BT DE Ll SUSPBIISIOWDE SPODS
:X.s lixiri.ats .turent a6l.augû l la aupe•ion de spores l raison de 1 :ml. de lixiv.l.ats par 0.1 Ill de la supeuion de spores
de aorte que ~ coacentration tiœle· dea spores daD8 le Él.a.Dp
6tait de
SO,ooo
spores/ml.4. ·
IlS ESSA.IS DE OBRMID.'l'IOMPour les essais de pr.ad.ration, des bettes de Pétri im'erties sel"'t'irent de· chambres l haute hulliditê. Le .tond de la chabre tut cov.wrt d •une feuille de papier filtre humide sur lequel .tut plac6e
une tige de verre recourbée en U deva.nt servir de support l la 1.aa
de wrre. Sur chaque bout de la laa de verre, une goutte du
23
les deux parties de la chambre furent scellées &"f'ec de 11eau
distil-168 de façon A ce que l'humidité relative A 11int6rieur fut l peu Pl"~• de 100% et l'évaporation réduite A un milliJIUDI. Les bottes de Pétri turent alors incubées A
16.SOo.
pour uœ durée de2h
heures.A la f'in de cette période, chaque goutte sur la lame de wrre tut e:xa:m:i.née au microscope A un grossissement de 12$ I. Les spores germées et non germées turent comptées de façon A ce que le total des deux comptes soit supérieur l 100. Iss spores turent couidé-rées gel"JJées lorsque la loDgœur du tube germinatif excédait la moitié du plus petit d.iamêtre de la spore. La loDgUSur du tuba ger-:m.iœ.tit ne fut pas prise an considération vu qua généralement, le
pourcentage de germination et la laqueur du
tube
germinatif' sont étroitement reliés. Dans ces expériences, le témoin eaploy-é consis-tait en uœ suspension de spores germées dans de l'eau distilUe.G. - LA. TECHNIQUE DE REOOLTE DES LIIIVIATS
La
récolte des lix1Viats se f'it salon une méthode employée par Long!!
.!.!·
(19.$6&). Un arlamae:,yar surmonté d'un eD.tonnoir en verre fut placé an-dessous des feuilles d •un pœaJ er.La
l.ix:l:via-tion se fit par pa.lvérisal.ix:l:via-tion d •eau distillée sur les feuilles l l'aide d'un pulvérisateur De Vilbiss de t:,r.pe GDS. L'air comprimé(20 lb. par pouce carré) pour la Taporiaation provenait d •un compres-seur De Vilbiu (Figure 1). la vaporiaation d •eau sur las feuilles se fit de telle façon que saule 1 •eau veœnt en contact avec les feuilles coulait dans l'entonnoir at était récoltée. La lixhiation
Figure 1 - Technique utilisée pour la lixiviation des feuilles de pommier. A l'extrême droite, le vaporisateur avec les tuyaux d'ar-rivée d'eau et d'air comprimé.
2S
se poursuivait pour une dur6e de
24
heures. Au bout de cette période,le volae des lixl:viats rkolté1 tu.t •auré, l.es li:x:i:viats turent ensuite concentrés par mporation sous "vide partiel dans un évapo-rateur rotatif. Le volume total f'ut ainsi réduit
t
quelquesmilli-litres et utilisé tel quel pour les essais de ge:nr.d.nation.
R.- L tAD.LYSI DES LIIIVIATS
tes informations sur la nature chi:mique des substancea
pré-sentes dans les lix1 viats ont été obtenues par fractionœ•nt et chromato&raphie des li:x:ivia.ts selon les tecb:niques éœncées ci-apris.
(Figure 2).
1. SEPARATION SUR COJ..OHliES D tJ:ŒA.RGIU:RS D'IONS
Une f'ois les li:xiviats réduits l un petit volu:me, ils furent séparés en deux f'ractiona (acides llllinés et sucres) A. 11 aide de
co-lonnes d'échangeurs d1ions. Cette méthode perattait 61a1ement
l'éli-mination des ions inorganiques qui nuisaieut l la séparation des aci-des aminés et aci-des sucres par chraatog:raphie. Les lix:l 'Via ta turent tout d •abord passés l travers une colonne d •échangeurs de cations
(Amberlite IR-120 (:e:t) Robm & Baas Co.). Sur cette colonne, les aci-des aminés et les cations inorganiques sont retenus. Les sucres, lss substances organiques neutres, les anioœ inorganiques et les substances organiques chargées négativement passent l travers cette colonne sans être retenus. Cette traction f'ut donc passée l travers une colonne d1échangeursd'anions (Dowex l-IB. Dow Ohemical of'
canada
LIXIVIATS
1
CONCENTRATIONl
COLONNE .. D'~CHANIEURS D'IONS (AIIBERLITE IR-120(tt+)) ·!
ÉLUnON (4N NH4 0H) ·.
,
. ACIDES AMINES1
CONCENTRATI.ON. CHROMATOGRAPHIE CG-CHROMATOGRAPHIE1
IDENTIFICATION ANALYSE QUANTITATIVE - NINHYDRINE . -FILMSÀ
RAYONS X COLONNE D'ÉCHAN~EURS r(IONS. (DOWEX . 1~-8
( dtr)). 1
EFFL~ENT
SUCRES ET SUBSTANCES: NEUTRES
I
~TION
... ! . '• ' ,. f CHROMATOGRAPHIE CO-CHROMATOIRAPklt·1
IDENTIFICATION . ANALYSE QUANTITATIVE - ANISIDINE-P04'
-FILMS A RAYONS X -SPECTROMÈTREÀ
SCINTILLATEUR LIQUI~ . j,
·:~FIGURE 2- SCHEMA ILLUSTRANT . L'ORI)RE • DE· SUCCESSION DES TECHNIQUES UTILISÉES LORS DE
L1ANALYSE .. DES LIXIYIATS
Ltd. ). Cet écbarlgeur d'anions est vendu sous forme de chlorure (Cl-), il
tut
transformé en forme ( OH•) l l 1aide d 11Qàro:qrde . de sodium(10% p/v). Sur cette colonne les anions turent retenus mais les su-crea et les aubsta.Dces organiques œutres œ turent pas affectés et furent récoltés directement l la bue de la colonne. Les acides ami-nés retenus sur la colonne d'A:mberlite IR-120 furent Alués l l'aide d'ammo~ (4N). Les deux tractions ai.Jlsi récoltées (acides
ami-nés, sucres) furent concentrées sous vide partiel, l un voll11118 d1
ap-pro:r:1JIIativement l ml et utilisées pour la chro•togra.pbie.
2. TECHNIQUES DE CHROMATOGRAPHIE
.,
a} Chroatographie dea acides aminés.
Les acides aminés furent séparb;: par ehromtogra.phie
descen-dante bidimensionnelle sur feuilles de papier Whatman no. 1 (46 cm x
S7
ca). ·Deux lignes au cra,.on turent tracées sur le papier l8
CDt du bord et parallAles l•uœ âu coté le plus loug de la teuilJ.effèt l'autre à.u eetê la plus court. Cinquante &·llO gouttelette~ de 2 l3
microlitres chacune furent d.épos6es A 1.1interaeotion des deux lignessur la feuille l l'aide d'un JRioropipette., La tache ainsi formée tut séchée l 11aide d •un a6ohoir
A
chewux après chaque awlication. Lesfeuilles d.e papier turent ensuite placées daœ uœ cuve l chrouto-gra.phie et ensuite irriguées awc les solvants mentiows ci-desaous.
Trois aéthodes furent emploJ'ées lors de la ·séparation dea aci-des Ul'1nû. La premüre méthod.e oonaistait 1. irriguer les feuilles
ca:pos6 de butaDol, acide ao6tique, eau {67:10: 27 v/v/v){Weinbold, 1961). Aprtla cette prelldJre irrigation, les papiers t't:lreut a-'chû et vaperisû avec uœ aolation de tupen phosphate (pH 12.0), pré-paré dans les pr-oportiorœ suivantur $0 ml de o.o67 M BaH2:m4 et $0 lll de o.o67 M BaOH (McFarre:a, l9Sl). Apn\s s-'chage, les feuilles
de papier
turent
plac6ea daM 1II.D8 aatre cuve .l chro•tographie et 6qu1Ubr6es au cours de la ,Jluit dalla les vapeurs se d6ga.geant d •une solution de ph6nol et d •eau ( 80:20 v/Y). Ellesturent
ensuite ir-riga.6es dans leur plus grande dia:aaion avec un solTant composé de phénol fra1~nt distillé et de solution tapon phosphate (pH 12.0) dans les proportions suivantest p'b.6aol 80, tampon 20 v/v. A cesol-.
va.nt
nous avons ajouté o.o4% dfhldro:çquinoliœ pour retarder la dé-coaposition du ph6nol (Block, Durrw. et Zweig, l9S8).La d.eux:l.iD Jéthode était sellblable .l la prelldJre_, saut que la
papier œ tut poiut w.porisé avec la aolution tapon •.
La troisibe a6thode (:Misell ·et Si111:pson, 1961) comportait deu
solvantSJ le premier composé de butaDol, d'acide acétique et d'eau
(2S:6r2.5 v/v/v)(Woivod, 1949) et la second coaposé de butaool, de aéthyléth7lcétone et d'eau (2:2:1 v/v/v). Uœ cuvette contenant de la oyclohel!l'lala:i.œ (t raison de l ml par 2S ml de solvant) était
pla-cée dans le fond de la cuve l chroatographie. Les vapeurs de ce coa-posé pezwttent d'obtenir des couleurs plus distiœtiws pour les acides aminés lorsque le chromatograaae est n.poria6 avec la
'29 b) Chromatographie des sucres.
La séparation des sucres se fit par chromatographie unidimen-sionnelle descendante dans certaines expériences, ascendante dans d'autres, sur papier Whatman no. 1. Le papier fut irrigué â deux
reprises avec un solvant composé d •acide propionique, méthyléthylcétone et d'eau (25:75:30 v/v/v)(Himes, Metcalf'e et Ralston, 1961), le papier étant séché entre la premiêre et la deuxiême irrigation.
,3.
IDENTIFICATION DES ACIDES AMINES ET DES SUCRES a) Identification des acides aminés.Les acides a:minés sur les chromatogrammes obtenus furent iden-tifiés par la couleur de la tache formée aprês réaction avec la
nin-hydrine, par la position des taches les uœs par rapport aux autres, et par comparaison des chromatogrammes obtenus avec d'autres chroma-togra.nnnes témoins.
(~) Réaction des acides aminés avec la ninhydri.ne.
Les acides a:minés sur les chromatogrammes obtenus par irriga-tion avec les solvants butanol-acide acétique-eau et, phénol-tampon furent révélés par un réactif composé de o.5% {p/v) de n:inhydrine dans de l'acétone contenant 10% (v/v) d'acide acétique glacial. Les
chromatogra.I~~~œs furent rapidement trempés dans cette solution et en-suite suspendus dans uœ hotte et séchés. Les couleurs se dévelop-pêrent à la température ambiante {20 - 25oc.) et dans. le noir pour une période de 18 heures. Les acides aminés se révêlent sous la forme de taches bleuâtres ou pourpres avec ce réactif.
Ies acides aminés sur les chromatogrammes obtenus par irriga-tion avec les solvants, butanol-acide acétique-eau et, butanol-méthylé-thylcétone-eau, dans une atmosph•re saturée de vapeurs de cycloheJC;,Y-lamine furent révéUs. avec une solution de
0.25%
(p/v) de ninhydrine dans de l'acétone contenant7%
(v/v) d •acide acétique glacial. ,les chromatogrammes furent rapidement trempés dans cette solution et ensuite placés dans une étuve !45°C.
pour 1.5 minutes. Les acides aminés ainsi révélés apparaissent bleuâtres ou pourpres, avec aussi dea couleurs caractéristiques pour certains de ces acides aminés,..
,
(tryptophane, brun-gris; histipe, gris-vert; hydroJC;,Yproline, carmin; asparagine, beige).
(ii) Comparaison des chromatogrammes obtenus avec des chromatogrammes témoins.
Lors de chacune des expériences, la chromatographie des subs-tances présentes dans les 1ixi 'Viats se fit de concert avec la chro-matographie d •acides aminés authentiques. POur. ce faire, une solu-tion comprenant les
24
acides aminés suivants fut préparée: phéeyla-la.nine, leucine, isoleucine, thréonine, méthionine, tyrosine, valine, sérine, histidine, acide cystéique, proline, alanine, hydro~oline,glycine, cystine, (l-alanine, cystéine, lysine, arginine, acide gluta-mique, glutamine, acide aspartique 1 asparagine 1 ainsi que l'acide
1-aminobutyriqœ. La concentration de chaque acide aminé dans la solution était de 20 ~~ml d1eau distillée contenant 10% v/v
d'iso-propanol et juste assez d'acide chlorhydrique (2N) pour permettre la dissolution des acides aminés (Block et
!!•
11958).
Une solution31
de tryptophane (20 IJ.M/1111.) dans 10% v/v d'isopropanol .tut égale•nt préparée. Quelques gouttes de la solution d'acides aminés et de tryptophane .turent déposées sur une .feuille de papier Whatman no. 1; celle-ci .tut ensuite plao6e dana une cuve 1. chromatographie et ir-riguée avec les mêMs solvants que ceux employés pour la cbroato-graphie des acides aminés dans les lix:lv:Lats. IDrsque développé, avec la ninbydriœ, le chromatogramme obtenu et la position connue de chacun des acides aminés sur ce chromatogramme permirent l'iden-tification, par comparaison, des acides aminés présents dana les 1ix:l v:Lats.
b) Identif'ication des sucres.
Les sucres furent révélés 1. l'aide d •une solution de po-ard.ei-dine-phosphate et identifiés d •aprtls la position des taches par rap-port l celle de sucres authentiques sur des chro•togr8JIIIles témoins.
(1..) Rivélation des sucres avec la p-anisidiœ-phosphate. Nous avons emplo;yé le réactif de Mukhergee et Srivastava
(19,2) qui se prépare comme suit: dissoudre o.,Sg de p-anisidi.ne dans
2 ml H3
Pû4
(gravité spécifique 1. 7$), compléter le volume l $0 1111. avec de l'éthanol. I.e phosphate d 'anisidiœ f'ormé est retiré par fil-tration. I.e filtrat obtenu (.!) est gardé. I.e précipité est ensuite dissous dans uœ quantité :minimum d'eau distillée et le tout dilué avec une quantité égale d • éthanol. De 1 •acide phosphorique est alors ajouté jusqu •l une concentration f'inalè de 2% v/v pour f'or.mer la par-tie (B). (A) et (B) sont alors mélangés et les ohromatogr8lllllesvaporisés avec cette solution. La révélation des couleurs se fait A
95 -
100°C. pour une durée de 3 à5
minutes.Avec ce réactif les aldopentoses apparaissent brun•foncé; le fructose, jaune-citron; le rhamnose, brun-rosé; les aldohexoses, brun-clair; le sucrose, jaune-brun; le raffinose, brun-jaune et les acides glucuroniques produisent une couleur rose.
(ii) Comparaison des chromatogrammes obtenus avec des chromatogrammes témoins.
La
chromatographie des sucres dans les ,lixiviats se fitparal-l~lement à la chromatographie d'une solution de sucres authentiques. Cette solution de sucres étant composée de ribose, d1arabinose
1 de
fructose, de glucose, de sucrose et de raffinose; chaque sucre étant d'une concentration de 150 mg/ml de solution. Quelques gouttes de
cette solution furent déposées sur une feuille de papier Whatman no. 1, celle-ci fut placée dans une cuve à chromatographie et irriguée avec le
même solvant que celui employé lors de la chromatographie des sucres dans les lixiviats. Lorsque développé avec le réactif p-anisidine-phosphate, le chromatogramme obtenu et la position connue de chacun des sucres permirent l'identification par comparaison, des sucres présents dans les lixiviats.
I.. BCHIIQUE U!ILISEE LOBS DB LA. PHO'J."'SYBTHESE DAHS UNE ATMOSPHBRE ENRICHIE DB
o1ho
233
Lors de nos expériences sur l'intluence de la tavelure sur la quantit~ et la nature des substances présentes dans les lixiT.iats de feuilles de pommier~ nous aTOllS procédé l la lixiviation de fev.illes sai:œa et tawl6es ayant prûlablelllent fixé du
clbo2
par pbotoa;yntblse.Nous avons procédé selon la techniqa.e d~crite ci..apris (Figure
3).
Les t•tes de deux arbres, l'un taveU et l'autre sain, .turent recouwrtes d •un sac de poq~thylAœ solidtmeat attaché aux troD.ca des arbres. A l'int~eur du sac, un bêcher contenant; une solution de
la
2
~
(activ.Lté totale , lllillicurie) .tut attaché au tronc de 11un des arbres. Leo%
2 tut libéré de cette solution par addi-tion de 2 l
3
ml de H Cl04 l60%
l l'aide d •uœ seringue piquM dans le sac de po~thylAœ. Les feuilles f'bl):rent leclbo2
par photo-qllthèse durant une helll;"e; l la fin de cettepériode~
leo1ho
2 DOn fixé tut absorbé dans une tourl
absorption contenant7$
ml de O.lll Na.OH au moyen d'une pompe électrique.Le sac de poqêteyl.êne tut alors enlevé et les arbres retour-née dans la chambre de croissance pour un repos de
48
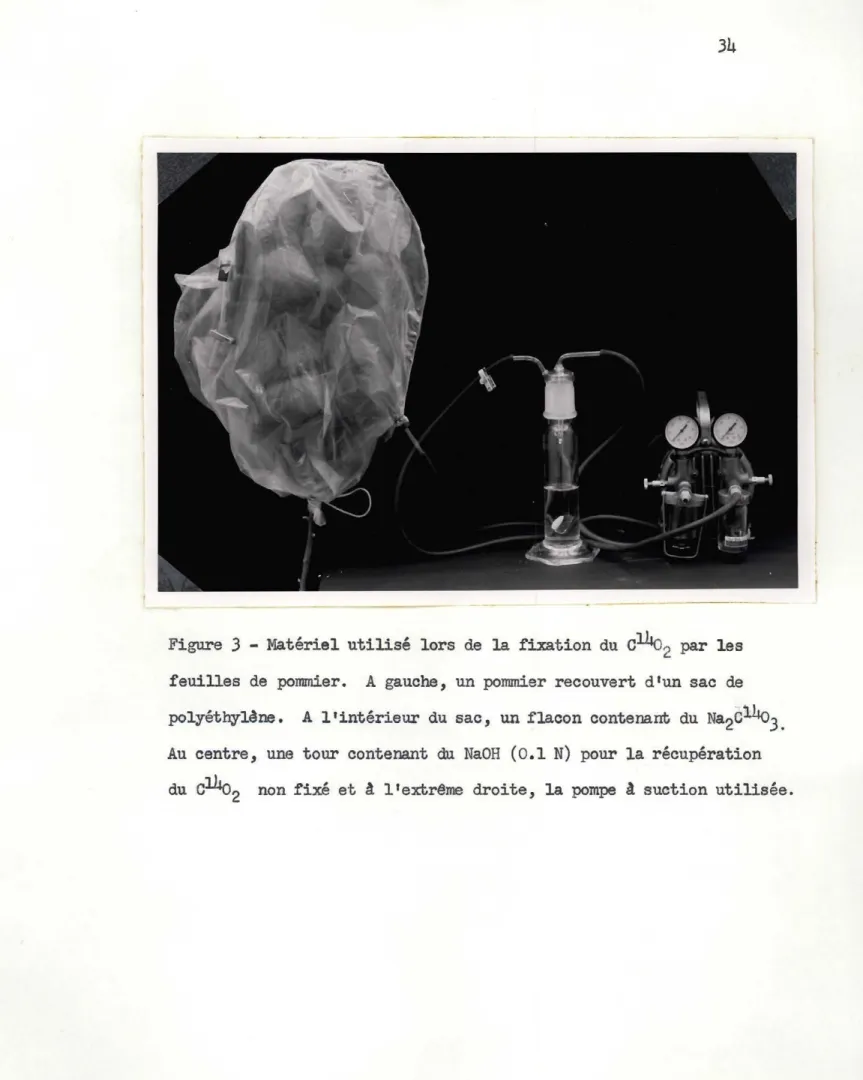
heures avant la lixi via ti on.Figure
3 -
Matériel utilisé lors de la fixation duc14o
2 par les feuilles de pommier. A gauche, un pommier recouvert d'un sac de polyéthylêne. A l'intérieur du sac, un flacon contenant du Na2
c1~3
. Au centre, une tour contenant du NaOH (0.1 N) pour la récupération duc14o
2 non fixé et â l'extrême droite, la pompe â suction utilisée..3S
J - REOOI4'I DES LIIIVIATS RlDIOACTIFSSur le pommier' tavelé, toutes les feuilles démcmtrant dea IIJIIlP'tO.s .turent gardées sur l'arbre. Les feuilles saiaea .tùrent enla'riea. SUr 1 'arbre tâoiD, UD DOJibre de feuilles saines 6gal au DDIIIbre de feuilles alades t'ut J.aüaê. les feuilles laissées
sur l'arbre sain oocupaient aœ puition correspoDda!rl;e l la posi-tion occupée par les feuilles sur l'arbre tavelé. les deux arbres
(sain et tavelé)
.turent
alors soumis l la lixiviation pour une durée de24
heures.Les
lix:l:ri.ata aiœi r6coltês.turent
concen-trés et séparés en deux fractiona {acides aminéset
aucres) 4 l'aide de colonnes d1éohangeurs d'ioœ. (Voir· Section H).X- CO-CHRClMA!OGRlPHD ft A.UfOBADIOGRAPHIE DES LIXIVIATS UDIOACTIFS
La chro•tograpb:ie des lixiviats radioactifs se fit de l a . _ façon que la chro•tograpbie des lixi.Tiats non radioactifs. Cepen-dant, la solution d 1acides aminés et de sucres autheDtiquea .tut
éga-le• nt appliquée
a
l'origine sur les feuilles de papier portant res-pectivement les acides aminés et les sucres radioactifs.Apr•s chroatogÏ-apbie, les chroatogr&JIIII8s portant les acides ami.nlls et les sn crea
turent
marqués d •un signe distinctif avec del'encre radioactive pour permettre l'identification 8Ubaéquente des
chro•togr&~~~~~es; chaque chro-.tog:rat~~~~e .tut alors
placé
sur un film l ltay'oœ I sans éoran (Oanaà:lan Kodak Co. Ltd}, et le tout placédisposé dana une presse
toraât
de deux plaDchas de boia serrées en-sablAt par des vis A pression et le tout placé dans uœ boite t 11é-preuve de la lmli•re. Laa bottes furent placées dans une chambre froide gardée
t
UD8 température de6
t
aoc.
juaqu •• exposition sut-tisant• des films A Rayoux.
Au bout de cette période~ les films A Ra)"'DS X turent déve-loppés dans du révélateur Kodak D-19b pendant
3
llinu.tes A 1lD8tea-p6rature de 200C. et tix6s dans du tilrateur F-7 pendant 20 milmtes (Baadbook
ot
Cb.c!md.at17am
Ph78ios, 1941, Ohemioal Rubber Publishi.Dg Oo., Clewland, Ohio). Les til.Bs turent enauite lavés dans l'eau pendallt au 110i.Ds trois beures.Dana certains cas, les taches obtenues sur les Ba;,oœ X étaient
d8
ta:ihle iDtensit,. Ces films .turent donc immergés dans uœ solution intensitiante telle que décri te par Blake, Roderick et Ulllberger et 'VOici couaent se tait cette préparation:Solution A. Solution B. Solution
c.
Eau (:t 2100.) .A:oide digl.Joollique Bydrox:;vde de aodiua Eau (± 21°C.) Nitrate ferrique • 9HZ 0 Fluorure de potassium .2 H2 0 Eau (± 21°0.) Ferricyanure de potassiUII. Nitrite de sodium Volwae total:?SO.O
ml.6o.o
g •36.0
g. 100.0 ml.lh.O
g. 1.0 g. 100.0 ml.s.o
g. 1.0 g. 1000.0 ml.37
Les ingr6d1ents pour la préparation dea solutions A, B et C sont ajoutés dana 11ordre prescrit et dissous avant l'addition du
sui"V''lnt. Verser la soluti.on B dans la solution A en deux miœtes en agitaut. Ajouter la solution C aux solutions A et B en deux mi• nutes en agitant. Agiter le tout pendant une mimte.
Le film. l intensifier est i.JErgé dans la solution i.Dtensi-fiante préparée pour une période de 2 l 8 minutes, selon 1 'inten-sification désirée. L'inten'inten-sification se fait l la lumitlre ordinaire. la fillll est ensuite lavé l 1 •eau pour uœ durée ma.ximnm de
S
minutes. laa taches sur le film. rêsultan:t apparaissent bleu foncé. Si onregarde le film l la lUDliare rouge, on peut obtenir une augmentation de vitesse du film d'A peu pres cinq fois: c'est-à-dire, le même ré-sultat que 1 1 on obtiendrait apris e:xposition du film au
chromatogram-me radioactif pour une période cinq fois plus longue, sans utiliser 11intensitication.
Apris développeœnt des films, les chromatogrammes turent trempés dans les réactifs spécifiques pour les acides aminés et les sucres. L'identification se fit par superposition du film â Rayons X sur le chromatogramme; une substance fut considérée identifiée lors-que la tache formée sur le fil:il correspondait A la tache formée par cette substance connue sur le chromatogramme.
~ - UTILISATION DU SBSOTRDMETRE A SCINTILLATEUR LIQUIDE
le spectromt!tre â scintillateur liquide Tri-carb, série
3l..4E
( Packa.rd Instrument Oo. , La. Orange, Illinois), est un instrument bien adapté pour le comptage de substances â faible radioacti vi. té. Nous l'avons donc employé pour déter:m:i.œr de façon quantitati-ve la radio-activité relative sur chromatogrammes. Chacun de ceux-ci {des bandesde papier mesurant
35
A40
cm de long par4
cm de large) furent dé-coupés sur la longueur en languettes de0.5
cm x4
cm. Chaque lan-guette fut nwnérotée et déposée en diagonale dans une bouteille de verre spécialeœnt conçue pour le spectromêtre (Pa.cka.rd Instrument Co.), et l 1on versa15
ml d •une solution scintillante dans la39 (1,
4,
bis - {2-5- pheeylo:rayo:cyl) (-be~ne), 5.0g/l PFO (2, 5-d.:i-pheuyl-o:myol), 1000 ml de toluène (•sc:l.Dtillation grade•). Les deux premiers ingrédi.ents furent obtenus de Pa.ckard InstrumentCo.,
et le tolwl:œ de lluclear Enterprises, Wirmipeg, Canada. les bouteilles i'u.rent ensuite placées dans le spectromêtre et analysées pour leur teneur en radioactivité sous les conditions suivantes de l'appareil:11Tap voltagett pour el4, 5.25 (lo85 volts); A' •settingll lOO (•monitor
base line"); "Gain controls" 1000; A, C, "settings" lOO; B, D, "settings" 1000. Chaque échantillon fut compté jusqu •l l'accumulation d •un total de 1000 cpm de façon l obtenir un pourcentage de déviation égal l
3%.
Chaque échantillon fut compté trois fois, et la moyenne des trois comptes prise comme résultat final.AprE}s le comptage de tous les échantillons, les languettes de chromatogramme.