Mobilité de l'arsenic dans les sédiments de lacs
subarctiques contaminés par l'activité minière.
Mémoire
Emilie Leclerc
Maîtrise en chimie - avec mémoire
Maître ès sciences (M. Sc.)
Mobilité de l’arsenic dans les sédiments de lacs
subarctiques contaminés par l’activité minière
Mémoire
Émilie Leclerc
Sous la direction de :
Résumé
L’objectif de ce mémoire est de quantifier la diagenèse de l’arsenic (As) dans les sédiments, d'utiliser ceux-ci comme archive environnementale et d’identifier les réactions clés de l’As. Huit lacs ont été visités en juin 2018 et mai 2019, le long d’un transect de 80 km au nord-ouest de la mine d’or Giant, à Yellowknife, dans les Territoires du Nord-Ouest, Canada, pour y prélever de l’eau de surface, des carottes de sédiments et de l’eau porale. Ces échantillons ont été analysés afin d’obtenir les concentrations dissoutes et solides de carbone organique, d’As, de fer (Fe), manganèse (Mn) et d'aluminium (Al) et des anions nitrate, sulfate, sulfure et chlorures. Les concentrations d’As dans l’eau porales ont été interprété à l’aide de la modélisation diagenétique inverse et de calculs thermodynamiques.
L'historique des flux d’As solide déposés au fond des lacs a été calculé après correction pour l'influence de la diagenèse. Les flux diffusifs d’As à l’interface eau-sédiment en réponse à la contamination causée par l’activité minière ont été calculés pour les deux années d'échantillonnage. Les résultats montrent que la diagenèse est plus importante dans les lacs avec des taux de sédimentation plus faibles. Après correction, les données indiquent que les flux d'As maximaux coïncident avec la période d'activité de la mine. Néanmoins, les lacs près de la mine sont toujours sous l’influence d’apports importants d’As dissous depuis leur bassin versant, et montrent des flux diffusifs élevés d’As vers la colonne d’eau.
Les calculs thermodynamiques de spéciation et des indices de saturations suggèrent que la mobilité de l'As est liée à celle des oxydes de fer et au soufre. Le sulfure de fer amorphe se forme dans les sédiments et l’As co-précipite ou s’adsorbe sur cette phase minérale. Enfin, le moment de la fonte du couvert de glace, qui permet l’arrivée de l’oxygène, semble déterminer la mobilité de l’As au printemps. Dans le contexte où les changements climatiques influencent la durée du couvert de glace, une étude approfondie de l’effet du couvert de glace sur les conditions d’oxydoréduction est souhaitable.
Abstract
The goal of this thesis is to quantify the diagenesis of arsenic (As) in the sediments, using them as environmental archives and identify the key reactions of As. Eight lakes have been visited in June 2018 and May 2019, along an 80 km transect northwest from the gold mine Giant, near Yellowknife in the Northwest Territories, Canada to collect surface water, sediment cores and porewater. These samples have been analyzed to obtain the dissolved and solid concentration of organic carbon, As, iron (Fe), manganese (Mn) and aluminium (Al) and anions (nitrate, sulfate, sulfide and chloride). As concentrations in porewater were interpreted using inverse diagenetic modeling and thermodynamics calculations.
The history of the fluxes of solid As deposited at the bottom of the lakes was calculated after correction for the influence of diagenesis. Diffusive fluxes of As at the sediment-water interface in response to contamination from mining activity were calculated for the two years of sampling. The results show that diagenesis is greater in lakes with lower sedimentation rates. After correction, the data indicates that the maximum As fluxes coincide with the period of mine activity. Nonetheless, lakes near the mine are still influenced by large inputs of dissolved As from their watersheds, and show high diffusive fluxes of As to the water column.
Thermodynamic calculations of speciation and saturation index suggest that the mobility of As is related to that of iron oxides and sulfur. Amorphous iron sulfide forms in the sediment and As co-precipitates or adsorbs to this mineral phase. Finally, the timing of the melting of the ice cover, which allows the arrival of oxygen, seems to determine the mobility of As in the spring. In the context of climate change shortening the duration of ice cover, an in-depth study of the effect of ice cover on redox conditions is desirable.
Table des matières
Résumé ... iii
Abstract ... iv
Table des matières ... v
Liste des figures ... vii
Liste des tableaux ... ix
Liste des abréviations ... x
Remerciements ... xii
Avant-propos ... xiv
Introduction ... 1
i. L’arsenic ... 1
ii. Contamination à l’arsenic par les activités minières au Canada : Le cas de la mine Giant, Yellowknife, Territoires du Nord-Ouest. ... 3
iii. Objectifs ... 8
iv. Sites d’études ... 9
v. Les sédiments comme archives environnementales ... 10
Chapitre 1. Quantifying arsenic post-depositional mobility in lake sediments impacted by gold ore roasting in sub-arctic Canada using inverse diagenetic modelling ... 17
1.1 Résumé ... 17
1.2 Abstract ... 18
1.3 Introduction ... 18
1.4 Materials and Methods ... 20
1.5 Results ... 25
1.6 Discussion... 32
1.7 Environmental Significance ... 34
1.8 References... 35
Chapitre 2. Influence des changements saisonniers sur les conditions rédox et la mobilité de l’arsenic ... 40
2.1 Introduction ... 40
2.2 Matériels et méthodes ... 43
2.3 Résultats. ... 45
2.5 Implication sur la mobilité de As causée par les changements climatiques. ... 64
2.6 Conclusion partielle. ... 64
Conclusion ... 66
Bibliographie ... 68
Annexe A. Concentrations mesurées dans les eaux porales en 2018. ... 76
Annexe B. Concentrations mesurées dans la phase solide en 2018. ... 84
Annexe C. Concentrations mesurées dans les eaux porales en 2019. ... 100
Liste des figures
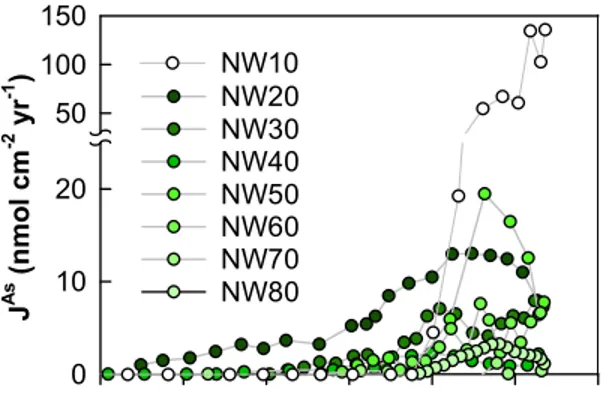
Figure 1. Réactions typiques de l'As avec le fer et le soufre dans les sédiments. Adapté de Henke (Henke, 2009). ... 2 Figure 2. Emplacement de la mine Giant près de la ville de Yellowknife, dans les Territoires du Nord-Ouest (Fawcett et al., 2015). Rose des vents qui présente combien d’heure par année le vent provient de la direction indiquée. Le vent souffle en grande partie de l’est vers l’ouest et du sud-est vers le nord-ouest. (Galloway et al. (2018)). ... 4 Figure 3. Distribution des concentrations d'arsenic dissous dans l'eau de surface des lacs situés autour des mines Giant et Con (Figure crée par Izabela Jasiak, à partir des résultats de Palmer et al., 2015). ... 6 Figure 4. Localisation du site d'étude et des huit lacs du transect ainsi que la mine Giant. ... 10 Figure 5. Schéma de la chaîne de désintégration de 238U et de la répartition du 210Pb dans l’environnement. Adaptée de Oldfield and Appleby (1984). ... 12 Figure 6. Exemples de profil de concentration d’eau porale (Bohrmann et al., 2006). ... 13 Figure 7. Exemple de correction d’archive sédimentaire (Couture et al., 2008). L’encart en bas à droite représente la mobilité de As ({As}diag). À gauche, le profil mesuré (en vert) est similaire au profil historique corrigé (en blanc). À droite, le profil mesuré est différent au profil historique, montrant un besoin de correction pour la diagenèse. ... 16 Figure 8. Porewater concentration profiles of Fe (pink squares), Mn (blue diamonds) and As (circles) at each site, along with modelled As (thin red line) and net reaction rates (thick blue line) calculated with PROFILES. Goodness-of-fit between model and data (R2) is indicated in the lower right corner while modelled fluxes through the SWI (J; µg cm-2 yr-1) are given in the top right corner. ... 25 Figure 9. Present-day diffusive As fluxes across the SWI (µg cm-2 yr-1 and nmol cm-2 yr-1 ; vertical bars) calculated with the code PROFILE along with porewater [As] (at peak concentrations, green circles) and surface water [As] (black circles) for each lake. ... 28 Figure 10. Depth profiles of measured sedimentary Fe (squares; mmol g-1 d.w.) and Mn (diamonds; µmol g-1 d.w.) along with solid-phase measured (green circles), diagenetic (open circles; see section 2.6) and corrected for the influence of diagenesis (black circles) As concentrations in each lake. The interval (1949-1999) of the mine operation obtained from 210Pb dating is highlighted in yellow for each core. An example of the dates obtained is shown in the NW40 profile. ... 30 Figure 11. Reconstructed records of anthropogenic As deposition fluxes (JAs) in the sediments for lakes NW10-80. ... 31 Figure 12. Inventories of As measured (µmol cm-2 g-1 d.w.; green bars), corrected for diagenesis (black) and corrected for measured vs expected 210Pb inventories (dashed) at each site. ... 32 Figure 13. Variations annuelles des concentrations en As dissous (cercles, µg L-1), antimoine dissous (losange, µg L-1) et les ions majeurs (étoiles, mg L-1) dans la colonne d'eau de Handle Lake (figure tirée de Palmer et al., 2019). ... 41 Figure 14. Profils de concentration de COD dans les eaux porales pour chacun des lacs. À noter qu’un seul échantillon pour NW70 n’a été recueilli pour l’analyse par manque de volume lors de l’extraction aux autres profondeurs. ... 46
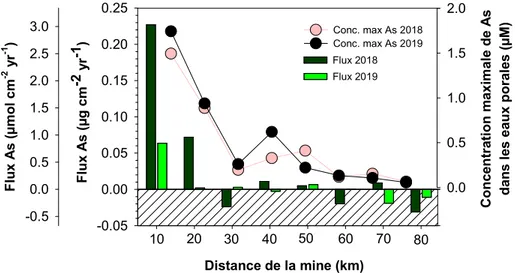
Figure 15. Profils de concentration de l'Al dans les eaux porales pour chaque lac. ... 47 Figure 16. Profils de concentration de As dans les eaux porales en 2018 (cercles rouges) et en 2019 (cercles noirs). Noter les différences dans les axes de concentration selon les lacs. ... 48 Figure 17. Flux diffusifs actuels de As à l'interface eau-sédiment pour 2018 (barres vert foncé) et 2019 (barres vert pâle) ainsi que les concentrations maximales de As dans les eaux porales pour 2018 (rouge) et 2019 (noir). ... 49 Figure 18. Profils de concentrations dans les eaux porales de Fe (carrés orange 2018; carrés brun 2019) et Mn (losanges vert pale 2018; vert foncé 2019). ... 51 Figure 19. Profils de concentrations des SO42- (carré blanc) et
S2- (cercle jaune) dans les eaux porales. Noter la différence dans les axes pour le lac NW40. ... 52 Figure 20. Profils de concentration en soufre (S) dans le sédiment (en % et en mmol g-1). ... 53 Figure 21. Profils de concentrations de As mesurées (noir) dans les eaux porales avec la simulation réalisée par PROFILE (ligne rouge) et les taux nets de réaction (ligne bleu) (a-d). Profils de concentration de As(III) (en mauve) et As(V) (en rose) dans les eaux porales (e-h) ainsi que les profils de concentration en Fe(II) (en brun) et Fe(III) (en orange) (i-l) et les indices de saturation (m-p) pour les espèces précisées dans l’encadré en bas à droite pour les lacs NW10-NW40. ... 54 Figure 22. Profils de concentrations de As mesurées (noir) dans les eaux porales avec la simulation réalisée par PROFILE (ligne rouge) et les taux nets de réaction (ligne bleu) (a-d). Profils de concentration de As(III) (en mauve) et As(V) (en rose) dans les eaux porales (e-h) ainsi que les profils de concentration en Fe(II) (en brun) et Fe(III) (en orange) (i-l) et les indices de saturation (m-p) pour les espèces précisées dans l’encadré en bas à droite pour les lacs NW50-NW80. ... 55 Figure 23. Précipitations annuelles totales (mm) et température moyenne annuelle (°C) à Yellowknife en 2018 (bleu) et 2019 (orange). Les points gris représentent d'autres années (Aukes et al.). ... 56 Figure 24. Concentrations en COD en fonction des concentrations d’Al dans les eaux porales pour tous les lacs. La ligne indique une relation linéaire et R2 le coefficient de détermination par rapport à la droite. ... 57 Figure 25. Schéma représentant la différence dans l’avancement de la saison pour les deux années d’échantillonnage. L’année 2019 se déroulant durant une fonte tardive avec un nouvel apport d’oxygène dissous (OD) et l’année 2018 se déroulant plus tard dans la saison avec des flux de carbone plus élevés. ... 58 Figure 26. Diagramme de Pourbaix (Eh-pH) de As. La zone en jaune représente la gamme de pH des lacs étudiés (Schweitzer and Pesterfield, 2010). ... 61Liste des tableaux
Table 1. Location and characteristics of the study lakes ... 21
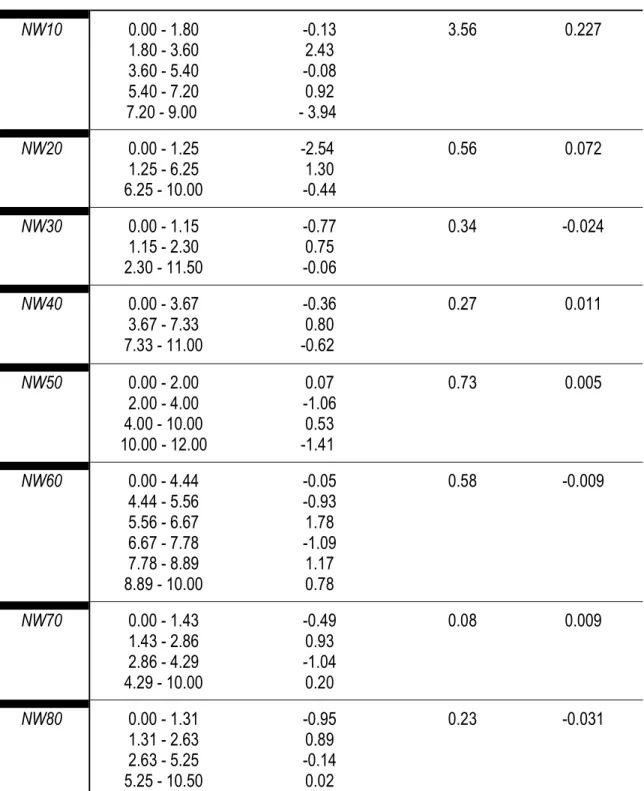
Table 2. RAsnet for each depth interval in each lake calculated by the code PROFILE. Estimated fluxes of As due to particle settling (Js) and transport of dissolved As across the sediment-water interface by diffusion (JD). ... 27
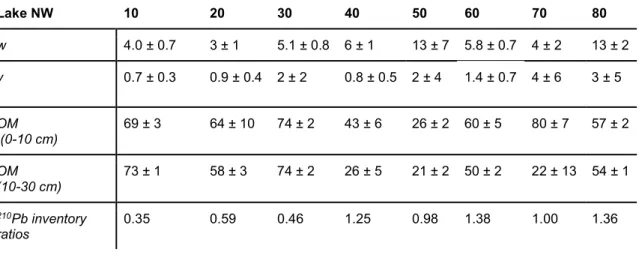
Table 3. Sediment mass accumulation rates (w, mg cm-2 yr-1) and burial rates (v, mm yr-1) calculated using 210Pb dating, along with average total organic matter content (OM; %) over the 0-10 and 10-30 cm depth ranges, and the measured to expected 210Pb inventories ratios in each core. ... 34
Tableau 4. Moyennes des ratios molaires sulfates/sulfures (SO42-/S2-), des pourcentages de As(V) et des ratio Astot/S2- dans chaque lac. Moyenne de la concentration en phase solide du Mn et du Fe pour les deux premiers centimètres (µmol g-1) et pH pour chaque lac. ... 61
Tableau 5. Lac NW10. Concentration dans les eaux porales. 1er juin 2018. ... 76
Tableau 6. Lac NW20. Concentration dans les eaux porales. 2 juin 2018. ... 77
Tableau 7. Lac NW30. Concentration dans les eaux porales. 1er juin 2018. ... 78
Tableau 8. Lac NW40. Concentration dans les eaux porales. 2 juin 2018. ... 79
Tableau 9. Lac NW50. Concentration dans les eaux porales. 1er juin 2018. ... 80
Tableau 10. Lac NW60. Concentration dans les eaux porales. 3 juin 2018. ... 81
Tableau 11. Lac NW70. Concentration dans les eaux porales. 3 juin 2018. ... 82
Tableau 12. Lac NW80. Concentration dans les eaux porales. 3 juin 2018. ... 83
Tableau 13. Lac NW10. Concentration dans la phase solide. 1er juin 2018. ... 84
Tableau 14. Lac NW20. Concentration dans la phase solide. 2 juin 2018... 86
Tableau 15. Lac NW30. Concentration dans la phase solide. 1er juin 2018. ... 88
Tableau 16. Lac NW40. Concentration dans la phase solide. 2 juin 2018... 90
Tableau 17. Lac NW50. Concentration dans la phase solide. 1er juin 2018. ... 92
Tableau 18. Lac NW60. Concentration dans la phase solide. 3 juin 2018... 94
Tableau 19. Lac NW70. Concentration dans la phase solide. 3 juin 2018... 96
Tableau 20. Lac NW80. Concentration dans la phase solide. 3 juin 2018... 98
Tableau 21. Lac NW10. Concentration dans les eaux porales. 26 mai 2019. ... 100
Tableau 22. Lac NW20. Concentration dans les eaux porales. 26 mai 2019. ... 101
Tableau 23. Lac NW30. Concentration dans les eaux porales. 26 mai 2019. ... 102
Tableau 24. Lac NW40. Concentration dans les eaux porales. 26 mai 2019. ... 103
Tableau 25. Lac NW50. Concentration dans les eaux porales. 27 mai 2019. ... 104
Tableau 26. Lac NW60. Concentration dans les eaux porales. 27 mai 2019. ... 105
Tableau 27. Lac NW70. Concentration dans les eaux porales. 27 mai 2019. ... 106
Tableau 28. Lac NW80. Concentration dans les eaux porales. 27 mai 2019. ... 107
Tableau 29. Concentration en carbone et soufre (en %) dans la phase solide pour chaque lac. 26 au 31 mai 2019. ... 108
Liste des abréviations
AsO33- - arsénite (As(III)) AsO43- - arséniate (As(V))
AVS – soufre volatile après acidification (acid volatile sulfides) COD – carbone organique dissous
CRS – sulfures réduit par le chrome (chromium reducible sulfides) ES – soufre élémentaire (elemental sulfur)
HCl – acide chlorhydrique HNO3 – acide nitrique
ICP-QQQ-MS – spectrométrie de masse à plasma à couplage inductif avec triple quadrupôles ICP-AES – spectrométrie d’émission atomique à plasma à couplage inductif
IS – force ionique (ionic strength) MOD – matière organique dissoute OM – matière organique (organic matter) ppm – partie par million (mg L-1)
ppb – partie par milliard (µg L-1)
RAsnet – taux nets de réactions de l’arsenic SAMMS – Sub-Arctic Metal Mobility Study SI – indice de saturation
v – vitesse de sédimentation (mm yr-1)
“The fight isn’t over until you win.”
Remerciements
J’aimerais d’abord remercier mon directeur de recherche, Raoul-Marie Couture, de m’avoir confié non seulement ce projet mais aussi la responsabilité de démarrer ton laboratoire. Merci beaucoup pour ton aide, ta patience et surtout d’avoir répondu à mes mille et une questions. Grâce à ce projet, j’ai eu l’occasion de relever plusieurs défis et découvrir un domaine qui m’intéresse énormément. Je n’aurais pu avoir un meilleur directeur de recherche pour m’épauler, j’espère avoir été à la hauteur de tes attentes!
Je voudrais remercier James Telford qui a récolté chacune de mes carottes sédimentaires et qui était toujours prêt à m’aider et faire usage de sa créativité pour résoudre nos problèmes. Merci à mes collègues du projet SAMMS, Izabela Jasiak et Mackenzie Schultz, avec qui j’ai toujours eu du plaisir à échanger, aider et discuter. Merci de votre patience envers mon anglais et de m’avoir aidé à m’améliorer. Merci aux assistants de terrain qui ont permis d’accélérer considérablement le travail et l’échantillonnage : Caitlin, Jenny, Mia et Tanner. Merci aux professeurs Brent Wolfe, Roland Hall et Jason Venkiteswaran pour leur aide et bons conseils, notamment pour la rédaction de l’article.
Merci aux membres du groupe Couture, spécialement à Sarah-Michèle Cormier, ma stagiaire, pour toute l’aide apporter sur les analyses et la préparation de mes échantillons. Merci pour tous tes trucs concernant l’extraction des AVS et tes réflexions pour améliorer notre piètre rendement. Merci surtout pour les rires et le bon temps passé au lab à une époque où j’étais encore très solitaire. Merci aux autres stagiaires, Marie et Bia pour toute l’aide avec la préparation de mes échantillons. Merci aux autres membres du groupe qui se sont ajoutés peu à peu : Marianne Côté, Audrey Laberge-Carignan et Thomas Bossé-Demers. C’est toujours plaisant de discuter avec vous.
Je voudrais remercier Global Water Future – SAMMS pour le financement, ainsi que le programme de formation scientifique dans le nord (PFSN) et Sentinelle Nord.
Merci beaucoup à ma famille pour tout le support, les encouragements et l’intérêt porté sur mon projet, même si ce que je vous disais parfois devait sembler bien compliqué et abstrait. Merci d’avoir suivi à la trace mes vols en avion afin de vous assurer que j’arrivais bien à la bonne destination saine et sauve!
Finalement, merci Julien d’avoir toujours été là pour moi, pour me supporter dans les bons comme dans les mauvais moments. Merci d’avoir endurer mes hypothèses, mes questions et mes frustrations et d’être toujours resté attentif et essayé de m’aider à trouver des pistes même si le sujet dépassait tes connaissances. Merci de ta présence et de tes encouragements. Sans toi, j’aurais bien eu de la misère à passer au travers de la maîtrise. Merci pour tout!
Avant-propos
Ce mémoire inclut l’insertion de l’article “Quantifying arsenic post-depositional mobility in lake sediments impacted by gold ore roasting in sub-arctic Canada using inverse diagenetic modelling” dans le premier chapitre. Cet article est en révision au journal Environmental Pollution. Il a été soumis le 3 décembre 2020.
Je suis la première auteure de cet article. J’ai échantillonné les sédiments et les eaux porales en 2018 et 2019, fait les analyses en laboratoire de l’eau porale, modélisé et interprété les résultats, et rédiger l’article.
Coauteurs :
Raoul-Marie Couture, Département de Chimie, Université Laval, Québec, QC & Centre d’études nordiques (CEN) – supervision, écriture, révision, conceptualisation et acquisition de financement Jason J. Venkiteswaran, Department of Geography and Environmental Studies, Wilfrid Laurier University, Waterloo, ON – révision, conceptualisation et acquisition de financement
Izabela Jasiak, Department of Biology, University of Waterloo, Waterloo, ON – collecte et interprétation de données
James V. Telford, Department of Geography and Environmental Studies, Wilfrid Laurier University, Waterloo, ON – collecte de données et conceptualisation
Brent B. Wolfe, Department of Geography and Environmental Studies, Wilfrid Laurier University, Waterloo, ON – révision, conceptualisation et acquisition de financement
Roland I. Hall, Department of Biology, University of Waterloo, Waterloo, ON – révision, conceptualisation et acquisition de financement
Mackenzie D. J. Schultz, Department of Geography and Environmental Studies, Wilfrid Laurier University, Waterloo, ON – collecte et interprétation de données
Introduction
i.
L’arsenic
La contamination à l’arsenic (As)suscite beaucoup d’inquiétudes dû à sa présence dans les plans d’eau et les nappes phréatiques et les risques importants qu’elle pose sur la santé humaine. Les sources naturelles d’As sont dominées par l’As associés aux oxyhydroxydes de Fe susceptibles d’être remobilisés, dans beaucoup d’aquifères d’Asie du Sud-Est (Polya and Charlet, 2009). Les sources anthropiques sont quant à elles dominées par l’oxydation de la pyrite issue de l’activité minière (Nordstrom and Archer, 2003; Smedley and Kinniburgh, 2002). L’As est cancérigène et les effets d’une exposition chronique sont bien connus. Cette exposition peut mener au cancer de la peau, des poumons, du foie, de la vessie et des reins. L’As peut également causer des maladies vasculaires, des complications chez les femmes enceintes, des lésions cutanées et une mortalité accrue (Mitchell, 2014). C’est un contaminant prioritaire non seulement dans la loi canadienne sur la protection de l’environnement mais également au niveau global, par exemple dans les listes de l’organisation mondiale de la santé (OMS). Il est parmi les dix contaminants préoccupants pour la santé publique mondiale selon cette organisation (OMS, 2010). Les recommandations pour la qualité des eaux en ce qui a trait l’As aux fins de la protection de la vie aquatique (CCME, 2001) est de 5 µg L-1, et pour l’eau potable, 10 µg L-1. Finalement, les recommandations provisoires pour la qualité des sédiments (RPQS) et concentrations produisant un effet probable (CEP) établies pour l’As sont respectivement de 5,9 et 17 mg kg-1 ps.
L’As est un métalloïde et possède certaines propriétés chimiques des métaux et des non-métaux. Il est le 20e élément le plus abondant de la croute terrestre, avec des concentrations moyennes de l’ordre du ppm. Sous forme réduite trivalente, il se retrouve en particulier avec les sulfures dont l’arsénopyrite (FeAsS(s)) est le plus commun (Smedley and Kinniburgh, 2002). La pyrite (FeS2s)) quant à elle peut contenir jusqu’à 5% d’As. Sous forme oxydée pentavalente, il est sous forme d’oxyanion et est généralement associé avec les oxydes des métaux dont le fer, l’aluminium et le manganèse ou avec des cations comme le calcium.
L’As est un élément rédox-sensible dans les sédiments. Ses degrés d’oxydation les plus communs sont (-3), (0), (+3) et (+5) et sont nommés respectivement arsine (AsH3), arsenic (As0), arsénite (AsO33-) et arséniate (AsO43-). Sa spéciation dans les sédiments est gouvernée par les
processus rédox et le pH (Campbell and Nordstrom, 2014; Smedley and Kinniburgh, 2002) et est étroitement liée aux interactions avec les oxydes de Fe et de Mn, le soufre (S) et la matière organique (MO) (Campbell and Nordstrom, 2014; Couture et al., 2010; Guénet et al., 2016; La Force et al., 2000).
Figure 1. Réactions typiques de l'As avec le fer et le soufre dans les sédiments. Adapté de Henke (Henke, 2009).
Dans un lac sous des conditions oxiques, l’arsenic est oxydé rapidement de As(III) à As(V). Sous sa forme pentavalente et à pH légèrement acide il possède une affinité élevée pour les surfaces des oxyhydroxydes de fer, lesquelles peuvent séquestrer As par adsorption ou co-précipitation (Figure 1) (Guénet et al., 2016; Kneebone et al., 2002; Lock et al., 2018; Root et al., 2007; Torres et al., 2015). Lorsque les microorganismes qui contrôlent la décomposition de la matière organique dans le sédiment auront consommé tout l’oxygène, ils se tourneront vers d’autres accepteurs d’électrons terminaux (TEA) soit les nitrates via la dénitrification, la réduction des oxydes de manganèse et ensuite des oxydes de fer, la réduction des sulfates et finalement le bicarbonate par la méthanogenèse (Canfield et al., 2005). Dans ces conditions anoxiques, la dissolution réductive des oxydes de fer et de manganèse entraîne également la dissolution de l’arsenic et sa subséquente réduction en As(III). Une fois dissous, l’arsenic peut diffuser vers les couches plus profondes du sédiment ou vers le haut pour rejoindre l’interface eau-sédiment et être remobilisé vers la colonne d’eau. Il peut être ainsi recyclé plusieurs fois avec les oxydes de fer et de manganèse.
Si les conditions anoxiques persistent et la réduction des sulfates survient, les sulfures et l’As (III) sont susceptibles de co-exister dans les eaux porales. L’arsenic peut alors s’absorber sur FeS et être enfouis dans le sédiment (Figure 1) (Bostick and Fendorf, 2003; Burton et al., 2013; O'Day et al., 2004; Tang et al., 2019). En fonction des concentrations ambiantes de sulfure et de soufre élémentaire, FeS peut ensuite former de la pyrite framboïdale (FeS2) (Benning et al., 2000 Shuh, Thiel; Burton et al., 2013; Butler and Rickard, 2000; Schuh et al., 2019; Thiel et al., 2019). La pyrite agit comme un minéral clé pour l’enfouissement de As. Ce dernier est adsorbé ou remplace le soufre dans la pyrite et dans les composés de monosulfure de fer (Burton et al., 2013; Neumann et al., 2013; Schuh et al., 2019). Il peut également y avoir formation de composé d’As et de S comme l’orpiment ou le réalgar, si les concentrations en Fe sont faibles et qu’il y a suffisamment de sulfures libres dans les eaux porales (Wilkin and Ford, 2006). Finalement, les groupes thiols dans les sédiments peuvent également lier l’arsénite et former des composés As-SH(s) (Couture et al., 2013; Knappová et al., 2019; Langner et al., 2012; Schuh et al., 2018).
ii.
Contamination à l’arsenic par les activités minières au Canada : Le cas
de la mine Giant, Yellowknife, Territoires du Nord-Ouest.
Dû à sa présence dans plusieurs minéraux d’importances pour l’exploitation minière, l’arsenic est souvent un sous-produit majeur, ce qui peut causer des rejets dans l’environnement. Au Canada, plusieurs cas de contaminations ont été recensés, en particulier dans les lacs (Martin and Pedersen, 2002; Roberts et al., 2020; Sprague and Vermaire, 2018). Ceux-ci sont en effet souvent le site final de dépôt des déchets miniers et cela résulte en des charges importantes d’arsenic dans les lacs (Harrington et al., 1998). On peut citer en exemple le lac Balmer en Ontario qui a servi de dépôt de déchets miniers pour deux mines d’or souterraines (Campbell et Red Lake) dont les résidus de flottation étaient directement versés dans le lac avant 1970. Des concentrations d’arsenic élevées ont été mesurées dans le sédiment avec une moyenne de ~ 4 500 mg kg-1 (Martin and Pedersen, 2002). Un autre cas important représente la contamination causée par d’anciens dépôts miniers centenaires d’une mine d’argent dans la région de Cobalt en Ontario. Des concentrations très élevées de 972 µg L-1 et 10 800 mg kg-1 ont été recensées respectivement dans l’eau de surface et dans les sédiments des lacs (Sprague and Vermaire, 2018). Un autre exemple en Alberta présente des concentrations élevées dans les eaux souterraines de la région de Cold Lake qui sont couramment utilisées pour
l’agriculture et par la population (Javed and Siddique, 2016). Ces exemples dépassent les concentrations règlementaires de plusieurs ordres de grandeur. Enfin, le cas de contamination par l’As le plus sévère au Canada est lié aux activités de la mine Giant dans les Territoires du Nord-Ouest.
L’activité minière est depuis des décennies le moteur économique des Territoires du Nord-Ouest. Une course vers l’or s’est déroulée dans les années 1930 avec l’ouverture de plusieurs mines dans la région. Aujourd’hui, la plupart d’entre elles sont abandonnées. Deux des plus importantes situées près de la ville de Yellowknife sont la mine Giant, ouverte en 1948 puis officiellement fermée en 2004, et la mine Con (Consolidated), ouverte en 1938 puis fermée en 2003 (INAC, 2010). Cette dernière a une production d’or moins élevée que la mine Giant, ainsi la mine Giant est considérée comme étant la plus grande source anthropique d’As dans la région (Mackenzie Valley Review Board, 2013).
Figure 2. Emplacement de la mine Giantprès de la ville de Yellowknife, dans les Territoires du Nord-Ouest (Fawcett et al., 2015). Rose des vents qui présente combien d’heure par année le vent provient de la direction indiquée. Le vent souffle en grande partie de l’est vers l’ouest et du sud-est vers le nord-ouest. (Galloway et al. (2018)).
La compagnie Giant Yellowknife Gold Mines Ltd. a effectué l’extraction de l’or à partir de l’arsénopyrite à la mine Giant de 1949 à 1999. Le procédé d’extraction est spécifique aux anciennes mines d’or. Le minerai est réfractaire et nécessitait d’abord le grillage de l’arsénopyrite à haute température, en présence d’oxygène (équation 1) (Schuh et al., 2018), puis la complexation de l’or par cyanuration (Walker et al., 2015). Ce procédé mène à la formation de trioxyde d’arsenic :
2 FeAsS(s) + 5 O2(g) ∆
→ Fe2O3(s) + As2O3(s) + 2 SO2(g) (Éq. 1)
Plus de 20 milles tonnes de trioxyde d’arsenic ont été émises dans l’atmosphère durant les cinquante années d’opération, dont 86% pendant les quatorze premières années d’activités de 1949 à 1963 (Wrye, 2008). Cette pollution s’est par la suite déposée sur les sols et dans les lacs de la région, s’ajoutant à la contamination par les lixiviats près du site minier. Beaucoup d’études ont été menées depuis sur la concentration de As dans les sols (Bromstad et al., 2017; Hutchinson et al., 2007), les sédiments et leurs eaux porales (Fawcett et al., 2015; Galloway et al., 2018; Schuh et al., 2018; Schuh et al., 2019; Thienpont et al., 2016; Van Den Berghe et al., 2018; Wagemann et al., 1978); ou sa concentration dissoute dans la colonne d’eau (Fawcett et al., 2015; Houben et al., 2016; Palmer et al., 2015; Thienpont et al., 2016; Van Den Berghe et al., 2018; Wagemann et al., 1978). Elles se sont concentrées sur l’étendue de la contamination dans un rayon de 30 km autour du site minier. Bien qu’elles soient pertinentes dû à la proximité de la ville, et aux risques posés à l’environnement et la santé humaine, elles pourraient ne pas représenter adéquatement les trajectoires d’émission atmosphériques enregistrées durant l’exploitation de la mine (Palmer et al., 2015). Les concentrations et les flux présents d’arsenic dans les sédiments des lacs et les bassins versants plus éloignés restent mal connus.
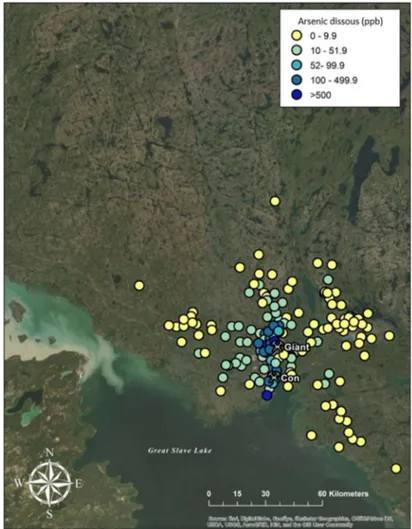
Figure 3. Distribution des concentrations d'arsenic dissous dans l'eau de surface des lacs situés autour des mines Giant et Con (Figure crée par Izabela Jasiak, à partir des résultats de Palmer et al., 2015).
Les études réalisées dans les lacs et les sites près de la mine ont révélé des concentrations au-delà de la norme gouvernementale canadienne sur la quantité maximale d’arsenic dans l’eau potable. En effet, la concentration maximale acceptable d’arsenic dans l’eau potable est de 10 µg L-1 et celle-ci est dépassée d’une ou deux échelles de grandeur selon les mesures faites par Stantec (2014) dans les lacs situés juste à proximité de la propriété de la mine Giant. Palmer et al. (2015) a également effectué des recherches dans des lacs situés à l’ouest et au nord dans un périmètre de 30 km. Ces résultats ont démontré des concentrations plus élevées d’arsenic dissous dans les lacs que celles observées dans certains lacs près de la mine, ce qui présente l’influence des vents dominants sur le transport atmosphérique (Figure 3). Les vents prédominants enregistrés à l’aéroport de Yellowknife viennent de l’est et du sud-est (Figure 2), ce qui explique les concentrations supérieures
aux normes recensées à l’ouest et au nord-ouest de la mine, lesquelles diminuent avec de la distance de la mine Giant (Palmer et al., 2015). De plus, les recherches menées par Cheney et al. (2020) sur la toxicologie dans des lacs situés jusqu’à 40 km de la mine, démontrent que certains lacs demeurent toujours un risque élevé pour le biote aquatique, et ce, vingt ans après la fermeture de la mine.
Avec les changements climatiques en cours, cette région subarctique est soumise à des variations de température qui peuvent influencer la stabilité du pergélisol (Romanovsky et al., 2010). Celui-ci contient une quantité importante de matière organique qui s’est accumulée avec le temps. Le dégel du pergélisol entraîne des flux importants de matière organique dissoute (MOD) vers les lacs environnants. Ces changements peuvent avoir un impact sur la qualité de l’eau de surface, notamment par le brunissement des eaux et l’augmentation de la production primaire qu’il peut causer (Creed et al., 2018). La MOD peut également transporter une charge supplémentaire de contaminants associés. Ce phénomène est bien documenté pour les métaux cationiques, puisque la MOD est naturellement chargée négativement (Tipping, 2002). Pour les oxyanions comme l’arsénite (à pH > 9,2) et l’arséniate, un cation comme le Fe3+ ou le Ca2+ doit intervenir pour faire le pont entre la matière organique et l’arsenic dissous (Hoffmann et al., 2013; Ritter et al., 2006). Des études récentes ont aussi démontrés que l’arsenic à une forte affinité pour les groupes thiols (-SH) de la matière organique (Langner et al., 2012).
Ces perturbations du cycle de la matière organique dissoute affecteront la santé à long terme des écosystèmes ainsi que la qualité de l’eau potable consommée. Enfin, un changement significatif dans l’apport de carbone organique vers les lacs et sédiments peut influencer leurs conditions d’oxydoréduction. En effet, le carbone est une source d’électron pour la respiration microbienne. Lorsque l’oxygène s’appauvrit, les microorganismes doivent se tourner vers d’autres accepteurs d’électron terminaux sous conditions anoxiques et réductrices, ce qui vient remobiliser certains éléments sensibles à ces conditions dont le fer, le manganèse et l’arsenic. Il est donc possible que les changements climatiques viennent augmenter l’impact anthropogénique lié à l’activité minière, en favorisant la remobilisation de l’arsenic accumulé dans les lacs au fil du temps.
C’est dans ce contexte que le projet Sub-Arctic Metal Mobility Study (SAMMS), financé par le programme Global Water Future (CRSNG Apogee), vise à étudier comment la contamination minière
historique représente un risque accru sous l’effet de l’augmentation dans les flux de la matière organique dissoute causé par les changements climatiques dans les Territoires du Nord-Ouest. Ces études se concentrent sur la compréhension du transport et du comportement de la matière organique dissoute et des métaux/métalloïdes dans les écosystèmes terrestres et aquatiques dans des lacs le long d’un transect avec la mine Giant comme point de départ (Wolfe and Venkiteswaran, 2018).
iii.
Objectifs
L’objectif de ce projet de maîtrise est d’évaluer la mobilité de l’arsenic dans les sédiments de lacs subarctiques contaminés par la mine Giant. Pour ce faire, je vais évaluer si la diagenèse doit être prise en compte pour permettre l’interprétation des archives sédimentaires et ce, dans plusieurs lacs le long d’un transect. La diagenèse de l’As a été étudié dans le passé, notamment par Couture et al. (2008), mais sur quatre lacs indépendants plutôt que sur une trajectoire linéaire s’éloignant d’une source d’émission de contaminants. Ce projet de maîtrise se divise en plusieurs trois énumérés ci-dessous.
1- Évaluer l’impact de la diagenèse sur la contamination de As dans les sédiments L’utilisation des sédiments comme archives environnementales de la contamination à l’arsenic demande d’y évaluer l’impact de la diagenèse. C’est-à-dire, l’impact des processus physiques et biologiques ainsi que les réactions chimiques qui se produisent dans le sédiment et qui contrôlent la distribution de l’As après sa déposition. Pour ce faire, l’analyse des profils de concentration dans les eaux porales des sédiments est propice à l’observation des différentes réactions de l’arsenic dans le sédiment. En principe, la mobilité de l’arsenic devrait être liée à celle du fer et du soufre. De plus, ces profils devraient présenter des concentrations maximales d’arsenic diminuant avec l’éloignement de la mine, comme celles observées par Palmer et al. (2015).
La modélisation inverse des profils de concentration d’As dans l’eau porale avec le code PROFILE permet de quantifier les taux nets de réaction dans les eaux porales. Cette information est nécessaire afin de corriger les archives sédimentaires pour l’influence de la diagenèse. Cette correction permet de reconstruire la concentration historique de l’arsenic, soit sa concentration au moment de sa déposition. L’hypothèse formulée est que la concentration historique maximale d’arsenic révélée après
correction devrait coïncider avec les dates d’opérations de la mine Giant, soit entre 1949 et 1999. La correction de la diagenèse devrait également être nécessaire afin de pouvoir reconstituer un profil sédimentaire fiable de concentration d’arsenic.
2- Évaluer les flux diffusifs à l’interface en réponse à la contamination de la mine Giant. La modélisation permettra également de quantifier les flux d’arsenic à travers l’interface eau-sédiment en réponse à la contamination causée majoritairement par la mine Giant. Ces flux représentent les concentrations d’arsenic diffusant du sédiment vers la colonne d’eau. Dû aux concentrations élevées recensées dans les autres études, il est probable que les sédiments des lacs près de la mine soient toujours une source d’arsenic, et cela même 20 ans après l’arrêt des activités de la mine.
3- Étude de l’impact de la saisonnalité sur les conditions rédox et les flux diffusifs. Les deux saisons d’échantillonnage et les huit lacs étudiés apportent un jeu de données important qui permet d’évaluer l’impact de la saisonnalité sur les flux diffusifs sur deux années, ce qui est peu réalisé présentement. La saisonnalité des lacs, notamment la période de la fonte du couvert de glace, a un effet important sur les conditions rédox qui prévalent dans la colonne d’eau et les sédiments.
iv.
Sites d’études
Les sites d’étude se situent dans la région de la taïga du Bouclier canadien. Le climat de la région est caractérisé par des hivers longs et des étés courts et les températures tombent sous zéro généralement au début de l’automne jusqu’à la fin avril (Environment Canada, 2018). La plupart des lacs, majoritairement les plus petits, sont ainsi couvert de glace pendant la moitié de l’année. Les lacs étudiés sont situés dans un transect de 80 km au nord-ouest de la mine Giant. Huit lacs, NW10-NW80, ont été échantillonné à un intervalle d’environ 10 km. Ce sont tous des lacs de tête afin de limiter l’influence de lac ou cours d’eau en amont sur les flux d’arsenic et de limiter aux apports atmosphériques et ceux apportés par le bassin versant. Ce sont des lacs éloignés de la population qui ne sont pas accessible par les routes. Ainsi, les lacs ont été visité par hélicoptère du 1er au 3 juin
2018 et du 26 au 31 mai 2019. Ces sites d’études sont décrits plus en détails dans le chapitre 1, à la section 1.4.1.
Figure 4. Localisation du site d'étude et des huit lacs du transect ainsi que la mine Giant.
v.
Les sédiments comme archives environnementales
Le suivi de la qualité de l’air à la fois limité dans l’espace et le temps rend difficile la détermination de l’historique de la contamination par l’As survenue il y a environ soixante-dix ans à la mine Giant. Les archives environnementales, notamment les archives sédimentaires lacustres, sont d’excellents outils afin de révéler cette contamination. En effet, les sédiments accumulent avec les années les matières organiques et minérales provenant autant de la déposition atmosphérique que de l’érosion et du transport aquatique. Des quantités importantes de contaminants potentiels peuvent conséquemment être contenu dans ces sédiments. Cela est dû au fait que les oxyanions, comme l’arsenic, possèdent une grande affinité pour les surfaces chargées positivement à pH sous la neutralité, tels les oxydes de fer. Les métaux divalents, quant à eux, ont une forte affinité pour les surfaces minérales, chargées négativement ainsi que pour la matière organique dissoute. Les
sédiments étant très hétérogènes, ils peuvent liés une large gamme de composés. L’analyse de la distribution verticale des concentrations dans une carotte sédimentaire rend donc possible, en principe, la reconstruction des dépositions atmosphériques d’un contaminant. Ces archives nécessite de dater les sédiments, et ainsi révéler des tendances historiques de déposition (Shotyk and Mackenzie, 2004). Plusieurs études ont démontré l’efficacité de l’utilisation des carottes sédimentaires datées pour retracer l’historique des contaminations par l’exploitation minière (p. ex.: Belzile and Tessier, 1990; Couillard et al., 2008; Tropea et al., 2010; Wiklund et al., 2017).
Géochronologie des sédiments lacustres
La méthode de datation couramment utilisée est celle de la datation au plomb-210 (210Pb). Cet élément est un radionucléide naturellement présent dans l’environnement dû à la chaîne de désintégration de l’uranium-238 (238U). Le 210Pb possède une demi-vie de 22,2 ans et est utilisé comme géo-chronomètre afin d’étudier les changements survenus dans les écosystèmes au cours des 150 dernières années (Sanchez-Cabeza, 2012). Dans un système sédimentaire, on distingue habituellement deux types de 210Pb. Premièrement, une partie du 210Pb est formé par la désintégration in situ du radium-226 (226Ra) et est donc supporté par les processus ayant lieus dans les sédiments, c’est-à-dire en équilibre séculaire. Deuxièmement, on dénote le 210Pb en excès, aussi appelé non supporté. Ce plomb provient de l’atmosphère suite à la désintégration du radon-222 (222Rn), un gaz formé dans les sols à la suite de la désintégration du 226Ra et diffusé vers l’atmosphère. Le 222Rn se désintègre en une succession de radioisotopes à courte demi-vie pour finalement former le 210Pb. C’est l’excès de 210Pb, non supporté par la désintégration du 226Ra dans les sédiments, qui est interprété lors de la datation des sédiments lacustres (Paul Phillip, 2015).
Trois modèles peuvent être employés pour dater les sédiments, choisi en fonction des hypothèses posés sur le comportement des particules qui sédimentent: le modèle CIC (Constant initial concentration) suppose que le flux 210Pb change proportionnellement au flux de particules qui sédimentent, le CF-CS (Constant flux, constant sedimentation) suppose que les flux de 210Pb et de particules sont constant et finalement le modèle CRS (Constant rate of supply) suppose que le flux de 210Pb est constant et que le flux de particules peut changer. Le modèle choisi doit par la suite être validé avec des marqueurs stratigraphiques, comme le césium-137 (137Cs). Le 137Cs est un radioisotope employé comme marqueur stratigraphique puisqu’il est produit artificiellement et que les
le maximum d’émissions de ce radioisotope sont documentés en 1963 lors des essais nucléaires atmosphériques et en 1986 suite à l’accident de Tchernobyl. Dans le cadre du projet, le modèle CRS est préférable puisque l’étude se porte sur des milieux altérés par l’activité humaine ou le climat, avec des flux de particules en évolution (Appleby, 2001).
Figure 5. Schéma de la chaîne de désintégration de 238U et de la répartition du 210Pb dans l’environnement. Adaptée de Oldfield and Appleby (1984).
Interprétation des profils de concentration dans les eaux porales
Les profils de concentration dans les eaux porales représentent les réactions d’un élément sous forme de gradient. En effet, ces profils présentent la remobilisation du sédiment, la précipitation ou adsorption en phase solide ainsi que d’autres processus tels la diffusion, le transport par advection, la bioturbation et la bioirrigation. Puisque l’arsenic, et d’autres éléments, sont présents majoritairement sous forme solide dans le sédiment, leur concentration en phase dissoute dans les eaux porales est très sensible aux changements qui s’y produisent. Les eaux porales sont donc des bons indicateurs de la diagenèse et l’analyse de leur profils verticaux facilitent l’observation des différentes réactions. La figure suivante présente les différents types de profils typiques dans les eaux porales.
La figure 6a représente la diffusion d’un composé non-réactif, par exemple le chlorure, alors que le profil b présente un composé dont la concentration diminue dans les premières couches, par exemple l’oxygène. Le profil c représente une substance qui est consommé dans une certaine couche
réactive alors que le profil e démontre une substance produite dans l’eau porale dans une certaine couche réactive. Le profil d représente une substance étant introduite dans les premières couches d’eau porale, près de l’interface eau-sédiment. Finalement, le profil f présente une substance étant consommée des eaux porales dans les couches réactives 1 et 3 ainsi que produite dans l’eau porale dans la couche réactive 2.
Figure 6. Exemples de profil de concentration d’eau porale (Bohrmann et al., 2006).
Ces différents profils peuvent être modélisés afin d’obtenir des taux nets de réactions, c’est-à-dire des taux où l’arsenic est ajouté (positif) ou retiré (négatif) de l’eau porale. Ces taux de réactions sont utiles afin de quantifier la diagenèse et pouvoir éventuellement corriger ce processus du profil sédimentaire. Ils permettent aussi de formuler des hypothèses sur les réactions qui s’y produisent sans toutefois être précis sur leur identification. Il est également possible d’obtenir les taux des flux diffusifs à l’interface eau-sédiment, qui indique si le sédiment est actuellement une source ou un puits d’arsenic à la colonne d’eau.
Modélisation cinétique inverse des profils d’eaux porales
Les réactions qui se produisent dans une colonne sédimentaire peuvent être quantifiées et prisent en compte grâce à un modèle cinétique basé sur, l’équation de la diagenèse. Elle définit, pour une profondeur donnée dans les sédiments, la variation de la concentration d’un élément en fonction du temps (Boudreau, 1997) :
( [ ] ) = − + ∑𝑅 (Éq. 2)
où [C] représente la concentration de l’élément (mol L-1), t le temps (s), x une profondeur donnée sous l’interface eau-sédiment (cm), F est la valeur du flux de l’élément (mol cm-2 s-1) et la somme de R représente la somme des réactions se produisant à la profondeur donnée qui affectent l’élément étudié (en mol cm-3 s-1).
En tenant compte de tous les processus physiques, biologiques et les réactions chimiques mentionnés précédemment, l’équation de la diagenèse pour la concentration d’un analyte est formulée comme suit :
( [ ]) = 𝜙(𝐷 + 𝐷 ) [ ] + 𝜙 𝛼 [𝐶] − [𝐶] + 𝑅 (Éq. 3)
où [C] mol est la concentration de l’analyte dans les eaux porales (mol L-1), ɸ la porosité, DS le coefficient de diffusion (cm2 s-1), DB le coefficient de biomélange (cm2 s-1), α le coefficient de bioirrigation (s-1), [C]irrigation représente la concentration irrigée (mol L-1) et Rnet est le taux net de réaction, soit de production lorsque positif ou de consommation lorsque négatif (en mol cm-3 s-1).
Si on émet l’hypothèse d’un état stationnaire dans les sédiments, c’est-à-dire qu’il n’y a pas de modification de la masse dans une couche de sédiment pour une période donnée, on peut poser que le terme de gauche de l’Eq. 3 est égal à zéro, et isoler la valeur de Rnet. Enfin, il est raisonnable de considérer que le biomélange, la bioirrigation sont négligeables dans les eaux porales de lacs saisonnièrement anoxique. Cela permet ainsi de simplifier l’équation 3 :
𝑅 = (𝜙𝐷 ( [ ]) (Éq. 4) La résolution de cette nouvelle équation est réalisée par le code PROFILE lorsque tous les autres termes de l’équation sont connus. PROFILE estime les taux nets (ci-après référés comme zones) à l’aide des profils de concentration dans les eaux porales en reproduisant avec la meilleure simulation le profil de concentration mesuré. La meilleure simulation est sélectionnée lorsque le profil modélisé est le plus similaire au profil observé tout en ayant le moins de zone possible, grâce au coefficient de corrélation (R2). Cette modélisation a été utilisée dans d’autres études notamment sur la diagenèse de l’As (Couture et al., 2008), du CH4 et carbone organique dissous (COD) (Clayer et al., 2018) et du Pb (Gallon et al., 2004).
PROFILE calcule à la fois les taux nets de réaction de production ou de consommation et les flux diffusifs de l’arsenic à l’interface eau-sédiment. Ces derniers résultats sont utiles notamment pour déterminer si les sédiments sont une source d’arsenic à la colonne d’eau (flux positif) ou s’ils agissent plutôt comme un puits (flux négatif). Les taux nets (zones) estimés aide à prédire les réactions clés se produisant dans le profil sans toutefois être précis sur celles-ci.
Correction des profils pour la diagenèse
Ces taux nets de réaction permettent de quantifier la diagenèse et ainsi évaluer la fiabilité de l’archive sédimentaire étudiée. Cette procédure demande de relier les différentes zones de production ou de consommation avec la densité du sédiment et le taux de sédimentation pour des intervalles profondeurs données. L’équation 5 démontre cette relation :
{𝐴𝑠} = − ∫ × 𝑑𝑥 = − ∑
× ∆𝑥 (Éq. 5)
où {As}diag représente la concentration d’arsenic en phase solide remobilisée par la diagenèse, soit sa concentration ajoutée ou retirée à une couche de sédiment donnée, à chacune des zones déterminées par le modèle (ug g-1), x est la profondeur dans le sédiment (cm), xi est une profondeur
d’une couche de sédiment (cm), DBD représente la densité du sédiment (g cm-3) et vS sa vitesse de sédimentation (cm s-1).
Une fois la diagenèse quantifiée, on peut effectuer la correction de celle-ci afin de révéler la concentration d’arsenic au moment de sa déposition, appelée concentration historique {As}hist. Pour ce faire, la concentration en {As}diag est soustraite de la concentration d’arsenic mesurée en phase solide. La figure suivante présente des exemples d’une archive fiable (à gauche) ainsi que d’une archive nécessitant la correction (à droite). Dans le premier cas, l’arsenic n’a pas une mobilité élevée (voir l’encart en bas à droite) et donc le profil corrigé est très similaire à celui mesuré. Le deuxième exemple présente un cas où l’arsenic est très mobile et donc la correction pour la diagenèse devient nécessaire afin d’obtenir la concentration en arsenic au moment de sa déposition. Dans l’exemple présenté, la correction révèle également un pic historique plus prononcé que dans le profil mesuré.
Figure 7. Exemple de correction d’archive sédimentaire (Couture et al., 2008). L’encart en bas à droite représente la mobilité de As ({As}diag). À gauche, le profil mesuré (en vert) est similaire au profil historique corrigé (en blanc). À droite, le profil mesuré est différent au profil historique, montrant un besoin de correction pour la diagenèse.
Ce mémoire comporte deux chapitres. Le premier, sous forme d’article, porte sur la quantification de la mobilité de As après sa déposition. Il discute de la correction de la diagenèse, des flux diffusifs et de la mobilité de As avec le fer et le manganèse. Le deuxième présente l’impact de la saisonnalité sur les conditions rédox et la mobilité de As. Il discute de l’effet de la fonte des glaces sur la mobilité et des réactions qui enfouissent l’arsenic dans le sédiment, notamment liées au soufre. Ce mémoire se termine par une conclusion, la bibliographie et les annexes.
Chapitre 1. Quantifying arsenic post-depositional mobility in
lake sediments impacted by gold ore roasting in sub-arctic
Canada using inverse diagenetic modelling
1.1 Résumé
Les sédiments lacustres sont largement utilisés comme archives environnementales pour reconstituer les dépôts historiques de contaminants, à condition que les éléments déposés restent immobiles. L'arsenic (As) est un élément sensible rédox qui sera redistribué dans les sédiments durant la diagenèse précoce, avec le fer et le manganèse, et donc ses profils de profondeur pourraient ne pas être fiables. Ici, nous nous appuyons sur la modélisation diagenétique pour interpréter les archives sédimentaires de As dans une région d’extraction de l’or par les mines Giant et Con dans les Territoires du Nord-Ouest, Canada.
Des carottes de sédiments ont été prélevées pour la datation au 210Pb, l'analyse des concentrations de métaux(loïdes) en phase solide et l'extraction des eaux porales. Nous reconstruisons l'historique de la disposition de As en corrigeant les différents patrons de mobilité grâce à la modélisation diagenétique et calculons les flux de As contemporains dans huit lacs le long d'un transect de 80 km de la mine Giant, dans les Territoires du Nord-Ouest, au Canada.
Le calcul des flux de déposition révèle des pics d'As anthropiques coïncidant avec le début de la période de fortes émissions des mines pour les lacs situés à plus de 20 km des mines. Cependant, dans les lacs à moins de 20 km, l'As émis il y a 70 ans continue d'entraîner des flux d'As actuels élevés provenant de l'interface eau-sédiments. Une correction pour la diagenèse était nécessaire pour deux des huit lacs, probablement en raison de leurs taux de sédimentation plus faibles qui permettent un contact plus long entre l'As déposé et les zones réactives près de l'interface eau-sédiment.
1.2 Abstract
Lake sediments are widely used as environmental archives to reconstruct historical contaminants deposition, provided that the elements remain immobile after deposition. Arsenic (As) is a redox-sensitive element that may be redistributed in the sediments during early diagenesis, along with iron and manganese, and thus depth profiles of As might not provide a reliable, unaltered record of deposition history. Here, we rely on diagenetic modelling to interpret As sedimentary records in lakes near a region of past gold ore roasting at Giant and Con mines, Northwest Territories, Canada.
The sediment cores were dated using 210Pb methods and analysed for solid-phase and porewater metal(loids) concentrations. We then used inverse diagenetic modelling to reconstruct the history of As deposition by correcting for the varying mobility patterns and calculate As contemporary fluxes in eight lakes along a 80-km transect from the mines.
Calculation of deposition fluxes reveals anthropogenic As peaks coinciding with the start of the period of high emissions from the mines for lakes >20 km from the mines. However, at near-field lakes <20 km from the mines, the As emitted 70 years ago continues to result in high present-day As fluxes from the sediment-water interface. Correction for diagenesis was necessary for two of the eight lakes, likely due to their lower sedimentation rates which allows longer contact between deposited As and reactive zones close to the sediment-water interface.
1.3 Introduction
Wastes produced by mining and smelting activities during past decades contain high levels of metal(loids), which may pose risks to humans and ecosystems. Management and monitoring of mine emissions are thus of global concern (Barats et al., 2020; Barcelos et al., 2020; de Souza Neto et al., 2020; Schneider et al., 2020).Unfortunately, monitoring records of metal(loid) deposition are too short and too sparse across remote mining areas, including the Canadian boreal zone where substantial mining and processing has occurred during the past century (Roberts et al., 2020). Thus, the rates of anthropogenic metal(loid) deposition remain poorly constrained despite that spatial and temporal patterns of deposition are important to inform environmental regulation. In fact, in remote and sparsely populated sub-arctic and arctic regions, a posteriori reconstruction of past contaminant deposition is
likely the only way to access both temporal trends relevant to environmental regulation, and contemporary fluxes that continue to be supplied from legacy deposition.
Lakes are depositional basins that are often the end point of contaminant transport pathways, and materials supplied via their airshed and watershed typically become deposited in the bottom sediments in a time-ordered sequence. Thus, lake sediment cores are widely used as a posteriori archives of spatio-temporal patterns of contaminant deposition from natural and anthropogenic sources (Couillard et al., 2008; Tropea et al., 2010; Wiklund et al., 2017). Because lakes are often permanent features of the landscape and are widespread in the northern hemisphere (Downing et al., 2006), they can be selected for collection and analysis of sediment cores to reveal the spatio-temporal influence of point and diffuse sources of concern.
As recognized by Outridge and Wang (2015), sedimentary archives of contaminants are only reliable if the elements deposited at the sediment surface remain immobile. While elements such as lead (Pb) (Gallon et al., 2004) and mercury (Hg) (Cooke and Bindler, 2015) have been shown to remain stable in sediments during extended periods of time, redox-sensitive elements such as As (Couture et al., 2008; Couture et al., 2010) and molybdenum (Mo) (Chappaz et al., 2008) can be redistributed during diagenesis. Arsenic can be sorbed to, and remobilised with, iron (Fe) (Kneebone et al., 2002; Root et al., 2007) and manganese (Mn) (oxy)hydroxides (Lock et al., 2018) as they are recycled below the sediment-water interface (SWI). Under sulfate-reducing conditions, As can be sequestered with sulfides (Bostick and Fendorf, 2003; Couture et al., 2010; O'Day et al., 2004) and thiols (Langer et al., 2012; Schuh et al., 2018). Such diagenetic redistribution implies that stratigraphic profiles of the concentration of such elements may not be faithful records of its depositional flux.
In addressing this issue, Couture et al. (2008) have assessed As post-depositional mobility by accounting for the quantity of As added to, or removed from, the sediment during burial. This is achieved by combining information on burial rates, obtained via sediment core dating, and reaction rates estimated by inverse diagenetic modelling (Boudreau, 1997) of dissolved As concentrations in the porewater. The extent to which the sediment records of redox-sensitive elements such as As systematically require correction for diagenesis remains, however, unclear. Here we use measurements of sedimentation rate, As concentrations in sediment and porewater and inverse diagenetic inverse modelling to reconstruct the temporal variation in As deposition at lakes along a 80-km transect from Giant and Con mining area in the Canadian sub-arctic, and determine the extent to
which legacy emissions that peaked 70 years ago continue to be mobilized from the sediments to the water column.
1.4 Materials and Methods
1.4.1 Study Sites.
Giant (62o 29’N, 114o 21’W) and Con (62o 26’N, 114o 22’W) mines are located in the sub-arctic Yellowknife area, Northwest Territories, Canada, where gold from arsenopyrite ore (FeAsS) was extracted from 1949 to 1999. This refractory ore required roasting, which led to the formation of arsenic trioxide (As2O3(s) ). Specifically, Giant Mine has been the largest single source of As emissions in the area. It is estimated that more than 20,000 tonnes of As trioxide were released directly into the atmosphere (Wrye, 2008), with most emissions during the 1950s. Widespread As contamination in the vicinity of the mine has been extensively documented (Andrade et al., 2009; Bromstad et al., 2017; Fawcett et al., 2015; Galloway et al., 2015; Galloway et al., 2012; Galloway et al., 2018; Houben et al., 2016; Hutchinson et al., 2007; Palmer et al., 2020; Palmer et al., 2019; Palmer et al., 2015; Schuh et al., 2018; Schuh et al., 2019; Thienpont et al., 2016; Van Den Berghe et al., 2018; Wagemann et al., 1978).
We collected water samples and sediment cores from eight lakes along an 80-km transect northwest of Giant Mine, near the city of Yellowknife. These lakes (Table 1) are located at approximately ~10 km increments from each other in the direction of the prevalent winds from the southeast to the northwest (Galloway et al., 2018; INAC, 2010). Lakes were visited by helicopter on June 1-3, 2018.
Table 1. Location and characteristics of the study lakes
Name Coordinates (DMS) Distance
from the mine (km) Max depth (m) pH Catchment Area : Lake Area ratio Elevation (m.a.s.l.) Ionic strength (μS cm-1) NW10 62°33'10"N114°31'34"W 10.5 1.5 6.43 8.56 191 46.9 NW20 62°36'30"N114°36'19"W 17.8 4 6.19 5.68 194 48.5 NW30 62°40'20"N114°48'43"W 29.8 3 6.17 11.54 180 68 NW40 62°44'20"N114°57'30"W 40.7 8 6.4 19.36 182 115.1 NW50 62°49'32"N115° 0'34"W 49.6 24 6.75 6.25 191 103.9 NW60 62°50'4"N115° 9'30"W 55.7 3.5 6.3 11.94 183 105.6 NW70 62°57'4"N115°22'2"W 72.5 5 6.6 3.72 192 105 NW80 63° 0'7"N115°26'40"W 79.0 7 6.6 1.11 173 141.4
1.4.2. Sampling and sample treatment.
Surface water samples were collected prior to sediment collection ~10 cm below the surface. The sample was collected with an acid-washed syringe, rinsed with lake water. 10-15 ml of sample passed through a Whatman 0.45 µm syringe filter and into 15 ml Falcon tubes. Samples were stored at 4°C until analysis.
Rhizon lysimeters (Seeberg-Elverfeldt et al., 2005) were used to extract porewater from the sediment cores at 1-cm intervals from 1-2 cm above the sediment-water interface (SWI) down to 10 cm below. A predrilled core tube was used with holes at 1-cm intervals for the insertion of the Rhizons (Couture et al., 2018). All Rhizons were rinsed with 0.2% HNO3 prepared with double-distilled acid, then flushed with ultra pure water. The porewater samples were extracted using 10 ml syringes and transferred directly into acid-washed 12 ml HDPE vials (Vacuette) containing 200 µL of double-distilled HNO3 and stored at 4˚ C until analysis.
Sediment cores were collected at or near the deepest location of each lake, assessed with a handheld depth sounder. Two sediment cores were retrieved from each lake (Table 1) using a Uwitec gravity corer equipped with 9-cm diameter core tube. One core was set aside for 210Pb dating and used for measurements of total solid-phase element concentrations, and porewater was extracted from one core immediately upon return by helicopter to the field base. The first sediment core was sectioned at 0.5-cm intervals and samples down to 40 cm were placed in Whirl-Pak bags and refrigerated at 4oC. The second core was discarded after porewater retrieval. The LOI water content was determined using the weights before and after baking at 90°C. Organic content was determined by loss on ignition (LOI) at 550˚C.
1.4.3. Chemical Analyses.
Surface water samples were processed at ALS Laboratories (Vancouver) for total and dissolved As, Fe and Mn concentrations in water following the EPA standards 200.22/6020A and APHA standards 3030B/6020A.
Porewater As concentrations were determined using inductively coupled plasma triple quad mass spectrometry (ICP-QQQ-MS, Agilent 8900) while those of major elements (Fe, Mn, Ca, S) were determined by inductively coupled plasma atomic emission spectrometry (ICP-AES, Thermo Scientific duo iCAP 7400) at Université Laval. Five measurements of the certified reference material SLRS-6 (river water, National Research Council of Canada, 0.57 ± 0.08 µg L-1 As) yielded a mean As concentration of 0.55 ± 0.02 µg L-1, or 96% of the certified value. Dissolved concentrations are identified by brackets (e.g., [As]).
Sediment samples were processed at ALS Laboratories (Waterloo) for solid-phase concentrations of 33 elements, including As, Fe and Mn, which will be discussed here. Sediments were sieved (2 mm) prior to mineralization using heated digestion in nitric and hydrochloric acids. Analyses were performed using a collision/reaction cell (CRC) ICP-MS, following EPA standards 200.2/6020A, yielding an accuracy of 98% against the certified reference material TILL-2. Solid-phase concentrations are identified by curly braces (e.g., {As}).
1.4.4. Sediment core dating.
Stratigraphic variation of 210Pb (46.5 keV), 137Cs (661 keV), 214Bi (609 keV) and 214Pb (295 keV and 351 keV) activities in the sediment cores were determined by low-background gamma-ray spectrometry (co-axial HPGe; Ortec GWL-120-15) at the University of Waterloo’s WATER Lab according to Appleby et al. (1992) after equilibration of the sealed sample for >20 days. Excess 210Pb activity was obtained by subtracting the 226Ra activity (estimated as the weighted average activity of daughter isotopes 214Bi and 214Pb), from measured total 210Pb activity. For all the lakes, sediment age was determined from the 210Pb data using the CRS (Constant Rate of Supply) age model, assuming no mixing (Appleby, 2001; Appleby and Oldfield, 1978). Further details on dating methods and results are reported in Jasiak (2020).
1.4.5. Diagenetic Modelling.
Inverse modelling was performed on each As porewater profile with the code PROFILE (Berg et al., 1998) to extract an optimised value of the net reaction rates (RAsnet), following the approach outlined in Couture et al. (2008). This code solves a transport-reaction equation representing diagenesis (Boudreau, 1999), which assumes steady-state and neglects advective transport. Based on reported anoxia in the hypolimnion of small lakes in this region, both under ice and during summer (Palmer et al., 2019), we further assumed that transport by bioirrigation and bioturbation could be neglected (Couture et al., 2010), such that:
𝑅 = (φ𝐷 [ ]) (Eq. 6)
where x is depth (positive downward from SWI), 𝜑 is porosity obtained with organic matter content and water content (Avnimelech et al., 2001), Ds is the diffusion coefficient for arsenate (H2AsO 4-) in sediments, [As] the concentration in the porewater, and RAsnet is the net production rate of As (or consumption if negative) in mol cm-3 s-1.
The diagenesis equation was solved with PROFILE using porewater [As] profiles, the porosity, and Ds values as inputs. Ds was assumed to be 𝜑2D, where D is the diffusion coefficient in water for H2AsO4- (Boudreau, 1999), yielding a value of 4.72 × 10-6 cm2 s-1 adjusted at 4˚C with the Stokes-Einstein equation (Li and Gregory, 1974). Top and bottom boundary conditions were set as the