1 Université de Picardie Jules Verne
UFR de Médecine AMIENS
Année 2017
Thèse pour le Diplôme d’État de Docteur en Médecine
(Spécialité Chirurgie Orthopédique et Traumatologie)
Quel bénéfice pour les patients allergiques aux
métaux réopérés par des prothèses revêtues ?
Étude rétrospective à propos de 30 cas de PTG
AS e.motion®.
Présentée et soutenue publiquement le 06 juillet 2017 Par BULAÏD Yassine
Président du Jury : Monsieur le Professeur MERTL Membres du Jury : Monsieur le Professeur JARDE
Monsieur le Professeur GABRION Monsieur le Docteur CAZENAVE Monsieur le Docteur DEHL Directeur de Thèse : Monsieur le Professeur HAVET
2
RÉSUMÉ
Introduction : Les reprises d’arthroplastie de genoux pour suspicion d’allergie aux métaux
nécessitent la pose d’implants hypoallergéniques dont l’utilité est en court d’évaluation. Cette étude avait pour objectif d’évaluer les résultats fonctionnels postopératoires à court terme lors de reprises d’arthroplastie de genou par des prothèses revêtues pour suspicion d’allergie aux métaux. Les objectifs secondaires étaient de rapporter les résultats cliniques et radiologiques ainsi que la survie de ces prothèses.
Matériel et Méthodes : Il s’agit d’une étude rétrospective, monocentrique portant sur une série
continue de 30 prothèses revêtues de nitrure de zirconium AS e.motion® B. Braun, Aesculap, (Tuttlingen, Allemagne), implantées entre mai 2011 et novembre 2016 pour suspicion d’allergie. Les critères de non inclusion comprenaient les antécédents d’arthrite septique du genou opéré, ainsi que les malpositions. Le critère de jugement principal était l’évolution du score IKS du genou. Les critères de jugements secondaires comprenaient l’évolution des amplitudes articulaires, des douleurs ainsi que du score de qualité de vie SF36 et du score radiologique d’Ewald. La survie a été calculée en suivant la méthode de Kaplan-Meier.
Résultats : Le score IKS moyen a augmenté de 39 points [51,4 - 26,4] entre la mesure
préopératoire et celle effectuée au recul moyen de 3 ans. Le gain en amplitude articulaire au recul était de 17° [9,5 - 24,5]. Le score SF36 était de 44,6 et 44,2 au recul pour respectivement le ‘score composite physique’ et le ‘score composite mental’. Nous avons retrouvé 6% de liserés radiologiques non évolutifs. La survie était de 92%.
Conclusion : Il existait une amélioration fonctionnelle significative ainsi qu’un gain
d’amplitude articulaire lors de la reprise de PTG pour allergie aux métaux. La survie des prothèses AS e.motion® à 3 ans semble être bonne.
D’autres évaluations à plus long terme devraient être effectuées afin de confirmer ces résultats.
Mots clés : Arthroplastie totale de genou – Reprise – AS e.motion® – Allergie –
3
Introduction
L’hypersensibilité aux métaux utilisés dans la fabrication des prothèses totales de genou (PTG) ou aux ciments utilisés pour sceller ces prothèses est un sujet discuté (1,2). Des recommandations récentes fournissent aux chirurgiens des outils diagnostiques et des algorithmes de prise en charge lors d’une suspicion d’allergie. Ainsi, le diagnostic se fait au moyen d’une anamnèse rigoureuse à la recherche d’une ou de plusieurs intolérances et par la positivité des tests épicutanés considérés comme le gold standard.
L’hypersensibilité aux métaux peut être suspectée après la mise en place d’une PTG. La symptomatologie est alors diverse et souvent assez peu spécifique. Le patient peut présenter des douleurs au repos, non mécaniques, une raideur, des épanchements récidivants, un retard de cicatrisation, une dermatite allergique localisée en regard de la cicatrice ou généralisée, une impotence fonctionnelle, voire une instabilité ou encore un descellement (2). Ces symptômes apparaissent le plus souvent dans la première année et doivent faire éliminer une cause infectieuse ou un syndrome douloureux régional complexe (SDRC) (3).
Il existe 2 types d’implants « hypoallergéniques ». Les premiers sont des implants fabriqués avec les métaux habituels (chrome, cobalt, nickel) mais revêtus d’une couche d’un matériau de type céramique : nitrure de zirconium (e.motion® ou Columbus® Knee System, B. Braun, Aesculap, Tuttlingen, Allemagne), nitrure de titane (PFC Sigma®, Raynham, MA, États-Unis) ou oxyde de zirconium (Oxinium® Genesis II®, Smith & Nephew, Warsaw, IN, États-Unis) avec un nombre et des épaisseurs de couches variables (4). Les autres sont des boucliers fémoraux fabriqués entièrement en céramique : alliage de titane ou de zirconium (Multigen Plus® Total Knee system, Lima Corporate, Villanova di San Daniele del Friuli, Italie). Les boucliers de chaque type peuvent s’implanter avec une embase dédiée en métal, (TiAL6V4 pour la Multigen-Plus®) ou à des embases tibiales en polyéthylène (All-Poly® Genesis II®, Smith & Nephew, Warsaw, IN, États-Unis) (5).
À notre connaissance, aucune étude n’a encore évalué le bénéfice et les résultats fonctionnels d’une reprise de prothèse de genou pour allergie aux métaux par des implants revêtus. Notre objectif principal était de préciser l’amélioration fonctionnelle chez les patients opérés d’une reprise de PTG pour suspicion d’allergie aux métaux par des implants revêtus de nitrure de zirconium (PTGRNZ) au recul moyen de 3 ans. Secondairement, nous en avons estimé les résultats cliniques et radiologiques ainsi que la survie de ces implants.
4
Matériels et méthode
Concept de l’étude
Il s’agit d’une étude monocentrique, rétrospective et multi-opérateur d’une série continue d’un service hospitalier universitaire.
Population
Nous avons inclus une série continue de patients opérés de mai 2011 à novembre 2016 d’une reprise de PTG avec pose de PTGRNZ de la gamme AS Solution® (B. Braun®, Aesculap, Tuttlingen, Allemagne).
Les critères d’inclusions étaient toutes les reprises de PTG par PTGRNZ pour suspicion d’allergie aux métaux avec un recul minimum de 6 mois. La suspicion diagnostique d’intolérance reposait sur l’anamnèse et sur la positivité des tests épicutanés.
Les critères de non inclusion étaient l’existence d’une étiologie infectieuse, mécanique, ou neurogène pouvant expliquer la symptomatologie. Celles-ci étaient systématiquement recherchées par un examen clinique, des bilans biologiques répétés : dosage sanguin de la protéine C réactive (CRP) et des leucocytes, une ou deux ponctions du genou, une scintigraphie aux leucocytes marqués, un bilan radiographique ainsi qu’une tomodensitométrie (TDM). Les douleurs neuropathiques (DN), recherchées par le questionnaire DN4 (6,7) et prises en charge en consultation de la douleur sans amélioration notable ne faisaient pas partie des critères de non inclusion.
Au total, 34 reprises de PTG avec pose de PTGR ont été effectuées chez 32 patients. Trente de ces reprises ont été réalisées pour suspicion d’allergie aux métaux chez 28 patients (figure 1). Vingt-six patients ont été revus en consultation par deux examinateurs indépendants et deux ont été revus par leur opérateur et interrogés par téléphone.
5
Figure 1 : Flow chart
Technique opératoire et implant
Les patients ont été opérés par 4 chirurgiens séniors avec le même protocole. L’incision cutanée reprenait la cicatrice initiale. L’arthrotomie était para-patellaire médiale, excepté pour un patient dont la patella baja a indiqué une arthrotomie latérale avec ostéotomie de la tubérosité tibiale. Tous les implants ont été scellés au ciment Palacos® gentamicine (Zimmer® Biomet, Warsaw, USA) ou Ceraver® (Roissy-en-France, France).
Tous les implants de reprise étaient du système e.motion® de la gamme AS Solution® (B. Braun, Aesculap, Tuttlingen, Allemagne). Il s’agit d’une PTG métallique postéro-stabilisée composée d’un alliage de CoCrMo (ISO 5832-4) contenant de 58,65% à 64,65% de cobalt, de 26,5% à 30,0% de chrome, de 4,5% à 7,0% de molybdène, et moins d’1,0% de nickel. Un revêtement multicouche (multilayer coating system - Advanced Surface®, B. Braun) recouvre cet alliage afin de réduire le relargage d’ions métalliques. Le revêtement comprend successivement une fine couche adhérente de chrome, cinq couches alternées d’un alliage de chrome, nitrure de chrome et nitrure de carbone (CrNCrCN), ainsi qu’une couche finale de nitrure de zirconium (ZrN). Ce système de revêtement à sept couches a une épaisseur de 4 µm
6
Protocole de révision
Le critère de jugement principal était l’évolution du score de la Knee Society (IKS) (2011 en version française) avant et après chirurgie (9).
Les critères secondaires incluaient l’évolution des amplitudes articulaires en considérant une raideur comme une amplitude articulaire inférieure à 75°, ou un flessum de plus de 15° ou des amplitudes articulaires inférieures à 90° chez des patients dont les griefs principaux étaient la raideur et la douleur (10). Nous avons également recherché le score de qualité de vie SF36 au recul, comprenant un score composite physique (PCS) et un score composite mental (MCS), ainsi que la survie des implants (11). La mesure de l’IKS a été effectuée en préopératoire ainsi qu’à la dernière consultation considérée comme la date de recul.
Les mesures radiologiques étaient semi-automatiques en utilisant le logiciel IMAGIKA® (View tech®), sur des clichés de genou de face et de profil en charge, un défilé fémoro-patellaire à 30° de flexion, ainsi que sur un cliché EOS de face et de profil en charge. Nous avons retenu l’index de Caton-Deschamps (ICD), la pente de l’implant tibial (σ), l’angle de flexion de l’implant fémoral (ϒ), le centrage et la bascule de la patella, les angles HKA et HKS, l’angle mécanique fémoral (AMF), l’angle fémoral de face (α), l’angle tibial (β) (12,13). Nous avons également recherché la présence de liserés selon les zones définies par la Knee Society, et l’existence d’un descellement possible ou certain.
Traitement des données
Le recueil des données et les analyses statistiques ont été réalisés grâce au logiciel SPSS® (IBM v24.0, Chicago, USA). L’analyse du critère de jugement principal a été réalisée par le test t de Student pour les variables quantitatives appariées. Nous avons effectué une analyse univarié afin d’étudier l’IKS global préopératoire et au recul selon le délai entre la PTG de première intention et la pose de la PTGRNZ.
L’analyse des critères secondaires a été effectuée avec le test t de Student pour les variables quantitatives appariées. La survie a été calculée selon la méthode de Kaplan-Meier. L’échec a été défini comme toute ablation et changement d’un implant. Tous les tests statistiques ont été effectués en considérant le risque de première espèce à 5%.
7
Résultats
Les 28 patients (30 RPTG) revus étaient 22 femmes et 6 hommes, d’un âge moyen au moment de l’intervention de reprise de 60,2 ans (de 38 à 82). Il s’agissait du genou gauche dans 16 cas et du genou droit dans 14 cas. L’indice de masse corporelle était en moyenne de 29 kg/m2 (de 23 à 37). La reprise a été réalisée en moyenne à 37 mois (de 3 à 92) après la PTG initiale. Le score ASA moyen avant la chirurgie de reprise était de 2. Parmi les prothèses initiales, 5 n’étaient pas cimentées et 3 n’étaient cimentées qu’au niveau de l’embase tibiale. Huit étaient descellées. Onze genoux ont été opérés plusieurs fois avant la pose de PTGRNZ, 5 pour reprise (RPTG), 3 pour mobilisation sous anesthésie et 3 pour arthrolyse sous arthroscopie.
Vingt-quatre patients avaient des antécédents d’intolérance aux objets contenant du métal et des tests épicutanés positifs aux métaux suspectés. Quatre avaient uniquement des antécédents d’intolérance aux objets et des tests épicutanés non concluants. Vingt-trois patients étaient allergiques au nickel uniquement, 2 au chrome uniquement, 1 au cobalt uniquement, 1 au nickel et au chrome, 1 au chrome et au cobalt. Une dermatite allergique était retrouvée chez 3 patients (11%) des cas. Le délai moyen entre la mise en place de la première PTG et l’apparition des premiers signes cliniques était de 3 mois (de 2 jours à 10 mois).
Résultats cliniques au recul
Le recul moyen était de 35 mois (de 6 mois à 71 mois). La moyenne du score IKS global est passée de 96 à 135, soit une amélioration moyenne statistiquement significative de 39 points [51 - 26] (t = 6,342 et p < 0,001), soit +40% au recul. Cette amélioration a concerné 29 PTG. L’IKS objectif moyen est passé de 43 à 62 soit une augmentation de 19 points [10 - 29] (p < 0,001). L’IKS subjectif moyen est passé de 52 à 72 soit une augmentation de 20 points [12 - 27] (p < 0,001) (tableau 2).
Le score IKS global préopératoire était influencé par le délai entre la pose de la PTG de première intention et celle de la PTGRNZ. Plus ce délai était long et plus ce score était bas. Le coefficient de corrélation était de 0,24. L’IKS global postopératoire n’était pas influencé par le délai de reprise (coefficient de corrélation de 0,02). Il ne semblait pas exister une amélioration du score IKS global postopératoire en fonction du recul (coefficient de corrélation de 0,08).
8
Tableau 2 : résultats au recul
Figure 2 : IKS global préopératoire selon le délai de reprise
Figure 3 : résultats sur les critères de jugement au recul
Pré opératoire Post opératoire Différence Écart-type p
IKS total 96 135 39 33,6 <0,001 IKS objectif 43 62 19 25 <0,001 IKS subjectif 52 72 20 19,5 <0,001 Flexion 85 102 17 20 <0,001 PCS / 44,6 / / / MCS / 44,2 / / / y = -0,2414x + 104,2 0 20 40 60 80 100 120 140 160 0 2 0 4 0 6 0 8 0 1 0 0 IKS P R ÉO PÉ R A TO IR E
DELAI (MOIS) ENTRE LA POSE DE LA PTG DE PREMIERE INTENTION ET LA REPRISE PAR PTGRNZ
9
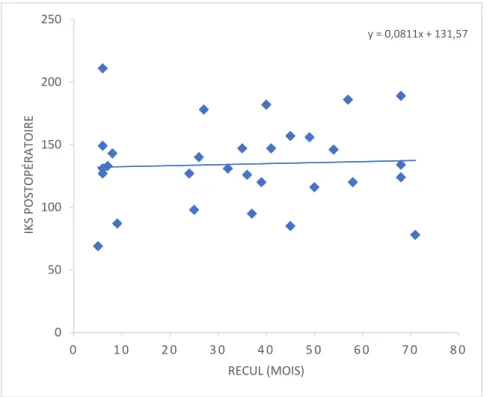
Figure 3 : IKS global postopératoire selon le délai de reprise
Figure 4 : IKS global postopératoire selon le recul
y = -0,0207x + 135,17 0 50 100 150 200 250 0 2 0 4 0 6 0 8 0 1 0 0 IKS P O ST O PÉ R A TO IR E
DELAI (MOIS) ENTRE LA POSE DE LA PTG DE PREMIERE INTENTION ET LA REPRISE PAR PTGRNZ y = 0,0811x + 131,57 0 50 100 150 200 250 0 1 0 2 0 3 0 4 0 5 0 6 0 7 0 8 0 IKS P O ST O PÉ R A TO IR E RECUL (MOIS)
10
Vingt-trois genoux étaient raides en préopératoire, 6 l’étaient au recul. Le gain d’amplitude articulaire était statistiquement significatif de 17° [9,5 - 24,5] (t = 4,640 et p < 0,001). Cette amélioration concernait 25 genoux. Les amplitudes articulaires des 5 autres genoux n’ont pas évolué.
Le score SF36 de qualité de vie au recul était de 44,6 pour le score composite physique et 44,2 pour le score composite mental.
Pour une patiente, le score IKS global est passé de 109 à 69 au recul. Son score PCS était de 14 et son MCS de 21. Un autre patient présentait une augmentation du score IKS global de moins de 6 points, minimum perceptible par le test. Ses scores PCS et MCS étaient respectivement de 55 et 47.
Quinze des vingt-huit patients (15 genoux) présentaient des douleurs neuropathiques postopératoires dont cinq nécessitaient une neurostimulation. Parmi ces patients, 6 étaient suivi pour dépression.
Toutes les dermatites allergiques avaient disparu en postopératoire.
Résultats radiologiques au recul
Au recul, l’angle HKA moyen était de 181° (de 173 à 188). L’angle AMF moyen était de 89° (de 84 à 92), l’angle α moyen de 98° (de 95 à 102) et l’angle β moyen de 88° (de 85 à 92). L’angle γ moyen était de 7° (de 4 à 16) et l’angle σ moyen de 4° (de 0 à 13). L’ICD moyen était de 0,8 (de 0,4 à 1,4) avant la reprise et de 0,9 (de 0,6 à 1,4) au recul. La bascule et le centrage patellaires moyens étaient respectivement de 9,3° (de 0 à 19) et de 2,4 mm (de 0 à 12). Nous avons retrouvé 6% de liserés radiologiques non évolutifs.
Survie
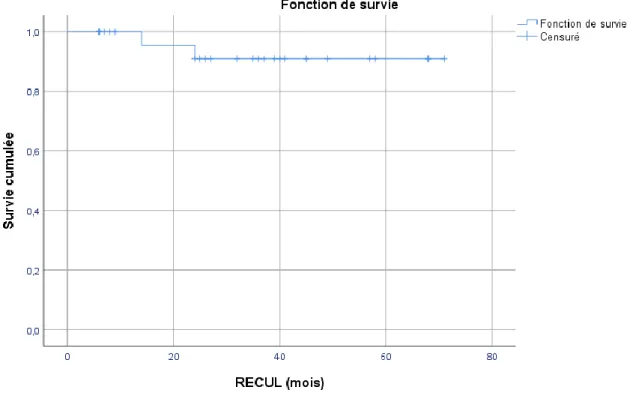
Nous avons défini comme échec toutes les reprises chirurgicales avec changement d’au moins un implant de la prothèse. En se basant sur ce critère, le taux de survie moyen était de 93,3% à 3 ans de recul moyen (figure 5). Une patiente a été reprise pour luxation de la patella à 2 ans de la pose de PGRNZ et l’autre pour enfoncement du plateau tibial à 1 an. Deux patients ont nécessité une mobilisation sous anesthésie générale à 1 mois de la reprise. Le taux de complication était donc de 13,3 %.
11
Figure 5 : courbe de survie selon la méthode de KAPLAN MEIER
Discussion
Critiques de l’étude
Notre étude concerne une série continue, sans aucun perdu de vue. Par ailleurs, tous les patients ont bénéficié du même protocole diagnostique préopératoire et des mêmes modalités de suivi. Néanmoins, elle est rétrospective. Un biais de sélection du fait de la pathologie étudiée ne peut être exclu. En effet, la population étudiée présentait des caractéristiques pouvant influer sur les critères de jugements principaux et secondaires. Il s’agissait majoritairement de femmes, allergiques avec des scores fonctionnels préopératoires bas et des genoux raides.
Nous avons utilisé le nouveau score IKS en tant que critère de jugement principal pour les avantages qu’il procure et la possibilité de comparaison par rapport aux autres séries (9). Les critères secondaires ont été choisis en fonction du retentissement de la pathologie étudiée. Nous avons donc insisté sur la raideur car elle est décrite comme l’une des principales doléances des patients allergiques aux métaux (2,14,15). Nous avons utilisé le score SF36 car certains auteurs, comme Nam et al (16), ont montré que le fait de rapporter une allergie à un métal pouvait influencer l’état mental ou physique des patients en plus des scores fonctionnels.
12
L’allergie aux métaux : un diagnostic difficile
L’allergie aux métaux sur PTG est un diagnostic difficile. Un interrogatoire rigoureux est essentiel à la démarche diagnostique. Ainsi, en Allemagne, les chirurgiens ont l’obligation médicolégale de dépister les allergies avant la mise en place d’une PTG de première intention ou de reprise. Ils peuvent alors s’aider d’un questionnaire sur le mode de vie et les antécédents pour rechercher une intolérance aux métaux : nickel (bijoux métalliques, boutons de pantalon), chrome (présent dans les gants et les ceintures en cuir), cobalt. Une version traduite en français est disponible sur le site de la Société Française de chirurgie de la Hanche et du Genou (17).
Le diagnostic d’allergie ou d’hypersensibilité aux métaux est considéré comme un diagnostic d’élimination. Pour Park et al (18), il ne doit être évoqué qu’après avoir éliminé les diagnostics différentiels : infection, instabilité, malpositions, clunk syndrome, douleurs fémoro-patellaires, descellements aseptiques précoces et SDRC. Aucun signe clinique ne permet de distinguer l’allergie aux métaux de l’infection à bas bruit (19). Lachiewicz et al(20)
recommandaient aussi d’effectuer un dosage sanguin de la CRP et des leucocytes, ainsi que des analyses répétées du liquide articulaire avec cultures prolongées aérobies et anaérobies, mais sans recherche de levures.
Une fois les diagnostics différentiels éliminés, s’il existe une suspicion d’allergie aux métaux, des tests épicutanés doivent être menés par des allergologues ou des dermatologues. Le panel de métaux testés a fait l’objet de recommandations. Il convient de tester les métaux présents dans les implants : chlorure de cobalt, sulfure de nickel, trichlorure de chrome, dichromate de potassium, aurothiosulfate de sodium, titane, trichlorure de vanadium, oxyde de zirconium, manganèse, niobium, ainsi que ceux présents dans le ciment : méthyl-méthacrylate, peroxyde de benzoyle, gentamycine et mupirocine (21,22).
Si les tests épicutanés restent le gold standard actuel, il faut apporter une attention particulière à leurs effets secondaires : irritation cutanée locale, « angry back syndrome » (hyper irritabilité pouvant influencer les résultats des tests adjacents) et risque théorique de sensibilisation pouvant induire des faux positifs (23). Ces tests ne seraient ni suffisants ni nécessaires pour suspecter une hypersensibilité aux métaux (20,23,24). En effet, ils ne détecteraient que les mécanismes d’allergies cutanées. Ces derniers sont connus et surviennent par la médiation de cellules dendritiques, puis de lymphocytes T. Les mécanismes des allergies intra-articulaires sont peu connus. Les test in vitro comme le LTT en serait un meilleur reflet
13
stimulation d’ions métalliques. Le résultat s’exprime sous forme d’index de stimulation (IS)
(26). Le Memory Lymphocyte Immuno-Stimulation Assay MELISA® (Health Diagnostics and Research Institute, South Amboy, NJ, USA) qui est un LTT modifié aurait une reproductibilité de 94% si l’IS < 3 et de 99% si l’IS > 3 (27). La spécificité du test semble être bonne. Dans une étude prospective sur 56 patients allergiques au Titane, avec des tests épicutanés négatifs et un LTT positif, 54 ont accepté l’ablation de l’implant et ont vu une résolution complète de leur symptomatologie. Quinze de ces patients ont effectué le LTT à distance avec des résultats devenus négatifs (28). Cependant la mise en œuvre du LTT impose des contraintes
d’acheminement et de conservation du prélèvement sanguin afin de limiter les faux positifs du fait de la destruction des lymphocytes T. En effet, l’acheminement doit être rapide, idéalement dans les 24 heures après le prélèvement et la conservation à température ambiante, à moins de 30°C (23). La leucopénie et la prise de traitement stéroïdien sont des contre-indications. Du fait de ces contraintes et du prix élevé du LTT, les test épicutanés restent le gold standard (24)
Selon Pinson et al, le dosage sanguin des métaux ne semble pas être utile car il n’existe pas de corrélation entre la concentration sanguine d’un ion métallique et l’expression clinique d’une hypersensibilité (22).
Le diagnostic formel d’une réaction allergique à un implant est impossible en préopératoire. Selon Middleton et Toms, il ne pourrait être confirmé qu’« à posteriori » sur la résolution de la symptomatologie après ablation des implants suspects (1). Basko-Plluska et al, rapportaient 5 cas de réactions cutanées après mise en place d’implants orthopédiques (2 ostéosynthèses et 3 prothèses totales de hanche) avec des patch tests et LTT négatifs. La résolution des troubles cutanés après changement d’implants par des prothèses revêtues a été immédiate (29). En pratique, nous pensons que le diagnostic avant la reprise repose sur un faisceau d’arguments : une anamnèse compatible, l’apparition des symptômes dans un délai court (les premiers mois), la positivité des test épicutanés et/ou LTT (même si leur spécificité et leur sensibilité resterait à définir) et l’absence d’autres étiologies (14,20).
Selon les projections, le nombre de PTG de première intention devrait augmenter de 673% entre 2005 et 2030 aux États-Unis (30). Parallèlement, la sensibilisation aux métaux augmente également du fait de nos habitus (31,32). Ainsi, 1,13% des patients porteurs de PTG seraient concernés par une hypersensibilité au nickel ou au cobalt et 1/3 d’entre eux seraient susceptibles d’être repris pour ce motif (29,33). Le nombre de RPTG pour suspicion d’allergie devrait donc
14
augmenter. Par ailleurs, dans une méta-analyse sur les tests d’hypersensibilité aux métaux avant arthroplastie, Granchi et al ont rapporté 4 fois plus de descellement de PTG chez les patients ayant des antécédents d’hypersensibilité avant la mise en place de l’implant (24).
Les résultats des prothèses de type hypoallergénique ont déjà fait l’objet d’études, mais aucune n’a cherché à spécifier ces résultats chez les patients allergiques aux métaux. Nous avons retrouvé une amélioration fonctionnelle statistiquement significative, chez les patients opérés pour suspicion d’allergie aux métaux sur PTG avec pose de PTGRNZ.
Comparaison avec les résultats des implants en Chrome-Cobalt
Nos résultats statistiques en analyse univariée semblaient inférieurs à ceux des séries de RPTG chez des patients non allergiques. Dans une méta analyse, Saleh et al (34), ont cherché à évaluer les résultats fonctionnels après RPTG par des implants habituels. Le Global Knee Score (GKS), comprenant le score IKS et le score du Hospital for Special Surgery (HSS), avait doublé entre l’évaluation préopératoire et le recul moyen de 53 mois, passant de 30,8 points à 66,2 points. Plusieurs facteurs pourraient expliquer nos résultats inférieurs. Ainsi, Kasmire et al (35)
dans une étude rétrospective de 175 RPTG ont montré que le sexe féminin, le niveau de douleurs préopératoires, les scores fonctionnels préopératoires bas, le fait de rapporter une allergie quelconque ou spécifique aux métaux, le motif de reprise comme la raideur, et le nombre de reprises seraient prédictifs de mauvais résultats fonctionnels. Dans leur étude, les scores IKS, WOMAC, ainsi que le SF36 avaient été effectués avant la reprise et à 2 ans de suivi. L’IKS fonction et l’IKS objectif ont été améliorés respectivement de 44,5 à 57,8 et de 46,4 à 76,3. Notre série étudiait des patients allergiques dont une majorité de femmes ayant des scores préopératoires bas et des genoux multi-opérés, raides et douloureux.
Le nombre d’allergies, tout type confondu, semble influencer également les résultats. Ainsi, Mc Lawhorn et al (36), sur une analyse multivariée d’une série rétrospective de 257 PTG, ont montré une relation significative du nombre d’allergies sur le taux de satisfaction dans la réalisation des tâches ménagères, des activités quotidiennes et dans le score de qualité de vie. Dans leur étude, chaque allergie déclarée augmentait de 50% le risque d’insatisfaction. Cette influence concernait également les scores fonctionnels, notamment la douleur et la raideur sans
15
pour autant atteindre les seuils de significativité clinique. Nam et al (16) se sont intéressés plus spécifiquement aux allergies aux métaux. Ils ont trouvé une association entre l’allergie aux métaux rapportée par le patient et les résultats fonctionnels. Sur les 589 PTG étudiées, 24 patients se sont déclarés allergiques aux métaux, dont 21 ont reçu une PTG hypoallergénique. Après appariement entre les patients allergiques et non allergiques, ils ont montré une évolution significativement plus faible du score IKS subjectif chez les patients allergiques. Celui-ci est passé de 43,8 en pré opératoire à 50,8 en post opératoire contre 49,8 à 73,3 pour les non allergiques. L’évolution du PCS du SF12 était plus modérée dans le groupe PTG avec allergie que dans l’autre groupe avec respectivement une différence de 6,2 contre 16,6 (p<0,001). Dans notre série, les scores post opératoires PCS et MCS du SF36 semblaient comparables avec les résultats retrouvés dans les séries d’arthroplasties du genou (11). La seule patiente dont l’IKS global a diminué se plaignait de DN et était suivie pour un syndrome dépressif. Le SF36 était bas et témoignait d’un fort retentissement tant au niveau fonctionnel qu’au niveau de la qualité de vie. Le seul patient dont l’amélioration de l’IKS était infra clinique avait un SF36 dans la norme.
La raideur précoce est l’un des trois signes principaux d’allergie sans que la physiopathologie ne soit décrite (2,16,20,37). Or, la RPTG pour raideur semble être aussi un facteur de mauvais pronostic. Pour Van Kempen et al (38) et Baker et al (39), l’amélioration de l’IKS objectif ainsi que du score douleur étaient moins bons dans les suites des RPTG pour raideur que dans celles effectuées pour douleurs inexpliquées ou descellements aseptiques. Les premiers ont évalué de manière prospective 150 RPTG au recul moyen de deux ans et rapporté une évolution du score IKS objectif significativement plus faible en cas de raideur (de 34 +/- 22 à 48 +/- 18) que dans la série générale (de 57 ± 17 à 76 ± 2). Ils ont également montré une évolution plus lente. La meilleure évolution des scores IKS objectif et subjectif est survenue à 3 mois post opératoire sauf pour le groupe des RPTG pour raideur. Sur 998 RPTG, la deuxième équipe retrouvait une amélioration du score Oxford de 36% pour les raideurs, 57% pour les douleurs et 70% pour les descellements aseptiques à 7 mois de recul. De même, les taux de satisfaction, respectivement de 47%, 58% et 72%, montraient aussi l’influence de la raideur. À l’opposé, les scores fonctionnels et le score de qualité de vie au recul était respectivement de 28% et 44% pour les raideurs, de 15% et 35% pour les douleurs et de 16% et 33% pour les descellements aseptiques. Nos résultats semblent être comparables.
16
En croisant les données du registre danois de PTG et la base de données des centres d’allergologie de la région de Copenhague, Münch et al (40) ont montré que les reprises itératives pouvaient accroitre l’incidence des phénomènes allergiques et ainsi augmenter le risque d’échec d’implants. La libération d’ions métalliques favoriserait l’ostéolyse en augmentant la concentration d’ostéoclastes stimulant des cytokines. Il s’agit donc chez ces patients d’effectuer le bon diagnostic de manière précoce afin d’éviter les reprises itératives et un cercle vicieux qui grèverait le score fonctionnel.
Il en ressort que l’allergie aux métaux sur PTG est un phénomène chronique, les signes cliniques apparaissent rapidement et peuvent limiter la récupération fonctionnelle post opératoire précoce. Les douleurs et l’épanchement limitent les amplitudes articulaires, ce qui peut aboutir à un genou raide, douloureux et peu fonctionnel. Il est alors essentiel d’évoquer l’hypersensibilité aux métaux de manière rapide et adéquate. Brander et al (41) ont étudié l’influence de la douleur et de la dépression sur les résultats d’une cohorte prospective de 83 patients (109 PTG de première intention) à 5 ans. Parmi les 12 patients (13 PTG) considérés comme très douloureux à 1 an (Visual Analog Pain Scale (VAS) > 40), seuls 3 patients (3 PTG) avaient un VAS > 40 à 5 ans de recul. Une seule patiente était insatisfaite. Ainsi, lors d’une arthroplastie de genou de première intention, il existe une amélioration des scores fonctionnels avec le temps. A l’inverse, dans notre série, les scores préopératoires diminuaient avec le délai de reprise. Nous pensons donc que dans un contexte d’allergie aux métaux, la reprise chirurgicale doit être effectuée rapidement, à fin d’éviter l’enkystement des phénomènes de raideur.
Comparaison avec les résultats des implants hypoallergéniques
Les résultats des implants hypoallergéniques ont surtout été étudiés lors de chirurgies de première intention chez des patients non allergiques. Les résultats à court et à moyen terme semblent être bons et la survie comparable à celle des PTG usuelles (tableau 3)(42–48,31).
18
Tableau 3 : études sur les implants « hypoallergéniques »
1ère int : première intention ; PNA : population non allergique ; CCP conservation du croisé postérieur ; PS : postérostabilisé ; OKS : Oxford Knee Score ; ZrN : nitrure de zirconium ; Ti6Al4V : titane aluminium vanadium ; CoCrMo : chrome cobalt et molybdène ; UHMWPE : polyéthylène ultra-haute densité ; TiNbN : nitrure de titane-nobium ; LTT : test de transformation lymphocytaire ; IKS : Internation Knee Score ; HSS : Hospital for Special Surgery score ; WOMAC : West Ontario MacMaster universities osteoarthritis index score ; UCLA : University of California Los Angeles score ; OxZr : oxyde de zirconium ;
1 : B. Braun, Aesculap (Tuttlingen, Allemagne) ; 2 : Lima Corporate (Villanova di San Daniele del Friuli, Italie) ; 3 : Zimmer-Biomet ( Warsaw IN États-Unis) ; 4 : Smith and Nephew ( Memphis, TN, États-Unis) ;
19
Selon Ajwani et Charalambos (5), l’avantage des PTG revêtues par rapport aux PTG en céramique serait qu’elles conservent la même technique de pose (même ancillaire, mêmes disponibilités de quilles et de calles revêtues) et les mêmes propriétés tribologiques que la plupart des prothèses. Galetz et al (49), lors d’une étude sur la résistance à l’abrasion des revêtements d’oxyde de zirconium et de nitrure de titane ont rapporté un risque d’altération du revêtement lié à la différence entre la dureté des matériaux de l’implant et du revêtement. Il existerait donc un risque d’atteinte du revêtement, soit lors de la pose soit à plus long terme, qui exposerait le patient à une possible nouvelle réaction allergique par contact des couches sous-jacentes de chrome et de cobalt. Par ailleurs, Lützner et al (47) ont décrit l’apparition d’une réaction allergique aux métaux suite à la pose d’une PTGRNZ. Ils suspectaient des facteurs extérieurs aux implants, comme les instruments chirurgicaux ou les conditions au bloc opératoire. Pour eux, les débris métalliques générés par les instruments en acier inoxydable comme les scies seraient une source importante de nickel biodisponible. En effet, les lames scies contiendraient 10 à 14% de nickel (20). D’ailleurs, la présence de débris d’acier inoxydable dans les tissus péri-prothétiques des patients opérés avec pose d’implant ne contenant pas ces matériaux a déjà été documentée (50).
Les implants composés entièrement de céramique (alliage de titane ou de zirconium) réduiraient le risque d’exposition au nickel, au cobalt, et au chrome (51). En contrepartie, il existerait un risque théorique de fracture du bouclier fémoral. Ainsi, Bergschmidt et al (52) ont rapporté un cas de fracture d’implant à la suite d’un traumatisme, sur 109 PTG. Les implants tibiaux en céramique ne sont pas commercialisés. Par contre, il est possible d’associer aux boucliers en céramique un implant tibial de type full-polyéthylène.
Controverse
La conduite à tenir, tant diagnostique que chirurgicale, reste un sujet controversé. L’existence même du diagnostic d’hypersensibilité aux métaux est remise en cause alors qu’elle est admise dans d’autres spécialités comme la chirurgie cardiaque ou la gynécologie (23,24,53). Les mises au point récentes et les revues de la littérature recommandent de ne pas utiliser d’implants hypoallergéniques de façon systématique, même s’il existe une suspicion d’hypersensibilité avec des test épicutanés positifs et un LTT concordant (1). Pourtant, la pose d’un implant hypoallergénique préviendrait de potentielles réactions (45). Ces derniers sont en cours d’évaluation à moyen et long terme.
20
Cependant, les habitudes semblent changer. Les conclusions d’une récente enquête rapportent que 84% des chirurgiens allemands préféreraient utiliser un implant hypoallergénique pour leurs patients (3). A l’inverse, au Royaume Uni, 90 experts choisis sur leurs publications concernant les arthroplasties du genou concluaient que les tests épicutanés ne devaient pas être effectués en routine chez tous les patients opérés de PTG et que les implants habituels à base de chrome et de cobalt devaient continuer à être utilisés, quel que soit le statut allergique du patient (54).
Pourtant, les résultats des patients réopérés pour reprise de PTG ne seront jamais aussi bon que lors d’une PTG de première intention (55). Pour éviter ces reprises aux résultats moins bons, il faut donc se poser la question de l’utilisation d’implants adaptés au statut allergique du patient dès la pose de PTG de première intention.
Conclusion
La reprise de PTG par des PTGRNZ dans le cadre des hypersensibilités aux métaux est une intervention qui permet d’améliorer les scores fonctionnels des patients et répond aux problèmes de raideurs qu’ils rencontrent. Il convient cependant de diminuer les attentes des patients et de prendre en charge l’apparition des douleurs neuropathiques. Les implants revêtus de nitrure de zirconium semblent être une bonne réponse à la problématique posée. Cependant, l’étude des résultats à long terme de ces prothèses reste nécessaire.
21
Bibliographie
1. Middleton S, Toms A. Allergy in total knee arthroplasty: a review of the facts. Bone Jt J. avril 2016;98‑B(4):437‑41.
2. Faschingbauer M, Renner L, Boettner F. Allergy in Total Knee Replacement. Does It Exist?: Review Article. HSS J Musculoskelet J Hosp Spec Surg. février 2017;13(1):12‑9.
3. Lohmann CH, Hameister R, Singh G. Allergies in orthopaedic and trauma surgery. Orthop Traumatol Surg Res. février 2017;103(1, Supplement):S75‑81.
4. Sansone V, Pagani D, Melato M. The effects on bone cells of metal ions released from orthopaedic implants. A review. Clin Cases Miner Bone Metab. 2013;10(1):34‑40. 5. Ajwani SH, Charalambous CP. Availability of Total Knee Arthroplasty Implants for Metal
Hypersensitivity Patients. Knee Surg Relat Res. décembre 2016;28(4):312‑8.
6. Spicher C, Estebe J-P, Létourneau E, Packham TL, Rossier P, Annoni J-M. Critères diagnostiques du syndrome douloureux régional complexe (SDRC). Douleur Analgésie. mars 2014;27(1):62‑4. 7. Bouhassira D. Le questionnaire DN4 : le nouvel outil d’aide au diagnostic des douleurs
neuropathiques. Douleurs Eval - Diagn - Trait. octobre 2005;6(5):297‑300.
8. Reich J, Hovy L, Lindenmaier H-L, Zeller R, Schwiesau J, Thomas P, et al. Preclinical evaluation of coated knee implants for allergic patients. Orthop. mai 2010;39(5):495‑502.
9. Debette C, Parratte S, Maucort-Boulch D, Blanc G, Pauly V, Lustig S, et al. Adaptation française du nouveau score de la Knee Society dans l’arthroplastie de genou. Rev Chir Orthopédique
Traumatol. septembre 2014;100(5):387‑91.
10. Moya-Angeler J, Bas M, Cooper J, Hepinstall MS, Rodriguez J, Scuderi G. Revision Arthroplasty for the Management of Stiffness After Total Knee Replacement. Bone Jt J. mars 2017;99‑B(SUPP 5):31‑31.
11. Laucis NC, Hays RD, Bhattacharyya T. Scoring the SF-36 in Orthopaedics: A Brief Guide. J Bone Joint Surg Am. octobre 2015;97(19):1628‑34.
12. Ewald FC. The Knee Society total knee arthroplasty roentgenographic evaluation and scoring system. Clin Orthop. novembre 1989;(248):9‑12.
13. Caton J. [Method of measuring the height of the patella]. Acta Orthop Belg. 1989;55(3):385‑6. 14. Gao X, He R, Yan S, Wu L. Dermatitis associated with chromium following total knee arthroplasty.
J Arthroplasty. juin 2011;26(4):665.e13-16.
15. Eben R, Walk R, Summer B, Maier S, Thomsen M, Thomas P. [Implant allergy register--a first report]. Orthopade. juin 2009;38(6):557‑62.
16. Nam D, Li K, Riegler V, Barrack RL. Patient-Reported Metal Allergy: A Risk Factor for Poor Outcomes After Total Joint Arthroplasty? J Arthroplasty. septembre 2016;31(9):1910‑5.
22 17. SFHG - Société Française de Chirurgie Hanche et Genou - * Questionnaire allergie SFHG
[Internet]. [cité 13 juin 2017]. Disponible sur :
https://www.sfhg.fr/app/download/24098353/QUESTIONNAIRE+ALLERGIE++SFHG.pdf
18. Park CN, White PB, Meftah M, Ranawat AS, Ranawat CS. Diagnostic Algorithm for Residual Pain After Total Knee Arthroplasty. Orthopedics. avril 2016;39(2):e246-252.
19. Anand A, McGlynn F, Jiranek W. Metal hypersensitivity: can it mimic infection? J Arthroplasty. août 2009;24(5):826.e25-28.
20. Lachiewicz PF, Watters TS, Jacobs JJ. Metal Hypersensitivity and Total Knee Arthroplasty. J Am Acad Orthop Surg. février 2016;24(2):106‑12.
21. Granchi D, Cenni E, Giunti A, Baldini N. Metal hypersensitivity testing in patients undergoing joint replacement. J Bone Jt Surg Br. août 2012;94‑B(8):1126‑34.
22. Pinson ML, Coop CA, Webb CN. Metal hypersensitivity in total joint arthroplasty. Ann Allergy Asthma Immunol Off Publ Am Coll Allergy Asthma Immunol. août 2014;113(2):131‑6. 23. Schalock PC, Menné T, Johansen JD, Taylor JS, Maibach HI, Lidén C, et al. Hypersensitivity
reactions to metallic implants - diagnostic algorithm and suggested patch test series for clinical use. Contact Dermatitis. janvier 2012;66(1):4‑19.
24. Teo Wendy ZW, Schalock PC. Hypersensitivity Reactions to Implanted Metal Devices: Facts and Fictions. J Investig Allergol Clin Immunol. 2016;26(5):279‑94.
25. Hallab NJ, Caicedo M, Epstein R, McAllister K, Jacobs JJ. In vitro reactivity to implant metals demonstrates a person-dependent association with both T-cell and B-cell activation. J Biomed Mater Res A. février 2010;92A(2):667‑82.
26. Hallab NJ, Caicedo M, Finnegan A, Jacobs JJ. Th1 type lymphocyte reactivity to metals in patients with total hip arthroplasty. J Orthop Surg. février 2008;3:6.
27. Valentine-Thon E, Schiwara H-W. Validity of MELISA for metal sensitivity testing. Neuro Endocrinol Lett. avril 2003;24(1‑2):57‑64.
28. Müller K, Valentine-Thon E. Hypersensitivity to titanium: clinical and laboratory evidence. Neuro Endocrinol Lett. décembre 2006;27 Suppl 1:31‑5.
29. Basko-Plluska JL, Thyssen JP, Schalock PC. Cutaneous and systemic hypersensitivity reactions to metallic implants. Dermat Contact Atopic Occup Drug. avril 2011;22(2):65‑79.
30. Kurtz S, Ong K, Lau E, Mowat F, Halpern M. Projections of primary and revision hip and knee arthroplasty in the United States from 2005 to 2030. J Bone Joint Surg Am. avril
2007;89(4):780‑5.
31. Kim SH, Gaiser S, Meehan JP. Epidemiology of Primary Hip and Knee Arthroplasties in Germany: 2004 to 2008. J Arthroplasty. décembre 2012;27(10):1777‑82.
32. Thyssen JP, Menné T. Metal allergy--a review on exposures, penetration, genetics, prevalence, and clinical implications. Chem Res Toxicol. février 2010;23(2):309‑18.
23 33. Thomsen M, Rozak M, Thomas P. [Use of allergy implants in Germany: results of a survey].
Orthopade. août 2013;42(8):597‑601.
34. Saleh KJ, Dykes DC, Tweedie RL, Mohamed K, Ravichandran A, Saleh RM, et al. Functional outcome after total knee arthroplasty revision: a meta-analysis. J Arthroplasty. décembre 2002;17(8):967‑77.
35. Kasmire KE, Rasouli MR, Mortazavi SMJ, Sharkey PF, Parvizi J. Predictors of functional outcome after revision total knee arthroplasty following aseptic failure. The Knee. janvier
2014;21(1):264‑7.
36. McLawhorn AS, Bjerke-Kroll BT, Blevins JL, Sculco PK, Lee Y, Jerabek SA. Patient-Reported Allergies Are Associated With Poorer Patient Satisfaction and Outcomes After Lower Extremity Arthroplasty: A Retrospective Cohort Study. J Arthroplasty. juillet 2015;30(7):1132‑6.
37. SFHG - Société Française de Chirurgie Hanche et Genou - * Allergies et Prothèses [Internet]. [cité 23 juin 2017]. Disponible sur :
https://www.sfhg.fr/app/download/25478834/Allergies-Prothèses-diagnostic.pdf
38. Van Kempen RWTM, Schimmel JJP, van Hellemondt GG, Vandenneucker H, Wymenga AB. Reason for revision TKA predicts clinical outcome: prospective evaluation of 150 consecutive patients with 2-years followup. Clin Orthop. juillet 2013;471(7):2296‑302.
39. Baker P, Cowling P, Kurtz S, Jameson S, Gregg P, Deehan D. Reason for revision influences early patient outcomes after aseptic knee revision. Clin Orthop. août 2012;470(8):2244‑52.
40. Münch HJ, Jacobsen SS, Olesen JT, Menné T, Søballe K, Johansen JD, et al. The association between metal allergy, total knee arthroplasty, and revision. Acta Orthop. juin
2015;86(3):378‑83.
41. Brander, V., Gondek, S., Martin, E., & Stulberg, S. D. (2007). THE JOHN INSALL AWARD: Pain and Depression Influence Outcome 5 Years after Knee Replacement Surgery. Clinical orthopaedics and related research, 464, 21-26.
42. Beyer F, Lützner C, Kirschner S, Lützner J. Midterm Results After Coated and Uncoated TKA: A Randomized Controlled Study. Orthopedics. mai 2016;39(3 Suppl):S13-17.
43. Bergschmidt P, Ellenrieder M, Bader R, Kluess D, Finze S, Schwemmer B, et al. Prospective comparative clinical study of ceramic and metallic femoral components for total knee arthroplasty over a five-year follow-up period. The Knee. octobre 2016;23(5):871‑6. 44. Thienpont E. Titanium niobium nitride knee implants are not inferior to chrome cobalt
components for primary total knee arthroplasty. Arch Orthop Trauma Surg. décembre 2015;135(12):1749‑54.
45. Innocenti M, Carulli C, Matassi F, Carossino AM, Brandi ML, Civinini R. Total knee arthroplasty in patients with hypersensitivity to metals. Int Orthop. février 2014;38(2):329‑33.
46. Hofer JK, Ezzet KA. A minimum 5-year follow-up of an oxidized zirconium femoral prosthesis used for total knee arthroplasty. The Knee. janvier 2014;21(1):168‑71.
24 47. Lützner J, Hartmann A, Dinnebier G, Spornraft-Ragaller P, Hamann C, Kirschner S. Metal
hypersensitivity and metal ion levels in patients with coated or uncoated total knee arthroplasty: a randomised controlled study. Int Orthop. octobre 2013;37(10):1925‑31.
48. Nouta KA, Verra WC, Pijls BG, Schoones JW, Nelissen RGHH. All-polyethylene tibial components are equal to metal-backed components: systematic review and meta-regression. Clin Orthop. décembre 2012;470(12):3549‑59.
49. Galetz MC, Fleischmann EW, Konrad CH, Schuetz A, Glatzel U. Abrasion resistance of oxidized zirconium in comparison with CoCrMo and titanium nitride coatings for artificial knee joints. J Biomed Mater Res B Appl Biomater. avril 2010;93(1):244‑51.
50. Jacobs JJ, Urban RM, Schajowicz F, Gavrilovic J, Galante JO. Particulate-Associated Endosteal Osteolysis in Titanium-Base Alloy Cementless Total Hip Replacement. janv 1992 [cité 24 mai 2017]; Disponible sur: http://www.astm.org/DIGITAL_LIBRARY/STP/PAGES/STP14851S.htm 51. Hallab N, Merritt K, Jacobs JJ. Metal Sensitivity in Patients with Orthopaedic Implants. J Bone Jt
Surg-Am Vol. mars 2001;83(3):428‑36.
52. Bergschmidt P, Bader R, Ganzer D, Hauzeur C, Lohmann CH, Krüger A, et al. Prospective multi-centre study on a composite ceramic femoral component in total knee arthroplasty: Five-year clinical and radiological outcomes. The Knee. 1 juin 2015;22(3):186‑91.
53. Guenther D, Thomas P, Kendoff D, Omar M, Gehrke T, Haasper C. Allergic reactions in arthroplasty: myth or serious problem? Int Orthop. février 2016;40(2):239‑44.
54. Razak A, Ebinesan AD, Charalambous CP. Metal Allergy Screening Prior to Joint Arthroplasty and Its Influence on Implant Choice: A Delphi Consensus Study Amongst Orthopaedic Arthroplasty Surgeons. Knee Surg Relat Res. décembre 2013;25(4):186‑93.
55. Greidanus NV, Peterson RC, Masri BA, Garbuz DS. Quality of Life Outcomes in Revision Versus Primary Total Knee Arthroplasty. J Arthroplasty. juin 2011;26(4):615‑20.