ARBRES
FRUITIERS
ET
VIRUS
:LE
DIAGNOSTIC MOLECULAIRE
par J.
KUMMERT
et P. LEPOIVRECentre national de Phytovirologie (Section
l)
Faculté universitaire des Sciences agronomiques de Gembloux. Unité de Ph.v-topathologie
Ministère des Classes moyennes et de I'Agriculture
Direction générale Recherche et Développement
-
Recherche contractuelle(Exrrair
d'AGRICONTACT.
no -302I
1998)INTRODUCTION
Des
directives
européennes
(directives
9ll682lCEE.
92t33lCEE
et
92l34lCEE)
et
lesrèglementsnationaux [Arrêté Royal
du
l5i05i 1995er
Règlement''fruits
07197"
de
la
Directiongénérale de
la
Qualité des matières premières-Service lvlatériel
de
Reproduction
(ùlinistèrefédéral des Classes moyennes et de l'Agriculture)l
régissent le contrôle de la qualité phytosanitaire du
matériel
de multiplication
des plantsfruitiers
etornementaux commercialisés
(matériel
de
pré-base, de base et certifié).
Cette
réglementationexige l'inscription
detout fournisseur de plants auprès du lvlinistère des Classes moyennes et de
l'Agriculture
et le respect des prescriptions del'AR
précité. Dans ce cadre. lematériel végétal
doit
subir une
procédure decontrôle de qualité permettant
au
producteur decertifier
qu'il
est conformeaux
normes définiespour
les
marchés communautaires. Par ailleurs. chaque organisation professionnelle demeure libred'imposer.
pour
lesfilières de
production dont elle est responsable. des seuils plus sévères que les norrnes légales afin de valoriser un label de qualité via les lois du marché.Quelle que soit la culture concernée, la mise en
place
de filières de multiplication
de
plantes certifiées erige :- la
disponibilité
d'un
matériel végétal
cie prébase assaini (matériel micropropagé.pieds-mères issus
de
culture
in
vitro
et/ou
dethermothérapie);
-
une conduite des parcs à bois et des pepinièrespermettant
de
satisfaire
aux
normes phytosanitaires:-
l'existence
de
techniques
de
diagnosticsensibles. rapides, faciles à mettre en ceuvre et
dont le coût est économiquement jusrifié par la
valeur du produit.
Dans
ce
contexte. les progrèsde
la
biologiemoléculaire
ont
permis
l'émergencede
nom-breuses techniquesqui
pourraient connaître très prochainement des développements conduisant à une commercialisation de tests de diagnostic desagents pathogènes des plantes.
Il
importe dès lorsque
les
utilisateurs de ces différentes techniques(pathologistes. producteurs
de
plants.
servicesofficiels.
laboratoires agréés....)
soientcorrecte-ment informés des avancées technologiques qui
s'y
rapportent.de
leurs potentialitéset de
leurs limites.Le
présent article analyse les potentialités deces
techniques moléculaires
de
détection
etd'identification des virus d'arbres fruitiers en vue de leur utilisation dans
la
pratique horticole.Il
estbasé sur les résultats obtenus dans
le
cadre d'unprosramme de recherche subsidié par
le
fulinistère fédéral des Classes moyennes et de l'Agriculture (DG6)
qui
concernaitla
mise au pointd'un
testde
diagnostic moléculaire desvirus
des
tacheschlorotiques
du
pommier
(ACLS!'),
de
la cannelure des tigesdu
pommier(ASGV) et
du bois strié du pommier (ASPV).LES EXIGENCES AUXQUELLES DOIVENT SATISFAIRE LES TESTS DE DIAGNOSTIC
D'une
manière
générale.Ie
diagnostic
del'infection
virale peut reposer sur(i)
la
détectiond'entités
infectieusesde l'agent
pathogène par inoculation de plantes indicatrices(=
testsd'inde-xage biologique),
(ii)
la
mise
en
évidence de molécule(s) synthétisée(s)par l'agent
pathogène grâce aux tests sérologiquesou
(iii)
Ia révélationde
séquences d'acides nucléiques spécifiques augénome de cet agent pathogène
(-
tests molécu-laires) (Lepoivre etal..
1994).Quelle que
soit
la
technique adoptée.
Iavalidation
d'un
test de diagnostic pour le contrôlede
la
qualité
sanitairedu
matérielde
plantationdoit
se prémunir
desdeux types d'erreurs
qui peuvent se produire à l'issue d'une telle analyse :(i)
un résultat faussementpositif
sila
plante saineest déclarée infectée
à
l'issue de l'analyseet
(ii)
un
résultat faussement né_eatifsi le
test conclut à l'absence de l'agent pathogène alors que Ia plante est contaminée.Tout
protocole d'analyse réalisépar
un
laboratoire agréédevrait
donnerl'assu-rance
que
les
probabilités
de
ces
deux
typesd'erreurs sont confinées dans une fourchette de
valeurs explicitement connues et acceptées par le demandeur du test (le producteur) et
l'administra-tion chargée de garahtir les bonnes pratiques de la
procédure.
Une
telle
démarche
d "'assurancequalité"
de
I'analyse repose
sur
un
choix appropriédes
techniquesde
diagnostic
et
desmodalités de |'échantillonnage.
La
détectiond'un
agent pathogène exige quela
sensibilité dela
technique adoptée permette la mise en évidence des infections latentes chez lesplantes ne présentant pas de s1,mptômes. Outre ces exigences de sensibilité (qui réduisent à un niveau acceptable
les
risquesd'un
résultat faussementnégatif)
et
de
spécificité
(qui
réduisent
laprobabilité
d'un
résultat faussementpositif).
lestests de diagnostic devront également être faciles à
manipuler
afin
de les appliquer en routine sur un nombre important d'échantillons.Enfin, la
duréedu
protocole d'analysedoit
être compatible avec les exigences de la commercialisation (idéalement les tests devraient être réalisables sur bois dormantou
matériel en végétationet
donner des résultats avantla
saison suivante de greffage,le
toutà
un coût supportable par les utilisateurs).LES
LIMMES
DES TESTS BIOLOGIQUESET SEROLOGIQI.JES
conditions de réalisation
du
test. les rendent mal adaptésaux
exigences des transactions commer-ciales (trop grande lenteur de l'analyse) et au suivi régulier de l'état sanitaired'un
parc à bois(néces-sitant l'analyse
d'un
grand
nombred'échantil-lons). Par ailleurs,
le
nombreréduit
d'espècesindicatrices
le
plus
souvent utilisées
par
leslaboratoires
pratiquant ces
analyseset
la
non specificité des symptômes induits sur certaines deces plantes tests. rendent l'identification des virus imprécise.
Les tests sérolo-qiques reposent sur la réaction
entre
un
anti_gène(par
exemple
une
protéinevirale)
et
les anticorps produits parun
animal à sang chaud immunisé par injection de ces mêmesmolécules. La spécificité des réactions anticorps
-antigène
et le
marquage enzymalique
des anticorps en vue en vue de rér'éler la formation ducomplexe anticorps-antigène.
a
conduit
à
lacommercialisation
d'un
ensemble
de
tests immuno-enzymatiques (principalementles
testsELISA
sur plaque de microtitration) par plusieurs sociétés prir,ées. Dansle
cas particulier des virus d'arbres fruitiers travaillés parle
programme, cessérums sont soit commercialement inexistants (en ce
qui
concernel'ASPV) ou
leur utilisation n'estpossible
que
pendant
une courte
période
decroissance active de
la
plante (en ce qui concernel'ACLSV
et
l'ASGV) en
raison
de
la
faibleconcentration en virus des tissus ligneux alors que
le
contrôle
sanitaire
du
matériel
devrait
être possible toute l'année(y
compris surdu
matérielligneux dormant faisant
l'objet
d'une commercia-lisation). Les tests sérologiques peuvent également être rendus peu fiables par la grande variabilité dessouches
virales
(comme
c'est
le
cas
pourl'ACLSV)
qui
augmente les risquesde
résultats faussement négatifs.LES TECHNIQUES
MOLECULAIRES
: LEURS POTENTIALITES ET LEURSLIMITES
Chez
les ligneux fruitiers
et
ornementaux.l'indexage biologique
par
greffe
sur
plantes Le
principe
de
l'hybridation
moléculaire ligneuses demeure.à
ce
jour.
le
systèmede
repose sur la capacité que possèdent deux chaînes référenceutilisé pour
la
miseen
évidenced'un
d'acides nucléiques complémentaires, placées dansgrand nombre d'infections virales (Nemeth.
des conditions adéquates de salinité et de pH, de se1986).
La
duréede
ces protocolesde
détection
dissocier lorsqu'elles
sont
portées
à
une(parfois plus
de
2
ans).
leur coût (incluant
température élevée (prochede
100"C),et
de
sel'amortissement des serres
ou d'un
vergeret
la
réassocier
lorsqu'elles
sont
soumises
à
un main-d'æuvre nécessaireà
l'entretien desplantes
refroidissement lent.pendant une telle période). ainsi que la
variabilité
Dela
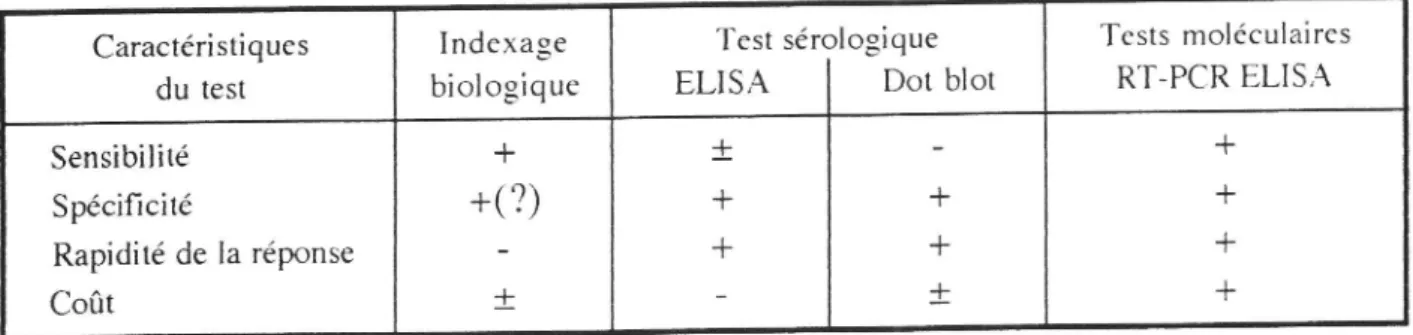
même manière, des séquences marquéesTableau
/ -
Analyse I'infectioncomparative des performances virale applicables aux arbres
des différents tests de diagnostic de
fruitiers et ornementaux Caractéristiques du test Indexage biologique Test sérologique
ELISA I
Dot btotTests moléculaires RT-PCR ELIS,{ Sensibilité Spécificité Rapidité de la réponse Coût
+
+(?)
+
+
+
+
+
+
+
+ ++
+l'agent
pathogène(=
séquences sondes) sont capables, sous certaines conditions. de s'h1'brider specifiquement aux séquences conlplémentaires (= séquences cibles)qui
sont présentes dans l'extraitd'une
plante infectée. en formant des molécules bicaténaires stables marquées, permettant.de
lasorte,
de
conclure
à la
présencede
l'agentpathogène.
LES TESTS
D'HYBRIDATION
MOLECULAIRE
PAR"DOT
BLOT''
La
technique d'hybridation moléculaire réali-sée sur membranes de nitrocellulose ou de nylon.sur lesquelles
a
été préalablement déposé et fixél'échantillon
à
tester (techniquedu "dot
blot"). constitueune
techniquede
diagnosticfacile
etrapide
pour
la
détection
de
différents
typesd'agents pathogènes. Des sondes dites "froides"
(car ne
comportant pas
d'éléments radioactifspour
leur
marquage)ont été développées depuisune
dizaine d'années (Kummertet
al..
1995b).Bien
que
leur
utilisation
entraîneune
moindresensibilité des
testsd'hybridation
moléculaire.l'intérêt
de
telles sondes réside dansle
fait
queleur synthèse et leur utilisation ne nécessitent pas
d'infrastructures spécialement équipées et agréées
pour
la
manipulationet
le
stockage des produits radioactifs.La
détection de ces chambres froidesfait
appelà
des systèmes enzymatiques simples(peroxydase
ou
phosphatase
alcaline),
qui transfornrentun
substrat incolore et soluble en unprécipité coloré
ou
luminescent. permettant ainsi sa visualisation rapide. Quand la concentration envirus
de
l'échantillon
à
anall'ser
est
éler'ée'l'hybridation par
"dot blot"
présente l'avantagede
pouvoir être
réaliséeà
partir
d'extraits
peupurifiés
de
plante
et
de
permettre
l'analysed'échantillons multiples
sur un
même support.Dans les cas des virus d'arbres fruitiers étudiés. de
telles
réactions
d'hybridation par
"dot
blot"
permettent
d'identifier
aisément les agents virauxétudiés
ASGV. ASPV
et
ACLSV)
dans
despréparations virales purifiées ou dans des ertraits préparés à partir de plantes tests (plarites herbacées
cultir'ées en terre
et
multipliant abondanrment lesvirus
étudiés). Par contre. cette nrênre technique apparaît insuffisamment sensible pour détecter cesvirus dans les extraits d'acides nucléiques totaux
des
plantes
ligneusesdont les
concentrations virales sont faibles. L'utilisation des testsd'hybri-dation
par
"dot blot"
pour la
certification
desplants
fruitiers se trouve donc limitée par
lenombre
de
molécules
cibles
présentes dansl'échantillon à caractériser'
LA
REACTION
DE POLYMERISATIONEN CHAINE
(PCR")
Læ recours à l'amplification moléculaire. r'ia la
réaction
de
polymérisationen
chaînede
l'ADN
(PCR) permet de multiplier un très grand nombre de
fois
les séquences cibles de l'agent pathogènereculant
ainsi
les
limites
de
sensibilité
des techniques de diagnostic basées sur l'hybridationmoléculaire.
Au
niveau de la recherche.la
PCR aégalement
grandementfacilité les
opérationsd'obtention
et
de clonage des sondes (utilisablespour
les
analysespar
dot
blot),
lorsque
les séquences nucléotidiques de l'agent pathogène encause
sont
connues
mais que l'obtention
depréparations purifiées de cet agent pose problème (r'irus instable tel que l'ASPV).
Dans
les
conditions
d'un
laboratoire
de recherche.l'extrait
végétal utilisé pour réaliser lcsréactions de RT-PCR consiste en des préparations purifiées
d'ARNs
totaux. Leur obtention requiertdes protocoles
d'extraction
relativement
col-tl-plexes
faisant appel
à
des produits
toxiques (phénol. chloroforme...')'
Cette préparation. troplourde dans
la
perspectived'un
test routinier. estpourtant habituellement requise pour les
virus
à génomed'ARN,
pour lesquels la réaction PCR ne peut être réalisée qu'après une rétro-transcriptionsous
forme
d'ADNc
des
ARN
viraur
(d'oùl'appellation
RT-PCR). Ces deux étapesdu
testRT-PCR peuvent être inhibees par Ia présence de
contaminants
en
concentrationtrop
éler'ée dans des préparations insuffisamment purifiées.D'autre part.
la
sensibilité etla
specificité dutest
dépendent des performancesde
l'ensemble des étapes d'amplification PCR et de détection des produits amplifiés par PCR. La révélation classiquedes
produits d'amplification PCR
par
leurfluorescence sous Uv- après électrophorèse sur gel
d'agarose coloré
aû
bromure d'éthidium est unetechnique relativement peu sensible (générant des risques significatifs de faux négatifs pour les virus des arbres fruitiers dont la concentration est faible
en
dehors des périodes de croissance active desarbres).
De
plus,
une caractérisationde
ces produitsd'amplification basée sur leur seule taille n'exclut pas les risques de
faux
positifssi
desamplifica-tions non
spécifiques
ou
des
contaminations accidentellesont
généré des produits d'amplifica-tion de taille identique à celle qui est attendue. Ladétection
des
produits d'amplification
par Southernblot
après électrophorèse (détection desproduits d'amplification
par
hybridation
à
unesonde après
leur
transfert
sur
membrane)rencontre
ces
exigencesde
sensibilité
et
despécificité mais s'avère inapte au traitement d'un
grand nombre d'échantillons.
Avec les techniques optimales d'extraction des
ARN
totaux.la
RT-PCR suivie d'une rér'élationdes produits d'amplification
par
le
bromured'éthidium permet néanmoins de détecter les trois
virus
concernéstoute
l'annéeà
partir de
tissusligneux (Kummert et
al..
1998).Dans
une
perspectived'utilisation
routinièrede
la
PCR. des problènres subsistent cependantétant donné
(i)
la
lourdeur des
protocoles depréparation des échantillons.
(ii)
les
risques decontaminations accidentelles des échantillons et
(iii)
la
sensibilité etla
spécificité insuffisantes del'étape de détection des produits d'amplification.
La simplification des protocoles de RT-PCR et
l'augmentation de
leur
sensibilité permetd'envi-sager
une
utilisation routinière des tests
dedétection moléculaire.
La
réduction
des risques decontamination
liés aux manipulationsDes kits récents nous ont permis de
râliser
lesdeux réactions de
la
RT-PCR (transcription del'
ARN et
amplification de
séquencesd'ADN)
demanière séquencielle
dans
un
même
tube, réduisant de cefait
les manipulations et les risquesde contamination des échantillons
(Mallet et
al., 1995).La simplification
des protocoles de préparationdes échantillons
Là
littérature
commence
à
proposer
desalternatives
à
l'extraction
classiquedes
acides nucléiquestotaux
en
vue
de
l'amplification
de séquences virales par PCR.Une approche très prometteuse en termes de
simplification de
la
préparation des échantillons àanalyser repose sur la capture des particules virales
sur plaque
de
microtitration
par
des anticorpsappropriés (immunocapture),
suivie
de
PCR (Wetzel etal.,
1992). Cette techniqued'immuno-capture-PCR (IC-PCR)
a
été utilisée avec succèspour
I'ACLSV
(Kummert etal..
1995a). Lorsque l'absencede
sérum commercialement disponible ne permet pas d'envisagerle
recours à l'IC-PCR, un protocole de préparation des acides nucléiquespar adsorption/désorption
sur silice a été
utiliséavec
succèsavec
I'ASVP
et
s'avère adapté àI 'automatisation.
Enfin les caractéristiques des amorces PCR qui
ont
été
conçues
pour l'ASGV
pernlettent
la réalisation des différentes étapes du processus dansun seul
et
même tubeà
partir d'extraits bruts detissus ligneux.
Ce
système s'est montré fonctionnelpour
la détection de ce virus tout au long de l'année dansdes tissus (feuilles et tiges) de pommiers infectés.
La plus grande specificité et sensibilité de l'étape de détection des produits d'amplification
Différents protocoles
ont
été
récemment proposés dansla
littérature
pour
augmenter lasensibilité
de
l'étape
de
détection des produitsd'amplification. Nous travaillons actuellement au
développement
d'un
protocole
PCR-ELISAperformant. Ce test est basé sur la détection. dans
une plaque
multipuits,
des produitsd'amplifica-tion
PCR par une hybridation sandwich [capturedes produits
d'amplification par
une
premièresonde
(dite
"de
capture")
liée
à
la
plaque demicrotitration
et
révélation colorimétrique de cesderniers
à
I'aide d'une
2ènesonde
(dite
"derévélation")l
(Lassneret
al..
1995; Lageet
al.. 1996).Cette technique de révélation sensible
(le
seuil de détection pourI'ASGV
a été estimé à4
pg devirus)
permet
d'allier
la
puissancede
I 'étaped'amplification. cette technique, qui est également
en
cours
de
développementpour
l'ACLSV
etl'ASPV,
pennet dès à présent de détecter en moinsde
24
heuresla
présencede I'ASGV
à
partir d'extraits bruts de tissus ligneux prélevés tout auIong de I'année (Daniels et
al..
1998), rencontrant ainsi les exigences de sensibilité, de spécificité et de convivialité auxquels doivent satisfaire les testsde diagnostic.
CONCLUSION
Le
potentiel d'application
des
tests
de diagnostic doit être évalué en termes de sensibilité.de
spécificité
et de coût. en
relation avec
lesparticularités de chaque problème à résoudre.
La
simplicité
et
la
rapiditéd'emploi
consti-tuent également des critères appréciables dans le
choix des méthodes à mettre en æuvre. Si les kits de diagnostic sérologique des agents phytopatho-gènes connaissent depuis
de
nombreuses annéesune
commercialisation importantepar
plusieurssociétés
privées
étrangères.les
kits
basés surl'hybridation
moléculaire
ont
connu
peu
dedéveloppement
commercial dans
le
secteur agronomique. alors que cette même technologieconnaît dès
à
présent des applications pratiques dans les domaines médical et vétérinaire.La
diffusion de
ces techniques moléculairesdemande
que
l'on
s'attacheà
développer desprotocoles
qui
allient
simplicité,
robustesse,rapidité, sensibilité
et
spécificitéafin
de stimulerl'installation
de
Iaboratoires agrééspour
leurutilisation,
de
donner une impulsion
à
leurcommercialisation sous
forme
de
kits et
depouvoir ainsi répondre aux besoins exprimés par
la profession.
Les
progrès réalisés dansle
cadrede
notreprogramme
avec
les
techniques
moléculairesbasées sur la PCR. tant au niveau de la préparation des échantillons (extraction avec silice, immuno-capture
ou
utilisation d'extraits bruts dilués selonles
virus) qu'au
niveaude
la
révélation(PCR-ELISA).
rendent réalistes
les
perspcctit'csd'automatisation
de
ces
techniques
et
leurutilisation en routine pour
l'analysed'un
grarrdnombre
d'échantillons. Ces
protocoles doivent encoreêtre
optimisés(meillcure
définition
dessondes de capture et de révélation. marquage de la sonde de révélation,
...).
Par ailleurs. le coût desappareils spécifiquenrent associés à ces techniqucs moléculaires (cycleur) diminue et
Ia
PCR-ELISAutilise
un équipenrent (lectcurELISA)
largemerrt répandu dans les laboratoires d'analyse utilisant les tests sérologiques. Ces considérations ouvrentdes
perspectives réalistesd'un
coût
d'analyse acceptablepour les
utilisateurs.Le tttbleuu I
compare
les
performances
potentiellcs
desdifférents tests
pour
les
virus
concernéspar
le programme.Néanmoins, le marché des trousses de
diagnos-tic
moléculaire des agents phytopathogèncs devrait concerneren priorité
les productions agricoles àhaute
valeur
ajoutée (plantes
ornementales ct fruitièresà
multiplication végétative. semences debase. cultures alimentaires présentant
un
intérêt commercial important comme la pomnre de tcrre.le
bananier, etc).Il
conviendra cependant dedé-finir
les protocoles d'échantillonnagc satisfaisant aux standards de qualité tout en étant adaptés aux caraéctéristiques particulièrcs de ces kits(sensibili-té, ...)
et aux
spécificités des agents pathogènes ciblés (distribution dans l'arbre. tissu à prélever,.).BIBLIOGRAPHIE
-
DanielsJ..
Marinho
V.L.A..
KummertJ.
etLepoivre
P.
1998. Developmentof
colorimc-tric RT-TCR tests
for
ASGV detection in apple trees. Acta Horticult.(in
press;.-
Kummert
J., Marinho
V.L.A..
Rufflard
G.,Colinet
D.
&
Lepoivre
P.
I998.
Sensitivedetection
of
apple
stem grooving and apple stempitting
virusesfrom
infected apple treesby RT-PCR. Acta Horticult. (in press).
-
Kummert
J.,
Rufflard
G..
Colinet
D.
&
Lepoivre
P.
1995a. Detection
of
applechlorotic
Ieaf
spot
virus
and apple
stemgrooving
virus
by
RT-PCR and IC-RT-PCR.\{ed.
Fac. Landbouww.
Uni.
Gent60
(2a). 277-287.-
Kummert J.. ColinetD.
&
LepoivreP'
1995b.Detection
of
plant
viruses
by
molecular h1'bridizationusing
non-radioactive probes.Bulletin OEPP 25. 301-313. LE FRUIT BELGE n'473
-
1998Lage
4.P..
Fauconnier
A.,
Burette 4.,
Glupczynski
Y.,
Bollen
A.
&
Godfroid
E. 1996. Rapid colorimetric hybridization assayfor
detecting amplifiedHelicobacter pylori
DNA
in
gastricbiopsy
specemens.J.
Clin. Microbiol.34
:
530-533.Lassner
D.
1995. Quantitationof
mRNA
by theELISA
technique using external standards. Pagesll7-123
in
Quantitationof
mRNA
by polymerasechain
reaction:
non
radioactive PCR methods. Kohler Th., l-assner D., Rost A.-K., Thamm8.,
Pustowoit B.&
Remke H.. edsSpringer Germany.
Lepoivre P.. Kummert J.. Colinet D.. Duterme
O.
&
AnceauC.
1994. Techniquesmolécu-laires
de
déteetion
et
d'identification
desagents pathogènes. Cahiers agricultures
3
:2t7-225.
Mallet F., Oriol G., Mary C.,
Verrier
B.
&
Mandrand
B.
1995. Continuous RT-PCR usingAMV-RT
and TaqDNA
poll'merase:
charac-terization
and
comparison
to
uncoupled procedures.Bio
Techniquesl8
:678487.
Nemeth
M.
1986.Virus.
mycoplasma, andRickettsia
Diseasesof
Fruit
Trees. KluwerAcademic Press. Hingham, MA.
Wetzel
T.,
CandresseT..
Macquaire
G., RavelonandroM.
&
DunezI.
1992.A
highlysensitive
immunocapture polymerase chainreaction method
for
plum
pox
potvirusdetection. J.
Virol.
Methods 39 :2-l-37.ARB ORI
CIIL TURE FRIII
TI
ERE
Un
nouveau
traité
d'arboriculture
fruitièrevient de paraître en Suisse. Réalisé par une équipe de spécialistes æuvrant au sein de
la
Commission intercantonale romandeet
tessinoise d'arboricul-ture, cet ouvrage de272
pages associeun
texte résolument actuel à une abondante illustration par photos, graphiques et schémas.Après une
présentation
de
I'arboriculture
suisse, on envisage successivement :-
le milieu : sol, climat,-
la botanique et la physiologie des arbres,-
la multiplication,-
la conduite et les formes.-
la création d'un verger.-
son entretien : fertilisation-
sol-
protection phytosanitaire-
régulation de la croissance etde la charge en fruits, lutte antigel, irrigation,
-
la récolte et la conservation des fruits.-
les espèces à pepins et à noyau,-
l'économie et la gestion.Ce
livre
est destiné principalement aux profes-sionnelset
aux jeunes arboriculteursqui
suivent uneformation specialisée, mais également à tous lesamateurs éclairés ou passionnés d'arboriculture. Références :
Arboriculture fruitière. .1' édition: 272 pages
ISBN
3-906679-58-6Vente au prix de 65 F.S. + frais de port. Centrale des moyens d'enseignement agricole,
L?inggasse 79.
CH-3052 ZOLLIKOFEN (Suisse) A.S.
Conservation
et
Utilisation
des
Ressources Phytogénétiques
La
conservation des ressources génétiques. etnotamment
des
plantes,
est
un
sujet
qui
a progressivement attiré l'attention publique, et aussicelle des autorités, au cours des dernières années.
Sauf
pour
certains scientifiques.la
conservationgénétique
est
un
sujet neuf,
qui
méritait
uneclarification quant aux motifs
qui
l'animent, aux buts qu'elle poursuit et àl'utilité
qu'elle présente.Cette
clarification est aujourd'hui
chose faite,grâce aux exposés de ce colloque
qui
a eulieu
à Gembloux le 261311997.Ces exposés sont organisés en deux volets. Le premier volet, concerne I'organisation des activités
en matière
de
ressources phytogénétiquessur
le plan mondial, surle
plan del'Union
Européenne, et sur le plan national (exemple de la France).Le
deuxièmevolet
comprend deux exposés à proposde
travaux effectuésen
Belgique sur lesressources génétiques
de
cultures d'origine
tropicale, suivi de trois exposés qui concernent des travaux menés également dans notre pays sur les
ressources génétiques d'espèces végétales des
régions tempérées, notamment les arbres fruitiers
et leur résistance aux maladies (13 p.).
L'ouvrage compte 76 pages et est édité par le Centre de Recherches agronomiques de Gembloux
22, avenue de la Faculté, 5030 Gembloux
Té1.: 081/61 19
55
-
Fax : 081i61494l
L'ouvrage est disponible au prix de 200 BEF à verser au compte 000-1692586-33
de la Personnalité juridique du CRA, D8