HAL Id: dumas-01910356
https://dumas.ccsd.cnrs.fr/dumas-01910356
Submitted on 31 Oct 2018HAL is a multi-disciplinary open access
archive for the deposit and dissemination of sci-entific research documents, whether they are pub-lished or not. The documents may come from teaching and research institutions in France or abroad, or from public or private research centers.
L’archive ouverte pluridisciplinaire HAL, est destinée au dépôt et à la diffusion de documents scientifiques de niveau recherche, publiés ou non, émanant des établissements d’enseignement et de recherche français ou étrangers, des laboratoires publics ou privés.
Évaluation de la qualité de vie chez les femmes traitées
pour endométriose profonde : stratégie médicale versus
stratégie chirurgicale
Aïda Gana
To cite this version:
Aïda Gana. Évaluation de la qualité de vie chez les femmes traitées pour endométriose profonde : stratégie médicale versus stratégie chirurgicale. Médecine humaine et pathologie. 2018. �dumas-01910356�
Université de Bordeaux
U.F.R DES SCIENCES MEDICALES
Année 2018 Thèse n°139
Thèse pour l’obtention du
DIPLÔME D’ÉTAT DE DOCTEUR EN MÉDECINE Discipline: Médecine Générale
Présentée et soutenue publiquement par
Aïda GANA
Née le 29/06/1987 à Alger Le 2 octobre 2018
ÉVALUATION DE LA QUALITÉ DE VIE CHEZ LES FEMMES
TRAITÉES POUR ENDOMÉTRIOSE PROFONDE
Stratégie médicale versus stratégie chirurgicale
Directeur de thèse
Professeur Jean-Luc BRUN
Jury
Monsieur le Professeur Claude HOCKE Président
Monsieur le Professeur Dominique DALLAY Juge Monsieur le Maître de Conférence Yves MONTARIOL Juge
Madame le Docteur Edwige JACQUET Juge Monsieur le Docteur Benjamin MERLOT Rapporteur et Juge Monsieur le Professeur Jean-Luc BRUN Directeur et Juge
REMERCIEMENTS
À Monsieur le Professeur Claude HOCKE, président du jury
Professeur des Universités, Praticien Hospitalier
Chef de service de Chirurgie Gynécologique et de Médecine de la Reproduction au Centre Hospitalier Universitaire de Bordeaux.
Vous me faites l’honneur de présider ce jury de thèse. Je vous remercie pour l’attention que vous avez portée à mon travail et pour votre disponibilité. Veuillez trouver ici l’expression de mon plus grand respect.
À Monsieur le Professeur Dominique DALLAY, membre du jury
Professeur des Universités, Praticien Hospitalier
Département de Gynécologie-Obstétrique – CHU de Bordeaux
C’est un honneur pour moi de vous avoir dans mon jury. Je vous remercie pour votre disponibilité et pour l’intérêt que vous portez à mon travail. À vous mon immense gratitude.
À Monsieur le Maître de Conférence Yves MONTARIOL, membre du jury
Médecin spécialiste en Médecine Générale
Maître de conférence associé au Département de Médecine Générale de l’Université de Bordeaux
Vous m’avez fait l’honneur d’accepter de juger ce travail. Merci pour votre implication et votre engagement pédagogique en tant qu’enseignant du Département de Médecine Générale. Soyez assuré de ma profonde reconnaissance.
À Madame le Docteur Edwige JACQUET, membre du jury
Médecin Spécialiste en médecine générale
Je suis honorée que vous ayez accepté de juger ce travail. Votre avis en tant que médecin généraliste pratiquant la gynécologie en ambulatoire m’est précieux. Veuillez trouver ici l’expression de mes sincères remerciements pour votre disponibilité et votre implication.
À Monsieur le Docteur Benjamin MERLOT, rapporteur de thèse
Chirurgien gynécologue – Bordeaux
Tu me fais l’honneur de juger et rapporter ce travail. Je te remercie pour tes conseils avisés et ton soutien. Je tiens à t’exprimer ici toute ma reconnaissance.
À Monsieur le Professeur Jean-Luc BRUN, directeur de thèse
Professeur des Universités, Praticien Hospitalier
Département de Gynécologie-Obstétrique – CHU de Bordeaux
Ce fut un honneur d’effectuer ce travail sous votre direction. Je vous remercie de m’avoir fait confiance et de m’avoir accompagnée tout au long de ce travail que j’espère à la hauteur de vos attentes. Je tiens à vous exprimer ici tout mon respect et ma plus sincère reconnaissance.
À ma famille :
À mes modèles, mes parents, qui m’ont toujours encouragée. Votre soutien indéfectible et votre présence ont été salutaires. Vous m’avez enseigné l’importance de toujours se donner les moyens et d’aller au bout des choses. Merci pour votre générosité et votre patience. J’espère vous avoir rendus fiers.
À mes frèros, Zac et Sam, sur lesquels je sais que je pourrai toujours compter, quoiqu’il arrive. J’ai hâte de voir ce que l’avenir a en réserve pour nous trois. Et comme dirait quelqu’un de très connu : « …Autant en emporte le vent… ».
À mes amis d’enfance :
Pauline et Ghislain que je connais depuis l’époque des appareils dentaires. Vous êtes toujours présents plus de 15 ans après, et j’espère que vous le serez pour au moins 50 ans de plus.
À mes plus anciens amis de la fac, les membres de la Jacky Team avec lesquels j’ai grandi :
Clémo, membre officiel du club des bouclettes, amie attentive et compréhensive. Audro, ma partenaire de voyage, il nous reste encore tellement de pays à explorer ma doudou. Véro et son sens de l’humour inégalé. Ben, mon vieil ami que j’ai rencontré à la première soirée de médecine, je te souhaite le meilleur avec Marine et les jumeaux. Martin, le boute-en-train, qui a pris la sage décision de revenir dans le Sud. Lio, heureux propriétaire du plus célèbre déhanché de la Martinique.
À Claire, je suis tellement contente d’avoir eu la chance de te découvrir après mon retour sur Bordeaux. Merci d’être cette belle personne, douce, à l’écoute, à qui il est si simple de se confier. Encore une fois félicitations à Gilles et à toi, et merci d’être là.
À Romain que j’ai redécouvert à Périgueux. Merci pour ta présence, ta précieuse amitié, tes conseils pendant la rédaction de cette thèse. Merci pour tes discours d’encouragement. Merci de m’inspirer autant.
À mes découvertes de l’internat :
La Team Bergerac : Jen, Marine et Marion. Le 1er semestre a été inoubliable grâce à vous. À Ophélie, Georgie, ma Georgia, LA rencontre du 2e semestre. A notre « duo qui donne la pêche ». Merci pour ton amitié, ta franchise, ton écoute. Tu es un petit diamant brut.
À la Team Périgueux : Gri, Anaïs, Nadia… mes belles rencontres du semestre d’été ! À Romain et Céline que j’ai retrouvés là-bas. À Alex le musicos, et à nos cessions « répètes ».
À la MIMI Team : Clairon, André-Anne et Camille, barquette d’or de la meilleur team d’internes.
À mes Doud’s : Clairon, quelle belle découverte tu as été ! Une vraie perle. Merci pour ton amitié que je chéris précieusement. Merci pour ta présence et ton soutien de tous les instants.
À Adeline, que j’ai découvert en fin d’internat, et qui partage mes pérégrinations bordelaises. À nos « cessions thèse » dans les cafés. Merci de m’avoir motivée Dr Fallot !
À Marion, mon ancienne coloc, qui m’a supportée pendant la rédaction. Bon courage pour ta thèse !
À ces nouvelles rencontres que je commence tout juste à découvrir : Pam, Sophie, Adeline,
Margaux…
À toutes leséquipes médicales et paramédicales que j’ai eu la chance de croiser pendant mon
internat, et qui ont contribué à ma formation.
À mes collègues, médecins et paramédicaux des urgences de Bergerac. Je vais enfin pouvoir
TABLE DES MATIÈRES
REMERCIEMENTS ... 2
TABLE DES MATIÈRES... 6
INDEX DES ILLUSTRATIONS ... 8
INDEX DES TABLEAUX ... 8
ABRÉVIATIONS ... 9
1 INTRODUCTION ... 10
1.1 Définition anatomique de l’endométriose profonde et prévalence... 10
1.2 Présentation clinique de l’endométriose profonde ... 11
1.3 Etat des lieux des prises en charge thérapeutiques de l’endométriose ... 11
1.4 Qualité de vie ... 13
1.5 Problématique et Objectifs de l’étude ... 13
2 MATÉRIEL ET MÉTHODES ... 14
2.1 Type d’étude ... 14
2.2 Population de l’étude ... 14
2.3 Critères d’inclusion et d’exclusion ... 14
2.4 Ethique ... 14
2.5 Protocole ... 15
2.6 Questionnaires ... 15
2.7 Critère de jugement principal ... 16
2.8 Critères de jugement secondaires ... 16
2.9 Analyse statistique ... 16
3 RÉSULTATS ... 17
3.1 Population ... 17
3.1.1 Répartition des patientes ... 17
3.1.2 Caractéristiques des patientes ... 18
3.2 Critère de jugement principal : évaluation de la qualité de vie ... 21
3.3 Critères de jugement secondaires ... 22
3.3.1 Impact des localisations digestives sur les résultats ... 22
3.3.2 Évaluation de l’effet du temps sur l’efficacité thérapeutique ... 24
3.3.3 Facteurs pronostiques ... 24
4.2 Impact de la stratégie thérapeutique en première intention ... 26
4.3 Impact des localisations digestives ... 27
4.3.1 Atteintes digestives ... 27
4.3.2 Sans atteinte digestive ... 29
4.4 Effet du temps sur l’efficacité thérapeutique ... 29
4.5 Impact de l’âge et de la parité ... 30
4.6 Forces et limites de l’étude ... 31
4.6.1 Forces ... 31 4.6.2 Limites ... 31 5 CONCLUSION ... 33 6 BIBLIOGRAPHIE ... 34 7 ANNEXES ... 38 SERMENT D’HIPPOCRATE ... 51 RÉSUMÉ ... 52
INDEX DES ILLUSTRATIONS
Figure 1 : Diagramme de flux des patientes………..17 Figure 2 : Répartition des groupes d’étude………18 Figure 3 à 6 : Résultats des scores de qualité de vie, selon la prise en charge thérapeutique………..21 Figures 7 à 10 : Résultats des scores de qualité de vie test par test pour les patientes sans atteinte digestive……….………....22 Figures 11 à 14 : Résultats des différents scores pour les patientes avec atteinte digestive ………...23
INDEX DES TABLEAUX
Tableau1: Caractéristiques générales des patientes………...18 Tableau2: Caractéristiques des patientes sans atteinte digestive………...19 Tableau 3 : Caractéristiques des patientes avec atteinte digestive………...20 Tableau 4 : Scores de qualité de vie des femmes traitées pour endométriose profonde depuis 36 mois ou moins………...24 Tableau 5 : Scores de qualité de vie des femmes traitées pour endométriose profonde depuis plus de 36 mois……….24 Tableau 6 : Scores de qualité de vie selon la parité chez les femmes ayant eu un traitement médical en première intention………..25 Tableau 7 : Scores de qualité de vie selon la parité chez les femmes traitées chirurgicalement en première intention. ………...25
ABRÉVIATIONS
AINS Anti-inflammatoires non stéroïdiens
C1 Traitement chirurgical en première intention EAN Échelle d’autoévaluation numérique
EHP-5 Endometriosis Health Profile 5 EHP-30 Endometriosis Health Profile 30 FSFI Female Sexual Function Index HAS Haute Autorité de Santé
IRM Imagerie par résonnance magnétique KESS Knowles Eccersley Scott Symptom M1 Traitement médical en première intention rAFS score Score de l’American Fertility Society révisé SF-36 Short Form 36
1 INTRODUCTION
L’endométriose se définit par la présence, en dehors de la cavité utérine, de tissu endométrial hormono-dépendant ayant les mêmes caractéristiques histologiques que l’endomètre (glandes et stroma) (1).
Il s’agit d’une pathologie bénigne qui touche les femmes jeunes en âge de procréer, avec une prévalence estimée entre 2 et 10 %, atteignant 50% chez les femmes infertiles (2).
L’endométriose est généralement divisée en trois entités : péritonéale superficielle, ovarienne et profonde. L’endométriose profonde est définie comme une lésion endométriosique pénétrant dans l’espace sous-péritonéal et/ou la paroi des organes pelviens (3).
Ces lésions sont responsables d’une symptomatologie pelvienne douloureuse souvent invalidante, dont l’intensité est corrélée de façon significative à la profondeur de pénétration des lésions (4). La symptomatologie associe à des degrés d’intensité divers des dysménorrhées, dyspareunies profondes et douleurs pelviennes chroniques, ayant des répercussions indéniables sur la qualité de vie des femmes atteintes (5,6).
Cette pathologie pose souvent des problèmes de prise en charge thérapeutique. Le médecin doit tenir compte du contexte mais aussi de l’âge de la patiente, de son désir de grossesse, de la sévérité de ses symptômes, du stade de la maladie et de son retentissement socio-professionnel.
1.1 Définition anatomique de l’endométriose profonde et prévalence
L’endométriose profonde se définit par une infiltration d’au moins 5 mm en profondeur de l’espace sous-péritonéal par du tissu endométrial, ou par l’atteinte des structures musculaires lisses environnant l’utérus (rectum, vagin, utérus, vessie, uretère, intestin grêle, etc.) (3). Cela concerne deux territoires : l’espace sous-péritonéal postérieur et l’espace sous-péritonéal antérieur.
L’endométriose profonde affecterait 20 à 35% des patientes souffrant d’endométriose. Elle concerne par ordre décroissant de fréquence les ligaments utérosacrés, le rectum, le colon, le sigmoïde, le vagin et la vessie.
L’atteinte digestive correspond à l’infiltration d’au moins la musculeuse des parois digestives, par opposition aux implants endométriosiques infiltrant uniquement la séreuse digestive et considérés comme des lésions superficielles. Présentes dans 4 à 37% des cas, ces atteintes sont le plus souvent localisées sur le recto-sigmoïde (75 à 90% des cas) et plus rarement dans la région iléo-caeco-appendiculaire (4 à 16% des cas) (7).
1.2 Présentation clinique de l’endométriose profonde
L’endométriose est une affection très polymorphe avec une symptomatologie variée. Le maitre symptôme de cette pathologie est la dysménorrhée, la dyspareunie profonde et les douleurs pelviennes chroniques, parfois associées à l’infertilité.
Le caractère cyclique des symptômes avec recrudescence cataméniale est évocateur, toutefois aucun symptôme n’est spécifique de la maladie. De même des formes asymptomatiques d’endométriose peuvent exister. Ce manque de spécificité rend le diagnostic parfois compliqué à poser, entrainant un retard diagnostic avec un délai moyen entre le début des symptômes et la prise en charge estimé à 6-7 ans (2).
Le diagnostic est habituellement porté dans trois circonstances : les algies pelviennes chroniques, l’infertilité et la découverte d’une masse annexielle.
Dans le cas de l’endométriose profonde, l’infiltration des organes de voisinage est à l’origine d’une symptomatologie spécifique : digestive (dyschésie, épreinte, ténesme, diarrhée, constipation, spasmes intestinaux)(3,4) et urinaire (dysurie, impériosité)(8).
Il existe une bonne corrélation entre le type de douleurs décrites et la localisation des nodules d’endométriose profonde. La présence de dyspareunies profondes, de douleurs à la défécation à périodicité mensuelle, de signes fonctionnels urinaires, ou de signes fonctionnels digestifs est très bien corrélée respectivement à l’atteinte des ligaments utérosacrés, de nodules de la cloison rectovaginale, de nodules vésicaux ou d’une atteinte digestive (4,9).
1.3 Etat des lieux des prises en charge thérapeutiques de l’endométriose
- Traitement médical :
D’après les dernières recommandations de la Haute Autorité de Santé (HAS) (10) les traitements hormonaux recommandés en première intention dans la prise en charge de l’endométriose douloureuse sont la contraception par oestroprogestatifs et le système intra-utérin au lévonorgestrel.
Les traitements hormonaux de deuxième intention concernent la contraception microprogestative orale au désogestrel, l’implant à l’étonogestrel, le dienogest et les agonistes
de la GnRH en association à une add-back thérapie (association d’un macroprogestatif et d’un œstrogène dans le but de réduire la baisse de densité minérale osseuse et d’améliorer la qualité de vie des patientes).
La prescription d’anti-inflammatoires non stéroïdiens (AINS) au long cours n’est quant à elle pas recommandée en raison des effets secondaires importants gastriques et rénaux.
- Traitement chirurgical :
La chirurgie de l’endométriose pelvienne réduit les douleurs à court et moyen terme (10). L’objectif est de réaliser une exérèse complète des lésions, puisque l’efficacité du traitement chirurgical dépend de la radicalité de la résection. En particulier dans l’endométriose avec atteinte colorectale, la réalisation d’une chirurgie incomplète augmente le taux de récidive des douleurs post-opératoires (11). C’est la localisation des lésions d’endométriose profonde qui
dicte la technique opératoire.
En effet dans l’endométriose colorectale, plusieurs techniques chirurgicales sont utilisées suivant la profondeur des atteintes :
• Le shaving consiste à peler la face antérieure du rectum sans ouverture de la lumière rectale.
• La résection antérieure discoïde emporte toute l’épaisseur de la paroi et peut parfois nécessiter une suture directe de la paroi en cas d’ouverture de la lumière digestive. • La résection segmentaire consiste à réséquer un segment de recto-sigmoïde et nécessite
une anastomose colorectale.
Il n’existe pas d’étude de niveau de preuve suffisamment élevé permettant de définir la supériorité d’une technique sur une autre. Mais des études rétrospectives rapportent que les techniques conservatrices permettent de meilleurs scores de constipation et de qualité de vie digestive par rapport à la résection segmentaire.
Les complications post-opératoires de ce type de chirurgie sont à prendre en compte lors du choix de la prise en charge. Le taux de complications per-opératoires d'une chirurgie d'endométriose profonde est de 2.1%, et post-opératoires de 13.9% (9.5% mineures, 4.6% majeures) (2). Parmi les complications majeures, on retrouve les fistules anastomotiques, les fistules recto-vaginales, l’occlusion intestinale, l’hémorragie digestive, la fistule urinaire et l’abcès pelvien profond. Les complications mineures concernent essentiellement la dysurie post-opératoire ou toute complication autre (10).
Il n’existe pas encore à l’heure actuelle de consensus sur la stratégie thérapeutique à privilégier. Les données de la littérature ne permettent pas la comparaison du traitement chirurgical à un traitement médical hormonal dans le traitement de l’endométriose, à fortiori digestive.
1.4 Qualité de vie
L’endométriose est une pathologie qui affecte directement le quotidien des femmes avec une altération fréquente de leur qualité de vie.
L’évaluation de la qualité de vie est multidimensionnelle, prenant en compte des paramètres physiques, psychiques et sociaux. Elle est également dynamique, variant au fil du temps. Plusieurs facteurs sont imputables à cette diminution de la qualité de vie chez ces femmes souffrant d’endométriose (12) : l’association des symptômes, leur intensité, leur chronicité, l’infertilité, les effets secondaires des thérapeutiques instaurées, l’impact sur la vie sociale, professionnelle et sexuelle etc… Il ressort que les patientes souffrant de douleurs chroniques ont une réduction considérable de la qualité de vie. (13)
Plusieurs questionnaires sont disponibles comme le Short Form-36 Item Health Survey (SF-36), le Short Form-12 (version simplifiée du SF-(SF-36), toutefois ceux-ci manquent de spécificité. Seuls l’Endometriosis Health Profile-30 (EHP-30) et sa version simplifiée l’EHP-5 sont spécifiques de l’endométriose.
L’aspect pluridimensionnel de cette pathologie justifie l’utilisation d’autres questionnaires employés par les gastro-entérologues et les sexologues afin d’explorer la fonction digestive et sexuelle (Female Sexual Function Index ou FSFI, Knowles Eccersley Scott Symptom score ou KESS).
1.5 Problématique et Objectifs de l’étude
Évaluer les répercussions de la maladie et des traitements sur la qualité de vie des femmes est primordial dans le choix de la stratégie thérapeutique. C’est dans cette optique que cette étude a été initiée.
Il n’existe pas de consensus permettant de privilégier une stratégie par rapport à l’autre. Dans le cas de l’endométriose profonde, et en particulier en cas d’atteinte digestive, la décision entre attitude médicale et chirurgicale relève souvent de l’expérience personnelle du praticien et du choix de la patiente. Si la stratégie chirurgicale était souvent rapidement plébiscitée en cas de lésion profonde, de plus en plus d’auteurs appellent à considérer les thérapies hormonales en première intention.
L’objectif principal de notre étude est de définir si la stratégie médicale en première intention est une stratégie aussi efficace que la stratégie chirurgicale en terme de qualité de vie dans l’endométriose profonde.
Les objectifs secondaires sont d’évaluer l’impact des atteintes digestives dans la réponse aux soins et de rechercher des facteurs pronostiques d’efficacité.
2 MATÉRIEL ET MÉTHODES
2.1 Type d’étude
Il s’agit d’une étude observationnelle, transversale, monocentrique, réalisée au CHU de Bordeaux (Centres de Pellegrin et de Saint-André).
2.2 Population de l’étude
Notre population comporte les patientes dont le diagnostic d’endométriose profonde était confirmé, et répondant aux critères d’inclusion et d’exclusion.
Les groupes ont été constitués comme suit :
- Le groupe « stratégie médicale » correspond à des patientes traitées médicalement en première intention. Selon l’évolution de la maladie et de la demande de soins, un traitement chirurgical était envisagé.
- Le groupe « stratégie chirurgicale » correspond à des patientes opérées en première intention. Selon le projet des patientes et leur demande, un traitement médical post-opératoire pouvait être proposé.
Cette étude évalue donc deux stratégies thérapeutiques.
2.3 Critères d’inclusion et d’exclusion
Les patientes dont le diagnostic d’endométriose profonde était confirmé à l’imagerie, et prises en charge entre 2008 et mai 2016 étaient incluses consécutivement dans l’étude.
Étaient exclues de l’étude, les patientes dont le diagnostic d’endométriose profonde n’était pas certain ou non-confirmé par l’imagerie par résonnance magnétique (IRM), les patientes dont la prise en charge s’est faite en dehors des dates d’inclusion, les patientes souffrant de maladie inflammatoire pelvienne non-endométriosique (MICI…), les patientes avec atteinte endométriale seule, les endométriomes ovariens seuls, les atteintes endométriosiques profondes non-postérieures seules.
2.4 Ethique
Une information orale a été donnée à toutes les patientes avec recueil de consentement écrit (par message ou mail) avant leur inclusion dans l’étude.
2.5 Protocole
Un questionnaire numérique a été élaboré. Il regroupait :
- Une échelle d’auto-évaluation des femmes sur leur qualité de vie globale basée sur une échelle numérique (EAN)
- Trois questionnaires validés: l’EHP-5 (14), le FSFI (15) et le questionnaire de constipation ou KESS (16).
Les patientes ont été contactées par téléphone afin de leur expliquer l’étude et de favoriser le taux de participation. Avec leur accord, le lien vers le questionnaire en ligne leur a été envoyé par mail (Annexe 1) :
https://docs.google.com/forms/d/e/1FAIpQLSfIDjzTfNJBXapERIQTNs9UAECzKym98AY7 BcAnpB2giaR5Bw/viewform
2.6 Questionnaires
Les patientes recevaient un questionnaire numérique comportant plusieurs parties (Annexe 1) : - La qualité de vie globale évaluée par l’échelle d’autoévaluation numérique (EAN) : il
s’agit d’une échelle cotée de 1 à 10 permettant aux femmes de juger leur qualité de vie de façon très générale sachant que 1 = Très insatisfaite, et 10 = Très satisfaite.
- La version française validée de l’Endometriosis Health Profile-5 ou EHP-5 (14) correspond à une adaptation courte de l’EHP-30, le seul questionnaire de qualité de vie spécifique de l’endométriose. L’EHP-5 contient 11 questions et comporte deux parties. Cinq questions abordent la douleur, le contrôle et l’impuissance, le bien-être émotionnel, le soutien social et l’image de soi. Les six autres items concernent les répercussions sur le travail, les relations avec les enfants, les rapports sexuels et les sentiments concernant la profession médicale, le traitement et l’infertilité. Les patientes doivent répondre aux questions et évaluer leur qualité de vie en se basant sur les quatre dernières semaines.
Le score était calculé en faisant la somme des réponses aux onze questions : Jamais = 0 point, Rarement = 25 points, Parfois = 50 points, Souvent = 75 points, Toujours = 100 points. Les scores peuvent donc s’étendre de 0 (meilleure qualité de vie envisageable) à 1100 (pire qualité de vie envisageable).
- Le Knowles–Eccersley–Scott Symptom Questionnaire ou score de KESS est un questionnaire de 12 items qui évalue l’importance de la constipation avec un score variant de 0 à 39, 39 correspondant à une constipation totale. On parle de constipation pour un score > 10. (16)
- Le Female Sexual Function Index (FSFI) est un score validé permettant une étude multidimensionnelle de la fonction sexuelle féminine. Il contient 19 questions qui balaient le désir, l’excitation, la lubrification, l’orgasme, la satisfaction et la douleur. Le score maximal est de 36. Plus le score est élevé, meilleure est la qualité de vie. Un seuil de 26,55 a été proposé comme valeur seuil en dessous duquel se pose le diagnostic de dysfonction sexuelle. (15)
2.7 Critère de jugement principal
Le critère de jugement principal est le résultat obtenu au questionnaire d’évaluation de qualité de vie, regroupant les quatre échelles d’évaluation, en fonction de la stratégie thérapeutique.
2.8 Critères de jugement secondaires
Les critères de jugement secondaires sont :
- L’évaluation de l’impact des atteintes digestives sur le critère de jugement principal selon les différentes stratégies thérapeutiques
- L’évaluation de l’effet du temps sur l’efficacité thérapeutique - La recherche de facteurs pronostiques dans la réponse au traitement.
2.9 Analyse statistique
Toutes les données ont été recueillies sur un tableur Excel pour l’analyse. Les données ont été exprimées en moyenne (déviation standard), ou médiane [écart interquartile] en cas de distribution non-paramétrique. La comparaison inter-groupes des variables quantitatives a été faite avec le test non-paramétrique de Mann-Whitney et le test de Student selon les effectifs. Les variables qualitatives ont été analysées par le test du χ2 ou le test de Fisher selon leur effectif. Les données ont été analysées avec le logiciel BiostaTGV. La différence entre les groupes était significative lorsque p-value < 0.05.
3 RÉSULTATS
3.1 Population
3.1.1
Répartition des patientes
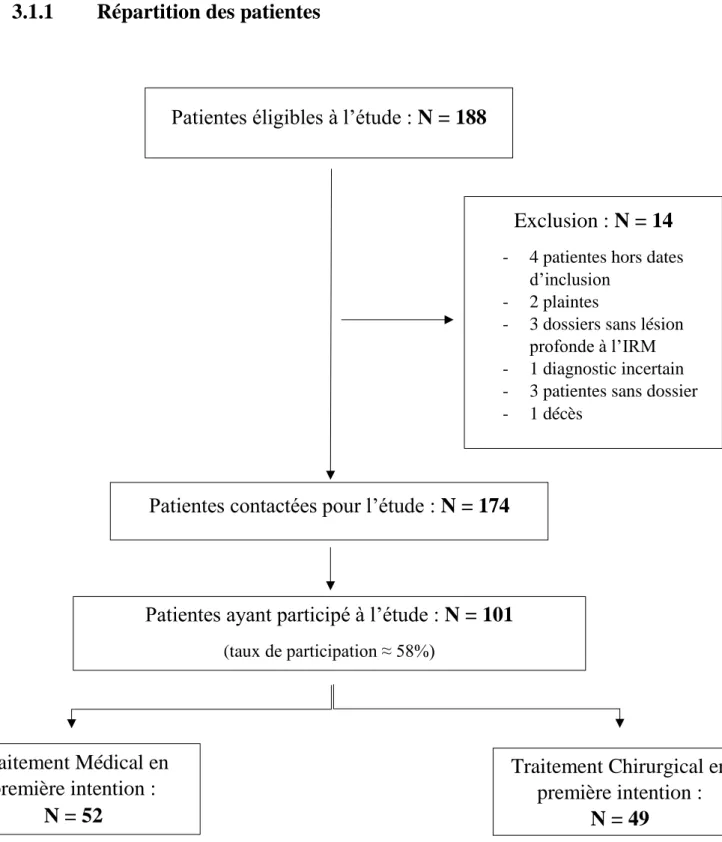
Figure 1 : Diagramme de flux des patientes
101 patientes ont été inclues dans l’étude, 52 dans le groupe traitement médical en première intention et 49 dans le groupe traitement chirurgical en première intention.
Patientes éligibles à l’étude : N = 188
Exclusion : N = 14
- 4 patientes hors datesd’inclusion - 2 plaintes
- 3 dossiers sans lésion profonde à l’IRM - 1 diagnostic incertain - 3 patientes sans dossier - 1 décès
Patientes contactées pour l’étude : N = 174
Patientes ayant participé à l’étude : N = 101
(taux de participation ≈ 58%)Traitement Médical en
première intention :
N = 52
Traitement Chirurgical en
première intention :
N = 49
Figure 2 : Répartition des groupes d’étude
La figure 2 détaille le traitement reçu par les patientes en fonction de leur groupe et de leur type d’atteinte (digestive ou non).
3.1.2
Caractéristiques des patientes
Les caractéristiques générales des patientes sont détaillées dans le Tableau 1.
Il n’y avait pas de différence concernant l’âge, la parité ou le recul sur la prise en charge. Les patientes du groupe chirurgie en première intention avaient significativement plus de lésions digestives (p<0,001).
67% des femmes ayant eu un traitement médical en première intention ont nécessité une chirurgie de seconde ligne. 30% des femmes opérées en première intention ont pris un traitement hormonal en post-opératoire.
Variable Traitement Médical en
première intention (n=52)
Traitement Chirurgical en
première intention (n=49) p
Âge (années) 38,4 ± 7,4 38 ± 6,2 0,746
Parité (n) 0,55 ± 0,7 0,6 ± 0,8 0,641
Délai entre traitement et
évaluation (mois) 38,4 ± 26,4 47,5 ± 20,6 0,056
Atteinte digestive 27 (52%) 43 (87%) <0,001
Traitement médical (n) 52 (100%) 15 (30%) <0,001
Traitement chirurgical 35 (67%) 49 (100%) <0,001
Tableau1: Caractéristiques générales des patientes.
Traitement Médical en
première intention :
N = 52
Traitement Chirurgical en
première intention :
N = 49
Atteinte digestive : N = 27 (52%) Atteinte digestive : N = 43 (88%) Pas d’atteinte digestive : N = 25 (48%) Pas d’atteinte digestive : N = 6 (12%)Traitement médical
exclusif : N = 17 (33%)
Traitement chirurgical
exclusif : N = 34 (70%)
Traitement
Médico-Chirurgical : N = 35
(67%)
(chirurgie de seconde ligne)Traitement
Médico-Chirurgical : N = 15
(30%)
(traitement médical post-opératoire)Une description plus exhaustive des patientes est réalisée dans les tableaux 2 et 3. Celles-ci sont réparties en sous-groupes selon la présence ou non d’une atteinte digestive de l’endométriose.
Tableau2: Caractéristiques des patientes sans atteinte digestive. Les valeurs sont exprimées en moyenne (±écart-type) et en nombre.
Parmi les patientes sans localisation digestive de l’endométriose, 25 ont bénéficié d’une stratégie médicale en première intention, et 6 patientes ont bénéficié d’une chirurgie de première ligne (Tableau 2).
Les caractéristiques de base des patientes étaient comparables dans les 2 groupes. La localisation des atteintes ne différait pas (p=0,322).
Seules les interventions thérapeutiques étaient significativement différentes entre les groupes, comme attendu (p=0,01 ; p=0,04).
Une complication post-opératoire de grade I a été constatée (Annexe 2). Variable
Traitement médical en première intention (n=25)
Traitement chirurgical en première
intention (n=6) p
Âge (années) 37,8 ± 7,7 36,1 ± 3,8 0,467
Parité (n) 0,6 ± 0,8 0,3 ± 0,8 0,393
Délai entre traitement et évaluation
(mois) 38,7 ± 29,6 41,5 ± 25,5 0,67
Localisations (n) 0,322
Ligament utérosacré 17 (68%) 1 (17%)
Torus 8 (32%) 3 (50%)
Cul de sac vaginal postérieur 7 (28%) 2 (33%)
Utérus 1 (4%) 1 (17%) Vessie 1 (4%) 0 (0%) Ovaire 11 (44%) 4 (66%) Traitement médical (n) 25 (100%) 3 (50%) 0,01 Traitement médical pré-opératoire 25 (100%) 0 (0%)
Traitement médical post-
opératoire 6 (24%) 3 (50%)
Type de traitement médical (n) 0,532
Pilule (Oestro) Progestative 13 (52%) 3 (50%)
Analogues de la LH-RH 6 (24%) 0 (0%)
Traitement chirurgical (n) 13 (52%) 6 (100%) 0,04
Type de traitement chirurgical (n) 0,444
Résection nodule torus/LUS 13 (52%) 5 (83%)
Annexectomie +/- Ovariectomie 4 (16%) 1 (17%) Hystérectomie concomittante 1 (4%) 1 (17%) Kystectomie ovarienne 3 (12%) 4 (66%) Complications post-opératoires (n) 1 (4%) 0 (0%) 0,7 Grade I-II 1 0 Grade III-IV 0 0
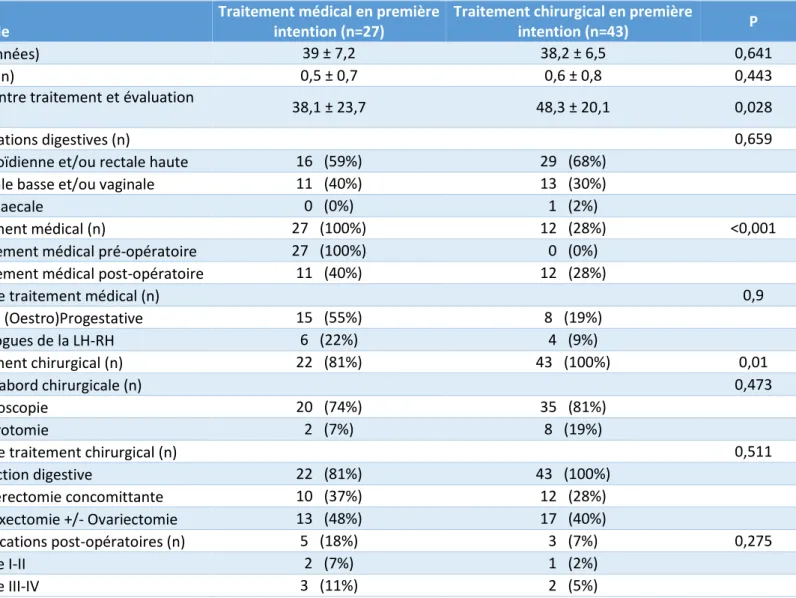
Tableau 3 : Caractéristiques des patientes avec atteinte digestive. Les valeurs sont exprimées en moyenne (±écart-type) et en nombre.
Variable
Traitement médical en première intention (n=27)
Traitement chirurgical en première
intention (n=43) P
Âge (années) 39 ± 7,2 38,2 ± 6,5 0,641
Parité (n) 0,5 ± 0,7 0,6 ± 0,8 0,443
Délai entre traitement et évaluation
(mois) 38,1 ± 23,7 48,3 ± 20,1 0,028
Localisations digestives (n) 0,659
Sigmoïdienne et/ou rectale haute 16 (59%) 29 (68%)
Rectale basse et/ou vaginale 11 (40%) 13 (30%)
Iléo-caecale 0 (0%) 1 (2%)
Traitement médical (n) 27 (100%) 12 (28%) <0,001
Traitement médical pré-opératoire 27 (100%) 0 (0%)
Traitement médical post-opératoire 11 (40%) 12 (28%)
Type de traitement médical (n) 0,9
Pilule (Oestro)Progestative 15 (55%) 8 (19%)
Analogues de la LH-RH 6 (22%) 4 (9%)
Traitement chirurgical (n) 22 (81%) 43 (100%) 0,01
Voie d'abord chirurgicale (n) 0,473
Coelioscopie 20 (74%) 35 (81%)
Laparotomie 2 (7%) 8 (19%)
Type de traitement chirurgical (n) 0,511
Résection digestive 22 (81%) 43 (100%) Hystérectomie concomittante 10 (37%) 12 (28%) Annexectomie +/- Ovariectomie 13 (48%) 17 (40%) Complications post-opératoires (n) 5 (18%) 3 (7%) 0,275 Grade I-II 2 (7%) 1 (2%) Grade III-IV 3 (11%) 2 (5%)
Parmi les patientes présentant une atteinte digestive, 27 femmes ont reçu un traitement médical en première ligne, et 43 femmes ont été opérées en première intention (Tableau 3).
Les patientes ayant bénéficié de la stratégie chirurgicale présentaient un recul plus important sur leur traitement (p=0,028).
Les localisations digestives étaient comparables entre les groupes (p=0,659).
Les prises en charge thérapeutiques, traitement médical et traitement chirurgical, étaient significativement différentes (p<0,001 et p = 0,01).
3.2 Critère de jugement principal : évaluation de la qualité de vie
Les femmes traitées chirurgicalement en première intention (C1) présentaient des scores de qualité de vie EHP-5, KESS et FSFI significativement meilleurs que les patientes ayant eu un traitement médicamenteux en première ligne (M1). On retrouvait un score d’EHP-5 médian à 525 pour le groupe M1 et 467 pour le groupe C1 (p=0,032). Le résultat médian au score de KESS était de 17 dans le groupe M1 et de 13 dans le groupe C1 (p=0,035). Le FSFI médian était à 18,2 pour le groupe M1 et à 21 pour le groupe C1 (p=0,049).
Il n’y avait pas de différence sur l’EAN avec une médiane à 6,5 pour le groupe « traitement médical en première intention » et à 7 pour le groupe « chirurgie première » (p=0,4) (Figures 3 à 6).
Figure 3 à 6 : Résultats aux scores de qualité de vie, selon la prise en charge thérapeutique. Les valeurs sont exprimées en médianes et écarts interquartiles. La ligne centrale correspond à la valeur médiane. Les barres d’erreur correspondent aux valeurs extrêmes.
3.3 Critères de jugement secondaires
3.3.1
Impact des localisations digestives sur les résultats
3.3.1.1 Patientes sans atteinte digestiveIl n’y avait pas de différence significative entre les prises en charge thérapeutiques pour les femmes n’ayant pas d’atteinte digestive. Le score médian de l’EAN était de 7 pour le groupe M1 et de 6 pour le groupe C1 (p=0,648). Le score médian de l’EHP-5 était de 475 pour le groupe M1 et de 575 pour le groupe C1 (p=0,94). Le KESS médian était de 17 pour le groupe M1 et de 13 pour le groupe C1 (p=0,452). Le score FSFI médian était de 15,6 pour le groupe M1 et 4,45 pour le groupe C1 (p=0,548) (Figures 7 à 10).
3.3.1.2 Patientes avec atteinte digestive
Les scores de qualité de vie EHP-5 et KESS étaient significativement meilleurs chez les femmes avec atteinte digestive ayant eu une chirurgie en première intention. L’EHP-5 médian était élevé à 600 pour le groupe M1 contre 425 pour le groupe C1 (p=0,02). Le score de KESS médian était de 18 pour le groupe M1, et de 13 pour le groupe C1 (p=0,038).
Il n’y avait pas de différence concernant le FSFI et l’EAN (respectivement p=0,113 et p=0,342). Le FSFI médian était à 20,1 pour le groupe M1 et 21,9 pour C1. L’EAN médian était à 6 pour le groupe M1 et 7 pour le groupe C1 (Figures 11 à 14).
Figures 11 à 14 : Résultats des différents scores pour les patientes avec atteinte digestive. Les valeurs sont exprimées en médiane et écarts interquartiles. La ligne centrale correspond à la valeur médiane.
3.3.2
Évaluation de l’effet du temps sur l’efficacité thérapeutique
3.3.2.1 Jusqu’à 36 mois de traitementOn ne constatait pas de différence significative entre les stratégies médicale et chirurgicale dans les résultats aux scores de qualité de vie des patientes traitées depuis moins de 36 mois (Tableau 4).
Tableau 4 : Scores de qualité de vie des femmes traitées pour endométriose profonde depuis 36 mois ou moins. Les valeurs sont exprimées en médianes et écarts interquartiles.
3.3.2.2 Prise en charge de plus de 36 mois
Les patientes traitées par chirurgie en première intention depuis plus de 36 mois présentaient un score EHP-5, KESS et FSFI significativement meilleur (Tableau 5). Il n’y avait pas de différence sur l’échelle d’auto-évaluation numérique entre les deux groupes.
Variable Traitement médical en première intention
(n=31)
Traitement chirurgical en première intention
(n=25) p
EAN 7 [5-8] 7 [7-8] 0,249
EHP-5 525 [437-725] 425 [175-650] 0,04
KESS 20 [13-29,5] 13 [8-16] 0,017
FSFI 15,6 [6-23,7] 22 [16,3-29,6] 0,035
Tableau 5 : Scores de qualité de vie des femmes traitées pour endométriose profonde depuis plus de 36 mois. Les valeurs sont exprimées en médianes et écarts interquartiles.
3.3.3
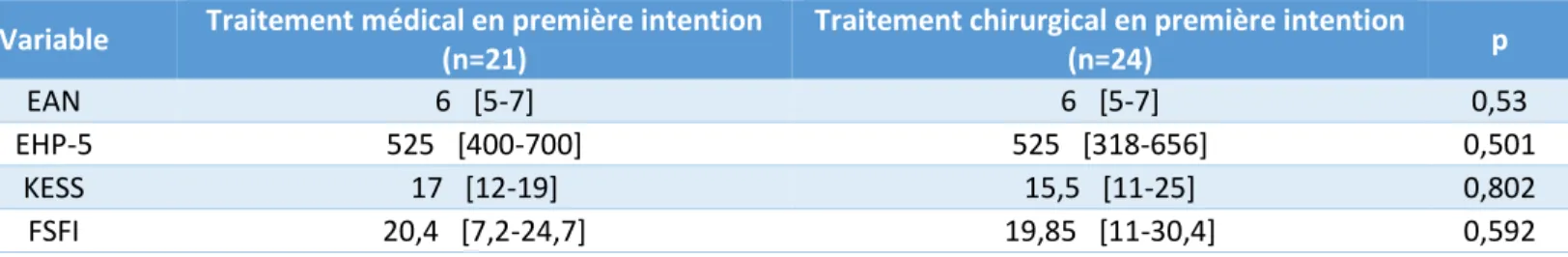
Facteurs pronostiques 3.3.3.1 L’âge3.3.3.1.1 Traitement médical en première intention
Il n’a pas été trouvé de corrélation entre l’âge des patientes et leur réponse à la prise en charge médicale. Parmi les patientes ayant été traitées médicalement en première intention, on ne
Variable Traitement médical en première intention
(n=21)
Traitement chirurgical en première intention
(n=24) p
EAN 6 [5-7] 6 [5-7] 0,53
EHP-5 525 [400-700] 525 [318-656] 0,501
KESS 17 [12-19] 15,5 [11-25] 0,802
Le score de l’EAN, l’EHP-5 ainsi que le FSFI semblaient meilleurs chez les patientes de plus de 35 ans mais de façon non-significative (p=0,134, p=0,636 et p=0,184).
Le KESS quant à lui était comparable dans les 2 groupes (p=0,63).
3.3.3.1.2 Traitement chirurgical en première intention
Les patientes de plus de 35 ans traitées chirurgicalement en première intention avaient une EAN significativement meilleure que les patientes plus jeunes (p=0,019). Toutefois on ne constatait pas de différence sur les autres scores (p=0,247, p=0,073 et p=0,792).
3.3.3.2 La parité
3.3.3.2.1 Traitement médical en première intention
38% des patientes traitées par stratégie médicale ont eu un ou plusieurs enfants. Ces patientes présentaient un score sur l’EAN et KESS meilleur que les femmes nullipares. Il n’y avait pas de différence significative sur les scores EHP-5 et FSFI (Tableau 6).
Variable Nullipare (n=32) Primi/Multipare (n=20) p
EAN 6 [5-7] 7 [5,7-8] 0,028
EHP-5 575 [475-706] 475 [393-718] 0,322
KESS 19 [13,7-29,2] 14 [5,7-22] 0,04
FSFI 19,45 [7-23,5] 16,8 [7,4-26,4] 0,534
Tableau 6 : Scores de qualité de vie selon la parité chez les femmes ayant eu un traitement médical en première intention. Les valeurs sont exprimées en médianes et écarts interquartiles.
3.3.3.2.2 Traitement chirurgical en première intention
43% des femmes ayant eu une chirurgie première sont primipares ou multipares. Elles présentaient un score sur l’EAN et d’EHP-5 significativement meilleur que les femmes nullipares (respectivement p=0,022 et p=0,04). Les scores de constipation et de fonction sexuelle ne sont pas différents (p=0,847 et p=0,678) (Tableau 7).
Variable Nullipare (n=28) Primi/Multipare (n=21) p
EAN 6,5 [4,7-7] 7 [7-8] 0,022
EHP-5 550 [400-675] 300 [175-550] 0,04
KESS 13 [7,7-19,2] 13 [9-23] 0,847
FSFI 22,55 [16,9-30,4] 20,6 [8-28,1] 0,678
Tableau 7 : Scores de qualité de vie selon la parité chez les femmes traitées chirurgicalement en première intention. Les valeurs sont exprimées en médianes et écarts interquartiles.
4 DISCUSSION
Le résultat principal de notre étude est que la stratégie chirurgicale en première intention semble être plus efficace en terme de qualité de vie chez les femmes atteintes d’endométriose profonde. Ce résultat est à pondérer par la présence ou non d’atteinte digestive de la maladie.
4.1 Qualité de vie des femmes traitées pour endométriose profonde
De façon globale, notre échantillon de patientes présente des scores de qualité de vie mitigés. Le score de l’échelle d’autoévaluation numérique semble satisfaisant avec un score médian de 7/10 [5-8]. Le score EHP-5 médian était médiocre à 500/1100 [325-675], et 46% des patientes avaient un score EHP-5 supérieur ou égal à 550.
Toutefois il est important de souligner que dans l’ensemble, et indépendamment de la stratégie thérapeutique, les résultats aux scores de KESS et FSFI restent globalement mauvais.
Le KESS médian total était de 15/39 [9-24], 73% des femmes présentent toujours après traitement un problème de constipation. Enfin le score FSFI était également médiocre, avec un résultat médian à 20,4/36 [7,6-26,1]. Seules 24% des femmes traitées ne présentent pas de dysfonction sexuelle.
Ces résultats sont corroborés par les données de la littérature. Si les traitements permettent une amélioration de la symptomatologie, les résultats sont modérés (17–19). Cela est particulièrement constaté dans l’exploration de la fonction sexuelle (20,21).
Ces données nous permettent d’une part d’appréhender l’importance des répercussions de la maladie sur le quotidien de ces femmes mais aussi d’entrevoir l’impuissance des soignants à les soulager totalement, laissant entrevoir une marge de manœuvre dans l’optimisation de la prise en charge et notamment le choix de la stratégie thérapeutique.
4.2 Impact de la stratégie thérapeutique en première intention
Dans notre étude, le choix d’une stratégie chirurgicale semblait donner de meilleures performances en terme de qualité de vie.
Ces résultats vont à l’encontre de la tendance actuelle qui est de privilégier les thérapies médicamenteuses en première intention dans l’endométriose profonde. Plusieurs études réalisées ces dernières années mettent en évidence l’efficacité des traitements médicamenteux dans l’amélioration de la symptomatologie endométriosique dans les endométrioses profondes (22–26).
Dans la revue de la littérature effectuée fin 2015 par Ferrero et al (27), les auteurs avancent que l’hormonothérapie devrait être proposée en première intention dans la gestion de la douleur des patientes atteintes d’endométriose profonde, et suggèrent de recourir à la chirurgie en seconde ligne (si persistance de la douleur malgré hormonothérapie, sténose intestinale ou urétrale,
contre-indication à la prise médicamenteuse, refus de la patiente ou désir de grossesse). Ils précisent néanmoins que la chirurgie s’avère très efficace pour soulager la douleur dans l’atteinte profonde.
Plusieurs travaux ont en effet démontré que la chirurgie dans l'endométriose améliorait non seulement les symptômes douloureux mais également la qualité de vie et la fonction sexuelle (28–30). Le choix de l’approche thérapeutique la plus appropriée dans le traitement de l’endométriose profonde fait encore débat, et à ce jour les données de la littérature ne permettent pas de trancher la question (10).
A notre connaissance, seules 3 études du même auteur comparent la stratégie médicale à l’approche chirurgicale dans la prise en charge de l’endométriose profonde (17–19). Deux de ces travaux (17,18) ont été réalisés chez des femmes atteintes d’endométriose stade III ou IV (Classification rAFS) ayant toutes déjà bénéficié d’une chirurgie, et s’intéressaient donc à comparer la meilleure stratégie dans le traitement de seconde ligne. La 3e étude concerne exclusivement l’endométriose colorectale (19).
En 2012 et 2013, Vercellini (17,18) a décrit les effets d'une chirurgie conservatrice par laparotomie versus un traitement médical par progestatifs faiblement dosés sur la dyspareunie mais également la qualité de vie sexuelle, le bien-être psychologique et la qualité de vie générale. Cette étude ne montre pas de différence significative à 12 mois chez le sous-groupe de femmes avec atteinte rectovaginale, alors que le degré de satisfaction était meilleur pour les femmes sans atteinte digestive traitées médicalement.
De la même façon, une distinction majeure est à prendre en compte dans l’interprétation de nos résultats, à savoir la présence ou non de lésions digestives associées.
4.3 Impact des localisations digestives
Notre étude met en exergue l’impact des atteintes digestives dans la réponse aux traitements. En effet, en cas d’endométriose digestive la stratégie chirurgicale parait plus efficace, alors que les résultats aux scores semblent montrer qu’en l’absence de ces atteintes il n’existe pas de différence de qualité de vie entre les patientes ayant bénéficié d’une stratégie médicale en première intention et celles ayant bénéficié de la stratégie chirurgicale.
Sachant que notre échantillon est composé à 69% de femmes présentant une atteinte digestive, il est probable que nos résultats globaux soient le reflet de cette distribution.
4.3.1
Atteintes digestives
Le traitement chirurgical est communément admis comme étant le traitement de choix pour les lésions d’endométriose profonde avec atteinte digestive (30,31), d’autant que l’essor de l’approche coelioscopique donne des résultats fonctionnels identiques à la laparotomie tout en réduisant le risque opératoire (32). Les résultats de notre étude semblent consolider cette hypothèse.
Sur l’EHP-5 et le KESS :
Dans notre étude, l’EHP-5 et le score de KESS étaient significativement meilleurs chez les patientes avec atteinte digestive ayant eu une chirurgie en première intention. Cela peut s’expliquer par le fait que les traitements médicamenteux exercent un effet sur l’endomètre et le muscle lisse du nodule endométriosique, mais pas sur la composante fibrotique à l’origine des symptômes de constipation. Pour certains auteurs cela limiterait les bénéfices d’une hormonothérapie et donc ferait de la stratégie chirurgicale la meilleure option (33–35). L’efficacité des traitements hormonaux sur l’amélioration de la symptomatologie digestive a néanmoins déjà été démontrée. Ferrero a observé que l’acétate de noréthistérone améliorait grandement la symptomatologie diarrhéique et les crampes intestinales, mais sans retrouver de bénéfice concernant la constipation, le ballonnement abdominal ni la sensation d’évacuation incomplète des selles (36). Bien que l’hormonothérapie ne guérisse pas l’endométriose, le degré de satisfaction des femmes est nettement amélioré sous traitement médicamenteux (22,36,37). Et plusieurs travaux appellent à considérer les traitements médicamenteux comme une option thérapeutique incontournable pour les femmes qui ne souhaitent pas de grossesse et sans symptomatologie sub-occlusive (17–19,38). Mais la présence non négligeable d’effets secondaires, de recrudescence douloureuse sous traitement (39)(40), et le peu d’efficacité sur la constipation peuvent expliquer la différence que nous avons retrouvée en terme de qualité de vie.
L’étude récente menée par Vercellini (19) ne concorde pas avec ces données. Elle s’attelle à comparer l’approche médicale et l’approche chirurgicale chez des femmes atteintes d’endométriose colorectale, sur une durée de 3 ans, à l’aide de plusieurs échelles dont une EAN, le score de KESS et le FSFI. Les auteurs n’ont pas retrouvé de différence entre les deux groupes. Néanmoins, ils reconnaissent que le degré de satisfaction du groupe « chirurgie » aurait pu être meilleur si toutes les procédures avaient été réalisées par laparoscopie et non laparotomie (76% des patientes). Ils concluaient en préconisant de toujours inclure le traitement médical dans les options thérapeutiques, et de réserver la chirurgie comme traitement de seconde ligne.
Sur l’EAN et le FSFI :
Dans notre étude, il ne semblait pas y avoir de différence entre les deux approches thérapeutiques concernant l’échelle d’auto-évaluation numérique et le FSFI.
Les améliorations minimes de la qualité de la vie sexuelle sous traitement ont déjà été observées (19–21). Le peu de progression de la qualité de vie sexuelle peut s’expliquer par le fait que des années d’expériences de douleurs coïtales ont un effet durable sur le bien être psychologique. L’expérience de la douleur et la perte de plaisir durant l’acte s’ancrent au fil des années. Ce processus de répétition peut créer un schéma cognitif néfaste dans lequel l’anticipation de la douleur perturbe la vie sexuelle (28). On peut également supposer que le sentiment d’échec
vis-à-vis de son partenaire et la perturbation de l’estime de soi sont autant de facteurs qui vont impacter la qualité de la vie sexuelle.
Si les résultats de notre étude suggèrent que la stratégie chirurgicale semble donner de meilleurs résultats en terme de qualité de vie dans les endométrioses digestives, il n’existe pas encore à notre connaissance d’étude comparative randomisée sur le sujet. Les données de la littérature
ne permettent pas la comparaison du traitement chirurgical à un traitement médical hormonal administré avant, après ou à la place du traitement chirurgical (10). Néanmoins, un essai randomisé et contrôlé français, comparant les traitements médical et chirurgical dans l’endométriose rectale, est actuellement en cours et devrait apporter les premiers éléments de réponse fin 2019 (NCT01973816).
4.3.2
Sans atteinte digestive
En l’absence de lésion digestive endométriosique, on ne retrouvait pas de différence entre les deux stratégies thérapeutiques. À l’exception du score de constipation, tous les autres scores semblaient meilleurs dans la stratégie médicale, mais de façon non-significative.
Dans les travaux de Vercellini, le sous-groupe de patientes exemptes d’endométriose digestive traitées médicalement présentaient des résultats aux scores de qualité de vie significativement meilleurs que celles ayant bénéficié d’une chirurgie (17,18). Les femmes opérées n’avaient pas reçu d’hormonothérapie en post-opératoire comme cela pouvait être le cas dans notre étude, ce qui peut expliquer cette différence.
Ces résultats nous laissent à penser qu’il est légitime de proposer aux femmes n’ayant pas d’atteinte digestive une stratégie médicale en première intention. En l’absence de bénéfice objectivé d’une stratégie sur une autre en terme de qualité de vie, proposer une hormonothérapie permet de ne pas exposer les patientes aux risques inhérents à une chirurgie (complications per et post-opératoires, risque anesthésique). Il est également rappelé que le niveau de technicité nécessaire pour une chirurgie d’endométriose profonde étant plus élevé, les résultats observés restent très opérateurs dépendants (41).
Cependant la suggestion d’une hormonothérapie n’a de sens qu’en l’absence de désir de procréation et de complications nécessitant une intervention chirurgicale. La décision finale incombe à la femme, après que celle-ci ait pris connaissance des risques et bénéfices de chaque option thérapeutique proposée.
4.4 Effet du temps sur l’efficacité thérapeutique
Dans notre étude, nous avons constaté que les patientes traitées depuis plus de 36 mois par stratégie chirurgicale semblaient présenter une meilleure qualité de vie que celles ayant bénéficié de l’approche médicale.
En effet, les femmes traitées médicalement depuis plus de 36 mois avaient un score de KESS et FSFI qui semblaient moins bons (mais résultat non significatif) que les femmes traitées depuis moins longtemps. A l’inverse, les patientes opérées depuis plus de 36 mois avaient un score sur l’EAN significativement meilleur que les patientes opérées plus récemment. On retrouvait la même tendance pour les autres scores mais de façon non significative.
Ces résultats ne concordent pas avec la revue de la littérature.
L’étude prospective de Vercellini de 2012 s’est intéressée à comparer l’efficacité du traitement médical et chirurgical dans la prise en charge de la dyspareunie profonde dans l’endométriose
rectovaginale (17,18). Si à 3 mois le degré de satisfaction était significativement plus élevé dans le groupe "chirurgie", cette différence s'amendait à 6 mois, si bien qu'à 1 an on ne constatait aucune différence entre les deux groupes (18). Il en allait de même pour la qualité de vie, le bien-être psychologique et la fonction sexuelle.
Une des explications avancées par les auteurs est le délai d’action nécessaire de l’hormonothérapie pour permettre une diminution progressive de l'état inflammatoire pelvien, alors que l’excision des lésions permettrait une diminution rapide et substantielle de la douleur. Toutefois, une récidive progressive des symptômes au bout de 6 mois post-chirurgie expliquerait qu’à un an l’avantage à court terme de la chirurgie ne soit plus.
Dans une étude plus récente de Vercellini (19), avec une période de suivi des patientes bien plus importante (médiane à 40 mois), les résultats semblaient similaires. Les scores de qualité de vie n’étaient pas différents entre l’approche médicale et l’approche chirurgicale.
Dans notre étude, le recul médian sur la prise en charge était de 38 mois pour le groupe « médical » et 47 mois pour le groupe « chirurgie ». On ne constatait pas de différence de satisfaction chez les patientes traitées depuis moins de 36 mois, ce qui corrobore les résultats retrouvés dans la littérature. Toutefois au-delà de 36 mois, on notait une différence significative en faveur de la stratégie chirurgicale sur les scores EHP-5, KESS et FSFI.
En considérant la nature de la maladie et son caractère chronique, ces résultats peuvent être expliqués par le taux d’échappement au traitement médical, les problèmes d’intolérance et les effets secondaires imputables à tout traitement administré au long cours.
L’excision des lésions endométriosiques ne guérit pas la maladie et ne prévient pas l’apparition de nouvelles lésions puisque la chirurgie n’intervient pas sur les mécanismes pathogènes de la maladie.
Néanmoins, les observations de notre étude montrent un avantage à moyen/long terme d’une approche chirurgicale. 30% des patientes opérées ont eu une hormonothérapie post opératoire, mais 67% traitées médicalement en première intention ont eu une chirurgie de seconde ligne (dont 42% pour les femmes avec atteinte digestive).
4.5 Impact de l’âge et de la parité
Nous avons cherché à extraire de nos données des facteurs pronostiques pertinents dans la réponse aux soins susceptibles de nous guider dans le choix de la proposition thérapeutique la plus adaptée à chaque patiente.
L’âge ne semble pas être un facteur discriminant dans la réponse aux soins. Parmi les patientes traitées médicalement, il n’y avait pas de différence sur les scores de qualité de vie entre les patientes de moins de 35 ans et celles de plus de 35 ans.
Les femmes de plus de 35 ans traitées chirurgicalement avaient un score sur l’EAN meilleur que les femmes opérées plus jeunes, sans qu’il n’y ait de différence significative sur les autres scores. On peut supposer que le résultat soit dû à un taux de récurrence moindre chez les femmes plus âgées. En 2004, Fedele fait cette corrélation entre l’âge et la récurrence douloureuse post-chirurgie dans l’endométriose rectovaginale. Plus la patiente est jeune, plus le risque de
Dans notre étude, la parité semble être un facteur protecteur. Que ce soit pour la stratégie médicale ou chirurgicale, les femmes primipares ou multipares avaient des scores de qualité de vie significativement meilleurs que les nulligestes. Nos résultats sont confortés par les données de la littérature. La nulligestité est associée à une plus grande prévalence de l'endométriose (43). L'hypothèse la plus communément acceptée est que la grossesse a un effet protecteur sur l'endométriose et ses symptômes, dû à l'anovulation et à l'aménorrhée qui empêchent le saignement du tissu endométriosique, mais aussi à différents changements métaboliques, hormonaux, immunitaires et d'angiogenèse liés à la grossesse (44).
Par ailleurs, on sait que les femmes atteintes d’endométriose sont plus sujettes à des problèmes de fertilité potentiellement source d’une détresse psychologique. On peut supposer que l’accession à la maternité chez ces femmes soit vécue comme une victoire sur la maladie, et soit corrélée à une meilleure satisfaction globale de leur qualité de vie.
4.6 Forces et limites de l’étude
4.6.1
ForcesÀ notre connaissance, il s’agit de l’une des rares études descriptives dont l’objet est de comparer la stratégie médicale à la stratégie chirurgicale, en première intention, chez des patientes atteintes d’endométriose profonde avec et sans atteinte digestive.
L’évaluation de la qualité de vie a été faite à l’aide de scores validés, ce qui renforce la validité de nos résultats.
Le taux de réponse global était de 58%, ce qui est très satisfaisant et révélateur d’un désir d’implication des patientes dans l’étude de leur pathologie.
Les délais d’inclusion larges nous ont permis d’obtenir un recul important sur l’évaluation des prises en charge thérapeutiques.
4.6.2
Limites
La principale limite de notre étude est l’absence de randomisation de nos groupes. Notre travail est avant tout un travail descriptif effectué sur un recueil rétrospectif des données avec une évaluation transversale de la qualité de vie à un instant donné. Notre étude n’est donc pas prospective. Le choix des traitements n’a pas été randomisé, mais basé sur la préférence des patientes après une information éclairée. Cette démarche présente néanmoins l’avantage de créer une meilleure adhésion aux soins. Par ailleurs, mettre en place des essais randomisés contrôlés dans le cas d’études comparant des stratégies thérapeutiques avec d’importantes différences en terme de risques et de comorbidités peut engendrer de grosses difficultés de recrutement.
Nous n’avions pas de données antérieures sur la qualité de vie des femmes avant la mise en place des traitements. Il nous était donc impossible de savoir si nos groupes étaient comparables en terme de qualité de vie avant l’instauration de leur traitement.
Notre étude ne permet pas de conclure sur l’efficacité des traitements médicaux et chirurgicaux seuls, puisqu’elle évalue des stratégies thérapeutiques (médical +/- chirurgical). Cela peut être un facteur confondant dans la détermination du rôle joué par tel ou tel traitement dans le résultat aux scores de qualité de vie. La présence d’une association médicochirurgicale dans l’historique thérapeutique de certaines patientes est probablement due au fait que l’on a un recul important sur les prises en charge. Ceci nous permet en revanche d’appréhender l’évolution naturelle de la maladie et ses conséquences sur les traitements (récurrences douloureuses, intolérance, effets secondaires nécessitant un switch thérapeutique), ce qui correspond plus à la réalité en pratique clinique.
Les patientes n’ont pas toutes reçu le même traitement hormonal, toutefois l’objet de notre étude n’était pas de comparer plusieurs traitements hormonaux, mais de déterminer l’impact de différentes stratégies, médicale ou chirurgicale.
Enfin, les femmes incluses dans notre étude sont toutes suivies au CHU de Bordeaux. On peut supposer que cela engendre un biais de sélection, avec des patientes nécessitant une prise en charge en soins tertiaires. Il s’agit d’une population hétérogène : certaines femmes consultent au CHU en première ligne et d’autres sont adressées après échec de traitements antérieurs réalisés hors CHU.
5 CONCLUSION
Dans notre étude, nous n’avons pas retrouvé de différence en terme de qualité de vie entre les stratégies thérapeutiques pour les patientes souffrant d’endométriose profonde sans localisation digestive. Il est donc licite de proposer à ces femmes un traitement médicamenteux en première intention, et de réserver la chirurgie à celles qui échappent au traitement, ne le tolèrent pas ou encore à celles qui manifestent un désir de grossesse.
En revanche, les femmes atteintes d’endométriose digestive opérées en première intention ont une meilleure qualité de vie que celles ayant bénéficié d’une stratégie médicale. Des études comparatives randomisées sont nécessaires afin de déterminer la meilleure approche thérapeutique dans le traitement de l’endométriose digestive.
L’âge n’est pas discriminant dans la réponse aux soins, alors que la parité semble être un facteur protecteur.
6 BIBLIOGRAPHIE
1. Velemir L, Krief M, Matsuzaki S, Rabischong B, Jardon K, Botchorishvili R, et al. Physiopathologie de l’endométriose. Httpwwwem-Premiumcomdocelecu-Bordeauxfrdatatraitesgy00-44636 [Internet]. 2008 Jul 23 [cited 2017 Sep 19]; Available from:
http://www.em-premium.com.docelec.u-bordeaux.fr/article/178873/resultatrecherche/1
2. Dunselman G a. J, Vermeulen N, Becker C, Calhaz-Jorge C, D’Hooghe T, Bie BD, et al. ESHRE guideline: management of women with endometriosis. Hum Reprod. 2014 Mar 1;29(3):400–12. 3. Cornillie FJ, Oosterlynck D, Lauweryns JM, Koninckx PR. Deeply infiltrating pelvic endometriosis:
histology and clinical significance. Fertil Steril. 1990 Jun;53(6):978–83.
4. Koninckx PR, Meuleman C, Demeyere S, Lesaffre E, Cornillie FJ. Suggestive evidence that pelvic endometriosis is a progressive disease, whereas deeply infiltrating endometriosis is associated with pelvic pain. Fertil Steril. 1991 Apr;55(4):759–65.
5. Vercellini P, Frontino G, Pietropaolo G, Gattei U, Daguati R, Crosignani PG. Deep endometriosis: definition, pathogenesis, and clinical management. J Am Assoc Gynecol Laparosc. 2004
May;11(2):153–61.
6. Van Aken MAW, Oosterman JM, van Rijn CM, Ferdek MA, Ruigt GSF, Peeters BWMM, et al. Pain cognition versus pain intensity in patients with endometriosis: toward personalized treatment. Fertil Steril. 2017 Sep 11;
7. Dumontier I, Roseau G. Manifestations digestives de l’endométriose. Hépato-Gastro Oncol Dig. 2002 Feb 12;9(1):45–50.
8. Berlanda N, Vercellini P, Carmignani L, Aimi G, Amicarelli F, Fedele L. Ureteral and vesical endometriosis. Two different clinical entities sharing the same pathogenesis. Obstet Gynecol Surv. 2009 Dec;64(12):830–42.
9. Chapron C, Fauconnier A, Dubuisson J-B, Barakat H, Vieira M, Bréart G. Deep infiltrating
endometriosis: relation between severity of dysmenorrhoea and extent of disease. Hum Reprod. 2003 Apr 1;18(4):760–6.
10. Haute autorité de Santé. Prise en charge de l’endométriose [Internet]. 2017 [cited 2018 Jun 13]. Available from:
https://www.has-sante.fr/portail/upload/docs/application/pdf/2018-01/prise_en_charge_de_lendometriose_-_recommandations.pdf
11. Carmona F, Martínez-Zamora A, González X, Ginés A, Buñesch L, Balasch J. Does the learning curve of conservative laparoscopic surgery in women with rectovaginal endometriosis impair the recurrence rate? Fertil Steril. 2009 Sep 1;92(3):868–75.
12. Daraï E, Coutant C, Bazot M, Dubernard G, Rouzier R, Ballester M. Intérêt des questionnaires de qualité de vie chez les patientes porteuses d’une endométriose. Gynécologie Obstétrique Fertil. 2009 Mar 1;37(3):240–5.
13. Laursen BS, Bajaj P, Olesen AS, Delmar C, Arendt-Nielsen L. Health related quality of life and quantitative pain measurement in females with chronic non-malignant pain. Eur J Pain Lond Engl. 2005 Jun;9(3):267–75.