Cancer du sein : Expérience du service de gynécologie obstétrique A à la maternité du CHU Mohammed VI Marrakech
Texte intégral
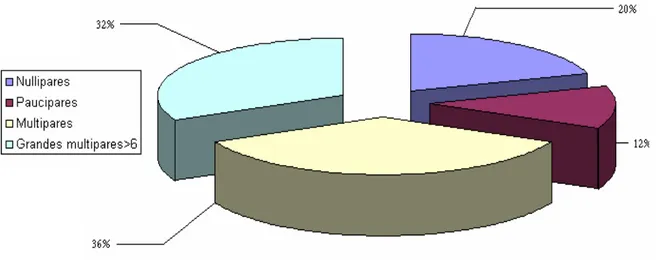
Figure


Documents relatifs
In this work, we apply a singular value decomposition (SVD) based matrix compression method to an IE forward solver for global geomagnetic induction: After employing
Deux études (1 prospective et 1 rétrospective) menées essentiellement chez des patientes admissibles à une CCS (selon l’imagerie conventionnelle) ont rapporté l’effet de l’IRM
Devant la forte fixation des nodules des seins au TEP et dans la crainte de métastases pulmonaires du cancer du sein qui serait classé stade IV et qui serait de meilleur pronostic
Proprio a causa della varietà delle tematiche affrontate il libro può apparire discontinuo, per quanto la trattazione lasci comunque intravedere un filo rosso dall’acqui-
Aussi la place des différentes techniques n’est elle pas toujours respectée pour ceci ; nous insistons sur l’utilisation d’une technique codifiée, rigoureuse
• Dyslipidemia + grade 3 hypertension • Chronic kidney failure + microalbuminuria.. - Also this study allowed us to establish a score to calculate the probability of carrying
Dans notre étude, l’hémoculture a été faite chez tous nos malades, elle était positive dans 65% des cas.. Une infection de la voie urinaire ou rénale peut être le point de départ
La présente étude, a été réalisée auprès de 100 médecins œuvrant au sein du CHU Mohammed VI de Marrakech sur une période de 6 mois ; avec comme objectif principal de percevoir