FACULTE DE CHIRURGIE DENTAIRE
Année : 2013 Thèse n°2013-‐TOU3-‐3041
THESE
pour le
DIPLOME D’ETAT DE DOCTEUR EN CHIRURGIE DENTAIRE
Présentée et soutenue publiquementPar
MOURLAN Loïc
Le 9 Juillet 2013
PENETRATION DE CIMENT DE SCELLEMENT ENDODONTIQUE
DANS LES TUBULES DENTINAIRES : PRE-‐ETUDE EN MICROSCOPIE A
FLUORESCENCE DE 3 TECHNIQUES D’OBTURATION.
Directeur de Thèse : DOCTEUR Franck DIEMER
JURY
Président Professeur Danielle DUFFAUT Assesseur Docteur Mélanie DEDIEU Assesseur Docteur Rachel DARDE Assesseur Docteur Franck DIEMER
UNIVERSITE TOULOUSE III – PAUL SABATIER FACULTE DE CHIRURGIE DENTAIRE
Année : 2013 Thèse n°2013-‐TOU3-‐3041
THESE
pour le
DIPLOME D’ETAT DE DOCTEUR EN CHIRURGIE DENTAIRE
Présentée et soutenue publiquementPar
MOURLAN Loïc
Le 9 Juillet 2013
PENETRATION DE CIMENT DE SCELLEMENT ENDODONTIQUE
DANS LES TUBULES DENTINAIRES : PRE-‐ETUDE EN MICROSCOPIE A
FLUORESCENCE DE 3 TECHNIQUES D’OBTURATION.
Directeur de Thèse : DOCTEUR Franck DIEMER
JURY
Président Professeur Danielle DUFFAUT Assesseur Docteur Mélanie DEDIEU Assesseur Docteur Rachel DARDE Assesseur Docteur Franck DIEMER
FACULTÉ DE CHIRURGIE DENTAIRE -‐-‐-‐-‐-‐-‐-‐-‐-‐ â DIRECTION DOYEN Mr SIXOU Michel ASSESSEURS DU DOYEN • ENSEIGNANTS :
Mme GRÉGOIRE Geneviève Mr CHAMPION Jean Mr HAMEL Olivier Mr POMAR Philippe
• PRÉSIDENTE DU COMITÉ SCIENTIFIQUE
Mme GRIMOUD Anne-Marie
• ÉTUDIANT : Mr HAURET-CLOS Mathieu CHARGÉS DE MISSION Mr PALOUDIER Gérard Mr AUTHER Alain RESPONSABLE ADMINISTRATIF
Mme GRAPELOUP Claude
â HONORARIAT DOYENS HONORAIRES Mr LAGARRIGUE Jean È Mr LODTER Jean-Philippe Mr PALOUDIER Gérard Mr SOULET Henri â ÉMÉRITAT Mr PALOUDIER Gérard -‐-‐-‐-‐-‐-‐-‐-‐-‐-‐-‐ â PERSONNEL ENSEIGNANT 56.01 PÉDODONTIE
Chef de la sous-section : Mr VAYSSE
Professeur d'Université : Mme BAILLEUL-FORESTIER
Maîtres de Conférences : Mme NOIRRIT-ESCLASSAN, Mr VAYSSE
Assistants : Mr DOMINÉ, Mme GÖTTLE
Chargés d’Enseignement : Mme BACQUÉ, Mme PRINCE-AGBODJAN, Mr TOULOUSE
56.02 ORTHOPÉDIE DENTO-FACIALE
Chef de la sous-section : Mr BARON
Maîtres de Conférences : Mr BARON, Mme LODTER, Mme MARCHAL-SIXOU, Mr ROTENBERG,
Assistants : Mme ELICEGUI, Mme OBACH-DEJEAN, Mr PUJOL
Chargés d'Enseignement : Mr GARNAULT, Mme MECHRAOUI, Mr MIQUEL
56.03 PRÉVENTION, ÉPIDÉMIOLOGIE, ÉCONOMIE DE LA SANTÉ, ODONTOLOGIE LÉGALE
Chef de la sous-section : Mr HAMEL
Professeur d'Université : Mme NABET, Mr PALOUDIER, Mr SIXOU Maître de Conférences : Mr HAMEL
Assistant : Mr MONSARRAT
Chargés d'Enseignement : Mr DURAND, Mr PARAYRE, Mr VERGNES
57.01 PARODONTOLOGIE
Chef de la sous-section : Mr BARTHET
Maîtres de Conférences : Mr BARTHET
Assistants : Mr MOURGUES, Mme VINEL
Chargés d'Enseignement : Mr. CALVO, Mme DALICIEUX-LAURENCIN, Mr LAFFORGUE, Mr PIOTROWSKI, Mr SANCIER
57.02 CHIRURGIE BUCCALE, PATHOLOGIE ET THÉRAPEUTIQUE, ANESTHÉSIOLOGIE ET RÉANIMATION
Chef de la sous-section : Mr CAMPAN
Professeur d'Université : Mr DURAN
Maîtres de Conférences : Mr CAMPAN, Mr COURTOIS, Mme COUSTY
Assistants : Mme BOULANGER, Mr FAUXPOINT, Mme FERNET-MAGNAVAL
Chargés d'Enseignement : Mr GANTE, Mr L’HOMME, Mme LABADIE, Mr PLANCHAND, Mr SALEFRANQUE
57.03 SCIENCES BIOLOGIQUES (BIOCHIMIE, IMMUNOLOGIE, HISTOLOGIE, EMBRYOLOGIE. GÉNÉTIQUE, ANATOMIE PATHOLOGIQUE, BACTÉRIOLOGIE, PHARMACOLOGIE
Chef de la sous-section : Mr KÉMOUN
Professeurs d'Université : Mme DUFFAUT
Maîtres de Conférences : Mme GRIMOUD, Mr KEMOUN, Mr POULET
Assistants : Mr BLASCO-BAQUE, Mme GAROBY-SALOM, Mme SOUBIELLE, Mme VALERA Chargés d'Enseignement : Mr BARRÉ, Mme DJOUADI-ARAMA, Mr SIGNAT
58.01 ODONTOLOGIE CONSERVATRICE, ENDODONTIE
Chef de la sous-section : Mr GUIGNES
Maîtres de Conférences : Mr DIEMER, Mr GUIGNES, Mme GURGEL-GEORGELIN, Mme MARET-COMTESSE Assistants : Mr ARCAUTE, Mlle DARDÉ, Mme DEDIEU, Mme DUEYMES, Mme FOURQUET,
Mr MICHETTI
Chargés d'Enseignement : Mr BALGUERIE, Mr BELAID, Mlle BORIES, Mr ELBEZE, Mr MALLET, Mlle PRATS, Mlle VALLAEYS
58.02 PROTHÈSES (PROTHÈSE CONJOINTE, PROTHÈSE ADJOINTE PARTIELLE, PROTHÈSE COMPLÈTE, PROTHÈSE MAXILLO-FACIALE)
Chef de la sous-section : Mr CHAMPION
Professeurs d'Université : Mr ARMAND, Mr POMAR
Maîtres de Conférences : Mr BLANDIN, Mr CHAMPION, Mr ESCLASSAN
Assistants : Mr CHABRERON, Mr DESTRUHAUT, Mr GALIBOURG, Mr HOBEILAH, Mme SOULES Chargés d'Enseignement : Mr ABGRALL, Mr DEILHES, Mr FARRÉ, Mr FLORENTIN, Mr FOLCH, Mr GHRENASSIA,
Mr KAHIL, Mme LACOSTE-FERRE, Mme LASMOLLES, Mr LUCAS, Mr MIR, Mr POGEANT,
Mr RAYNALDY
58.03 SCIENCES ANATOMIQUES ET PHYSIOLOGIQUES, OCCLUSODONTIQUES, BIOMATÉRIAUX, BIOPHYSIQUE, RADIOLOGIE
Chef de la sous-section : Mme GRÉGOIRE
Professeur d'Université : Mme GRÉGOIRE Maîtres de Conférences : Mme JONIOT, Mr NASR
Assistants : Mr AHMED, Mr CANIVET, Mr DELANNÉE
Chargés d'Enseignement : Mme BAYLE-DELANNÉE, Mme MAGNE, Mr TREIL, Mr VERGÉ ---
L'université Paul Sabatier déclare n'être pas responsable des opinions émises par les candidats.
(Délibération en date du 12 Mai 1891).
Je dédie cette thèse …
A ma tante Monique, disparue trop tôt, trop vite. Tu as toujours veillé sur moi, comme sur ton propre fils, et tu continues même après ta disparition, ce qui rend ton absence encore plus insupportable… Je t’aime.
A mes parents, qui m’ont toujours soutenu, épaulé, et poussé quand il l’a fallu. Merci d’avoir fait les choses comme vous les avez faites, merci d’être mes parents. Papa
j’espère qu’un jour je te ferai aimer les dentistes. Maman, j’espère que je n’ai pas fait trop de fautes d’orthographe ! J’ai de la chance de vous avoir, même si je ne vous le dis pas assez souvent…
A ma famille,
Mes deux grands mères adorées, et mes oncles/tantes et cousins/cousines que je prend toujours plaisir à retrouver en toutes occasions, et surtout autour d’un bon repas de famille !
A Magalie, merci à toi, merci d’être à mes côtés, tu comptes énormément à mes yeux et j’espère que nous continuerons encore longtemps notre chemin ensemble…
A Lucie, mon binôme, avec qui j’ai passé 3 années de cliniques exceptionnelles. Ta patience a bien atténué mon impatience et vice versa ! On s’associe quand tu veux ! Spéciale dédicace à « la chèvre de Mr Seguy » et au papillome de lumière…
A Seb et Niko, mes deux potes du tout début ! Ces 5 années d’études resteront gravées dans ma mémoire, que de bons moments passés ensemble, de crit, de God… et autant à venir je l’espère ! N’oublions pas d’embarquer Charles, il risquerait de se perdre !
Aux copains de promo, Sacha, Caro, Bertrand, Laura, Laurine, Laurie, Antoine, Vincent, Mathieu, Sophie, Cyrielle, David… Et tous ceux que j’oublie. J’espère que l’on continuera à réunir la promo encore longtemps !
A Anais et Chloé, toujours là pour bien se marrer...
Aux membres de l’AECDT, Elsa, Amaury, Romain, Kevin, Sylvain, Renaud, Chacha, Léti, Joffrey … Merci pour ces années d’associatif, très chronophages mais si enrichissantes ! Un grand merci à Sauveur, sans qui bien des choses n’auraient pas été possibles à la fac.
A tous ceux de la Bodega, les vieux, Bube, Guigui, Touti, Mathieu… comme les jeunes, Fiston, François, Astérix, qui reprennent le flambeau avec brio !
A mes copains du Comité, Lionel, Olivier, Damien, Cédric, Totoche, Bety, Barné, on se reforme quand vous voulez ! Et à mes frères du « Cercle », longue vie au Comminges et aux Commingeois !
A Decap et ses repas pré-‐exams sans lesquels rien n’aurait été possible !
Aux copains du rugby, Moute, Bidoche, KB, Pêcheur, Gnialy, Lolo, Pep…
Au Docteur Rouffiac pour ses conseils avisés, si précieux en début d’exercice.
Et surtout, à mon petit village, Saint Martory ! Souvent raillé, jamais égalé !
A notre président de jury,
Madame le Professeur Danielle DUFFAUT-LAGARRIGUE
- Professeur des Universités, Praticien Hospitalier d’Odontologie, - Lauréat de la Faculté de Médecine,
- Docteur en Chirurgie Dentaire,
- Docteur en Sciences Odontologiques, - Docteur d'État en Odontologie,
- Habilitée à Diriger des Recherches
Nous vous sommes très reconnaissant d’avoir accepté de présider ce jury. Nous vous remercions pour votre grande gentillesse et votre disponibilité en clinique qui ont su nous guider jusqu’à ce jour. Nous avons par ailleurs déjà eu l’honneur de siéger à vos côtés en Conseil de Faculté, lors duquel les échanges se sont toujours fait en bonne intelligence et écoute mutuelle. Avec nos remerciements, veuillez trouver ici l’expression de notre respect et de notre gratitude.
A notre directeur de thèse,
Monsieur le Docteur Franck DIEMER
- Maître de Conférences des Universités, Praticien Hospitalier d’Odontologie, - Docteur en Chirurgie Dentaire,
- Diplôme d’Etudes Approfondies en Education, Formation et Insertion Toulouse Le Mirail
- Docteur de l’Université Paul Sabatier, - Lauréat de l'Université Paul Sabatier
Vous nous avez fait le très grand honneur d’être l’instigateur de ce sujet et de diriger ce travail. Merci pour tous vos conseils et votre disponibilité qui nous ont été offert durant l’ensemble de notre cursus universitaire et clinique. Nous vous remercions également d’avoir partagé vos immenses compétences pendant notre stage actif dans votre cabinet libéral, et de nous avoir toujours accueilli vous observer travailler. Vos qualités humaines comme professionnelles imposent une sincère admiration et un immense respect à votre égard. En attendant de peut être travailler à nouveau à vos cotés, puisse ce travail être le témoignage de notre profonde gratitude.
A notre jury de thèse,
Madame le Docteur Mélanie DEDIEU
- Assistante hospitalo-universitaire d’Odontologie, - Docteur en Chirurgie Dentaire,
- Master 1 « Biosanté », mention Anthropologie, ethnologie et sociologie de la santé
Nous sommes très reconnaissant de votre présence à notre jury de thèse. Nous vous remercions pour votre grande gentillesse et vos conseils avisés durant notre cursus. Nous prenons plaisir à travailler avec vous dans le cadre des travaux pratiques d’endodontie, qui se déroulent toujours dans la bonne humeur. Soyez assurée de notre considération et de notre plus profond respect.
A notre jury de Thèse,
Madame le Docteur Rachel DARDÉ
-Assistante hospitalo-universitaire d’Odontologie, -Docteur en Chirurgie Dentaire,
-Master 1 : Sciences de la Vie et de la Santé – mention : Analyse fonctionnelle des génomes
-CES de Chirurgie Dentaire : Prothèse dentaire, option : Prothèse scellée, -Lauréate de l'Université Paul Sabatier.
Merci de la spontanéité avec laquelle vous avez accepté de prendre part à ce jury. Merci pour votre gentillesse, votre bonne humeur et votre disponibilité en clinique. Veuillez trouver ici l’expression de notre gratitude et profonde considération.
SOMMAIRE
SOMMAIRE………..p. 11 INTRODUCTION ……….….p. 15 I. METHODES D’EVALUATION DES OBTURATIONS ENDODONTIQUES……… .……..p. 18 1. Outils d’évaluation des obturations endodontiques………..p. 19 1.1. La radiographie………p. 19 1.1.1. Le cliché rétroalvéolaire………...p. 19 1.1.2. L’imagerie 3D : le micro CT et le CBCT………p. 21 1.2. Les tests de percolation apicale……….p. 21 1.2.1. Test de pénétration d’un colorant………..p. 22 1.2.2. Test de pénétration de radio-‐isotopes……….p. 24 1.2.3. Test de pénétration bactérienne……….p. 25 1.2.4. Test de pénétration de fluides sous pression………..p. 26 1.3. Le pourcentage de remplissage endodontique en Gutta-‐Percha (PGFA) en ciment et en vides canalaires………...p. 28 1.4. Pénétration du ciment dans les tubuli dentinaires………..….p. 28 2. Les ciments de scellement endodontiques : propriétés et comportements……..…..p. 33 3. Etudes comparatives des ciments de scellement endodontiques ……….…p. 37 3.1. Etude de la percolation apicale de 4 ciments endodontiques par pénétration des fluides sous pression : Pommel and coll (2003)……….…p. 37 3.1.1. Matériels et méthodes………...p. 37 3.1.2. Résultats et discussions………....p. 37 3.2. Etude de la pénétration et de l’adaptation du ciment dans les tubuli dentinaires au microscope électronique à balayage, Balguerie and coll (2011)………....p. 38 3.2.1. Matériels et méthodes………...p. 38 3.2.2. Résultats et discussions………p. 39 3.3. Etude de la percolation apicale à l’aide d’un CBBF : comparaison de plusieurs ciments, AH Plus®, Real Seal® et Adper Scotchbond®. Roth and coll (2012).p. 41 3.3.1. Matériels et méthodes………...…p. 41 3.3.2. Résultats et discussions………..….p. 42 3.4. A propos des ciments contenant du MTA ………..p. 43 4. Etudes comparatives des techniques d’obturation endodontiques ………....p. 48
4.1. Etude comparative entre la condensation latérale à froid et la technique monocône : Evaluation de la qualité des obturations par deux clichés radiographiques. Hörsted-‐Bindslev and coll (2007)………p. 48 4.1.1. Matériels et méthodes………...p. 48 4.1.2. Résultats et discussions………p. 49 4.2. Etude comparative de la percolation apicale par pénétration des fluides sous pression entre le System B, la technique monocône, la condensation latérale à froid, la condensation verticale à chaud et le Thermafil de Pommel and coll (2001) ………..p. 49 4.2.1. Matériels et méthodes………...p. 49 4.2.2. Résultats et discussions………....p. 50 4.3. Etude comparative à l’aide d’un lysozyme radioactif de la percolation apicale de 3 techniques d’obturation : condensation latérale, Thermafil®, et Mac Spadden. Haikel and coll, (2000) ………...p. 51 4.3.1. Matériels et méthodes………...p. 51 4.3.2. Résultats et discussions………p. 51 4.4. Etude comparative de la condensation latérale à froid et du thermocompactage : évaluation de la qualité radiographique et comparaison de la percolation apicale par pénétration d’un colorant. Al Dewani and coll (2000)………...p. 52 4.4.1. Matériels et méthodes…..……….p. 52 4.4.2. Résultats et discussions………p. 53 4.5. Etude du pourcentage de remplissage endodontique en gutta percha (PGFA) sur des canaux ovalaires entre quatre techniques d’obturation : condensation latérale, thermocompactage, condensation verticale à chaud et Thermafil®. De-‐ Deus and coll (2008) ………...p. 54 4.5.1. Matériels et méthodes………...p. 54 4.5.2. Résultats et discussions………p. 54 5. Les limites des études comparatives ………..p. 62
II. ETUDE DE LA PENETRATION TUBULAIRE DU CIMENT DE SCELLEMENT AU MICROSCOPE OPTIQUE A FLUORESCENCE : COMPARAISON DE 3 TECHNIQUES D’OBTURATION. ………..p. 70
1. Matériels et méthodes : ………...p. 71 1.1. Préparation du ciment de scellement ………...p. 72 1.2. Obturation canalaire du groupe 1 ………...p. 72 1.3. Obturation canalaire du groupe 2 ………...p. 73 1.4. Obturation canalaire du groupe 3 ………...p. 74 1.5. Section des échantillons ………p. 76 2. Résultats ………...p. 77 3. Discussion ………p. 79 CONCLUSION………...………...p. 85 LISTE DES FIGURES………..………..p. 87 LISTE DES TABLEAUX………...………p. 90 REFERENCES BIBLIOGRAPHIQUES……….……….p. 92
INTRODUCTION
Depuis « Le Chirurgien Dentiste ou Traité des dents » de Pierre Fauchard en 1746 (20) à aujourd’hui, la chirurgie dentaire, et notamment l’endodontie, sont en constante évolution. Le praticien se doit de prodiguer des soins en accord avec les données acquises de la science, qui sont perpétuellement renouvelées. Du pansement arsenical à l’utilisation de l’anesthésie locale en 1898 (41), de l’utilisation des cônes d’argent à l’arrivée de la Gutta Percha dans les années 1950, et de l’instrumentation manuelle aux débuts de l’instrumentation rotative mécanisée dans les années 1980 ; l’endodontie a été bousculée par plusieurs petites révolutions.
Un traitement endodontique bien réalisé est indispensable pour assurer la réussite et la pérennité des reconstitutions directes ou indirectes sur dent dépulpée. Il peut permettre également la cicatrisation d’une pathologie péri-‐apicale. L’élimination du parenchyme pulpaire est obtenue après élimination du tissu carieux et après isolation de la dent traitée par un champ opératoire étanche (digue dentaire). La synergie d’action entre les instruments de mise en forme canalaire et les différentes solutions d’irrigation permettent une élimination chimique et mécanique des micro-‐organismes et des débris dentinaires. L’action chimique permet également de nettoyer des zones inaccessibles à la préparation mécanique (canaux accessoires, isthmes, canaux latéraux…). Ceci facilitera la pénétration du ciment de scellement dans les tubules dentinaires lors de l’obturation endodontique. Ce phénomène est dépendant de plusieurs facteurs qui sont entre autre : les propriétés du ciment de scellement, la technique d’obturation utilisée mais aussi l’âge et l’anatomie canalaire de la dent obturée.
Devant le nombre important de techniques d’obturation, c’est la littérature scientifique qui doit aider le clinicien à choisir l’une d’elle pour une utilisation quotidienne en cabinet dentaire. Ce choix sera guidé par une simplicité de mise en œuvre et un coût moindre, mais ils devront écarter celles qui ne sont pas (ou plus) en accord avec les données acquises de la science. Néanmoins, le nombre important de références bibliographiques sur le sujet ne permet pas d’établir une distinction claire entre les avantages ou les inconvénients propres à chacune d’entre elles.
Comme le suggère le Journal of Endodontics dans son éditorial de décembre 2007 (59), il est nécessaire d’évaluer les outils qui permettent de comparer les procédés d’obturation endodontique. Il est également nécessaire de standardiser les protocoles des études sur le sujet, pour obtenir des résultats reproductibles, non biaisés et comparables. Une application clinique directe ainsi que la recherche d’un Gold Standard doivent être au cœur de ces protocoles d’évaluation.
Dans un premier temps l’évaluation des obturations endodontiques sera détaillée : les méthodes d’évaluation et leurs limites ainsi qu’un état des lieux de la littérature concernant la comparaison de ces techniques sera fait. Dans un second temps un protocole expérimental visant à évaluer une nouvelle technique d’obturation endodontique (la condensation latérale mécanisée utilisant le mouvement de rotation continue ou de réciprocité) sera proposée. Grâce à la microscopie à fluorescence et à l’utilisation d’un colorant, la pénétration du ciment endodontique dans les tubuli dentinaires sera mesurée sur dents humaines.
I. METHODES D’EVALUATION DES
OBTURATIONS ENDODONTIQUES
1. Outils d’évaluation des obturations endodontiques :
1.1. La radiographie :
1.1.1. Le cliché rétroalvéolaire :
La radiographie est un outil d’évaluation clinique et de diagnostic pour le praticien, mais elle s’inscrit également dans le cadre légal puisque la Haute Autorité de Santé (HAS) recommande aux praticiens de réaliser 3 clichés rétroalvéolaires lors d’un traitement endodontique :
-‐ un cliché préopératoire donnant des informations sur l’anatomie canalaire ainsi que sur l’intégrité du parodonte. Ce cliché à visée diagnostique, permettra non seulement de juger de la difficulté du traitement à effectuer mais aussi d’adapter la thérapeutique en fonction du cas clinique. En effet, certains instruments de préparation canalaire rotatifs sont contre-‐indiqués dans le cas de très fortes courbures (ou de double courbure). De plus, une technique d’obturation peut être préférée à une autre selon le diamètre du canal à obturer.
-‐ Un cliché peropératoire permettant de contrôler la longueur de travail et de vérifier l’adaptation du maître cône avant l’obturation.
Figure 1 : Détermination de la longueur de travail à l’aide d’un cliché vestibulo-‐lingual (à gauche) et d’un cliché mesio-‐distal (à droite) qui permet de bien différencier les deux canaux sur cette prémolaire maxillaire. Kytridou, 1999, (59)
-‐ Un cliché post-‐opératoire qui fait l’objet de référence dans le suivi du patient. Un traitement endodontique est considéré comme réussi s’il est radiologiquement dense, qu’il est tridimensionnel et qu’il s’approche autant que possible de la jonction cémento-‐dentinaire, tout en respectant le péri-‐apex (18). Tout dépassement de matériau au delà de l’apex est
indésirable pour le succès du traitement endodontique (27).
Dans certaines études (1) l’évaluation se fait selon une échelle de 4 points, appliquée en
séparant la dent en deux parties (coronaire et apicale) et après la prise de deux clichés radiographiques (cliché vestibulo-‐lingual et cliché mésio distal, le dernier étant difficile à reproduire in vivo puisqu’il pose un problème de superposition (25)) :
-‐ l’obturation est bien condensée si elle obture la totalité du canal préparé, si elle est adaptée aux parois canalaires ou qu’elle montre une petite quantité de zones radioclaires, inférieures à 0,25mm de diamètre
-‐ l’obturation est imparfaitement condensée si elle possède des irrégularités d’adaptation inférieures à 1mm (et supérieures à 0,25 mm) -‐ l’obturation est insuffisamment condensée si elle possède des
irrégularités d’adaptation inférieures à 2 mm (et supérieures à 1mm) -‐ l’obturation est très peu condensée quand elle présente des irrégularités
supérieures à 2mm
Cependant, d’un point de vue scientifique, le cliché radiographique, qu’il soit argentique ou numérique, n’est pas un moyen fiable de comparaison de l’efficacité des différentes techniques d’obturation. En effet, il existe des variations d’interprétations de ces clichés d’un praticien à l’autre, mais aussi d’un cliché à l’autre (clichés excentrés et clichés normocentrés). Sont également source de variations l’expérience de l’observateur ainsi que son habitude du système radiographique utilisé. De plus il faut souligner que ces clichés sont une représentation en deux dimensions de trois dimensions, ce qui augmente leur imprécision (52).
Hörsted-‐Bindslev (25) souligne que le cliché vestibulo-‐lingual seul, ne permettrait pas
d’évaluer l’obturation en totalité, puisque les vides et les irrégularités présents en lingual (ou palatin) ne seraient pas observés, du fait de la superposition, surtout quand le canal est plus large en vestibulo-‐lingual qu’en mésio-‐distal.
1.1.2. L’imagerie 3D : Le micro-‐CT et le CBCT :
L’imagerie 3D a permis de nombreuses avancées notamment en ce qui concerne le diagnostic (détection des pathologies péri-‐apicales…) et en ce qui concerne la recherche puisqu’elle apporte une précision que n’offrait pas les clichés 2D. En effet elle permet d’analyser canal par canal l’homogénéité d’une obturation, de vérifier l’obturation des canaux accessoires ou du MV2. Son aide est d’autant plus précieuse dans les régions postérieures (prémolaires et molaires) puisqu’elle permet de s’affranchir du « bruit » provoqué par l’épaisseur de l’os alvéolaire et donc de n’étudier que la région intéressant le praticien (30).
Il est à noter que ces examens sont bien plus irradiants qu’un cliché rétroalvéolaire classique (ou qu’un orthopantomogramme), ils ne sont donc réalisés qu’en seconde intention (avec un CBCT pour le diagnostic) ou sur dents extraites (avec un Micro-‐CT).
1.2. les tests de percolation apicale :
En 1994, l’AAE définit la percolation comme le mouvement de fluides tissulaires périradiculaires, de micro-‐organismes et de leurs toxines le long de l’interface entre les parois dentinaires et les matériaux d’obturation canalaire (25). Celle ci
serait une des causes d’échec des traitements endodontiques (53).
Cette micropercolation serait favorisée par l’anatomie du système canalaire, de plus en plus complexe au fur et à mesure que le foramen apical se rapproche (canaux accessoires, multiples foramina…) et par la capacité de scellement des matériaux d’obturation. (18) Il est donc important d’évaluer les différentes techniques d’obturation
et les différents matériaux utilisés notamment leur capacité à réaliser un scellement hermétique de la région apicale.
1.2.1. tests de pénétration d’un colorant :
Cette technique consiste en la mesure linéaire de pénétration d’un colorant entre les parois canalaires et le matériau grâce aux phénomènes de capillarité ou de diffusion selon le vide (18).
L’apex (ou la partie coronaire de la dent) est immergé dans du colorant qui va pénétrer dans les vides de l’obturation canalaire qui existent entre les parois dentinaires et le matériau d’obturation.(53) La pénétration du colorant peut être induite par une pression positive ou négative, ou être réalisée sous vide (8).
L’application d’une pression positive permettrait de s’affranchir des interférences créées par les vides présents dans l’obturation. La pénétration du colorant sous vide éliminerait l’air enchâssé dans les obturations (33), car celles-‐ci seraient responsables d’une moins bonne diffusion du colorant, lorsque celui ci pénètre passivement (56). Pour être observés, les échantillons sont préparés par section longitudinale ou transversale (53).
La pénétration du colorant ne serait pas un bon moyen d’étudier la percolation apicale, car celle ci ne serait pas uniforme le long des parois canalaires : la section nécessaire pour l’observation des échantillons qui se fait au hasard pourrait intéresser une zone de plus faible pénétration du colorant, non représentative de l’échantillon total (8). Ceci peut
entraîner une surestimation ou une sous estimation de la percolation réelle (53).
Il existe deux autres méthodes qui permettent de s’affranchir de ce biais :
-‐ l’extraction du colorant. Après immersion dans le colorant, les échantillons sont dissouts dans de l’acide nitrique, et la totalité du colorant est libérée dans la solution de dilution. La densité optique de la solution est ensuite mesurée par un spectrophotomètre, et la quantité de colorant qui a pénétré le réseau canalaire est connue et quantifiable (8).
-‐ rendre la dent transparente, ce qui permet une observation tridimensionnelle de la perte d’étanchéité (18). La dent est totalement déminéralisée, déshydratée ce qui la
rend totalement transparente. L’anatomie canalaire est alors visible en trois dimensions, tout comme la pénétration d’un colorant, qui peut être étudiée en totalité sans délabrer les échantillons. Des zones de déminéralisation incomplète seraient retrouvées, si le temps de déminéralisation est insuffisant, et ceci créerait des erreurs d’observation. Egalement, les produits utilisés pour déminéraliser pourraient dissoudre une partie du colorant ou du ciment endodontique, ce qui perturberait les résultats (53).
Figure 2 : Un exemple d’une dent décalcifiée et rendue transparente par immersion dans une solution de méthyl-‐salicylate. Le colorant pénètre au delà du foramen apical jusqu’au point A. Baumgardner, 1990, (11)
Deux colorants ont été les plus utilisés : le bleu de méthylène et l’encre de Chine en raison de leur faible poids moléculaire donc de leur meilleure pénétration au sein du système canalaire. La taille des particules du colorant, son pH, et sa réactivité chimique affectent son degrés de pénétration (53).
D’après Mente (33) les particules de l’encre de Chine ont une taille oscillant entre 0,1 et 2 µm ce qui serait comparable à de nombreuses bactéries présentes dans la flore bactérienne canalaire. En revanche les particules du bleu de méthylène, 1000 fois plus petites que les bactéries, ne seraient pas représentatives de la percolation apicale in vivo. Un des avantages du bleu de méthylène est en revanche son coût très faible (53). Ceci n’est pas en accord avec l’étude de De-‐Deus en 2008 (12), qui conclue que les
résultats entre la technique d’extraction du colorant (bleu de méthylène) et la pénétration bactérienne sont identiques. Cependant il entrainerait des résultats contradictoires dans les différentes études qui l’ont utilisé, en raison de son pH acide qui entraine une déminéralisation de la dentine. La percolation est donc surévaluée dans les études n’ayant pas tamponné le pH du Bleu de méthylène. L’encre de Chine est donc préférée, car son pH est neutre (33).
1.2.2. tests de pénétration de radio isotopes :
Les radio-‐isotopes ont l’avantage d’être plus petits et de diffuser plus rapidement que les colorants. Au début, le Calcium était utilisé mais il serait responsable d’échanges ioniques avec les cristaux d’apatite de la structure dentinaire, ce qui perturberait le phénomène de percolation (23). On utilise des marqueurs radioactifs (combinaison
d’iodine et de lysozymes) car ils permettent d’obtenir des mesures quantitatives facilement analysables et comparables (18).
Figure 3 : Schéma de l’appareil d’immersion des échantillons dans la solution de lysozyme
radioactifs. Haikel, 2000, (23)
1 : Piston ; 2 : Chambre coulissante ; 3 : revêtement plombé ; 4 : seringue ; 5 : tube en PVC ; 6 : échantillon ; 7 : tube stérile ; 8 : solution radio active
Un autre avantage est le fait qu’ils ont une taille moins importante que les colorants et diffuseraient plus rapidement que ceux ci.
1.2.3. test de pénétration bactérienne :
Les radios isotopes ne seraient pas représentatifs de ce qu’il se passe in-‐vivo. En effet, ils seraient plus des indicateurs d’échanges ioniques et de diffusion au sein des tissus que des indicateurs d’une véritable perte d’étanchéité. C’est pourquoi certains auteurs ont proposé d’utiliser des bactéries de faible taille et de grande mobilité (S. epidermidis, P. Vulgaris), qui donnent des résultats plus proches de la réalité clinique
(18). Le matériel de l’étude se compose en général d’un système à chambre double,
reliées chacune à une extrémité de l’échantillon, l’une comprenant les bactéries.
Les études de pénétration bactérienne varient dans leurs résultats, car les bactéries utilisées sont souvent différentes d’une étude à l’autre (53).
Des études récentes s’intéressent aux endotoxines qui sont des produits bactériens responsables d’infections pulpaires et péri-‐radiculaires, et qui peuvent pénétrer le système canalaire après obturation, par la partie coronaire, le foramen apical, les canaux latéraux, les fractures et les canaux accessoires. La prise incomplète ou retardée du ciment favoriserait la pénétration d’endotoxines dans le réseau canalaire (55).
Des bactéries unitaires telles que les Enterococci sont également associées aux échecs de traitement endodontiques. Enterrococcus Faecalis est retrouvée dans la flore buccale humaine et est responsable de nombreuses infections avec d’autres bactéries aérobies, et aussi des anaérobies. Elle est donc utilisée dans les études de pénétration bactérienne, puisqu’elle est représentative de ce qui se passe in vivo (58).
De Deus and coll (12) font remarquer que la pénétration bactérienne ne simule pas
exactement les conditions de la cavité buccale (température, influence de l’alimentation, flux salivaire). Cette technique permettrait seulement d’étudier certaines périodes spécifiques (sur un temps donné et des conditions bien particulières), il serait donc nécessaire de les réaliser sur des périodes beaucoup plus longues.
Un des outils permettant de simuler ce qu’il se passe in vivo serait le CBBF (Chemostat Based-‐biofilm Fermentor) qui permet de cultiver des bactéries du biofilm buccal, comme Enterococcus feacalis ou Streptoccocus Mutans, sur des échantillons tel que des dents. Il reproduit les conditions de la cavité buccale à savoir une température de 37 °C et un flux continu d’une solution contenant du glucose imitant la salive (43).
1.2.4. test de pénétration de fluides sous pression :
Dans les tests de pénétration de colorant, de grosses variations ont été constatées dans la profondeur de pénétration du colorant (8). Ceci peut être expliqué non seulement par
des erreurs expérimentales et des variations propres à chaque technique mais aussi par la présence de bulles d’air dans les vides de l’obturation. Cette présence d’air ou de liquide diminuerait la pénétration du colorant(56).
On mesure ici le mouvement de fluides au sein du réseau canalaire par déplacement d’une bulle d’air à l’intérieur d’un capillaire, exprimé en µl min-‐1.
La partie coronaire de la racine est reliée à un tube rempli d’eau sous une légère pression (environ 1atm), alors que la partie radiculaire est reliée à un capillaire également rempli d’eau. On utilise une seringue pour injecter une bulle d’air. L’air emprisonné dans les vides de l’obturation est ensuite éliminé grâce à cette légère pression. Les mesures peuvent alors se faire grâce au déplacement de la bulle d’air préalablement injectée mettant en évidence les mouvements de fluide le long du canal (39).
Figure 4 : Schéma du dispositif de mesure des fluides sous pression, Emery, 2002, (18)
Cette technique permet de s’affranchir des biais opérateur dépendants puisque les résultats sont enregistrés automatiquement (40)(53).
Un de ses avantages est également le fait qu’elle permet de ne pas sectionner les échantillons, et donc sont réutilisables pour être étudiés a postériori (53). De plus elle permet de s’affranchir des biais provoqués par la taille moléculaire, l’affinité pour la dentine et le pH puisqu’aucun colorant n’est utilisé dans cette technique (39).
Un des inconvénients de cette technique est que la filtration diminue au fil du temps, car l’eau remplit peu à peu les irrégularités avant d’atteindre un plateau. Il faudrait donc 24 heures de mesure (par échantillon) pour obtenir un relevé de la filtration représentatif de la dent (8).
1.3. Le pourcentage de remplissage endodontique en Gutta Percha (PGFA), en ciment et en vides canalaires :
Il n’existe pas d’adhésion directe de la Gutta-‐percha sur les parois dentinaires. Une couche de ciment doit nécessairement être interposée pour obtenir un scellement de cette interface microscopique, sur l’ensemble de l’endodonte (35). La dissolution des ciments de scellement augmente les phénomènes de percolation le long des parois après obturation, ce qui implique donc que la couche de ciment doit être la plus fine possible au profit d’un PGFA élevé. En effet, la Gutta Percha est stable dimensionnellement alors que les ciments présentent des variations dimensionnelles pendant leur prise et sont pour certains solubles dans le temps (42).
La présence de vides au sein de l’obturation témoigne de l’inhomogénéité du traitement endodontique, et donc d’une moins bonne adaptation aux parois et aux irrégularités canalaires.
1.4. Pénétration du ciment dans les tubuli dentinaires :
La pénétration du ciment dans les tubuli dentinaires est importante, car elle permet d’augmenter l’étanchéité de l’obturation, elle diminue l’interface entre la dentine et le matériau, et elle offre une rétention mécanique par invasion de ces tubuli (48). Ceci permet également d’isoler les bactéries restantes dans les tubuli, et de les priver de leur source nutritive ce qui empêche leur prolifération (9).
L’élimination de la smear layer est indispensable, car elle va permettre aux matériaux d’obturation de pouvoir pénétrer dans les tubuli et de réduire l’infiltration coronaire et apicale (46). En effet, la préparation mécanique, qu’elle soit manuelle ou rotative, génère des débris qui viennent obturer les tubuli dentinaires. Cette boue dentinaire est composée de restes de tissu pulpaire, de processus odontoblastiques, éventuellement de salive, de sang, de cellules et de bactéries. L’irrigation à l’hypochlorite de sodium à 5,25 % lors de la mise en forme ainsi que l’irrigation finale à l’hypochlorite 5,25 % et à l’EDTA à 17 % permettrait d’en éliminer la quasi totalité (48).
Cette suppression de la smear layer permet aux ciments de pénétrer dans les tubuli dentinaires selon une profondeur variable en fonction du type de ciment (26).
Ce phénomène est décrit par l’équation de Washburn, qui décrit la pénétration d’un liquide (ciment non pris) dans un solide poreux (dentine). Cette équation suppose que le solide poreux est couvert de capillaires ouverts et donc que la pénétration du liquide est guidée par les forces de capillarité (9).
La pénétration du ciment sur des échantillons in vitro serait comparable à ce qui se passe in vivo (4).
Figure 5 : Photographie de l’obturation de plusieurs canaux latéraux, Al-‐Dewani, 2000, (1)
La pénétration du ciment dans les tubuli dépend de plusieurs facteurs : -‐ l’élimination de la smear layer (48)
Figure 6 : Observation au microscope électronique à balayage de l’aspect de la surface dentinaire avant élimination de la smear-‐layer (A) et après élimination de celle-‐ci par des solutions d’irrigation (B), Kokkas, 2004, (26)
-‐ la perméabilité dentinaire (nombre et diamètre variable des tubuli selon la région radiculaire) : la partie apicale contient moins de tubuli que la partie coronaire et ceux ci ont un diamètre inférieur. On peut également retrouver dans la partie apicale des zones de dentine sclérosée qui vont empêcher la pénétration des solutions d’irrigation et du ciment d’obturation (9).
Le diamètre des tubuli est différent selon la partie canalaire : o 2,5 μm dans la portion coronaire
o 1,2 μm dans la portion médiane o 0,9 μm dans la portion apicale
La densité des tubuli varie également entre 90000 et 4900 par mm2. Cette densité diminue de la partie coronaire vers la partie apicale le long du canal, mais également de la partie externe à la partie interne de la racine.
Il n’y a pas que la densité tubulaire qui diminue vers l’apex, il y a également la perméabilité de ces tubuli : la dentine apicale est plus souvent sclérosée et plus minéralisée que la dentine coronaire (9).
Le partie supérieure du tiers médian du système canalaire serait la zone présentant la plus grande pénétration de ciment dans les tubuli : c’est à cet endroit que le diamètre de ceux ci serait le plus large et que les forces appliquées lors de la condensation latérale seraient les plus bénéfiques à la pénétration du ciment (35).
Il est à noter que dans la partie apicale, un peu de cément peut remonter au delà du foramen apical et venir obstruer certains tubuli dentinaires (4).
-‐ diamètre canalaire : il diminue plus la dent est âgée
-‐ propriété physique et chimique du ciment (4) : la tension de surface, plus
elle est faible, mieux le ciment pénètre (9).
Weis (54) indique en 2004 que la profondeur de pénétration du ciment n’est pas influencée par la technique d’obturation utilisée.
L’écoulement du ciment est une des propriétés physique/chimique les plus importantes pour la pénétration tubulaire : elle correspond à la capacité du ciment à envahir les irrégularités, les canaux accessoires et les tubuli dentinaires, et elle est déterminée par la consistance, la température, le diamètre du canal radiculaire, la taille des particules du ciment, et le taux de cisaillement (4).
L’observation de la pénétration du ciment dans les tubuli va dépendre du type de section des échantillons. En effet, les tubuli dentinaires sont pour la plupart perpendiculaires à la lumière canalaire (4). Il existe deux types de sections :
longitudinale et transversale.
La pénétration du ciment a longtemps été étudiée grâce au microscope optique. La grande difficulté avec la lumière optique est l’impossibilité à distinguer le ciment de la dentine radiculaire : l’utilisation d’un colorant dans la microscopie à fluorescence permettrait d’éliminer cette contrainte.
L’utilisation du microscope électronique à balayage a permis d’observer en détail les différentes structures dentaires et l’intégrité de l’état de surface des ciments : il offre la possibilité d’étudier le ciment dans les tubuli dentinaires à distance des parois canalaires, où la densité tubulaire est moins importante (48). Il permet également de mettre en évidence et de déterminer la densité des « tags » de ciment dans les tubuli (35).
Figure 7 : « Tags » de ciment observés au microscope électronique à balayage (x1000), Moradi, 2009, (35)
L’inconvénient majeur est de ne pas pouvoir obtenir une vue d’ensemble détaillée à faible grossissement, ce qui rend les analyses systématiques difficiles.
La microscopie à balayage produirait également des artefacts pendant la phase de préparation des échantillons : ils doivent subir une pulvérisation d’or et l’observation se fait sous vide, ce qui prend beaucoup de temps. L’utilisation d’un faible vide (low
vacuum) sur certains microscopes électroniques à balayage autorise la visualisation
directe, sans métallisation, de l’échantillon et à des niveaux de pression n’endommageant pas l’intégrité de celui-‐ci (crack, fissures, fractures…).
La microscopie confocale permet de s’affranchir des défauts des deux techniques précédentes, et permet aussi de contrôler la profondeur de champ, d’éliminer ou de réduire le bruit du plan focal, et d’observer de nombreuses coupes même à travers un échantillon épais (9).
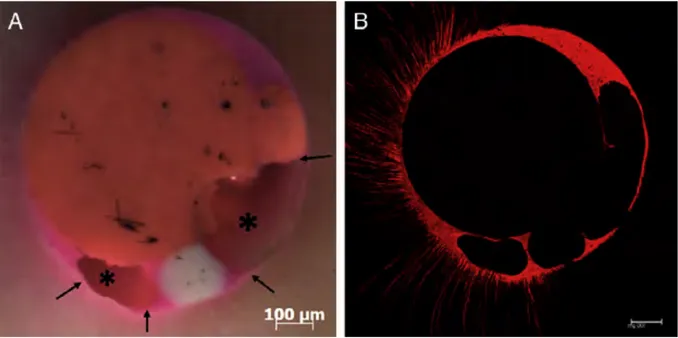
Figure 8 : Observation à la loupe binoculaire (à gauche) et au microscope confocal (à droite) de la section transversale d’un canal obturé par condensation latérale. Deux vides sont mis en évidence (*) ainsi que plusieurs lacunes à l’interface ciment/dentine. Marciano, 2011,
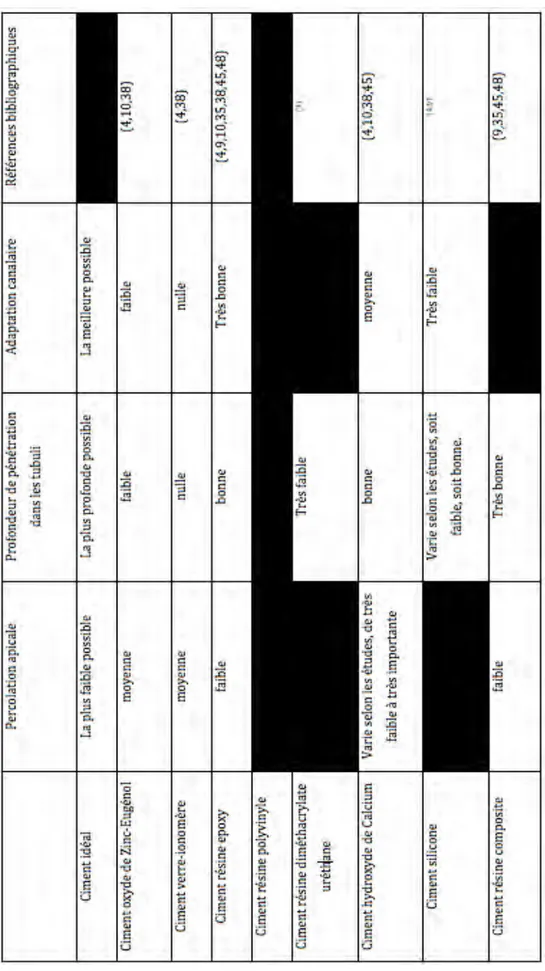
2. Les ciments de scellement endodontiques : Propriétés et comportement :
Le ciment est l’élément incontournable de l’obturation canalaire : il va faire le lien entre le noyau de gutta percha et les parois dentinaires. En effet, il n’existe pas d’adhésion propre de la gutta percha aux parois dentinaires, c’est pour quoi le ciment de scellement endodontique joue un rôle d’interface entre ces deux éléments (35). Son rôle sera également d’assurer la lubrification du canal pour une mise en place optimale des cônes du Gutta-‐Percha (38).
Il viendra combler les espaces qui n’ont pas été préparés mécaniquement (tubuli dentinaires, canaux accessoires…) et empêchera le développement de micro-‐ organismes(9).