Intérêt de la déformation longitudinale globale du
ventricule gauche chez les patients atteints de sténose
aortique à bas débit et bas gradient avec basse
fraction d’éjection
Mémoire
Abdellaziz Dahou
Maîtrise en médecine expérimentale
Maître ès sciences (M.Sc.)
Québec, Canada
iii
Résumé
La sténose aortique est la valvulopathie la plus fréquente dans les pays industrialisés. Environ 5 à 10% des patients ayant une sténose aortique sévère présentent un état de bas débit cardiaque avec altération de la fraction d’éjection du ventricule gauche (FEVG). La présence d’un faible débit cardiaque s’accompagne souvent d’un bas gradient, ce qui peut fausser l’évaluation de la sévérité de la sténose et par conséquent conduire à une mauvaise décision thérapeutique. Deux principaux défis se posent chez ces patients. Le premier est de différentier une SA vraiment sévère d’une SA pseudo-sévère, c.à.d. un ventricule gauche défaillant qui est incapable d’ouvrir complètement une valve légèrement ou modérément sténosée. Cette distinction est cruciale car le remplacement valvulaire est bénéfique seulement dans le cas de SA vraiment sévère. Le deuxième défi est de quantifier précisément les dommages myocardiques. À cet effet, l’évaluation de la réserve contractile est importante car les patients qui n’ont pas ou peu de réserve contractile ont un haut risque de mortalité opératoire lors du remplacement valvulaire. Malheureusement, les paramètres traditionnels dérivés de l’échocardiographie de repos ou de stress qui sont utilisés pour évaluer la sévérité de la SA et la dysfonction du myocardique sont loin d’être optimaux. Par conséquent, la quantification de la sévérité de la maladie et la prise en charge thérapeutique peuvent ne pas être appropriées dans une proportion non négligeable de ces patients.
Le principal objectif de ce projet de maîtrise est de déterminer l’utilité de la déformation
longitudinale globale du ventricule gauche (DLG) mesurée au repos et lors d’une échocardiographie de stress à la dobutamine pour la stratification du risque et son impact sur le pronostic et la prise en charge des patients ayant une SA à bas débit et bas gradient (SABD) avec basse FEVG.
Notre hypothèse est la suivante: la DLG du ventricule gauche est supérieure à la FEVG pour prédire la mortalité chez les patients avec SABD et basse FEVG inclus dans l’étude TOPAS.
v
Summary
Aortic stenosis is the most common valvular heart disease in developed countries. Approximately, 5 to 10 % of patients with severe aortic stenosis have a low cardiac output with impaired left ventricular ejection fraction (LVEF). The presence of a low cardiac output can distort the assessment of the severity of the aortic stenosis and thus lead to non-adequate therapeutic decision. Two main challenges are posed by these patients. The first is to differentiate a truly severe AS from a pseudo-severe AS, i.e. a failing left ventricle unable to fully open valve slightly or moderately stenotic. This distinction is crucial because the aortic valve replacement will be beneficial only in the case of true-severe AS. The second challenge is to accurately quantify myocardial damage. To this effect, the contractile reserve is important to assess because patients who do not have contractile reserve have a high risk of operative mortality following AVR. Unfortunately, traditional parameters derived from rest or stress echocardiography that are used to assess the severity of AS and myocardial dysfunction are not adequate in low flow state. Therefore, quantification of the disease severity and the ensuing therapeutic management may not be appropriate in a large proportion of these patients.
The main objective of this project is to determine the usefulness of left ventricular longitudinal deformation measured at rest and during stress echocardiography with dobutamine for risk stratification and its impact on prognosis and management of patients with low-gradient aortic stenosis with impaired LVEF.
Our hypothesis is as follows: The left ventricular global longitudinal strain is superior to the LVEF to predict mortality in patients having LF-LG AS with low EF included in the TOPAS study.
vii
Table des Matières
Résumé………...iii
Summary………...v
Table des matières………...vii
Liste des tableaux………..ix
Liste des figures………...xi
Liste des abréviations………...xv
Dédicace………..……xvii
Avant-propos………...xix
Introduction………1
Chapitre 1 : Sténose aortique à bas débit-bas gradient avec basse fraction d’éjection………...3
1.1. Difficultés diagnostiques et défis………..4
1.1.1. Intérêt de l’échocardiographie de stress à la dobutamine………4
1.1.1.1. Reserve contractile ou réserve de flux………..5
1.1.1.2. Diagnostic de la sévérité de la sténose aortique………...8
1.1.1.3. Limitations de l’échocardiographie de stress à la dobutamine…...11
1.1.1.4. Intérêt de l’AVA projetée à un débit normal (250 mL/s)………...12
1.1.2. Intérêt de la tomographie axiale commandée par ordinateur…………....15
1.2. Pronostic des patients porteurs d’une sténose aortique à bas débit avec fraction d’éjection abaissée……….…24
1.3. Prise en charge thérapeutique………...30
1.4. Conclusion………..32
Chapitre 2 : Intérêt des paramètres de déformation myocardique du ventricule gauche dans l’évaluation de la fonction ventriculaire gauche chez les patients avec une sténose aortique……….33
2.1. Contexte………..34
2.2. Fonction longitudinale globale et déformation myocardique ou « strain »..………..34
2.3. Évaluation de la déformation myocardique par technique du Speckle tracking…….36
2.3.1. Concept et aspects techniques………36
2.3.2. Avantages………...39
2.3.3. Limitations……….39
2.4 Fonction longitudinale et fibrose myocardique ………..40
Hypothèses et objectifs………43
Chapitre 3 : Résultats : l’article………...45
3.1. Résumé.………...47 3.2. Abstract………...48 3.3. Introduction……….49 3.4. Methods………...50 3.4.1. Study protocol………....50 3.4.2. Clinical data………....50 3.4.3. Doppler-Echocardiography………....51 3.4.4. Statistical Analysis………...52 3.5. Results……….53
viii
3.5.1. Baseline patient characteristics………..53
3.5.2. Comparison of patient’s characteristics according to rest GLS………….53
3.5.3. Correlates of rest and stress GLS………...54
3.5.4. Survival according to rest GLS………..54
3.5.5. Survival according to stress GLS………...55
3.6. Discussion………...………...…...57
3.6.1. Prognostic value of rest GLS in low EF, LG AS………...57
3.6.2. Prognostic value of stress GLS in low EF, LG AS………58
3.6.3. Clinical implications………..60
3.6.4. Study limitations………61
3.7. Conclusion………..62
Chapitre 4 : Discussion………....73
4.1. Valeur pronostique de la DLG de repos dans la SABD avec basse FEVG…………74
4.2. Valeur pronostique de la DLG de stress dans la SABD avec basse FEVG…………75
4.3. Implications cliniques……….77
4.4. Limitations de l'étude………...78
Conclusion et perspectives……….….79
ix
Liste des tableaux
Chapitre 1
Tableau 1: Définition, prévalence et pronostic de la SAPS dans des séries de patients avec SA à bas débit avec basse FEVG.
Tableau 2:Précision de la calcification valvulaire aortique mesurée par tomographie pour identifier la sévérité de la sténose aortique
Chapitre 3
Table 1: Baseline Clinical and Doppler-Echocardiographic Characteristics of the Study Population According to Rest GLS
Table 2:Multivariable Analysis of the Effect of Rest and Stress Global Longitudinal Strain on All-Cause Mortality
xi
Liste des figures
Chapitre 1
Figure 1-1 : Intérêt de l’échocardiographie de stress à la dobutamine pour
l’évaluation des patients avec sténose aortique à bas-débit avec basse fraction d’éjection.
Figure 1-2 : Courbes de survie estimée par la méthode de Kaplan-Meier en fonction
du groupe et du type de traitement. Groupe I : patients ayant de la réserve flux; Groupe II : patients sans réserve flux.
Figure 1-3 : Fraction d’éjection du ventricule gauche avant et après remplacement
valvulaire aortique chez des patients avec et sans réserve de flux.
Figure 1-4 : Évolution de l’impact de la réserve de flux préopératoire sur le risque
de mortalité postopératoire selon le modèle de Gray.
Figure 1-5 : Évolution de l’aire valvulaire aortique en fonction du débit
transvalvulaire sous dobutamine de différents patients et Concept d’aire valvulaire aortique projetée à débit normal.
Figure 1-6 : Méthode de calcul de l’AVAproj.
Figure 1-7 : Comparaison des pourcentages de classification correcte observée avec
l’utilisation de différents critères pour distinguer les sténoses aortiques vraiment sévères des sténoses aortique pseudo-sévères, in vivo.
Figure 1-8 : Mesure de la calcification valvulaire aortique (flèche) par tomographie.
AV : valve aortique; AU : unité d’Agatston.
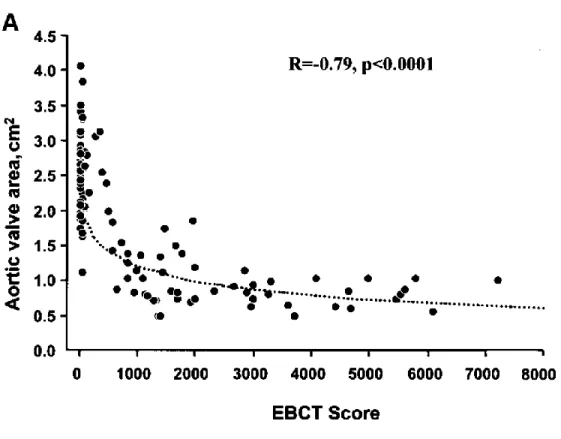
Figure 1-9: Corrélation entre le score calcique mesuré par tomographie à faisceau
d’électron (EBCT) et la mesure par échocardiographie de l’aire valvulaire aortique.
Figure 1-10 : Courbe de ROC pour un diagnostic de sténose aortique sévère (AVA<1
cm2) utilisant le score calcique mesuré par tomographie.
Figure 1-11 : Corrélations entre la calcification de la valve aortique mesurée par
tomographie axiale assistée par ordinateur et les paramètres hémodynamiques de la sténose aortique mesurés par écho-Doppler cardiaque.
xii
Figure 1-13 : Courbe de ROC pour le diagnostic de la sténose aortique sévère en fonction (A) de l’aire valvulaire aortique (<1cm2), (B) de l’aire valvulaire indexée à la surface corporelle (<0,6cm2/m2), (C) du gradient transvalvulaire moyen (>40mmHg) et (D) de la vélocité aortique maximale (>4m/s) utilisant la calcification valvulaire aortique mesurée par tomographie axiale.
Figure 1-14 : Algorithme décisionnel pour la prise en charge diagnostique et thérapeutique des patients avec SABD et basse FEVG.
Figure 1-15: Impact du Duke Activity Status Index (DASI, panel A), test de marche
de 6-minutes (6-MWT, Panel B), FEVG sous dobutamine (Panel C), et de l’AVAproj (Panel D) sur la survie.
Figure 1-16 : Courbes de survie de Kaplan-Meier selon les valeurs de base de BNP
<550 ou ≥550 pg/mL (Panel A) pour la population entière de l'étude, (Panel B) pour les patients traités médicalement, (Panel C) pour les patients traités chirurgicalement et (Panel D) pour la population entière de l’étude en fonction de la réserve de flux définie par une augmentation du volume d'éjection systolique ≥20% sous dobutamine.
Figure 1-17 : Survie des patients porteurs d’une sténose aortique à bas débit-bas
gradient et FEVG abaissée, en fonction du gradient transvalvulaire moyen. (Panel A) Chez des patients ayant subi un remplacement valvulaire aortique (n=180); (Panel B) Chez des patients sans réserve de flux (n=81).
Figure 1-18 : Risque relatif de mortalité à court terme en fonction de la
disproportion patient-prothèse et de la fraction d’éjection du ventricule gauche préopératoire.
Figure 1-19 : Effet de la fonction ventriculaire gauche préopératoire et de la DPP
sur l'incidence cumulée de symptômes, d'insuffisance cardiaque ou de décès liés à une insuffisance cardiaque, 3 ans après un remplacement valvulaire aortique.
Figure 1-20 : Survie brute (Panel A) et ajustée (Panel B) après remplacement
valvulaire aortique, selon la dysfonction ventriculaire gauche et la disproportion patient-prothèse.
Figure 1-21 : Indications pour le remplacement valvulaire aortique chez les patients
avec sténose aortique.
Chapitre 2
Figure 2-1: Supériorité du raccourcissement longitudinal sur la fraction d’éjection
du ventricule gauche (LVEF) pour identifier la dysfonction systolique du myocarde dans la sténose aortique.
xiii
Figure 2-3: le strain mesure la déformation du tissu qui est définie comme le
changement de dimension ou longueur (L1−L0) normalisé par rapport à la longueur initiale (L0) de la région d’intérêt. La vitesse à laquelle se changement se fait est le strain rate.
Figure 2-4: Procédure de mesure et présentation du strain 2D par technique du
Speckle tracking
Figure 2-5: Déplacement de l’anneau mitral en échocardiographie avec le mode M
dans différents groupes de patients selon la sévérité de la fibrose myocardique (sur les biopsies faites lors du remplacement valvulaire aortique.
Figure 2-6 : Corrélation inverse entre l’étendu de la fibrose myocardique sur les
biopsies et le déplacement de l’anneau mitral en échocardiographie avec le mode M.
Chapitre 4
Figure 1: Flow Chart of the Study Population
Figure 2: Correlation between Rest and Stress Global Longitudinal Strain.
Figure 3: All-cause Mortality According to Rest Global Longitudinal Strain and Type
of Treatment. Panel A shows the survival in patients with GLS>|9|% versus those with GLS<|9|% and Panel B the survival in these groups after further dichotomization for the type of treatment (i.e. AVR vs. Conservative: i.e. no AVR).
Figure 4: Impact of Stress Global Longitudinal Strain on All-causes Mortality. Panel
A shows the survival in patients with Stress GLS>|10.5|% versus those with Stress GLS<|10.5|% and Panel B the survival in these groups of patients after further dichotomization for the type of treatment (i.e. AVR vs. Conservative).
xv
Liste des abréviations et des sigles
AVA : Aire Valvulaire Aortique
AVAproj : Aire Valvulaire Aortique Projetée à débit normal AVC : Calcification de la Valve Aortique
BD : Bas Débit
BNP : Peptide Natriurétique de type B DLG : Déformation Longitudinale Globale DPP : Disproportion Patient-Prothèse ΔP : Gradient de Pression
ESD : Échocardiographie de Stress à la Dobutamine FEVG : Fraction d’Éjection du Ventricule Gauche MG : Gradient Moyen
PAC : Pontage Aorto-Coronarien Q : Débit transvalvulaire moyen
RVA : Remplacement Valvulaire Aortique SA : Sténose Aortique
SABD : Sténose Aortique à Bas Débit SAVS : Sténose Aortique Vraiment Sévère SAPS : Sténose Aortique Pseudo-Sévère
TACO : Tomographie Axiale Commandée par Ordinateur TAVI : Implantation Transcathéter de Valve Aortique VA : Valve aortique
VES : Volume d’Éjection Systolique VG : Ventricule Gauche
xvi
AS: Aortic Stenosis AVA: Aortic Valve Area
AVAproj: Projected Aortic Valve Area at a normal transvalvular flow rate AVC: Aortic Valve Calcification
AVR: Aortic Valve Replacement BNP: B-type Natriuretic Peptide CAD: Coronary Artery Disease
COPD: Chronic obstructive Pulmonary Disease DASI: Duke Activity Status Index
DSE: Dobutamine Stress Echocardiography GLS: Global Longitudinal Strain
ΔP: Gradient LF: Low Flow LG: Low Gradient LV: Left Ventricle
LVEF: Left Ventricular Ejection Fraction MG: Mean Gradient
NYHA: New-York Heart Association PPM: Patient-Prosthesis Mismatch ROC: Receiver operating characteristic SV: Stroke Volume
TAVI: Transcatheter Aortic Valve Implantation TOPAS: True Or Pseudo Severe Aortic Stenosis
xvii À mes chers parents pour leur aide
et leur soutien depuis toujours; À ma chère épouse Rihab et mon fils Yacine
pour leur accompagnement et les bons moment passés ensembles;
xix
Avant-propos
Après avoir terminé ma spécialité en France et exercer la cardiologie à temps plein pendant deux ans, j’ai senti le besoin d’avoir des outils qui me permettraient de rapporter des cas ou de séries de cas intrigants ou qui sortaient de l’ordinaire. L’idée de faire une maitrise était exotique mais il m’a fallu beaucoup de courage pour laisser la clinque et replonger dans les cours. Ce parcours était très enrichissant pour moi, à la fois sur le plan scientifique et sur le plan relationnel.
J’aimerais tout d’abord à remercier mon directeur de maitrise le Professeur Philippe
Pibarot qui m’a accueilli chaleureusement dans son laboratoire et m’a aider tout au long
de mon cheminement pour la réalisation de ce travail et d’autres. Sa modestie, son écoute, son optimisme et ses compétences font de lui un directeur et une personne exceptionnels. Un grand merci du fond du cœur pour tout.
Je remercie également mon co-directeur le Dr Josep Rodés-Cabau de m’avoir donnée l’occasion d’assister aux procédures de remplacement valvulaires aortique par voie percutanée et de travailler sur les régurgitations périprothétiques avec son équipe.
Un grand merci à Marie-Annick Clavel et Romain Capoulade pour leur accueil à mon arrivée au laboratoire et pour leur aide précieuse, notamment pour monter la base de données ainsi que pour me familiariser avec les statistiques.
Merci à Isabelle Fortin, Jocelyn Beauchemin, Jacinthe Aubé, Martine Parent,
Martine Poulin et Yvette Parent pour leur aide de loin ou de près tout au long de la
1
Introduction
La sténose aortique (SA) est la pathologie valvulaire la plus fréquente dans les pays industrialisés1-3. La SA à bas débit et bas gradient (SABD) avec diminution de la fraction d’éjection du ventricule gauche (FEVG) peut être rencontrée chez 5-10% des patients avec SA sévère 4, 5. Elle est définie par la combinaison d’une aire valvulaire aortique (AVA) compatible avec une sténose sévère (AVA≤1.0 cm2 ou AVA indexée ≤0.6 cm2/m2), un gradient transvalvulaire aortique moyen bas (<40 mmHg) et une FEVG diminuée (<50 %), avec un état de bas débit (volume d’éjection systolique indexé <35 mL/m2 ou index cardiaque <3.0 L/min/m2) 6-9. Cette situation de bas débit peut être le résultat de la SA elle-même, situation dans laquelle la baisse de la FEVG serait : i) la conséquence de la charge hémodynamique (« afterload mismatch ») exercée par la valve aortique sévèrement sténosée sur le VG 10, ou ii) la conséquence d’une cardiomyopathie d’origine ischémique ou non ischémique concomitante à une sténose aortique. Le défi majeur dans cette condition est de faire la distinction entre une SA vraiment sévère (SAVS) qui est donc responsable au moins en partie de la baisse de la fraction d’éjection et du bas débit cardiaque, d’une SA légère ou modérée dite SA pseudo-sévère (SAPS) concomitante à une cardiomyopathie sous-jacente responsable du bas débit. Cette distinction est cruciale à la fois pour le pronostic et la prise en charge thérapeutique. Les patients avec SAVS vont bénéficier du remplacement valvulaire aortique (RVA) alors que ceux avec SAPS ne vont pas en bénéficier. Le pronostic des patients avec SAVS est médiocre en l’absence de RVA avec un taux de survie inférieur à 50% à 3 ans, et le bénéfice du RVA -même s’il permet d’améliorer la survie chez ces patients- demeure limité par une mortalité péri-opératoire élevée, allant de 6 à 33% dépendamment de la présence ou l’absence de réserve contractile et des comorbidités associées 4, 6, 11-20. En particulier, une grande proportion (46-79%) des patients avec SABD et basse FEVG ont une maladie coronaire concomitante qui pourrait avoir un impact négatif sur le pronostic indépendamment de la sévérité de la SA 4, 6, 20. Il est donc nécessaire de préciser à la fois sévérité de la SA et celle de l’atteinte myocardique pour mieux stratifier le risque et guider le traitement.
3
Chapitre 1
La sténose aortique à bas débit-bas gradient avec basse
4
1.1. Difficultés diagnostiques et défis
Dans le cas d’une basse fraction d’éjection avec bas débit cardiaque, les forces appliquées sur les feuillets de la valve aortique peuvent ne pas être suffisantes pour ouvrir complètement la valve conduisant à une sous-estimation de l’AVA effective calculée en écho-Doppler et par conséquent une surestimation de la sévérité de la sténose aortique. De l’autre côté, le gradient transvalvulaire est diminué, entrainant une sous-estimation de la sévérité de la sténose. Du fait de cette discordance AVA-gradient, le recours à d’autres tests diagnostiques en plus de l’échocardiographie Doppler de repos est nécessaire. Il s’agit essentiellement de l’échocardiographie de stress et la tomographie axiale assistée par ordinateur.
1.1.1. Intérêt de l’échocardiographie de stress à la dobutamine
Depuis sa première description par deFilippi et al. en 1995 21, plusieurs études ont démontré que l’échocardiographie de stress à la dobutamine (ESD) à faible dose (5-20µg/kg/min) est utile pour déterminer la réserve contractile (ou réserve de flux) la stratification du risque opératoire, ainsi que pour distinguer une SAVS d’une SAPS 22, 23, (Figure 1-1).
5
Figure 1-1 : Intérêt de l’échocardiographie de stress à la dobutamine pour l’évaluation des patients avec sténose aortique à bas débit-bas gradient avec basse fraction d’éjection. Reproduit avec permission d’après 22, 23.
1.1.1.1. Reserve contractile ou réserve de flux
La réserve contractile a été traditionnellement définie par une augmentation du volume d’éjection du VG (VE) > 20% sous dobutamine 24. Cependant, les guides de pratique récents de l’ESC_EACTS et ACC-AHA suggèrent d’utiliser le terme de réserve de flux plutôt que réserve contractile. En effet, l’augmentation du volume d’éjection sous dobutamine peut être influencée par plusieurs autres facteurs que la réserve contractile comme telle. Approximativement un tiers des patients avec SABD et basse FEVG 6, 21,
25-27 n’ont pas de réserve de flux et ces patients ont, en général, une prévalence plus élevée
de maladie coronarienne 6. Ces patients sans réserve de flux ont une mortalité opératoire beaucoup plus élevée (22-33%) comparativement à ceux qui ont une réserve (5-8%), (Figure 1-2) 6, 28.
6
Figure 1-2 : Courbes de survie estimée par la méthode de Kaplan-Meier en fonction du groupe et du type de traitement. Groupe I : patients ayant de la réserve flux; Groupe II : patients sans réserve flux. Reproduit avec permission d’après 6.
Plusieurs mécanismes non nécessairement reliés à une atteinte intrinsèque de la contractilité du VG pourraient contribuer à l’absence d’augmentation du VE sous dobutamine incluant : 1) « afterload mismatch » ou phénomène de désadaptation à la charge due à un déséquilibre entre la sévérité de la SA et la réserve du myocarde ventriculaire gauche 10; 2) augmentation inadéquate du flux sanguin myocardique liée à une maladie coronaire associée; 3) l’existante de dommages myocardiques irréversibles dus à un infarctus du myocarde ou une fibrose myocardique extensive; 4) la présence d’un asynchronisme de contraction VG 29; 5) la tachycardie et la limitation du remplissage diastolique; 6) la majoration de l’insuffisance mitrale.
Cependant, il est très important de souligner que la présence/absence de réserve contractile n ne permet pas de prédire la récupération de la fonction VG ou le devenir à long terme des patients après RVA. En effet, l’évolution de la FEVG après RVA est
7 similaire quel que soit le statut de la réserve contractile en préopératoire (Figure 1-3)16. Quant à la survie à long terme, dans cette
Figure 1-3: Fraction d’éjection du ventricule gauche avant et après remplacement valvulaire aortique chez des patients avec (Group I) et sans (Group II) réserve de flux. Reproduit avec permission d’après 16.
même étude, les taux de survie à 2 ans chez les patients ayant survécus à la chirurgie sont similaires dans le groupe de patients avec réserve contractile comparativement au groupe de patients sans réserve contractile (92±7 vs. 90±5 %; p=0.63) 16. Une autre étude faite par le même groupe montre que l’impact de la réserve contractile n’est pas constant au fil du temps et semble beaucoup plus marqué pendant la période péri-opératoire et post-opératoire précoce. L’effet de ce facteur devient non significatif après 10 mois post RVA (Figure 1-4) 30.
8
Figure 1-4 : Évolution de l’impact de la réserve de flux préopératoire sur le risque de mortalité postopératoire selon le modèle de Gray. La ligne continue représente l'évolution du rapport de côte de mortalité dans le temps et les lignes en pointillés l’intervalle de confiance à 95%. Reproduit avec permission d’après 30.
1.1.1.2. Diagnostic de la sévérité de la SA : Distinction entre SAVS et SAPS
Comme mentionné précédemment, la distinction entre ces deux situations est cruciale pour la décision clinique chez un patient donné. Elle est essentiellement basée sur les changements de l’AVA et des gradients transvalvulaires durant l’ESD (Figure 1-1). Typiquement, la SAPS est caractérisée par une augmentation de l’AVA et une augmentation faible ou absente des gradients en réponse à l’augmentation du débit. À l’opposé, la SAVS est caractérisée par l’absence ou une faible augmentation de l’AVA et une augmentation congruente des gradients en réponse à l’augmentation du débit.
9 Plusieurs paramètres et critères ont été proposés dans la littérature pour identifier les patients avec SAPS durant l’ESD incluant : un gradient transvalvulaire moyen sous dobutamine ≤30 ou <40mmHg dépendamment des études, une AVA sous dobutamine >1.0 ou 1.2 cm2 et/ou une augmentation absolue de l’AVA ≥0.3 cm2 (Tableau 1) 6, 11, 21
27, 31. La prévalence de la SAPS est de l’ordre de 20 à 30% parmi les patients avec SABD
10
Auteur - Année
Critères d’inclusion pour la sténose aortique à bas débit
Méthode de stress
Critère pour la sténose aortique pseudo-sévère
Prévalence Suivi Taux de mortalité (SAPS) Références deFilippi 1995 FEVG≤45%, GM≤30mmHg, AVAI≤0.5cm2/m2 ESD jusqu’à 20 μg/kg/min ΔWMSI>20% et ΔAVA≥0.3 cm2 5/18 (28%) 12 mo. 20% 21 Schwammenthal 2001 FEVG≤40%, GM≤40mmHg, AVA≤1cm2 ESD jusqu’à 20 μg/kg/min ΔAVA≥0.3 cm2, AVA au pic de l’ESD>1cm2 8/24 (30%) 14 mo. 25% 11 Nishimura 2002 FEVG≤40%, GM≤40mmHg, AVA≤1cm2 ESD jusqu’à 40 μg/kg/min AVA au pic de l’ESD≥1.2 cm2, GM au pic de l’ESD<30mmHg 7/32 (22%) 32 mo. 57% 27 Monin 2003 IC≤3.0L/min/m2, AVA≤1cm2, GM≤40mmHg ESD jusqu’à 20 μg/kg/min ΔAVA≥0.3 cm2, AVA au pic de l’ESD>1cm2 7/136 (5%) 19 mo. 50% 6 Zuppiroli 2003 FEVG≤40%, GM≤30mmHg, AVA≤1cm2 ESD jusqu’à 20 μg/kg/min ΔAVA≥0.25 cm2 10/48 (21%) 24 mo. 70% 31 Blais 2006 FEVG≤40%, GM≤40mmHg, AVA≤1.2cm2 ESD jusqu’à 20 μg/kg/min AVAproj>1cm2, AVAIproj>0.55cm2 8/23 (35%) - - 32
Tableau 1 : Définition, prévalence et pronostic de la SAPS dans des séries de patients avec SA à bas débit avec basse FEVG.
AVA : Aire valvulaire aortique; AVAproj: Aire valvulaire aortique projetée à débit normal; AVAIproj: AVAproj indexée pour la surface corporelle du patient; ESD : Échocardiographie de stress à la dobutamine; FEVG : Fraction d’éjection du ventricule gauche; GM : Gradient moyen; IC : Index cardiaque; ΔAVA : Augmentation de l’AVA sous dobutamine; ΔWMSI : Augmentation de l’index du score de mouvement de la paroi du ventricule gauche sous dobutamine.
11 1.1.1.3. Limitations de l’ESD
L’ESD présente certaines limitations. Une de ces limitations majeures est due au fait que l’augmentation du débit transvalvulaire sous dobutamine est différente d’un patient à l’autre. Or tous les indices de sévérité de la sténose aortique (AVA, gradient, ratio de vélocités etc.) sont dépendants du débit. Par conséquent, l’interprétation des changements de ces paramètres dans des conditions de débit variable peut être problématique. Pour s’affranchir de cette limitation, un nouveau paramètre dérivé des mesures réalisées lors de l’ESD a été proposé par les investigateurs de l’étude TOPAS : il s’agit de l’AVA projetée (AVAproj) à un débit normal de 250ml/s (Figure 1-5) 25, 32. Cette valeur de 250 ml/s a été choisie car elle correspond à la valeur médiane du débit transvalvulaire chez les patients ayant une SA et une fonction ventriculaire gauche normale.
Figure 1-5 : Évolution de l’aire valvulaire aortique en fonction du débit transvalvulaire sous dobutamine de différents patients et Concept d’aire valvulaire aortique projetée à débit normal. Reproduit avec permission d’après 32.
12
1.1.1.4. Intérêt de l’AVA projetée à un débit normal (250ml/s)
Le calcul de l’AVAproj est particulièrement utile en cas de persistance de la discordance AVA-gradient transvalvulaire sous dobutamine. Cette situation peut être rencontrée lorsque le débit transvalvulaire reste bas malgré une stimulation par dobutamine (Patients #1 et #5 dans la Figure 1-5) ou plus rarement lorsqu’il devient supra-physiologique sous dobutamine (Patient #3 dans la Figure 1-5).
Blais et al. 32 ont proposé en 2006 d’utiliser l’AVA projetée à débit normal pour l’évaluation de la sévérité de la SA chez les patients atteints de SABD avec basse FEVG en tenant compte des changements relatifs du débit transvalvulaire sous dobutamine. Durant une infusion graduelle de faibles doses de dobutamine (2.5 à 20 µg/kg/min), l’AVA est calculée par équation de continuité34 à chaque stade de dobutamine et exprimée en fonction du débit transvalvulaire moyen (Q= volume d’éjection / temps d’éjection systolique) (Figure 1-6).
Figure 1-6 : Méthode de calcul de l’AVA projetée. ESD : échocardiographie de stress à la dobutamine. Reproduit avec permission d’après 32.
13 La pente de la droite de régression entre l’AVA et le débit transvalvulaire correspond à la «compliance valvulaire» (CV) et représente le degré de dépendance de l’AVA par rapport au débit. L’AVAproj est calculée à partir de la CV et des AVA et débit de repos en utilisant l’équation de régression :
AVAproj=AVArepos + CV (250-Qrepos)
Où AVArepos et Qrepos sont l’AVA et le Q au repos.
Dans cette étude, l’AVA projetée à un débit standardisé de 250 ml/s a démontré sa supériorité par rapports aux indices classiques de sévérité de la SA, pour la distinction entre la SAVS et la SAPS (Figure 1-7)32.
Figure 1-7 : Comparaison des pourcentages de classification correcte observée avec l’utilisation de différents critères pour distinguer les sténoses aortiques vraiment sévères des sténoses aortique pseudo-sévères, in vivo. Reproduit avec permission d’après 32.
14
Ces données ont été validé à la fois in vitro sur des valves artificielles et in vivo sur des patients atteints de SABD avec basse FEVG inclus dans l’étude TOPAS. L’AVAproj était plus étroitement corrélée à la sévérité de la sténose, la réserve de flux VG ainsi que la survie des patients comparativement aux indices classiques de sévérité de la SA32. La classification correcte du degré de sévérité de la SA chez les patients inclus dans cette étude était de 83% avec l’AVAproj (<1cm2), 91% avec l’AVAproj indexée (<0.55 cm2/m2) alors qu’elle n’était que de 65% en se basant sur l’AVA maximale mesurée sous dobutamine (AVA<1.0 cm2), 61 % pour une augmentation de l’AVA sous dobutamine (ΔAVA<0.30 cm2) et 74% pour un gradient moyen maximal sous dobutamine>30 mmHg (Figure 1-7).
En 2010, Clavel et al.25 ont proposé une méthode simplifiée pour le calcul de l’AVAproj. Dans cette méthode la compliance valvulaire CV est calculée de la façon suivante :
CV=∆AVA/∆Q où ΔAVA et ΔQ sont les augmentations absolues de AVA et Q durant
l’ESD. Il y avait une forte corrélation entre l’AVAproj calculée par la méthode simplifiée et la méthode originale (r=0.95; p<0.0001). Les 2 méthodes ont montré une performance similaire dans la différentiation des SAVS et SAPS (pourcentage de classifications correctes [%CC] pour une AVAproj≤1cm2: 94 et 92% respectivement) et cette performance était supérieure à celle des indices d’ESD conventionnels (%CC: 60-77%). Classiquement, les patients sans réserve de flux n’augmentent pas suffisamment leur volume d’éjection sous dobutamine et par conséquent l’AVA et les gradients peuvent rester inchangés par rapport aux mesures de repos. Dans ce cas, la distinction entre les SAVS et les SAPS est impossible (Figure 1). Cependant, certains de ces patients peuvent tout de même augmenter leur débit transvalvulaire suffisamment pour permettre de calculer l’AVAproj; cette augmentation de débit malgré une absence d’augmentation du volume d’éjection est due au raccourcissement du temps d’éjection systolique en rapport avec l’augmentation de la fréquence cardiaque 25, 32. Il reste néanmoins entre 10 et 20% des patients chez qui l’augmentation du flux reste insuffisante pour permettre de calculer l’AVAproj 25, 32. Dans ces cas ainsi que dans les cas où les résultats de l’ESD sont ambigus, d’autres méthodes s’avèrent nécessaires pour distinguer les SAVS des SAPS.
15 La tomographie axiale assistée par ordinateur (TACO) peut être particulièrement utile dans cette situation (Figure 1-8).
Figure 1-8 : Mesure de la calcification valvulaire aortique (flèche) par tomographie. AV : valve aortique; AU : unité d’Agatston.
1.1.2. Intérêt de la Tomographie Axiale Commandée par Ordinateur
Des études ont montré que le degré de la calcification valvulaire évaluée par échocardiographie est un puissant prédicteur de la survenue d’événements cardiaques
16
chez les patients asymptomatiques ayant une SA sévère 35. Cependant, l’évaluation semi-quantitative visuelle des calcifications par échocardiographie est dépendant des réglages de l’appareil et a une reproductibilité inter- et intra- observateur modeste. En 2004, Messika-Zeitoun et al.36 ont montré que la tomographie à faisceau d’électron est une méthode de mesure fiable de la calcification de la valve aortique. De plus, la quantité de calcium valvulaire était fortement et inversement corrélée à l’aire valvulaire mesurée au repos (Figure 1-9) et permet donc de quantifier la sévérité de la SA (Figure 1-10). Les auteurs de cette étude suggèrent que cette mesure de la calcification de la valve aortique, non dépendante du débit, pourrait être particulièrement utile dans la sténose aortique à bas débit. Cependant, dans cette étude, il n’y avait pas ou très peu de patients avec une fraction d’éjection inférieure à 50%.
Figure 1-9: Corrélation entre le score calcique mesuré par tomographie à fasiceau d’électron (EBCT) et la mesure par échocardiographie de l’aire valvulaire aortique. Reproduit avec permission d’après 36.
17
Figure 1-10 :Courbe de ROC pour un diagnostic de sténose aortique sévère (AVA<1 cm2) utilisant le score calcique) mesuré par tomographie. AUC=aire sous la courbe. Les flèches indiquent les seuils avec sensibilité maximale (score de 500), meilleur ratio sensibilité-spécificité (score de 1100) et spécificité maximale (score du 2000). Reproduit avec permission d’après 36.
Plus récemment, la même équipe a montré dans une autre étude utilisant la TACO que la calcification valvulaire aortique mesurée par tomographie était bien corrélée aux paramètres hémodynamiques de sévérité de la SA (Figure 1-11) 37. Avec cette modalité d’imagerie, le meilleur seuil pour identifier une sténose sévère est un score > 1650 AU. Cette cohorte incluait 179 patients avec FEVG >40% et 49 patients avec FEVG ≤40%, parmi lesquels, seulement 20 patients avaient une SABD (Figure 1-12).
18
Figure 1-11 : Corrélations entre la calcification de la valve aortique mesurée par tomographie axiale assistée par ordinateur et les paramètres hémodynamique de la sténose aortique mesurés par écho-Doppler cardiaque. Reproduit avec permission d’après 37.
19
Figure 1-12 : Diagramme des patients avec une fraction d’éjection inférieure à 40%. AVA: aire valvulaire aortique; AS : sténose aortique; MG : gradient moyen. Reproduit avec permission d’après 37.
20
Dans cette étude, un score de calcification valvulaire >1650 AU permettait d’identifier les SA hémodynamiquement sévères (Figure 1- 13), avec une sensibilité de 82%, et une spécificité de 80% dans le sous-groupe de 179 patients avec FEVG>40%.
Figure 1-13: Courbe de ROC pour le diagnostic de la sténose aortique sévère en fonction (A) de l’aire valvulaire aortique (<1cm2), (B) de l’aire valvulaire indexée à la surface corporelle (<0,6cm2/m2), (C) du gradient transvalvulaire moyen (>40mmHg) et (D) de la vélocité aortique maximale (>4m/s) utilisant la calcification valvulaire aortique mesurée par tomographie axiale. AUC : aire sous la courbe. Les flèches indiquent les seuils offrant le meilleur ratio sensibilité-spécificité. Reproduit avec permission d’après 37.
21 Le même seuil (1650 AU) a été testé dans le sous-groupe de patients ayant une SABD avec une FEVG diminuée donnant une sensibilité de 95%, une spécificité de 89%, une valeur prédictive négative de 80% et une valeur prédictive positive de 97% pour déterminer la sévérité de la SA.
Cependant, des études plus récentes suggèrent d’utiliser des seuils plus bas de score calcique chez les femmes que chez les hommes pour identifier la sténose sévère 38, 39. Cette différence selon le sexe persiste même après indexation du score calcique par la taille de l’anneau aortique (c.a.d densité calcique) (Tableau 2) 39.
Cette étude suggère qu’un seuil de l’ordre de 1200 AU pour les femmes et 2000 AU pour les hommes s’avère le plus précis pour identifier une sténose sévère. L’évaluation de la CVAT apparait donc comme un outil diagnostic particulièrement utile dans les situations où la sévérité de la SA reste difficile à déterminer après avoir effectué une ESD ou dans les cas où celle-ci ne peut être réalisée (Figure 1-14).
22
Sexe AUC Seuil Sensibilité (%) Spécificité (%) VPP (%) PVN (%)
CVA
Femme 0.91
Seuil spécifique 1681AU 69 95 95 65
Meilleur seuil 1274AU 86 89 93 79
Seuil sensible 791AU 95 63 81 88
Homme 0.90
Seuil spécifique 3381AU 59 95 95 59
Meilleur seuil 2065AU 89 80 88 82
Seuil sensible 1661AU 95 70 84 90
CVAi
Femme 0.91
Seuil spécifique 1071AU/m2 59 95 96 59
Meilleur seuil 637AU/m2 91 85 91 85
Seuil sensible 476AU/m2 95 69 84 89
Homme 0.89
Seuil spécifique 1733AU/m2 55 95 95 57
Meilleur seuil 1067AU/m2 86 79 87 77
Seuil sensible 776AU/m2 95 61 80 88
CVAd
Femme 0.93
Seuil spécifique 580AU/cm2 73 95 96 68
Meilleur seuil 292AU/cm2 92 81 87 86
Seuil sensible 228AU/cm2 95 68 83 89
Homme 0.92
Seuil spécifique 727AU/cm2 65 95 95 63
Meilleur seuil 476AU/cm2 90 80 88 82
Seuil sensible 402AU/cm2 95 70 84 90
Tableau 2 : Précision de la calcification valvulaire aortique pour identifier la sévérité de la sténose aortique 39. AUC= aire sous la courbe; VPP=valeur prédictive positive; VPN=valeur prédictive négative; CVA=calcification valvulaire aortique; CVAi=calcification valvulaire aortique indexée par la surface corporelle; CVAd= densité de calcification : c.a.d. calcification valvulaire aortique indexée par la surface de section de l’anneau aortique. Reproduit avec permission d’après39.
23
Figure 1-14 : Algorithme décisionnel pour la prise en charge diagnostique et thérapeutique des patients avec SABD et basse FEVG. VAo: valve aortique; AVA: aire valvulaire aortique; AVA projetée: aire valvulaire aortique projetée à un débit normal (250 ml/s); ΔP: gradient transvalvulaire moyen; TACO: tomographie axiale assistée par ordinateur; SA sténose aortique; VE: volume d’éjection; RVAC: replacement valvulaire aortique chirurgical; PAC : pontage aortocoronarien; TAVI: replacement valvulaire aortique transcathéter; IC : insuffisance cardiaque. Adapté à partir de : « Dynamic echocardiography », Chapitre 119, A. Dahou, P. Pibarot et JG. Dumesnil; sous presse.
24
1.2. Pronostic des patients porteurs d’une sténose aortique à bas débit
avec fraction d’éjection abaissée
Le pronostic de ces patients en l’absence de RVA est médiocre avec un taux de survie<50% à 3 ans, et la mortalité péri-opératoire en cas de RVA est élevée, allant de 6 à 33% dépendamment de la présence ou l’absence de réserve contractile (ou réserve de flux) et des comorbidités associées 4, 6, 11-20
Dans le groupe de patients traités médicalement, les facteurs de risque de morbidité et de mortalité identifiés dans des études antérieures sont : une capacité fonctionnelle réduite (Duke Activity Status Index <20 ou test de marche de 6-min <320m), présence de maladie coronaire, sévérité de la SA mesurée par l’AVA projetée (<1.2 cm2), et FEVG sous stress dobutamine <35% 12, 20, 25, 33 (Figure 1-15).
Figure 1-15 : Impact du Duke Activity Status Index (DASI, Panel A), du test de marche de 6-minutes (6-MWT, Panel B), de la FEVG sous dobutamine (Panel C), et de l’AVAproj (Panel D) sur la survie. LVEF peak : fraction d’éjection du ventricule gauche à la dose maximal de dobutamine, AVAproj : aire valvulaire aortique projetée. Reproduit avec permission d’après 12.
25 Un taux plasmatique élevé (>550 pg/ml) de peptide natriurétique de type B (BNP) apparait comme un puissant prédicteur de mortalité chez les patients avec SABD, quel que soit le type de traitement (médical ou chirurgical), indépendamment de la présence/absence de réserve de flux17 (Figure 1-16).
Figure 1-16 : Courbes de survie de Kaplan-Meier selon les valeurs de base de BNP <550 ou ≥550 pg/mL (Panel A) pour la population entière de l'étude, (Panel B) pour les patients traités médicalement, (Panel C) pour les patients traités chirurgicalement et (Panel D) pour la population entière de l’étude en fonction de la réserve de flux définie par une augmentation du volume d'éjection systolique ≥20% sous dobutamine. Reproduit avec permission d’après17.
26
Quant aux patients traités chirurgicalement (remplacement valvulaire aortique : RVA), les facteurs de risque de mortalité péri-opératoire les plus puissants sont : l’absence de réserve de flux (Figure 1-2, Chapitre 1), un gradient transvalvulaire aortique moyen bas (<20 mmHg ou <30 mmHg selon les études) (Figure 1-17), la présence de maladie coronarienne multi-tronculaire et la disproportion patient-prothèse (DPP) (Figure 1-18)
4-6, 19, 20, 40.
Figure 1-17 : Survie des patients porteurs d’une sténose aortique à bas débit et bas gradient et FEVG abaissée, en fonction du gradient transvalvulaire moyen (MG). (Panel A) Chez des patients ayant subi un remplacement valvulaire aortique (n=180)4 (Panel B) Chez des patients sans réserve de flux (n=81. Reproduit avec permission d’après 20.
27
Figure 1-18 : Risque relatif de mortalité à court terme en fonction de la disproportion patient-prothèse et de la fraction d’éjection du ventricule gauche (LVEF)
28
Les prédicteurs de mortalité à long terme après RVA dans cette population sont : un EuroSCORE élevé, un antécédent de fibrillation atriale, une maladie coronarienne multi-tronculaire, un gradient transvalvulaire moyen préopératoire bas, un taux de BNP élevé et la présence de DPP (Figure 1-19 et 1-20) 5, 6, 19. Certaines études ont rapporté qu’un pontage aortocoronarien concomitant au RVA avait un impact favorable sur le pronostic
12, 18. Le degré de viabilité myocardique et l'étendue de la fibrose myocardique avaient
aussi un impact sur le pronostic 41-43.
Figure 1-19 : Effet de la fonction ventriculaire gauche préopératoire et de la disproportion patient-prothèse (PPM) sur l'incidence cumulée de symptômes,
d'insuffisance cardiaque ou de décès liés à une insuffisance cardiaque, 3 ans après un remplacement valvulaire aortique. Reproduit avec permission d’après 44.
29
Figure 1-20 : Survie brute (Panel A) et ajustée (Panel B) après remplacement valvulaire aortique, selon la dysfonction ventriculaire gauche et la disproportion patient-prothèse. Reproduit avec permission d’après 44.
30
1.3. Prise en charge thérapeutique
Selon les guides de pratique, le RVA est indiqué chez les patients présentant une sténose aortique sévère (AVA<1 cm2 ou < 0.6 cm2/m2, gradient moyen >40 mmHg, Vmax>4 m/s) causant des symptômes (angine de poitrine, syncope, dyspnée ou insuffisance cardiaque) ou une diminution de la FEVG (< 50 %) 22, 45. Le rôle du RVA chez les patients avec SABD et basse FEVG a été plus controversé. Les anciennes recommandations de l’ACC/AHA 23 ne fournissaient aucune recommandation spécifique pour le traitement de ces patients, alors que les recommandations de l’ESC/EACT 22 recommandent le RVA (classe IIa, niveau d’évidence C) dans le sous-groupe de patients avec réserve de flux ayant une évidence de sténose sévère. La recommandation est de niveau IIb pour les patients n’ayant pas de réserve de flux. Cependant, les nouvelles recommandations de l’ACC/AHA 45 recommandent le RVA (classe IIa, niveau d’évidence B) dans le sous-groupe de patient avec SABD et basse FEVG si la SA s’avère sévère (AVA<1 cm2, gradient moyen >40 mmHg) sous dobutamine, sans toutefois donner des recommandations spécifiques pour les patients n’ayant pas de réserve de flux (Figure 1-21).
Les valeurs seuil d’AVA <1.0 cm2 ou gradient moyen ≥ 40 mmHg (ou Vmax>4 m/s) proposées dans les lignes directrices ont été dérivées à l'origine de patients ayant une FEVG préservée et il est possible que des valeurs-seuil moins strictes (par exemple AVA ou AVAproj ≤ 1.2 cm² et gradient moyen >30-35 mmHg) seraient plus appropriées pour les patients atteints de SABD et basse FEVG 25, 27, 33. Les patients qui n’ont pas de réserve de flux représentent un sous-groupe tout aussi difficile à gérer, à la fois sur le plan diagnostique et thérapeutique. Le RVA peut certainement être envisagé chez les patients présentant une évidence de SA sévère basée sur les données de l’écho de stress à la dobutamine ou la tomographie. Dans les recommandations de l’ESC22, le RVA a reçu une recommandation de classe IIb (niveau d’évidence C) pour les patients avec SABD et FEVG basse et n’ayant pas de réserve de flux. Étant donné que le risque opératoire pour la chirurgie à cœur ouvert est généralement très élevé en l'absence de réserve de flux, l’implantation de prothèse par voie percutanée (TAVI : tanscatheter aortic valve implantation) pourrait représenter une bonne alternative chez ces patients, même si les
31 taux de morbidité et de mortalité peuvent être plus élevés que chez les patients avec SA à débit normal 46-48. En effet, des études récentes ont rapporté une amélioration plus importante et plus rapide de la FEVG chez les patients traités par TAVI comparativement à ceux traités par RVA standard46. Cependant, le TAVI est associé à une incidence plus élevée de régurgitation aortique paravalvulaire, ce qui peut éventuellement avoir un impact négatif sur le devenir des patients 49-51.
Figure 1-21 : Indications pour le remplacement valvulaire aortique chez les patients avec sténose aortique. Reproduit avec permission d’après 45.
AS : sténose aortique; AVA; aire valvulaire aortique; AVR : remplacement valvulaire aortique par chirurgie standard ou transcatheter; BP : pression artérielle; DES : échocardiographie de stress à la dobutamine; ETT : épreuve d'effort sur tapis roulant; LVEF : fraction d’éjection du ventricule gauche; ΔP mean : gradient de pression moyen; Vmax : vélocité maximale.
32
1.4. Conclusion
La sténose aortique à bas débit, bas gradient avec altération de la fraction d’éjection du ventricule gauche est parmi les situations les plus difficiles rencontrées chez les patients atteints de cardiopathie valvulaire. La détermination de la sévérité de la sténose dans cette situation nécessite souvent d'autres tests diagnostiques supplémentaires outre l’échocardiographie-Doppler effectuée au repos. L’échocardiographie de stress à la dobutamine et l'utilisation de l’AVA projetée facilite grandement la détermination de la sévérité de la sténose, la stratification du risque et la prise de décision clinique chez ces patients. La quantification du calcium valvulaire aortique par tomographie et le dosage de BNP plasmatique peuvent également être utiles pour la prise en charge de ces patients, particulièrement ceux qui n'ont pas de réserve contractile et ceux chez qui l’ESD est non concluante. Le remplacement valvulaire aortique est recommandé chez les patients avec une SA sévère et réserve de flux, et doit être considéré chez les patients avec une SA sévère et sans réserve flux, puisque le pronostic est très mauvais sous traitement médical. Ces patients sont plus vulnérables que les patients avec FEVG normale à la surcharge de pression sur le VG causée par la disproportion prothèse-patient ; un effort particulier devrait donc être fait pour éviter cette complication. Enfin, le TAVI peut être une alternative prometteuse chez les patients à haut risque chirurgical et particulièrement ceux sans réserve de flux.
33
Chapitre 2
Intérêt des paramètres de la déformation myocardique du
ventricule gauche dans l’évaluation de la fonction ventriculaire
34
2.1. Contexte
Comme souligné précédemment, la SABD avec basse FEVG est l’une des situations les plus difficile rencontrées chez les patients atteints de valvulopathies, car les paramètres de sévérité de la SA (aire valvulaire et gradients transvalvulaires) ainsi ceux utilisés pour quantifier la gravité de la dysfonction ventriculaire gauche (fraction d’éjection) mesurés à l’échocardiographie de repos ne reflètent pas la sévérité réelle de la maladie. .
En pratique clinique courante, le paramètre échocardiographique couramment utilisé pour quantifier la fonction systolique ventriculaire gauche et le degré de son altération est la FEVG. C’est d’ailleurs le seul paramètre de fonction systolique mentionné dans les guides de pratique 22, 45, 52. Cependant, plusieurs études ont montré les limites de la FEVG notamment en présence de remodelage concentrique du VG et/ou de régurgitation mitrale, deux situations fréquemment rencontrées chez les patients avec SABD et basse FEVG 53-58.
Partant de ces constatations, il est nécessaire de développer et valider de nouveaux indices échocardiographiques pour mieux préciser le degré d’atteinte myocardique dans ce contexte.
2.2. Fonction longitudinale globale et déformation myocardique ou « strain »
La contraction ventriculaire gauche est très complexe avec sa composante longitudinale, radiale et circonférentielle combinées à la composante rotation ou « twist ». La composante longitudinale est particulièrement intéressante. Plusieurs études ont montré que la fonction longitudinale globale du VG est plus sensible que la FEVG pour l’évaluation de la fonction systolique ventriculaire gauche chez les patients atteints de SA avec une FEVG préservée (>50%) (Figure 2-1) 41, 42, 54-56, 59-62. De plus, plusieurs études indiquent que jusqu'à un tiers des patients avec SA asymptomatique avec une FEVG préservée ont une diminution significative de leur fonction myocardique systolique 57, 59,
60, 63. En effet, une FEVG tout à fait normale, voire même augmentée, peut être associée à
un raccourcissement longitudinal du VG nettement diminué. Dans les cas où il y a un remodelage concentrique de VG, comme c’est généralement le cas, chez les patients avec sténose aortique, la FEVG surestime la fonction systolique du VG et ne permet donc pas
35 de détecter les dommages myocardiques sous-jacents, et en particulier ceux dans la région sous-endocardique. En effet, cette région est celle qui est atteinte plus précocement et plus gravement. Les fibres myocardiques de la couche sous-endocardique étant orientées longitudinalement, le raccourcissement longitudinal est, à la différence de la FEVG, un bon marqueur de la fonction sous-endocardique.
Figure 2-1 :Supériorité du raccourcissement longitudinal sur la fraction d’éjection du ventricule gauche (LVEF) pour identifier la dysfonction systolique du myocarde dans la sténose aortique. Reproduit avec permission d’après 54.
36
Plusieurs méthodes permettent de quantifier la fonction longitudinale du VG. La déformation (ou strain) longitudinale globale (DLG) du VG évaluée par la technique du Speckle tracking semble être la plus prometteuse.
2.3. Évaluation de la déformation myocardique par Speckle tracking
2.3.1. Concept et aspects techniques
Cette technique a été développée pour permettre une quantification objective et précise de la fonction régionale et globale du VG 64, 65. Les « Speckles » sont des marqueurs acoustiques naturels présents dans le tissu myocardique, obtenus à partir de l’échelle du gris sur les images 2D. Ils sont générés par le faisceau d'ultrasons réfléchi et leurs profil est unique pour chaque région du myocarde (Figure 2-2) 66, 67.
37
Figure 2-2 : Image typique des « Speckles » (flèches) en échocardiographie 2D de la paroi septale du ventricule gauche. Reproduit avec permission d’après 66.
38
Le suivi (« Tracking ») de ces « Speckle », image par image tout au long du cycle cardiaque permet de mesurer entre autre 1) la déformation du tissu ou « strain » qui est définie comme la variation de la longueur, normalisée à la longueur d'origine et 2) la vitesse de cette déformation ou « strain rate » (Figure 2-3) 65, 66.
Figure 2-3: Le « strain » mesure la déformation du tissu qui est définie comme le changement de dimension ou longueur (L1−L0) normalisé par rapport à la longueur
initiale (L0) de la région d’intérêt. La vitesse à laquelle se changement se fait est le
strain rate. Reproduit avec permission d’après 65.
La plupart des machines d’échocardiographie récentes permettent de calculer la déformation (« strain ») en « offline », sur des images numérisées. De plus, des appareils disponibles dans le commerce permettent de calculer tous les paramètres de déformation sur des images stockées sous forme de boucles. La mesure peut être faite sur un ou plusieurs cycles cardiaques (moyenne de 3 cycles en général) en un temps très court (de l’ordre de quelques secondes) (Figure 2-4) 66-68
39
Figure 2-4 : Procédure de mesure et présentation des résultats du strain 2D par technique du Speckle tracking. Reproduit avec permission d’après 67.
2.3.2. Avantages
La DLG mesure le raccourcissement des fibres myocardiques situées dans la région sous-endocardique qui est la première à être atteinte en cas de surcharge de pression (due à une SA et/ou une hypertension artérielle), ce qui permet une détection précoce des dommages myocardiques bien avant la diminution de la fraction d’éjection, l’apparition des symptômes et l’installation de fibrose irréversible. Sur le plan technique, la mesure est indépendante de l’angle de mesure et des conditions hémodynamiques, facile à faire, peu ou pas dépendante de l’opérateur avec une bonne reproductibilité des mesures54, 60-62, 66,
69.
2.3.2. Limitations
Une mauvaise qualité d’image aura pour conséquence une mauvaise détection des mouvements du myocarde qui se traduit par une mauvaise évaluation de la déformation myocardique. Néanmoins, la technique est faisable chez la grande majorité des patients. Par ailleurs, plusieurs plateformes peuvent être utilisées pour la mesure de la déformation
40
myocardique et ces plateformes ne donnent pas nécessairement les mêmes résultats.. Cette limitation peut être surmontée en utilisant le même appareil pour le suivi d’un patient donné. Enfin, cette technique reste essentiellement, pour le moment, un outil de recherche malgré de nombreuses évidences de son utilité clinique. La standardisation des mesures et la « vulgarisation » de la technique devrait permettre son utilisation en pratique clinique courante dans le futur66, 69.
2.4. Fonction longitudinale et fibrose myocardique
Il a été démontré que la fonction longitudinale du VG mesurée par le déplacement de l’anneau mitral ou par la déformation longitudinale du VG était bien corrélée à la sévérité de la fibrose myocardique quantifiée par imagerie par résonnance magnétique ainsi que sur des biopsies myocardiques faites au moment du RVA; Plus la fibrose est sévère, moins la fonction longitudinale et le pronostic sont bons41, 42. (Figure 2-5). Dans l’étude de Herrmann et al.41, le groupe de patients avec SA à bas gradient et basse fraction d’éjection présentait un niveau plus sévère de fibrose myocardique et un moins bon raccourcissement longitudinal comparativement aux patients avec une FEVG préservée (>50%) et ceux avec un débit normal et un gradient élevé (Figure 2-6).
Figure 2-5 : Déplacement de l’anneau mitral en échocardiographie avec le mode M dans différents groupes de patients selon la sévérité de la fibrose myocardique (sur les biopsies faites lors du remplacement valvulaire aortique. Reproduit avec permission d’après 42.
41
Figure 2-6 : Corrélation inverse entre l’étendu de la fibrose myocardique sur les biopsies et le déplacement de l’anneau mitral en échocardiographie avec le mode M. Reproduit avec permission d’après 41.
La fonction longitudinale du VG semble donc mesurer la fonction contractile intrinsèque du myocarde et les dégâts myocardiques avant même que la FEVG commence à diminuer. Cependant, la supériorité de la DLG sur la FEVG chez les patients avec SABD et basse FEVG reste à démontrer.
42
Par ailleurs, la réserve de flux (définie par une augmentation du volume d’éjection≥20% sous dobutamine par rapport aux valeurs de repos) a montré sa valeur pronostique et son utilité pour la stratification du risque opératoire dans l’étude multicentrique européenne6. Cependant, d’autres études n’ont pas trouvé une telle association entre la réserve de flux et la mortalité opératoire 12. De plus, le pronostic à long terme (symptômes, récupération de la FEVG et survie à long terme) ne semble pas liée à la présence/absence de réserve de flux 12, 16, 30. Ces limitations de la réserve flux peuvent s’expliquer par le fait que celle-ci ne reflète pas uniquement la réserve contractile mais peut aussi être influencée par d’autres facteurs concomitants (insuffisance mitrale, chronotropie, asynchronisme, etc.) À cet effet, la DLG mesurée sous stress à la dobutamine pourrait être un paramètre plus sensible et plus spécifique que la réserve de flux pour estimer la réserve contractile 29.
43
Hypothèses et objectifs
44
Comme soulignés précédemment, deux questions essentielles se posent face aux patients avec SABD et basse FEVG. 1) La première étant : est-ce que la SA est sévère ou non? Nous avons vu que le calcul de l’AVAproj à partir de l’ESD et la quantification du calcium valvulaire aortique par tomographie au besoin permettent dans la grande majorité des cas de répondre à cette question. 2) La deuxième question étant : quel est le degré de l’atteinte ventriculaire gauche qui est un déterminant important du pronostic? Actuellement, en pratique clinique, la FEVG reste le paramètre le plus utilisé pour quantifier la performance du VG ou le degré de sa dysfonction. Cependant, nous avons vu que ce paramètre est loin d’être optimal pour toutes les raisons que nous avons citées plus haut (cf chapitre 2).
Plusieurs études ont montré que le strain longitudinal du VG est plus sensible que la FEVG pour quantifier la fonction systolique VG chez les patients avec SA et FEVG conservée (>50%). Cependant ce paramètre reste à valider chez les patients avec SABD et basse FEVG.
L’Objectif de ce travail était donc de valider l’utilité de la DLG pour la stratification du
risque des patients avec SABD
Notre hypothèse est que la déformation longitudinale globale du VG (DLG) mesurée au repos et sous stress à la dobutamine est supérieure à la FEVG pour prédire le devenir clinique des patients (représenté ici par la mortalité toutes-causes).
45