UNIVERSITÉ DU QUÉBEC À MONTRÉAL
ASSOCIATION ENTRE L'UTILISATION DE L'HABITAT D'UN OISEAU OMNIVORE EN MILIEU URBAIN ET SA SIGNA TURE TISSULAIRE EN
MÉTAUX
MÉMOIRE PRÉSENTÉ
COMME EXIGENCE PARTIELLE DE LA MAÎTRISE EN BIOLOGIE
PAR
LUDOVICK BROWN
Service des bibliothèques
Avertissement
La diffusion de ce mémoire se fait dans le respect des droits de son auteur, qui a signé le formulaire Autorisation de reproduire et de diffuser un travail de recherche de cycles supérieurs (SDU-522 - Rév.0?-2011 ). Cette autorisation stipule que <<Conformément à l'article 11 du Règlement no 8 des études de cycles supérieurs, [l'auteur] concède à l'Université du Québec à Montréal une licence non exclusive d'utilisation et de publication de la totalité ou d'une partie importante de [son] travail de recherche pour des fins pédagogiques et non commerciales. Plus précisément, [l'auteur] autorise l'Université du Québec à Montréal à reproduire, diffuser, prêter, distribuer ou vendre des copies de [son] travail de recherche à des fins non commerciales sur quelque support que ce soit, y compris l'Internet. Cette licence et cette autorisation n'entraînent pas une renonciation de [la] part [de l'auteur] à [ses] droits moraux ni à [ses] droits de propriété intellectuelle. Sauf entente contraire, [l'auteur] conserve la liberté de diffuser et de commercialiser ou non ce travail dont [il] possède un exemplaire."
AVANT-PROPOS
Ce projet de maîtrise s'inscrit dans le cadre du programme de recherche de Jonathan Verreault, en collaboration avec David Widory. Ce mémoire présente une des premières études à avoir documenté la relation entre 1 'utilisation de 1 'habitat et l'accumulation de métaux chez les goélands à bec cerclé à l'aide d'émetteurs GPS fixés sur ces oiseaux. Mes travaux permettent de mieux comprendre l'accumulation de métaux chez une espèce d'oiseau adaptée au milieu urbain. Ce mémoire est présenté par article et se divise en deux chapitres; le premier consiste en une revue de littérature concernant le plomb et les terres rares. Le deuxième chapitre est un article scientifique rédigé en anglais qui présente les résultats obtenus pendant ma maîtrise. Cet article a été soumis à la revue Environmental Research en juin 2018.
REMERCIEMENTS
Avant toutes choses, j'aimerais prendre le temps de remercier mon superviseur Jonathan Verreault de m'avoir offert l'opportunité de prendre part à ce projet de recherche et pour m'avoir fourni le soutien financier nécessaire afin d'y arriver. Ses précieux conseils et ses connaissances m'ont permis de mener ce projet à terme et ont été d'une grande importance pour moi. J'aimerais aussi prendre le temps de remercier mon codirecteur David Widory, ainsi qu'André Poirier et Maikel Rosabal qui ont tous été d'une grande aide pour les analyses chimiques et 1' interprétation des résultats. Leurs conseils m'ont permis de me familiariser rapidement avec le domaine analytique et leurs contributions ont été vitales pour ce projet.
Je voudrais aussi saluer les contributions de ma collègue de laboratoire Marie-Line Gentes qui a collecté les échantillons de foie durant les années 2011 et 2012. Merci à Françis St-Pierre, notre technicien de la faune, et Roxanne Camiré, notre stagiaire pour avoir aidé à la collecte des échantillons durant l'été 2016. Je voudrais aussi souligner le travail de Manon Sorais qui était en charge de la logistique pour la saison d'échantillonnage en 2016 et qui, avec François S. Chamberland, a contribué à 1' élaboration de la carte d'utilisation du territoire qui a été essentielle pour faire les analyses spatiales. Je tiens aussi à remercier tous mes collègues de laboratoire, Antoine Simond, Manon Sorais, Christine Dépatie, Julie Reinling, Marie-Line Gentes, Alexandre Bernier-Graveline, Romy Técher, Anthony François, Anaïs Kerric et Justine Hadrava pour avoir contribué à instaurer une merveilleuse ambiance de travail durant les deux dernières années
lV
Sur une note plus personnelle, j'aimerais pendre le temps de remercier mes parents, Denis Brown et Nancy Ouellet qui m'ont supporté inconditionnellement tout au long de mon cheminement. Merci à mes Grands-parents, Claire Leclerc et Marc-André Ouellet pour m'avoir initié à la pêche à un tout jeune âge. Toutes ces heures passées assis sur un rocher ou à marcher dans une rivière m'ont permis de développer mon intérêt pour l'environnement. Cette passion pour le monde naturel que vous m'avez transmise est la raison derrière mon choix de faire carrière en biologie. J'aimerais terminer cette section en remerciant une personne qui occupe une place importante dans ma vie. Carole, merci de croire en moi et de m'encourager dans la poursuite de mes rêves.
TABLES DES MATIÈRES
A V ANT -PROPOS ... ii
REMERCIEMENTS ... iii
LISTE DES FIGURES ... viii
LISTE DES TABLEAUX ... x
LISTE DES ABRÉVIATIONS, DES SIGLES ET DES ACRONYMES ... xi
LISTE DES SYMBOLES ET UNITÉS ... xiii
RÉSUMÉ ... xiv
INTRODUCTION ... 1
CHAPITRE I ÉTAT DES CONNAISSANCES ... 4
1.1 Le plomb ... 4
1.1.1 Généralités ... 4
1.1.2 La toxicité du plomb ... 5
1.1.3 Législation et situation du plomb au Canada ... 5
1.1.4 Isotopes stables du plomb ... 6
vi
1.2 Les terres rares (REE) ... 9
1.2.1 Généralités ... 9
1.2.2 Toxicité des REE ... 1 0 1.2.3 REE dans 1' environnement et la faune ... 11
1. 3 Utilisation de 1 'habitat et télémétrie ... 12
1.3.1 Télémétrie ... 12 1.3.2 Télémétrie et écotoxicologie ... 13 1.4 Objectifs et hypothèses ... .' ... 14 1.4.1 Objectifs spécifiques ... 15 1.4.2 Hypothèses spécifiques ... 15 CHAPITRE II HABITAT USE STRATEGY INFLUENCES THE TISSUE SIGNATURE OF ELEMENTS (PB AND REE) IN AND URBAN-ADAPTED OMNIVOROUS BIRD ... 16
2.1 Abstract ... 17
2.2 Introduction ... 18
2.3 Materials and methods ... 22
2.3 .1 Sample collection ... 22 2.3.2 GPS-based tracking ... 23 2.3.3 Elemental analysis ... 24 2.3.4 Pb isotope analysis ... 25 2.3.5 Statistical analysis ... 26 2.4 Results ... 28
2.4.2 Isotope ratios and elemental concentrations and patterns ... 30
2.4.3 Relationships between elemental concentrations and habitat use ... 32
2.5 Discussion ... 35
2.5.1 Characterization of foraging habitat use ... : ... 35
2.5.2 Pb concentrations and relationships with habitat use ... 36
2.5.3 Pb stable isotope ratios ... 38
2.5.4 REE concentrations and their relationships with habitat use ... 39
2.6 Conclusions ... 42 2. 7 Acknowledgements ... 42 2.8 Supporting information ... .43 2.9 References ... 45 CONCLUSIONS GÉNÉRALES ... 52 BIBLIOGRAPHIE ... 55
LISTE DES FIGURES
Figure
2.1 Mean (± SEM) time spent (h) in major foraging habitats near Montreal (QC, Canada) by incubating ring-billed gulls (20 males, 18 females).
*
Page
indicates significant difference between males and females ... 30
2.2 Correlations between concentrations (ng/g dw) of the surn of light (L) and heavy (H) rare earth elements (REE) in li ver of incubating male (n = 45) and female (n = 42) ring-billed gulls from Montreal area (QC, Canada).... 31
2.3 Rare earth element (REE) concentrations normalized to Post-Archean Australian shale (PAAS) (log10 mean sample/mean P AAS± SEM) in li ver of incubating male (n = 45) and female (n = 42) ring-billed gulls from Montreal area (QC, Canada). Missing points indicate that no mean was generated as concentrations were above the method limits of quantification in at least 60% of li ver samples.
*
indicates significant difference between males and females. Lines between means facilitates the visualisation of sex-specific differences... 322.4 Correlations between hepatic Pb concentrations (~tg/g dw) and time spent (h) foraging in landfills (A) and wastewater treatment plants (WWTP, B) for combined incubating male (n = 20) and female (n = 18) ring-billed gulls from Montreal area (QC, Canada)... 33
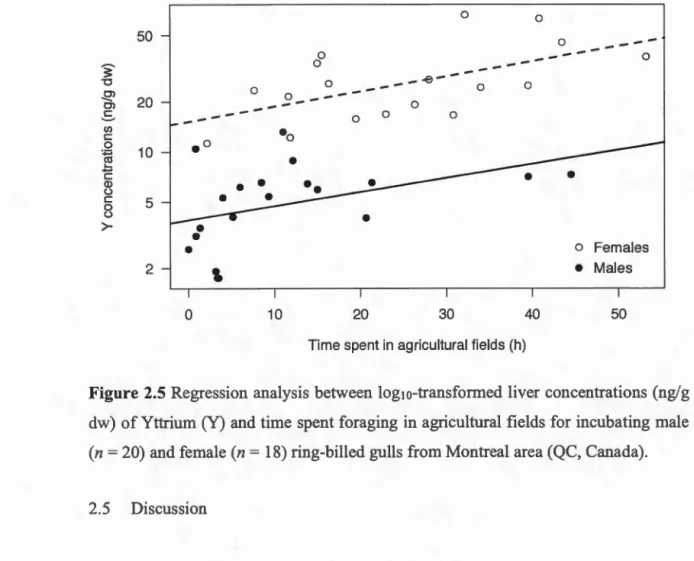
2.5 Correlations between log10-transformed liver concentrations (ng/g dw) of Yttrium (Y) and time spent foraging in agricultural fields for incubating male (n
=
20) and female (n = 18) ring-billed gulls from Montreal area (QC, Canada)... 362.6 Relationships between Pb concentrations (1/~g/g dw) and 206PbP07Pb determined in liver of incubating male and female ring-billed gulls (n = 38) from Montreal area (QC, Canada). Graph A represents Pb signatures
of ring-billed gulls that visited landfills, whereas B represents those of
ring-billed gulls that did not visit this habitat. Boxes represent approximate
Pb signature ranges of sources to which ring-billed gulls are potentially exposed (Carignan et al., 2002; Gulson et al., 1994a & 1994b; Kesler et al., 1994; Sangster et al., 2000) ... .
46
LISTE DES TABLEAUX
Tableau
2.1 Regression models predicting the hepatic Yttrium (Y) concentrations (ng/g
dw) in incubating male (n = 20) and female (n = 18) ring-billed gulls from
Montreal area (QC, Canada). Models were ranked based on the Akaike
Information Criterion corrected for small sample size (AICc). k and ro
represent the number of parameters and the Akaike weight of candidate
Page
models, respectively ... 35
2.2 Mean(± SEM) and range concentrations (ng/g dw) as well as percentage
(%) of sam pies above the method limits of quantification (MLOQs) of rare
earth elements determined in li ver of incubating male (n = 45) and female
(n = 42) ring-billed gulls from the Montreal area (QC, Canada). Means
were generated only for elements that were above MLOQs in at !east 60% of samples. . . . .. . . .. . . 44
2.3 Mean (± SEM) and range concentrations as well as percentage (%) of
samples ab ove the method limits of quantification (MLOQs) for Pb
concentrations (J...Lg/g dw) and stable Pb isotope ratios determined in liver
of combined incubating male (n = 45) and female (n
=
42) ring-billed gullsAI Cc Ce DNA Dy Er Eu Gd GPS HFR Ho HREE ICP-MS La LET LREE Lu Nd MC-ICP-MS MLOQ
MRI
Second-order Akaike Information Criterion Cerium Deoxyribonucleic acid Dysprosium Erbium Europium Gadolinium
Global Positioning system Halogenated flame retardant Holmium
Heavy rare earth element
Inductively-coupled plasma mass spectrometry Lanthanum
Lieu d'enfouissement technique Light rare earth element
Lutetium Neodymiurn
Multi-collector inductively-coupled plasma mass spectrometer Method limits of quantification
X Il
PAAS Post-Archean Australian Shales
PAH Polycyclic aromatic hydrocarbon
Pb Plomb
Pr Praseodymium
REE Rare earth elements
RFH Retardateur de flamme halogéné
Sc Scandium
SEM Standard error of the mean
Sm Samarium
Tb Terbium
Tm Thulium
y Yttrium
oc
Degrés Celsiush Heure
Km Kilomètre
Km/h Kilomètre par heure
1-lg/g Microgramme par gramme
!-!L Micro litre
mg/kg Milligramme par kilogramme
mL Millilitre
M Concentration molaire
ng/g Nanogramme par gramme
ppb Partie par billion
- · -- - - -- -- - -
-RÉSUMÉ
L'utilisation de l'habitat est un important déterminant de l'exposition, et ultimement,
de l'accumulation de contaminants dans les tissus d'oiseaux. Cependant, très peu
d'études se sont intéressées à la relation qui existe entre les mouvements d'oiseaux à
l'échelle du territoire et 1' exposition aux contaminants chez ces derniers. La
télémétrie à haute résolution (ex. émetteurs GPS) est un moyen efficace de
caractériser les déplacements d'oiseaux qui se nourrissent en milieux hétérogènes.
Cette technologie pourrait être utilisée afin d'établir un lien entre l'utilisation de
l'habitat et l'accumulation de métaux dans les tissus d'oiseaux. Les concentrations de
Plomb (Pb) et de terres rares (REE) varient naturellement à cause de différences entre
les environnements géologiques ainsi que des émissions provenant des activités
anthropiques, de sorte que les oiseaux qui se nourrissent dans différents types
d'environnement pourraient posséder différents profils d'accumulation tissulaire en
Pb et en REE. L'objectif du présent mémoire de maîtrise était donc de déterminer si
les mouvements de goélands à bec cerclé (Larus delawarensis) reconstruits par suivi
GPS pouvaient prédire les concentrations de Pb et de REE dans le foie de ces oiseaux.
Nous avons capturé des goélands à bec cerclé en période d'incubation que nous avons
équipé d'émetteurs GPS pour une période de 10 jours. Après le suivi télémétrique, les
goélands ont été euthanasiés et nous avons déterminé les concentrations et ratios
d'isotopes stables du Pb ainsi que les concentrations de REE dans leur foie. Nos
résultats montrent que les concentrations hépatiques de Pb chez les goélands à bec
cerclé augmentent avec le temps passé à se nourrir dans les dépotoirs. De plus, les
goélands qui ont passé plus de temps en milieux agricoles avaient des concentrations
hépatiques d'Yttrium (Y) plus élevées que ceux y ayant passé moins de temps. Les
concentrations hépatiques d'Y étaient aussi systématiquement plus élevées chez les
femelles relativement aux mâles. Cette différence ne semble pas être liée à des
variations intersexuelles dans l'utilisation du territoire, mais plutôt à des différences
physiologiques qui pourraient exister entre les oiseaux mâles et femelles durant la
période d'incubation. Cette étude améliore nos connaissances concernant les sources
potentielles de métaux pour la faune aviaire de la région de Montréal. Cette étude
fournit aussi des valeurs de bases concernant 1' accumulation de contaminants
d'intérêts émergents (REE) dans les tissus d'oiseaux.
INTRODUCTION
L'exposition aux contaminants chez la faune peut être influencée par plusieurs facteurs tels que l'âge, le sexe, la diète et l'utilisation de l'habitat des individus (Schipper et al., 2008; Smith et al., 2007). Bien que 1 'utilisation de l'habitat soit de plus en plus reconnue comme étant un déterminant majeur de l'exposition, et ultimement de 1' accumulation de contaminants chez les oiseaux, les mouvements d'individus à l'échelle du territoire demeurent une variable sous-utilisée en écotoxicologie.
La majorité des études portant sur la relation entre l'utilisation de l'habitat et l'exposition aux contaminants consistent en des comparaisons de niveaux de contaminants dans les tissus d'oiseaux provenant de différentes colonies situées à travers un gradient de pollution. À titre d'exemple, King et al. (2014) ont comparé les taux de mutations dans l'ADN de cormorans à aigrettes (Phalacrocorax auritus) provenant de trois colonies avec différents niveaux de contamination par des hydrocarbures aromatiques polycycliques (PAH) dans la région de Grand Lacs (Ontario, Canada). Leurs résultats montrent que les oiseaux les plus exposés aux PAH présentaient des taux de mutations plus élevés que ceux provenant des colonies situées dans des environnements moins contaminés. Dans un autre cas en Pologne, il a été démontré que la composition du territoire (% urbain versus agriculture) entourant des colonies de mouettes rieuses (Chroicocephalus ridibundus) influençait les concentrations de 17 éléments traces, incluant le plomb (Pb) et le cadmium, dans les coquilles d'œufs de ces oiseaux (Kitowski et al., 2017). Ces précédentes études démontrent que les types d'habitats qui entourent les colonies influencent fortement les niveaux de contaminants dans les tissus d'oiseaux.
2
Documenter la relation entre l'utilisation de l'habitat et l'accumulation de
contaminants dans les tissus d'un oiseau en se basant sur une approche inter-colonie
est facilement applicable chez les espèces ayant un comportement d'alimentation
prévisible (ex. Cormorans spécialisés en milieux aquatiques). Cependant, cette
pratique peut dans certains cas, être difficile à appliquer et mener à une perte d'information sur l'écologie des espèces étudiées, ce qui nuit ultimement à
1' identification de sources de contaminants dans 1' environnement (Ramos et al.,
2013). Cette problématique est particulièrement marquée chez les espèces d'oiseaux
omnivores comme le goéland à bec cerclé (Larus delawarensis) dans la région de Montréal (QC, Canada) qui se nourrissent dans une mosaïque d'habitats naturels et anthropiques.
Le développement d'appareils de géolocalisation pouvant être fixés sur des oiseaux de tailles moyennes permet de suivre les déplacements de goélands à bec cerclé à
travers différents types d'habitats (Caron-Beaudoin et al., 2013; Patenaude-Monette
et al., 2014) et d'associer ces déplacements avec des concentrations de contaminants
accumulés dans leurs tissus (Gentes et al., 2015). Dans l'étude de Gentes et al. (2015),
les auteurs ont été en mesure d'associer l'utilisation de sites d'enfouissement avec
l'accumulation de DecaBDE (mélange technique de retardateurs de flamme) dans le plasma de goélands à bec cerclé mâles. L'étude de Gentes et al. (2015) démontre
qu'incorporer la technologie GPS dans les études écotoxicologiques peut aider à
mieux comprendre les sources de contaminants à 1' échelle du paysage.
À ce jour, aucune étude n'a utilisé la technologie GPS pour tenter d'identifier dans quels habitats composant le milieu urbain les oiseaux accumulent le plus de métaux.
L'abondance du Pb est reconnue pour varier géographiquement en fonction de
l'environnement géologique et des activités anthropiques qui relâchent du Pb dans l'environnement (Komarek et al., 2008). Donc, les oiseaux qui visitent différents habitats devraient accumuler différentes concentrations de Pb et devraient aussi
présenter différents ratios d'isotopes stables de Pb, puisque les sources d'émissions varient en fonction du territoire (ex. chasse en milieux ruraux et raffineries en milieux industriels). D'autres parts, des éléments comme les terres rares pourraient aussi être rejetés en milieux urbains et péri-urbains. Puisque ces éléments ont de multiples applications dans diverses industries (Gonzalez et al., 2014), leur abondance en milieux industrialisés pourrait varier en fonction des habitats ainsi que des activités humaines et ces différences pourraient se refléter dans les tissus d'oiseaux dépendamment des sites qu'ils visitent.
L'objectif de ce projet est de détem1iner s'il y a un lien entre l'utilisation de l'habitat des goélands à bec cerclé et 1' accumulation de Pb et de REE dans le foie de ces derniers. Dans ce document, je teste l'hypothèse selon laquelle les concentrations de Pb et de REE dans le foie des goélands augmentent avec par le temps passé dans des habitats sous forte influence anthropique.
CHAPITRE I
ÉTAT DES CONNAISSANCES
1.1 Le plomb
1.1.1 Généralités
Le Pb est un métal toxique naturellement présent dans 1' environnement, mais dont le cycle géochimique est influencé par les activités humaines. Le Pb est libéré dans 1' environnement par des processus naturels tels que 1' érosion du substrat rocheux ou la désintégration radioactive de l'uranium et du thorium (238U~206Pb; 235U~2ü7Pb; 232Th~208Pb ), mais la majeure partie des émissions de Pb proviennent directement des activités humaines comme l'exploitation minière, le raffinage des métaux, l'usage de combustibles fossiles, l'incinération des déchets et la chasse (Cheng et Hu, 2010; Komârek et al., 2008; Meyer et al., 2008).
À cause de sa présence dans divers produits manufacturés, le Pb peut s'accumuler
chez les oiseaux qui y sont exposés par ingestion ou inhalation. Les oiseaux peuvent ingérer du Pb lors du nettoyage de leurs plumes ou en se nourrissant dans des sols contaminés ainsi qu'en respirant de fines particules provenant de milieux industriels
(Scheifler et al., 2006). Lorsque le Pb est assimilé, il entre d'abord dans la circulation
sanguine où il peut y rester pour une période allant de quelques jours à quelques
dans ces organes pendant plusieurs semaines (- 1 mois) avant d'être dirigé vers les os qui vont accumuler le Pb auquel les oiseaux ont été exposés durant toute leur vie (Fisher et al., 2006).
1.1.2 La toxicité du plomb
Puisque le Pb est particulièrement toxique, l'exposition chronique ou aigue à des concentrations de Pb élevées peut avoir plusieurs effets délétères chez la faune aviaire. Les oiseaux exposés au Pb peuvent subir une réduction de l'activité enzymatique (par
exemple celle l'acide delta aminolévulinique) et de l'hématocrite ainsi que des
changements de comportement (revu par Fisher et al. 2006 et Pain et al. 2009). Le Pb peut aussi réduire ou inhiber la spermatogénèse et causer une atrophie testiculaire
chez les oiseaux (Mazliah et al., 1989). De plus, une récente étude par Ecke et al. (2017) a démontré que les aigles royaux (Aquila chrysaetos) ayant des concentrations sanguines de Pb aussi basses que 0,025 j.lg/g ww volent moins haut et moins loin que les aigles ayant de plus faibles concentrations, ce qui augmente leur risque de mort
accidentelle causée par des collisions avec des véhicules ou des structures. Cette étude (Ecke et al., 2017) indique que même les plus infimes concentrations de Pb peuvent avoir des effets délétères chez les oiseaux. Cette affirmation a aussi été faite
par Pain et al. (2009) selon qui, il n'existe aucune concentration de plomb jugée sécuritaire pour les oiseaux.
1.1.3 Législation et situation du plomb au Canada
Après 1' interdiction d'utiliser des essences contenant des ad di tifs de Pb au début des
années 1990, les niveaux de Pb atmosphériques ont chuté rapidement (Nriagu, 1990).
Au début des années 1970, plusieurs études ont démontré la toxicité des émissions
d'essences plombées contribuant ainsi à la mise en place de mesures visant à réduire
6
1990). Cependant, bien que ces mesures aient permis de réduire la vitesse à laquelle le Pb s'accumule dans l'environnement, les concentrations de Pb dans les sols ne sont toujours pas revenus à leurs niveaux préindustriels (Pratte et al., 20 13). Cela s'explique en partie parce que le Pb persiste longtemps dans les sols et aussi par l'existence de plusieurs sources d'émissions qui continuent de relâcher du Pb dans l'environnement, incluant la combustion d'énergies fossiles, la production de batteries, le raffinage de métaux, les activités minières ainsi que les projectiles d'armes à feu utilisés pour la chasse (Berglund et al., 2008; Liu et al., 2006; Stevenson et al., 2005).
Au Canada les restrictions concernant l'utilisation de projectiles de Pb pour la chasse ont débuté au début des années 1990. Ce n'est qu'en 1999 que la grenaille de Pb a été bannie pour la chasse à tous les oiseaux migrateurs (Stevenson et al., 2005). À ce jour, il est cependant encore tout à fait légal d'utiliser des projectiles à base de Pb (grenailles et balles) pour chasser les espèces d'oiseaux terrestres ainsi que le petit (perdrix, lièvres, etc.) et le gros gibier (Orignaux, cerfs, ours, etc.). Plusieurs études ont démontré que l'utilisation de tels projectiles est une source majeure de Pb dans les tissus de plusieurs espèces d'oiseaux (Behmke et al., 2015; Finkelstein et al., 2012;
Legagneux et al., 2014; Madry et al., 2015; Scheuhammer et al., 2003).
1.1.4 Isotopes stables du plomb
Les isotopes représentent des atomes d'un même élément n'étant différenciés que par un nombre de neutrons distinct. Nous pouvons classer les isotopes en deux grandes catégories, les isotopes stables et les isotopes radioactifs. Ces derniers se désintègrent avec le temps formant ainsi de nouveaux isotopes, alors que les isotopes stables, qui représentent moins de 1 0% de tous les isotopes connus, ne subissent aucune désintégration radioactive (Fry, 2002).
Le Pb possède quatre isotopes stables
e
04Pb, 206Pb, 207Pb, 208Pb) qui proviennentmajoritairement de la désintégration radioactive de l'uranium (U) et du thorium (Th).
L'isotope 208Pb est le plus abondant (52%) et provient de la désintégration du 232Th
(Gulson, 2008). Les isotopes 207Pb et 206Pb proviennent de la désintégration du 235U et 238U et représentent, respectivement 23% et 24% des isotopes de Pb (Gulson, 2008;
Komarek et al., 2008). L'isotope le moins abondant est 204Pb. Ce dernier ne possède
aucun parent radioactif connus et représente environ 1% du total de Pb dans la croûte
terrestre. La distribution des isotopes de Pb est généralement exprimée sous la forme
de rapports isotopiques, tels que 208PbP04Pb et 206Pbf2°7Pb (Gulson, 2008; Komârek et al., 2008).
1.1. 5 Le plomb dans 1' environnement
Les isotopes stables du Pb ne sont pas fractionnés durant le raffinage des métaux de
sorte que toutes les variations dans les ratios d'isotopes stables du Pb sont causées par
le mélange de minerais provenant de différents environnements géologiques (Shiel et
al., 2010). En faits, les ratios d'isotopes stables du Pb dans un échantillon dépendent
de la quantité de Pb primordial, de U et de Th, ainsi que de la période radioactive des
isotopes radioactifs de ces deux derniers éléments (Erel et al., 2001 ).
Conséquemment, chaque source d'émission de Pb possède une signature isotopique
unique lorsque normalisée au 204Pb ou, du moins, qui se chevauche partiellement avec
celle d'une autre source lorsque normalisée avec les autres isotopes (Gulson, 2008;
Scheuhammer et Templeton, 1998). Cette particularité permet de différencier les
sources de Pb naturelles et anthropiques, faisant de cet élément un outil de traçage
précis et couramment utilisé dans les études environnementales (Komarek et al.,
2008).
Plusieurs études ont utilisé les isotopes stables du Pb pour déterminer les sources de
8
entre autres, relié à celui provenant de munitions grâce à la comparaison de leurs ratios d'isotopes stables de Pb. Les résultats de Behmke et al. (2015) montrent clairement que la signature isotopique du Pb dans les tissus d'urubus à tête noire
(Coragyps attratus) (2°7Pbf2°6Pb = 0,806-0,881) et d'urubus à tête rouge (Cathartes
aura)
e
07Pbf2°6Pb=
0,812-0,851) chevauche la signature de projectiles de Pb utiliséspour la chasse
e
07Pbf2°6Pb=
0, 786-0,871 ). Cela suggère que les urubus et autresespèces opportunistes se nourrissant de carcasses d'animaux abandonnées s'exposent
possiblement à de grandes concentrations de Pb. Dans une étude similaire, Legagneux
et al. (2014) ont déterminé que les corbeaux (Corvus corax) ayant des concentrations de Pb sanguin élevées(> 100 ).!g/L dw) présentaient aussi des ratios d'isotopes stables s'apparentant à ceux de munitions, alors que les ratios d'isotopes mesurés chez les
corbeaux ayant des concentrations de Pb sanguin plus basses(< 100 ).!g/L dw) étaient caractéristiques du Pb naturel.
L'abondance et les ratios d'isotopes stables du Pb sont aussi reconnus pour varier géographiquement de sorte que les oiseaux vont présenter des signatures différentes dépendamment de l'endroit où ils ont été échantillonnés (Berglund et al., 2008; Komarek et al., 2008). C'est notamment le cas d'oiseaux insectivores échantillonnés
autour d'une raffinerie de sulfite en Suède. Berglung et al. (2008) ont observé que les
échantillons de foie d'oiseaux (Ficedula hypoleuca) collectés près de l'usine avaient
des concentrations de Pb plus élevées (2,5 km; 5,6
±
3,8 ).!g/g ww) que ceuxprovenant de sites plus éloignés (90 km; 0,08
±
0,12 ).!g/g ww). De plus, les ratios d'isotopese
06Pbf2°7Pb=
1,15±
0,01) mesurés dans des invertébrés et le foie d'oiseaux échantillonnés près de la fonderie s'apparentaient à ceux du sol à cet endroite
06Pbf2°7Pb = 1,17±
0,01). De façon similaire, les concentrations de Pb sontplus élevées chez les oiseaux urbains par rapport à leurs congénères provenant d'un milieu rural à cause des anciennes émissions d'essences plombées (Scheifler et al. 2006).
Le plomb anciennement émis se trouve encore aujourd'hui dans les sols urbains et d'autres sites contaminés (ex. champs de tir), car cet élément peut persister jusqu'à 300 ans dans les sols (Hui, 2002). La concentration et les ratios d'isotopes stables du Pb sont, par exemple, reflétés dans les tissus d'invertébrés, tels que les vers de terre, qui vivent dans les sols (Kennette et al., 2002). Les résultats de Scheuhammer et al.
(2003) montrent aussi qu'il y a une corrélation entre les concentrations de Pb dans les sols et celles des vers de terre. Comme ces invertébrés sont une source de nourriture pour plusieurs espèces d'oiseaux, ces-derniers sont susceptibles d'être exposés au Pb en se nourrissant dans des environnements contaminés. De plus, Fritsch et al. (2012) ont démontré qu'il y avait une forte corrélation entre les concentrations de Pb dans les sols où les oiseaux (Turdus meru/a) se nourrissent et les concentrations de Pb dans leurs plumes. Ces résultats suggèrent que les oiseaux peuvent aussi être exposés au Pb en inhalant ou en ingérant (durant le toilettage) des poussières provenant de leurs sites d'alimentation.
1.2 Les terres rares (REE)
1.2.1 Généralités
Les terres rares (REE) sont des éléments du tableau périodique comprenant le scandium (Sc, #21), l'yttrium (Y, #39) ainsi que les lanthanides qui regroupent les éléments entre le lanthane (La, #57) et le lutétium (Lu, #71 ). Les lanthanides sont un groupe d'éléments ayant un comportement chimique similaire à l'exception du cérium (Ce) et de l'europium (Eu) qui sont redox-sensibles et qui peuvent présenter différents états d'oxydation. Les REE sont aussi généralement divisées en deux groupes : le premier groupe est composé de REE légères (LREE) qui comprennent le Sc (#21) ainsi que les éléments entre le La (#57) et le gadolinium (Gd, #64) et le deuxième groupe composé de REE lourdes (HREE) comprend l'Y (#39) et les éléments entre le terbium (Tb, #65) et le Lu (#71). Contrairement à ce que leur nom
10 indique, ces éléments ne sont pas rares et peuvent même être plus abondants que le Pb et le cuivre dans certains environnements géologiques (Liang et al., 2014). Les REE suivent la règle d'Oddo-Harkins qui stipule que les éléments ayant un numéro
atomique pair dans le tableau périodique sont plus abondants que les éléments adjacents avec un numéro impair (Gonzalez et al., 2014). Cette particularité entraîne
donc un patron en dent de scie lorsque les niveaux de REE sont comparés graphiquement. Afin de faciliter de telles comparaisons, il est préférable de normaliser les concentrations de REE d'un échantillon avec des valeurs de chondrites ou de shales qui correspondent à 1' abondance moyenne de ces éléments dans la croûte terrestre. Cette procédure a pour effet de lisser le patron de REE et facilite
l'identification d'enrichissements anthropiques dans un échantillon.
1.2.2 Toxicité des REE
Les REE sont des contaminants d'intérêt émergeant, ce qui signifie que bien que ces éléments soient utilisés depuis plusieurs années, 1 'intérêt pour leurs impacts
toxicologiques est relativement nouveau. Le fait que les REE aient des applications en agriculture et en production animale indique que ces éléments pourraient suivre
une courbe de réponse hom1étique et ainsi avoir des effets bénéfiques à petites doses
ou avoir des effets néfastes si administrés en plus grandes doses (revue par Pagano et al., 2015). Wang et al. (2017) n'ont toutefois pas observé d'effet sur la masse, la
mortalité et divers paramètres biochimiques (sang et urine) après avoir exposé des
rats par voie orale à 0, 10, 30 et 90 mg/kg de nitrate d'Y durant une période de 90
jours. Contrairement à ces résultats, Pagano et al. (2016) ont rapporté divers défauts de développement chez des larves d'oursins exposées à des solutions contenant
diverses concentrations (1
o
-
8 à 10-4 M) d'Y, de La, de Ce, de Nd, d'Eu et de Gd. Ces auteurs ont aussi été en mesure d'associer la formation de dérivés réactifs d'oxygèneet de nitrites chez les embryons d'oursins exposés à l'Y, au Ce et au néodyme (Nd) (1
o-
6 M). Les émissions de diésel (Ce02) sont aussi reconnues pour affecter l'intégritédes alvéoles pulmonaires chez les rats qui y ont été exposés par inhalation (Snow et
al., 2014).
1.2.3 REE dans l'environnement et la faune
Les études portant sur l'accumulation de REE dans les tissus de vertébrés ne sont pas très nombreuses, mais il a été suggéré que l'écologie des espèces pouvait influencer l'accumulation de REE dans les tissus d'organismes. Mayfield et Fairbrother (2015) ont déterminé les concentrations de REE dans les muscles et les carcasses (os et
organes internes) de plusieurs espèces de poissons provenant d'un réservoir localisé dans une zone non-industrialisée de l'État de Washington aux États-Unis. Leurs résultats montrent des profils d'accumulation de REE différents chez les poissons
situés au bas de la chaîne alimentaire (Meuniers, Castotomus sp.) et les espèces
prédatrices (truite arc-en-ciel, Onchoryncus mykiss; achigan à petite bouche;
Micropterus dolomieu, doré jaune; Sander vitreus). MacMillan et al. (2017) ont obtenu des résultats similaires en comparant les concentrations de REE chez des
organismes situés à différents niveaux trophiques dans les écosystèmes aquatiques, terrestres et marins de l'Arctique canadien. De plus, selon les auteurs de cette
dernière étude, les organismes situés au bas de la chaine alimentaire (végétation et
invertébrés) accumulent de plus grandes concentrations de REE comparativement à ceux situés à des niveaux trophiques plus élevés (poissons, oiseaux et mammifères).
Les résultats de ces deux études indiquent que le type de nourriture consommée ainsi
que le type d'habitat dans lequel les espèces vivent peuvent influencer l'accumulation de REE dans les tissus de ces dernières.
La détection et l'abondance des REE dans les vertébrés semblent aussi dépendre du
type de tissus analysés (MacMillan et al., 2017). En effet, cette étude a démontré que
les eiders à duvet (Somateria millissima) et les lagopèdes (Lagopus lagopus) collectés
12
concentrations de REE dans leur foie que dans leurs muscles. Cela indique que le foie
serait une meilleure option pour évaluer l'accumulation de REE chez les oiseaux. D'autre part, la cinétique des REE n'est pas bien documentée, mais il semblerait que les concentrations hépatiques de ces éléments reflètent une exposition à moyen terme.
Cela a été démontré par Snow et al. (2014) qui ont exposé des rats à 1000 f.lg/m3 de Ce par inhalation. Après l'exposition et suivant une période de dépuration durant laquelle les rats étaient exposés à de 1' air filtré, les concentrations hépatiques de Ce
ont chutées de 59% en 14 jours.
La majorité des études portant sur l'accumulation de REE dans les vertébrés sont
basées en régions éloignées et, à ma connaissance, il n'existe à ce jour aucune étude portant sur les REE dans les tissus de vertébrés provenant de milieux urbains en
Amérique du Nord. Nous savons cependant que les émissions provenant des voitures
peuvent contaminer l'atmosphère des villes avec des particules de Ce, comme cela a été démontré pour la ville de Madrid en Espagne (Moreno et al., 2013). De plus, l'impact de l'exposition aux particules de Ce a déjà été étudié en laboratoire (Snow et
al., 2014), mais il n'y a présentement pas d'étude concernant l'exposition et
l'accumulation de cet élément potentiellement toxique chez une espèce faunique en
milieu industrialisé. Il en va de même pour d'autres REE, tels que l'yttrium et le lanthane qui sont présents dans des engrais minéraux régulièrement appliqués et qui pourraient s'accumuler en milieux agricoles (Otero et al., 2005). Le milieu urbain (et
périurbain) comprend plusieurs sources potentielles de REE auxquelles les oiseaux pourraient être exposés (ex. émissions des voitures, eaux usées, champs agricole),
mais il n'existe toujours pas d'étude ayant investigué le lien entre l'utilisation d'habitats contaminés par des REE et l'accumulation de ces éléments dans les tissus d'oiseaux.
1.3 Utilisation de l'habitat et télémétrie
1.3.1 Télémétrie
L'utilisation de l'habitat est définie comme étant n'importe quelle façon dont un
organisme utilise son environnement. L'écologie spatiale et les comportements de
quête alimentaire en font partie de façon intégrante (Johnson, 1980). Le
développement d'appareils de télémétrie pouvant être fixés sur des oiseaux de tailles
moyennes facilite grandement l'obtention de données sur les déplacements de ces
derniers. Par exemple, Patenaude-Monette et al. (2014) ont caractérisé la sélection d'habitats chez les goélands à bec cerclé nichant dans la région de Montréal (QC, Canada) à l'aide d'émetteurs GPS (Global Positioning system). Lors de cette étude, il a été démontré que les goélands à bec cerclé sélectionnaient les zones agricoles afin de se nourrir, mais seulement durant le labourage et la période des semences dans le sud du Québec. Sans l'usage de GPS, il n'aurait pas été possible pour ces auteurs de
déterminer l'importance des zones agricoles dans l'alimentation des goélands. De
façon similaire, l'usage d'émetteurs GPS a aussi permis à Rock et al. (2016) de suivre
en détail les déplacements de goélands argentés (Larus argentatus) nichant dans la
région de St-Yves (Cornwall, UK). Cette étude a révélé qu'il y avait des variations
interindividuelles dans les comportements d'alimentation des goélands argentés
nichant en milieu urbain. En effet, les auteurs ont constaté que ces oiseaux n'allaient pas se nourrir aux mêmes endroits malgré le fait qu'ils provenaient tous de la même colonie.
1.3.2 Télémétrie et écotoxicologie
La majorité des études de terrain en toxicologie supposent que tous les oiseaux d'une
même colonie adoptent des comportements de quête alimentaire similaires. Cette
14
se nourrissant en milieu hétérogène (Caron-Beaudoin et al., 2013; Patenaude-Monette et al., 2014; Rock et al., 2016). Cela peut mener à une perte d'information pouvant nuire à la caractérisation de l'exposition, et ultimement de l'accumulation de
contaminants chez la faune (Ramas et al., 2013).
Les smvts télémétriques offrent un sérieux avantage par rapport aux méthodes traditionnellement utilisées en toxicologie, car ils permettent de suivre les déplacements des oiseaux à travers divers habitats et de caractériser les déplacements de chaque individu (Rock et al., 2016). La caractérisation des mouvements
individuels des oiseaux permet entre autres d'établir un lien entre les concentrations de contaminants accumulés dans les tissus d'oiseaux et les habitudes alimentaires de
ces derniers. Ackerman et al. (2007) ont équipé des oiseaux (Avocette d'Amérique,
Recurvirostra americana et Échasse d'Amérique, Himantopus mexicanus) avec des
transmetteurs radio pour suivre leurs déplacements daus la région de le Baie de San
Fraucisco (Californie, USA). Des variations daus les concentrations de mercure déterminées daus le sang des deux espèces d'oiseaux étudiées ont été attribuées à des différences dans l'utilisation de l'habitat. Dans cette étude (Ackerman et al.,. 2007),
un lien de causalité entre l'utilisation de l'habitat et l'accumulation de mercure a pu
être établi, car le suivi télémétrique a révélé que les individus étaient fidèles à leurs
sites d'alimentation. L'utilité de la technologie GPS dans un contexte
écotoxicologique a aussi récemment été démontrée par Gentes et al. (2015) qui ont établi un lien entre l'utilisation de lieux d'enfouissement technique et les
concentrations plasmatiques de retardateurs de flamme halogénés (RFH) chez les
goélands à bec cerclé mâles. Les résultats obtenus lors de cette étude suggèrent que les goélands ont été exposés aux RFH en inhalant de la poussière ou en l'ingérant lors du nettoyage de leurs plumes.
1.4 Objectifs et hypothèses
L'objectif général de la présente étude est de déterminer s'il y a un lien entre la
signature tissulaire en métaux (Pb et REE) et l'utilisation de l'habitat chez le goéland à bec cerclé nichant sur la colonie de l'île Deslauriers (Varennes, QC). Cet oiseau omnivore se nourrit de façon opportuniste dans une mosaïque d'habitats naturels et
anthropiques entourant son lieu de nidification, mais certains individus se spécialisent
dans un type d'habitat en particulier. Ce comportement pourrait engendrer des différences interindividuelles dans l'exposition et l'accumulation de métaux chez cette espèce.
1.4.1 Objectifs spécifiques
1- Déterminer si le temps passé dans les lieux d'enfouissement technique (LET),
les bassins de traitement d'eaux usées et les champs agricoles influencent les concentrations hépatiques de Pb et de REE chez les goélands à bec cerclé
2- Déterminer si l'utilisation de différents habitats d'alimentation influence les ratios d'isotopes stables du Pb dans le tissu hépatique des goélands à bec cerclé
1.4.2 Hypothèses spécifiques
1- Les oiseaux qui passent plus de temps dans les LET accumulent plus de Pb que ceux n'y allant pas ou qui y passent moins de temps. Les oiseaux qui
visitent les bassins de traitement d'eaux usées accumulent plus de Gd, alors
que ceux qui visitent les champs agricoles accumulent les REE qu'on retrouve
16 2- L'utilisation de l'habitat du goéland influence les ratios d'isotopes stables du Pb de sorte que les oiseaux visitant les milieux ruraux ou aquatiques présentent des ratios qui s'apparentent à ceux des projectiles de Pb (chasse),
alors que ceux des oiseaux visitant les milieux urbains s'apparentent plus aux ratios provenant de l'essence des voitures.
HABITAT USE STRATEGY INFLUENCES THE TISSUE SIGNATURE OF
ELEMENTS (PB AND REE) IN AND URBAN-ADAPTED OMNIVOROUS BIRD
Ludovick Browna, Maikel Rosabala,c, Manon Soraisa, André Poirierb, David Widorya,b, Jonathan Verreaulta
a Groupe de recherche en toxicologie de l'environnement (TOXEN), Département des sciences biologiques, Université du Québec à Montréal, P.O. Box 8888, Succursale Centre-ville, Montreal, QC, H3C 3P8, Canada
b Centre de recherche en géochimie et géodynamique (GEOTOP), Département des sciences de la terre et de l'atmosphère, Université du Québec à Montréal, P.O. Box 8888, Succursale Centre-ville, Montreal, QC, H3C 3P8, Canada
c Groupe de recherche interuniversitaire en limnologie et en environnement aquatique (GRIL), Université du Québec à Montréal, Montréal, QC, H2X l Y4, Canada
18
2.1 Abstract
Habitat use is an important determinant of contaminant exposure in birds but few
studies have documented the relationship existing between exposure and individual
bird movements at the landscape level. Despite its accuracy, GPS-based telemetry is
still scarcely used in field-based toxicological studies to investigate habitat use and metal accumulation in urban-adapted birds that forage in heterogeneous landscapes. Lead (Pb) and rare earth element (REE) concentrations vary naturally between
geological environments and emissions from anthropogenic activities. Thus, birds that visit different habitat types should accumulate different element concentrations and patterns. The objective of the present study was to determine if GPS-based telemetry could be used to determine the sources of Pb and REE exposure in ring-billed gulls. Birds (n = 38) were equipped with miniature GPS units to reconstruct
their movements. Following the telemetrie survey, gulls were recaptured and Pb contents and isotope ratios and REE concentrations were determined in liver samples. Gulls foraging in landfills accumulated higher Pb concentrations relative to birds that
visit other sites to forage. A correlation was found between the time spent foraging in agricultural fields and hepatic concentrations of yttrium. Heavy REE concentrations
were also significantly higher in female gull liver samples relative to those of males, although this was not associated with habitat use strategy. This study provided
valuable information on the potential sources of metal exposure in an urban
environment as well as novel information on the accumulation of metallic
contaminants (REE) of emerging concem in free-ranging birds.
2.2 Introduction
Contaminant exposure in birds can be influenced by several factors including age, sex, diet composition, and habitat use (Schipper et al., 2008; Smith et al., 2007). However, there are only a few studies that have investigated the specifie role of landscape use in the accumulation of contaminants in bird tissues. Methods for assessing the impact of habitat use on contaminant exposure, and accumulation, in birds are traditionally based on comparisons in tissue/egg contaminant levels between nesting areas from reference and polluted sites. For example, Kitowsky et al. (2017) compared the concentrations of 17 elements including Pb and cadmium (Cd) in eggshells of black-headed gulls (Chroicocephalus ridibundus) from five colonies located in Northem Poland, and reported inter-colony differences in concentrations for most elements depending on landscape features ( e.g., percentages of agricultural vs. urbanized areas) around the colonies. However, using an inter-colony approach to compare contaminant levels in omnivorous bird species ( e.g., gulls) that forage in heterogeneous landscapes may ultimately lead to a loss of information because it does not account for inter-individual differences in habitat use.
The development of miniature tracking deviees for small- and medium-sized species allows characterisation of individual bird movements, thereby improving our understanding of contaminant exposure in birds. For example, a study by Gentes et al. (20 15) using miniature bird-bome GPS deviees showed th at male ring-billed gulls
(Larus delawarensis) in the Montreal area (Quebec, Canada) that visited landfills
exhibited higher plasma concentrations of halogenated flame retardants (HFRs) relative to males that did not visit landfills. In this study, it was concluded that male ring-billed gulls that visited landfills were exposed to HFRs predominantly by ingestion (during preening) or inhalation of dusts and particles, thus suggesting that habitat use strategy is the major determinant of HFR exposure in this species relative to dietary intake. This demonstrates that a fine-scale characterisation of habitat use is
20 essential to better understand contaminant exposure in omnivorous birds including gulls and other wildlife that forage opportunistically in bath natural (terrestrial and aquatic) and anthropogenic habitats ( agricultural fields, landfills, ci ti es, etc.) (Ackerman et al., 2007; Caron-Beaudoin et al., 2013).
Lead (Pb) is a non-essential metal for biological functions and its abundance vary geographically due to natural variations between geological environments and anthropogenic activities. Spatial variations in metal levels can be reflected in their concentrations in tissues of birds and other wildlife species that forage or live near contaminated sites (Fritsch et al., 2012; Kennette et al., 2002; Van den Brink and Ma, 1998). As such, birds sampled in urban environments often exhibit higher Pb concentrations relative to birds sampled in rural areas. This was shawn for example in a study of common black birds (Turdus meru/a) in which Pb concentrations in feathers and blood were found to be three times higher in urban areas relative to rural areas (Scheifler et al., 2006).
Sources of Pb exposure in birds can also be determined using Pb stable isotopes (Behrnke et al., 20 15; Berglund et al., 2008; Church et al., 2006; Finkelstein et al.,
2012; Legagneux et al., 2014; Scheuhammer et al., 2003). Pb bas four stable isotopes
e
04Pb, 206Pb, 207Pb and 208Pb) and three of thesee
06Pb, 207Pb and 208Pb) are theend-products of uranium (235U and 238U) and thorium (232Th) radioactive decay. Relative
abundances of Pb isotope content in a sample is thus highly dependent on the concentration of primordial Pb and the concentrations of U and Th, and its geological age (decay rates being very low), which vary geographically. Furthermore, Pb isotopes are not undergoing significant mass-dependent fractionation due to the isotope's heavy mass and subsequently their small relative mass difference (Shiel et al., 2010), anthropogenic Pb will be isotopically identical to the signature its original ore deposit; mines having a defined field of composition. It is thus possible to trace the geological origin of Pb in samples, thereby allowing to discrimina te natural from
antbropogenic Pb sources through the analysis of its stable isotope ratios and
concentrations. For example, pied flycatchers (Ficedula hypoleuca) that foraged in
the vicinity of a sulphide ore smelter in Sweden were reported to accumulate greater
hepatic Pb concentrations and had 206PbP07Pb values that resembled those of smelter
emissions rather than those from the local natural background (Berglund et al., 2008).
However, in addition to atmospheric depositions, Pb exposure in birds can originate
from a local point source. As such, Pb-based ammunitions used by hunters are now
recognized as a major source of Pb exposure for predatory (e.g., eagles and vultures)
and insectivorous (e.g., woodcocks) birds (Behmke et al., 2015; Finkelstein et al.,
2012; Kerr et al., 2011; Madry et al., 2015; Scheuhammer and Templeton, 1998;
Stevenson et al., 2005). Legagneux et al. (2014) reported that Pb isotope ratios
e
06Pbf2°7Pb and 208PbP06Pb) in common ravens (Corvus corax) exhibiting high bloodPb concentrations showed Pb isotope signature within a similar range to ammunitions,
while individuals with low Pb concentrations showed Pb isotope ratios doser to that
of soils. Therefore, birds that visit different habitat types should present isotope ratios
that reflect tho se of the antbropogenic emission sources to which they are exposed.
Antbropogenic enrichment of rare earth elements (REE) in ecosystems might also
lead to accumulation in bird tissues. However, limited information is available on the
fa te of REE in wildlife species and in the environment in general. REE include the 15
lanthanides (atomic numbers #57 to #71) along with yttrium (#39) and scandium (#21)
and can be divided into two subgroups: light REE (LREE) that includes scandium
and the lanthanides between lanthanum (#57) and gadolinium (#64) and the heavy
REE (HREE), which include yttrium and the lanthanides between terbium (#65) and lutetium (#71).
REEs have multiple applications in medicine, agriculture and emergent technologies,
which lead to increased antbropogenic emissions in the environment due to surface
22
wastewater (Gonzalez et al., 2014). The most notorious example is the use of
gadolinium (Gd)-based compounds as contrasting agent for magnetic resonance imagery in hospitals, which end up in wastewater treatment plants and ultimately in water bodies (Bau and Dulski, 1996). Moreover, cerium (Ce) is comrnonly used in automotive catalytic converters sin ce the 1980s and bas been used as marker of traffic
emissions though the release of Ce particles (Moreno et al., 2013). Chronic exposure
to Ce emissions resulting from diesel fuel combustion was reported to damage lung alveoli and lead to higher Ce concentrations in lung and liver in rats (Snow et al., 2014). This suggests that certain REEs can be harmful to animais, however, the
extent to which urban-adapted birds are exposed and accumulate Ce as weil as other REE is currently unknown.
The literature on REE in free-ranging birds is scarce and currently lacks studies
reporting concentrations of these elements in birds from more exposed regions including urban and sub-urban areas. A recent study by MacMillan et al. (2017)
revealed that REE concentrations in marine, freshwater and terrestrial organisms including birds decreased with increasing trophic level in the Canadian Arctic.
Moreover, it was demonstrated by Mayfield and Fairbrother (20 15) that bottom-dwelling fish (suckers) presented higher detection frequencies and concentrations of REE relative to predatory fish (trout, bass and walleye). In this study, it was suggested that fish with contrasting foraging behaviours and physiology accumulate different REE concentrations. Therefore, birds foraging in habitats where anthropogenic activities release REE might accumulate higher concentrations of these
elements relative to birds spanning less-exposed environrnents.
The objective of the present study was to investigate the relationships between li ver concentrations of a comprehensive suite of elements including Pb and REE as weil as
Pb stable isotopes, and foraging habitat use (time spent in landfills, urban areas, agricultural fields, etc.) in ring-billed gulls breeding in Montreal area (QC, Canada).
It was hypothesized that gulls spending more time in urban areas and landfills would show higher liver Pb concentrations and different isotope ratios compared to gulls
that forage more in agricultural fields and na tura! habitats ( e.g., ri vers and lakes ). It
was further hypothesized that gulls that visit certain habitats susceptible of being contaminated by REE (landfills, wastewater treatment plants and agricultural fields)
exhibit higher liver REE concentrations. This study will contribute to a better understanding of the major exposure sources of Pb and REE, which are of
environmental concern, in ring-billed gulls and potentially other urban-adapted bird species exposed to these metals in anthropogenic and natural habitats.
2.3 Materials and methods
2.3.1 Sample collection
Breeding ring-billed gulls were collected for tissue samples (20 11, n
=
29; 2012, n=
20; 2016, n = 38) during the incubation period between April and June on Deslauriers Island (45°42'44.93"N, 73°26'24.66"W) in the St. Lawrence River,
approximately 3 km downstream from the city of Montreal (QC, Canada). This
colony supports approximately 32,000 pairs of ring-billed gulls during the nesting
season, and is surrounded by a mosaic of habitats that include agricultural fields, waste management facilities (landfills and waste water treatrnent plants), urban and suburban areas (industrial and residential) as weil as rivers and lakes (Giroux et al., 2016).
Ring-billed gulls were captured randomly in all sections of the colony while
incubating using a dip net or a remote-controlled trap. In order to monitor their movements, birds captured in 2016 (n
=
38) were equipped with a miniature GPS unit(mode! GiPSy2; TechnoSmArt, Rome, Italy) affixed on two tai! feathers (Gentes et
24 euthanized by cervical dislocation. The liver was extracted and put in clean plastic tubes and stored in ice while in the field (maximum 8 h). Upon return to the laboratory, liver samples were stored at -30°C until elemental (section 2.3.3) and Pb isotope analyses (section 2.3.4). Liver was selected among other tissues as it is known to accumulate Pb and other elements including REE (MacMillan et al., 2017).
Moreover, the analysis of liver tissues provide reliable information regarding metal exposure and accumulation during the last few weeks ( ~ one month) of vertebrates (Fisher et al., 2006; Snow et al., 2014 ). The relationships between these concentrations and the time spent in foraging habitats can then be investigated by means of a 1 0-day telemetrie survey because ring-billed gulls from Montreal repeatably travel to the same areas to forage during the breeding period (Sorais et al., unpublished data). Bird capture and handling methods were approved by the Institutional Committee on Animal Care of the Université du Québec à Montréal (permits no. 768 and 885).
2.3.2 GPS-based tracking
GPS tracking data were processed using methods described by Gentes et al. (20 15).
Briefly, geographical positions obtained from the GPS deviees recorded every 10 min along with ground speed (km/h) were overlaid on a high-resolution map of Montreal area created using ArcGIS (ESRI, Redlands, Califomia, USA). Major foraging habitats delimited on this map were are as follows: agricultural fields, wastewater basins (wastewater treatment plants), industrial areas (various industries), landfills,
urban parks, green areas (areas with grass that are not urban parks or golf courses), St. Lawrence River, other rivers and lakes, industrial basins (wastewater basins excluding wastewater treatment plants), golf courses, commercial areas (e.g.,
restaurants, grocery stores, etc.), shipping ports and quarries (stone and sand pits). Only geographical positions associated with ground speeds equal to or below 4 km/h and outside of the colony (Deslauriers Island) were included in further analysis as
they were more likely to be associated with foraging activities (Gentes et al., 20 15; Shamoun-Baranes et al., 2011). Geographical positions that were recorded in golf courses (n = 9), shipping ports (n = 4), and quarries (n = 2) were excluded from further analyses as tao few birds visited these foraging habitats, thus precluding robust statistical analyses.
2.3.3 Elemental analysis
Ring-billed gullliver samples (n = 87) were freeze-dried and digested in a HN03 and H202 solution as described in Rosabal et al. (2014) with minor modifications. Briefly,
liver samples (- 10 mg dw) were digested in 375 ~-tL ofhigh purity 16N HN03. Once cooled, 150 ~-tL of high purity H202 (Optima grade, Fisher Scientific, Ottawa, Ontario, Canada) was added to the samples and kept at room temperature. The resulting solution was then kept for 1 day before the total volume was completed to 10 mL with ultrapure water.
Concentrations of Pb and REE (Sc, Y, La, Ce, Pr, Nd, Sm, Eu, Gd, Tb, Dy, Ho, Er,
Tm, Yb and Lu) were determined by inductively coupled plasma mass spectrometry (ICP-MS; Thermo Elemental X Series, Winsford, England, UK). The reference materials DOLT-5 (n
=
6, Dogfish liver, National Research Council Canada, Ottawa,Ontario, Canada) and BCR-668 (n = 6, Musse! tissue; European Commission, Geel, Belgium) were used for Pb and REE analyses, respectively. Concentration recoveries (%
±
SEM) calculated based on the certified values for the 15 elements deterrnined in the reference materials were: 97 ± 10% for Pb, 86 ± 1 % for Y, 101 ± 3% for La, 97± 3 % for Ce, 90 ± 3 % for Pr, 97 ± 3% for Nd, 92 ± 5 % for Sm, 89 ± 1 % for Eu,
110 ± 2 % for Gd, 77 ± 3% for Tb, 82 ± 1 % for Dy, 77 ± 2% for Ho, 84 ± 6% for Er, 86
±
2% for Yb and 81±
5% for Lu. In general, blank levels (n = 4) were below detection limits for ail elements, therefore, no blank-correction was applied.26 Scandium (Sc) and Thulium (Tm) were excluded from further analysis as concentrations in samples could not be determined due to analytical interferences.
For graphical representation of REE concentrations, mean element concentrations were normalized to post-Archean Australian shale (PAAS) values obtained from Pourmand et al. (2012). Normalisation procedures consisted of dividing the concentrations of each REE by its mean P AAS value (mean crus ta! abundance) and reporting them on a logto-scale. This procedure eliminates the Oddo-Harkins effect, that is, the so-called saw-tooth pattern originating from elements with an even Z number in the periodic table that are more abundant than adjacent odd-numbered elements (Gonzalez et al., 2014). Following this normalization, concentrations typically yie1d a smooth trend line that can be concave up or down according to the mineralogy of the source material (ultimately geological), and may reveal anthropogenic inputs of REE that appear as anomalies (i.e., sharp peaks for one or severa! elements).
2.3.4 Pb isotope analysis
Ring-billed gull liver samples (n = 87) were freeze-dried for two days and approximatively 15 mg (dw) was digested using a Teflon beaker in 250 !-tL of ultra-pure 16N HN03 at 65°C following methods described by Font et al. (2012) with minor adjustments. Briefly, after digestion of the liver sample, 150 !-tL of H202 (Optima grade, Fisher Scientific, Ottawa, Ontario, Canada) was added to digest any additional organic materials left in the solution and after 24h, it was evaporated for at !east 12h at 100°C. Pb was extracted from samples using an ion-exchange column filled with AG 1-X8 resin (Analytical grade, Bio-Rad, Mississauga, Ontario, Canada) in HBr/HCl (Manhes et al., 1978). Procedural blanks were added at all steps of these measurements and Pb content in blanks were al ways found to be below 1% of the ring-billed gullliver samples.
Pb stable isotope ratios (2°8Pb/ 204Pb, 207PbJ2°4Pb, 206PbJ2°4Pb, 207Pb/ 206Pb, and 208PbJ2°6Pb) were determined using a multi-collector inductively coup led plasma
mass spectrometer (MC-ICP-MS, NuPlasma 11) in static mode with a Cetac Aridus II desolvating membrane as introduction deviee, yielding a transmission of better than
800V/ppm Pb on Faraday cups equipped with 1011ohms resistors. Pb isotope measurements in liver samples and blanks were obtained from 1 mL of diluted HN03
(2%, volume ratio) that contained 1.25 ppb Thallium (SRM997, NIST, Gaithersburg, Maryland, United-States) for instrumental mass bias evaluation (Belshaw et al., 1998; Woodhead, 2002). The Pb isotope standard NIST-SRM-981 (National Institute of
Standards and Technology, Gaithersburg, Maryland, USA) was used to bracket the Pb sample measurements and determine the relative mass biases between Pb and
thallium (Woodhead, 2002) for a given analytical sequence. Measurement of Pb isotope ratios in an in-bouse Pb standard (CGPB-1) was used to verify data accuracy,
and showed that all 204Pb-normalized ratios were within the laboratory's long term
extemal reproducibility (+/- 0.005).
2.3.5 Statistical analysis
The assumptions of normality and homogeneity of variance were tested using the Shapiro-Wilk and Levene's tests, respectively. A log10-transformation was applied to Pb and REE concentrations when necessary to meet the assumption of normality. Mean element concentrations were generated only for elements that were above the method limits of quantification (MLOQs) in at least 60% of the liver samples. Arithmetic means are presented with confidence intervals that represent
±
1 standard error of the mean (SEM). This approach was selected rather than the standarddeviation because it is a better estimate of how close the means from this study are from the true population mean (Streiner, 1996).