Photothérapie dans le traitement des dermatoses 57 cas
Texte intégral
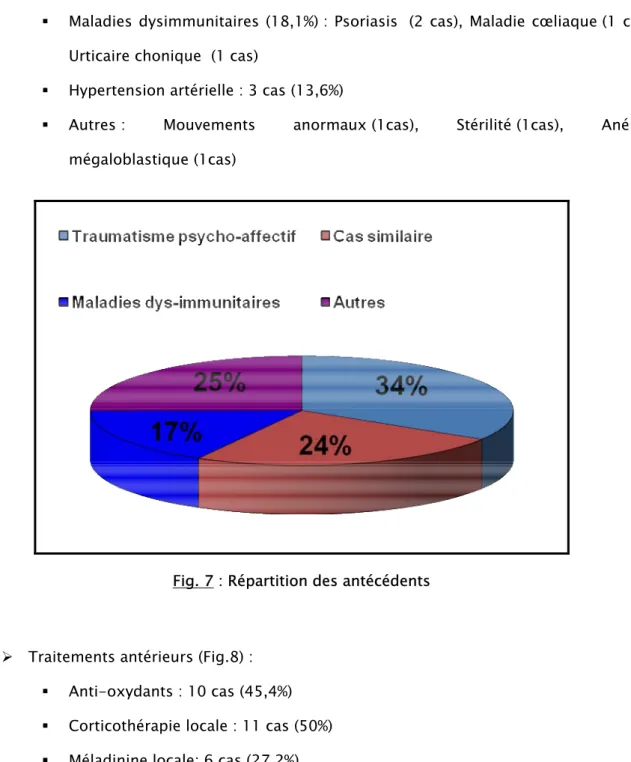
Figure



Outline
Documents relatifs
The blood pressure of the patient presented did not fall in early pregnancy, in contrast to the response expected in normal pregnancy even in women with chronic hypertension
Arthur (1966) has shown that one factor in this process is associative learning. H e theorizes that "after finding and parasitizing a few hosts of a particular
La technologie développée par Brochier Technologies de tissage de fibres optiques avec un traitement de surface spécifique pour obtenir une émis- sion latérale de lumière,
El Programa Papa Andina/ Innovación y Competi- tividad de la Papa (INCOPA) (www.papandina.org) del Centro Internacional de la Papa (CIP), en alianza con más de veinte socios del
Analytic S matrix theory elastic amplitude dominated at large s by singularities in the complex j plane in the case of simple poles simple poles imply cuts unknown functions
Dans notre série, l’âge moyen de nos patients est de 46,7 ans, avec des extrêmes à 23 à 54 ans, 12 patients étaient de sexe masculin ; il s’agissait de 11 patients DT2,
D’autres indications médicales de la PDT émergent de la littérature, donnant ainsi un véritable espoir pour demain dans des domaines aussi différents que les infections
intra-tumorale. de ta survie.. Pour les stades Okuda III, toutes les series japonai- ses et européennes [6,14,16] s'accordent sur l'inefficacité de tout traitement et





