Toxidermies médicamenteuses graves : expérience du service de dermatologie CHU Mohamed VI
Texte intégral
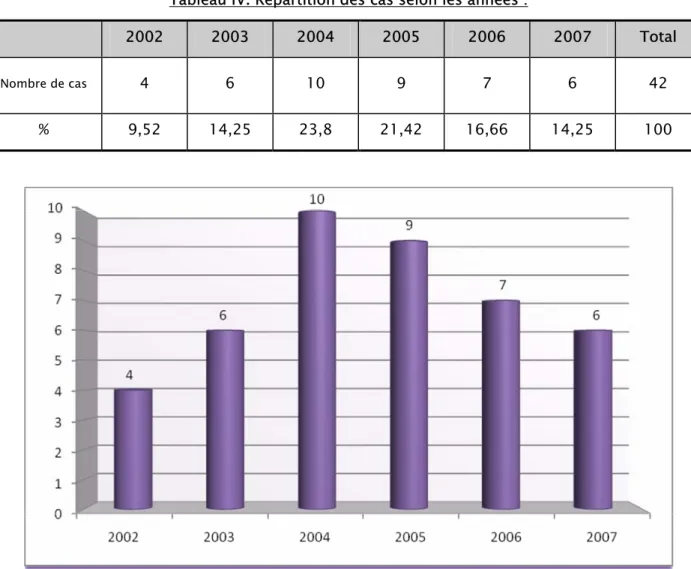
Figure


Documents relatifs
Notre étude descriptive a pour but de déterminer la fréquence et les caractéristiques cliniques et étiologiques des pleurésies hospitalisées au service de pneumologie de l’hôpital
Second primary tumors in patients with head and neck squamous cell carcinoma. Kaanders J,
En effet, cette étude, qui a inclus pour l’essentiel des patients en bas grade ayant des anévrysmes de la circulation cérébrale antérieure a mis en évidence une diminution du
Le but de notre travail est d’analyser les résultats du traitement chirurgical des cals vicieux du radius distal dans notre série et ses conséquences sur la
Les critères d’inclusion des patientes : toutes les patientes opérées pour un cancer du col utérin prouvé histologiquement et sont exclues les patientes qui n’ont pas
Nous avons donc formulé les questions afin d’essayer d’explorer certains aspects de la pratique de la médecine générale, du point de vue du médecin généraliste lui-même, qui
Le stade C de Balthazar était le plus fréquent chez plus de 25 cas, le score de Ranson a été inférieur à 3 chez 67 malades (78,8%), le score de BISAP était à 1 chez 32 cas, ainsi
Au Maroc, la tuberculose ganglionnaire est toujours en hausse [7], son diagnostic repose le plus souvent sur l’histologie malgré le progrès qu’a connue la microbiologie