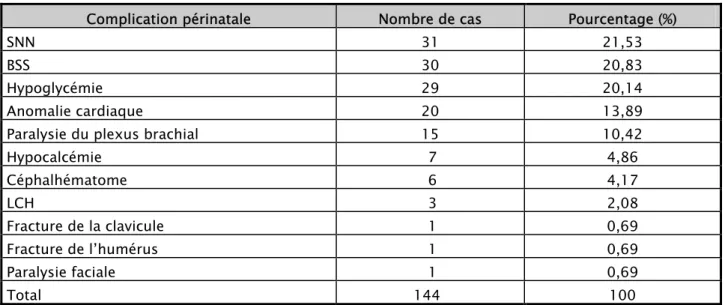
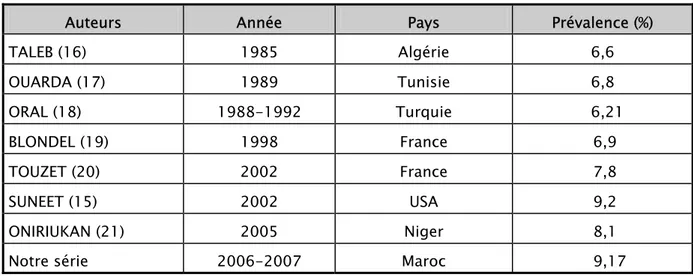
Macrosomie : à propos de 139 cas
93
0
0
Texte intégral
Figure
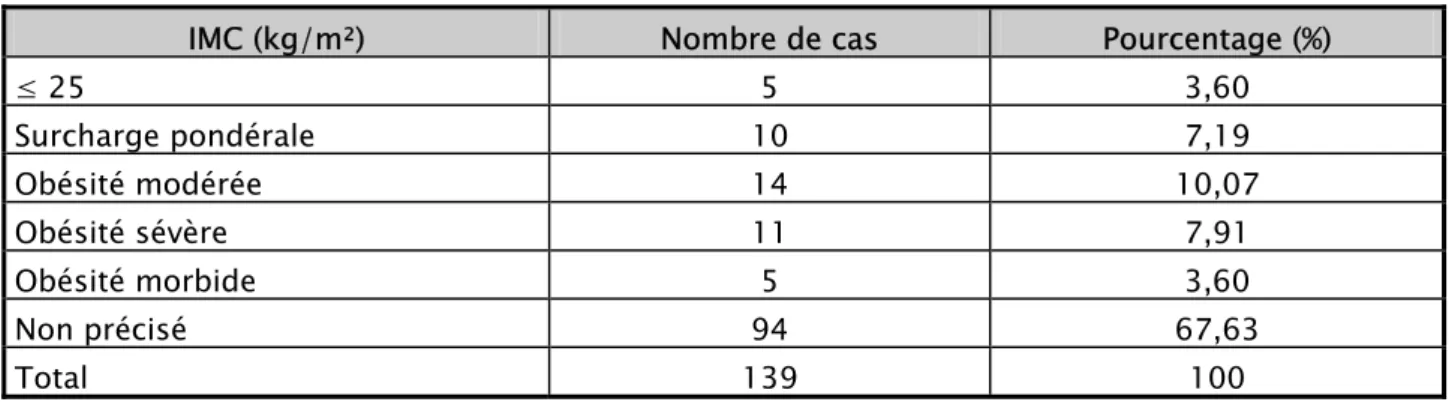
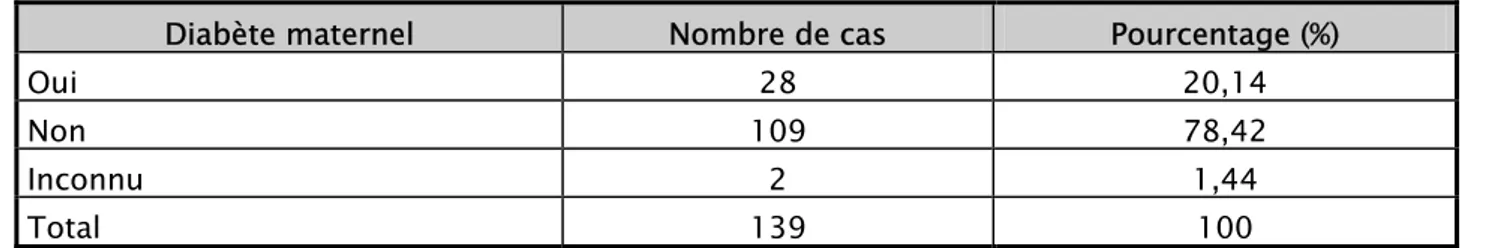
+7
Outline
Documents relatifs