© Sarah Beausoleil, 2019
Évolution fonctionnelle et clinique d'individus ayant une
amputation du membre inférieur
Mémoire
Sarah Beausoleil
Maîtrise en kinésiologie - avec mémoire
Maître ès sciences (M. Sc.)
ii
Évolution fonctionnelle et clinique d’individus
ayant une amputation du membre inférieur
Mémoire
Sarah Beausoleil
Sous la direction de :
iii
Résumé
L’utilisation d’une nouvelle prothèse à la suite d’une amputation d’un membre inférieur (MI) demande une ré acquisition de la capacité de marcher, ce qui peut mener à différentes stratégies de mouvement. Malgré les connaissances actuelles des stratégies de mouvement employées chez la population des individus ayant une amputation du MI (IA), aucune étude n’a évalué leur évolution lors d’un exercice de marche prolongée et à la suite d’un retour en milieu écologique. Pourtant, une diminution des performances à la marche pourrait être observée suivant l’apparition de la fatigue et/ou suivant une diminution du temps alloué aux activités physiques quotidiennes. C’est pourquoi l’objectif de cette étude est de quantifier les paramètres de marche des IA 1) lors d’un test de marche de six minutes (TM6) à la fin de leur réadaptation et 2) lors d’un TM6 six semaines suivant la fin de leur réadaptation. Nous posons l’hypothèse que l’ajout de centrales inertielles lors de l’évaluation de la marche des IA en milieu clinique permettra de caractériser les stratégies adoptées. Nous nous attendons à une dégradation de ces paramètres sur une période de six minutes de marche en continu ainsi que sur une période de six semaines suivant la fin des traitements de réadaptation. Pour ce faire, des centrales inertielles ont été utilisées, puisqu’elles permettent de quantifier les paramètres spatio-temporels et cinématiques de la marche dans différents environnements et populations, permettant l’acquisition de données « sur le terrain ».
Au total, 17 IA on fait le TM6 à T1 et T2 avec des centrales inertielles posées sur chacun de leur pied pour enregistrer leurs paramètres de marche (c.-à-d. dégagement minimal des orteils (minTC), phase de chargement (LDr), phase de pied plat (FFr), largeur de pas en phase oscillante, longueur de foulée, vitesse et cadence). Une analyse ANOVA non paramétrique a comparé 1) l’évolution des paramètres de marche sur une période de six minutes et 2) l’évolution des paramètres de marche entre T1 et T2. Un test de Wilcoxon des rangs signés a été exécuté lorsqu’une interaction était détectée dans l’ANOVA (P < 0.05).
Contrairement à l’hypothèse posée en début de projet, une amélioration des performances au membre prothétique (AL) entre T1 et T2 a été observée (largeur de pas en phase d’oscillation,
iv
vitesse et cadence augmentées, et la phase d’appui diminuée). Cependant, le minTC n’a pas évolué proportionnellement à la vitesse de marche.
Finalement, les capacités physiques et à la marche se sont améliorées entre T1 et T2 dans la population des IA malgré une incapacité d’adapter leur minTC (c.-à-d.., d’augmenter le minTC proportionnellement à la vitesse de marche) à l’augmentation de leur vitesse de marche. Ce phénomène pourrait être expliqué par un patron de marche déficient utilisant la stratégie de « hip
hiking » caractérisé par un large minTC et petite largeur de pas à T1 qui s’est amélioré à T2.
Toutefois, un petit minTC est aussi relié à un plus grand risque de chute. Ainsi, l’évaluation des paramètres de marche des IA en milieu clinique de même qu’un programme de réadaptation à distance ciblant l’amélioration des paramètres de marche en lien avec la réduction du risque de chute est primordial pour assurer un retour sécuritaire en communauté.
v
Abstract
The use of a new prosthetic limb following a lower limb amputation demands a reacquisition of the ability to walk, leading to different gait strategies. Although those strategies have been identified in the lower limb amputee (LLA) population, no studies have assessed their evolution following a return in the ecological environment. Indeed, decreased gait performances could be observed following the onset of fatigue and/or a decline of the daily active time. Therefore, the aim of this study was to quantify the gait parameters of the LLA 1. Along a six-minute walk test (6MWT) following their rehabilitation and 2. Along a 6MWT six weeks following the end of the rehabilitation. It is hypothesized that the use of inertial sensors during the assessment of the IA’s gait parameters will allow the characterisation of their adopted gait strategies. We are expecting a deterioration of the gait parameters along a six-minute continuous walk and six weeks following the end of the rehabilitation treatments. To do so, inertial measurement units (IMU) have been used, as they are effective to quantify gait in different environments and populations, allowing data acquisition in “real-life”.
Seventeen LLA performed a six-minute walk test (6MWT) at T1 and T2 with inertial sensors fixed on both feet to register their gait parameters (i.e. minimum toe clearance (minTC), loading ratio (LDr), flat foot ratio (FFr), swing width, step length, speed and cadence). A non-parametric ANOVA compared 1) the evolution of the gait parameters over a 6MWT and 2) the evolution of the gait parameters over T1 and T2. Post-hoc Wilcoxon signed-rank tests were performed if a main effect was detected (P < 0.05).
A performance improvement on the amputated limb (AL) between T1 and T2 has been observed (swing width, speed and cadence increased, added to a decreased stance phase). However, the minTC did not evolve proportionally to the speed.
Physical capacity and walking abilities have increased between T1 and T2 in LLA population despite the inability to adapt their minTC (i.e. to increase the minTC proportionally to the gait
vi
speed) to an increased speed. It could be explained by a poor walking pattern using a hip hiking strategy including a high minTC and a small step width at T1 that improved (lower minTC than at T1) at T2. However, a small minTC is related to higher risks of fall. Therefore, the evaluation
of the LLA’s gait parameters in clinical settings added to a home rehabilitation programme focused on the reduction of the risks of fall is primordial to ensure a secure return in the community.
vii
Table des matières
Résumé ... iii
Abstract ... v
Table des matières ... vii
Liste des tableaux ... ix
Liste des figures ... x
Liste des abréviations ... xi
Remerciements ... xiii
Avant-propos ... xiv
Introduction ... 1
Chapitre 1 : Mise en contexte et cadre théorique de l’étude ... 4
Amputation du membre inférieur ... 4
Étiologie ... 5
Appareillage ... 8
Limitations fonctionnelles ... 16
Chapitre 2 : Problématique et objectifs de l’étude ... 18
Quantification de la capacité fonctionnelle des individus ayant une amputation du membre inférieur en milieu clinique ... 18
Évaluations fonctionnelles actuelles ... 18
Principaux avantages des tests fonctionnels actuels ... 20
Limites principales des tests fonctionnels actuels ... 20
Objectifs de l’étude ... 21
Hypothèses de recherche ... 22
Chapitre 3 : État de l’art de l’analyse spatio-temporelle de la marche ... 23
Évaluation de la marche... 23
Description de la marche ... 25
Identification des paramètres d’intérêts à la marche chez les individus ayant une amputation du membre inférieur ... 27
Paramètres cinématiques et spatio-temporels de la marche ... 27
Chutes ... 30
Influence du type de prothèses lors de la marche... 31
Quantification de la marche : du laboratoire au milieu clinique ... 34
Description technique des centrales inertielles ... 39
Accéléromètres ... 39
Gyroscopes ... 41
Magnétomètres ... 42
Centrale inertielle utilisée dans le cadre de cette étude ... 43
Chapitre 4 : Méthodologie générale ... 44
Population étudiée ... 44
Parcours des participants lors de leur réadaptation à l’IRDPQ ... 44
Critères d’inclusion à l’étude ... 46
Instrumentation ... 46
Centrales inertielles ... 46
Cardiofréquencemètre ... 48
Mesures de perception des participants ... 49
viii
Analyse générale des données ... 52
Chapitre 5 : Situation des articles dans le mémoire ... 54
Chapitre 6 : Evolution of Gait Parameters in Individuals with a Lower-Limb Amputation During a Six-Minute Walk Test ... 56
Résumé. ... 56
Abstract. ... 57
Introduction ... 58
Material and methods. ... 60
Apparatus ... 62
Procedures ... 62
Data analysis ... 63
Statistical analysis ... 64
Results ... 64
Evolution of HR during the 6MWT ... 66
Functional Level and Pain ... 67
Discussion ... 67
Evolution of Gait Parameters Over the 6MWT ... 67
Evolution of HR during the 6MWT ... 68
Functional Level and Pain ... 68
Limitations 69 Conclusions ... 69
Chapitre 7: Assessment of Gait Characteristics Using Inertial Sensors: Evolution of Individuals with a Lower-Limb Amputation Post-Rehabilitation ... 73
Résumé. ... 73
Abstract. ... 74
Introduction ... 75
Material and methods. ... 76
Results ... 79
Discussion ... 83
Conclusion ... 85
Chapitre 8: Discussion Générale ... 88
Évolution des paramètres de marche sur une période de six minutes et sur six semaines ... 88
Paramètres spatio-temporels de la marche des IA ... 89
Paramètres cinématiques de la marche des IA ... 91
Niveau fonctionnel ... 92 Limites de l’étude ... 93 Participants ... 93 Évaluations ... 94 Instrumentation ... 94 Perspectives ... 95 Conclusion générale ... 96 Références ... 98
ix
Liste des tableaux
Tableau 1 Caractéristiques des pieds prothétiques ... 15
Tableau 2 Caractéristiques des genoux prothétiques ... 16
Tableau 3 Paramètres de marche connus chez une population IA ... 30
Tableau 4 Caractéristiques des participants ... 45
Tableau 5 Characteristics of the participants ... 61
Tableau 6. Kinematics characteristics of the amputated limb (AL), the non-amputated limb (NAL) and their interactions within the 6MWT (mean ± SD) intervals ... 65
Tableau 7. Characteristics of the participants – 2nd publication... 77
Tableau 8. Clinical and demographic data ... 80
Tableau 9. Gait parameters of the AL and NAL at in the first 30 seconds (I1) and the last 30 seconds (I12) of the 6MWT ... 82
x
Liste des figures
Figure 1. Niveaux d'amputation du membre inférieur ... 4
Figure 2. Incidence de l'amputation du membre inférieur au Canada entre 2006 et 2012 ... 5
Figure 3. Exemple de la constitution d'une prothèse pour IATT ... 8
Figure 4. Angles articulaires aux hanches, genoux et chevilles chez les IATT, IATF et individus sains ... 10
Figure 5. Schématisation des pieds prothétiques mono-axial, bi-axial et à restitution d'énergie ... 11
Figure 6. Les divisions du cycle de marche. ... 25
Figure 7. Phases du cycle de marche ... 27
Figure 8. Systèmes de suspension pour prothèses trans-tibiales. ... 32
Figure 9. Évaluations cliniques versus valeurs de référence: Mesures subjectives, semi-subjectives et objectives ... 35
Figure 10. Zone d’acquisition du mouvement... 35
Figure 11. GAITRite®, NJ, US. ... 38
Figure 12. Schéma des étapes de calibration standard des accéléromètres ... 41
Figure 13. Référentiel du gyroscope versus référentiel inertiel ... 42
Figure 14. Centrales inertielles Gait Up ... 43
Figure 15. Centrale inertielle : orientation des axes et polarité de rotation ... 47
Figure 16. Centrale inertielle Physilog® 4 ... 48
Figure 17. Cardiofréquencemètre Polar RS800CX ... 48
Figure 18. Diagramme de la répartition des tests sur 6 mois ... 50
Figure 19. Parcours du 6MWT ... 51
Figure 20. Diagramme de mouvement du nombre de participants ... 51
Fig. 21. Rehabilitation program design. ... 60
Figure 22 Two inertial sensors (Physilog®4, Lausanne) worn on both feet. ... 63
Figure 23 Relative treatment effect along the 6MWT for each intervals of 30 seconds ... 66
Figure 24. Comparison of I1 and I12 at T1 and T2 on AL and NAL. ... 81
Figure 25. Distance moyenne parcourue lors du TM6 aux T1 et T2 ... 89
Figure 26. Proportion de la phase d'appui du cycle de marche (%) lors des 12 intervalles de 30 secondes du TM6 ... 90 Figure 27. Cadence, largeur d'oscillation, vitesse de marche et minTC (AL et NAL) aux T1 et T2 91
xi
Liste des abréviations
3D : Tridimensionnel/ trois dimensions 6MWT: Six-Minute Walk Test
AMP: Amputee Mobility Predictor©
AMPPRO: Amputee Mobility Predictor© (avec utilisation de la prothèse) AMPnoPRO: Amputee Mobility Predictor© (sans utilisation de la prothèse) AL : Membre prothétique (prosthetic limb)
AP : Activités physiques
AVC : Accident vasculaire cérébral AVQ : Activités de la vie quotidienne CI : Contact initial
CdM : Centre de masse
EVA : Échelle visuelle analogue FA: Feet adjacent
FFr : Phase de pied plat (flat foot ratio)
GRF : Force de réaction au sol (ground reaction force) HRe : Fréquence cardiaque (heart rate)
HR: Heel rise
I1-I12 : Intervalle 1 à intervalle 12 IA : Individus ayant une amputation
IATT : Individus ayant une amputation trans-tibiale IATF : Individus ayant une amputation trans-fémorale IC: Initial contact
IMU: Centrale inertielle (inertial measurement unit)
IRDPQ : Institut de réadaptation en déficience physique de Québec
K0-K5 : Classification des niveaux fonctionnels de 0 à 5, selon Medicare, États-Unis LL: Lower limb
LLA: Lower Limb Amputees
LDr : Phase de chargement (loading ratio) LP : Période de latence (latency period) MAP : Maladie artérielle périphérique
maxHC : Dégagement maximal du talon (maximum heal clearance)
maxTC1 : Premier dégagement maximal des orteils (first maximal toe clearance) minTC : Dégagement minimal des orteils (minimum toe clearance)
MI : Membre inférieur
MOCAP : Capture de mouvement (motion capture) MPOC : Maladie pulmonaire obstructive chronique NAL: Membre biologique (biological limb)
OI: Opposite initial contact OT: Opposite toe-off
PPA: Prosthetic Profile of the Amputee Pur : Phase de poussée du pied (push ratio) SACH: Solid Ankle Cushion Heel
SF-12: Short Form Health-Survey questionnaire SF-36: Long Form Health-Survey questionnaire T1-T3 : Temps 1 à temps 3
TO: Toe-off
xii TUG: Time up and go
TV: Tibia vertical
xiii
Remerciements
La réalisation de ce mémoire a été possible grâce à des personnes m’étant chères et étant dotées d’innombrables qualités. C’est pourquoi j’ose vous voler un instant dans cette lecture pour rapidement les remercier.
Tout d’abord un immense merci à Katia Turcot, directrice de ce projet. M’étant une référence précieuse au niveau académique, tu as été un modèle dans toutes les sphères de la vie d’une petite étudiante qui ne savait pas assez se faire confiance.
Également, un énorme merci à tous les mentors que j’ai rencontrés sur mon passage au CIRRIS, qui m’ont nourri de motivation et de connaissances. Je remercie aussi l’équipe de recherche dans laquelle j’ai eu la chance de grandir, Ludovic Miramand, Hananeh Younesian, Vincent Richard, Thomas Legrand et Cassandra Gélinas.
Je remercie le comité directeur du Fonds Claude-Bouchard-et-Monique-Chagnon, qui m’a permis d’être l’heureuse récipiendaire d’une bourse d’excellence et d’implication dans le milieu de la kinésiologie. Cette première bourse d’excellence m’a procuré une motivation inégalable pour la poursuite de mon cheminement académique.
Sur une note plus personnelle, il me serait impensable de ne pas remercier mes parents, ma grand-mère Monette et Hugues pour leur support (même quand j’étais moins supportable). La « fiole » désire aussi remercier Pierre et Nicole, pour tout ce qu’ils sont et tout ce qu’ils représentent à mes yeux, ainsi que pour les conseils et la sagesse qu’ils m’apportent, notamment lors de nos rencontres formelles du dimanche.
En terminant, merci à cet Homme qui a partagé avec moi tous ces moments, les faciles, mais aussi les moins roses. Te savoir à mes côtés dans toutes les situations m’a permis d’évoluer encore plus remarquablement.
xiv
Avant-propos
Evolution of Gait Parameters in Individuals with a Lower-Limb Amputation During a Six-Minute Walk Test
Beausoleil Sarah, Miramand Ludovic, Turcot Katia
Cet article a été soumis à la revue scientifique Gait & Posture le 2018/09/5.
Tous les auteurs ont donné leur approbation pour ce manuscrit. Sarah Beausoleil et Ludovic Miramand ont participé à la collecte de données sous la supervision de Dr Katia Turcot. L’article a principalement été rédigé par Sarah Beausoleil.
Assessment of Gait Characteristics Using Inertial Sensors: Evolution of Individuals with a Lower-Limb Amputation Post-Rehabilitation
Beausoleil Sarah, Miramand Ludovic, Turcot Katia
Cet article a été soumis à la revue scientifique Gait & Posture le 2018/11/01.
Tous les auteurs ont donné leur approbation pour ce manuscrit. Sarah Beausoleil et Ludovic Miramand ont participé à la collecte de données sous la supervision de Dr Katia Turcot. L’article a principalement été rédigé par Sarah Beausoleil.
1
Introduction
Au Canada, entre 2006 et 2009 1, l’amputation du membre inférieur (MI) représentait 5,342 chirurgies réparties dans 207 centres hospitaliers et centres de réadaptation et touchait principalement les hommes (68%) de 67 ± 13 ans. La majorité de ces chirurgies provient de complications du diabète (81%), d’une maladie cardiovasculaire (6%) ou d’un cancer (3%). Plus précisément, les principales causes d’amputation du MI au Canada sont le diabète, l’hypertension, la cardiopathie ischémique, l’insuffisance cardiaque et l’hyperlipidémie. Ce type d’amputation a un impact important sur la diminution des capacités fonctionnelles, dont la marche. En effet, l’amputation d’un MI cause une altération de la marche des individus, notamment en perturbant l’équilibre, la mobilité et le potentiel ambulatoire 2-4.
Une marche dite « normale » est considérée comme l’une des habilités motrices les plus importantes de l’être humain puisqu’elle permet de maintenir la mobilité et l’indépendance. Des facteurs tels qu’une difformité fonctionnelle des tissus (ex. contracture musculaire, gonflement articulaire), une faiblesse musculaire (ex. force musculaire insuffisante pour répondre aux exigences de la marche), une perte de sensibilité (ex. diminution de la proprioception, neuropathie), de la douleur et un contrôle moteur altéré sont connus pour créer des anormalités de la marche et favoriser l’adoption de stratégies compensatoires 5 pouvant, à long terme, mener à une perte d’autonomie. Ainsi, l’évolution du potentiel ambulatoire de la personne amputée après avoir suivi une réadaptation en centre, qui est encore peu connue, pourrait dépendre de ces facteurs.
L’évaluation quantitative de la marche de la personne amputée est habituellement effectuée en laboratoire à l’aide de technologies permettant une analyse précise du mouvement, notamment de la cinématique et des paramètres spatio-temporels de la marche. Les électrogoniomètres et les systèmes d’analyse de mouvements basés sur des systèmes optoélectroniques à une ou plusieurs caméras sont parmi les technologies les plus utilisées 5. Cette quantification permet l’obtention de paramètres de marche précis au niveau des articulations et segments ainsi que de façon globale
2
en étudiant les mouvements du corps dans son ensemble. Malgré ces avantages, ces systèmes de mesures ne sont pas adaptés à l’intervention clinique quotidienne en raison de leur complexité, du temps d’utilisation, de l’expertise requise, du besoin d’espace et de leur prix élevé.
À l’inverse, la marche chez l’amputé peut aussi être analysée qualitativement ou semi qualitativement en contexte clinique à l’aide de tests basés sur les observations des cliniciens, à l’œil nu ou avec l’utilisation d’un chronomètre et/ou de questionnaires. Ce type d’évaluation permet d’obtenir une distance de marche, un temps nécessaire pour parcourir une distance prédéterminée, ou encore la capacité ou non d’effectuer une tâche spécifique (par exemple se lever d’une chaise et marcher trois mètres). Toutefois, la variabilité intra- et inter-observateur(s) ainsi que le niveau de précision de ces résultats ne permet pas de représenter clairement les subtilités cinématiques et les paramètres spatio-temporels de la marche, les compensations et stratégies de mouvement utilisées chez cette population. De plus, ces tests permettent difficilement de quantifier l’évolution de la marche à deux périodes distinctes.
L’instrumentation des tests cliniques, par exemple à l’aide de centrales inertielles (c.-à-d. technologies permettant l’enregistrement d’accélérations linéaires à l’aide d’accéléromètres, de vitesses angulaires à l’aide de gyroscopes et de l’orientation du capteur à l’aide d’un magnétomètre) pourrait permettre l’obtention de données quantitatives lors d’évaluations cliniques permettant de quantifier l’évolution de la marche des IA pendant la réadaptation ainsi que lors de leur retour en milieu écologique suivant la réadaptation.
Comme son titre l’indique, ce mémoire avait pour but d’étudier l’évolution fonctionnelle et clinique des IA. Cette évolution a été étudiée chez des IA terminant une réadaptation physique à la suite d’une amputation. L’étude s’est déroulée en deux temps, soit à la fin de leur traitement et six semaines suivant cette date afin de quantifier l’impact de l’arrêt des traitements de réadaptation et du retour en milieu écologique.
3
Dans ce mémoire, les capacités fonctionnelles (paramètres spatio-temporels et cinématique du pied par rapport au sol) des IA sont évaluées, via deux centrales inertielles lors de la marche.
Le premier chapitre de ce mémoire fait l’état des connaissances actuelles sur l’amputation du MI et sur l’évaluation de ce type de marche pathologique. Le deuxième chapitre introduit la problématique et les objectifs de l’étude. Le troisième chapitre présente une revue de la littérature en lien avec les paramètres d’intérêt à la marche chez les IA et la quantification de la marche à l’aide de centrales inertielles. La description technique des centrales inertielles utilisées dans cette étude s’y retrouve également. Le quatrième chapitre explique la méthodologie générale liée à ce mémoire. Le cinquième chapitre situe les deux articles réalisés lors de ce mémoire.
Les chapitres subséquents présentent les deux articles écrits dans le cadre de cette maîtrise. Le premier article porte sur la caractérisation de la marche chez les IA sur un test de marche de six minutes (TM6). Le deuxième article présente l’évolution des paramètres de marche chez les IA entre la fin des traitements de réadaptation en centre et six semaines suivant leur retour en milieu écologique.
Le huitième chapitre consiste en une discussion générale résumant les liens entre la revue de littérature (chapitre 3) et les résultats des deux articles (chapitre 6 et chapitre 7) présentés dans ce mémoire. Les limites et perspectives de l’étude y sont également présentées.
4
Chapitre 1 : Mise en contexte et cadre théorique de l’étude
Ce premier chapitre permettra de mettre en contexte et de poser un cadre théorique sur plusieurs éléments essentiels à la compréhension de ce projet, c’est-à-dire la définition et l’épidémiologie de l’amputation du MI, les types d’appareillages utilisés et les limitations fonctionnelles de cette population.Amputation du membre inférieur
L’amputation représente l’ablation d’un membre ou d’un segment de membre. Elle peut être volontaire lorsqu’un acte chirurgical doit être pratiqué pour éviter que des affections incurables se propagent dans le corps (ex. gangrène) ou involontaire lors d’un traumatisme ou d’une amputation congénitale. L’ablation chirurgicale d’une partie d’un MI au niveau trans-fémoral ou trans-tibial représente un enjeu substantiel relié aux capacités fonctionnelles des individus. Pour procéder à un tel acte, l’état d’un patient doit présenter un risque majeur pour sa santé.
Figure 1. Niveaux d'amputation du membre inférieur
Trans-tibial Désarticulation Trans-fémoral Désarticulation du genou de la hanche
5
Les amputations du MI sont divisées en plusieurs catégories, tel qu’illustré à la figure 1 : trans-fémorale, trans-tibiale, désarticulation à la hanche, désarticulation au genou et au niveau du pied. Plus le niveau d’amputation est proximal, plus l’impact sur les capacités fonctionnelles est élevé. De plus, l’amputation d’un MI engendre une augmentation de la dépense énergétique variant selon le niveau d’amputation, le type de prothèse utilisé et l’alignement de ses composantes 6.
Ainsi, une augmentation de la dépense énergétique de 10-40% peut engendrer une fatigue précoce lors de tâches fonctionnelles, notamment à la marche 7 et altérer le mouvement.
Étiologie
Entre le 1er avril 2006 et le 31 mars 2012, il y a eu 44,430 amputations du MI au Canada (fig. 2) 8. L’âge moyen lors de ces amputations étaient de 65.7 ± 16.6 ans et 68.8% étaient des hommes.
Les amputations trans-tibiales sont les plus communes et comptent pour plus de 30.9% des amputations du MI. Le diabète représentait la cause principale d’amputation du MI (65.4%). Au Québec, pendant cette période, 9,312 amputations du MI ont été réalisées, soit 21% des amputations totales au Canada 8.
Les causes de l’amputation d’un MI sont variées. En 1992, Ebskov a classifié les amputations selon quatre causes principales : trouble vasculaire, diabète, traumatisme et cancer. Déjà à ce
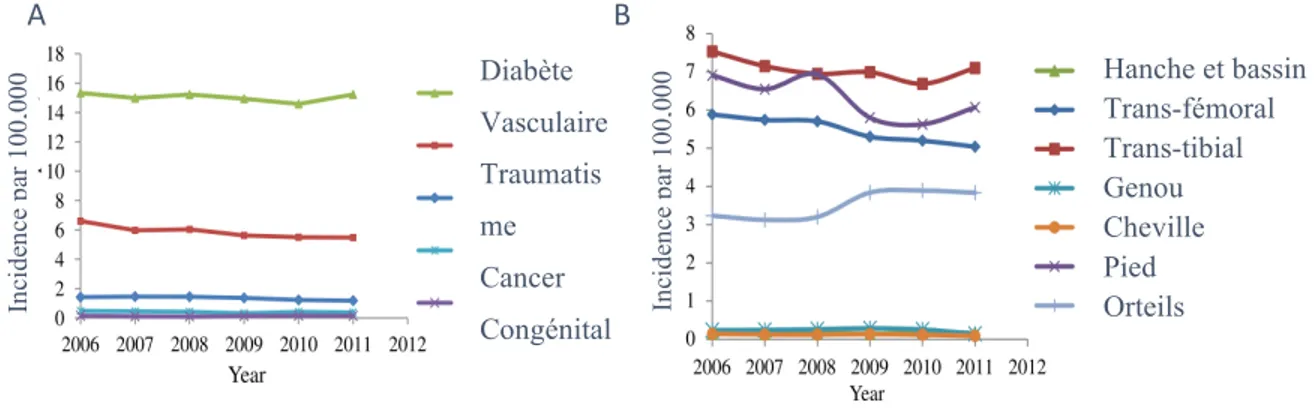
A B Inc ide nc e pa r 10 0, 000 Inc ide nc e pa r 10 0, 000 Diabète Vasculaire Traumatis me Cancer Congénital Hanche et bassin Trans-fémoral Trans-tibial Genou Cheville Pied Orteils
Figure 2. Incidence de l'amputation du membre inférieur au Canada entre 2006 et 2012 (Imam et al., 2017) A) Taux d’incidence d’amputation du membre inférieur par cause d’amputation pour 100,000 habitants. B) Taux d’incidence de l’amputation du membre inférieur par niveau d’amputation pour 100,000 habitants.
6
moment, les problèmes de type vasculaire en étaient majoritairement la cause 9. Le nombre élevé
d’amputations de type vasculaire est lié au diabète, au tabagisme, à l’hypertension et à l’hypercholestérolémie 10. En 2005, ce type d’amputation représentait la majorité de toutes les
causes confondues (94.3%) dont 86.5% étaient dues à des maladies artérielles périphériques. Les autres 5.7% sont reliés à des traumatismes, au cancer, à des fractures s’étant compliquées en ostéomyélites (c.-à-d. une inflammation de la moelle osseuse et du tissu osseux adjacent causée par une infection) ou sont de causes congénitales 11. Comparativement aux amputations de type
vasculaire, les amputations de type traumatique représentent une plus petite proportion, étant la deuxième cause principale d’amputation. De 1940 à 1960, cette catégorie représentait 20-30% du nombre total d’amputations 12 et en 2011, on retrouvait un ratio d’amputations vasculaires
contre traumatiques de 7.88 pour une, respectivement 13. Finalement, les amputations dues à des
déficiences congénitales sont maintenant répertoriées et comptent pour 0.8 % de toutes les amputations 10.
Le risque d’amputation est augmenté avec l’âge, et ce, indépendamment des types d’amputations, de l’ethnicité et du sexe. La moyenne d’âge des IA du Canada entre 2006 et 2009 était de 67 ± 13 ans 1. Les hommes semblent aussi être plus à risque d’amputation que les femmes, surtout
dans les cas vasculaires et traumatiques (68% des IA au Canada 1) 10, 14. Suivant cette amputation,
la majorité des patients doivent être suivis dans des établissements de soins de longue durée (65%) et une minorité est retournée à leur domicile suivant l’opération (27%) 1.
En 1995, Medicare aux États-Unis a adopté un système de classification du niveau fonctionnel des IA à cinq niveaux (K0, K1, K2, K3, K4). Avec ce système, les physiothérapeutes et prothésistes déterminent le potentiel du patient à atteindre « un état fonctionnel défini dans une période de temps raisonnable » 15.
- K0 : N’a pas les capacités ou le potentiel de se déplacer ou de transférer de façon sécuritaire avec ou sans assistance et une prothèse n’améliore pas la qualité de vie ou la mobilité.
7
- K1 : A les capacités ou le potentiel d’utiliser une prothèse pour les transferts ou pour se déplacer sur des surfaces planes à une cadence fixe. Typique des individus se déplaçant de façon limitée ou non dans leur domicile.
- K2 : A les capacités ou le potentiel de se déplacer et de traverser de petits obstacles environnementaux tels que des trottoirs, des escaliers ou des terrains accidentés. Typiques des individus se déplaçant de façon limitée en communauté.
- K3 : A les capacités ou le potentiel de se déplacer a des cadences variables. Typique des individus se déplaçant en communauté ayant les capacités de traverser la majorité des barrières environnementales et peuvent avoir une vocation, une thérapie ou des activités physiques qui requièrent une utilisation prothétique allant plus loin que la simple locomotion.
- K4 : A les capacités ou le potentiel pour une utilisation prothétique excédant les compétences liées à la locomotion, démontrant de forts impacts, stress ou niveaux d’énergie. Typique de la demande prothétique des enfants, des adultes actifs ou des athlètes.
Le potentiel de réadaptation des AI est intimement lié à leur condition initiale, incluant les comorbidités. Une comorbidité se définit comme toute condition clinique additionnelle et distincte du principal problème de santé (c.-à-d. l’amputation), qui existait avant ce dernier ou pouvant survenir lors du parcours clinique du patient 16. De nombreuses comorbidités sont
retrouvées chez les IA : maladie artérielle périphérique (MAP) (83%) 16, obésité (57.21%),
diabète (48.32%), arthrite (28.86%), dépression (15.77%), troubles visuels (13.09%), dégénérescence des disques (12.75%), anxiété/troubles paniques (11.58%), maladies gastro-intestinales (9.23%), crise(s) cardiaque(s) (8.05%), troubles auditifs (6.88%), maladies pulmonaires obstructives chroniques (MPOC) (5.87%), infarctus (4.70%), asthme (4.20%), angine (3.02%), ostéoporose (2.35%) 17, 18. Les comorbidités prédictives du niveau de mobilité
sont l’âge, l’histoire d’accident vasculaire cérébral (AVC), MAP et l’anxiété/ les troubles paniques (R = 0.388) 18. En effet, les IA ayant souffert d’AVC, de MAP ou d’anxiété/troubles de
8
Figure 3. Exemple de la constitution d'une prothèse pour IATT
(http://streams.univlyon1.fr/videoStream/streams/lyon1/modules/59093/files/188543_1380a3fce4a.jpg)
0.022, respectivement) ainsi qu’aux autres IA ayant des comorbidités autres que cette comorbidité (P = 0.001, 0.001 et 0.011, respectivement). Les IA de 65 ans et plus avaient une mobilité réduite comparativement aux plus jeunes (P = 0.001) 18. Aussi, cinq pourcents des IA
n’ont pas de comorbidité, 16% des IA ont une comorbidité, 20% des IA ont deux comorbidités, 20% ont trois comorbidités, 17% ont quatre comorbidités, 10% ont cinq comorbidités, sept pourcents ont six comorbidités, cinq pourcents ont sept comorbidités et un pourcent a huit comorbidités 16. Ainsi, l’ensemble de ces comorbidités rend la population des IA très hétérogène
et son étude très complexe.
Appareillage
À la suite d'une amputation du MI, l’utilisation d’une prothèse à la marche est un élément important pour préserver l’indépendance 19. Ces aides à la marche sont normalement constituées
9
Pour assurer une réadaptation optimale, l’appareillage doit être effectué dans des conditions où le moignon du patient est rétabli à la suite de la chirurgie. Une augmentation du temps de guérison du moignon et une mobilité réduite à l’articulation proximale à l’amputation peuvent causer des délais d’appareillage prothétique 20. Des critères pré appareillage doivent être respectés : la
condition générale du patient, la cause de l’amputation, la longueur, la forme, la qualité de la peau, la mobilité et la douleur au moignon, le niveau de l’amputation, la présence de douleur fantôme et la charge maximale pouvant être soutenue par l’extrémité portante 21. De nouvelles
approches de mesures quantitatives standardisées de la santé du moignon utilisant la mesure d’oxygène transcutanée, la perfusion, la fonction de barrière de la peau, et l’hydratation de la peau sont maintenant utilisées 22. Lorsque ces critères sont atteints, le patient accède à une
prothèse transitoire qui permet l’activation du patient sans devoir attendre la réduction complète du volume du moignon. Elle permet aux patients de prévenir les complications secondaires à l’amputation résultant d’une immobilité pouvant être un facteur de risque chez la population âgée. Le port de la prothèse définitive est possible lorsque le volume du moignon est stabilisé. Pour l’instant, les prothèses préparatoires sont constituées des éléments de base d’une prothèse définitive, mais ont une apparence esthétique non finie. Le port de prothèses définitives requiert un entraînement préalable et les habiletés spécifiques pour l’utilisation de composantes avancées comme, par exemple, les genoux à microprocesseurs. Il a été suggéré 23 d’inclure ce type de
composantes dans la prothèse préparatoire et de ne modifier que l’emboîture selon le changement de volume du moignon. De cette façon, les performances à la marche, la stabilité et la sécurité seraient améliorées et le développement de mauvaises compensations liées à l’utilisation de prothèses préparatoires pourraient être évitées dans l’entraînement à la marche 23. Les sections
suivantes présentent les différentes composantes d’une prothèse du MI.
Pieds prothétiques
Les pieds prothétiques, de type actif ou passif, ont comme fonction principale de générer la puissance nécessaire à la marche. Ils sont propulsés par le mouvement du corps ou par l’effet de microprocesseurs intégrés au pied prothétique. Ils diffèrent d’une cheville biologique (fig. 4) principalement par une dépense énergétique supérieure causée par leur fonction limitée 24 ainsi
10
Les pieds prothétiques de type passif sont utilisés chez les individus ayant une capacité à la marche limitée (K1). Le plus simple de ceux-ci est le Solid Ankle Cushion Heel Foot (SACH) composé d’une cheville non articulée. Il permet une certaine souplesse avec un talon en mousse se compressant lors du contact initial du talon au sol et retournant à sa forme lors du moment de pousser du pied vers la phase d’oscillation.
Le pied mono-axial permet un mouvement de deux degrés de liberté à l’entour de l’axe médio-latéral avec une amplitude de mouvement de cinq à huit degrés en dorsiflexion et de 15-20° en flexion plantaire et permet une amélioration de l’extension au genou 25. Utile chez les individus
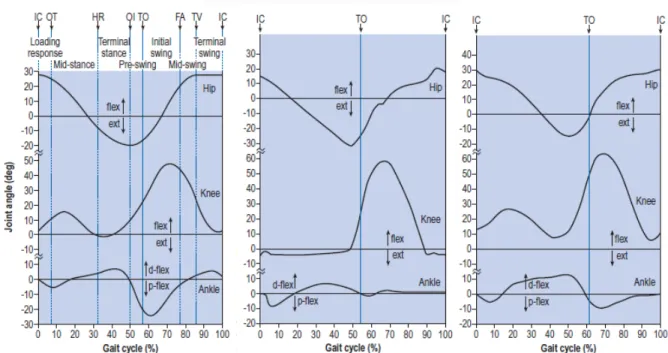
4c. Angles articulaires dans le plan sagittal lors d’un cycle de marche chez un IATT.
4b. Angles articulaires dans le plan sagittal lors d’un cycle de marche chez un IATF
4a. Angles articulaires dans le plan sagittal lors d’un cycle de marche au niveau de la hanche, du genou et de la cheville du côté droit chez un individu sain.
11
Figure 5. Schématisation des pieds prothétiques mono-axial, bi-axial et à restitution d'énergie
(http://streams.univ-lyon1.fr/videoStream/streams/lyon1/modules/59093/files/188543_1380a3fce4a.jpg)
ayant une faiblesse du quadriceps ou pour les individus ayant un genou prothétique manquant de stabilité lors de l’appui, ce pied augmente la stabilité au genou par l’amortissement supérieur à celui du SACH lors de l’attaque du talon au sol. Le pied prothétique multi-axial permet un mouvement similaire à celui permis par le pied mono-axial autour de l’axe médiolatéral tout en permettant également un mouvement autour de l’axe vertical et de l’axe antéro-postérieur 26 (fig.
5). Les mouvements permis autour de ces différents axes se rapprochent d’un mouvement naturel du pied tout en permettant une adaptabilité de la marche en terrains accidentés, ce qui rend ce type de pied prothétique accessible aux individus ayant un niveau fonctionnel supérieur (K2-K4)
27. Viennent ensuite les pieds à réponse élastique dynamique ou à restitution d’énergie. Ces
prothèses flexibles permettent de reproduire près de la moitié du travail de poussée d’un pied biologique par un système permettant d’emmagasiner et de libérer l’énergie 24. Finalement, les
pieds prothétiques passifs à microprocesseurs diminuent le ratio de chargement sur le membre prothétique et la résistance à la cheville est réglable selon la vitesse de marche de l’individu et le type de surfaces sur lesquelles la marche est généralement effectuée 28.
Les pieds prothétiques actifs sont de types propulsifs ou apropulsifs. Les prothèses apropulsives ont pour but d’augmenter le dégagement du pied par rapport au sol (minTC) en phase d’oscillation principalement en augmentant la dorsiflexion à la cheville. Les prothèses propulsives peuvent être munies de moteurs électroniques et de ressorts permettant une reproduction du mouvement de poussée de pied vers la phase d’oscillation 24. Le type de prothèse
12
de pieds à microprocesseurs comparé aux pieds passifs peut être jusqu’à 63% plus efficace lors d’une transition d’un pas à un autre pendant la marche, augmentant le degré de flexion plantaire à la cheville et la puissance de poussée. La raison pour laquelle, malgré ces avantages biomécaniques, le pied prothétique actif propulsif ne permet pas la reproduction totale de la fonction d’une cheville biologique est que la prothèse n’a qu’un effet mono-articulaire (cheville) et ne peut reproduire le mouvement créé par le gastrocnémien (muscle biarticulaire) 24.
Genoux prothétiques
Les genoux prothétiques, de type actif ou passif, ont comme fonction principale d’absorber les forces générées à la marche chez les individus ayant une amputation trans-fémorale (IATF) ou de niveau supérieur. Ils doivent également permettre une stabilisation en phase d’appui et de poussée tout en limitant la flexion au genou en phase d’oscillation.
Le genou prothétique mono-axial permet un mouvement de flexion-extension à l’articulation du genou en phase d’oscillation et une friction constante peut être établie pour augmenter la stabilité de la marche. Ce type de prothèse s’adresse principalement aux individus ayant une faible capacité à la marche puisqu’elle ne peut être ajustée qu’à des vitesses inférieures aux normes (K1). À l’inverse, le genou prothétique de contrôle d’appui permet une stabilité supplémentaire lors de la mise en charge sur la prothèse où un frein s’active. Le genou polycentrique est généralement composé de quatre axes de rotation (c.-à-d.. axe autour duquel tourne un solide à un instant donné), efficaces pour assurer une stabilité de marche par une projection instantanée du centre de rotation derrière le vecteur vertical des forces de réaction au sol (vGRF) lors de l’extension complète du genou. À l’inverse, après quelques degrés de flexion du genou, le centre de rotation instantané passe devant le vGRF, créant une flexion au genou de façon automatique. L’utilisation de ce type de genou permet donc une phase d’appui plus stable et une phase d’oscillation plus économique au niveau énergétique. Les genoux à verrouillage manuel sont contrôlés par l’utilisateur qui peut bloquer son genou. Créant une meilleure stabilité en phase d’appui, ce blocage demande une compensation lors du soulèvement du pied du sol pour permettre un dégagement du pied adéquat. Les genoux à contrôle hydraulique et pneumatique
13
créent une marche plus naturelle. Toutefois, les gaz contenus dans les genoux pneumatiques sont plus compressibles par rapport aux composantes hydrauliques, les rendant plus instables et moins conseillés chez les individus ayant une stabilité précaire. Des genoux hybrides sont également accessibles. Ils utilisent des composantes de différents types. Une combinaison populaire est le genou à contrôle hydraulique en phase d’oscillation joint à un genou polycentrique, permettant une démarche douce ainsi qu’un contrôle de la flexion du genou économique.
Les genoux prothétiques actifs, en plus de leur rôle d’absorption des forces générées à la marche, permettent une propulsion lors de différentes tâches, telle l’ascension en terrains accidentés.
Emboîtures
Lors du port de la prothèse, l’extrémité distale du moignon doit être protégée contre les différents impacts et forces créés à la marche. La forme interne des emboîtures permet une suspension du moignon sur ses parties solides supérieures aux reliefs de l’emboîture. Les emboîtures doivent permettre une attache rigide des parties distales du moignon, notamment au pied prothétique et au système de suspension (détaillé dans la section 1.1.2.4). Les emboîtures ont également une fonction de transfert d’énergie entre le moignon et le point de contact rencontré. Ces emboîtures peuvent être classées en trois catégories : emboîtures de support tendon rotulien, emboîture de support total et emboîture de conception hybride. Le premier type répartit la pression dans les zones plus tolérantes. Le deuxième type répartit les pressions de façon constante sur la doublure en gel. Le dernier type se base sur le principe des emboîtures de support tendon rotulien et des emboîtures de support total en répartissant les forces totales appliquées sur le moignon, mais également en diminuant la répartition de pressions dans des zones plus localisées. Un bon choix d’emboîture est essentiel pour assurer une symétrie de marche et donc un patron de marche se rapprochant de la norme 29.
14 Systèmes de suspension
Le port d’une prothèse engendre des forces de traction qui tendent à éloigner la prothèse du moignon lors de la marche. Les systèmes de suspension visent à diminuer cet effet de pistonnage. Ces systèmes visent également à minimiser les mouvements de translations et de rotations entre le moignon et le bas de la prothèse. Le mouvement du bas à l’intérieur de la prothèse est utilisé comme indicateur de la qualité du système de suspension pour les prothèses d’amputations trans-tibiales dans certaines études 30. Trois types de systèmes de suspension existent pour les
amputations trans-tibiales : les sangles anatomiques, les systèmes de suspension mécanique et les systèmes de suspension atmosphérique. Ces systèmes de suspension regroupent les systèmes de support de surface totale (systèmes de verrouillage, système de succion, système de verrou magnétique), de support tendon rotulien, supracondylaire et suprapatellaire. Aucun consensus n’a encore été obtenu en lien avec les recommandations de choix de type de prothèse selon la condition du patient ou de l’état du moignon. Certaines études 29, 31, 32 rapportent que les systèmes
de succion permettent de diminuer le déplacement du moignon à l’intérieur de la prothèse, diminuant ainsi l’asymétrie et la douleur à la marche en comparaison aux autres systèmes de suspension 31. Par contre, ces systèmes seraient plus difficiles à mettre et enlever 31. Les systèmes
de support total causeraient une augmentation de la transpiration au moignon. La prothèse de support total avec système de verrouillage est préférée des utilisateurs. Finalement, le choix du type de suspension est fait selon l’expérience du prothésiste avec les différents types de prothèses ainsi que le confort rapporté par le patient 29.
Quatre types de systèmes de suspension existent pour les IATF : les bandes pelviennes, les ceintures Silesian, les doublures de silicone ou les bas de succion. Ces systèmes d’attache incorporent l’articulation de la hanche. Aucun consensus de recommandations claires n’existe pour le choix du type de système de suspension 32.
Les systèmes d’ostéointégration consistent en une intervention chirurgicale permettant de fixer la prothèse à la jambe du patient. Cette intervention n’est toutefois pas très utilisée, notamment
15
à cause du temps de réadaptation supérieur comparativement aux systèmes de suspension non chirurgicaux ainsi qu’en raison du risque de fracture, d’infection et du prix élevé.
Prothèses utilisées par les participants de l’étude
Le choix du type de prothèse portée par les patients dépend de : leur niveau fonctionnel pré-morbide, leurs assurances, leurs besoins et de la perception des professionnels de la santé. Les types de pieds et genoux décrits ci-dessous sont tous conçus pour une utilisation sur des prothèses modulaires. Veuillez vous référer à l’Annexe A pour les fiches détaillées de chacune des composantes prothétiques décrites dans cette section.
Les tableaux suivants présentent les types de prothèses de pied (Tableau 1) et de genou (Tableau 2) utilisés par les participants dans le cadre de ce mémoire.
Tableau 1Caractéristiques des pieds prothétiques
Marque Modèle Niveaux
fonctionnels Masse maximale du patient Mouvements permis Ottobock® 1D10 K1-K2 150 kg Uniaxial Ottobock® 1C11 K1-K2 175 kg Multiaxiaux Ottobock® 1C63 K3-K4 150 kg Multiaxiaux
Ossür® Assure K1-K2 136 kg Multiaxiaux
Ossür® Pro-Flex XC K1 à K3 166 kg Multiaxiaux
16
Tableau 2 Caractéristiques des genoux prothétiques
Limitations fonctionnelles
L’amputation d’un MI est connue pour apporter plusieurs limitations fonctionnelles diminuant la capacité des IA à fonctionner adéquatement et de manière autonome en société. La limitation fonctionnelle se définit ici comme une atteinte permanente à l'organisme, qui l’empêche de remplir l'une ou l'autre des fonctions qu'il est normalement en mesure de remplir. C’est la limitation des mouvements articulaires considérés comme normaux.
Cet effet est illustré entre autres par un score fonctionnel post-réadaptation inférieur au score fonctionnel pré-morbide (précédant l’amputation) 33, une dépense énergétique supérieure lors de
la marche 34, une difficulté à effectuer des transferts, une capacité ambulatoire diminuée 35 ainsi
qu’une modification des paramètres de marche (ces paramètres seront détaillés au point 3.1.1.). Tel que retrouvé dans l’étude de Greive et Lankhorst 36, différents facteurs pourraient être
déterminants par rapport à l’impact fonctionnel d’une amputation du MI. Le diabète, présent chez une grande proportion des IA, représente un facteur négatif chez la population âgée, notamment en lien avec la plus grande incidence de réamputation y étant associée. L’âge des patients lors de l’amputation semble être un facteur significatif. Ce facteur pourrait expliquer l’effet et le nombre des comorbidités ainsi que le faible niveau de condition physique des patients. Le tabagisme, l’alcoolisme, l’indice de masse corporelle et la dépendance fonctionnelle préopératoire seraient
Marque Modèle Niveaux
fonctionnels Masse maximale du patient Angle maximal permis au genou Ottobock® 3R49 K1-K2 100 kg 150° Ottobock® 3R78 K2-K3 100 kg 150° Ottobock® 3R80 K3-K4 150 kg 150° Ottobock® X3 Genium K2-K3-K4 150 kg 135°
17
des facteurs prédictifs du statut ambulatoire suivant l’opération 35. La longueur supérieure du
moignon chez les IA ayant une amputation trans-tibiale (IATT) favorise aussi leur capacité de marcher de plus longues distances. L’effet est aussi observé chez les IA trans-fémoral (IATF), cependant cette association est plus faible. L’inverse est aussi vrai où, plus la longueur du moignon est courte, moins grandes sont les capacités fonctionnelles des IA. La motivation des IA reliée à leur réadaptation a aussi un impact positif/négatif sur les capacités fonctionnelles. Plusieurs autres comorbidités peuvent avoir un impact sur les capacités fonctionnelles des IA suite à une réadaptation telles que les maladies pulmonaires obstructives chroniques, les problèmes locaux au moignon, infarctus, contractures musculaires et différents troubles mentaux
18
Chapitre 2 : Problématique et objectifs de l’étude
Ce deuxième chapitre exposera la problématique de l’analyse de la marche des IA en milieu clinique ainsi que les objectifs de cette étude. Les sections de ce chapitre exposeront les méthodes actuelles d’évaluation clinique des conditions fonctionnelles des IA et débattront des avantages et limites de ces méthodes. En découlera la présentation des objectifs et hypothèses de l’étude.
Quantification de la capacité fonctionnelle des individus ayant une
amputation du membre inférieur en milieu clinique
À la suite d’une amputation du MI, le but principal de la réadaptation est un retour à des capacités fonctionnelles se rapprochant du niveau pré-morbide des IA. Pour évaluer ce niveau fonctionnel et son évolution au cours d’une réadaptation en centre, différents tests fonctionnels sont utilisés et/ou validés pour cette population. Les tests fonctionnels utilisés dans le cadre de ce mémoire sont des tests connus/validés et établis en réadaptation physique pour la population amputée.
Évaluations fonctionnelles actuelles
En plus des données anthropométriques telles que les mesures de poids, taille, âge et sexe des individus, plusieurs outils permettant d’évaluer les capacités fonctionnelles des IA sont utilisés en clinique. Par exemple, afin d’évaluer le niveau d’activités de la vie quotidienne (AVQ) 37, les
tests de marche sont couramment utilisés. Ils peuvent entre autres évaluer la distance maximale parcourue par un individu en un temps prédéterminé. Les principaux tests utilisés en clinique sont les suivants :
19
- Le test de marche de six minutes (TM6), ayant démontré sa fiabilité 37, est de durée suffisante
pour défier les capacités fonctionnelles des IATT/IATF, leur équilibre et leur contrôle postural. Ce test aérobie d’endurance sous-maximale évalue la distance de marche maximale parcourue sur six minutes. Il a été démontré que la population des IA parcourait une distance moyenne (110.26 ± 34.11 m) 38 inférieure à celle des individus sains (572 ± 92 m) 39 du même groupe
d’âge.
- Le Time Up and Go test (TUG) est le test le plus utilisé pour quantifier l’équilibre des IA selon Loiret 4. Il consiste à mesurer le temps nécessaire pour se lever d’une chaise, parcourir trois
mètres en ligne droite et pour se rasseoir sur cette même chaise. Son utilisation a démontré que ce test est valide, reproductible 40 et qu’il est approprié pour les IA âgés. De plus, ce test est
aussi reconnu pour renseigner sur les capacités des IA à déambuler à l’intérieur de leur domicile
41.
- Le L-Test est un test fiable incorporant les habiletés motrices de base nécessaires à l’indépendance fonctionnelle dans une population utilisant une prothèse 42. Décrit comme une
version modifiée du TUG, ce test fonctionnel chronométré débute en position assise avec le dos appuyé sur le dossier de la chaise et s’effectue sur un couloir de marche ayant la forme d’un « L » de 3 X 7 m, demandant de tourner à gauche et à droite, lors de l’allée et du retour. Le chronomètre s’arrête lorsque le participant est de retour en position assise, le dos appuyé à la chaise 42.
- L’Amputee Mobility Predictor© (AMP) évalue aussi les capacités fonctionnelles des IA. Il a été créé entre autres pour être réalisable en milieu clinique (temps et ressources) ainsi que pour faciliter le classement du niveau fonctionnel des patients IA (K1-K4). Ce test, ayant démontré une bonne fiabilité, peut évaluer les capacités fonctionnelles des patients portant (AMPPRO) ou non (AMPnoPRO) une prothèse 15. Il a été démontré que le résultat des IA au AMPPRO
concorde avec leur niveau fonctionnel (c.-à-d.. : K2 = 35, K3 = 41 et K4 = 45/45) 43.
- Le Prosthetic Profile of the Amputee (PPA) évalue la satisfaction des IA par rapport à leur prothèse. Cet instrument est utilisé en milieu clinique spécifiquement pour le suivi des IA 44.
En effet, il mesure l’utilisation de la prothèse et les facteurs reliés à cette utilisation à la suite de la sortie de réadaptation des IA. Il comporte 44 questions réparties en six thèmes : condition
20
physique, prothèse, utilisation de la prothèse, environnement, activités de loisirs et informations générales 45.
Plus de détails sur la technique d’administration de chacun des tests peuvent être retrouvés dans les références.
Principaux avantages des tests fonctionnels actuels
En général, l’administration des tests cliniques présente l’avantage d’être facile d’utilisation, peu coûteux et rapide. Par exemple, le TM6 est un test qui s’effectue avec un minimum de matériel. Il permet d’extraire plusieurs informations générales telles que la vitesse moyenne sur les dix premiers mètres et la distance totale parcourue. Ces données quantitatives permettent une comparaison de l’évolution de la distance parcourue et de la vitesse de marche sur les dix premiers mètres entre plusieurs temps de mesure. Le TUG est utilisé à titre de test prédictif du développement d’incapacités fonctionnelles. Il établit aussi un seuil à neuf secondes pour identifier le risque de développer des incapacités fonctionnelles et de 10 à 15 secondes pour prédire le risque de chutes 46. Le L-test est un indicateur de mobilité qui renseigne non seulement
sur le statut fonctionnel des aînés ayant une amputation et étant plus limités, mais également chez les aînés en santé et chez les plus jeunes individus ne présentant pas d’incapacités 42. Le
AMPPRO permet de classifier les individus selon un niveau fonctionnel et il rend possible une comparaison de ce niveau fonctionnel pré-post réadaptation.
Limites principales des tests fonctionnels actuels
Le TM6 est propice aux erreurs, notamment à cause de la mesure du temps qui est prise par le clinicien à l’aide d’un simple chronomètre. Malgré la capacité de prédiction subjective d’incapacités fonctionnelles et de chutes chez les individus souffrant préalablement d’incapacités fonctionnelles, il ne permet pas de prédire ces paramètres chez une population âgée saine ou à haut fonctionnement 47. Le AMPPRO, en dépit de sa bonne fiabilité 15, n’est pas standardisé, ce
21
qui peut créer une différence intra- ou inter-évaluateur(s) et peut aussi engendrer une sur- ou sous-prescription des composantes prothétiques nécessaires au fonctionnement des individus évalués. Dans tous les tests discutés dans les dernières pages, l’évaluation de la condition des individus peut être différente d’un évaluateur à l’autre selon leur propre perception du patient. La motivation de l’individu à compléter les tests peut être changeante d’un test à l’autre, ayant une répercussion sur les résultats obtenus. De plus, l’ensemble de ces tests renseignent principalement de façon subjective, qualitative ou semi-quantitative sur le statut fonctionnel des individus et leur capacité à réaliser une tâche et non sur la qualité des mouvements pour y parvenir.
Dans le contexte clinique actuel, la quantification précise des paramètres de marche (telle que décrit dans le Chapitre 3 : État de l’art de l’analyse spatio-temporelle de la marche) n’est pas utilisée. Cette quantification permettrait de connaître les types de stratégies et compensations à la marche utilisées par les IA et permettrait, en perspective, d’améliorer les programmes de réadaptation de ces individus. En effet, la quantification des paramètres de marche tout au long du processus de réadaptation, et même dans un contexte de suivi, permettrait aux cliniciens de suivre leur évolution de façon précise et ainsi, maximiser la prise en charge des patients IA.
Objectifs de l’étude
L’objectif général du mémoire est d’instrumenter les IA lors d’un TM6 afin de caractériser leur évolution fonctionnelle et clinique à la suite de une réadaptation en centre. Le présent mémoire se divise en deux sous-objectifs découlant de l’objectif général :
1) Quantification des paramètres de marche des IA sur une période de six minutes à l’aide de
centrales inertielles à la fin de leur réadaptation.
2) Quantification et évolution des paramètres de marche à l’aide de centrales inertielles six
22
Hypothèses de recherche
L’hypothèse générale de ce mémoire, est que l’instrumentation des IA lors du TM6 permettra de quantifier une dégradation des paramètres spatio-temporels et cinématiques du pied lors de la marche après un retour en environnement écologique post-réadaptation.
1) L’hypothèse sous-jacente au premier objectif spécifique est que les paramètres de marche
(détaillés dans la section 3.3.1.) des IA se dégraderont sur une période de six minutes de marche dû à l’apparition d’un état de fatigue physique affectant leurs performances.
2) L’hypothèse sous-jacente au deuxième objectif spécifique est que les paramètres de marche
(détaillés dans la section 3.3.1.) des IA se dégraderont sur une période de six minutes de marche ainsi qu’entre le TM6 de leur sortie de réadaptation et le TM6 de suivi à six semaines suivant le retour en milieu écologique.
23
Chapitre 3 : État de l’art de l’analyse spatio-temporelle de
la marche
Ce chapitre consiste en une revue de littérature se concentrant principalement sur les paramètres spatio-temporels et cinématiques de la marche chez les IA, l’impact des prothèses sur ces paramètres et les paramètres les plus pertinents pour l’analyse des chutes chez les IA. Elle introduira aussi la littérature portant sur la quantification de ces paramètres en laboratoire et en clinique à l’aide de technologies portables, telles que les centrales inertielles.
Évaluation de la marche
Cette section décrira brièvement l’histoire de l’analyse de la marche et présentera la description du cycle de marche de façon détaillée.
La marche inclut le départ, l’arrêt, les changements de vitesse, les altérations de direction et la modification des paramètres de marche par rapport à l’inclinaison du sol. Ces événements transitoires sont superposés à un modèle de base. Ce modèle est défini comme un déplacement rythmique de parties du corps qui maintient la personne en progression vers l’avant 48. Nos
ancêtres ont adopté cette démarche particulière comme leur forme de locomotion unique autant lors d’une simple promenade que lors d’une course à toute allure pour éviter les prédateurs 49
depuis plus de six à sept millions d’années 50. Il semblerait que l’Homme soit passé du mode de
locomotion quadrupède vers le mode bipède dans le but d’utiliser les membres supérieurs à d’autres fins que la locomotion tout en permettant une diminution du coût énergétique associé au déplacement. La marche se définit actuellement comme une méthode de locomotion impliquant l’utilisation des deux jambes, alternativement, pour assurer support et propulsion, suscitant l’intérêt scientifique depuis plusieurs années 6.
24
Aristote serait le premier à avoir fait allusion à l’analyse de la marche dans ses écrits, discutant de la trajectoire verticale de la tête en « zig-zag » causée par l’enchaînement de la levée et du dépôt du pied au sol 51. La première analyse de la marche a été faite par Borelli qui a déduit qu’un
mouvement medio-lateral de la tête était créé lors de la marche. Ces observations étaient basées sur l’observation d’un pôle par rapport à un autre qu’il avait aligné devant lui en position statique. Lorsqu’il entamait la marche, le pôle le plus près de lui semblait bouger de gauche à droite par rapport au deuxième pôle, d’où sa déduction du mouvement médio-latéral de la tête lors de la marche. Les frères Heinrich et Willhelm ont mis en évidence l’effet de la vitesse de marche sur la longueur de pas et la cadence 52. Au cours des mêmes années, mais sur deux continents
différents, Muybridge a inventé l’utilisation d’une série de caméras déclenchées en alternance pour étudier le mouvement du corps à la marche chez l’Homme et les animaux (États-Unis) pendant que Marey a créé le chronophotographe, un obturateur permettant la capture de plusieurs images sur la même plaque photographique (France) 52. Les analyses de la marche en
trois-dimensions ont fait leur apparition par la suite, grâce à Fischer. En 1945, dû aux conséquences de la Deuxième Guerre mondiale, le Conseil national de recherches a créé un comité portant sur l’amélioration des prothèses (en raison de la nouvelle incidence d’amputation) et près de 40 scientifiques ont été réunis dans un laboratoire de biomécanique de l’Université de Californie à Berkeley. Ils ont d’abord approfondi les connaissances reliées à la marche dite normale pour pouvoir ensuite améliorer les connaissances de la marche avec prothèses. Plus récemment (1974-1992) 5, 53, Perry a développé une approche méthodologique de l’analyse de la marche incluant
l’observation ainsi que certaines méthodes d’instrumentation pour mesurer les paramètres spatio-temporels simples et la cinématique de la marche 51. La marche demeure une tâche fonctionnelle
essentielle et son analyse est des plus pertinente afin de comprendre l’évolution de plusieurs pathologies affectant le système musculosquelettique, particulièrement au niveau des paramètres spatio-temporels et cinématiques requérant des outils d’analyse de la marche à la fine pointe de la technologie.
25
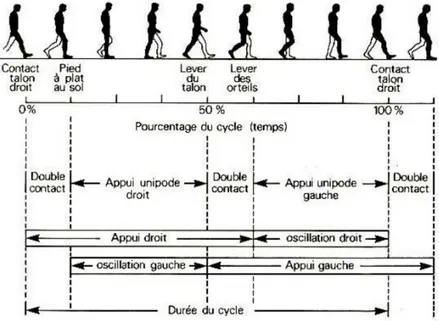
Figure 6. Les divisions du cycle de marche.
Description de la marche
La marche se définit comme un déplacement périodique des segments corporels incluant des mouvements répétitifs 54. L’analyse quantitative de la marche s’effectue par sa décomposition en
cycle. Un cycle de marche (CdM) représente les mouvements d’un seul côté. Il est défini comme la période de temps entre le contact d’un pied au sol jusqu’au prochain contact du même pied au sol 55. Lors de l’analyse isolée des mouvements d’un seul MI, le CdM est divisé en deux phases
principales, soit la phase d’appui et la phase d’oscillation, représentant respectivement 60% et 40% du cycle de marche (voir Figure 6). La phase d’appui, ayant comme rôle principal le support du membre au sol en simple appui ainsi que le transfert de poids sur le pied porteur, est caractérisée par la période durant laquelle le pied est en contact avec le sol et est divisée en cinq sous-phases, soit le contact initial (CI), la phase de chargement (LDr), la phase de contact intermédiaire, la phase de contact terminal et la phase de pré-oscillation. Elle est également délimitée par deux phases de double appui au début et à la fin de la phase d’appui qui sont séparées par une phase de simple appui, où un seul pied est en contact avec le sol (fig. 6). À l’inverse, la phase d’oscillation, ayant comme rôle principal la progression du membre oscillant vers l’avant du corps, est définie par la période pendant laquelle le pied n’est pas en contact avec le sol et est divisée en trois sous-phases, soit la phase d’oscillation initiale, la phase d’oscillation intermédiaire et la phase d’oscillation terminale 5.
26
Le détail des différentes sous-phases de la marche est décrit ci-dessous et illustré à la Figure 7.
Phase d’appui
Contact initial (A) : Cette phase débute lorsque le pied entre en contact avec le sol. Il y a transfert de poids du corps sur ce pied (double appui).
Phase de chargement ou phase taligrade (B) : Cette phase poursuit le mouvement entamé par le contact talon initial et continue jusqu’à ce que le pied controlatéral quitte le sol (double appui).
Phase de contact intermédiaire ou phase plantigrade (C) : Cette phase débute lorsque le pied controlatéral a quitté le sol et continue jusqu’à ce que le poids du corps soit aligné avec l’avant-pied (simple appui).
Phase de contact terminale ou phase digitigrade (D) : Cette phase débute avec le soulèvement du talon et continue jusqu’au contact talon du pied controlatéral. Cette phase marque la fin du simple appui.
Phase pré-oscillatoire (E) : Cette phase débute avec le contact talon du pied controlatéral et se termine par le soulèvement des orteils du pied ipsilatéral.
Phase d’oscillation
Phase d’oscillation initiale (F) : Cette phase débute lorsque le pied est soulevé du sol et se termine lorsque le pied controlatéral est opposé au pied d’appui.
27
Phase d’oscillation intermédiaire (G) : Cette phase débute lorsque le pied controlatéral est opposé au pied d’appui et termine lorsque le membre en oscillation est à l’avant du corps et que le tibia est vertical.
Phase d’oscillation terminale (H) : Cette phase débute lorsque le membre oscillant est vers l’avant et que le tibia est vertical. Elle se termine lorsque le pied entre en contact avec le sol.
Identification des paramètres d’intérêts à la marche chez les individus
ayant une amputation du membre inférieur
L’amputation d’un MI entraîne nécessairement une dégradation des capacités fonctionnelles, dont la capacité de marche. Suite à une amputation, le but principal de la réadaptation est de retrouver un état fonctionnel se rapprochant de l’état fonctionnel pré-morbide. Une revue de la littérature portant sur les paramètres de marche chez les IA est présentée dans les paragraphes suivants.
Paramètres cinématiques et spatio-temporels de la marche
La cinématique se définit comme la branche de la mécanique classique qui s’occupe de l’étude
du mouvement d’un objet sans prendre en considération les forces qui le produisent 6, 56. La
cinématique articulaire décrit la mobilité d’un segment par rapport à un autre ou en lien avec un A B C D E F G H Figure 7. Phases du cycle de marche