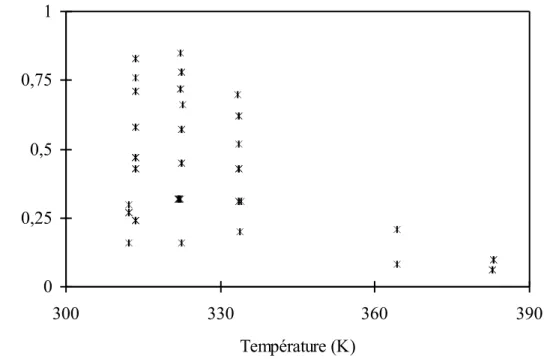
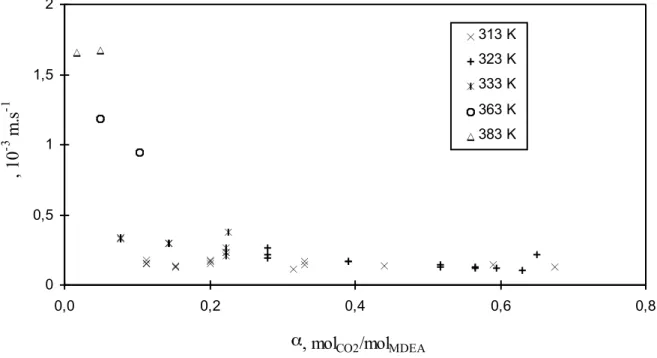
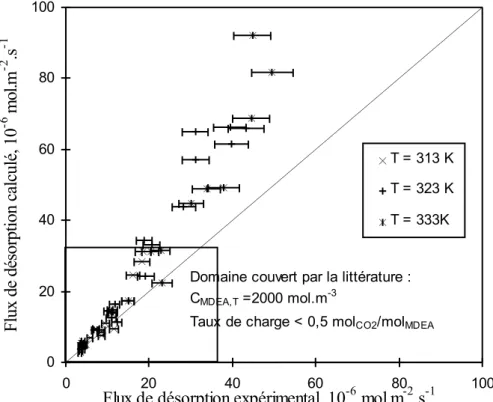
Acid gases absorption/desorption by alkanolamines aqueous solutions
Texte intégral
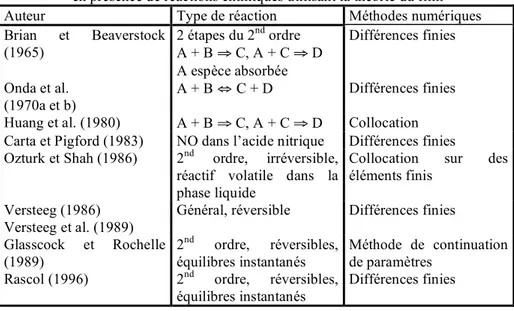
Figure


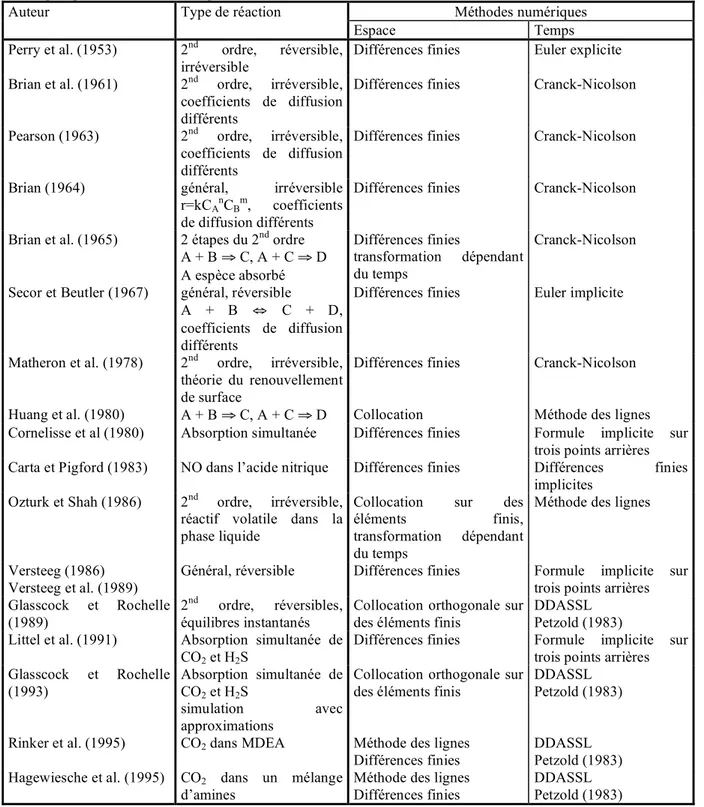
Documents relatifs
La concentration en masse C d'une espèce chimique (jouant le rôle de soluté) en solution est la masse de cette espèce chimique dissoute par litre de solution.. Elle s'exprime par
La conductivité électrique s mesure l'aptitude d'un matériau au déplacement de charges électriques.. C’est l’inverse de la résistivité (qui correspond à la notion de
Un complexe est un ´edifice polyatomique form´e d’un atome ou ion central et entour´e de mol´ecules ou anions appell´es ligands.. Indice de coordination d’un complexe : nombre
Dans une solution aqueuse, le courant électrique est dû à la double migration simultanée des ions : les ions positifs se déplacent dans le sens conventionnel du courant
Dans un viscosimètre, un volume d’eau prend 1min pour se déplacer de 1cm, tandis que le même volume de sang d’un malade prend 3min et 20s pour le même déplacement
forme alors des ions ………en quantité ………..a celle des ions chlorure pour que la solution soit électriquement neutre.. L’équation chimique de la réaction
-La masse volumique d’un corps dépend de la température car son volume peut varier en fonction de la température. Expérimentalement on peut la mesurer à l’aide
- Introduire le solide dans la fiole jaugée avec un entonnoir puis rincer la capsule avec de l’eau distillée (fig a) - Remplir la fiole jaugée aux ¾ avec de l’eau