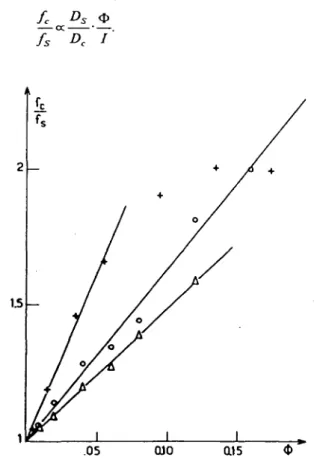
HAL Id: tel-00011858
https://tel.archives-ouvertes.fr/tel-00011858
Submitted on 9 Mar 2006
HAL is a multi-disciplinary open access
archive for the deposit and dissemination of
sci-entific research documents, whether they are
pub-lished or not. The documents may come from
teaching and research institutions in France or
abroad, or from public or private research centers.
L’archive ouverte pluridisciplinaire HAL, est
destinée au dépôt et à la diffusion de documents
scientifiques de niveau recherche, publiés ou non,
émanant des établissements d’enseignement et de
recherche français ou étrangers, des laboratoires
publics ou privés.
Diffusion, solubilisation et propriétés interfaciales dans
les solutions isotropes d’amphiphiles
Didier Chatenay
To cite this version:
Didier Chatenay.
Diffusion, solubilisation et propriétés interfaciales dans les solutions isotropes
d’amphiphiles. Analyse de données, Statistiques et Probabilités [physics.data-an]. Université Pierre
et Marie Curie - Paris VI, 1987. Français. �tel-00011858�
ORSAY UNIVERSITE PARIS-SUD n° d’ordre CENTRE D’ORSAY
DÉPARTEMENT
DE
PHYSIQUE
DE
L’ÉCOLE
NORMALE
SUPÉRIEURE
THESE DE DOCTORAT D’ETAT ès
Sciences
Physiques
présentée
à l’Université de PARIS-SUD par. Didier CHATENAY pour obtenirle
grade
de
DOCTEUR ESSCIENCES
Sujet
dela
thèse :
"DIFFUSION,
SOLUBILISATION
ETPHENOMENES INTERFACIAUX
DANS LES SOLUTIONS
ISOTROPES
D’AMPHIPHILES"
Soutenue le 30
Septembre
1987 devant laCommission d’examen
MM. E. GUYON
Président
J. CHARVOLIN R. ZANA MINSSIEUXExaminateurs
M. WAKSExaminateurs
Mmes A.M.
CAZABAT
UNIVERSITE DE PARIS-SUD CENTRE D’ORSAY
THESE DE DOCTORAT D’ETAT ès Sciences
Physiques
présentée
à l’Université de PARIS-SUD par Didier CHATENAY pour obtenirle
grade
de Docteur ès SciencesSujet
de la thèse :"DIFFUSION,
SOLUBILISATION ET PHENOMENES INTERFACIAUX DANS LES SOLUTIONS ISOTROPES D’AMPHIPHILES"Soutenue le 30
Septembre
1987 devant la Commission d’examenMM. E. GUYON Président
J. CHARVOLIN R. ZANA
MINSSIEUX Examinateurs
M. WAKS
Mmes A.M. CAZABAT D. LANGEVIN
REMERCIEMENTS
Je remercie vivement Monsieur le Professeur J. BROSSEL et
Monsieur J. DUPONT-ROC de m’avoir chaleureusement accueilli dans leur
laboratoire.
Madame D.
Langevin
et Monsieur J. Meunier ont encadré tout cetravail et m’ont fait
profiter
de leurs trèsgrandes compétences
scientifiques
ainsi que de leurs non moinsgrandes
qualités
humaines.Je remercie Messieurs
Guyon,
Zana, Charvolin,
Waks,
Minssieux etMadame A. M. Cazabat d’avoir bien voulu faire
partie
dujury
de cette thèse.Je tiens à remercier Monsieur Minssieux et l’Institut
Français
du Pétrole de m’avoir fait bénéficier d’une bourse de thèse durant lespremières
années de ce travail.J’ai eu le
plaisir
durant tout ce travail decotoyer
ungrand
nombre decollègues
que je tiens à remercier ici : A.Pouchelon,
P. H.Guering,
D.Guest,
O.Sorba,
C.Stenvot,
V.Thominet,
R.Messager,
O.Abillon,
B. Binks. Tous ont contribué à la bonne ambiance
régnant
au sein dugroupe.
Une mention
spéciale
doit être décernée à A. M. Cazabat et W.Urbach avec
lesquels j’ai partagé
lesjoies
et les peines inhérentes à cetype
de travail. Tous deux ont fait preuve à monégard
d’une infiniepatience
et d’unedisponibilité
à touteépreuve.
J’ai
également grand plaisir
à remercier mescollègues
duCollège
de France avec
lesquels
j’ai
souvent eu delongues
et fructueuses discussions : D.Ausserré,
J. M. DiMeglio,
P.Favre,
L.Auvray,
G.Guyot :
L.Léger
m’aprodigué
avecbeaucoup
degentillesse,
de nombreux conseils lors de la mise aupoint
del’expérience
de fluorescence :qu’elle
Je tiens
également
à remercier tous les chercheurs du laboratoire deSpectroscopie
Hertzienne au côtédesquels
j’ai
passé
de si bons moments, ainsi que tous les chercheurs du GRECO Microémulsions.C’est peu de dire que
je
remercie l’ensemble dupersonnel
technique
du laboratoirequi
m’ont tousfait,
à un moment ou à un autre,profiter
de leurgentillessse, compétence
et savoir-faire : A.Clouqueur,
B.Legaut,
B.Giron,
J. C.Bernard,
B. Laisne pourl’électronique ;
J. P.Cassou,
J.C. Guillaume J.Lagadec
pour lamécanique
ainsi que P.Bouniol,
I.Brodschi,
C. Emo pour le secrétariat.Enfin un
grand
coup dechapeau
à MesdamesEmo,
Audoin et1
INTRODUCTION
La
physique
des solutionsd’amphiphiles
est unexemple
d’inte-ractionsprofitables
entre rechercheappliquée
et fondamentale : en effet cen’est que sous
l’impulsion
descompagnies pétrolières,
intéressées parl’application
de cessystèmes
à larécupération
assistée dupétrole,
qu’un
vaste effort de recherche fondamentale s’est dessiné sur ce thème.Si l’intérêt initial s’est fixé sur les mécanismes d’obtention de
basses tensions interfaciales dans les
mélanges
eau-huile-amphiphiles,
lestravaux réalisés
depuis
ont faitapparaître
un monde d’unegrande
richesse. En effet de telsmélanges
donnent lieu à ungrand
nombred’équilibres
dephases
(isotropes
ou cristalliquide).
Chacune de cesphases
est alors undéfi lancé à
l’imagination
des structuralistes. Un gros effortthéorique
a étéfait en vue de rendre
compte
desdiagrammes
dephase
observés. On aégalement
vuapparaître
dans ce thème desconcepts
liés à laphysique
des cristauxliquides
et desphénomènes critiques.
En ce qui nous concerne, nous nous sommes
plus
particulièrement
intéressés à
l’aspect système
colloïdal des solutionsd’amphiphiles.
En effetdans un certain nombre de cas de tels
systèmes
peuvent être décritscomme une
dispersion d’objets plus
ou moinsidentiques.
Onpeut
alors les utiliser en tant quesystèmes
modèles aussi bien pour des études detype
statique,
telles que celles effectuées en diffusion de neutrons, oudynami-ques telles que celles effectuées en diffusion
quasi-élastique
de la lumière. C’est à ce dernieraspect
que nous nous sommesplus particulièrement
attachés. En effet si on
dispose
maintenant d’outilsthéoriques
satisfaisants pour décrire lespropriétés d’équilibres statiques
des solutions colloïdales (fonction de distribution depaires
ou facteur destructure),
lespropriétés
dynamiques quant à
elles sont bienplus
difficiles à traiter : dans cesdécrire les
propriétés d’équilibre
statiques,
apparaissent
également
des interactionshydrodynamiques qui
sont àl’origine
des difficultés d’un traitementthéorique
despropriétés
d’équilibre dynamique.
Si de gros effortstant
théoriques qu’expérimentaux
ont été consacrés à l’étude des modes collectifs de fluctuation deconcentration,
telsqu’on
peut
les mesurer pardiffusion
quasi-élastique
de lalumière,
il n’en demeure pas moins que la situation n’estparfaitement
comprise
que pour lessystèmes
dilués ; par ailleurs un gros travail reste à faire en vue de l’étude des mécanismes d’auto-diffusion dans cessystèmes.
Nous nous sommes donc
attachés,
dans lapremière partie
du travailprésenté
ici,
à étudier cespropriétés
dynamiques
d’équilibre
dessolutions colloïdales en utilisant deux
techniques optiques.
Lapremière
deces
techniques
est la diffusionquasi-élastique
de la lumièrequi
permet
d’avoir accès au mode collectif de fluctuation de concentration ; laseconde,
plus originale,
est le Recouvrement de FluorescenceAprès
Photoblanchiment
qui
permet
d’avoir accès au mode d’auto-diffusion. Nous montrerons comment ces deux modes sont affectés par les intéractionsdirectes entre
particules
en solution et par la concentration de cesparticules.
Nous verrons comment les résultatsexpérimentaux
obtenuspermettent
de clairementséparer
lespropriétés
de ces deux mécanismes ausujet
desquels
arégné
jusque là une certaine confusion dans la littérature.Les résultats obtenus ne
représentent
toutefois quel’aspect
colloïdal"classique"
des solutionsd’amphiphiles.
Or ces colloïdes sont d’untype
particulier puisqu’ils
sont formésd’agrégats
de molécules ; ceci se traduit par un ensemble dephénomènes étrangers
au monde des colloïdesusuels,
tels que les
échanges
des constituants desagrégats
ou bien depossibles
évolutions structurales obtenues en concentrant la
phase
dispersée.
Nousverrons comment cet
aspect
particulier
de nossystèmes
peut
se manifester dans les mécanismes d’auto-diffusion.Dans la deuxième
partie
de cemémoire,
nous montrerons que lesoutils
expérimentaux
utilisés dans le cadre de l’étude décrite ci-dessuspeuvent
apporter
quelques
informations dans un domaine de recherche récent consistant à utiliser les solutionsd’amphiphiles
commesystèmes
bio-mimétiques .
En effet de telssystèmes
offrent à des moléculesbiologiques
3
(ici des
protéines)
un environnementproche
du leur dans lessystèmes
biologiques.
Il est ainsipossible
de solubiliser dans ces solutions desprotéïnes qui
seraientdénaturées,
voire mêmeinsolubles,
dans tout autresolvant. Se
posent
alors lesproblèmes
de localisation de cesprotéines
dans les
agrégats
et bien évidemment de la structure de cesagrégats
enprésence
deprotéines
solubilisées. C’est à cetype
deproblèmes que
nous nous sommes Intéressés dans le cadre de ce travail.Enfin dans une dernière
partie
nous aborderons cequi,
historique-ment, a constitué notre
premier
centre d’intérêt à savoirl’origine
des basses tensions interfaciles dans leséquilibres
multiphasiques
observées dans lesmélanges
eau-huile-amphiphiles.
4
CHAPITRE A
LES AMPHIPHILES
I -
INTRODUCTION
Les
systèmes
étudiésici,
s’ils relèvent par certainsaspects
des théories utilisées habituellement pour lescolloïdes,
constituent néanmoinsune famille
particulière
en ce sensqu’ils
sont formésd’agrégats
de molécules. Pourcomprendre
l’origine
de cesphénomènes
d’agrégation,
il est nécessaire dans un premiertemps
depréciser
des notions telles que : caractèrehydrophile,
hydrophobe
etamphiphile.
Ces notions étant relatives à des molécules solubilisées dansl’eau,
il sera nécessaireauparavant
de fairequelques rappels
sur la structure de l’eau.Il -
HYDROPHILICITE - HYDROPHOBICITE
1) L’eau
Il est bien connu que l’eau
présente
un certain nombre depropriétés
inhabituelles (hautestempératures
de fusion etd’ébullition,
densité du solide inférieure à celle du
liquide)
dues à laprésence
de"liaisons"
hydrogène
entre les molécules d’eau [1]. Cetype
de liaison estrelativement bien connu et on sait en
particulier qu’elles
sont de natureanisotrope.
Par ailleurs on saitégalement
que les interactionsresponsables
de ces liaisons sont, du
point
de vue desénergies
mises enjeu,
intermédiaires entre les liaisons covalentes et les interactions de
type
Van der Waals [2]. Deplus
ces interactionsdépendant
fortement del’orien-tation,
sontresponsables
de la structure locale de l’eau (coordination tetrahédrale) .2)
Hydrophobicite
Si on tente de solubiliser dans l’eau des molécules non
polaires
qui nepeuvent
pas former de liaisonhydrogène,
les molécules d’eau vont tenter de seréorganiser
localement autour de cette molécule. Cetteréorganisation
estentropiquement
très défavorablepuisqu’elle
suppose quel’on casse la structure locale de l’eau pour former autour de la molécule
hôte une structure
plus
ordonnée. C’estl’origine
de la très faible solubilitédes molécules non
polaires
(telles que leshydrocarbures
et les fluoro-carbures) dans l’eau. On dit alors que de telles substances sonthydrophobes.
De telles considérations sontégalement
utilisées pour décrirel’interaction
hydrophobe,
fortementattractive,
observée entre molécules nonpolaires
solubilisées dans l’eau[3,4].
3)
Hyrdrophilicité
On a vu
plus
haut que deux moléculeshydrophobes
solubilisées dans l’eau s’attirent fortement. Il existe un autretype
de molécules qui ontun
comportement
tout à fait différent : elles sont très solubles dans l’eau etcette fois-ci se
repoussent
très fortement [3]. De telles molécules (ougroupements
chimiques)
sont alorsqualifiées
d’hydrophiles;
elles sont parailleurs souvent
hygroscopiques
(i.e. adsorbent des molécules d’eau enprovenance de la
phase vapeur).
Appartiennent
à cette classe de molécules les ionshydratés ;
certaines molécules nonpolaires peuvent
même êtrehydrophiles
si elles ont la bonnegéométrie
et si elles contiennent des atomesélectronégatifs
pouvant
former des liaisonshydrogènes
avec les molécules d’eau (cas des atomesd’oxygène
des alcools etoxydes
depolyethylène,
des atomes d’azote dans les amines) .III - AMPHIPHILES
Il existe, outre les deux
catégories
vuesci-dessus,
un troisièmetype
de moléculesprésentant
simultanément un caractèrehydrophile
etFig.
A1
Une
molécule
amphiphile
formées de deux
groupements
chimiques,
l’unhydrophile
et l’autrehydro-phobe,
liés par une liaison covalente [3].Si on essaye de solubiliser dans l’eau de telles molécules on
peut
aisément
imaginer
la suite des évènements que l’on observera enaugmen-tant
progressivement
la concentration (cfFig
A-1).- A très faible concentration les molécules
resteront sous forme
de monomères dissous et iront se
placer
a l’interface eau-air,ce
qui
représente
unefaçon
pour reaud’expulser
les partieshydrophobes
desamphiphiles
(cette solution étantplus
favo-rable du
point
de vueentropique
quel’agrégation).
Si on continue à augmenter la concentration en
amphiphiles,
l’interface finira par se saturer.
puis
les moléculess’agrége-ront ce
qui
est la seule solution restante pour éviter le contact eau-partie hydrophobe. On définit ainsi la concentra-tion micellairecritique
(c.m.c).L’adsorption
des moléculesamphiphiles
aura pourconséquence
de modifier lespropriétés
de surface de la solution [s] ; c’est pour cetteraison que de telles molécules seront aussi
qualifiées
de tensio-actives.Dans ce manuscrit on utilisera indifferemment les deux
appelations :
amphiphiles
ou tensio-actifs.On
distingue généralement
deuxgrandes
classes de moléculesamphiphiles
suivant la nature de leurs têtespolaires.
-
Les
amphiphiles
ioniques dont le groupementhydrophile
est union
(cationique
si l’ion estchargé positivement,
anionique
dans le cas contraire). Dans ce cas le groupement
hydrophile
a très souvent un encombrement très
petit
par rapport augroupement
hydrophobe.
On utilise alors pourdésigner
cegroupement
le terme de tête polaire.Toujours
dans ce cas, il faut noter que les interactions entre têtespolaires
sont denature
électrostatique :
elles seront donc très sensibles à laprésence
de sel rajouté(qui
permet d’écranterplus
oumoins
ces interactions). Les propriétés des tensio-actifs ioniquesFig. A2
Amphiphiles
anioniques:
seront donc très sensibles à la
présence
(voire même à la nature) de tout selrajouté.
Elles seront par contre peusensibles à la
température.
-
Les
amphiphiles non-ioniques
dont legroupement
hydrophile
estun groupement du type
oxyde
d’éthylène.
Dans ce cas leparamètre
essentiel de contrôle des Interactions entregroupe-ments
hydrophiles
est latempérature.
Lespropriétés
de telstensio-actifs seront donc très sensibles à la température mais peu sensibles à la
présence
de sel ajouté.Dans
pratiquement
tous les cas, legroupement
hydrophobe
estconstitué d’une (ou deux) chaînes
aliphatiques
dutype (CH
2
)n.
Quelques
exemples d’amphiphiles
sont donnés enfigure
A-2.CHAPITRE B
MICELLES
I - INTRODUCTION
On ne s’intéressera ici
qu’à
dessystèmes
à troiscomposants :
eau, tensioactif et sel.
Dans de tels
systèmes,
onpeut
définir un certain nombre dequantités
telles que :- le
point
de Kraft : c’est la température au dessus delaquelle
la solubilité d’un
amphiphile
croît tresrapidement
(cf.figure
B-1)
-
la concentration micellaire critique (c. m. c) . c’est (à une
température
supérieure a la temperature de Kraft), laconcen-tration au dela de laquelle il y a
agrégation
des moléculesd’amphiphiles
(et donc formation de micelles).De nombreuses
propriétés
macroscopiquesprésentent
unerupture
de variation à cette valeur de la concentration (cf
fig
B2) :généralement
la valeuradoptée
pour la c. m. c.dépend
de lagrandeur
macroscopiquemesurée.
Il existe
quelques règles
permettant
decomprendre
les variations dela c.m.c. pour différents tensioactifs.
-
dans une série
homologue
(i.e. même têtepolaire)
la c.m.c.décroît
quand
la chaînes’allonge,
cequi
s’explique
par unemeilleure solubilité des molécules
amphiphiles à
chaînecour-te.
-
Fig.B2
Variation
de quelques propriétés
macroscopiques
Fig.B3
9
plus
basse pour une molécule à tétepolaire
nonionique
quepour une molécule à tête
polaire ionique
(en effet l’absence d’interationsélectrostatiques
entre têtespolaires
favorise la micellisation). Pour la mêmeraison, l’adjonction
de sel dansune solution
d’amphiphiles ioniques
abaisse la c.m.c. du fait derécrantage
des interactionsélectrostatiques
entre têtespolaires
par le sel.- enfin la
c.m.c.
dépend
peu de latempérature.
Par ailleurs la structure des
agrégats
aux concentrationssupérieures
à la c.m.c. a fait
l’objet
de très nombreuses études enparticulier
par destechniques
de diffusion derayonnement.
Ces études structurales ontpermis
de mettre en évidence de nombreusespossibilités
quant
à la structure desagrégats : sphères,
ellipsoïdes
de révolutionallongés
ouapplatis,
cylin-dres,
phases
lamellaires,
etc... D’unpoint
de vuethéorique, plusieurs
approches microscopiques
[3][6] ont étédéveloppées
afin de rendre compte de cepolymorphisme.
Plus récemment a étédéveloppée
uneapproche plus
géométrique
afin de classifier toutes les formespossibles
[7].Dans ce qui suit, nous
présenterons
un modèlethermodynamique
simplifié
del’agrégation.
Il - MODELE THERMODYNAMIQUE DE L’AGREGATION
II-1) Le modèle
d’équilibre
multiple
[3][4]On considère le
système
schématisé sur lafigure
B.3, à
savoir unesolution de molécules
amphiphiles
(fraction molaire X) où on aéquilibre
entre des
agrégats
constitués de s molécules (s étantquelconque
etpouvant
valoir1 ,
2,...,
N,....).
Le cas s = 1correspond
auxmonomères en solution. On supposera la solution
idéale,
i.e. onnéglige
les interactions
interagrégats
(cas des solutions diluées). Soit 03BCs lepotentiel
chimique
d’une moléculeamphiphile
dans unagrégat
de taille s. AOr 03BCs
peut
s’écrire :où
03BC
o
s
désigne l’énergie
libre moyenne d’une molécule dans unagrégat
de
taille s et le second membre du terme de droite
représente
la contributionentropique
aupotentiel
chimique,
X
s
étant la fraction molaire de monomères contenus dans desagrégats
de taille s.La solution du
problème
est alors donnée par lesystème
d’équa-tions :
où la seconde des deux
équations représente
la conservation de laquantité
totale de moléculesamphiphiles
Sur la
première
de ceséquations,
on constatequ’une
condition nécessaire pour la formationd’agrégats
degrande
taille est que03BC
o
s
soitune fonction décroissante de s, ou du moins
présente
un minimum. Pour de faibles concentrations en monomèresX
1
,
telles que .on obtient
X
1
>X
2
>X
3
... Ainsi aux faibles concentrations la plupartdes molécules sont en solution sous forme de monomères isolés.
s’approche
de1,
cettequantité
devient constante. Enparticulier
sil’association est
coopérative
(i.e. si03BC
o
s
présente
un minimum bienmarqué
ou une discontinuité pour une certaine valeur so des),
on pourraalors définir la concentration micellaire
critique
(c. m. c) par :Dans un tel cas les fractions molaires de monomères libres ou micellisés
varieront avec la concentration totale
d’amphiphiles
comme le montrent les courbes de lafigure
B.4.A ce stade pour
pouvoir
discuter des différentes formespossibles
desmicelles,
il est nécessaire depréciser
la forme des03BC
o
s
pour les différentesgéométries envisagées.
C’est ce que nous ferons dans leparagraphe
suivant en nous limitant à 2 cassimples :
les micellessphériques
et les micellescylindriques.
II-2) Modèle
simplifié
pour les03BC
o
s
Afin de calculer les
03BC
o
s
il est nécessaire de connaître les interactions entre moléculesamphiphiles
dans lesagrégats
et celles entremolécules
amphiphiles
et solvant (ici l’eau).On suppose
généralement
que dans unagrégat
onpeut
distinguer
deux contributions à
03BC
o
s
:
-une contribution de surface due à l’interaction
hydrophobe,
larépulsion
coulombienne (tensioactifsioniques)
oudipôle-dipôle
(non
ioniques)
entre têtespolaires,
l’hydratation
des têtespolai-res, l’interaction entre têtes
polaires
et contre-ions.-une contribution du coeur
aliphatique
due aux interactions de Van der Waals entre chaînes et àl’entropie
deconfiguration
des chaînes confinées dans le coeur desagrégats.
12
Dans le modèle
simplifié
dû à Tanford [4]présenté
ici,
on supposeque le coeur
hydrophobe
estliquide
et n’intervient que par des contraintesgéométriques :
volume (v) etlongueur
(LC) d’une chaînealiphatique.
Ence
qui
concernel’énergie
desurface,
onl’exprime
sous la forme de deux termes de tendancesopposées :
unpremier
termeprend
encompte
le contact eau-coeurhydrophobe
et tend donc à diminuer l’aire de contact(a),
un second termeprenant
encompte
les interactions entre têtespolaires qui
tend àaugmenter
cette même aire. Dans le cadre de cemodèle,
on écrit donc:où y est
typiquement
de l’ordre degrandeur
d’une tension interfacialeeau-huile
(03B3 ~
50dyn/cm);
onpeut
calculerexplicitement
C dans un modèlede
capacité
sphérique
pour des tensioactifsioniques.
Ilapparaît
ainsinaturellement une aire par tête
polaire optimale
ao donnée par :dont l’ordre de
grandeur
est dequelques
dizainesd’Å
2
.
Onpeut
alorsréécrire (4) sous la forme :
Ainsi la
géométrie
micellaireoptimale
est celle pourlaquelle
onsatisfait à la fois a ~ ao et < C.
On
peut
alors utiliser le nombre sans dimensionv/a
o
c
pour déterminer si l’on obtient :- des
agrégats sphériques
- des
agrégats non sphériques de type
cylindrique
(1 3
< v a
<1 2
)Chacune de ces structures
correspond
à unagrégat
de taille minimale oùtoutes les molécules
amphiphiles
ont uneénergie
libreminimale,
i.e. a ~a o .
Nous examinerons dans ce
qui
suit le cas des micellessphériques
et
cylindriques
qui
nous concernentplus particulièrement.
II-3) Micelles
sphériques
Dans ce cas on a :
Soit alors so le nombre
d’agrégation
correspondant
au minimum del’énergie
libre etR
o
le rayon micellaire associéEn utilisant le modèle
d’équilibre multiple
on a :ce qui
permet
d’exprimer
la loi de distribution des tailles des micelles : enunlisant
(6),
(avec s ~ so et s =403C0R
2
/a)
14
voisinage
de so dont lalargeur
est :Si on
prend
03B3 ~
50dyn/cm
et ao ~60A
2
,
on obtient :ce
qui
donne pours
o
~
60,
0394s ~ 8. On constate donc que dans ce cas la loi de distribution des nombresd’agrégation
est relativement étroite. Par ailleurs s estproportionnelle
au cube du rayonmicellaire,
on obtient ainsi :Dans le cas de micelles
sphériques,
on a donc unedispersion
de taille trèsétroite.
II-4) Micelles
cylindriques
Dans ce cas on a :
Dans une telle
géométrie,
il faut noterqu’il
existe des effets d’extrémitéimportants;
eneffet,
il est nécessaire de refermer les extrémités ducylindre
enplaçant
des molécules dans des calottessphériques
(cequi
représente
un coûténergétique
important).
Par ailleurs oncomprend
intuitivement que pour une telle
géométrie
lalongueur
descylindres
soit apriori
moins bien définie que le rayon des micellessphériques,
résultat que l’onpeut
obtenir àpartir
du modèled’équilibre multiple
décritplus
haut. Ce même modèleprévoit également
la loi d’accroissement du nombred’agré-gation
moyen < s > avec la concentration totale de moléculesamphiphiles
X :De nombreux travaux ont été consacrés à l’étude de ces micelles
cylindriques :
- étude de la
transition micelles
sphériques-micelles
cylindriques
[8] [9]-
étude de la flexibilité des micelles
cylindriques
géantes
[8].-
mise en
évidence,
par diffusionquasi-élastique
de la lumière, d’uneanalogie
de comportement entre cessystèmes
de micellesgéantes
et les solutions depolymères
enrégime
semi-dilué [10].
II-5)
Quelques
remarquesLe modèle
exposé
ci-dessus neprend
pas encompte
un certainnombre de
phénomènes
couremment observés dans lessystèmes
micel-laires. Même dans le cadre del’approximation
de solutionsidéales,
il estbien connu que l’effet du sel ne se réduit pas à l’effet
d’écrantage
des interactionsélectrostatiques
entre têtespolaires.
En effet pour une mêmemolécule
amphiphile
l’addition de certains selspeut
induirel’allongement
des micelles [11]. Il est donc nécessaired’envisager
des processusd’adsorption
spécifique
des contre-ions sur la surface micellaire. Laquantité
de contre-ions adsorbés est alors déterminée par unéquilibre
detype
chimique
dont la constantedépend
de la nature du contre-ion [8].Par ailleurs
l’approximation
de solution idéale nepeut
rendrecompte
des évolutions structurales observées en concentrant la solution en molé-culesamphiphiles,
et enparticulier
del’apparition
dephases
dutype
cristalliquide
[12]. Parexemple,
enprésence
de forcesélectrostatiques
répulsives
àlongue portée,
des micellessphériques
nepeuvent
s’éloigner
indéfiniment les unes des autres. Par contre, les moléculesamphiphiles
peuvent
seréorganiser
pour former un réseau decylindres
dont les surfaces serontplus
éloignées,
ou même former unempilement
de bicouches cequi
estencore
plus
favorable.Nous discutons brièvement le
problème
des interactions dans les solutions micellairessphériques
dans lechapitre
ci-dessous.III - INTERACTIONS
MICELLAIRES
On s’intéressera ici au cas d’une solution
micellaire,
àamphiphiles
ioniques,
dont lesagrégats
ont une formesphérique (rayon
R,
nombred’agrégation
s),
enprésence
de selrajouté.
On supposera ici que les micelles secomportent
comme desparticules
sphériques
rigides
perma-nentes
portant
unecharge
Q donnée par :où 03B1 est le
degré
d’ionisation de la surface micellaire. On suppose parailleurs que cette
charge
Q est uniformémentrépartie
à la surface de lamicelle.
L’approche
laplus simple
consiste à traiter le solvant et les ionsqu’ils
contiennent comme uncontinuum,
caractérisé par l’inverse de lalongueur
d’écran deDebye
Hückel donnée par :où i est la force
ionique
de la solution(ions/cm
3
)
reflétant laprésence
du selrajouté
et la contribution en contre-ions des moléculesamphiphiles,
ela
charge
de l’électron et ~ la constantediélectrique
du solvant.Les interactions micellaires sont alors décrites [13] par un
potentiel
d’interaction de
paires identique
à celui utilisé dans le cadre de la théorie DLVOexpliquant
la stabilité des solutions colloïdaies [14]. Cepotentiel
d’interaction est la somme d’unepartie répulsive
(V
R
)
due aux forcesélectrostatiques
écrantées et d’unepartie
attractive(V
A
)
dues aux forces deVan der Waals. Les
expressions explicites
despotentiels
utilisés dans le cadre de cette théorie sont données dans l’article consacré aux mesuresd’auto diffusion dans les
systèmes
micellaires. L’alluretypique
despotentiels
d’interaction obtenues est donnée sur lafigure
B5.17
un
puits
infinimentprofond
au contact de deux micelles. Si on essaye d’utiliser un telpotentiel
pourinterpréter
les données de diffusion de lalumière,
il sera nécessaire d’introduire une distance minimaled’approche
non nulle entre deux
micelles,
afin d’éviter desdivergences
dans les diversesintégrales
utilisées. S’il semble clair que cette distanced’approche
a une
origine physique
(couched’hydratation,
couche deStern),
il estclair
qu’à
de tellesdistances,
qui
sont de l’ordre dequelques Angströms,
il est illusoire d’utiliser lespotentiels
dont il a étéquestion plus
haut. Eneffet,
il a été démontréqu’à
de telles distances interviennent des forcesrépulsives
d’untype
nouveau, dites forcesd’hydratation,
d’uneportée
d’environ 20 à 30Angströms.
Ces forces ont été mises en évidenceexpérimentalement,
mais on nedispose
pas à l’heure actuelle d’une théorie satisfaisantepermettant
de lesintégrer
dans une théorie detype
DLVO.IV - DYNAMIQUE DES SYSTEMES MICELLAIRES
Dans la mesure où les micelles sont des colloïdes
d’association,
il n’est évidemment pas toujourspossible
de les considérer comme desobjets
permanents au même titre que les billes de silice ou de latex. Ceci est
paticulièrement
important dans le casd’expériences
telles que la diffusionde lumière dans
lesquelles
on a accès à ladynamique
de cessystèmes.
De nombreusestechniques expérimentales (absorption
ultrasonore,
saut detempérature,
saut depression)
ont permis de caractériser les processusdynamiques
dans lessystèmes
micellaires.L’image
résultant de ces études est brièvement résumée ci-dessous.La formation de micelles est
analysée
en termes de réactionschimiques
et ondistingue
deux processusessentiels,
de constantes detemps
différentes [15] [16].où A
désigne
une moléculeamphiphile
etA
s
unagrégat
de s molécules. Letemps
caractéristique
(
1
)
associé à cetéquilibre
est de l’ordre de10
-3
à10
-8
sec.
La valeur exacte de cetemps
dépend
bien évidemment de lamolécule considérée et de la concentration de
l’amphiphile ;
Cetemps
caractéristique
est par exemple d’autantplus
court que la chaînealiphatique
de la moléculed’amphiphile
est courte. Le deuxième processus est lent et est décrit parl’équilibre
de micellisation dissolution :Ce processus assure
l’équilibre
entre la concentration totale en monomèreset la concentration
globale
en nombre de micelles. Letemps
caractéristique
(
2
)
associé à cetéquilibre
est dans la zone 10-3 - 1 sec. Là encore lavaleur exacte de ce
temps
est fonction de la nature de la moléculeamphiphile
considérée et de sa concentration.19
CHAPITRE C
LES AMPHIPHILES AUX INTERFACES
I -
INTRODUCTION
Nous avons vu dans le
chapitre précédent quelques
aspects
ducomportement
desamphiphiles
en solution aqueuse; cela ne constitue que l’une des facettes despropriétés
de telles molécules. Une autre facette estconstituée par leur
comportement
d’agent
de surface. Eneffet,
commenous l’avons dit dans le
chapitre
deprésentation
de cesmolécules,
lesamphiphiles
s’adsorbent aux interfaces (eau/air ou eau/huile) et modifientdonc les
propriétés superficielles
ou interfaciales desliquides
où ils sontsolubilisés. C’est à cet
aspect
que nous nous intéresserons dans cechapitre.
Notons que c’est l’un desaspects
essentiels à lacompréhension
de la formation des microémulsions que nous décrirons dans lechapitre
suivant.
Il -
TENSION SUPERFICIELLE OU INTERFACIALE DES SOLUTIONS D’AMPHI-PHILES
II-a) Définition
L’augmentation
isotherme de dA de l’aire d’une surface libre d’unliquide
ou de l’interface entre deuxliquides,
nécessite un travail03B4W,
proportionnel
à dA. Le coefficient deproportionnalité
y est par définition la tensionsuperficielle
ou interfaciale dusystème.
Dans notretravail,
nousn’étudions que des interfaces fluide/fluide. Il existe bien sûr des tensions interfaciales
gaz/solide
ouliquide/solide.
Une tension de surface a la dimension d’uneénergie
par unité de surface. L’unité internationale en est leN/m, cependant,
nousemploierons
leplus
souvent lesystème
d’unités20
CGS,
danslequel
les tensions de surfaces’expriment
endyn/cm
(1 dyn/cm
équivaut
à 1mN/m).Considérons un
système
constitué de deuxphases
1 et 2 enéquilibre, séparées
par un interfaceplan,
d’aire A. Nous retrouveronsplus
loin l’idée que l’on
peut
d’ores etdéjà
souligner
ici,
que le passage de laphase
1 à laphase
2 ne se fait pas defaçon
brusque,
mais sur unecertaine
épaisseur
03C3(Fig
C-1). Onpeut
donc définir un certain volumeV
03C3
.
de
l’interface,
égal
à 03C3A. Notons, P
i
G
i
, V
i
, T
i
, Si
respectivement,
lesenthalpie libre, pression,
volume,
température,
etentropie
de laphase i,
ipouvant
prendre
les valeurs 1 et 2 oupouvant
devenir l’indice 03C3caractérisant la zone intermédiaire.
Le
système
étant àl’équilibre,
lesgrandeurs
intensives pression ettempérature
s’homogénéisent
dans lesystème :
On a ainsi, par différentiation :
d’où :
On déduit de ce
qui précède
que :De
même,
en notant Fl’énergie
libre dusystème,
on aurait pu démontrer que :Dans cette
première
introduction,
nous avonssupposé
que le nombre demolécules des divers constituants dans
chaque
phase
nechange
pas. Nouslèverons cette
hypothèse
par la suite. Eneffet,
après
avoir obtenu l’ordrede
grandeur
des tensions interfaciales eau/huilegrâce
à un modèleapproché,
nous étudierons l’influence del’adsorption
de molécules tensio-actives sur la tension de surface.II-b) Modèle
simplifié
pour le calcul de la tension interfaciale entredeux
liquides simples
Considérons deux
liquides
A et B :-
Représentons
le volumedisponible
auxliquides
A et B par unréseau de maille a, dont
chaque
molécule occupe un noeud.On
néglige
ici les fluctuationsthermiques
desmolécules,
a est donc une taillemoléculaire,
que l’onprend
iciidentique
pourles molécules A et B. On note z le nombre de
plus proches
sites voisins d’un site donné dans ce réseau.- On
note
E
aa
,
E
bb
,
E
ab
,
lesénergies
potentielles
d’interaction d’une paire de molécules voisines de typerespectivement
AA,BB,AB.
Dans un tel modèle,l’enthalpie
demélange
deN
A
molécules A etN
B
moléculesB,
a la forme [17]G
m
= NkT[03A6
A
Log 03A6
A
+03A6
B
Log 03A6
B
+03A6
A
03A6
B
] où N =N
A
+N
B
est le nombre total de sites du réseau.La
thermodynamique
montre que X caractérisecomplètement
la miscibilité des deuxliquides.
22
Si X est <
2,
lemélange
est stable. Lesliquides
A et B sontentièrement miscibles. Nous avons modélisé une solution
stricte-ment
régulière.
Si X est
> 2,
lemélange
n’est pas stable : Il y a démixtion endeux solutions de concentration
03A6’
A
et03A6’’
A
enA,
telles que03A6’
A
+
03A6’’
A
= 1. PlusX est
grand,
plus
03A6’
A
et03A6"
A
diffèrent de 1 etmoins les
liquides
sont miscibles.Nk
[03A6
A
Log 03A6
A
+03A6
B
Log 03A6
B
]
représente
l’entropie
demélange,
alors que NkT X03A6
A
03A6
B
correspond
àl’énergie
interne demélange positive.
(Laphase
étantcondensée,
on confondl’enthalpie
eténergie
libre demélange).
Dans le cas où lesliquides
ne sont pas du tout miscibles(X
’»2),
Il y acréation d’un interface entre les
liquides
A et B purs.Augmenter
l’aire A de l’interface de 03B4A =a
2
,
nécessite d’amener une molécule A et unemolécule B du volume où elles n’étaient entourées que de molécules
identiques,
à la surface où elles sont en contact l’une avec l’autre. Cela nécessite un travail 03B4W où :D’autre
part
03B4W =ya
2
d’oùy =
kT~/za
2
> 0Ce modèle conduit à un ordre de
grandeur
tout à faitreprésentatif
de la réalité; en effet :Dans le cas où il y a miscibilité
partielle,
03B4W est inférieure à kT/z carl’environnement Initial des molécules A et B que l’on
rapproche
pouraugmenter
l’aire de l’interface dea
2
est moins différent que dans le casprécédent.
Plus lesliquides
en contact sont miscibles etplus
la tension Interfaciale est faible. Parexemple
03B3
eau/butanol
= 1,8
dyn/cm .
Onprévoit
donc ici unpremier
cas où la tension interfaciale devient extrêmement basse;quand
lesystème s’approche
d’unpoint critique,
y chute suivant la loi y =03B3
o
(1 -
T/T
C
)03BC
oùT
c
est latempérature critique
et 03BC,l’exposant critique
de la tensioninterfaciale : 03BC
=1,26
est la valeurprévue
par les théories de renormalisation [18].II-C)
Thermodynamique
del’adsorption
L’adsorption
de molécules tensioactives à la surface libre d’unliquide
où à l’interface entre deuxliquides
fait chuter defaçon
radicale la tensionsuperficielle
ou interfaciale. A titre d’ordre degrandeur,
la tension interfaciale 03B3eau/huile tombe d’environ de 50dyn/cm
à 1dyn/cm
enprésence
d’un film de tensioactif. Ils’agit
ici de relier les valeurs de y àl’adsorption.
Dans ce qui suit, nous allons définir les notions de pression desurface,
et d’excès de surface pour une surface libre. Elles segénéralisent
au cas d’un interface. On se limitera au cas d’un tensioactifsoluble et on notera 03B3o la tension
superficielle
en l’absence detensioactif,
et y la tension
superficielle
enprésence
du film de molécules de tensioactifadsorbées.
Considérons une solution d’un tensioactif T dans un solvant S . La
surface libre de cette solution n’est pas infiniment fine. Elle a en fait une
certaine
épaisseur
03C3. De même lesprofils
de concentration des constituants(ici S et T) sont continus.
(Fig
C-1)On note
Ci
la concentration molaire du constituant i (i=T ou S). Onchoisit de
façon
arbitraire unplan
P
03C3
deséparation
entre l’air et lasolution; ce
plan
permet
de définir des nombres de moles d’excèsn
i
03C3
dechaque
constituant :n
i
03C3
est la différence entre le nombre réel de moles du24
concentration en trait
plein
sur lafig
(C-1),
et le nombre de moles de iqu’il
y aurait dans la zone interfaciale si leprofil
de concentration était discontinu et défini par leplan
P03C3(indiqué
enpointillés
sur lafig.
(C-1)). Si on note A l’aire totale de lasurface,
on définit aussi l’excès de surface0393
03C3
i
= n
i
03C3
/A.
Les nombres de moles d’excèsn
i
03C3
,
et0393
03C3
i
dépendent
du choix de P03C3. [19]Dans le cas
simple
où le soluté (ici le tensioactif T) est enconcentration très inférieure à celle du solvant
(S),
on choisit par convention leplan
P
03C3
,
tel quen
S
03C3
=0,
cequi correspond
à des aires hachuréeségales
pour le solvant(Fig
Cl). Nous nousplacerons
dans cecas
(C
T
«C
S
).
Onpeut,
une fois les définitionsposées,
continuer letraitement
thermodynamique
del’adsorption.
Soient U :l’énergie
interne,
S :l’entropie,
V : levolume,
P : lapression,
T : latempérature,
03BC
i
:
lepotentiel
chimique
du constituant i.L’énergie
interne de surface s’écrit :où l’indice 03C3
indique
que lagrandeur
considérée estprise
pour la surface.L’équation
de Gibbs s’écrit alors :De
l’équation
deGibbs,
on déduit :Dans le cas
C
T
«C
S
on a,grâce
au choixprivilégié
de P03C3.03BC T
=
03BC
T
° +
RTLog
03B1TC
T
où 03B1T est le coefficient d’activité dutensioactif,
qui
vérifie25
L’équation
de Gibbs fournit donc la relation entrel’adsorption
du tensioactifet la tension de surface :
Quand il y a
adsorption,
y est une fonction décroissante deC
T
.
De mêmequ’on
définit lapression
osmotique
d’une solution comme ladifférence entre la
pression
dans la solution et lapression
dans le solvant pur àtempérature
donnée,
on définit lapression
de surface par la différence entre la tensionsuperficielle
du solvant pur, et la tensionsuperficielle
de lasolution,
donc enprésence
du film detensioactif,
c’est-à-dire n =
03B3 o
- y. L’inversion de
signe
vient de ce que les termes PV etyA
ne sont pas affectés du mômesigne
dansl’énergie
interne : lapression
tend àaugmenter
levolume,
tandis que la tensionsuperficielle
tend à fairediminuer l’aire de la surface.
L’équation
de Gibbspeut
se mettre sous la forme :où 03A3 est l’aire par molécule tensioactive.
L’équation
de Gibbs reste valable dans le cas d’un interface entredeux
liquides.
II-d) Cas des solutions
d’amphiphiles
Tout en
supposant
C
T
suffisamment faible pourgarder
03B1
T
~
1,
onobserve en
général
trois zones différentes dans le domaine de variation deC
T
.
Ces trois zonescorrespondent
à des lois de variations différentes de yLorsque
C <C
o
,
les molécules tensioactives du filmn’interagissent
pas. La
pression
de surface 03A0 suit la loi des gazparfaits.
03A003A3 =kT, qui
s’écrit aussi 03B3o-03B3 = RT
0393
T
03C3
= -
(~03B3/~LnC
T
)
T
,
p etqui correspond à
unevariation linéaire de y avec
C
T
.
Lorsque
C
o
< C < c.m.c, y varie linéairement en fonction deLog
C
T
,
donc0393
T
03C3
est constant et le film estsaturé en molécules tensioactives. Quand C
augmente
deC
o
à la c. m. c.la concentration des molécules tensioactives isolées dans le volume
augmente.
Enfin,
lorsque
C
T
augmente
àpartir
de la c. m. c,l’équation
de Gibbs écrite ci-dessus reste valable à condition queC
T
nereprésente
plus
la concentration totale des molécules tensioactives dans levolume, mais,
uniquement
la concentration de cellesqui
restent sous forme de monomèresnon
agrégés
dans la solution. Cette dernière concentration restequasiment
constante etégale
à la c. m. c, tandis que les molécules tensioactivesajoutées
forment des micelles. QuandC
T
> c.m.c., le film restesaturé,
et y reste constante. Onpeut
noterqu’on
a trouvé une seconde caused’abaissement de la tension de surface : la