1
I
2
Les Spondylodiscites infectieuses sont définies comme une atteinte septique du rachis, comprenant une atteinte discale et osseuse sans préjuger de l’origine initiale de celle-ci. L’infection disco vertébrale représente un tiers des infections ostéoarticulaires. Elle est fréquente au delà de 50ans. Le siège est multifocal dans 10 à 30% des cas [1].
Les spondylodiscites se distinguent en :
spondylodiscites tuberculeuses : SDT de localisation habituellement dorsale ;
spondylodiscites non tuberculeuses SDNT (pyogènes, parasitaires) de localisation habituellement lombaire (L4 –L5).
En Afrique les spondylodiscites tuberculeuses sont plus fréquentes que les bactériennes et leur évolution est émaillée de complications neurologiques [2].
Les Spondylodiscites tuberculeuses SDT : (mal de Pott) est la localisation la plus fréquente des tuberculoses ostéo articulaires : 35 à 55%. Elle est due au bacille tuberculeux ou bacille de Koch (BK) (Mycobacterium tuberculosis) (la responsabilité de Mycobacterium bovis et de Mycobacterium africanum est ici exceptionnelle) ; la spondylodiscite tuberculeuse classique est caractérisée par l’atteinte du disque intervertébral et des deux vertèbres adjacentes [3]. Cette pathologie affecte essentiellement les patients âgés de plus de 60 ans et/ou ayant un facteur de risque tel que : éthylisme, cirrhose, immunodépression et les sujets vivants dans les zones d’endémie tuberculeuse : Afrique noire le plus souvent, Asie du Sud-Est, Péninsule Indienne, Afrique du nord et au Maroc cette fréquence représente 7,14% [4].
3
Elle est estimée à 1 pour 250 000 habitants [5]. Ce taux est probablement sous estimé. On en dénombre 4 à 13 nouveaux cas par an en moyenne en France dans chacun des services hospitaliers de rhumatologie [6].
Le problème de diagnostique se résume en 3 points essentiels :
Le diagnostic est difficile dans les formes atypiques, les spondylodiscites tuberculeuses dont la sémiologie clinique est trompeuse restent fréquentes et les prélèvements bactériologiques sont difficiles.
Ce travail a pour objectifs de :
Déterminer la fréquence des spondylodiscites tuberculeuses et à bactéries non spécifiques (non tuberculeuses).
Evaluer la sensibilité et la spécificité de l’examen anatomo-pathologique et de l’examen bactériologique direct par rapport à la culture afin de déterminer l’examen biologique le plus sensible et spécifique dans le diagnostic des spondylodiscites infectieuses.
4
P
P
A
A
R
R
T
T
I
I
E
E
I
I
:
:
G
G
E
E
N
N
E
E
R
R
A
A
L
L
I
I
T
T
E
E
S
S
5
1- RAPPELS ANATOMIQUES :
La colonne vertébrale ou rachis va du cou au coccyx et présente en son centre un canal appelé canal rachidien où se trouve la moelle. Elle est composée du :
rachis cervical : 7 vertèbres ; rachis dorsal : 12 vertèbres ; rachis lombaire : 5 vertèbres ;
rachis sacré : 4 à 5 vertèbres soudées constituant le sacrum ;
rachis coccygien qui comporte 4 à 5 vertèbres soudées constituant le coccyx.
La colonne vertébrale comprend 4 courbures : cervicale convexe en avant ; dorsale concave en avant (cyphose) ; lombaire convexe en avant (lordose) et sacro-coccygienne concave en avant.
1-1 Les vertèbres cervicales :
Parmi les vertèbres cervicales, deux sont particulières : la première vertèbre C1ou Atlas et la deuxième vertèbre C2 ou Axis.
L’Atlas est formé de deux masses latérales creusées d’un trou et s’articulant par une facette antérieure avec Axis. Il possède un arc postérieur creusé d’un trou transversal servant de passage à l’artère vertébrale ; un arc antérieur qui est une petite facette articulaire qui s’articule avec l’apophyse odontoïde de C2.
L’Axis est situé sous C1, sa particularité est qu’elle présente une volumineuse apophyse appelée apophyse odontoïde ou dent de l’Axis. Il présente également un massif articulaire de chaque côté, deux apophyses
6
transverses creusées d’un trou et l’apophyse épineuse qui est la fusion des deux lames.
Les autres vertèbres présentent un corps, deux apophyses transverses, deux lames qui fusionnent pour donner l’apophyse épineuse et un trou vertébral. La vertèbre C7 ne possède en général pas de trou transversal et son apophyse épineuse est plus large.
1-2 Les vertèbres dorsales :
Elles présentent un corps vertébral plus épais que celui des vertèbres
cervicales, avec deux surfaces articulaires appelées facettes costales ; deux pédicules larges ; deux lames aussi hautes que larges, aplaties et verticales qui fusionnent en arrière pour donner l’apophyse épineuse ; un trou vertébral ; deux apophyses transverses et deux apophyses articulaires supérieure et inférieure. Les corps vertébraux T11 et T12 ne possèdent pas de facettes articulaires costales.
Le rachis dorsal présente deux courbures physiologiques, une dans le plan sagittal à concavité antérieure, une autre dans le plan frontal dextro-convexe, étendue de T3 à T6.
1-3 Les vertèbres lombaires :
Elles présentent un corps vertébral plus volumineux à concavité postérieure; les pédicules qui sont épais diminuent de hauteur de L1 à L5 ; deux lames épaisses plus hautes que larges, dont la fusion donne l’apophyse épineuse; un trou vertébral central.
Les apophyses transverses ou apophyses costiformes présentent un tubercule accessoire à la base et les apophyses articulaires portent chacune un
7
trabécule mamillaire (saillie osseuse au bord postérieur). L5 se singularise par son volume important du corps vertébral.
1-4 Les vertèbres sacrées :
Les vertèbres sacrées 4 et 5 sont soudées et forment le sacrum. Le sacrum a une forme pyramidale quadrangulaire, aplati d’avant en arrière. On lui décrit quatre faces :
une face antérieure : les 5 vertèbres sont séparées par quatre crêtes
transversales, aux extrémités desquelles se trouvent quatre trous sacrés d’où sortent les branches antérieures des nerfs sacrés ;
une face postérieure qui présente aussi quatre trous sacrés d’où sortent les branches postérieures des nerfs sacrés ;
deux faces latérales ;
une base qui s’articule avec L5 par l’intermédiaire du disque L5-S1 ; un sommet inférieur s’articulant avec le coccyx.
1-5 Les vertèbres coccygiennes :
Les 4 vertèbres coccygiennes sont soudées et forment le coccyx. C’est un petit os triangulaire à base supérieure et sommet inférieur. On lui décrit deux faces, deux bords latéraux, une base s’articulant avec le sommet du sacrum et deux sommets.
1-6 Les articulations de la colonne vertébrale:
Un ensemble de structures assure la stabilité et la mobilité du rachis, et sont groupées sous le terme de segment mobile de Junghanns. Cet ensemble comprend : le disque intervertébral, l’articulation vertébrale postérieure (ou articulation inter-apophysaire), et les ligaments intervertébraux [7].
8
1-6-1 Le disque intervertébral :
C’est le principal moyen d’union entre les vertèbres. Il sert de moyen d’union dans les articulations inter-somatiques. Il est formé de deux parties : une centrale, gélatineuse appelée noyau gélatineux ou pulpus ou nucléus pulposus ; et une périphérique, fibreuse appelée noyau fibreux. L’épaisseur des disques intervertébraux lombaires varie de 10 à 15 mm, et augmente de L1-L2 à L4-L5.
1-6-2 L’articulation intervertébrale postérieure :
Elle unit les facettes portées par les apophyses articulaires supérieure et inférieure. Les apophyses articulaires sont unies par une capsule fibroélastique tapissée par la synoviale, mince au niveau cervical ; serrée et résistante au niveau dorsal et lombaire.
1-6-3 Les ligaments :
Il existe de nombreux ligaments : le ligament longitudinal antérieur, qui adhère la face antérieure des corps vertébraux et des disques ; le ligament longitudinal commun postérieur, qui adhère à la face postérieure des corps vertébraux et des disques ; les ligaments jaunes qui unissent les lames des vertèbres adjacentes ; les ligaments inter-épineux qui unissent les apophyses épineuses et les ligaments sus épineux qui unissent les sommets postérieurs des apophyses épineuses.
Le ligament sus épineux est très développé au niveau du rachis cervical.
1-7 L’espace épidural :
L’espace épidural se définit comme l’espace situé entre le sac dural et les parois rachidiennes, qui s’étend depuis le trou occipital (foramen magnum) en haut jusqu’à l’extrémité inférieure du canal vertébral en bas. Il est composé de deux compartiments : épidural antérieur et épidural dorso-latéral [8].
9
Il est occupé par des éléments artériels et veineux ; par les racines nerveuses et les graisses épidurales.
Le système veineux comprend les plexus épiduraux, les veines émissaires du trou de conjugaison et les veines lombaires ascendantes.
Au niveau cervical, il est pauvre en graisse mais très riche en plexus veineux anastomosés.
1-8 Les muscles para-vertébraux :
Au niveau dorsal, les muscles para-vertébraux sont repartis de façon symétrique de part et d’autre de l’apophyse épineuse et en arrière des apophyses transverses.
On distingue plusieurs groupes : le groupe profond avec les muscles épineux, les petits dentélés postérieurs et les muscles sus costaux ; le groupe moyen avec l’angulaire de l’omoplate, le rhomboïde et le grand dentélé ; le groupe superficiel avec le grand dorsal et le trapèze.
Au niveau lombaire, les muscles psoas avec leur chef ventral et le dorsal bordent le rachis de part et d’autre, on distingue aussi les muscles spinaux qui se divisent en trois faisceaux au niveau de L3, le muscle transverse épineux, le long dorsal, le muscle iliocostal et le carré des lombes.
2- SPONDYLODISCITES TUBERCULEUSES : 2-1 EPIDEMIOLOGIE :
La tuberculose vertébrale est l'atteinte infectieuse par le bacille tuberculeux des structures ostéoarticulaires du rachis, incluant le sacrum, qui comporte deux formes différentes, la discite et la spondylite. Fréquente dans les pays en voie de développement, elle reste d'actualité dans certains pays développés, où son diagnostic a bénéficié des progrès des techniques d'imagerie médicale et de
10
prélèvements percutanés. Le traitement médical est basé sur l'antibiothérapie antituberculeuse.
A- HISTORIQUE :
La description clinique de la tuberculose vertébrale est attribuée à SIR PERCIVAL POTT qui, vers 1782 décrivit un tableau associant une atteinte rachidienne cyphosante associée à des abcès et à une atteinte paralysante des membres inférieurs [9]. Son étiologie fut reconnue 1882 grâce à la découverte par ROBERT KOCH du bacille tuberculeux. Au début du siècle, la tuberculose pulmonaire constituait une des premières causes de mortalité en Europe où elle était très fréquente [10]. Son épidémiologie, et partant celle de la tuberculose ostéoarticulaire a été radicalement modifiée dans les pays développés par l’avènement des antibiotiques avec, la STREPTOMYCINE en 1945, puis dans les années 1950 les autres antituberculeux majeurs.
B- FREQUENCE :
A l'ère de l'antibiothérapie antituberculeuse, la tuberculose ostéoarticulaire représente 3 à 5% de l'ensemble des tuberculoses et 15% des tuberculoses extra pulmonaires [11, 12]. L'incidence annuelle a été estimée à 0,5 pour 100.000 au Canada (années 1980-1984) [13]. En France, la tuberculose ostéoarticulaire est certainement plus fréquente qu'au Canada et le Danemark. L'incidence annuelle de la tuberculose vertébrale a été estimée dans la région de Lille à 3,6 pour 100.000 dans les années 1970 et 1,2 pour 100.000 en 1990 [14]. Depuis 1992 l'incidence est augmentée en France. Les facteurs incriminés ont été l'infection par virus de l'immunodéficience (VIH), l'immigration et la précarité des conditions de vie de sous groupes sociaux défavorisés dans les grandes métropoles.
11
C-TERRAIN:
La tuberculose privilégie deux groupes de population : les autochtones âgés de plus de 60 ans ;
et celles vivants en zone d'endémie tuberculeuse dont l'âge moyen est de 45 ans [3].
D- FACTEURS FAVORISANTS :
La notion de contage tuberculeux 10% est moins fréquente que l'antécédent de tuberculose (18 à 43%) [3, 15]. La fréquence d'un facteur ou d'un état d'immunodépression est diversement appréciée selon les séries de 6 à 17% pour les tuberculoses vertébrales. Ces facteurs d'immunodépression sont : l'infection par le VIH, l'éthylisme chronique, la cirrhose hépatique, la corticothérapie prolongée, le diabète, les syndromes prolifératifs et le traitement immunosuppresseur associé [16].
2-2 LOCALISATION :
Le rachis dorsal et lombaire sont atteints à part presque égale par la tuberculose vertébrale, représentant à eux plus de 80% des localisations rachidiennes [15]. Le sacrum représente environ 5% et le rachis cervical varie de 3 à 22%.
L’atteinte mono-étagée est la plus fréquente. Les atteintes multi-étagées sont de fréquence variable dans la littérature. La classique spondylodiscite associe une atteinte discale et vertébrale. Les atteintes inhabituelles sont représentées par celles de l'arc postérieur, centrosomatique, sous ligamentaire et sous occipital [15, 17].
12
2-3 PHYSIOPATHOLOGIE :
Dans les lésions tuberculeuses, le bacille de Koch peut être extra ou intra cellulaire (macrophages). Les bacilles intracellulaires sont dits dormants car leur survie peut atteindre des dizaines d'années (quiescente) et se réactiver à l'occasion d'une baisse des défenses immunitaires [18]. La dissémination se fait par voie hématogène, à partir d'un foyer primaire qui est le plus souvent pulmonaire. Une dissémination par voie lymphatique à partir des lésions rénale ou pleurale a été évoquée. Le disque intervertébral n'est plus vascularisé après l'âge de 7 ans, ainsi la tuberculose vertébrale de l'adulte débute par la localisation du BK à l'os spongieux vertébral par voie hématogène [9]. L'extension vers le corps vertébral adjacent se fait probablement autour du disque intervertébral, soit par contiguïté sous le ligament longitudinal antérieur, soit par le biais d'anastomoses vasculaires. L'atteinte du disque intervertébral est secondaire. Elle survient quand les deux corps vertébraux adjacents sont touchés, ce qui entraîne un défaut de la nutrition passive par diffusion, suivie d'une extension de l'infection vers le disque intervertébral qui se pince secondairement. La tuberculose vertébrale s'étend assez fréquemment dans l'espace épidural ; cette extension pouvant prendre la forme d'une épidurite granulomateuse et/ou d'un abcès [19].
Les compressions médullaires et plus rarement celle de la «queue de cheval» sont le plus souvent dues à une épidurite tuberculeuse granulomatose et/ou abcédée. Elles peuvent être mécaniques par compression d'origine osseuse.
2-4 Etiologies :
Le germe en cause est bacille de koch surtout Mycobacterium tuberculosis qui est caractérisé par une évolution chronique.
13
Le germe arrive dans le foyer discovertébral par voie hématogène. La race Noir transplanté d’Afrique est plus exposé à la tuberculose. Une inoculation directe est très rare (après discographie).
2-5 Manifestations cliniques :
Le processus tuberculeux est généralement lent et la clinique pauvre. Ici, le mode de début est habituellement progressif, subaiguë ou chronique.
Le principal symptôme est la douleur rachidienne localisée et continue, aggravative. La spondylodiscite peut-être indolore et découverte au stade d’abcès des parties molles.
Les signes généraux sont inconstants : fièvre, asthénie, amaigrissement, sueurs nocturnes et une altération de l’état général. Les signes physiques sont à type de raideur segmentaire, de cyphose vertébrale et de douleur provoquée à la pression sur le rachis. Les signes neurologiques sont fréquents et estimés à 35 – 60 % des cas : radiculalgie, syndrome de la queue de cheval et des signes de compression médullaire [5]. Il peut également s’associer des signes d’autres localisations tuberculeuses. Parfois, on observe un psoïtis en cas d’abcès du psoas.
3-SPONDYLODISCITES NON TUBERCULEUSES 3-1 EPIDEMIOLOGIE :
A- FREQUENCE :
L’incidence des spondylodiscites non tuberculeuses est difficile à évaluer. On estimait à 1 pour 250000 habitants par an en 1979, et on dénombre 4 à 13 nouveaux cas par an en moyenne en France dans chacun des services hospitaliers de rhumatologie [1, 20, 6].
14
B-TERRAIN :
La plupart des études trouvent une prédominance masculine avec une sex-ratio moyenne de 3 hommes pour 2 femmes. La spondylodiscite non tuberculeuse peut survenir à tout âge, mais il existe deux pics de fréquence : le premier à l’adolescence, le deuxième autour de 60 ans. Dans les séries les plus récentes la proportion de sujets de plus de 60ans augmente et la prédominance masculine s’estompe [21].
C- FACTEURS FAVORISANTS :
Certains sont classiques : le diabète, l’éthylisme et la toxicomanie.
Depuis une vingtaine d’année on note une augmentation importante du nombre de sujets immunodéprimés, liée soit à l’infection par le VIH ou accompagnant une transplantation d’organe ou encore être la conséquence d’une chimiothérapie anticancéreuse ou du traitement d’une maladie auto-immune.
D- PORTE D’ENTREE :
Certaines portes d’entrée possibles sont bien connues : infections urogénitales, infections cutanées, infections de la sphère ORL, les endocardites, les diverticulites et les cancers coliques. Les spondylodiscites non tuberculeuses iatrogènes sont devenues plus fréquentes du fait de la pratique de plus en plus répandue de nouvelles techniques médicales ou chirurgicales potentiellement responsable de complications septiques : la mise en place de cathéter veineux profond et de pacemaker, la pratique de l’hémodialyse, la réalisation des manœuvres instrumentales dans la sphère urogénitale, la chirurgie lourde carcinologique ou non du petit bassin, la chirurgie discale et vertébrale et la pratique de ponction discale ou intra durale pour réaliser une chimionucléolyse, une simple discographie ou une rachianesthésie. Une spondylodiscite non
15
tuberculeuse peut aussi compliquer une intubation, une colonoscopie ou encore la mise en place d’une prothèse valvulaire ou articulaire [22, 23, 24, 25].
3-2 LOCALISATION :
Le siège des spondylodiscites infectieuses non tuberculeuses est plus lombaire que dorsal et encore plus rarement cervical. Les derniers disques lombaires sont atteints avec prédilection et notamment le disque L4-L5. Dans 10 à 30% des cas la spondylodiscite est multifocale [21].
3-3 PHYSIOPATHOLOGIE :
La contamination peut être directe. Elle est alors le plus souvent d’origine iatrogène, secondaire à une cure chirurgicale de hernie discale, à une chimionucléolyse, à une discographie ou plus rarement à une injection épidurale ou une ponction lombaire.
Le germe le plus souvent responsable est le staphylocoque doré. Le délai d’incubation des spondylodiscites par inoculation est court, de l’ordre de 1 à 2 semaines [6].
Dans la majorité des cas le germe parvient au rachis par voie hématogène. La porte d’entrée, iatrogène ou non est alors à distance, urogénitale dans un tiers des cas, cutanée dans 10 à 20% des cas, respiratoire ou ORL dans 20% des cas, digestive ou vasculaire faisant suite à un geste chirurgical le plus souvent [21]. Enfin parfois le germe peut provenir d’une endocardite infectieuse.
Le germe peut être véhiculé par voie artérielle ou veineuse et terminer sa course dans la partie antérieure d’une vertèbre, en région sous chondrale entraînant une spondylite. Ensuite par perforation de la corticale et du cartilage, le disque est atteint formant alors une spondylodiscite. Parfois le germe termine son cheminement vasculaire directement dans l’espace intervertébral,
16
responsable alors d’une discite. Les plateaux vertébraux adjacents sont infectés dans un second temps. Cette éventualité intéresse particulièrement les sujets jeunes, car il persiste jusqu’à l’âge de 20 ans des vaisseaux lymphatiques et sanguins dans l’annulus même [26].
3-4 Etiologies :
Les germes en cause sont les bactéries pyogènes, plus rarement les salmonelles et les brucelles. Ces germes sont caractérisés par une évolution aiguë et aussi une évolution chronique en cas d’infections à pyogènes refroidies par une antibiothérapie insuffisante.
Le germe arrive dans le foyer discovertébral par voie hématogène, par exemple bactériémie en postopératoire ou post-endoscopie urinaire.
Une inoculation directe est très rare (après discographie, nucléolyse à la papaïne ou cure chirurgicale de hernie discale).
3-5 Manifestations cliniques :
Le tableau classique associe :
la fièvre : présente dans un tiers des cas [21]. Elle est souvent irrégulière ou modérée, parfois décapitée par une antibiothérapie préalable, peut apparaître plusieurs jours ou semaines après la douleur mais peut également la précéder. Elle peut s’accompagner d’autres signes généraux : amaigrissement ou altération de l’état général.
la douleur rachidienne : elle est le maître de symptôme. Cette douleur est classiquement spontanée, segmentaire, intense et d’horaire inflammatoire. Elle peut être brutale ou d’apparition progressive ; une irradiation radiculaire est présente dans près de la
17
moitié des cas [1, 6]. La douleur est souvent banale, d’intensité modérée et d’horaire mécanique ; c’est alors la persistance qui doit attirer l’attention. Tous les intermédiaires sont possibles entre les douleurs peu intenses et les douleurs vives, insomniantes, résistantes à l’antalgique usuelle et responsable d’une impotence fonctionnelle majeure.
la raideur vertébrale segmentaire est pratiquement constante, franche ou au contraire très modérée. Une contracture des muscles para vertébraux peut s’y associer, responsable de torticolis au rachis cervical ou d’une attitude scoliotique au rachis dorsal et lombaire. la recherche d’une complication neurologique doit être systématique: une radiculalgie, un déficit moteur ou une compression de la queue de cheval.
un abcès peut se manifester par un empâtement para vertébral. Il peut aussi se manifester à distance, en particulier au triangle de Scarpa s’accompagnant d’un psoitis.
18
P
P
A
A
R
R
T
T
I
I
E
E
I
I
I
I
:
:
D
D
I
I
A
A
G
G
N
N
O
O
S
S
T
T
I
I
C
C
E
E
T
T
T
T
R
R
A
A
I
I
T
T
E
E
M
M
E
E
N
N
T
T
19
1-DIAGNOSTIC :
1-1 Circonstances de diagnostic :
Le diagnostic de spondylodiscite bactérienne est évoqué devant deux situations cliniques différentes :
-Douleur vertébrale intense en climat fébrile
La douleur est à début brutal : elle est permanente, insomniante, localisée mais pouvant irradier selon un trajet radiculaire. Elle s’accompagne rapidement d’une impotence fonctionnelle importante. L’examen clinique de rachis est alors impossible.
Il s’y associe des signes généraux : fièvre avec frissons, sueurs ou abattement.
Les signes généraux peuvent être au premier plan au cours d’une septicémie et c’est secondairement que le patient signale les douleurs vertébrales.
-Douleur vertébrale d’installation progressive d’allure mécanique, puis devenant plus continue.
Ce qui domine à l’examen clinique ; c’est la contracture musculaire paravertébrale et la raideur du segment vertébral douloureux. Tardivement on peut se trouver devant un trouble statique : cyphose dorsale avec gibbosité, ou inversion de la lordose lombaire. Plus rarement, c’est une radiculalgie ou une compression médullaire lente qui vient révéler l’affection.
Un abcès froid paravertébrale ou inguinal est plus exceptionnel actuellement. Il faut savoir le rattacher à une origine osseuse vertébrale.
20
1-2 Diagnostic radiologique :
a) Spondylodiscite non tuberculeuse :
L’imagerie par résonance magnétique (IRM) est la technique la plus sensible dans cette indication et doit être utilisée en première intention dès que le diagnostic de spondylodiscites est envisagé. Elle est toujours associée à des radiographies standards de face et de profil sur le segment rachidien douloureux, complétée par une incidence centrée sur la zone suspecte.
Elle doit être effectuée en urgence s’il existe des signes neurologiques faisant suspecter une épidurite ou une compression d’origine osseuse. L’aspect typique de spondylodiscites en IRM associe un ensemble de signes caractéristiques et rend le diagnostic très probable lorsque ces signes sont tous présents. En cas d’aspect atypique, il est recommandé de répéter l’IRM une à deux semaines plus tard. L’IRM est utile pour éliminer une spondylodiscite postopératoire si elle montre l’absence de signe d’inflammation des plateaux vertébraux et des parties molles.
Les radiographies standard sont le plus souvent normales durant les premières semaines d’évolution, mais elles sont utiles pour rechercher les signes précoces, comme l’effacement d’un plateau vertébral ou un pincement discal. Leur normalité ne doit pas faire conclure à l’absence de spondylodiscite. A la phase de spondylodiscite constituée, les radiographies standards permettent d’apprécier l’importance du pincement discal et des érosions vertébrales et leur retentissement sur la statique rachidienne : cyphose, scoliose ou dislocation.
La scintigraphie osseuse au 99mTc est recommandée en cas de
contre-indication à l’IRM, car elle est très sensible aux phénomènes inflammatoires. Il faut l’associer à des radiographies standards et à une TDM pour améliorer sa
21
spécificité, pour faire le bilan d’extension précis de la spondylodiscite, notamment au niveau des parties molles et du canal rachidien.
La TDM n’est pas recommandée en première intention. Sa sensibilité diagnostique est meilleure que celle des radiographies standards, mais inférieure à celle de l’IRM. Elle est donc faite en cas de contre-indication à l’IRM, après la scintigraphie osseuse qui indique la zone rachidienne atteinte. Elle peut aussi aider à guider la ponction-biopsie discovertébrale.
Dans la majorité des cas, les deux vertèbres contigües au disque infecté sont concernées, plus fréquemment dans les spondylodiscites à pyogènes (82 à 100%) que dans les tuberculoses vertébrales ou il peut exister une atteinte vertébrale isolée de (48 à 74%). L’atteinte initialement mono-vertébrale peut évoluer avec le temps et s’étendre au disque puis à la vertèbre contiguë. Les atteintes pluri-vertébrales (sup à 2) sont très fréquentes dans la tuberculose (60%) comparées aux spondylodiscites à pyogènes (25%) [27, 28, 29].
b) Spondylodiscites tuberculeuses :
Des radiographies standards de face et de profil sont réalisées devant les douleurs rachidiennes, elles sont centrées sur le segment douloureux. Le diagnostic repose sur l’imagerie par résonance magnétique (IRM), en dehors de contre-indication, qui est évocatrice de tuberculose, en particulier s’il existe des abcès péri-rachidiens volumineux ou une atteinte étagée non continue. Une spondylite isolée peut être observée dans 50% des cas d’atteintes tuberculeuses en particulier chez les sujets immigrés [17, 30].
22
Le diagnostic radiologique se résume dans le schéma suivant :
Figure 1 : Arbre décisionnel d’imagerie pour diagnostic de SDI [27] * Si anomalies IRM insuffisamment évocatrices de SD.
23
1-3 Diagnostic macroscopique : 1-3-1 Diagnostic microbiologique
a) Spondylodiscites non tuberculeuses :
La suspicion de spondylodiscite sur des arguments cliniques et d’imagerie nécessite de tout mettre en œuvre pour identifier le micro-organisme en cause, avant toute prescription d’antibiotique. Les deux principaux moyens sont les hémocultures et la ponction biopsie discovertébrale, les marqueurs de l’inflammation ne sont pas spécifiques, seule la protéine C-réactive (CRP) étant utile pour le suivi évolutif.
Les hémocultures permettent d’identifier le micro-organisme en cause dans 35 à 63% des spondylodiscites primitives, mais seulement dans moins de 20% des cas de spondylodiscites postopératoires.
La ponction biopsie discovertébrale est actuellement l’examen de référence pour le diagnostic microbiologique des spondylodiscites, lorsque les hémocultures sont négatives. Elle permet d’identifier le micro-organisme dans environ deux tiers des cas. La négativité des cultures de la ponction biopsie discovertébrale peut être due à un traitement antibiotique préalable et récent (moins de 2 semaines) ou à des prélèvements de volume ou de nombre insuffisant. Il est donc essentiel de réaliser plusieurs prélèvements, idéalement quatre prélèvements des plateaux vertébraux osseux (2 du plateau vertébral supérieur, 2 du plateau vertébral inférieur) et deux prélèvements discaux. Ces prélèvements doivent être adressés pour analyse microbiologique (3 ou 4 prélèvements), analyse anatomo-pathologique (1 ou 2 prélèvements) et éventuellement pour la réalisation ultérieure d’une Polymerase Chain Reaction (PCR). La ponction biopsie discovertébrale doit être réalisée dans des conditions
24
d’asepsie chirurgicale, sous contrôle fluoroscopique ou TDM. Des hémocultures doivent systématiquement être effectuées dans les 4 heures qui suivent la ponction biopsie. En cas de négativité d’une première ponction biopsie, une deuxième peut être discutée.
Une biopsie chirurgicale n’est envisagée que si une deuxième ponction-biopsie percutanée s’avère négative, si l’évolution clinique ou radiologique est défavorable sous un traitement probabiliste donc ce sont les infections à micro-organisme non pyogènes qui sont retrouvées (candidose, aspergillose, tuberculose, brucellose) [31, 1].
b) Spondylodiscites tuberculeuses :
Mycobacterium tuberculosis est isolé difficilement à partir de la
ponction-biopsie discovertébrale. Une ponction des abcès avec repérage échographique ou TDM doit être faite en première intention. En cas de forte suspicion de SDT, avec abcès péri-rachidien, la ponction de l’abcès permet d’isoler M.tuberculosis dans 50 à 93% des cas de spondylodiscites tuberculeuses plus facilement qu’à partir d’une biopsie tissulaire percutanée ou préopératoire. L’étude du prélèvement par Polymerase Chain Reaction (PCR) doit être associée aux techniques « classique » de microbiologie, car elle pourrait être positive dans près de 95% des cas [32, 1, 30].
25
Le diagnostic microbiologique se résume dans le schéma suivant :
Figure 2 : Diagnostic microbiologique et arbre décisionnel thérapeutique au
26
1-3-2 Diagnostic anatomopathologique :
L’examen anatomopathologique permet alors un diagnostic plus rapide en mettant en évidence des signes d’inflammation spécifique (inflammation granulomateuse avec nécrose caséeuse).
Cet examen est particulièrement utile pour le diagnostic de tuberculose ou pour éliminer une autre étiologie, en particulier tumorale.
En cas de spondylodiscite tuberculeuse ; cet examen est positive dans 55% des cas [1, 30, 33, 34, 35].
2-TRAITEMENT
2-1 Spondylodiscites tuberculeuses : 2-1-1 Traitement anti-infectieux
Le traitement de première intention repose sur une quadrithérapie : rifampicine – isoniazide – pyranizamide – éthambutol.
L’éthambutol étant arrêté dés que le profil de sensibilité de la souche est connu et l’autorise. La pyrazinamide est arrêtée à la fin du deuxième mois de traitement, le traitement d’entretien reposant sur la bithérapie : Rifampicine-isoniazide pour une durée totale de traitement de 9 à 12 mois.
Bien qu’il n’y ait pas d’élément de preuve, la durée de traitement proposée est de 9 ou 12 mois pour les formes extra-pulmonaires graves et les localisations osseuses [27, 36].
2-1-2 Traitement par immobilisation et réadaptation fonctionnelle
Le traitement de la spondylodiscite tuberculeuse n’est pas différent de celui des autres types de spondylodiscites. Les moyens utilisés sont le décubitus strict, la contention et des exercices quotidiens de renforcement musculaire et articulaire (entretien des mobilités articulaires et de la musculature des
27
membres) proprioceptive et de conditionnement cardiorespiratoire. Les procédures de rééducation permettent de limiter ou de compenser les déficiences, les incapacités et le handicap liés à une spondylodiscite [27].
2-1-3 Traitement chirurgical :
Le traitement chirurgical n’est pas différent des autres types de spondylodiscites.
Le but du traitement, s’il est nécessaire, est d’obtenir une décompression des structures neurologiques menacées par l’extension de l’infection. La règle de l’évacuation-lavage-drainage prévaut au même titre que le traitement chirurgical de n’importe quel abcès [27].
2-1-4 Eléments de la surveillance :
La surveillance est basée sur le contrôle :
syndrome inflammatoire ;
syndrome de la radiographie standard.
Et aussi, elle est basée sur l’étude de la tolérance des antibiotiques, le suivi clinique et biologique qui se traduit par une diminution des douleurs rachidiennes et la disparition de leur caractère inflammatoire : retour à l’apyrexie, normalisation de la protéine C-réactive (CRP) et stabilisation des images discovertébrales en radiologie standard [27].
2-2 Spondylodiscites non tuberculeuses : 2-2-1 Traitement anti-infectieux :
Le choix du traitement antibiotique est déterminé par le terrain, la porte d’entrée, le micro-organisme présumé et les caractéristiques pharmacocinétiques et pharmacodynamiques des molécules disponibles.
28
Le traitement d’attaque nécessite une association bactéricide de deux antibiotiques synergiques à posologie élevée. Il se fait par voie intraveineuse surtout s’il existe une bactériémie associé pendant deux à trois semaines selon l’évolution (si la CRP est normalisée) [37, 38]. Il est relayé par un traitement d’entretien.
Les aminosides gardent leur place dans le traitement d’attaque en cas de septicémie ou d’endocardite en raison de leur activité bactéricide marquée et rapide. Dans l’infection osseuse chronique, l’activité des antibiotiques peut être diminuée [39]. Les antibiotiques sont donc prescrits à leur posologie maximale. La clindamycine, les fluoroquinolones, la rifampicine, l’acide fusidique ont une bonne biodisponibilité par voie orale (Tableau 1) [40, 39, 41]. Ces antibiotiques sont utilisés pour le traitement d’entretien, mais leur utilisation en traitement d’attaque serait théoriquement déconseillée car, ils pourraient favoriser sur un inoculum important l’émergence de mutants résistants (Ce phénomène a surtout été observé lorsque ces antibiotiques ont été utilisés en monothérapie). En pratique, l’expérience clinique [42, 43, 44, 45] montre qu’en cas de spondylodiscite à germes sensibles sans septicémie ni endocardite ni déficit moteur, un relais per-os plus rapide et même un traitement per-os d’emblée associant des antibiotiques à très bonne diffusion osseuse peut être envisagé à condition de s’assurer de la bonne observance du patient et de l’absence d’interaction médicamenteuse. Les pansements gastriques, le sucralfate, le fer et les produits laitiers diminuent la biodisponibilité orale des fluoroquinolones : on veillera à respecter un intervalle d’au moins deux heures entre la prise des fluoroquinolones et celles de ces substances. La durée totale optimale du traitement antibiotique est difficile à établir : plusieurs études observationnelles
29
montrent qu’un traitement inférieur à quatre [46], six [47] ou huit semaines [48] augmente de façon importante le nombre de rechute (> 14 %, 10 %, > 15 % respectivement) comparativement à un traitement supérieur à 12 semaines (3,9%) [49]. En raison de l’importance du retard diagnostique habituel par rapport aux premiers signes cliniques (délai moyen = 6 [42] à 7 [38] semaines), nous considérons que les spondylodiscites doivent être traitées comme les ostéites chroniques par au moins 12 semaines d’antibiotiques [41]. Si le diagnostic et le traitement sont faits précocement dans les deux premières semaines d’évolution par rapport au début des signes cliniques, un traitement de six semaines [41] pourrait être suffisant, mais cette attitude devra être confirmée par une étude randomisée contrôlée multicentrique. Dans tous les cas, cette durée d’antibiothérapie doit être adaptée individuellement en fonction de l’évolution clinique, biologique et radiologique, du terrain (immunodéprimé ?) et de la multirésistance de la bactérie (surtout si elle nous contraint à prescrire des antibiotiques bactériostatiques et non bactéricides).
a)Diffusion osseuse des antibiotiques : [50]
Tableau 1 : ATB à diffusion osseuse
Pénétration osseuse excellente : Fluoroquinolones, Clindamycine, Rifampicine, Acide fusidique, Métronidazole.
Pénétration osseuse moyenne : βlactamines, Glycopeptides, Fosfomycine, Sulfamides. Pénétration osseuse faible : Aminosides (mais, augmentée à la phase inflammatoire).
30
b) Proposition d’antibiothérapie selon le germe : (Tableau 2)
Au sein de chaque classe thérapeutique, le choix d’un antibiotique a été guidé par des différences de pharmacocinétique, de modalité d’administration, de toxicité ou de coût. Ainsi, en relais per-os, la cloxacilline a été préférée à l’oxacilline, car elle a une meilleure biodisponibilité par voie orale [51]. La Nétilmicine a été préférée aux autres aminosides pour le traitement des infections à Gram positives en raison de sa moindre ototoxicité. La teicoplanine a été préférée à la vancomycine en raison de sa moindre néphrotoxicité et de sa modalité d’administration plus pratique [52]. La ciprofloxacine doit être préférée aux autres fluoroquinolones en cas d’infection à Pseudomonas aeruginosa ou aux autres bacilles Gram négatives en raison des concentrations minimales inhibitrices plus faibles de cet antibiotique pour ces bactéries [53]. Pour les infections à staphylocoque, l’ofloxacine a été préférée car il est moins cher que les nouvelles fluoroquinolones.
31
Tableau 2 : Proposition d’antibiothérapie selon le germe pour le traitement des
spondylodiscites [50]
Germe
Traitement d'attaque
Traitement Entretien
1ère intention Alternative
SAMS Oxaclline I.V pendant 2 à 3s
Nétilmicine I.V pdt 7à10j relayée par Ofloxacine
Si allergie aux βlactamines Teicoplanine (ouVancomycine) + Nétilmicine
Rifampicine+Ofloxacine (possible aussi en ttt d’attaque si SD compliquée
SARM
Teicoplanine (ouVancomycine)
pendant 3 s+ Nétilmicine I.V. pendant 7 à 10 j relayée par Rifampicine
Teicoplanine (ou Vancomycine) +Rifampicine
Si Ofloxacine sensible (rare) Ofloxacine + Rifampicine Si Lincomycine sensible Clindamycine + Acide Fusidique
Streptocoque Amoxicilline I.V. pendant 2 à 3 s + Nétilmicine I.V. pendant 7 à 10 j
Si allergie aux βlactamines : Teicoplanine (ou Vancomycine) + Nétilmicine
Amoxicilline
Entérocoque Amoxicilline I.V. pendant 2 à 3 s+ Nétilmicine I.V. pendant 7 à 10 j
Si Péni R : Teicoplanine (ou Vancomycine) + Nétilmicine
Amoxicilline + Rifampicine ou Clindamycine si Lincomycine sensible
BGN
Ceftriaxone ou Cefotaxime IV pendant 3 s + Amikacine I.V. pendant 7 à 10 j relayée par Ciprofloxacine
Céfotaxime + Ciprofloxacine Si allergie aux βlactamines : Ciprofloxacine + Amikacine
Ciprofloxacine
Pseudomonas
Ceftazidime I.V. pendant 6 s
+ Amikacine I.V. pendant 7 à 10 j, relayée par Ciprofloxacine
Imipénème + Amikacine Céfépime + Amikacine
Si allergie aux βlactamines : Ciprofloxacine + Amikacine Aztréonam + Amikacine
Ciprofloxacine
Anaérobies Métronidazole (sauf si Propionibacterium acnes) Clindamycine Clindamycine Brucella Doxycycline + Rifampicine (à 15 mg/kg)
SAMS : Staphylocoque aureus méti-S SARM : Staphylocoque aureus méti-R BGN : Bacille Gram Négative
SD : Spondylodiscite Pdt : Pendant
32
c) Propositions de posologies des antibiotiques
Adaptation en fonction des dosages biologiques :
La posologie des aminosides et des glycopeptides doit être systématiquement adaptée aux dosages sériques. Après avoir atteint la concentration sérique souhaitée, une surveillance au moins une fois par semaine reste nécessaire pour les aminosides et les glycopeptides [41].
Adaptation en fonction de la fonction rénale :
Il faut réduire la posologie : des βlactamines si la clairance de la créatinine est inférieure à 30 ml/min, celle des fluoroquinolones si la clairance de la créatinine est inférieure à 50 ml/min, celle des glycopeptides si la clairance de la créatinine est inférieure à 50 ml/min.
La dose de charge de la teicoplanine ne doit pas être adaptée à la fonction rénale ; en revanche, la posologie quotidienne pour le traitement d’entretien sera diminuée en cas d’insuffisance rénale [52]. Il faut modifier l’intervalle des injections des aminosides si la clairance de la créatinine est inférieure à 50 ml/min.
33
Tableau 3 : Proposition de posologie des antibiotiques pour le traitement des
spondylodiscites pour un adulte à fonction rénale normale [50]
Antibiotique (voie d'administration) Posologie
Nombre d'administration
Par 24 heures
ß-Lactamines
Oxacilline (P.O, I.V) Bristopen® 100 à 150 mg/kg/24 h 4
Cloxacilline (P.O, I.V) Orbénine® 100 à 150 mg/kg/24 h 4
Amoxicilline (P.O, I.V) 150 mg/kg/24 h 4
Ceftriaxone (I.V, I.M) Rocéphine® 50 à 70 mg/kg/24 h 1 à 2
Céfotaxime (I.V) Claforan® 150 mg/kg/24 h 3
Ceftazidime (I.V) Fortum® 100 mg/kg/24 h 3 à 4 ou perfusion
continue
Imipenem (I.V) Tiénam® 50 à 100 mg/kg/24 h 3 à 4
Cefépime (I.V) Axépim® 50 à 100 mg/kg/24 h 2 à 3
Cefpirome (I.V) Céfrom® 4 à 6 g/24 h 2 à 3
Aztréonam (I.V) Azactam® 6 g/24 h 3
Aminosides
Gentamicine (I.V, I.M) Gentalline® 3° mg/kg/24 h 1 ou 2 si
endocardite
Nétilmicine (I.V, I.M) Nétromicine® 4 à 6° mg/kg/24 h 1 ou 2 si endocardite
Amikacine (I.V, I.M) Amiklin® 15°mg/kg/24 h 1 ou 2 si endocardite ou
Pseudomonas Glycopeptides
Teicoplanine (I.V, I.M, S.C) Targocid® Dose de charge = 10° mg/kg/12 h 3 à 5 fois
1 après 3 à 5 doses de10mg/kg/12 h
Vancomycine (I.V) Dose de charge = 1 g/2 h puis
30° mg/kg/12 h SE
Fluoroquinolones (I.V, P.O)
Ofloxacine Cp et Amp à 200 mg (400) à 600 mg/24 h (2) à 3
Ciprofloxacine Cp à 500 et 750 mg P.O. 1500 mg/24 h (2 g Si
pseudomonas) 2
Amp à 200 mg I.V. 600 à 800 mg/24 h 2 à 3
Divers
Rifampicine Rifadine® (I.V, P.O) Gel à 300 mg 20 à 30 mg/kg/24 h 2 à jeun
Clindamycine Dalacine® (I.V, PO)gél à 300 mg 1,8 à 2,4 g/24 h 3 à 4
Acide fusidique Fucidine® (I.V, P.O) cp à 250 1,5 à 2 g/24 h 3
Doxycycline Cp à 100 mg pendant le repas 200 mg/24 h 1
P.O :per os ;
SE: seringue électrique; I.V: Intra-veineuse; I.M:Intra-Musculaire; S.C: Sous-cutané.
34
d) Surveillance de l’antibiothérapie :
Une surveillance clinique et biologique pendant la totalité du traitement antibiotique et dans les six mois qui suivent son arrêt [49] est indispensable. On doit s’assurer de l’absence de complications neurologiques, de la régression de la fièvre, des rachialgies et du syndrome inflammatoire. La CRP doit diminuer de 50 % toutes les semaines [45] et retrouver des valeurs normales vers quatre semaines [41]. La vitesse de sédimentation décroît plus lentement. La surveillance concerne également l’observance, la tolérance clinique (troubles digestifs, allergie…) et biologique (NFS, plaquettes, fonctions rénale et hépatique) des antibiotiques. La créatinémie doit être mesurée au moins deux fois par semaine en cas de traitement par aminosides [51].
2-2-2 Drainage des abcès :
Les abcès volumineux ou résistants au traitement antibiotique, les abcès de localisation extra vertébrale (psoas, plèvre…) doivent bénéficier d’un drainage par radiologie interventionnelle ou par ponction pleurale ou plus rarement d’un drainage chirurgical. Des images d’épidurite et de réaction inflammatoire paravertébrale sont fréquemment visualisées en IRM dans les spondylodiscites. Les abcès ne sont pas associés à un risque accru d’évolution défavorable ou de complications neurologiques [54, 55]. Ils régressent rapidement (un mois) sous antibiotiques [55]. Un abcès épidural primitif sans spondylodiscite est de plus mauvais pronostic [55], mais peut également évoluer favorablement sous antibiotiques [56]. Les caractéristiques des images d’IRM en T1 après injection de gadolinium peuvent fournir une aide à la décision de drainage [57]. Si le rehaussement est homogène (cas le plus fréquent), il s’agit d’un phlegmon (tissu inflammatoire contenant de multiples microabcès) ; si le rehaussement est
35
périphérique autour d’une zone centrale en hyposignal T1 et en hypersignal T2, il s’agit d’une réaction œdémateuse autour d’une collection abcédée pouvant nécessiter un drainage.
2-2-3 Immobilisation :
Le repos strict au lit sous-couvert d’une injection d’HBPM (héparines de bas poids moléculaire) doit être maintenu pendant trois à quatre semaines (si la CRP est normalisée) [55].
Le lever est effectué avec une contention (ceinture lombaire, corset ou minerve) qui sera portée pendant un à trois mois [55]. Pour les spondylodiscites comprises entre D4 et D9, le recours au corset ne sera pas systématique en raison du corset naturel formé par le gril costal.
2-2-4 Traitement chirurgical :
Le traitement chirurgical des spondylodiscites est devenu exceptionnel. Il doit se discuter en cas de déficit moteur (décompression radiculaire ou médullaire) en cas de syndrome de la queue-de-cheval, en cas de matériel étranger (arthrodèse) [39], de séquestre osseux et à distance de l’infection pour corriger une instabilité, une cyphose et/ou une scoliose. Les paraplégies complètes doivent bénéficier d’une décompression chirurgicale en urgence [38,
45]. Les parésies peuvent régresser sous traitements antibiotiques. 2-2-5 Eléments de la surveillance :
Radiographies
Des radiographies de face et de profil centrées sur le disque infecté sont systématiquement demandées à un et trois mois après le début des antibiotiques et à trois mois après la fin des antibiotiques. La progression des lésions
36
radiologiques à un mois est la règle liée au retard radiographique et ne doit pas remettre en cause l’antibiothérapie. Les clichés à un mois permettent d’apprécier l’étendue des lésions et servent de référence pour le suivi évolutif. À trois mois d’antibiothérapie, on doit voir les premiers signes de reconstruction osseuse (condensation des plateaux vertébraux et ostéophyte).
IRM
Une IRM de contrôle est le plus souvent inutile si l’évolution clinique et biologique est favorable [55]. Les anomalies de signal en IRM se modifient en effet plusieurs mois après la guérison [39]. S’il y avait initialement un abcès collecté, ou si l’évolution est défavorable, ou si le germe n’a pas été identifié malgré des hémocultures et deux ponctions biopsie discale, une IRM de contrôle peut être demandée après un mois de traitement pour voir s’il y a régression des images d’épidurite ou de réaction inflammatoire paravertébrale ou d’abcès [55]. L’absence de régression de ces images doit amener à reconsidérer le traitement.
37
P
P
A
A
R
R
T
T
I
I
E
E
I
I
I
I
I
I
:
:
E
38
MATERIELS
ET
39
1- Lieu et durée de l’étude :
Il s’agit d’une étude rétrospective réalisée à partir des données des Laboratoires de Microbiologie et d’Anatomie Pathologique de l’Hôpital Universitaire Cheikh Zaid. Cette étude a concernée 34 cas de spondylodiscites spontanées colligées, au cours d’une période de 3 ans (de juin 2005 à juillet 2008).
2- Les échantillons analysés :
Les prélèvements ont été réalisés par ponction biopsie discovertébrale scanno-guidée chez les Patients consultants ou hospitalisés.
La ponction biopsie scanno-guidée permet de faire deux types de prélèvements ; l’un est envoyé au laboratoire d’anatomie pathologique et l’autre est adressé au laboratoire de bactériologie pour une étude cytobactériologique et recherche de BK.
3- Etude bactériologique :
Les prélèvements adressés pour étude bactériologique et recherche BK arrivent dans des flacons stériles sous forme de biopsie.
3-1 Examen direct :
Tous les prélèvements ont été broyés avant la coloration.
3-1-1 Coloration de Gram :
Permet de connaître la morphologie, mode de groupement et classement des bactéries en cocci et bacilles Gram+ ou Gram- .
40
3-1-2 Coloration au bleu de méthylène :
Permet de donner des renseignements sur la morphologie, mode de groupement et évaluation de la réaction cellulaire.
3-1-3 Coloration de Ziehl – Neelsen :
Permet de mettre en évidence la présence de bacilles acido-alcoolo-résistant (BAAR).
3-2) Culture :
La culture permet l’isolement des bactéries.
Dans notre étude, la technique de culture utilisée pour chaque échantillon de pus ou de biopsie a été celle de l’anse calibrée : 10 microlitre est ensemencé sur les milieux suivants :
- BHI (Brain Heart Infusion) d’enrichissement qui doit être conservé pendant 7jours ;
- Mac Conkey : un milieu sélectif pour entérobactérie ; - Sabouraud : un milieu sélectif pour culture des mycoses ;
- Gélose au sang (G.S) : un milieu enrichie pour la culture des bactéries non spécifiques.
L’incubation des milieux de culture se fait à 37°C pendant 48 heures. Sauf G.S est incubé sous CO2 à 37°C pendant 48 heures.
La culture de BK se fait sur le milieu Lowenstein Jensen et l’incubation se fait à 37°C pendant 7 semaines environ.
41
4-Etude anatomopathologique : 4-1 Nature de prélèvement :
Il s’agit d’une carotte ou fragment osseux fixés au formol 10%.
4-2 Traitement :
Si le prélèvement contient de l’os, il doit être décalcifié à l’aide de l’acide nitrique. Après il va être traité comme les tissus mous.
4-2-1 Traitement proprement dite :
D’abord la carotte ou fragment est fixée au formol 10% puis traitée dans l’appareil de circulation « HISTOKINETTE » ; premièrement dans l’alcool à différentes concentrations allant de moins concentré vers le plus concentré (70° - 95° - 100°) pour la déshydrater, ensuite dans la toluène pour l’éclaircir et enfin dans la paraffine pour l’enrober. Le fragment paraffiné doit être chauffé dans l’étuve pendant 20 min et coupé à l’aide d’un microtone à des coupes de l’ordre 3 à 4 micromètres. Les lames obtenues sont d’abord réhydratées dans l’alcool à des concentrations décroissantes (100°-95°-70°) ensuite dans l’eau et puis colorées par la méthode H.E.S (Hématoxylène Erythrosine Safran). Après le montage à l’enkitte, la lecture est faite au microscope à différents objectifs.
5) Méthode statistique :
Tous les résultats ont été saisis et exploités à l’aide du programme Microsoft Office Excel 2007.
42
43
Au cours de la période d’étude, Trente quatre prélèvements ont bénéficié d’un examen bactériologique. Vingt neuf de ces échantillons ont été également analysés en subit un examen anatomopathologique.
1-Caractéristiques démographiques et anatomiques : 1-1 Distribution des spondylodiscites selon le sexe
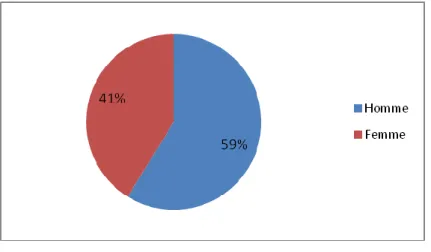
Il s’agissait de 20 hommes et 14 femmes soit respectivement 41% et 59% (figure 1).
Le sexe ratio H/F a été de l’ordre de 1,43.
Figure 3 : Pourcentage des patients
1-2 Distribution des spondylodiscites selon l’âge
La moyenne d’âge a été estimée à 56,58 ± 15,35 ans avec deux extrêmes 22 et 87 ans.
44
1-3 Distribution des spondylodiscites selon le siège de la lésion :
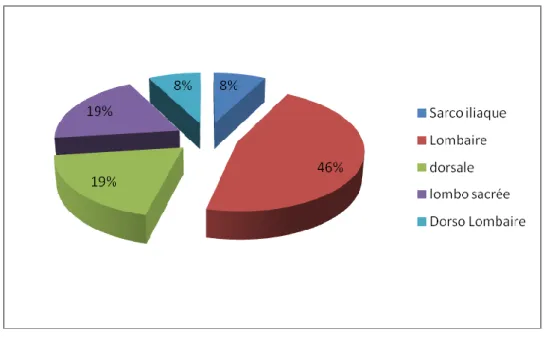
Tous les étages de la colonne vertébrale ont été concernés à l’exception du rachis cervical et du coccyx.
Dans notre étude le rachis le plus touché a été le rachis lombaire avec 46%, suivi par le rachis dorsal et le rachis lombo-sacré avec 19% et enfin on arrive au rachis sacro-iliaque et dorso-lombaire avec 8% (figure 4).
45
2-Resultats de l’examen bactériologique direct et culture :
Sur les trente quatre cas des spondylodiscites étudiées ; 12 cas ont été positifs à l’examen direct et/ou à la culture soit 35% :
- 4 cas sur 12 ont été positifs uniquement à l’examen direct ;
- 3 cas sur 12 ont été positifs à la fois à l’examen direct et à la culture ; - 5 cas sur 12 ont été positifs à la culture.
22 cas sur 34 ont été négatifs à la fois à l’examen direct et culture.
3- Distribution des spondylodiscites selon la nature des germes :
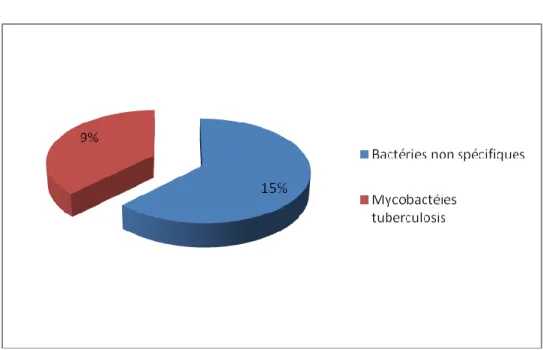
La culture a permis l’isolement d’une bactérie chez 8 cas sur 34 soit 23,5% :
- Les bactéries non spécifiques représentaient 5 cas sur 34 soit 15% ; - Les Mycobacterium tuberculosis répresentaient 3 cas sur 34 soit 9%. Les bactéries non spécifiques ont été représentés par : Staphylococcus
aureus, E. Coli, Acinetobacter, Klebsiella, Clostridium perfringens, Entérocoque comme l’indique le tableau ci-dessous :
Tableau 4 : Pourcentage des bactéries non spécifiques
Les bactéries spécifiques étaient répresentés uniquement par le
Mycobacterium teberculosis.
Staphylococcus aureus 2 40%
BGN 2 40%
Clostridium.perfringens 1 20%
46
Figure 5 : Pourcentage des bactéries non spécifiques et Mycobacterium tuberculosis
47
4- Résultats des examens anatomopathologiques :
Sur les trente quatre cas de spondylodiscites étudiés en bactériologie ; vignt neuf ont été également analysés par l’examen anatomopathologique.
Huit cas sur vignt neuf ont été déterminés comme une atteinte tuberculose, soit 27,6%.
Dans trois cas parmi 8 cas positifs à l’examen anatomopathologique, la culture a permis l’isolement de la Mycobacterium tuberculosis.
5- La Sensibilité et Spécificité de l’examen bactériologique direct par rapport à la culture.
La sensibilité de l’examen bactériologique direct par rapport à la culture était de 37,5 % et la spécificité de 84,6% avec une valeur prédictive positive de 43% et une valeur prédictive négative de 81,5%.
L’indice de Youden de l’examen bactériologique direct par rapport à la culture était de 0,22 avec une LR+ de 2,44 et LR- de 0,74.
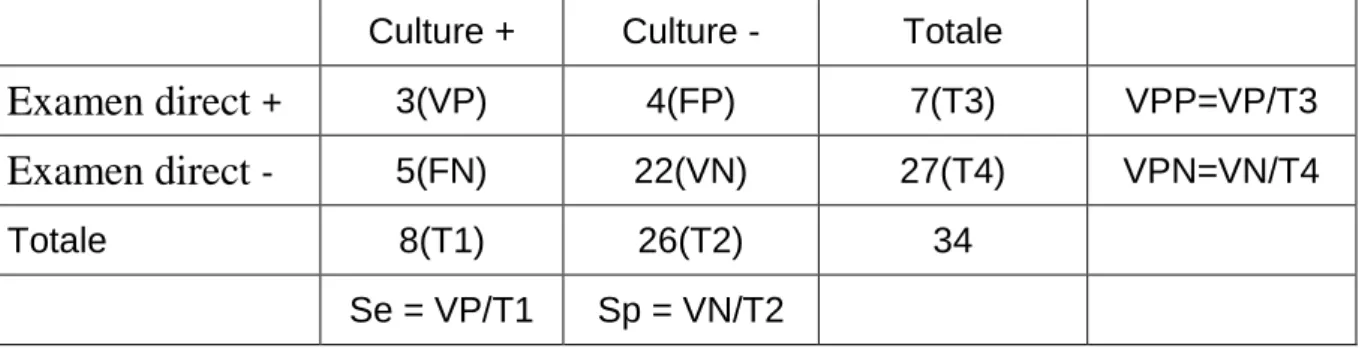
Tableau 5 : Distribution des SDS selon l’examen bactériologique direct et la
culture
Culture + Culture - Totale
Examen direct + 3(VP) 4(FP) 7(T3) VPP=VP/T3
Examen direct - 5(FN) 22(VN) 27(T4) VPN=VN/T4 Totale 8(T1) 26(T2) 34
48
Calculs : [58]
Sensibilité(Se) = Vrais Positifs/Vrais Positifs+Faux Négatifs = 3/8 = 37,5% Spécificité(Sp) = Vrais Négatifs/Vrais Négatifs+Faux Positifs = 22/26 = 84,6% Valeur prédictive positive(VPP) = Vrais Positifs/Vrais Positifs+Faux Positifs = 3/7 = 43%
Valeur prédictive négative(VPN) = Vrais Négatifs/Vrais Négatifs+ Faux Négatifs = 22/27 = 81,5%
Indice de Youden = Sensibilité + Spécificité – 1= 0,375 + 0,846 – 1 = 0,22 Likelihood ratio positive = Sensibilité/1-Spécificité = 0,375/1-0,846 = 2,44 Likelihood ratio négative = 1-Sensibilité/Spécificité = 1-0,375/0,846 = 0,74
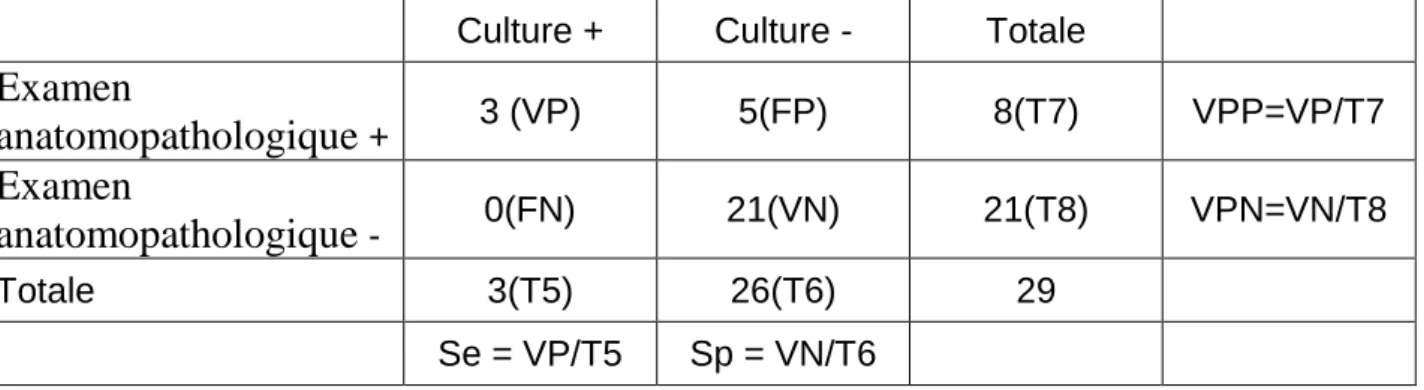
6- La Sensibilité et la Spécificité de l’examen anatomopathologique par rapport à la culture.
Dans le diagnostic des SDT l’examen anatomo-pathologique avait une sensibilité de 100% et une spécificité de 80,7% avec une valeur prédictive positive 37,5% et une valeur prédictive négative 100%.
L’examen anatomopathologique avait aussi une indice de Youden de 0,84 avec LR+ de 5,18 et LR- de 0.
Tableau 6 : Distribution des SDT selon l’examen anatomopathologique et la
culture
Culture + Culture - Totale
Examen anatomopathologique + 3 (VP) 5(FP) 8(T7) VPP=VP/T7 Examen anatomopathologique - 0(FN) 21(VN) 21(T8) VPN=VN/T8 Totale 3(T5) 26(T6) 29 Se = VP/T5 Sp = VN/T6
49 On applique les mêmes relations :[58] Sensibilité(Se) : VP/T5 = 100%
Spécificité(Sp) : VN/T6 = 80,7%
Valeur prédictive positive(VPP) = VP/T7 = 37,5% Valeur prédictive négative(VPN) = VN/T8 = 100% Indice de Youden = 0,81
Likelihood ratio positive = 5,18 Likelihood ratio négative = 0
L’efficience diagnostique de la technique ou l’exactitude de la technique c'est-à-dire le pourcentage de résultats où un diagnostic positif ou négatif correct a été posé, rapporté au nombre de biopsies effectuées est calculée : (VP + VN)/ (Nombre de biopsies) × 100 %.
50
51
Notre étude a porté sur 34 cas de spondylodiscites colligés en 3 ans. Certes cet effectif reste faible, cependant vu l’incidence de cette affection, ainsi que les difficultés de diagnostiques rencontrés, notre série restait comparable à certaines séries rapportées par d’autres auteurs ainsi Rivero et al, en Espagne, rapportaient 30 cas en 11 ans ; de Kappaler et al. 41cas [1, 20, 21].
Concernant les données démographiques, dans notre série la moyenne d’âge a été de (55,85± 15,35) ans. Cette moyenne a été supérieure à celle rapportée par certains auteurs : 41,9 ans pour BARRIERE V et coll., 43ans pour Cortet et coll. et 48 ans pour LOEMBE et al. En revanche nos résultats restaient inférieur à d’autres données ainsi Cissé, Friedman et al., et Cusmano et al., rapportaient dans leurs séries un moyen d’âge plus élevé respectivement 69,7ans, 69ans et 64ans [59, 60, 61, 62, 63].
Pour le sexe ratio, notre étude a regroupée 14 femmes et 20 hommes soit un sexe ratio d’H/F de 1,43. Cette prédominance masculine ressortie dans notre étude a été retrouvée dans d’autres études [64, 65].
Pour ce qui était de localisation de la lésion sur le rachis dans notre étude l’atteinte lombaire occupait la première place avec 46% des cas. Nos résultats étaient similaires aux données rapportées par d’autres auteurs : ainsi Narvàez et coll. et KEITA, rapportaient successivement une fréquence de 44% et 46% de localisations lombaires, cependant dans d’autres études, cette localisation ne représentait que 22 à 30%. [66, 67,65].
Dans la littérature, plusieurs auteurs s’accordaient sur la prédominance de la localisation lombaire dans le mal de Pott [68, 64].
La deuxième localisation était le rachis dorsal, elles représentaient 19 % dans notre série et 17 à 40 % dans la littérature [64].
52
M. KANE et coll., notaient une répartition égale entre le rachis dorsal et lombaire, à 50 % sur 10 cas de mal de Pott [69].
La localisation lombo-sacrée représentait 19 % dans notre série. Elle variait de 4 à 7 % dans la littérature [67]. Ce taux s’expliquait probablement par le nombre important d’atteinte lombaire, le retard de diagnostic et la chronicité des lésions qui s’étendaient de proche en proche.
L’atteinte dorso-lombaire était représentée dans 8% dans notre série et variait de 3 à 22 % dans la littérature [67]. Enfin l’atteinte sacro-iliaque a été retrouvée dans 8% dans notre série.
L’atteinte était mono-étagée dans notre étude dans 65 % des cas, et multi-étagée dans 35 % des cas. KADIRI et coll. ont trouvé une atteinte mono-multi-étagée dans 80,3 % des cas, et multi-étagée dans 19,7 % des cas [70]. Dans la littérature, l’atteinte mono-étagée était la plus fréquente, et l’atteinte multi-étagée était de fréquence variable [67].
Ces différents types de localisations peuvent être expliqués par les différentes modes de contaminations qui étaient la contamination hématogène qui représentait 60 à 80%, qui était plus fréquente surtout chez l’enfant du fait de la bonne vascularisation des disques alors qu’elle était plus rare chez l’adulte. Dans notre étude tous les patients ont été des adultes.
Le deuxième mode était l’inoculation directe dont la fréquence croissante des portes d’entrée iatrogènes, peut être responsable de 13 à 40%. La fréquence de ces ports d’entrée était très variable d’une série à l’autre : moins de 5% dans les séries françaises, elle atteinait 13% dans l’étude épidémiologique danoise
[71]. Et elles représentaient 33% dans la série de Carragee et al. [72]. Ces
53
ou moins systématique d’une antibioprophylaxie. Les portes d’entrée iatrogènes étaient très diverses : angiographie ; cathéter veineuse ; chirurgie viscérale, cardiaque, vasculaire, orthopédique ; extraction dentaire, geste urinaire …
D’où vient l’intérêt de rechercher avec soin dans les semaines et les mois précédents une intervention chirurgicale, instrumentale ou endoscopique pour la mise éventuel d’une localisation de spondylodiscite infectieuse.
Le troisième mode était l’inoculation par contiguïté à partir d’une infection de voisinage (abcès adjacent ou une greffe aortique infectée), dont la fréquence a été retrouvée dans 3%.
Concernant les résultats de l’examen direct et culture :
La culture est l’examen microbiologique de référence pour le diagnostic biologique des spondylodiscites [27].
Dans notre étude, l’examen direct et/ou culture ont été positifs dans 35% des cas.
Cependant, la culture a permis l’isolement d’une bactérie dans 8 cas sur 34 soit 23,5 % de total des prélèvements analysés. Notre taux restait proche de celui qui elle a rapporté par Seven et al. (27%), mais inférieur aux données qui ont été trouvées par Legrand et al: 40% [73,74]. Et aussi aux données de la littérature dont la ponction biopsie discovertébrale a permis d’identifier le germe en cause dans 50 à 70%. Mais il faut noter que dans notre étude au moins deux prélèvements qui ont été positifs à l’examen direct, mais la culture a été négative, chez des patients connus sous traitement antibiotiques. Ceci était comparable avec F. Brenac et al. Qui rapportaient que 6/210 prélèvements ont été négatifs à la culture chez des patients sous antibiotiques [75].
![Figure 1 : Arbre décisionnel d’imagerie pour diagnostic de SDI [27]](https://thumb-eu.123doks.com/thumbv2/123doknet/15051902.695442/22.892.118.782.142.929/figure-arbre-décisionnel-imagerie-diagnostic-sdi.webp)
![Figure 2 : Diagnostic microbiologique et arbre décisionnel thérapeutique au cours de SDI [27]](https://thumb-eu.123doks.com/thumbv2/123doknet/15051902.695442/25.892.110.788.138.782/figure-diagnostic-microbiologique-arbre-décisionnel-thérapeutique-cours-sdi.webp)

![Tableau 2 : Proposition d’antibiothérapie selon le germe pour le traitement des spondylodiscites [50]](https://thumb-eu.123doks.com/thumbv2/123doknet/15051902.695442/31.892.70.828.189.683/tableau-proposition-antibiothérapie-germe-traitement-spondylodiscites.webp)
![Tableau 3 : Proposition de posologie des antibiotiques pour le traitement des spondylodiscites pour un adulte à fonction rénale normale [50]](https://thumb-eu.123doks.com/thumbv2/123doknet/15051902.695442/33.892.80.778.182.851/tableau-proposition-posologie-antibiotiques-traitement-spondylodiscites-fonction-rénale.webp)