2005
Aucune section de la présente publication ne peut être reproduite ni transmise sous quelque forme que ce soit, ni par quelque procédé électronique ou mécanique que ce soit, y compris des photocopies, les enregistrements ou par tout autre moyen de stockaged’information et de recherche documentaire, qui existe ou non à l’heure actuelle, sans le consentement écrit de l’auteur qui en possède les droits. Ne sont cependant pas soumises à cette règle les personnes désirant citer de brefs passages pour une publication dans une revue, un journal ou encore pour une émission radiodiffusée ou télédiffusée.
Les demandes d’autorisation doivent être acheminées à :
Institut canadien d’information sur la santé 495, chemin Richmond,
Bureau 600 Ottawa (Ontario) K2A 4H6
Téléphone : (613) 241-7860 Télécopieur : (613) 241-8120 www.icis.ca
ISBN 1-55392-755-9 (PDF)
© 2005 Institut canadien d’information sur la santé
This publication is also available in English under the title:
Medical Imaging in Canada 2005
ISBN 1-55392-754-0 (PDF)
L’Institut canadien d’information sur la santé souhaite remercier les nombreux organismes et collaborateurs qui ont contribué à l’élaboration du présent rapport.
L’ICIS est responsable de l’Enquête nationale sur divers équipements d’imagerie médicale et des renseignements qui figurent dans le présent rapport. Le travail du personnel dévoué de la Division des dépenses de santé, dont Melissa Aggerwal, Ruolz Ariste, Geoff Ballinger, Ian Button, Gilles Fortin, Louise Ogilvie et Greg Zinck, était essentiel dans la compilation, l’analyse et la diffusion de l’information du rapport.
L’ICIS aimerait remercier les membres de ProMed Associates Ltd., particulièrement Ron Wood et Brian Lentle pour la révision du premier chapitre. Il souhaite également remercier l’ancien Comité consultatif sur les technologies d’information et les nouvelles technologies, qui était composé de représentants fédéraux, provinciaux et territoriaux, pour leur appui dans l’obtention et la validation des aspects des données figurant dans le rapport.
La production de ce rapport met à contribution beaucoup d’employés et de services de l’ICIS, dont des membres des publications, du contenu Web, de la traduction, des services de distribution, des communications et des ressources humaines de la santé.
Le présent rapport n’aurait pu voir le jour sans le généreux appui et l’aide de bien d’autres
personnes et organismes, y compris les nombreux hôpitaux et les établissements qui ont
répondu à l’Enquête nationale sur divers équipements d’imagerie médicale au Canada.
Points saillants
L’imagerie médicale dans la pratique — Évolution de la technologie et nouvelles applications
Le présent chapitre porte sur les derniers développements relatifs à l’évolution des appareils d’imagerie diagnostique.
!
La tomographie d’émission de positons couplée à la tomodensitométrie (TEP-TDM), une nouvelle technologie hybride qui produit des coupes à la fois de la fonction et de la structure, a fait son entrée au Canada. Elle pourrait bien remplacer sous peu les images diagnostiques des appareils conventionnels de médecine nucléaire.
!
L’Enquête nationale sur divers équipements d’imagerie médicale, 2005 étudie six types d’équipements de pointe en imagerie médicale dont au moins un équipement est
disponible dans seulement un tiers des hôpitaux et des établissements autonomes d’imagerie du Canada. Ces équipements sont les appareils d’IRM, les appareils de TDM, les caméras nucléaires, les laboratoires de cathétérisme cardiaque, les angiographes et les caméras à positons.
!
Environ 60 % des hôpitaux qui ont répondu au sondage font parvenir des images médicales numériques soit au système d’archivage et de transmission d’images (ou PACS) pour qu’un service puisse les regarder, soit aux services concernés de l’établissement. Toutefois, cette proportion ne représente qu’environ 20 % de tous les sites hospitaliers au Canada.
Technologies d’imagerie — Nombre et coût
Le présent chapitre donne un aperçu du nombre et de la répartition des appareils d’imagerie et de certains facteurs qui jouent un rôle dans la disponibilité des technologies d’imagerie au Canada et dans le monde.
!
Les appareils de TDM et d’IRM ont connu une hausse considérable depuis leur arrivée (en 1973 et 1982 respectivement). Entre 1990 et 2005, le nombre de
tomodensitomètres a augmenté de 163 appareils (82 %), tandis que le nombre d’appareils d’IRM a augmenté de 157 (826 %). Depuis 1997, on a installé un plus grand nombre d’appareils d’IRM que de TDM.
!
En date du 1
erjanvier 2005, on comptait seulement un appareil d’IRM contre
2,1 tomodensitomètres au Canada. Terre-Neuve-et-Labrador affichait le ratio le plus faible d’appareils d’IRM par rapport à ceux de TDM (1:10,0) et l’Alberta, le plus élevé avec un appareil d’IRM contre 1,2 tomodensitomètre.
!
De 1990 à 2001, la croissance du nombre d’appareils d’IRM au Canada était semblable
à celle de la France et de l’Allemagne. La hausse du nombre de tomodensitomètres en
Italie a été plus rapide qu’au Canada, qu’en Allemagne et qu’en France.
de TDM dans les établissements autonomes d’imagerie a augmenté jusqu’en 2004 pour se stabiliser en 2005. En janvier 2005, environ 3 % des appareils de TMD et 15 % des appareils d’IRM étaient dans des établissements autonomes d’imagerie.
!
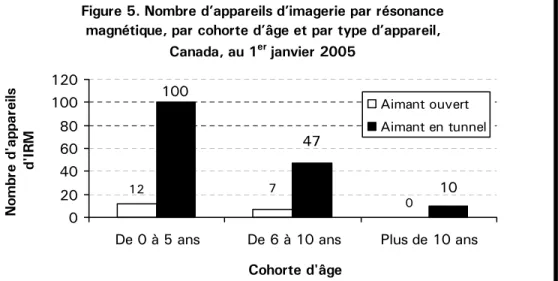
Bien qu’on ait installé davantage de tomodensitomètres que d’appareils d’IRM en 2005, la proportion d’appareils de TDM et d’IRM installés au cours des cinq dernières années a baissé par rapport à la proportion d’appareils de TDM et d’IRM installés il y a six à dix ans. Cette baisse est le résultat du vieillissement des appareils qui passent de la tranche des appareils de 0 à 5 ans en 2004 à celle de 6 à 10 ans en 2005, augmentant ainsi la proportion de la dernière cohorte d’âge.
!
En 2004, le Canada comptait 1 967 spécialistes en radiodiagnostic, soit une hausse de 3,0 % par rapport à l’an dernier.
Utilisation des services d’imagerie médicale
Le présent chapitre inclut une analyse des statistiques d’utilisation des appareils d’imagerie médicale (nombre d’examens et d’heures d’exploitation) au Canada et dans certains pays.
!
Dans l’ensemble, les provinces et les territoires qui comptaient moins d’appareils par million d’habitants en 2004-2005 affichaient de plus longues heures d’utilisation par semaine que les provinces et territoires qui comptaient un plus grand nombre
d’appareils par million d’habitants.
!
Bien qu’il y ait davantage d’appareils d’IRM et de TDM par million d’habitants aux
États-Unis, les appareils disponibles au Canada ont connu une utilisation plus intensive. Le nombre d’examens par IRM et par TDM par appareil en 2004-2005 était respectivement 37 % et 46 % plus élevé au Canada qu’aux États-Unis. Aussi, le Canada affichait environ un tiers d’examens par appareil d’IRM de plus que l’Angleterre.
!
En 2004-2005, le nombre d’examens par appareil d’IRM par 1 000 habitants variait à l’échelle nationale, l’Alberta affichant un taux plus de quatre fois supérieur à celui de Terre-Neuve-et-Labrador (36,6 et 8,5 respectivement). Le nombre moyen d’examens par IRM s’élevait à 25,5 par 1 000 habitants au Canada, contre 83,2 aux États-Unis et 19,0 en Angleterre.
!
Le nombre d’examens par TDM par 1 000 habitants en 2004-2005 n’a pas varié autant
que celui des examens par IRM. Il passait de 78,2 examens en Colombie-Britannique à
134,8 au Nouveau-Brunswick. La moyenne canadienne était de 87,4 examens, contre
172,5 aux États-Unis et 43,0 en Angleterre.
L’imagerie médicale au Canada, 2005 Table des matières
Remerciements... iii
Points saillants ...iv
Au sujet du présent rapport... 1
Quoi de neuf?... 2
Chapitre 1 L’imagerie dans la pratique — Évolution de la technologie et nouvelles applications ... 5
Le bon outil pour effectuer le bon travail ... 6
L’imagerie médicale dans le diagnostic de la coronaropathie ... 14
Tomodensitométrie ... 19
Imagerie par résonance magnétique (IRM) ... 26
Tomographie par émission de positons (TEP) et TEP-TDM ... 33
Systèmes PACS (Picture Archiving and Communications Systems)... 37
Références... 43
Chapitre 2 Technologies d’imagerie — Nombre et coût ... 55
Combien y a-t-il d’appareils?... 55
L’offre d’appareils d’imagerie au Canada ... 58
Le contexte international... 60
Où se trouvent les appareils d’imagerie ... 65
Vieillissement et renouvellement des appareils d’imagerie médicale... 66
Les coûts relatifs à l’imagerie ... 67
Références... 75
Chapitre 3 Utilisation des services d’imagerie ... 77
Nombre d’examens d’IRM et de TDM par province et territoire... 77
Exploite-t-on les appareils d’imagerie médicale de façon intensive? ... 80
Facteurs susceptibles de limiter l’accès aux examens d’IRM et de TDM ... 88
Références... 97
Annexe A — Les faits en bref... A–1
Annexe B — Notes méthodologiques... B–1
L’imagerie médicale au Canada, 2005 Liste des figures
Figure 1. Répartition en pourcentage des examens d’imagerie diagnostique dans les hôpitaux, Nouvelle-Écosse, Ontario et Colombie-Britannique, 2003-2004 ... 6 Figure 2. Nombre de tomodensitomètres, par cohorte d’âge et par type d’appareil,
Canada, au 1
erjanvier 2005 ... 20 Figure 3. Nombre d’appareils de TDM spiralée, par coupe, Canada, au
1
erjanvier 2005... 21 Figure 4. Nombre de tomodensitogrammes dans les services d’urgence, par partie
anatomique, Ontario, 2003-2004... 23 Figure 5. Nombre d’appareils d’imagerie par résonance magnétique, par cohorte
d’âge et par type d’appareil, Canada, au 1
erjanvier 2005... 27 Figure 6. Nombre d’appareils d’imagerie par résonance magnétique et force de champ,
par cohorte d’âge, aimant en tunnel, Canada, au 1
erjanvier 2005 ... 29 Figure 7. Nombre d’appareils d’imagerie magnétique et force de champ, par cohorte
d’âge, aimant ouvert, Canada, au 1
erjanvier 2005 ... 29 Figure 8. Nombre d’examen d’IRM en consultation externe, par partie anatomique,
Ontario, de 1993-1994 à 2003-2004... 30 Figure 9. Répartition des examens d’IRM en consultation externe, par type d’examen,
Ontario, 1993-1994 et 2003-2004... 31 Figure 10. Croissance du taux d’utilisation des examens radiologiques de la colonne
vertébrale, Ontario, de 1992 à 2001 ... 32 Figure 11. Nombre de caméras à positons, par type d’examen et cohorte d’âge,
Canada, au 1
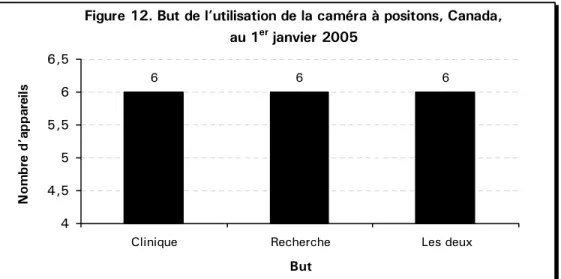
erjanvier 2005 ... 34 Figure 12. But de l’utilisation de la caméra à positons, Canada, au 1
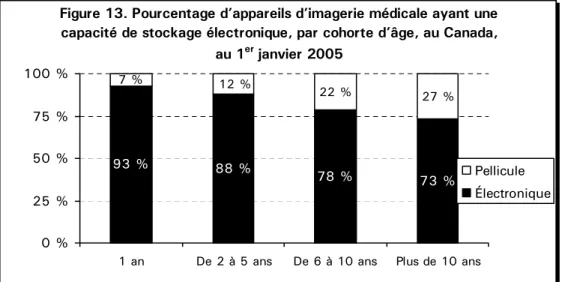
erjanvier 2005 ... 35 Figure 13. Pourcentage d’appareils d’imagerie médicale ayant une capacité de stockage
électronique, par cohorte d’âge, au Canada, au 1
erjanvier 2005 ... 40 Figure 14. Pourcentage d’appareils d’imagerie médicale reliés à un système PACS, par
type d’appareil, au 1
erjanvier 2004 et 2005 ... 42 Figure 15. Nombre d’appareils d’imagerie par résonance magnétique (IRM) et de
tomodensitométrie (TDM), Canada, de 1983 à 2005... 57 Figure 16. Nombre d’appareils d’imagerie médicale choisis par million d’habitants, au
Canada, au 1
erjanvier, de 2003 à 2005... 58 Figure 17. Nombre de tomodensitomètres par million d’habitants dans des pays
choisis de l’OCDE d’un million d’habitants ou plus et année de déclaration
des taux ... 61
L’imagerie médicale au Canada, 2005 Liste des figures (suite)
Figure 18. Nombre d’appareils d’IRM par million d’habitants dans des pays choisis de l’OCDE d’un million d’habitants ou plus et année de déclaration des taux... 62 Figure 19. Nombre de tomodensitomètres par million d’habitants dans des pays
choisis du G8 dont les données chronologiques étaient disponibles,
de 1990 à 2005... 63 Figure 20. Nombre d’appareils d’IRM par million d’habitants dans des pays choisis
du G8 dont les données chronologiques étaient disponibles,
de 1990 à 2005 ... 64 Figure 21. Nombre d’appareils d’IRM et de TDM dans les établissements autonomes
d’imagerie, au Canada, de 1998 à 2005 ... 65 Figure 22. Répartition d’appareils d’imagerie médicale choisis, par cohorte d’âge depuis
l’installation, par année d’enquête, au Canada ... 66 Figure 23. Répartition des frais d’exploitation liés aux services d’imagerie diagnostique
dans les hôpitaux canadiens, 2003-2004... 67 Figure 24. Dépenses totales d’exploitation des hôpitaux concernant certains types
d’imagerie médicale, en Ontario, 1999-2000 et 2003-2004 ... 70 Figure 25. Répartition des dépenses d’exploitation des hôpitaux concernant certains
types d’imagerie médicale, en Ontario, 2003-2004 ... 70 Figure 26. Total des dépenses en immobilisations (construction, matériel et équipement
dans les établissements hospitaliers, cliniques, de premiers secours et pour bénéficiaires internes), par payeurs des secteurs public et privé, au Canada, de 1990 à 2005 ... 71 Figure 27. Nombre d’examens d’IRM par 1 000 habitants, par province et territoire et
au Canada, 2003-2004 et 2004-2005 ... 79 Figure 28. Nombre d’examens de TDM par 1 000 habitants, par province et territoire
et au Canada, 2003-2004 et 2004-2005... 79 Figure 29. Nombre moyen d’examens d’IRM par appareil et par année, par province et
territoire et au Canada, 2003-2004 et 2004-2005 ... 81 Figure 30. Nombre moyen d’examens de TDM par appareil et par année, par province
et territoire et au Canada, 2003-2004 et 2004-2005 ... 82 Figure 31. Nombre moyen d’heures d’exploitation par semaine, appareils
d’imagerie médicale choisis, au Canada, 2003-2004 et 2004-2005 ... 83 Figure 32. Nombre moyen d’heures d’exploitation par semaine, appareils d’IRM,
par province et territoire et au Canada, 2003-2004 et 2004-2005 ... 84
L’imagerie médicale au Canada, 2005 Liste des figures (suite)
Figure 33. Nombre moyen d’heures d’exploitation par semaine, tomodensitomètres,
par province et territoire et au Canada, 2003-2004 et 2004-2005 ... 84 Figure 34. Nombre d’examens d’IRM et de TDM par technologue ETP,
Nouveau-Brunswick et Ontario, 2003-2004 ... 85 Figure 35. Nombre de professionnels d’imagerie médicale choisis, au Canada, 2004... 91 Figure 36. Pourcentage de technologues en radiation médicale, à temps plein et à
temps partiel, au Canada, de 2001 à 2004 ... 93 Figure 37. Nombre total de spécialistes en radiodiagnostic partis à l’étranger ou revenus
de l’étranger, au Canada, de 1991 à 2004... 94
Liste des tableaux à but spécifique
Tableau 1. Quel examen? ... 18 Tableau 2. Taux et nombre d’appareils d’imagerie choisis par million d’habitants, par
province et territoire et au Canada, au 1
erjanvier 2005... 59 Tableau 3. Nombre d’appareils d’IRM par rapport à ceux de TDM dans les hôpitaux
et les établissements autonomes d’imagerie, par province et territoire et au Canada, au 1
erjanvier 2005 ... 60 Tableau 4. Répartition en pourcentage des recettes d’exploitation par source de
financement des appareils d’imagerie médicale, et nombre total d’appareils installés dans les hôpitaux et les établissements autonomes d’imagerie, au Canada, au 1
erjanvier 2005. ... 69 Tableau 5. Engagements financiers du gouvernement fédéral pour l’équipement médical
selon les Accords sur la santé de 2001, 2003 et 2004... 73 Tableau 6. Nombre d’examens d’imagerie par résonance magnétique (IRM) et de
tomodensitométrie (TDM), par province et territoire et au Canada,
2003-2004 et 2004-2005 ... 78 Tableau 7. Nombre moyen d’heures d’exploitation par semaine, appareils d’imagerie
médicale choisis, par province et territoire et au Canada, 2003-2004
et 2004-2005 ... 83 Tableau 8. Nombre moyen d’examens d’IRM et de TDM par 1 000 habitants, par
appareil, par technologue ETP, et nombre moyen d’heures d’exploitation des appareils par semaine, États-Unis, Angleterre et Canada, 2004-2005 ou
dernière année... 86
Tableau 9. Règles d’évaluation des appareils médicaux... 89
Au sujet du présent rapport
Le dernier siècle a été marqué par de grands changements technologiques dans le domaine de la médecine. Il y va de même pour l’imagerie médicale. Les radiographies ont tout juste commencé à être utilisées à des fins médicales à la fin des années 1890. De nos jours, les radiologistes peuvent lire des radiographies et d’autres images diagnostiques produites à des milliers de kilomètres et transmises en quelques minutes. Les chirurgies qui exigeaient auparavant plusieurs jours d’hospitalisation sont maintenant pratiquées sans que le patient ne soit hospitalisé. Et plus de formes spécialisées d’imagerie médicale, comme la capacité de présenter des images de presque n’importe quelle structure du corps, deviennent essentielles pour fournir des soins et des traitements de nature générale et spécialisée.
Nous possédons peu de renseignements sur l’utilisation réelle de ces technologies au Canada. Le présent rapport cherche à combler cette lacune. Il se veut une référence consolidée de ce que nous savons des technologies d’imagerie médicale au Canada et un outil servant à éclairer les décisions à mesure que nous allons de l’avant. Nous nous penchons particulièrement sur le nombre de différents appareils au Canada et sur la façon dont ils sont utilisés ainsi que sur les professionnels de la santé qualifiés qui les font fonctionner et qui interprètent les résultats. En règle générale, le rapport traite principalement de certaines technologies d’imagerie récentes dont la base
d’information est riche. Bien des enjeux que nous présentons, toutefois, peuvent s’appliquer à l’ensemble des technologies d’imagerie.
Le rapport est divisé en trois chapitres :
Chapitre 1 : L’imagerie médicale dans la pratique — Évolution de la technologie et nouvelles applications présente d’une part l’information sur la façon dont ces technologies évoluent ainsi que sur leurs nouvelles applications et d’autre part un aperçu de l’information actuellement disponible sur les technologies d’imagerie au Canada.
Chapitre 2 : Technologies d’imagerie — Nombre et coûts donne un aperçu de l’information disponible sur le nombre d’appareils d’imagerie et où ceux-ci se trouvent au pays. Le chapitre présente également des renseignements sur les facteurs qui jouent un rôle sur le nombre d’appareils d’imagerie disponibles, y compris les coûts rattachés à leur acquisition.
Chapitre 3 : Utilisation des services d’imagerie médicale. Un plus grand nombre d’appareils ne garantit pas nécessairement que plus de gens recevront des services d’imagerie. Il se peut que les appareils soient sous-utilisés pour bon nombre de raisons, les ressources financières ou humaines limitées par exemple. L’objectif du chapitre est de présenter certaines statistiques sur l’utilisation des appareils d’imagerie médicale (le nombre d’examens et le nombre d’heures d’exploitation) par année et d’en évaluer le niveau d’intensité.
Dans la mesure du possible, le rapport dresse des comparaisons nationales et
internationales. Il inclut également la section Les faits en bref dans l’annexe A. Cette
section offre une large gamme de données comparatives sur les technologies d’imagerie médicale à l’échelle du pays.
Q U O I D E N E U F ?
Dans leur exploration de ce que nous savons et de ce que nous ignorons sur l’imagerie médicale au Canada, les auteurs du rapport L’imagerie médicale au Canada, 2005 se sont appuyés sur de nouvelles données et analyses de l’ICIS ainsi que sur des recherches provinciales, territoriales, nationales et internationales. Les lignes qui suivent fournissent des exemples de nouvelles données.
!
Nombre, âge et répartition de certains appareils d’imagerie médicale situés dans les hôpitaux et les établissements autonomes d’imagerie au Canada en date du 1er janvier 2005 et évolution de ces caractéristiques au fil du temps.
!
Utilisation de certaines technologies d’imagerie dans différents milieux.
!
Proportion des dépenses des hôpitaux de certaines provinces et certains territoires consacrée aux services d’imagerie médicale.
!
Notes méthodologiques qui fournissent des renseignements sur la méthodologie utilisée et la qualité des données.
Pour en savoir d’avantage
On peut se procurer gratuitement les points saillants et le texte intégral L’imagerie médicale au Canada, 2005 dans les deux langues officielles sur le site Internet de l’ICIS à
www.icis.ca. Pour commander d’autres exemplaires du rapport (des frais minimes s’appliquent pour compenser les coûts d’impression, de port et de manutention), veuillez communiquer avec :
Institut canadien d’information sur la santé 495, rue Richmond, bureau 600
Ottawa (Ontario) K2A 4H6
Tél. : (613) 241-7860
Téléc. : (613) 241-8120
Le Web : Une mine de renseignements
La version imprimée du présent rapport ne représente qu’une partie des renseignements figurant sur notre site Web (www.icis.ca). Le jour même de la publication du rapport L’imagerie médicale au Canada 2005 et dans les semaines et les mois à venir, nous ajouterons d’autres renseignements aux données déjà disponibles par voie électronique. Il sera possible, par exemple, de :
!
télécharger gratuitement le rapport en français et en anglais;
!
télécharger les points saillants du rapport et un index du contenu;
!
télécharger les données de l’Enquête nationale sur divers équipements d’imagerie médicale (2003, 2004 et 2005);
!
consulter les rapports annuels de l’ICIS, dont Tendances des dépenses nationales de santé, la série de rapports réguliers de l’ICIS portant sur les soins de santé au Canada, les ressources humaines de la santé, les services de santé ainsi que la santé de la population.
Nous vous invitons à nous faire part de vos commentaires et suggestions sur ce rapport et la façon d’améliorer les prochains rapports pour qu’ils soient plus utiles et instructifs.
Veuillez nous les transmettre par courriel à bdcs@icis.ca.
Chapitre 1
L’imagerie dans la pratique — Évolution de la technologie et nouvelles applications
Dans la société moderne de nos jours, la technologie est devenue un outil indispensable au quotidien. Il n’est pas surprenant de voir que l’utilisation de la technologie dans la médecine augmente et qu’elle s’améliore à un rythme effréné. Au cours du dernier siècle, les technologies de l’imagerie se sont taillé une place au sein de tout un arsenal d’outils utilisés pour déceler la maladie et la combattre. De nos jours, les cliniciens font souvent appel à des douzaines de types d’imagerie dès les premières étapes du diagnostic, avant même d’utiliser d’autres services de soins de santé ou tout simplement pour les éviter. Certaines technologies telles que les appareils à rayons X sont opérationnelles depuis plus d’un siècle. D’autres appareils,
notamment ceux de l’imagerie par résonance magnétique (IRM), de tomodensitométrie (TDM) et de tomographie par émission de positons (TEP) représentent les nouveaux arrivés d’une gamme de plus en plus sophistiquée d’appareils d’imagerie.
Selon l’Organisation mondiale de la Santé (OMS), environ 20 % à 30 % des cas de médecine dans le monde font appel à l’imagerie diagnostique, car les examens cliniques à eux seuls ne suffisent pas pour poser un diagnostic juste. Parmi les cas qui
nécessitent l’imagerie diagnostique, environ 80 % à 90 % des problèmes de diagnostics peuvent
généralement être résolus à l’aide d’examens de base, la radiographie ou l’échographie par exemple
1. Si l’on se fie aux données de la Nouvelle-Écosse, de l’Ontario et de la Colombie-Britannique, le Canada semble suivre les mêmes tendances. Les examens de base à l’aide de la radiographie ou de l’échographie représentent en tout près de 80 % de tous les tests d’imagerie médicale (sans
compter les angiographies) dans les hôpitaux des trois provinces en 2003-2004 (figure 1).
Les radiographies, y compris les mammographies, représentaient 63 % des examens et l’échographie, 16 %. Les examens de TDM, de médecine nucléaire, d’IRM et de
cathétérisme cardiaque affichaient respectivement 11 %, 7 %, 3 % et 1 % de l’ensemble des tests d’imagerie médicale.
Répartition en pourcentage des problèmes qui requièrent des services d’imagerie
diagnostique selon les estimations de l’OMS (total des problèmes = 100 %) :
Problèmes du thorax 40 % Accidents et blessures 20 % Problèmes liés à la grossesse 15 % Problèmes abdominaux 10 % Problèmes musculosquelettiques 10 %
Autres problèmes 5 %
Source : Organisation mondiale de la santé, Department of Essential Health Technologies, Essential Diagnostic Imaging (en ligne). Consulté le 26 septembre 2005.
Internet :
<http://www.who.int/eht/en/diagnosticimaging.pdf>.
Figure 1. Répartition en pourcentage des examens d’imagerie diagnostique dans les hôpitaux, Nouvelle-Écosse, Ontario et
Colombie-Britannique, 2003-2004
Tomodensi- tométrie
11 % Médecine nucléaire
7 %
Cathéterisme cardiaque
1 %
Radiographie (sans mammographie)
58 % Radiographie et
échographie 78 % IRM
3 %
Échographie 16 % Mammographie
4 %
Source : Base de données canadienne SIG, Institut canadien d'information sur la santé.
Remarque : Exclut les angiographies.
L E B O N O U T I L P O U R E F F E C T U E R L E B O N T R A V A I L
On peut avoir recours à l’imagerie médicale pour de nombreuses raisons : dépister une maladie chez les patients à risque, réduire l’incertitude sur un diagnostic afin de rassurer les patients et les dispensateurs de soins, éclairer les décisions concernant les choix à prendre en matière de soins, évaluer les traitements et les pronostics ou guider les interventions chirurgicales ou d’autres interventions
2, 3.
Il n’est pas facile de choisir le meilleur outil (ou les meilleurs outils) à utiliser dans chacun de ces contextes pour différents patients, compte tenu en particulier de l’évolution constante de la technologie d’imagerie, des résultats de recherche et des habitudes relatives à la pratique. Bien souvent, la valeur d’un type particulier d’imagerie est évidente et sans équivoque chez certains groupes de patients ou dans certains types de recherche, mais d’autres cas sont moins
évidents. Voici des exemples de facteurs qui peuvent influencer ces décisions :
!
L’efficacité technique, qui se mesure par l’efficacité d’une technique d’imagerie à représenter la structure physique de la partie du corps en question;
!
L’exactitude diagnostique, qui indique dans quelle mesure l’information relative à l’examen contribue à la détermination d’un diagnostic correct;
!
L’efficience comparative, qui permet de comparer la qualité de l’information diagnostique par rapport à d’autres méthodes (amélioration ou dégradation);
!
L’incidence thérapeutique, qui détermine le degré d’influence de l’information diagnostique sur les décisions à prendre en matière de soins;
!
Les résultats pour la santé, qui sont les effets prévus du diagnostic et du traitement sur
les résultats liés à la morbidité et la mortalité
4.
De plus, on peut tenir compte de facteurs non cliniques et d’autres facteurs lorsqu’on prend des décisions relatives à un choix d’appareils, notamment l’accès à la
technologie, le rapport coût-efficacité et les enjeux liés à la sécurité.
Les appareils récents, soit de TDM et d’IRM, sont de plus en plus utilisés pour étudier les symptômes non précis. Les facteurs sous- jacents à la hausse de l’utilisation
comprennent la demande croissante des patients pour ce genre de service, le meilleur accès aux appareils, l’inquiétude des
cliniciens de ne pas déceler une maladie curable et les préoccupations liées aux poursuites si une anomalie majeure n’est pas diagnostiquée. Il importe d’avoir des lignes directrices pour aider les cliniciens et les patients à déterminer quand l’examen par TDM ou IRM, ou toute autre intervention d’imagerie diagnostique, est indiqué.
Des progrès sont réalisés à cet égard au Canada, puisque l’Association canadienne des radiologistes rédige des directives fondées sur les preuves pour toutes les interventions d’imagerie diagnostique
8.
Bien que des millions de Canadiens reçoivent des services d’imagerie chaque année, on en sait encore relativement peu sur la façon dont ces technologies sont utilisées et touchent les soins aux patients et les résultats. On dispose toutefois de certains renseignements. Le rapport de l’an dernier, L’imagerie médicale au Canada, 2004, traite brièvement de deux modalités bien implantées pour diagnostiquer le cancer du sein et la coronaropathie : la mammographie et l’angiographie. Le présent chapitre étoffe davantage et permet
d’examiner l’utilisation des différents appareils d’imagerie (classiques ou nouveaux) pour diagnostiquer ces deux maladies. Le cancer du sein est la forme de cancer la plus souvent diagnostiquée chez les femmes canadiennes. La coronaropathie est responsable de plus de la moitié de l’ensemble des décès liés aux maladies cardiovasculaires au Canada. Le
chapitre porte ensuite sur l’évolution, depuis les toutes premières applications cliniques, des trois types d’imagerie, soit la TDM, l’IRM et la TEP (y compris la TEP-TDM), sur les caractéristiques des appareils installés au Canada et sur les nouvelles applications qui découlent des dernières percées technologiques. Finalement, le chapitre inclut une
discussion sur le système d’archivage et de transmission d’images (PACS) dans le contexte canadien. Le système PACS est un outil technologique d’information qui permet
d’enregistrer des images diagnostiques dans un endroit centralisé (le serveur du système PACS) et de les transmettre aux postes de travail reliés au serveur.
Sécurité de l’imagerie médicale
Les examens d’imagerie médicale, comme les autres interventions en santé, sont rarement sans risque. La radiographie par exemple comporte des risques associés à la radioexposition. Les technologies qui n’ont pas recours aux rayonnements ionisants peuvent comporter d’autres risques, notamment des effets
mécaniques, thermiques et biologiques
5. Pour bien des patients, les avantages possibles qu’ils peuvent retirer de
l’information obtenue à partir des examens l’emportent largement sur les risques prévisibles, y compris sur les
conséquences découlant de faux positifs ou de faux négatifs
6. Pour d’autres, il faut considérer attentivement les avantages possibles, les coûts ainsi que les risques.
Dans certains cas, il vaut mieux se fier à des approches utilisées depuis des siècles, comme observer attentivement ou tâter une articulation pour déceler une fracture.
Cet équilibre peut varier d’un examen à
l’autre, d’un endroit à l’autre, d’un patient
à un autre et au fil du temps
7.
L ’ I M A G E R I E M É D I C A L E P O U R
D I A G N O S T I Q U E R L E C A N C E R D U S E I N
Mammographie : Détecter le cancer du sein Selon l’Institut national du cancer du Canada, il y aura environ 21 600 nouveaux cas de cancer du sein et environ 5 300 décès attribuables à cette maladie chez les
Canadiennes en 2005. Ces chiffres font du cancer du sein la forme de cancer la plus souvent diagnostiquée chez les femmes, quoique le cancer du poumon soit la principale cause de décès des suites d’un cancer
9. La mammographie est une technique diagnostique courante pour dépister le cancer du sein chez les femmes asymptomatiques (c’est-à-dire les femmes qui n’ont soulevé aucune anomalie à l’égard de leurs seins, ni masse, ni douleur, ni écoulement). La mammographie classique est une radiographie des seins à faible dose de rayonnement. Il s’agit d’un système spécialement conçu pour produire des mammographies à contraste élevé et sur pellicule de haute résolution à partir
desquelles les radiologistes peuvent relever le plus de détails possibles
10. La plupart des experts en médecine s’entendent pour dire qu’un traitement réussi du cancer du sein passe d’abord par le diagnostic précoce
11. Le dépistage précoce du cancer du sein
augmente les chances de survie et réduit le nombre de chirurgies et de chimiothérapie ainsi que le stress chez les patientes et les membres de leurs familles. D’après la société américaine du cancer (American Cancer Society), un dépistage du cancer du sein au stade localisé avant qu’il ne se propage aux ganglions lymphatiques résulte en un taux de survie de 97 % sur cinq ans. Si le cancer s’est propagé aux ganglions lymphatiques sous le bras (axillaires), le taux atteint alors 79 %. S’il a atteint d’autres organes (au stade de métastase) tels que les poumons, la moelle osseuse, le foie ou le cerveau, le taux de survie sur cinq ans passe à 23 %
12.
La mammographie émet une faible dose ou une faible énergie de rayonnement pour visualiser les tissus internes du sein, grâce à l’absorption de certains rayons X dans les tissus et au passage d’autres à travers le sein; on obtient un cliché sur une pellicule (mammographie classique) ou une image numérique sur écran
(mammographie numérique). Les méthodes de mammographie sur film sont de loin les plus répandues. Les méthodes de
mammographie numérique viennent tout juste de faire leur entrée.
Sur les 688 appareils de dépistage du cancer du sein au Canada, 540 sont enregistrés auprès d’un programme d’accréditation volontaire géré par
l’Association canadienne des radiologistes (CAR). Selon une enquête du Globe and Mail basée sur les dossiers de la CAR, 148 hôpitaux et cliniques au Canada se servent d’appareils de dépistage du cancer du sein qui ne satisfont pas aux critères d’enregistrement (50), n’ont jamais été testés (48) ou ne sont plus testés (50). Le Globe and Mail a déclaré que la société canadienne du cancer du sein (Breast Cancer Society of Canada) et la Société canadienne du cancer préconise toutes deux un test de qualité obligatoire pour tous les appareils de mammographie au Canada afin d’éviter que les femmes soient soumises à des tests d’appareils désuets, aient affaire à un personnel sans formation ou éventuellement que leur cancer du sein ne soit pas dépisté.
Source : L. Priest, « Machines That Detect Cancer Need Check-up, Groups Say », The Globe and Mail, le 2 mai 2005.
En 2002, le Centre international de recherche sur le cancer de l’OMS a convoqué un groupe de travail qui a évalué les preuves disponibles sur le dépistage du cancer du sein.
Le groupe, composé de 24 experts de 11 pays, en a conclu qu’il existe suffisamment de preuves sur l’efficacité du dépistage mammographique chez les femmes de 50 à 69 ans.
D’après le groupe de travail, la mortalité liée au cancer du sein chez les femmes de 50 à 69 ans qui ont choisi de participer aux programmes de dépistage était réduite d’environ 35 %. Dans le cas des femmes de 40 à 49 ans, le groupe de travail n’a trouvé que peu de preuves de réduction de la mortalité liée au cancer du sein
13. Une étude réalisée en 2005 sur les articles portant sur des essais cliniques randomisés, lesquels évaluaient l’efficacité du dépistage du cancer du sein aux États-Unis, en Suède, au Canada et au Royaume-Uni, a fait ressortir que le dépistage mammographique réduit la mortalité liée au cancer du sein d’environ 20 % à 35 % chez les femmes de 50 à 69 ans après 14 ans de suivi
14. La preuve de la réduction de la mortalité est également appuyée par une autre étude publiée en 2005. Cette étude examinait les résultats du programme du service de mammographie de dépistage de Copenhague sur une période de 10 ans, soit de 1991 à 2001. Le groupe d’étude comprenait des femmes de 50 à 69 ans invitées à se soumettre au dépistage tous les deux ans. L’étude danoise a soulevé que, dans l’ensemble, la mortalité liée au cancer du sein avait chuté de 25 %, par comparaison à ce que les chercheurs auraient prévu s’il n’y avait pas eu de dépistage. Quant aux femmes qui ont choisi de participer au
programme de dépistage de Copenhague, leur mortalité liée au cancer du sein a diminué de 37 %
15.
La Société canadienne du cancer recommande aux femmes de 50 à 69 ans de subir une mammographie tous les deux ans
16. Selon l’Enquête sur la santé dans les collectivités canadiennes (ESCC) de 2003, 71 % des femmes âgées de 50 à 69 ans ont déclaré avoir subi une mammographie au cours des deux dernières années; 49 % de toutes les femmes dans ce groupe d’âge ont déclaré que cet examen était exclusivement un dépistage de routine
17. Tous les organismes médicaux principaux aux États-Unis, y compris la American Cancer Society, recommandent le dépistage dès l’âge de 40 ans, bien que les avantages du dépistage chez les femmes dans la quarantaine peuvent être moins importants que chez les femmes de 50 ans et plus. Les femmes dans la quarantaine ont une incidence inférieure de la maladie, des tissus mammaires denses (ce qui pourrait jouer sur la sensibilité de la mammographie) et, en moyenne, des cancers dont la vitesse de propagation est
supérieure
11, 14, 18. En août 2005, l’Agence d’évaluation des technologies et des modes d’intervention en santé (AETMIS) du Québec a publié un rapport qui traite de la pertinence de faire subir un test de dépistage aux femmes de moins de 50 ans. On en a conclu, dans le rapport, que les données des essais publiés à ce jour ne justifient pas, d’un point de vue scientifique, la recommandation du dépistage chez les femmes de moins de 50 ans.
Cependant, cette conclusion n’écarte pas la possibilité que le dépistage chez certaines
femmes, selon une évaluation personnalisée des risques, serait avantageux. Le rapport du
Québec indique que ces conclusions devraient être passées en revue dès la publication des
résultats de l’essai randomisé du dépistage démographique chez les femmes au début de la
quarantaine mené par le Comité de coordination de la recherche sur le cancer (Coordinating
Committee on Cancer Research) du Royaume-Uni
19.
Les premières images de la mammographie à elles seules ne suffisent pas toujours pour déceler un cancer ou en écarter le diagnostic. Dans le cas de 5 % à 15 % des
mammographies de dépistage, davantage de tests sont nécessaires, tels que les
mammographies supplémentaires ou l’échographie. Habituellement, la plupart de ces tests présentent des résultats normaux. Dans le cas contraire, un suivi ou une biopsie s’avérerait nécessaire. Généralement, la plupart des biopsies confirment l’absence d’un cancer. Aux États-Unis, on a estimé qu’une femme qui subit une mammographie tous les ans entre 40 et 49 ans a environ 30 % de chances que sa mammographie présente un faux résultat positif à un moment donné au cours de cette période. On estime que le taux de faux résultats positifs de mammographies est d’environ 25 % chez les femmes de 50 ans et plus
11. La mammographie classique ne décèle par non plus entre 10 % et 30 % des cancers du sein (faux résultats négatifs)
20, 21.
Bien que le résultat d’une mammographie par radiographie puisse être un faux positif ou un faux négatif, il s’agit encore de la méthode de premier recours pour le dépistage auprès des femmes asymptomatiques. Elle constitue la seule technique fiable pour dépister les microcalcifications et elle est assez sensible pour déceler le cancer chez les femmes aux seins adipeux. Toutefois, elle n’est pas fiable dans l’évaluation des tissus denses du sein
12, 14, 22.
Les technologies d’imagerie auxiliaires en complément à la mammographie sont utilisées ou explorées dans l’optique de réduire le taux de biopsies à la suite d’un faux résultat positif de mammographie et de détecter les cancers non décelés dans les faux résultats négatifs.
Certaines nouvelles méthodes d’imagerie des seins, ou méthodes expérimentales, font l’objet de tests pour remplacer la mammographie, plus particulièrement pour déceler les tumeurs chez les femmes aux seins denses et chez les femmes prédisposées
génétiquement au cancer du sein.
Technologies d’imagerie auxiliaires ou solution de rechange pour la mammographie
Échographie mammaire
L’échographie mammaire est le test complémentaire le plus répandu après la mammographie. Elle sert habituellement à cibler une zone précise suspecte que la mammographie a mise en évidence. L’échographie aide à faire la distinction entre les kystes et les masses solides ainsi qu’entre les tumeurs bénignes et cancéreuses. Toutefois, les petits dépôts de calcium, des signes précurseurs du cancer, ne sont pas visibles à l’échographie. Cette dernière est plus avantageuse parmi les femmes aux seins denses.
Des études ont d’ailleurs suggéré d’ajouter l’échographie dans le dépistage du cancer chez les femmes dont les seins sont denses
12. Une étude réalisée en Nouvelle-Zélande portant sur l’utilisation de l’échographie en tant qu’outil diagnostique de premier recours, au même titre que la mammographie, a conclu que d’utiliser ensemble l’échographie et la
mammographie est de loin la meilleure option que de se servir d’une seule modalité. En fait,
la combinaison des deux modalités a permis d’augmenter de 9 % le nombre de cancers du
sein détectés
23. Aux États-Unis, un essai clinique est en cours pour tenter de déterminer le
rôle, s’il en est un, de l’échographie dans le dépistage du cancer du sein chez les femmes
très à risque. Les participantes subiront tous les ans, pendant trois ans, un dépistage par
échographie et par mammographie
24.
Imagerie par résonance magnétique (IRM) De récentes recherches menées au Canada, aux États-Unis et en Europe font ressortir que l’IRM semble plus sensible que la
mammographie, l’échographie ou la
combinaison des deux dans le dépistage des tumeurs chez les femmes prédisposées
génétiquement au cancer du sein. Les résultats de ces études laissent croire que le dépistage effectué à l’aide de l’IRM pourrait devenir la pierre angulaire de la surveillance du cancer du sein chez les femmes à risque élevé d’en développer un
25, 26, 27. D’autres études ont également prouvé que l’IRM est plus sensible que la mammographie dans le dépistage du cancer dans les seins aux tissus
fibroglandulaires ou denses
28, 29. Malgré tout, la spécificité de l’IRM semble inférieure à celle de la mammographie, en raison des taux
supérieurs de faux résultats positifs. Les faux résultats positifs ont été liés à l’anxiété et aux coûts supplémentaires. L’IRM en tant qu’outil de dépistage n’a pas fait l’objet d’une étude au sein de la population générale. De plus, les résultats du dépistage par IRM chez les femmes à risque élevé ne s’appliquent pas nécessairement aux femmes moyennement à risque. Les facteurs susceptibles d’empêcher l’utilisation régulière de l’IRM dans le
dépistage auprès de la population générale, du moins dans un avenir rapproché, sont ses coûts élevés, sa spécificité relativement faible, son incapacité à déceler les
microcalcifications ainsi que le manque de techniques standard et de normes d’interprétation des examens du sein par IRM
12, 14.
Mammographie numérique
La mammographie sur film, la norme à l’heure actuelle, présente certaines limites inhérentes en terme de qualité de l’image. La mammographie est une des dernières interventions radiographiques à être numérisée
30. La mammographie numérique est
devenue une solution de rechange pratique, supposée améliorer la qualité de l’imagerie du sein et réduire la dose de rayonnement exigée.
La mammographie numérique comprend la saisie d’images numériques à l’aide de deux méthodes distinctes
31:
!
La mammographie par radiographie analogique est un système indirect : La radiographie est saisie sur une plaque photosensible à partir de laquelle on crée une image numérique.
!
La mammographie par radiographie numérique, aussi connue sous le nom
« mammographie numérique plein champ », est un système direct : La radiographie est convertie directement en image numérique.
Une étude clinique réalisée dans 22 centres répartis aux États-Unis, au Canada et en Allemagne pour
déterminer le rendement de l’IRM dans le dépistage du cancer du sein chez les femmes à risque élevé. Environ
1 000 femmes dont on a diagnostiqué le cancer dans un sein ont subi un examen d’IRM sur l’autre sein qui s’est révélé non cancéreux après la mammographie et l’examen physique. Les résultats seront publiés vers la fin de 2005.
Source : Radiological Society of North America, Radiology Info—News from the RSNA Media
Briefing—New Breast-Imaging Technology Could Save More Women’s Lives (en ligne), dernières
modifications en juin 2005. Internet :
<http://www.radiologyinfo.org/content/news/target.
cfm?ID=196>.
En 1991, un groupe d’experts du National Cancer Institute aux États-Unis a conclu que la mammographie numérique plein champ était la technologie la plus prometteuse dans l’amélioration du dépistage du cancer du sein. En 2000, la compagnie General Electric est devenue le premier fabriquant d’appareils de mammographie numérique plein champ approuvés par le Secrétariat américain aux produits alimentaires et pharmaceutiques. L’imagerie numérique n’est pas encore très répandue aux États-Unis, ni dans d’autres pays. En date du 1
ermai 2005, seulement 6,4 % des appareils enregistrés de mammographie aux États-Unis étaient
numériques
32, 33. La mammographie numérique plein champ permet la transmission électronique, le stockage et la consultation d’images. Le format numérique facilite également l’utilisation de logiciels de détection assistée par ordinateur qui peuvent relever des calcifications, des masses ou d’autres lésions à partir de la mammographie, augmentant ainsi le nombre de cancers
détectés. Il est possible, à l’aide de la mammographie numérique, de combiner plusieurs images, de les manipuler, d’en ajouter ou d’en retirer. De nouvelles techniques à l’étude comprennent la mammographie numérique par substance de contraste et la mammographie par soustraction d’images à deux longueurs d’ondes. Dans le cas de la mammographie numérique par substance de contraste, les images sont obtenues avant et après l’injection de la substance de contraste.
Ainsi, il est possible de soustraire les images sans contraste des images avec contraste. Dans le cas du cancer du sein, la quantité de substance de contraste retenue dans le sein atteint sera différente de celle absorbée par un sein normal. Quant à la seconde technique, la
mammographie par soustraction d’images à deux longueurs d’ondes, elle consiste à injecter une substance de contraste pour mettre en évidence les nouveaux vaisseaux sanguins qui se forment avec les masses malignes. Deux images sont saisies à des longueurs d’ondes
différentes, puis l’une est soustraite de l’autre afin de cerner une tumeur
20, 21, 34, 35, 36. La mammographie numérique est une nouvelle technologie qui n’a pas été étudiée en profondeur. En octobre 2002, l’Office canadien de coordination de l’évaluation des technologies de la santé (OCCETS) a conclu qu’à la suite d’une étude de la littérature, la mammographie numérique plein champ et la mammographie sur film avec écran présentaient des aptitudes comparables de détection du cancer. D’après l’OCCETS, la mammographie sur film était encore la technologie de choix en raison de son faible coût.
L’OCCETS a ajouté que les avantages cliniques probables de la mammographie numérique plein champ (c’est-à-dire meilleure précision diagnostique, courte durée de l’examen, faible dose de rayonnement) sont encore à prouver dans le milieu clinique
31. Des études
subséquentes ont soulevé suffisamment de preuves pour soutenir que la mammographie numérique est comparable à la mammographie sur film en ce qui a trait à la sensibilité et à la spécificité
14, 21, 33. Les résultats d’une étude clinique importante (American College of Radiology Imaging Network Digital Mammography Imaging Screening Trial) à laquelle ont participé plus de 40 000 femmes réparties dans 33 sites aux États-Unis et au Canada, ont été publiés récemment (le 16 septembre 2005). L’essai clinique, qui a commencé en juillet 2001, devait mesurer les avantages potentiels de la mammographie numérique dans le dépistage pour conclure que la précision diagnostique générale de la mammographie numérique en tant que moyen de dépistage du cancer du sein se compare à celle sur film avec écran. Cela dit, la mammographie numérique est plus précise dans le dépistage chez les femmes de moins de 50 ans, chez celles dont les seins sont denses, celles qui
approchent la ménopause et celles en périménopause. Ces résultats sont encourageants,
certes, mais les coûts élevés de la mammographie numérique représentent toujours un
obstacle de taille à la mise en œuvre
37.
Détection assistée par ordinateur
Le taux de fausses interprétations négatives produites par la mammographie classique est relativement élevé (entre 10 % et 30 %)
20, 21. Pour cette raison, la détection assistée par ordinateur est devenue de plus en plus utilisée dans le dépistage mammographique. La détection assistée par ordinateur, utilisée au cours des 10 dernières années dans la pratique clinique, est effectuée le plus souvent avec la mammographie sur film. Aussi, on a déclaré qu’elle améliore de 20 % la sensibilité des mammographies sur film. L’image de la
mammographie sur film est convertie en signal numérique par un numériseur. Ce signal est alors analysé par un ordinateur et affiché à l’écran. La détection assistée par ordinateur a recours à un logiciel pour parcourir l’image et fournir des messages, habituellement sous forme de signes et symboles à l’écran, pour avertir le radiologiste des caractéristiques qui auraient pu être, sans cela, omises. Les coûts rattachés au logiciel et à l’équipement (numériseurs, systèmes
multifenêtres, etc.) nécessaires pour numériser la mammographie sur film constituent, paraît-il, un obstacle de taille l’empêchant d’être largement utilisée dans la pratique médicale. La
mammographie numérique plein champ, quant à elle, facilite l’utilisation de la détection assistée par ordinateur et pourrait avoir un meilleur rapport coût-efficacité que la première solution, car les images sont déjà en format numérique
14, 21, 33, 38, 39.
Médecine nucléaire
La mammoscintigraphie et la tomographie d’émission de positons (TEP) sont deux techniques d’imagerie en médecine nucléaire qui pourraient servir à diagnostiquer le cancer du sein.
!
La mammoscintigraphie utilise un radiopharmaceutique émetteur de rayons gamma (radionucléide), un traceur d’une demi-vie de plusieurs heures excrété par le foie et la vésicule biliaire, et une caméra pour visualiser la lésion. Après l’injection du
radionucléide dans le patient, les isotopes émettent, dès leur désintégration, des rayons gamma. Ainsi, la répartition des isotopes dans les cellules cancéreuses du sein peut être détectée à la caméra gamma. D’après une étude effectuée en 2003 par le
Secrétariat des services consultatifs médicaux du ministère de la Santé et des Soins de longue durée de l’Ontario, le peu de données disponibles semblait révéler que la
mammoscintigraphie présentait une sensibilité élevée et donnait un rendement
légèrement meilleur à celui de l’échographie dans le cas de certaines tumeurs malignes de plus d’un centimètre. Le Secrétariat des services consultatifs médicaux a conclu que la mammoscintigraphie pourrait jouer un rôle technique complémentaire dans
l’évaluation des anomalies des seins
22.
!
La tomographie d’émission de positons (TEP) utilise une substance radioactive qui, une fois injectée dans le patient, produit une petite quantité de rayonnement détectée par la caméra à positons pour créer une image. La substance la plus répandue, la
fluodésoxyglucose, se métabolise dans le corps comme le sucre. Elle se rend à la zone où le métabolisme des tissus est le plus actif, et met particulièrement en évidence les tissus cancéreux. La TEP détecte les maladies métastatiques (l’étendue du cancer), mais sert peu à détecter le cancer du sein de premier recours, car elle ne décèle pas de façon fiable les tumeurs de moins d’un centimètre. Cependant, les appareils de
mammographie couplée à la tomographie d’émission de positons, actuellement en cours
d’élaboration, nourrissent des espoirs pour la détection des petites tumeurs
12, 40.
L ’ I M A G E R I E M É D I C A L E D A N S L E
D I A G N O S T I C D E L A C O R O N A R O P A T H I E
Dans l’Enquête sur l’accès aux services de santé de 2003 de Statistique Canada, environ 1 % des répondants de 15 ans et plus ont déclaré avoir subi une angiographie non urgente au cours des douze derniers mois. En général, les répondants étaient des Canadiens âgés de 45 ans ou plus; 54 % étaient des hommes. Dans la plupart des cas (83 %),
l’intervention a été pratiquée à l’hôpital ou dans une clinique publique
41. La plupart des angiographies sont pratiquées
pour détecter la coronaropathie. D’après la Fondation des maladies du cœur, les maladies cardiovasculaires sont responsables du plus grand nombre de décès chez les Canadiens que tout autre maladie, et 54 % des décès liés aux maladies cardiovasculaires en 2002 étaient attribuables à la coronaropathie
42. On parle de coronaropathie lorsque les artères qui transportent le sang au cœur se
rétrécissent ou s’obstruent limitant l’apport sanguin au cœur.
La coronarographie (ou cathétérisme cardiaque diagnostique) est considérée comme l’étalon-or dans le diagnostic de la coronaropathie. Il s’agit d’une intervention invasive dans laquelle on injecte une substance de contraste dans la circulation sanguine à l’aide d’un cathéter. La
coronarographie permet d’obtenir des images des vaisseaux sanguins ou des cavités du cœur. Il peut s’agir d’un outil important pour dépister une obstruction des artères coronaires, qui est souvent utilisé pour déterminer la nécessité de recourir à d’autres interventions, dont
l’angioplastie ou le pontage. Selon la Base de données canadienne SIG, en 2003-2004, le personnel de l’imagerie diagnostique des hôpitaux de la Nouvelle-Écosse, de l’Ontario et de la Colombie-Britannique a pratiqué 156 643 cathétérismes cardiaques.
Les risques liés au cathétérisme comprennent notamment
43:
!
Les saignements, l’infection et la douleur;
!
L’endommagement des vaisseaux sanguins;
!
La rupture du cathéter;
!
La formation de caillots sanguins sur le cathéter qui pourraient obstruer d’autres vaisseaux sanguins ailleurs dans le corps;
!