Rev Mali Infect Microbiol 2020, Tome 15
Page 27
Diagnostic de la primo-infection à VIH dans les centres de santé du District
de Bamako, Mali
Diagnosis of acute infection of HIV in health facilities of Bamako
Bouaré Y1, Guindo I 2,5, Dao S3, Yattara II4, Bougoudogo F 2,5
1 - Laboratoire de Microbiologie Appliquée, FST - Bamako 2 - Service de Bactériologie-Virologie, INRSP - Bamako
3 - Faculté de Médecine et d’Odontostomatologie, USTTB – Bamako 4 - Laboratoire de Microbiologie du sol, FST – Bamako
5 - Faculté de Pharmacie, USTTB – Bamako
RESUME Introduction
Le diagnostic de primo-infection reste insuffisamment évoqué compte tenu des moyens de diagnostic limités dans le contexte des pays à ressources limitées. Ce travail a pour but d’identifier les cas d’infection aigüe à VIH dans le district de Bamako au Mali.
Méthodologie
Il s’agit d’une étude prospective transversale et descriptive réalisée chez les tout-venants en consultation dans 12 centres de santé, de conseil et de dépistage volontaire de Bamako.
La démarche du diagnostic consistait à utiliser une approche clinique combinée à un counseling permettant d’obtenir les symptômes et les comportements à risque et une approche biologique consistant à réaliser les tests de diagnostic du VIH. Les marqueurs biologiques recherchés et la détermination des stades de l’infection aigüe ont été faits comme décrits par Fiebig et al.
Résultats
Sur 29130 sujets dépistés dans les 12 centres tous cas confondus, 19 avaient une infection aigue avec une anomalie hématologique associée (thrombopénie, lymphopénie ou neutropénie). La charge virale médiane était
de 58108 copies/ml (4,8Log10), le CD4 médian de 339 cellules/mm3 et le CD8 médian de 772 cellules/mm3. Les
stades d’infection aigues étaient les suivants : stade 1 (5 cas), stade II (1 cas), stade III (6 cas) et stade IV (7 cas). Le facteur d’exposition le plus fréquent était le rapport sexuel non protégé retrouvé dans 14 cas.
Conclusion
Dans le renforcement du dépistage, un accent particulier devrait être mis sur l’identification des infections aigues avec un renforcement du counseling dans les groupes à risque d’exposition élevé.
Mots-clés : Centre de santé, Mali, Primo-infection, Stade de l’infection aigue, VIH. SUMMARY
Introduction
The diagnosis of acute infection remains insufficiently discussed due to the limited means in the context of resource-limited countries. This work aims to identify cases of acute HIV infection in Bamako.
Method
It is a prospective cross-sectional and descriptive study carried out among the all-vets in consultation in 12 health facilities and counseling and voluntary testing center of Bamako.
The diagnostic process consisted of using a clinical approach with counseling to obtain symptoms and risk behaviors combined to a biological approach to performing HIV tests. The biological markers and the determination of the stages of acute infection have been made as described by Fiebig et al.
Results
Of the 29130 subjects screened in the 12 sites, 19 had acute infection with associated hematologic abnormalities (thrombocytopenia, lymphopenia or neutropenia). The median of viral load was 58,108 copies/ml (4.8Log10),
the median of CD4 was 339 cells/mm3 and the median of CD8 was 772 cells/mm3. The acute stages of HIV
were: stage 1 (5 cases), stage II (1 case), stage III (6 cases) and stage IV (7 cases). The most common exposure factor was unprotected sex found in 14 cases.
Conclusion
In the screening strategies, special emphasis should be placed on identifying acute infections with enhanced counseling in groups at high risk of exposure.
Rev Mali Infect Microbiol 2020, Tome 15
Page 28
INTRODUCTION
La primo-infection à VIH n’a pas de définition absolue. Elle est connue comme la détection de l’ARN viral ou de l’antigène p24 (Ag p24) avant l’apparition des anticorps (1). Cette définition dépend de la sensibilité des tests de détection de l’ARN viral et de l’Ag p24 mais aussi des tests utilisés pour la détection de la séroconversion. Elle est aussi affectée par les variabilités individuelles de la cinétique de la réplication précoce et de la réponse immunitaire (2). Le délai d’apparition des marqueurs en début d’infection à VIH a été décrit
par Fiebig et al. en 2003 (3)et connait des limites
liées au seul sous-type B étudié. Depuis lors, c’est l’étude repère de plusieurs études menées sur les infections aiguës à VIH (2, 4-6).Dépister le VIH en phase de primo-infection contribue à limiter la propagation de l’épidémie car le risque de transmission est plus élevé qu’en phase chronique. Au Mali la prévalence du VIH est estimée à 1,1% en 2013 (7) avec environ 88000 [74 000-100 000] PVVIH dont 4 200 nouvelles infections tout âge confondu (8). Le diagnostic de primo-infection en pratique courante demeure très timide et reste insuffisamment évoqué compte tenu des moyens de diagnostic limités allant des tests rapides, simples appelés tests de diagnostic rapide (TDR) aux tests
nécessitant des conditions d’équipement
particulières comme le western blot et la détection de l’ARN viral (4). Dans la cinétique des marqueurs du VIH, les tests moléculaires de recherche de l’ARN plasmatique permettent de détecter précocement une infection à VIH d’environ 10-11jours. Les tests sérologiques utilisés ne permettent de détecter les anticorps que dans les
20-21 jours. Cependant les tests sérologiques de 4ème
génération permettent de détecter l’Ag p24, raccourcissant ainsi la fenêtre sérologique (4).Le syndrome rétroviral aigu se présente chez deux tiers des patients comme un état grippal de durée et de sévérité variables. La primo-infection pourrait donc passer inaperçue à cause de la similitude avec cet état grippal et d’autres infections. Le constat est que beaucoup de patients consultent tard dans les centres de santé après un échec d’automédication ou de médication à base de recueil de plantes. Ce travail a donc pour but d’identifier les cas de primo-infection à VIH chez les sujets volontaires ou en consultation parmi les tout-venants dans les centres de santé et les centres de conseil et de dépistage volontaire de Bamako.
MATERIELS ET METHODES
Type et période de l’étude : Il s’agit d’une étude
prospective transversale et analytique qui a eu lieu d’Avril 2013 à Décembre 2015 dans 12 centres de Bamako, Mali.
Population : Population générale tout-venant en
consultation dans les centres de santé et les centres de conseil et de dépistage volontaire. Ont été inclus
dans l’étude, tous sujets de statut VIH non connu, venant en dépistage volontaire ou chez qui le dépistage du VIH a été prescrit, et ayant donné son consentement libre et éclairé.
Echantillonnage : Il s’agit d’un choix de 12 centres
prospectés de Bamako selon leur fréquentation par des populations clés, incluant les six districts sanitaires de Bamako, les Centres de Conseil et de Dépistage Volontaire (CCDV) et ONG impliquant tous les responsables de prises en charges des PV VIH dans ses structures.
Spécimens : Le spécimen prélevé était le sang total
utilisé directement ou le sérum / plasma obtenu par centrifugation du sang total prélevé soit sur tube sec soit sur tube EDTA.
Démarche du diagnostic
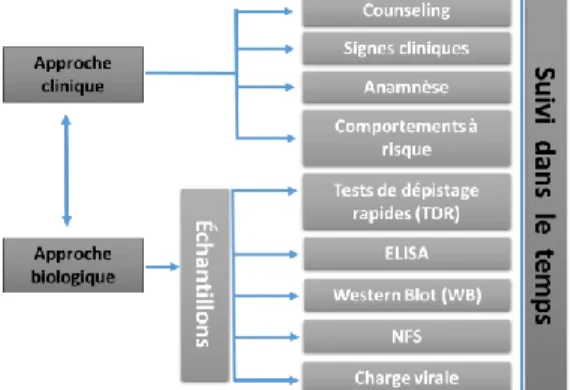
La démarche du diagnostic consistait à utiliser deux approches (voir figure 1) : une approche clinique combinée à un counseling permettant d’obtenir les symptômes observés, l’anamnèse (historique de l’infection) et les comportements à risque; et une approche biologique consistant à réaliser les tests de diagnostic du VIH et l’hémogramme à partir de prélèvements sanguins.
Figure 1 : Schéma de la démarche du diagnostic de
la primo infection
Les signes cliniques et les facteurs à risque. Les
signes non médicamenteux en faveur de la primo-infection VIH étaient ceux décrits précédemment (9, 10). Ceux sont les symptômes ayant poussé les sujets à consulter et ceux observés par les cliniciens à la consultation. Etaient considérés comme risque de transmission élevée les rapports hétérosexuels non protégés, l’homosexualité, les enfants nés de mères séropositives, les accidents d’exposition au sang (11).
Méthodes biologiques. Les marqueurs biologiques
recherchés et la détermination des stades de primo-infection ont été faits comme décrits par Fiebig et al. (3). Les tests utilisés pour la détermination de
ces marqueurs biologiques d’une
primo-infection étaient les suivants : Alère Détermine HIV combo (Alère Diagnostic) et Western Blot HIV 2.2 (MP Diagnostic) pour la recherche de l’antigène p24 et l’antigène p31; Alère Détermine HIV(Alère Diagnostic) pour l’apparition des anticorps anti-VIH , Immuno Comb II HIV BiSpot (Orgenics)
Rev Mali Infect Microbiol 2020, Tome 15
Page 29
pour déterminer le type de VIH, le Vironostika HIVAg/Ab (bioMérieux) pour la densité optique; M2000
rt (Abbott diagnostic) pour la détection de l’ARN viral plasmatique. En outre, l’hémogramme a été
réalisée pour déterminer la présence de
thrombopénie, de lymphopénie et de neutropénie un facteur important pour la confirmation d’une primo-infection. Les taux de CD4 et de CD8 ont aussi été déterminés. L’ensemble de ces tests ont été réalisés selon un algorithme comme décrit à la figure 2.
Figure 2 : algorithme biologique de détermination
de l’infection aigue à VIH
Analyse des données.
Les stades de Fiebig ont été utilisés pour classer les cas de primo-infection. Les médianes ont été déterminées pour caractériser la population.
RESULTATS Screening
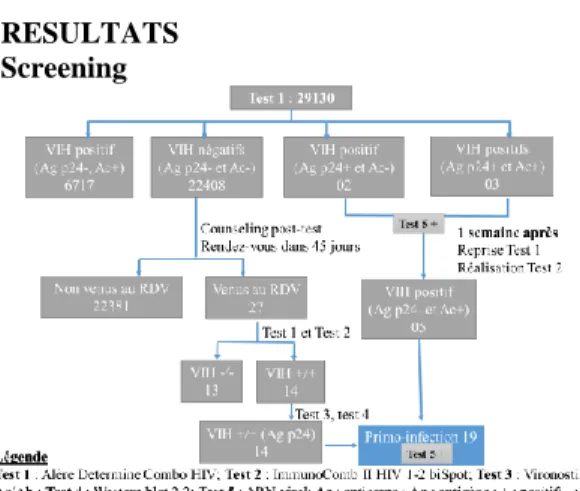
Figure 3 : diagramme de flux pour l’identification
des cas d’infection aigue
Sur 29130 sujets dépistés dans les 12 centres tous cas confondus, comme décrit à la figue 3, 6717 étaient positifs à l’anticorps anti-VIH, 22408 étaient négatifs à l’anticorps et à l’antigène p24, 5 étaient positifs à l’antigène p24 dont 2 à anticorps négatifs et 3 à anticorps positifs. L’ARN plasmatique a été détecté chez les 5 sujets avec une négativation une semaine plus tard de l’antigénémie p24, déterminant ainsi une infection aiguë. Parmi les 22408 sujets négatifs, certains ont été convoqués pour facteurs de risque et 27 d’entre eux ont repris 45 jours plus tard le dépistage. Treize (13) sujets étaient négatifs et 14 sont devenus positifs à l’anticorps et à l’antigène p24 déterminant
également une infection aiguë. L’ensemble des 19 sujets (les 5 et les 14) constituent nos sujets en primo-infection (voir tableau I).
Description des sujets
Les 19 patients en phase aiguë de l’infection avaient un âge médian de 28 ans avec une charge
virale médiane de 58108 copies/ml (4,8Log10), un
CD4 médian de 339 cellules/mm3 et un CD8
médian de 772 cellules/mm3 (voir tableau I). Dix
d’entre eux étaient de sexe masculin dont 5 mariés monogames et 5 célibataires, 5 élèves/étudiants. Parmi les neufs autres de sexe féminin, 6 étaient mariées dont 4 monogames et 2 polygames, deux étaient divorcées,
5 étaient ménagères et 2 des professionnelles de sexe (PS) ou femmes travailleuses de sexe (FTS) (Voir tableau II).
La durée médiane de l’infection à la date de dépistage était de 23 jours avec une durée minimum de 15 jours et une durée maximum de 29 jours y compris la période d’incubation. Les stades probables de primo-infection étaient les suivants : stade 1 (5 cas), stade II (1 cas), stade III (6 cas) et stade IV (7 cas) (voir tableau I).
Facteurs d’exposition
Le rapport sexuel non protégé était le facteur d’exposition de14 sujets parmi lesquels, d’une part deux jeunes de sexe masculin de 20 ans et de 22 ans ayant des rapports sexuels avec d’autres hommes, et d’autres parts deux sujets de sexe féminin qui sont des femmes travailleuses de sexe. Le facteur d’exposition de la fille de deux ans était l’allaitement maternel. Mais pour 4 sujets, le facteur n’était pas connu (voir tableau II).
Facteurs cliniques
Huit sujets ont consulté pour une grippe, 5 pour un paludisme, 4 pour une dermatose. Une fille de deux ans a été consulté pour suspicion d’oreillon (voir tableau II), elle présentait une polyadénopathie dont une axillaire (image 1 a). Un garçon de 10 ans avait consulté pour prurit costal avec des lésions sous l’effet de la démangeaison (image 1 b).
Image 1a Image 1b
Figure 1a : adénopathie (aisselle) observée chez
une fille de 2 ans
Figure 1b : lésion de grattage intercostale observée
chez un garçon de 10 ans
Rev Mali Infect Microbiol 2020, Tome 15
Page 30
La thérapie traditionnelle était le recours aux soinsavant consultation dans cinq cas, l’utilisation de médicaments déjà disponibles à domicile dans 6 cas et des médicaments conseillés en officine dans deux cas ; cependant, dans 5 cas aucune thérapie n’a été réalisée avant consultation (voir tableau II).
DISCUSSION
La recherche de la primo-infection ou infection aigue au VIH s’est déroulée dans un contexte d’identification très difficile des cas à Bamako, au Mali. Le screening a été réalisé dans des centres avec une grande file active. L’approche utilisée dans notre étude est une approche combinée qui a permis la détection transversale des infections aiguës à VIH dans la population générale et dans les populations à risque par la méthode de Fibieg
comme réalisée par Vermeulen et al. (12) et
utilisant la recherche de l’antigène p24 pour le screening comme décrit par Quinn et al. (13). Une autre approche tel que le suivi des cohortes ciblant les populations à risque comme décrit par van Loggerenberg et al. est largement utilisée (14) mais présente des limites décrites par Cohen et al. (2). Nous avons de plus fourni le counseling dans notre étude à population mixte (population générale et de population à risque), il était systématiquement demandé dans tous les cas de dépistage volontaire négatif, de refaire le depistage 45 jours après le test en tenant compte du facteur d’exposition et du contexte épidémiologique. Cependant, seuls 27 personnes sont venues aux rendez-vous motivées pour la plupart par un facteur de risque d’exposition, parmi lesquelles 14 infections aigües ont été détectées comprenant 4 personnes à haut risque (2 FTS et 2 hommes ayant des rapports sexuels avec d’autres hommes). La recherche de l’ARN viral n’était pas systématique chez tous nos patients. Cependant, elle l’a été dans les cas des
antigènes p24 positifs au 1er test. Sa recherche
systématique permettrait sans nul doute d’identifier les infections aiguës plus précocement car l’ARN viral est détectable avant l’antigène p24. Un test
ELISA de 4ème génération, le Vironostika HIV
Ag/Ab, a été également réalisé dans tous les cas de p24 positifs avec les tests rapides et chez les patients qui avaient une apparition des anticorps
constatée au 2ème test (sur un 2ème prélèvement)
réalisé 30 à 45 jours après le 1er test négatif à
l’antigène p24 et aux anticorps. L’utilisation de ce
test ELISA de 4ème génération est donc d’un apport
confortable dans le diagnostic des infections aigües à VIH comme décrit dans le travail de
Ananworanich et al, lequel a permis d’établir une nouvelle classification des stades des infections
aiguës à VIH (14, 15).
La charge virale médiane de notre étude était de
58108 copies/ml (4,8Log10) et le CD4 médian de
339cellules/mm3. Ammasari et al. avaient trouvé
une charge virale médiane de 7.00 (5.96-7.00)
Log10 pour les patients au stade II/III et de 5.71
(4.71-6.78) Log10 pour les patients au stade IV avec
respectivement des CD4 à 556 (366-696) mm3 et
535 (397-701) mm3 (6). Ces résultats montrent que
le diagnostic des infections aigues à VIH est bien possible à Bamako. Cependant, les tests de
screening de 1ère intention doivent comporter des
possibilités d’identification de l’Ag p24. En outre, avec le changement des recommandations de prise en charge visant à mettre systématiquement sous traitement tout patient dépisté, la recherche des infections aigues dans la population générale et en particulier dans les groupes cibles et à haut risque permettrait une identification précoce et une mise sous traitement précoce des patients. Un accent particulier devrait également être mis sur le renforcement du counseling permettant aux sujets à risque d’exposition élevé de respecter les rendez-vous pour le dépistage. L’augmentation de la disponibilité de la charge virale qui accompagne l’augmentation de l’accès au traitement devrait être mis à profit afin d’associer la charge virale au dépistage sérologique des patient à haut risque d’exposition.
CONCLUSION
Notre étude a permis d’identifier 19 cas d’infection aigues dans les centres de santé et les centre de conseil et dépistage volontaire de Bamako. A l’ère du renforcement du diagnostic biologique, un
accent particulier devrait être mis sur
l’identification des infections aiguës avec un renforcement du counseling dans les groupes à risque d’exposition élevé afin de les inciter à se faire dépister régulièrement.
REMERCIEMENTS
Les responsables de prise charge des 12 sites d’échantillonnage, les personnels de l’INRSP et aux personnels de la FST et de l’USTTB pour leur collaboration et pour nous avoir facilité la réalisation de ce travail.
CONFLITS D’INTERET
Pas de conflits d’intérêts
REFERENCES
1. Keele BF, Giorgi EE, Salazar-Gonzalez
JF, Decker JM, Pham KT, Salazar MG, et al. Identification and characterization of transmitted and early founder virus envelopes in primary HIV-1 infection. Proceedings of the National Academy of Sciences of the United States of America. 2008;105(21):7552-7.
2. Cohen MS, Gay CL, Busch MP, Hecht
FM. The detection of acute HIV infection. The Journal of infectious diseases. 2010;202 Suppl 2:S270-7.
3. Fiebig EW, Wright DJ, Rawal BD, Garrett
PE, Schumacher RT, Peddada L, et al. Dynamics of HIV viremia and antibody seroconversion in plasma donors: implications for diagnosis and
Rev Mali Infect Microbiol 2020, Tome 15
Page 31
staging of primary HIV infection. AIDS.
2003;17(13):1871-9.
4. Barin F, Simon F. Les outils du dépistage
de l'infection à VIH : concepts, progrès et limites. . Virologie. 2013;17(13):171-81.
5. McMichael AJ, Borrow P, Tomaras GD,
Goonetilleke N, Haynes BF. The immune response during acute HIV-1 infection: clues for vaccine
development. Nature reviews Immunology.
2010;10(1):11-23.
6. Ammassari A, Abbate I, Orchi N, Pinnetti
C, Rozera G, Libertone R, et al. Acute HIV infection (AHI) in a specialized clinical setting:
case-finding, description of virological,
epidemiological and clinical characteristics. Journal
of the International AIDS Society
2014;17(3):19676.
7. CPS/SS, INSTAT/MPATP, INFO-STAT,
ICF International. Enquête démographique et de santé au Mali (EDSM-V) - 2012-2013. Rock ville, Margland, USA2014. 577 p.
8. ONUSIDA. Rapport mondial : rapport
ONUSIDA sur l'épidémie mondiale de sida. Génève: ONUSIDA, 2013 ONUSIDA/JC2502/1/F.
9. Kahn JO, Walker BD. Acute human
immunodeficiency virus type 1 infection. The New England journal of medicine. 1998;339(1):33-9.
10. Kelley C, Barbour JD, Hecht FM. The
relation between symptoms, viralload, and viral load set point in primary HIV infection. J AIDS. 2007;45:445-8.
11. Quinn TC, Wawer MJ, Sewankambo N,
Serwadda D, Li C, Wabwire-Mangen F, et al. Viral load and heterosexual transmission of human immunodeficiency virus type 1. Rakai Project Study Group. The New England journal of medicine. 2000;342(13):921-9.
12. Vermeulen M, Lelie N, Sykes W, Crookes
R, Swanevelder J, Gaggia L, et al. Impact of individual-donation nucleic acid testing on risk of human immunodeficiency virus, hepatitis B virus, and hepatitis C virus transmission by blood
transfusion in South Africa. Transfusion.
2009;49(6):1115-25.
13. Quinn TC, Brookmeyer R, Kline R,
Shepherd M, Paranjape R, Mehendale S, et al. Feasibility of pooling sera for HIV-1 viral RNA to diagnose acute primary HIV-1 infection and estimate HIV incidence. AIDS. 2000;14(17):2751-7.
14. van Loggerenberg F, Mlisana K,
Williamson C. Establishing a cohort at high risk of HIV infection in South Africa: challenges and experiences of the CAPRISA 002 acute infection study. PLoS One. 2008;3(4):e1954.
15. Ananworanich J, Fletcher JL, Pinyakorn S,
van Griensven F, Vandergeeten C, Schuetz A, et al. A novel acute HIV infection staging system based on 4th generation immunoassay. Retrovirology. 2013;10:56
Rev Mali Infect Microbiol 2020, Tome 15
Page 32
Tableau I : tests biologiques de diagnostic de la primo-infection
Test 1 (Ac/Ag) Te st 2 T est 3 Te
st4 Test 5 : Charge virale Hémogramme immunolo- Test
gique Stade Primo- Infection 1 er p rélèv em en t 2 ème p rélèv em en t Ac DO Ag P2 4 Copies/ml Lo g 10 L y m p h o p én ie Neu tr o p én ie T h ro m b o p én ie CD4 CD8 Durée probable (jours) Stade probable 1 - + + 4,317 + 289000 5,5 - + + 94 >2000 29,1 IV 2 - + + 1,858 + 146109 5,2 + - + 03 401 20,3 II 3 Ag + + 1,032 + <20 <1,3 + - + 429 735 15 I 4 - + + 4,225 + 73853 4,9 + + 243 735 29,1 IV 5 - + + 3,816 + 1303152 6,1 + + + 246 724 23,5 III 6 - + + 3,653 + 33000 4,5 - - + 493 1563 29,1 IV 7 - + + 4,256 + 1032889 6,0 + - + 290 1946 29,1 IV 8 - + + 1,033 + 160000 5,2 + - - 463 680 15 I 9 - + + 0,869 + 2217 3,3 + - + 1012 1036 15 I 10 - + + 3,738 + 58108 4,8 + + + 242 772 23,5 III 11 - + + 4,289 + 29753 4,5 + - + 478 481 29,1 IV 12 - + + 1,037 + <40 <1,6 + - + 413 738 15 I 13 Ag + + 2,506 + 3695297 6,6 + + - 103 411 23,5 III 14 - + + 4,293 + 28100 4,4 + - + 467 884 29,1 IV 15 Ag + + 1,032 + 252025 5,4 + - + 156 1447 15 I 16 Ag + + 4,221 + 22194 4,3 + + + 218 697 23,5 III 17 Ag + + 1,036 + 35129 4,5 + - + 339 1368 23,5 III 18 - + + 4,352 + 6821 3,8 + + + 384 1065 29,1 IV 19 - + + 3,709 + 307176 5,5 + - + 387 1097 23,5 III
Test 1: Alère Determine Combo HIV Test 2 : Immuno Comb II HIV 1-2 biSpot Test 3 : Vironostika
HIV Ag/Ab
Rev Mali Infect Microbiol 2020, Tome 15
Page 33
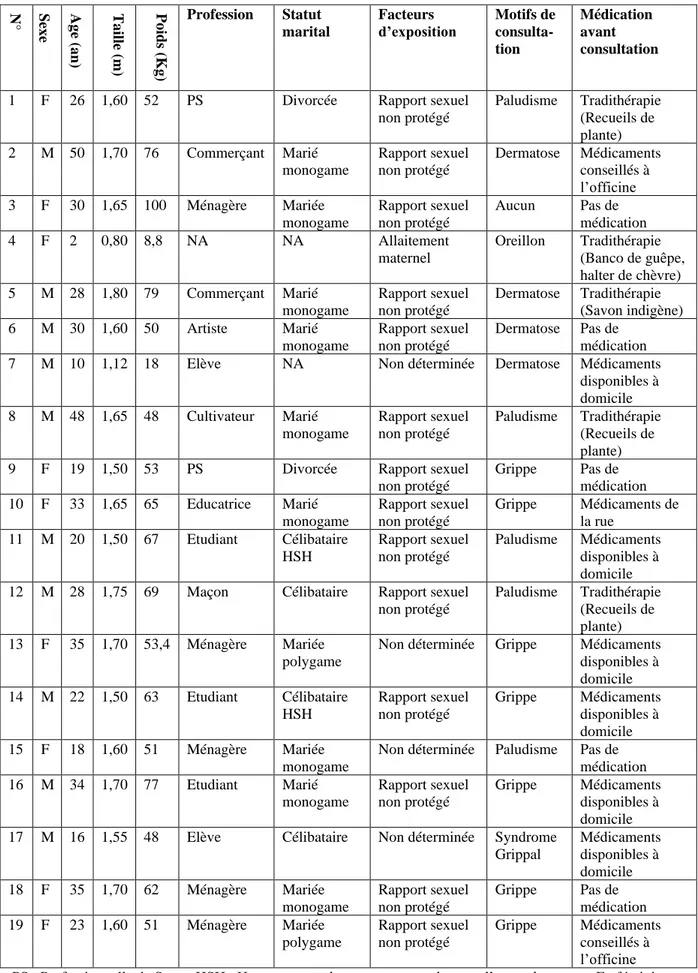
Tableau II : Caractéristiques sociodémographiques et cliniques des patients en séroconversion
N° Sex e Ag e (a n) T a ille ( m) P o ids ( K g ) Profession Statut marital Facteurs d’exposition Motifs de consulta-tion Médication avant consultation
1 F 26 1,60 52 PS Divorcée Rapport sexuel
non protégé Paludisme Tradithérapie (Recueils de plante) 2 M 50 1,70 76 Commerçant Marié monogame Rapport sexuel non protégé Dermatose Médicaments conseillés à l’officine 3 F 30 1,65 100 Ménagère Mariée monogame Rapport sexuel non protégé Aucun Pas de médication 4 F 2 0,80 8,8 NA NA Allaitement maternel Oreillon Tradithérapie (Banco de guêpe, halter de chèvre) 5 M 28 1,80 79 Commerçant Marié monogame Rapport sexuel non protégé Dermatose Tradithérapie (Savon indigène) 6 M 30 1,60 50 Artiste Marié monogame Rapport sexuel non protégé Dermatose Pas de médication
7 M 10 1,12 18 Elève NA Non déterminée Dermatose Médicaments
disponibles à domicile 8 M 48 1,65 48 Cultivateur Marié monogame Rapport sexuel non protégé Paludisme Tradithérapie (Recueils de plante)
9 F 19 1,50 53 PS Divorcée Rapport sexuel
non protégé Grippe Pas de médication 10 F 33 1,65 65 Educatrice Marié monogame Rapport sexuel non protégé Grippe Médicaments de la rue 11 M 20 1,50 67 Etudiant Célibataire HSH Rapport sexuel non protégé Paludisme Médicaments disponibles à domicile
12 M 28 1,75 69 Maçon Célibataire Rapport sexuel
non protégé Paludisme Tradithérapie (Recueils de plante) 13 F 35 1,70 53,4 Ménagère Mariée polygame
Non déterminée Grippe Médicaments
disponibles à domicile 14 M 22 1,50 63 Etudiant Célibataire HSH Rapport sexuel non protégé Grippe Médicaments disponibles à domicile 15 F 18 1,60 51 Ménagère Mariée monogame
Non déterminée Paludisme Pas de
médication 16 M 34 1,70 77 Etudiant Marié monogame Rapport sexuel non protégé Grippe Médicaments disponibles à domicile
17 M 16 1,55 48 Elève Célibataire Non déterminée Syndrome
Grippal Médicaments disponibles à domicile 18 F 35 1,70 62 Ménagère Mariée monogame Rapport sexuel non protégé Grippe Pas de médication 19 F 23 1,60 51 Ménagère Mariée polygame Rapport sexuel non protégé Grippe Médicaments conseillés à l’officine PS : Professionnelle de Sexe ; HSH : Homme ayant des rapports sexuels avec d’autres hommes ; F : féminin ; M : Masculin ; NA : non applicable