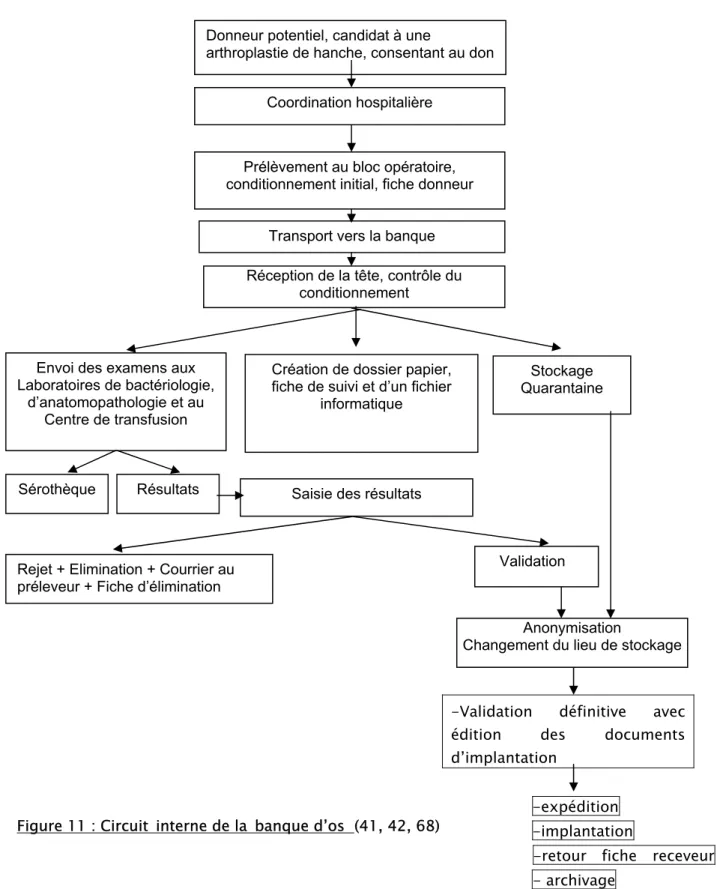
Projet d’une banque d’os à Marrakech
Texte intégral
Figure



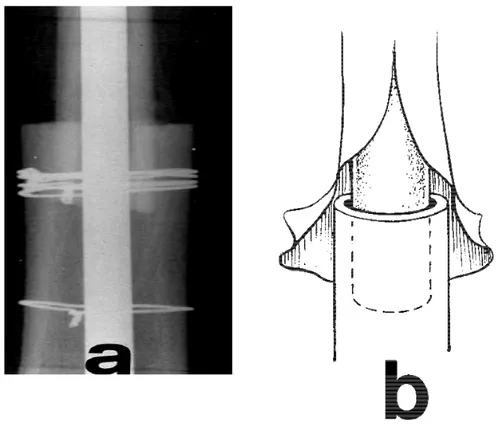
Documents relatifs
Rooommando a la Conforonco des I'linistr^s dos finances africains quo, nono"bstant Ios dispositions do 1'Article 3 do 1'Acoord portant creation do la Eanquc africaino
avec les actions suivantes : formation d'hygiénistes et de trésorier.e.s dans le domaine hydraulique, installation de deux plate-formes multi-fonctionnelles pour l'accès à
Le principe de l'unité de la forme signifie que le texte d'une initiative doit être présenté exclusivement sous la forme d'une proposition conçue en termes
D2 - Les méthodes et outils pour apprendre Organisation du travail personnel D3 - La formation de la personne et du citoyen Réflexion et discernement D4 - Les systèmes naturels
D1 – Les langages pour penser et communiquer Comprendre, s’exprimer en utilisant la langue française à l’oral et à l’écrit. SCIENCES
Activités de formation Connaissances associées Mise en relation avec le socle commun Domaines et compétences travaillées.. 2
Activités de formation Connaissances associées Mise en relation avec le socle commun Domaines et compétences travaillées.. 2
Sans revenir sur une question qui n'est pas près de sa solution (peut être parce qu'elle est mal posée) on constate que le Conseil est doté d'un statut procédural qui n'est pas